Services on Demand
Journal
Article
Indicators
Related links
Share
Ecología en Bolivia
Print version ISSN 1605-2528On-line version ISSN 2075-5023
Ecología en Bolivia vol.46 no.1 La Paz Apr. 2011
Artículo
Características reproductivas y alimenticias de Prionobrama filigera (Actinopterygii: Characidae, Pisces), una especie ornamental en la Tierra Comunitaria de Origen Takana, Bolivia
Reproductive and diet aspects of Prionobrama filigera (Actinopterygii: Characidae, Pisces), an ornamental species in the Takana Indigenous Territory, Bolivia
Magaly Mendoza1* & Guido Miranda-Chumacero1
Programa de Conservación del Gran Paisaje Madidi-Tambopata, Wildlife Conservation Society. La Paz, Bolivia
*mmendoza@wcs.org
Resumen
La ecología trófica y reproductiva del tetra cristal de cola roja Prionobrama filigera fue estudiada en la cuenca baja del Río Beni, dentro de laTierra Comunitaria de Origen Takana, entre julio de 2005 y marzo de 2006. Se capturaron 600 individuos y la identificación de sus estadios sexuales nos permitió determinar que la reproducción tendría lugar entre diciembre y febrero. Los individuos juveniles predominaron en las lagunas. La talla de madurez sexual se calculó en una longitud estándar de 42 mm para machos y 45 mm para hembras. Las hembras mostraron desove total y una fecundidad promedio de 919 ovocitos (0.74 mm de diámetro en promedio). Identificamos los contenidos estomacales y según la frecuencia de ocurrencia determinamos que Prionobrama filigera tiene una dieta invertívora. Los ítems más consumidos fueron himenópteros, dípteros, coleópteros y copépodos, aunque la dieta varió en tiempo y espacio. Los copépodos, que no fueron consumidos en época húmeda, figuran como un ítem adicional durante la época seca en arroyos y lagunas. Consecuentemente, estas características ecológicas, aplicadas a la pesca ornamental en la Tierra Comunitaria de Origen Takana, sugieren que la veda sea programada durante la época reproductiva (diciembre a febrero) y que la cosecha se realice durante la época seca (julio a septiembre) en arroyos y el río Beni, con redes de arrastre de 10 mm de malla para capturar individuos mayores a 45 mm. Igualmente, para garantizar una pesca ornamental sostenible, sugerimos que estas medidas sean complementadas con la determinación de cupos de extracción y así ayudar a mantener a largo plazo el buen estado de las poblaciones de peces en la Tierra Comunitaria de Origen Takana y su rol en el ecosistema.
Palabras clave: Bolivia, Dieta, Peces ornamentales, Prionobrama filigera, Reproducción.
Abstract
The reproductive and trophic ecology of the red-tailed glass tetra Prionobrama filigera was studied at the lower basin of the Beni river, in the Takana Indigenous Territory, from July 2005 to March 2006. Six-hundred individuals of this species were collected and had their sexual stages identified, allowing us to determine that reproduction occurs between December and February. Juveniles were found in lakes. Sexual maturity was reached at a standard length of 42 mm in males, and 45 mm in f emales. Females have a total spawning with an average fecundity of 919 ovocytes (0.74 mm mean diameter). We analyzed stomach contents and according to the frequency of occurrence of items, Prionobrama filigera was determined it to be a macroinvertebrate feeder. The most consumed items were Hymenoptera, Diptera, Coleoptera and Copepoda, but the ingestion of each item varied in time and space. Copepods, which were not ingested during the wet season, appeared as an additional dietary item during the dry season in streams and lakes. Consequently, these ecological characteristics, applied to the ornamental fishery in the Takana Indigenous Territory, suggests a fishing ban during breeding season (December to February) and the harvest season during dry season (July to September) in streams and the Beni river, by using seines of 10 mm mesh to capture individuals over 45 mm standard length. To ensure a sustainable fishery, we also recommend that these measures be complemented by determining harvesting quotas that can help to maintain healthy fish populations within the Takana Indigenous Territory over a long-term period and secure its role in the ecosystem.
Key words: Bolivia, Diet, Ornamental fish, Prionobrama filigera, Reproduction.
Introducción
La cuenca amazónica es la mayor del mundo, forma parte de un sistema de río-planicie de inundación, alberga la mayor diversidad de peces de agua dulce y se extiende en 66% del territorio boliviano (SNHN 1998, Myers et al. 2000, Reis et al. 2004). En esta cuenca, los peces con mayor abundancia y diversidad pertenecen a la familia Characidae, cuyas especies pequeñas, como los tetras Paracheirodon axelrodi (Schultz, 1956), Hyphessobrycon spp. y Prionobramafiligera(Cope, 1870), son utilizadas en pesquería ornamental debido a sus colores y formas exóticas (Barrera et al. 2002, Mancera-Rodríguez et al. 2008).
Países que desarrollan pesquerías de especies ornamentales han reportado impactos ambientales positivos de ésta actividad como los del proyecto Piaba en el Río Negro (Brasil), cuya propaganda de "compra un pez, salva un árbol" hace referencia a que las comunidades ribereñas se dediquen a la pesca ornamental en lugar de deforestar los bosques para poner cultivos o comercializar la madera (Norris & Chao 2002). En contraste, otros reportes indican que en Brasil esta actividad ha causado el colapso de las poblaciones del disco (Symphysodon aequifasciatus Pellegrin, 1904) debido a su sobreexplotación (Crampton 1999) y en Iquitos, Perú, ha reducido la diversidad y abundancia de peces ornamentales en ambientes naturales (Gerstner et al. 2006).
En este contexto y para evitar la sobreexplotación de peces ornamentales, se deben considerar, entre otras medidas de protección aplicables a la pesca ornamental, épocas de veda, áreas donde la cosecha sea permitida, especies protegidas y reglamentar los tipos de artes de pesca, definir límite de tallas y cupos de extracción (Borges 2003, Morison 2004). Para implementar el proceso de aprovechamiento es imprescindible conocer la ecología y biología de las especies sujetas a manejo. En Bolivia, gran parte de la información sobre peces está orientada hacia inventarios de especies; no obstante, en la TCO Takana del Departamento de La Paz se están haciendo esfuerzos para implementar la pesquería ornamental sostenible como una alternativa económica de desarrollo y ya se han realizado estudios preliminares impulsados por el CIPTA (Concejo Indígena del Pueblo Takana) en convenio con la WCS (Wildlife Conservation Society). Para coadyuvar al desarrollo de una pesquería sostenible, este trabajo presenta datos para un mejor conocimiento de la ecología trófica y reproductiva de Prionobrama filigera en la cuenca baja del Río Beni dentro de laTCO Takana.
Área de estudio
La TCO Takana (Fig. 1) se encuentra en la hidroecoregión de las llanuras aluviales de tierras bajas situada al norte del Departamento de La Paz. El área colinda al sur con la Reserva de la Biosfera Pilón Lajas, al suroeste con elÁrea Natural de Manejo Integrado Madidi y al este con el Río Beni (Lorini et al. 1998, Navarro & Maldonado 2002).
| Figura 1. Lugares de muestreo en la cuenca baja del Río Beni, TCO-Takana. El mapa de la TCO Takana muestra la zona alta en la que P. filígera fue muestreada. |
En la TCO Takana se pueden distinguir dos zonas: 1) Pie de monte entre 200-400 m y 2) la llanura de inundación, donde se realizaron los muestreos, entre 160-200 m. Los suelos tienen pendientes bajas, son arcillosos y arenosos, pobres en nutrientes y el pH ácido a neutro. Existen alrededor de 14 lagunas de origen fluvial, numerosos bajíos y cinco arroyos que desembocan en el Río Beni (CIPTA/ WCS 2002). En septiembre, este río y los arroyos llegan a su nivel más bajo; a mediados de octubre aumentan su caudal; y entre noviembre a diciembre el río crece más que los arroyos. En su confluencia, las aguas blancas del río se desbordan hacia los arroyos dando la impresión de correr en sentido contrario. Entre febrero y marzo, los arroyos fluyen hacia el río con aguas de color café transparente a rojizas. Las lagunas mantienen su nivel de agua bajo hasta noviembre y recién en diciembre comienzan a llenarse por las primeras lluvias. Ya entre febrero y marzo, las lagunas Japón, Supa, Corpo y Villa Fátima llegan a conectarse con el río, mientras que la Laguna Colorado está conectada con el arroyo Colorado (Miranda 2007).
Métodos
Sitios y fechas de muestreo
Se realizaron cuatro campañas de muestreo abarcando un ciclo hidrológico anual: julio-agosto (época seca), septiembre-octubre (Transición seca-húmeda) y diciembre en 2005 y febrero en 2006 (época húmeda). Las pescas se realizaron con redes de arrastre de 6 m de largo y 1.5 m de alto con 5 mm de abertura de malla.
Los sitios de muestreo fueron elegidos para abarcar todos los hábitats de la llanura inundable (160-200 m de altitud) de la TCO Takana, es decir cinco sitios en el Río Beni, cinco arroyos, cinco lagunas y tres bajíos. En cada punto a lo largo de 100 m aproximadamente, se hicieron hasta 30 arrastres (Fig. 1).
En el Río Beni se tomaron muestras en orillas, en cinco puntos cercanos a comunidades ribereñas a lo largo de 140 km. En los arroyos, hicimos los muestreos en lugares poco profundos en medio de bosques con doseles cerrados. Los muestreos en lagunas meándricas se hicieron en orillas que son en general poco profundas y con vegetación compuesta por hierbas acuáticas, flotantes y árboles. Finalmente, los bajíos aislados- cuerpos de agua estacionales en depresiones de poca profundidad que no sobrepasaron los 40 cm-se caracterizaron por vegetación emergente y flotante.
Reproducción
Para conocer la época de reproducción extrajimos las gónadas de 348 individuos (solo analizamos alrededor de 30 individuos por cada punto de muestreo, no la totalidad de los 600 ejemplares capturados) y determinamos el sexo y estadio de maduración según la escala de madurez sexual propuesta por Bagenal (1978). Con todo esto, determinamos la variación de la proporción de sexos en relación al tipo de hábitat por medio de una prueba de Chi cuadrado y además, se calculó para el mismo lote de individuos el índice gonadosomático (IGS) usado para determinar la variación del peso de las gónadas respecto del peso total corporal en cada época o período del año (Loubens 1986):
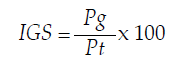
donde, Pg = peso de las gónadas, Pt = peso corporal. Calculamos la variación entre los meses de estudio de este índice por tallas y entre hábitats, mediante un análisis de varianza ANDEVA.
Para determinar la talla de madurez sexual (TMS) como fue propuesto por Loubens (1986), los peces se agruparon en siete clases de tallas. Para cada clase se determinó el porcentaje de individuos maduros (estadios IV, V y VI en hembras y III en machos). La talla en la que el 50% de los individuos presentaron estadios maduros correspondió a la talla media de madurez sexual (TMS).
Para determinar la fecundidad y diámetro de los ovocitos, 15 gónadas de hembras en estadio V fueron usadas para medir y cuantificar los ovocitos presentes, utilizando Image J, un software de análisis de imágenes digitales (http//:rsbweb.nih.gov/ij/). Este software permite el conteo automático a partir de fotografías digitales de los ovocitos distribuidos en cajas Petri y la respectiva medición del diámetro de los mismos. Para determinar el tipo de desove (parcial o total), se realizó un histograma de frecuencias de diámetros de los ovocitos y se observó la formación de uno o más picos en la gráfica resultante (Hunter et al. 1980).
Dieta
Para la determinación del hábito alimenticio analizamos 368 estómagos de individuos comprendidos entre 24-54 mm de LS, de los cuales cuantificamos e identificamos su contenido hasta el nivel de orden (Hyslop 1980). El espectro alimenticio, la importancia de cada recurso y su variación de acuerdo a la época y hábitat, se determinó mediante el cálculo de la frecuencia de ocurrencia (FO):
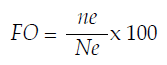
donde, ne = número de estómagos con un tipo de alimento, Ne = número total de estómagos no vacíos (Hyslop 1980). También se realizó un análisis de correspondencia de los ítems consumidos.
El ancho de nicho fue calculado mediante el índice de Levin estandarizado (Bi) (Krebs 1999):
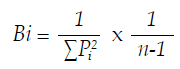
donde Pi = proporción de individuos que utilizan el recurso i, n= número de categorías de recurso. Valores cercanos a 0 representan individuos especialistas y cercanos a 1 indican generalistas. La significancia estadística fue calculada mediante el análisis de varianza Kruskal Wallis.
Resultados
Capturamos 600 individuos de P. filigera en la llanura inundable de la TCO Takana, de los cuales 216 fueron del Río Beni, 208 de arroyos (Colorado, Enapurera, Tarene, Tequeje y Undumo) y 180 de lagunas (Japón, Supa, Corpo y Villa Fátima). Mientras que en bajíos no se registró ningún individuo.
Época de reproducción
El número de individuos maduros capturados durante todos los muestreos fue muy bajo (25 machos y 30 hembras) representando tan solo el 9.1% de las capturas. Con esta aclaración, de acuerdo a la mayor proporción de machos y hembras maduros (Fig. 2) registrada durante la época de inundación, es decir, entre diciembre y febrero, se podría asumir que este período corresponde a la época de reproducción. Relacionado con esto, entre julio y octubre fue mayor la frecuencia de individuos jóvenes capturados.
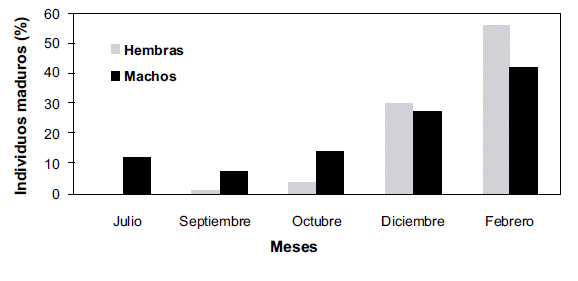
Figura 2. Porcentaje de hembras (estadios IV, V y VI) y machos (estadio III) maduros de P. filígera en diferentes meses.
El índice gonadosomático podría estar corroborando esta tendencia. Existe diferencia significativa de este índice respecto a la época (F= 9.6801, p= 0.0043) y a las tallas (F= 14.7, p= 0.000001), no fue así en relación a los tipos de hábitat (F=4.0002, p= 0.0619). Los IGS más altos se obtuvieron en época húmeda (febrero= 3.44 y diciembre= 3.07) y en clases de tallas mayores (45 - 54 mm) por lo que representan individuos con grado de maduración sexual más altos. Mientras que los valores más bajos se dieron en época seca (julio= 1.76, septiembre= 1.64 y octubre= 1.61) y en individuos más pequeños (30-44 mm) (prueba de Tukey, p< 0.01) (Fig. 3).
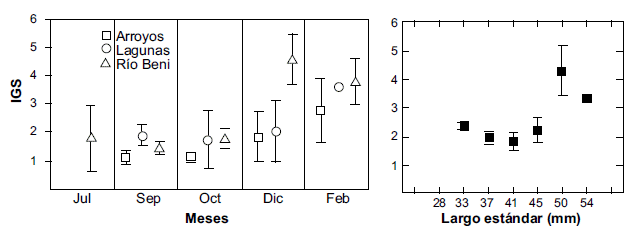
Figura 3. Índice gonadosomático de P.filigera en diferentes meses (izquierda) y tallas (derecha).
Madurez sexual y proporción de sexos por tipo de hábitat
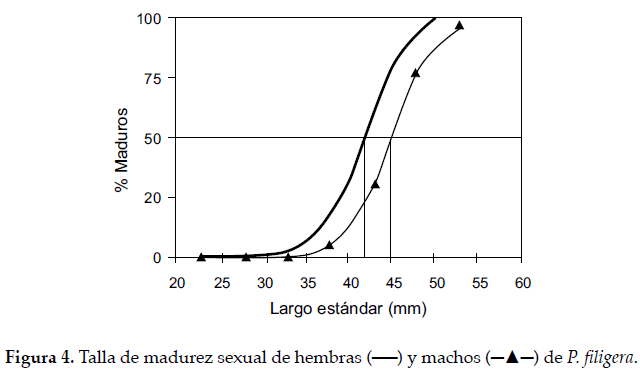
La talla de madurez sexual fue de 45 mm en hembras y 42 mm en machos, para estas tallas la media del alto máximo fue 10 mm (Fig. 4).
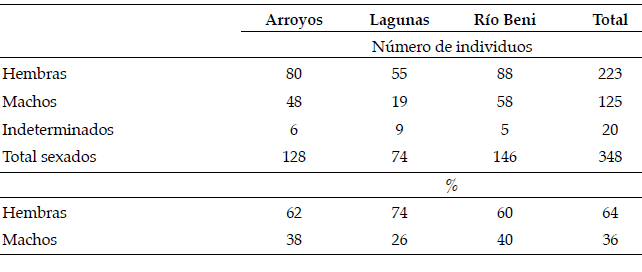
La proporción de machos respecto de las hembras fue 1:2 con 36% (n= 125) y 64% (n= 223) respectivamente. Las proporciones por cada sexo presentaron una diferencia estadísticamente significativa (X2=15.59, p=0.0004), las hembras predominaron en las lagunas en una proporción 1:2.8 pero en el Río Beni la diferencia entre las proporciones fue menor (1:1.5) (Tabla 1).
Tabla 1. Número individuos y proporción de sexos de P.filigera por hábitat.
Según nuestros resultados, parecería que la maduración tendría lugar en el Río Beni y el desove/ desarrollo en las lagunas. Mediante el análisis de correspondencia (Chi-2= 51.4, p= 0.00) observamos que en el río Beni hay la tendencia hacia una mayor cantidad de hembras maduras (III-V). En lagunas capturamos mayormente estadios juveniles, mientras que en arroyos encontramos tanto juveniles como adultos (I-IV y VI) (Fig. 5).
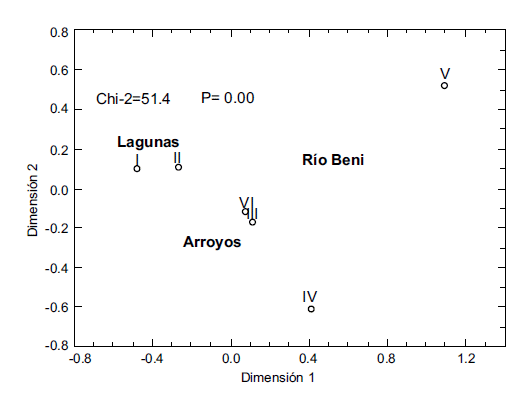
Figura 5. Análisis de correspondencia de la distribución de estadios sexuales de hembras en relación al tipo de hábitat.
Existe una diferencia significativa en las tallas de poblaciones de P. filigera según el tipo de hábitat (F= 82.7, P< 0.01). Así, en las lagunas encontramos más individuos de tallas menores, la base de la pirámide (clases de tamaño 1-3) fue mayor que las clases sucesivas (4-7). Por el contrario, en el río hubo más individuos de tallas grandes y pocos de tallas pequeñas. Finalmente, en arroyos las tallas medias fueron dominantes (Fig. 6).

Figura 6. Estructura de tamaños de P.filígera en tres tipos de hábitat.
Fecundidad y tipo de desove
Del total de hembras capturadas y analizadas de Prionobramafiligera, sólo se pudieron examinar 15 para un análisis de los ovocitos por el grado de maduración de los mismos. En promedio, se produjeron 950 ovocitos (σ=223) de 0.74 mm de diámetro (σ= 0.04), el menor número fue de 641 y el máximo de 1.327. El histograma de frecuencia por tamaño de ovocitos maduros, comprendido entre 0.6-0.9 mm de diámetro, es unimodal. Esto sugiere que P. filigera tiene un solo desove por época reproductiva, es decir que su estrategia reproductiva es el desove total anual (Fig. 7).

Figura 7. Histograma de frecuencia por tamaño de ovocitos de P.filígera.
Ecología trófica
En los contenidos estomacales de P. filigera identificamos 17 tipos de items pertenecientes a cuatro grupos: Crustacea, Insecta, Chelicerata y peces (ictioplancton y escamas). Fueron dominantes en la frecuencia de ocurrencia los items de Insecta y Crustacea (Fig. 8).
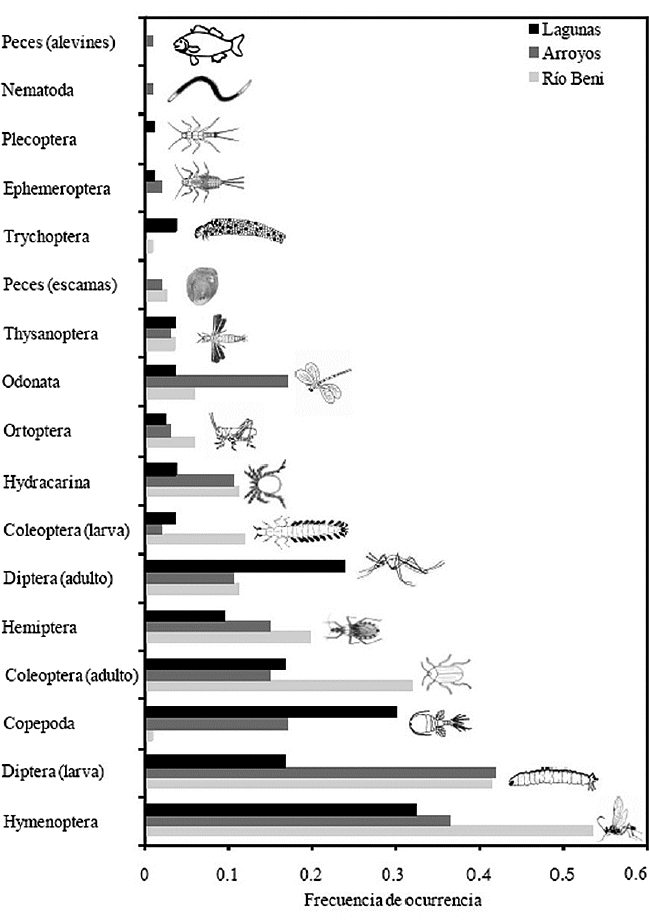
| Figura 8. Frecuencia de ocurrencia de los ítems alimenticios consumidos por P. filígera en arroyos, lagunas y el Río Beni. Para los códigos de los ítems ver tabla 3. |
El análisis de varianza Kruskal Wallis indica que no existe diferencia significativa en el ancho de nicho de P. filigera con relación a la época (H= 3.14, P< 0.151) y al tipo de hábitat (H= 0.998, P< 0.553), pero se puede ver que los individuos de los arroyos tienden a ser más generalistas mientras que en lagunas y el río tienden a ser especialistas. Comparando por época, se observó que en seca el ancho de nicho es menor mientras que durante la época húmeda y de transición éste incrementó (Tabla 2). El promedio para todos los hábitats y épocas fue de 0.5.
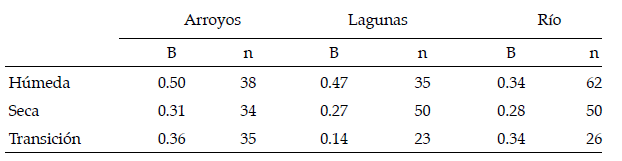
| Tabla 2. Variación del índice trófico de Levin (B) por épocas (H = 3.14, P < 0.151) y tipo de hábitat (H = 0.998, P < 0.553), n es el número de individuos analizados. |
Variación de la dieta por época y hábitat
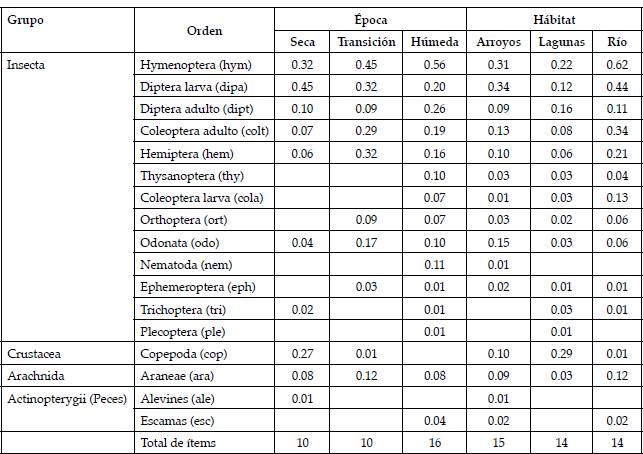
En los tres hábitats la riqueza de ítems fue mayor en la época húmeda, donde se encontraron 16 tipos, mientras que durante la época de transición y la época seca, solo se encontraron 10 (Tabla 3). Durante todo el ciclo hídrico, los ítems como himenópteros, dípteros, coleópteros, copépodos y hemípteros fueron comunes, pero otros variaron. Los copépodos fueron comunes durante la estación seca, pero pasaron a ser raros en la transición y ausentes en la época húmeda. En relación al tipo de hábitat, la frecuencia de ocurrencia de los copépodos fue mayor en lagunas (0.29), que en arroyos (0.10) y en el Río Beni (0.1).
| Tabla 3. Frecuencia de ocurrencia de los Ítems consumidos por época y hábitat. Entre paréntesis se indica el código para las figuras 8 y 9. |
Mediante el análisis de correspondencia (Chi-2= 114.7, p= 0.000) pudimos observar que los hábitos alimenticios de P. filigera varían según el periodo hidrológico. Durante la disminución de las aguas los ítems son mayormente de origen autóctono (copépodos, tricópteros, ictioplancton, dípteros y coleópteros acuáticos). La tendencia al subir el nivel de agua y durante la transición es de incluir en su dieta organismos alóctonos (tisanópteros, himenópteros y dípteros terrestres) (Fig. 8).
Los ítems alimenticios en común para los tres tipos de hábitats fueron himenópteros, hemípteros, tisanópteros, coleópteros terrestres, dípteros acuáticos e hidracáridos (análisis de correspondencia, Chi-2= 79.6, p= 0.000). Los ítems exclusivos para el Río Beni fueron coleópteros acuáticos, ortópteros y escamas; en arroyos fueron nemátodos, alevinos y efemerópteros; para lagunas tricópteros, plecópteros y copépodos (Fig. 9).
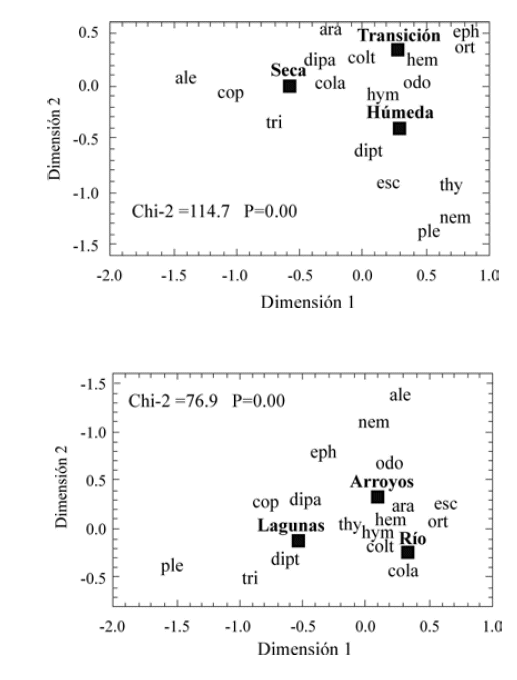
| Figura 9. Análisis de correspondencia de los ítems alimenticios de P.filígera en arroyos, lagunas y el Río Beni en un ciclo hídrico (códigos de los ítems según tabla 3). |
Discusión
Época de reproducción
Nuestro estudio sugiere que el período reproductivo de Prionobrama filigera podría iniciarse en diciembre (IGS= 4.5%) y prolongarse hasta febrero (IGS= 3.8%) que es cuando ocurre el desove. En la Amazonía, el comienzo de la época de lluvias, con el aumento de la temperatura, marca cronológicamente el inicio del desarrollo gonadal, mientras que el incremento del caudal de los ríos es una señal fuerte que motiva la migración reproductiva (Welcomme 1977), este es el caso de los carácidos Moenkhausia dichroura, Aphyocharax alburnus y Astyanax lineatus (Vazzoler 1996). Así, las condiciones ambientales son determinantes para el desarrollo de la reproducción. En laTCO Takana se registran las temperaturas máximas en noviembre y diciembre, mientras que el pico de las precipitaciones ocurre entre diciembre y marzo. Esta estrategia de reproducción durante aguas altas podría estar provocando la migración de larvas y alevinos de P. filigera hacia las lagunas donde encuentran ambientes para su protección, alimentación y desarrollo (Welcomme 1977).
Talla de madurez sexual y lugares de reproducción
La talla de madurez sexual fue prácticamente la misma para ambos sexos (hembras: 45 mm y machos: 42 mm). Sin embargo, la talla de madurez sexual diferencial en carácidos es recurrente en la literatura. Aún cuando encontramos individuos sexualmente maduros en arroyos, lagunas y río, hubo mayor proporción de jóvenes en lagunas (Figs. 4 - 5). Los carácidos tienen hábitos gregarios, forman cardúmenes de individuos adultos y jóvenes por separado (Welcomme 1977). Aparentemente P. filigera se puede reproducir en los tres hábitats, pero es en las lagunas donde podría estar ocurriendo el mayor reclutamiento por la predominancia de individuos jóvenes en este tipo de ambientes.
Fecundidad y tipo de desove
La fecundidad de P. filigera fue en promedio 919 y el diámetro promedio fue de 0.74 mm. Aunque otros carácidos pequeños tienen fecundidades de 345 ovocitos (Aphy ochar ax anisitsii), 513 (Cheirodon ibicuhiensis), 722 (Odontostilbe pequira) y 406 (Serrapinnus calliurus) (Bazzoli & Godinho1991). Esta amplitud en la fecundidad de los carácidos es frecuente dado que es afectada por variables ambientales y fisiológicas que influyen de diversas formas por especie, edad e individuo. Por ejemplo Bryconamericus iheringii tiene una fecundidad de 934 ovocitos mientras que en Bryconamericus stramineus es mucho menor con 371 (Bazzoli & Godinho1991).
El desove de P. filigera es total. La distribución de frecuencias de tamaño de ovocitos mostró un solopicopor año (Fig. 7). Por otro lado, el desove parcial es frecuente en otras especies como Moenkhausias anctaefilomenae, M.intermedia en el Río Cuibá (Rodríguez et al. 1991), Hyphessobrycon pulchripinnis (Burt et al. 1988), en las cuales los múltiples episodios de desove están vinculados con una amplia gama de factores que van desde el tamaño de la especie, el tamaño de los ovarios y la estabilidad estacional del sistema en el que se encuentren (Burt et al. 1988). Sin embargo, algunos estudios muestran otras especies pequeñas con evidencia de desove total, como en Hyphessobrycon poecilioides del río La Vieja (Garcia & Roman 2008).
Adicionalmente, el tipo de desove da cierta pauta del potencial reproductivo de estas especies. Relacionando los datos aquí obtenidos, como la fecundidad relativamente alta a comparación de otros carácidos como Aphyocharax anisitsi (344) y Odontostilbe pequira (722), se consideraría que P. filigera (919) tiene estrategia tipo "r", característica de especies que producen muchos huevos pequeños y no están sujetas a cuidado parental. Sato (1999) considera que los peces que presentan estas características, producen huevos libres o no adhesivos en contraposición a peces con baja fecundidad, que producen huevos grandes que se adhieren a algún sustrato y además tienen cuidado parental.
Proporción de sexos
La proporción de machos respecto a hembras de P. filigera fue 1:2. Según Vicentini & Araujo (2003), Moenkhausia sanctae filomenae y Micropogonias furnieri presentaron proporciones 1:1. Sin embargo, la tendencia de encontrar mayor proporción de hembras que de machos en carácidos es más común (Garcia & Roman 2008), lo que ha sido visto en especies como Bryconops, Hyphessobrycon eques, Moenkhausia intermediay Astyanaxfasciatus (Vazzoler 1996). Esta diferencia en la proporción sexual podría ser afectada por factores como la depredación y variaciones en las condiciones ambientales locales (Britton & Moser 1982).
Lourenco et al. (2008) atribuyen la mayor proporción de hembras a la elevada tasa de mortalidad de machos por ser más susceptibles a la depredación debido a que en algunas especies poseen colores llamativos y mayor actividad natatoria, como ocurre con Poecilia reticulata. Souza et al. (2004) indican que la predominancia de hembras de Moenkhausia intermedia (1:4) se debe a diferencias en las tasas de crecimiento entre sexos. En el caso de P. filigera podría existir mortalidad diferencial entre sexos ya que los machos serían más susceptibles a la depredación por presentar una mancha roja en la aleta caudal así como lo que ocurre en otras especies con colores llamativos como Poecilia reticulata (Endler 1980, Reznick et al. 1997). Sin embargo, esta diferencia proporcional de sexos requiere mayores estudios.
Ecología trófica
Prionobrama filigera tuvo una dieta principalmente invertívora, consumiendo 17 tipos de ítems entre insectos, crustáceos y quelicerados, aunque también ictioplancton y escamas (peces), pero los dos últimos con baja frecuencia de ocurrencia. No obstante, otros investigadores clasifican a P. filigera como insectívora (Bojsen 2005) e incluso como micrófaga (Garcia 2005). Esta amplia denominación del hábito alimenticio indica la plasticidad de esta especie, posiblemente dependiendo de la oferta alimenticia y del hábitat donde se encuentra.
Aun cuando se indica que P. filigera tiene plasticidad alimenticia (Garcia 2005), en la TCO Takana tiende a ser especialista, porque el ancho de nicho de Levin fue menor a 0.5. De igual manera, Bojsen (2005) la denomina como especialista con preferencia al consumo de invertebrados terrestres a comparación de Knodus gamma y Jupiaba zonata (carácidos pequeños con los que comparte hábitat) que incluyen en su dieta algas filamentosas y detritus además de invertebrados.
Espectro trófico y su variación por época y hábitat
La riqueza de ítems consumidos fue mayor en época húmeda y menor durante el resto del año (Tabla 4). García (2003), en la cuenca del Río Huallaga (Perú), determinó que Aphyocharax se alimentó de varios tipos de ítems durante aguas altas y se limitó al consumo de de tritus en aguas bajas. Probablemente porque el período de expansión del hábitat favorece una mayor disponibilidad de recursos.
Hymenoptera fue el grupo más consumido. En época seca la frecuencia de consumo fue de 0.32 y en húmeda 0.56. Bojsen (2005), en la Amazonía ecuatoriana, también observó la dominancia de himenópteros (donde las hormigas corresponden al 60% de la oferta alimenticia). Otros carácidos pequeños también presentaron este patrón, entre ellos siete especies de Bryconamericus en la Amazonía ecuatoriana (Escalante & Menni 1999) y Astyanax altiparanae e Hyphessobrycon eilyos en Brasil (Casatti et al. 2003). La mayor frecuencia de consumo de himenópteros (principalmente en época húmeda) en el presente estudio se debe probablemente a su elevada abundanciay a que se hace más disponible durante el ascenso del agua, cuando muchas hormigas son capturadas por caer al agua. Esto también fue observado por Welcomme (1977) y Goulding (1980), quienes además afirman que los himenópteros están entre los macroinvertebrados más abundantes en la Amazonía.
Los dípteros (larvas y adultos) tuvieron la mayor frecuencia de consumo después de los himenópteros. Según Lino et al. (2004), éste es siempre un recurso abundante con ciclos de vida variables y están adaptados a diversos ambientes, desde aguas limpias y oxigenadas hasta con abundante materia orgánica. En la Amazonía boliviana, según Cerqueira (1943) a altitudes menores a 1.200 m abundan dípteros (Culicidae) - vectores de enfermedades como dengue (Aedes aegypti), fiebre amarilla (Haemagogus capricornii), malaria (Anopheles darlingi) y leishmaniasis (Lutzomyiayucumensis) - y muchas especies de carácidos de pequeño a mediano porte (como el caso de P. filigera, cuya dieta incluye un elevado consumo de este grupo) y juveniles de peces grandes son por excelencia grandes consumidores de estos dípteros (Eigenmann 1922).
En lagunas, los copépodos tuvieron mayor frecuencia de consumo después de los himenópteros. Esto podría deberse a las características de hábitat, debido a que el plancton es más abundante en ambientes lénticos que en lóticos. En la laguna Sauce (Perú), la dieta de Prionobrama sp. se constituye de zooplancton, detritus, arena, restos vegetales e insectos (Garcia 2005). Este es un espectro diferente al que determinamos, posiblemente debido a que en la laguna Sauce la oferta de recursos privilegia al plancton (87%) sobre los demás componentes que sólo alcanzan el 13%, lo cual puede estar asociado a su mayor altitud que la zona del presente estudio.
En arroyos, los copépodos fueron el cuarto grupo en importancia de consumo. Aparentemente, porque este hábitat tiene características que favorecen la alta densidad zooplanctónica en relación al río debido a que en arroyos hubo menor corriente y menor turbidez.
En arroyos y lagunas, el consumo de zooplancton ocurrió principalmente durante la época seca y disminuyó durante la crecida. Paggi (1999) determinó que en el Río Paraná existe máxima densidad de zooplancton en época seca y baja densidad en época húmeda. Aun cuando este incremento de biomasa zooplanctónica se deba en general a un efecto de concentración de los individuos y no a un incremento real, la accesibilidad de estos se hace favorable en tales condiciones y lo que podría estar ocurriendo en la cuenca del Río Beni es que P. filigera esté usando este recurso cuando es abundante, es decir durante el descenso de las aguas. En general, esto puede deberse a la concentración de las presas potenciales en menos volumen de agua, con lo que se hacen más accesibles, por tanto el consumo puede concentrarse sólo en algunos de los ítems, mientras en la época húmeda están más dispersos con lo que las opciones de captura se reducen y por ende la captura no sería selectiva sino más oportunista, lo cual es apoyado por los valores del ancho de nicho trófico hallados.
Las diferencias en el espectro trófico vinculados al tipo de hábitat también podrían estar relacionados con el hecho que al parecer existe segregación poblacional por tipo de cuerpo de agua. Por lo tanto, los individuos juveniles podrían tener una dieta diferenciada a la de los adultos.
Aplicaciones al manejo
Conociendo las características reproductivas y tróficas de P. filigera y considerando que se encuentra entre las 30 especies de peces con potencial ornamental con mayor abundancia y amplia distribución (Miranda 2007), podría utilizarse para el desarrollo de una pesquería sostenible en la TCO Takana. Para ello, se debería tomar en cuenta datos como los aquí presentados, los cuales sugieren que la veda sea durante la época de reproducción (Diciembre a febrero) y la cosecha en la seca (entre julio y septiembre) en los arroyos y el Río Beni, excluyendo a las lagunas por ser sitios potenciales de reproducción, con redes de arrastre de 10 mm de malla para capturar individuos mayores de 45 mm. Estas medidas deberían ser complementadas con el establecimiento de cupos de extracción, debido a que una extracción no controlad a a largo plazo pondría en riesgo sus poblaciones localmente y al disminuir sus poblaciones se podría perturbar su rol como controlador natural de mosquitos. El análisis e información presentados son parte de una evaluación general del potencial de aprovechamiento de peces ornamentales en cuerpos de agua de la TCO Takana (Miranda 2007). A partir de ese análisis se han identificado al menos 30 especies con posibilidades de aprovechamiento, entre las cuales se encuentra P. filigera. Es necesario que se genere información similar para el resto de las especies con el fin de que a partir del análisis de esa información se elabore un plan de aprovechamiento sostenible de los peces ornamentales en la TCO Takana.
Agradecimientos
Agradecemos a los financiadores del proyecto: Moore FUNDATION y al proyecto LANDSCAPE USAID. A Robert Wallace de WCS (Wildlife Conservation Society) por sus valiosos comentarios al revisar el manuscrito. A los revisores anónimos por sus valiosos comentarios y sugerencias que enriquecieron el manuscrito. A los pobladores de las comunidades Takana: Carmen del Emero, San Antonio del Tequeje, Copacabana (antes Esperanza del Enapurera), Villa Fátima, Cachichira, Buena Vista, Tumupasa, Santa Rosa de Maravilla, Macahua y San Silvestre que participaron en el trabajo de campo. A Agustín Estívariz, por su valioso apoyo en trabajo de campo. A los asistentes del trabajo de campo y laboratorio: Paola Luna, Juan Victor Cuéllar, Kelvin Herbas, Claudia Zepita. A Julio Pinto y la Unidad de Limnología del Instituto de Ecología de la UMSA por su constante apoyo en todas las fases del estudio. A los dirigentes y técnicos del CIPTA, Neide Cartagena, Celín Quenevo, Jesús Leal, Aizar Terrazas, Antonio Fessy y Felzi González por su constante apoyo e interés en el proyecto.
Referencias
Bagenal, T. & F. Tesch 1978. Age and growth. 101-136 p. En: Tesh E. (ed.). Methods for Assessment of Fish Production in Freshwaters. Third edition. Blackwell Scientific. Publications. Oxford. [ Links ]
Barrera, S., J. Sarmiento. & R. Tejada. 2002. Plan de Manejo del Parque Nacional y Área Natural de Manejo Integrado Madidi. Diagnóstico de ictiofauna del Parque Nacional y Área Natural de Manejo Integrado Madidi. Proyecto de Apoyo al PNANMI, Rurrenabaque. 99 p. [ Links ]
Bazzoli, N. & H. Godinho. 1991. Reproductive biology of the Acestrorhynchus lacustris (Pisces: Characidae) from Tres Marias Reservoir, Brazil. Zoologischer Anzeiger 226: 285-297.
Borges, R. & N. Fabré. 2003. Biologia e diversidade dos recursos pesqueiros da Amazônia. Ibama/Pro Varzea, Manaus. 44 p. [ Links ]
Bojsen, B. 2005. Diet and condition of three fish species (Characidae) of the Andean foothills in relation to deforestation. Environmental Biology of Fishes 73: 61-73.
Britton, R. & M. Moser. 1982. Size specific predation by herons and its effect on the sex-ratio of natural populations of the mosquito fish Gambusia ajfinis Baird and Girard. Oecologia 53:146-151.
Burt A., Kramer L.D, Nakatsuru K. & Spry C. 1988. The tempo of reproduction in Hyphessobrycon pulchripinnis (Characidae), with a discussion on the biology of 'multiple spawning' in fishes. Environmental Biology of Fishes 22(1):15-27.
Ceneviva-Batos, M. & L Casatti. 2007. Oportunismo alimentar de Knodus moenkhausii(Teleostei, Characidae): uma espécie abundante em riachos do sistema do Alto Paraná no Estado de Sao Paulo. Iheringia, Série Zoologia 97: 7-15.
Casatti, L., H. Mendes & K. Ferreira. 2003. Aquatic macrophytes as feeding site f or small fishes in the Rosana Reservoir, Paranapanema River, southeastern Brazil. Brazilian Journal Biology. 63: 213-222.
Cerqueira, N. 1943. Algumas especies novas da Bolivia, e referencia a especies de Haemagogus (Diptera,Culicidae). Memorias do Instituto Osvaldo Cruz 39:1-22.
Concejo Indígena del Pueblo Takana -Wildlife Conservation Society. 2002. Estrategia de desarrollo sostenible de la TCO - Takana con base en el manejo de los recursos naturales 2001-2005. Publicación financiada por el Proyecto Implementación de la Estrategia de Manejo de Recursos Naturales en la TCO Takana. La Paz. 425 p. [ Links ]
Crampton, W. 1999. The impact of the ornamental fish trade on the discus Symphysodon aequifasciatus: a case study from the floodplain forest of Estacao Ecologica Mamiraua. pp. 29-44. En: Padoch, C., J. Ayres, M. Pinedo & A. Henderson (eds) Varzea: Diversity, Development and Conservation of Amazonian's Whitewater Floodplains, Botanical Garden Press, Nueva York. [ Links ]
Eigenmann, C. 1922. Yellow fever and fishes. Zoological Laboratory of Indiana University 193: 204-211.
Endler, J. 1980. Natural selection on color patterns in Poecilia reticulata. Evolution 34(1): 76-91.
Escalante, A. & R. Menni 1999. Feeding ecology of the relict fish Gymnocharacinus bergi, a characid from southern South America. Water South Africa 4: 529-532.
Ferreira, D. 2007. Biology and ecomorphology of stream fishes from the rio Mogi-Guaçu basin, Southeastern Brazil. Neotropical Ichthyology 5: 311-326.
Garcia, J. 2005. Hidrobiología. Zonificación ecológica y económica de la región de San Martín. Gobierno Regional de San Martín. Instituto de investigaciones de la Zonificación Ecológica y Económica de San Martín. Moyobamba. 46 p. [ Links ]
Garcia,C.&C.Roman.2008.Biología alimentaria y reproductiva de Hyphessobrycon poecilioides (Pisces: Characidae) en la cuenca del río La Vieja, Alto Cauca, Colombia. Revista del MuseoArgentino de Ciencias Naturales 10:17-27.
Gerstner, C., H. Ortega, H. Sánchez, & W. Graham. 2006. Effect of the freshwater aquarium trade on wild fish populations in differentially-fished areas of the Peruvian Amazon. Journal of Fish Biology 68: 862-875.
Goulding, M. 1980. The fish and the forest: explorations in Amazonian Natural History. University of California Press, Berkeley. 280 p. [ Links ]
Hunter, J. & S. Goldberg 1980. Spawning incidence and batch fecundity in northern anchovy, Engraulismordax. U.S. FishBulletin 77: 641-652.
Hyslop, E. 1980. Stomach contents analysis. A review of methods and their application. Journal of Fish Biology 17: 411-429.
Krebs, J. 1999. Ecological methodology. Harper Collins, Nueva York. 654 p. [ Links ]
Lino, F., O. Fossati, R. Apaza & E. Gotilla. 2004. Macroinvertebrados de las lagunas. p. 18. En: Poully, M., S. Beck, M. Moraes R. & C. Ibañez (eds.) Diversidad Biológica en la Llanura de Inundación del Río Mamoré. Importancia Ecológica de la Dinámica Fluvial. Centro de Ecología Simón I. Patiño, Santa Cruz. [ Links ]
Lorini, L., J. Quintanilla, J. Peña, R. Marín, & E. Salas. 1989. Diagnóstico del estado actual de los recursos pesqueros de la cuenca amazónica boliviana. Centro de Estudios Ecológicos y de Desarrollo Integral, La Paz. 143 p. [ Links ]
Loubens, G. & J. Aquim. 1986. Sexualidad y reproducción de los principales peces de la cuenca del río Mamoré, Beni, Bolivia. ORSTOM - CORDEBENI -UTB,Trinidad. 45 p. [ Links ]
Lourenco, L., L. Mateus & N. Machado. 2008. Sincronia na reproducao de Moenkhausia sanctaefilomenae (Steindachner) (Characiformes: Characidae) na planicie de inundacao do rio Cuibá, Pantanal Mato-Grossense, Brasil. RevistaBrasileira de Zoología 25: 20-27.
Mancera-Rodríguez, N. & R. Álvarez-León. 2008. The trade of ornamental fishes in Colombia. Acta Biológica Colombiana 1:23-52.
Miranda, G. 2007. Plan de manejo para la cosecha experimental de peces ornamentales en la TCO-Takana. WCS - Bolivia. Concejo Indigena del Pueblo Takana, La Paz ciudad. 62 p. [ Links ]
Myers, N., C. Mittermeier, G. Da Fonseca & J. Kent. 2000. Biodiversity hotspots for conservation priorities. Nature 403: 853-858.
Morison, A. 2004. Imput and output controls in fisheries management: a plea for more consistency in terminology. Fisheries Management and Ecology 11:411-413.
Navarro, G. & M. Maldonado (eds). 2002. Geografía ecológica de Bolivia: vegetación y ambientes acuáticos. Centro de Ecología Simón I. Patiño. Cochabamba. Bolivia. 719 p. [ Links ]
Norris, S. & N. Chao. 2002. Buy a fish save a tree? Safeguarding sustainability in an Amazonian ornamental fishery. Conservation in Practice 3: 30-35.
Paggi, J. 1984. Distribución estacional del zooplancton. Estudios limnológicos de una sección transversal del tramo medio del río Paraná. Revista de la Asociación de Ciencias Naturales del Litoral 15:135-155.
Reis, R., S. Kullander & C. Ferraris. 2004. Checklist of fresh-water fishes of South and Central America. Edipucrs, Porto Alegre. 729 p. [ Links ]
Reznick, D.N. Shaw H.F, Rodd F.H, Shaw G.R. 1997. Evaluation of the rate of evolution in natural populations of Guppies (Poecilia reticulata). Science 275(5308): 1934-1937.
Rodríguez, A., R. Santos, E. Campos, J. Camara & J. Mandelli. 1991. Tipo de desova e fecundidade de Moenkhausia intermedia (Eigerman, 1908) na represa de Ibitinga, Estado de São Paulo, Brasil. Brazilian Journal Veterinary Research Seropédica 28: 201-206.
Sato, Y., E. Sampaio, N. Fenerich-Verani & J. Verani. 2006. Biología reproductiva y reproducción inducida de dos especies de Characidae (Osteichthyes, Characiformes) de la cuenca de San Francisco, Minas Gerais, Brasil. Revista Brasileira de Zoología 23: 267-273.
SENAHMI (Servicio Nacional de Hidrografía Nacional). 1998. Hidrografía de Bolivia. Primera Edición, La Paz. 359 p. [ Links ]
Souza, R., G. Santos & N. Bazzoli. 2004. Reproductive biology of Moenkhausia intermedia (Eigenmann) (Pisces, Characiforormes) in Itumbiara reservoir, Goiás, Brazil. Revista Brasileira de Zoologia 2: 519-524.
Vazzoler, A. 1996. Biologia da reproducao de peixes teleosteos. Editora da Universidade Estadual de Maringa. Sao Paulo. 169 p. [ Links ]
Vicentini R. & F. Araújo 2003. Sex ratio size structure of Micropogonias furnieri (Desmarest, 1823) (Perciformes, Sciaenidae) in Sepetiba bay, Rio de Janeiro, Brasil. Journal of Biology 63: 559-566.
Welcomme, L. 1977. Fisheries ecology of floodplain rivers. Longman. Londres. 312 p. [ Links ]
Artículo recibido en: Febrero de 2011.
Manejado por: Diana Silva
Aceptado en: Abril de 2011.












 uBio
uBio 


