Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Ecología en Bolivia
versión impresa ISSN 1605-2528versión On-line ISSN 2075-5023
Ecología en Bolivia v.44 n.1 La Paz mayo 2009
Nota
Uso de metodologías de censos muestrales indirectos de fecas para evaluar endoparásitos en mamíferos silvestres: Un ensayo en la Reserva Privada de San Miguelito, Santa Cruz, Bolivia
Use of indirect census methodologies of feces to evaluate endoparasites in wild mammals: a survey performed in the private reserve of San Miguelito, Santa Cruz, Bolivia
Lucio Fabián Beltrán-Saavedra1, 2, Sixto Angulo3 & José Luis Gonzales4
1Universidad Técnica Privada Cosmos, Facultad de Ciencias de la Salud, Carrera de Medicina Veterinaria y Zootecnia, Cochabamba, Bolivia.
2 Dirección actual: Avenida 16 de Julio, Ed. Alameda, Bloque B, Dpto. # 406. La Paz, Bolivia. Email: fabeltrans@yahoo.com
3 Wildlife Conservation Society, dirección postal: 6272, Santa Cruz, Bolivia.
4 Central Veterinary Institute of WUR, Houtribweg 39.8821RA, Lelystad, Holanda
Las enfermedades están presentes en todos los sistemas biológicos participando en la regulación de la diversidad biológica a través de procesos evolutivos, como la distribución geográfica de las especies y la especiación (Suzán-Azpiri et al. 2000). Para que esto ocurra, las enfermedades pueden tener una frecuencia normal de presentación en una población, situación que es conocida como endemia. Los incrementos irregulares, asociados generalmente a factores externos, son conocidos como epidemias (Thrusfield 1990), que conllevan consecuencias negativas en las poblaciones silvestres afectadas y además pueden afectar a la sanidad de los animales domésticos y viceversa, así como a la salud humana (Vallat 2008). Por ejemplo, los endoparásitos propios de camélidos sudamericanos y transmitidos por ovejas, correlacionados a varios factores antropogénicos generaron una mortandad del 80% de poblaciones silvestres de guanacos (Lama guanicoe Müller 1776) de la Reserva de Vida Silvestre Cabo Dos Bahías en Chubut (Argentina) (Beldomenico et al. 2003, Baldi et al. 2006). En Bolivia existen estudios que identificaron endoparásitos mediante análisis coproparasitológico de muestras fecales obtenidas de mamíferos silvestres de vida libre por capturas (Fiorello et al. 2006, Deem et al. 2008) y de cacería de subsistencia (Deem et al. 2004), para evaluaciones sanitarias.
En los censos muestrales indirectos comúnmente se aplican capturas, observaciones directas y signos indirectos, como el conteo de huellas y la identificación de heces como estimadores para determinar especies en una zona o un hábitat específico (Painter et al. 1999). El uso de heces permite obtener datos no invasivos de la biología animal de fauna silvestre como identificación taxonómica de dietas (Pacheco et al. 2004), medición de hormonas y su relación con la conducta reproductiva (Hernández-Jáuregui et al. 2005) y biología molecular para identificar taxones animales (Prug & Ritland 2005), pero también pueden aprovecharse para investigar endoparásitos. Por ejemplo, Page et al. (2001), estudiaron la dinámica de transmisión del nemátodo Baylisascaris procyonis (Sprent 1968) entre granívoros y mapaches (Procyon lotor, Linnaeus 1758) en letrinas y Marathe et al. (2002) estudiaron patrones de abundancia y diversificación de endoparásitos heteroxenos, dispersados vía fecal por tigres (Panthera tigris, Linnaeus 1758) mediante seguimientos por radiotelemetría en la reserva Tadoba-Andahari Tiger (India). Por ende, el muestreo de heces puede servir para obtener datos no invasivos sobre los endoparásitos propios de los ecosistemas y/o alertar sobre su introducción por actividades antropogénicas como la ganadería.
La Reserva Privada de San Miguelito dedica aproximadamente 13.000 ha de sus tierras a la conservación de una alta riqueza de especies de mamíferos (n= 73) y su principal actividad productiva es el ganado vacuno de corte (Rumiz et al. 2002). Lo que implica una coexistencia de animales silvestres, domésticos y humanos, propiciando una dinámica de introducción y diseminación de enfermedades que es necesario conocer para la adecuada toma de decisiones en futuras medidas de manejo. El objetivo del presente trabajo fue utilizar registros básicos indirectos aplicados en censos muestrales para colectar heces de mamíferos silvestres y realizar una evaluación de los endoparásitos presentes en estos animales.
La Reserva Privada de San Miguelito está ubicada a 180 km al noreste de la ciudad de Santa Cruz, en las provincias Velasco y Ñuflo de Chávez (17°00’37”-17°12’21”S y 61°30’39”62°00’00” W) con una extensión de 38 684.39 ha; dentro esta reserva se encuentra la zona de “Los Remates” con una extensión de 4 346.25 ha en la cual se realizó el presente estudio.
Durante una campaña de estudios biológicos, en febrero de 2004, realizamos un ensayo colectando muestras fecales frescas de jaguares (Panthera onca, Linnaeus 1758) (n= 2) y de Mazama spp. (n= 2), dando un total de cuatro. Estas muestras se colectaron del suelo y para identificar al mamífero del que procedían las mismas, se tomó en cuenta la morfometría y contenido no digerible en carnívoros (Chame 2003), además se identificó las huellas in situ según Painter et al. (1999) y Simonetti & Huareco (1999).
Todas las muestras fueron conservadas en formol al 10% y guardadas en frascos plásticos herméticos, codificados hasta su posterior análisis coproparasitológico empleando los métodos de flotación con solución sobresaturada de cloruro de sodio de Willis y el método de sedimentación modificada de Niah. A partir de los mismos y por microscopía de luz, se realizó la identificación morfológica y métrica (en micras) de huevos de helmintos para constatar los taxones correspondientes y descritos previamente por otros autores (Ueno & Gutierres 1983). Las muestras fueron analizadas en el Laboratorio de Investigación y Diagnóstico Veterinario (LIDIVET) de Santa Cruz.
De las cuatro muestras analizadas, en tres se observaron formas parasitarias mixtas (dos muestras identificadas de jaguares y una muestra identificada de Mazama spp.) y una muestra (Mazama spp.) fue negativa (tabla 1).
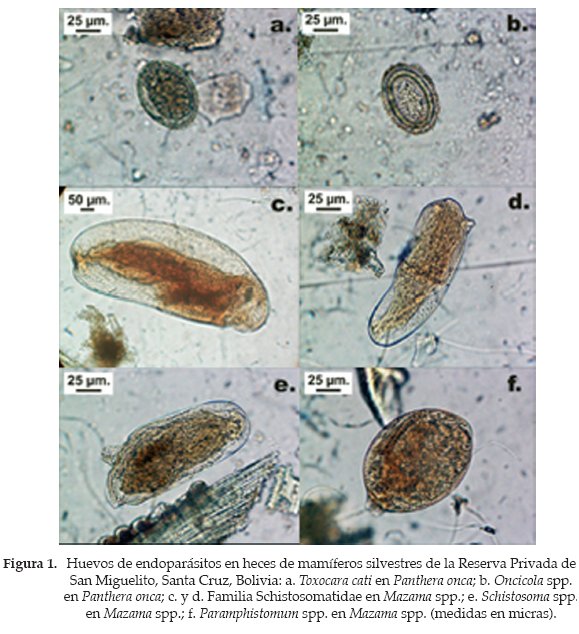
En el orden Carnivora, dos muestras fecales identificadas de jaguares presentaron huevos de nemátodos Toxascaris leonina (v. Linstow 1902) y Toxocara cati (Schrank 1788) (Fig. 1a) y huevos de acantocéfalos Oncicola spp. (Fig. 1b). En una de las muestras fecales identificadas como de un jaguar, también se encontraron huevos de nemátodos Ancylostoma spp. así como huevos pertenecientes al género Capillaria y huevos operculados de cestodos del género Spirometra.
En una de las muestras fecales de ciervos del género Mazama (Orden Artiodactyla) - ya que no fue posible distinguir las huellas entre urinas (Mazama americana Erxleben 1777) y huasos (Mazama gouazoubira Fischer 1814) debido al sustrato rocoso - se observaron huevos de tremátodos del género Paramphistomum (Fig. 1f). También se observaron huevos de tremátodos de la familia Schistosomatidae (Poche 1907) de distintos tamaños, pero sus géneros no fueron identificados (Figs. 1c, d) y Schistosoma spp. (Fig. 1e), estos últimos podrían corresponder a S. mansoni por la morfometría observada (Sambon 1907).
La existencia de Schistosoma en el país puede ser respaldada por la presencia de caracoles de agua dulce del género Biomphalaria, que actúan como hospederos intermediarios. En Bolivia d’Orbygni (1835) registró a B. tenagophila en la localidad de Guayaramerín (citado por Paraense 2001) y Pointier et al. (2002) identificaron B. amazonica (Paraense 1966) en una estancia ganadera de la provincia Warnes. La identificación de huevos del género Schistosoma abre la posibilidad de la presencia de esta zoonosis tropical en Bolivia, con importancia en salud pública (WHO 1993) y estos resultados deben confirmarse, buscando identificar nuevamente el parásito en humanos como en mamíferos domésticos y silvestres. El hallazgo de huevos de acantocéfalos del género Oncicola en dos muestras de Panthera onca y del tremátodo del género Schistosoma en una muestra de Mazama spp. son los primeros reportes de identificación de estos géneros en Bolivia.
La utilización de recursos básicos de censos muestrales indirectos no solamente permitieron identificar a mamíferos silvestres, sino también realizar evaluaciones sanitarias indirectas dando una orientación de la ocurrencia de los parásitos en estos animales sin el inconveniente de ejecutar capturas por trampeo, que en ciertas especies puede resultar factible pero en otras puede resultar dificultoso, especialmente en áreas con vegetación de bosques ribereños y transicionales del paisaje Chiquitano, como se da en la Reserva Privada de San Miguelito. Los muestreos indirectos tienen la ventaja de ser más sencillos de aplicar y suelen ser una alternativa más económica y muchas veces la única para estudiar la distribución y abundancia de determinadas especies raras o difíciles de observar (Painter et al. 1999).
Sin embargo, la colecta de heces implica ciertos requisitos para que sean útiles en coproparasitología y son: a) Heces frescas (colectadas en la mañana, al atardecer o a la noche) de las cuales se tiene la certeza de ser recientes y no asoleadas o viejas porque los huevos de helmintos eclosionan, b) heces no contaminadas con tierra, ya que debe eliminarse con un cuchillo la parte que estuvo en contacto directo con el suelo para descartar la posibilidad de contaminación por geo-helmintos que podrían derivar en diagnósticos erróneos, c) la conservación pronta en formol al 10% para garantizar resultados confiables después de las campañas y d) en caso de los censos muestrales indirectos existe la posibilidad de colectar muestras fecales de un mismo individuo en distintos sitios, que podrían diferenciarse por medio de estudios de biología molecular usando otras secciones de cada una de las muestras fecales. En este estudio se eliminaron muestras fecales que no cumplían los requisitos a, b y c de colecta, según lo expuesto.
La inclusión exitosa de coproparasitología en metodologías de censos muestrales indirectos sugiere que se podría contribuir de este modo al desarrollo de programas de control de enfermedades, permitiendo una mejor evaluación de los riesgos sanitarios a los que son expuestos los animales silvestres por el cada vez mayor contacto con animales domésticos. Por lo que de esta manera se puede entender mejor el rol epidemiológico que pueden jugar los animales silvestres en el control de enfermedades, como las parasitosis precautelando la salud de los ecosistemas.
Por ejemplo, la colecta de heces en ungulados silvestres podría ser una herramienta de monitoreo de enfermedades parasitarias, de probable ciclo doméstico – silvestre, con el objeto de controlar posibles efectos negativos en la población silvestre, como aquellos observados en guanacos de Argentina y que poseían un origen antropogénico (Beldomenico et al. 2003).
La posible aplicación de estudios parasitarios indirectos correlacionados a estudios poblacionales por censos muestrales puede ser una opción para muchas especies de mamíferos, generando además de los datos de interés biológico aquellos de interés sanitario que se complementan al momento de plantear y ejecutar acciones de conservación donde interactúan la biología con la medicina veterinaria.
La identificación de mamíferos silvestres por morfometría fecal y de huellas para realizar evaluaciones coproparasitológicas permitió generar información endoparasitaria en jaguares y ciervos de Mazama spp. de la Reserva Privada de San Miguelito en forma indirecta y rápida.
Agradecimientos
A las biólogas Claudia Venegas, Juliet Healy y Rosario Arispe que apoyaron en el trabajo de campo. Al Dr. Gustavo Morales ex director del Laboratorio de Investigación y Diagnóstico Veterinario por brindar los ambientes, equipo y material necesario para los análisis. A los Drs. Andrew Noss y Damian Rumiz, coordinadores de WCS-Santa Cruz (Wildlife Conservation Society), por el apoyo personal e institucional, que permitieron el desarrollo de los trabajos de campo. Al Dr. Félix Saavedra ex jefe de la carrera de Medicina Veterinaria y Zootecnia de la Universidad Técnica Privada Cosmos, por el apoyo personal e institucional.
Referencias
Baldi, R., D. De Lamo, M. Failla, P. Ferrando, M. Funes, P. Nugent, S. Puig, S. Rivera & J. Von Thüngen. 2006. Plan nacional del manejo del guanaco (Lama guanicoe) -República Argentina. Anexo 1. Secretaría de Ambiente y desarrollo Sustentable de la Nación, Buenos Aires. 40 p.
[ Links ]Beldomenico, P. M., M. Uhart, M. F. Bono, C. Marull, R. Baldi & J. L. Peralta. 2003. Internal parasites of free - ranging Guanacos from Patagonia. Veterinary Parasitology 118: 71-77.
[ Links ]Chame, M. 2003. Terrestral mammal feces: a morphometric summary and description. Memorias del Instituto Oswaldo Cruz 98(1): 71-94.
[ Links ]Deem, SH., A. J. Noss, R. Villarroel, M. M. Uhart & W. B. Karesh. 2004. Disease survey of free-ranging Grey Brocket Deer (Mazama gouazoubira) in the Gran Chaco, Bolivia. Journal of Wildlife Diseases 40(1): 92-98.
[ Links ]Deem, SH., E. Bronson, S. Angulo & L. H. Emmons. 2008. Monitoreo sanitario del borochi (Chrysocyon brachyurus) en el Parque Nacional Noel Kempff Mercado, Bolivia. Revista Boliviana de Ecología y Conservación Ambiental 22: 41-50.
[ Links ]Fiorello, C. V., R. G. Robbins, L. Maffei & S. E. Wade. 2006. Parasites of free-ranging small canids and felids in the Bolivian Chaco. Journal of Zoo and Wildlife Medicine 37(2): 130-134.
[ Links ]Hernández-Jáuregui, D. Ma., F. Galindo, R. A. Valdez, M. Romano & A. Schuneman. 2005. Cortisol en saliva, orina y heces: Evaluación no invasiva en mamíferos silvestres. Veterinaria México 36(3): 325-337.
[ Links ]Marathe, R. R., S. S. Goel, S. P. Ranade, M. M. Jog & M. V. Watve. 2002. Patterns in abundance and diversity of faecally dispersed parasites of tiger in Tadoba National Park, central India. BioMed Central Ecology 2: 6.
[ Links ]Pacheco, L. F., A. Lucero & M. Villca. 2004. Dieta del puma (Puma concolor) en el Parque Nacional Sajama, Bolivia y su conflicto con la ganadería. Ecología en Bolivia 39(1): 75-83.
[ Links ]Page, L. K., R. K. Swihart & K. R. Kazacos. 2001. Seed preferences and foraging by granivores at raccoon letrines in the transmission dynamics of the Raccoon Roundworm (Baylisascaris procyonis). Canadian Journal of Zoology 79: 616-622.
[ Links ]Painter, L., D. Rumiz, D. Guinart, R. Wallace, B. Flores & W. Townsend. 1999. Técnicas de investigación para el manejo de fauna silvestre. Manual del III Congreso Internacional sobre Manejo de Fauna Silvestre en la Amazonía, Documento técnico 82/1999, Proyecto de Manejo Forestal Sostenible BOLFOR, Santa Cruz. 81 p.
[ Links ]Paraense, W. L. 2001. The schistosome vectors in the Americas. Memorias del Instituto Oswaldo Cruz 96: 7-16.
[ Links ]Pointier, J. P., W. L. Paraense, R. J. Dejong, E. S. Loker, M. D. Bargues & S. Mas-Coma. 2002. A potential snail host of schistosomiasis in Bolivia: Biomphalaria amazonica Paraense, 1966. Memorias del Instituto Oswaldo Cruz 97(6): 793-796.
[ Links ]Prug, L. R. & C. E. Ritland. 2005. Molecular testing of observer identification of carnivore feces in the fi eld. Wildlife Society Bulletin 33(1): 189-194.
Rumiz, D. I., A. F. Fuentes, K. Rivero, J. L. Santiváñez, E. Cuellar, R. Miserendino, Fernández, L. Maffei & A. B. Taber. 2002. La biodiversidad de la Estancia San Miguelito, Santa Cruz - Bolivia: Una justificación para establecer reservas privadas de conservación. Documentos Ecología en Bolivia, Serie Biodiversidad (1): 1-67.
[ Links ]Simonetti, J. A. & I. Huareco. 1999. Uso de huellas para estimar diversidad y abundancia relativa de los mamíferos de la Reserva de la Biosfera – Estación Biológica del Beni, Bolivia. Mastozoología Neotropical 6(1): 139-144.
Suzán-Azpiri, G., F. Galindo & G. Ceballos. 2000. La importancia del estudio de enfermedades en la conservación de fauna silvestre. Veterinaria México 31(3): 223-230.
[ Links ]Thrusfield, M. 1990. Epidemiología veterinaria. Acribia, S.A., Zaragoza. 339 p.
[ Links ]Ueno, H. & V. C. Gutierrez. 1983. Manual para diagnóstico das helmintoses de rumiantes. Facultade de Medicina Veterinaria, Universidade Federal do Rio Grande do Sul Porto Alegre - Japan Internacional Cooperation Agency, Porto Alegre. 176 p.
[ Links ]Vallat, B. 2008. Mejora de la vigilancia de los animales salvajes para proteger su salud y protegernos de las enfermedades que nos transmiten. Editorial del Director General, Boletín Organización Mundial de Sanidad Animal, (3): 1-3.
[ Links ]WHO (World Health Organization). 1993. The control of schistosomiasis. Second report of the WHO expert committee. World Health Organization Technical Report Series (728): 1-86.
[ Links ]
Nota recibida en: Abril de 2009.
Manejado por: Luis F. Aguirre.
Aceptado en: Junio de 2009.












 uBio
uBio