Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Ecología en Bolivia
Print version ISSN 1605-2528On-line version ISSN 2075-5023
Ecología en Bolivia vol.42 no.1 La Paz Apr. 2007
Artículo
Diversidad y ecología de epífitas vasculares en bosques montanos primarios y secundarios de Bolivia
Diversity and ecology of vascular epiphytes in natural montane forests and fallows of Bolivia
Thorsten Krömer1, 2*, S. Robert Gradstein1 & Amparo Acebey3
1Institute of Plant Sciences, Systematic Botany, University of Göttingen, Untere Karspüle 2, 37073 Göttingen, Alemania *Autor de correspondencia: tkroemer@ibiologia.unam.mx
2Dirección actual: Centro de Investigaciones Tropicales, Universidad Veracruzana, Interior de la Ex-hacienda Lucas Martín, Privada de Araucarias s/n, Col. 21 de Marzo, Xalapa, C.P.
1019 Veracruz, México
3Institute for Crop and Animal Production in the Tropics, University of Göttingen, Grisebachstr. 6, 37077 Göttingen, Alemania
Resumen
La diversidad de epífitas vasculares en el bosque natural y barbechos adyacentes de hasta 15 años fue estudiada en tres localidades diferentes en los Yungas de Bolivia - en bosque piedemonte en el Parque Nacional Madidi (350 m), en bosque submontano cerca de Sapecho (500-1.200 m) y en bosque montano en el Parque Nacional Cotapata (1.500-2.200 m). Aproximadamente 530 especies de epífitas (25 familias, 113 géneros) fueron registradas. Las orquídeas fueron la familia más importante en lo que se refiere a números de especies, seguida por los helechos. Una parcela de 1.0 ha compuesta de ocho subparcelas con una superficie total de 0.32 ha tenía 175 especies, mostrando que estos bosques montanos forman parte de los más ricos a nivel mundial, en lo que se refiere a la diversidad de epífitas. El pico máximo de diversidad de epífitas vasculares a altitudes intermedias postulada previamente fue confirmado. Los barbechos tenían 60-70% menos especies que el bosque natural adyacente. El número de especies de orquídeas, bromeliáceas, Hymenophyllaceae y Grammitidaceae era mucho más bajo en barbechos que en el bosque primario, pero la riqueza era similar de aráceas hemiepifíticas, Polypodiaceae y Aspleniaceae. La reducción de diversidad de especies de epífitas en barbechos puede explicarse por las características estructurales y la joven edad de los árboles, la falta de una capa de musgos densa y el microclima más seco en este tipo de vegetación.
Palabras clave: Bosques andinos, epífitas vasculares, gradiente altitudinal, vegetación secundaria, Bolivia.
Abstract
We studied vascular epiphyte diversity in primary forest and adjacent 15 yr. old fallows in three different sites in the Yungas of Bolivia - in Andean foothill forest in the Parque Nacional Madidi (350 m), in submontane forest near Sapecho (500-1,200 m) and in montane forest in the Parque Nacional Cotapata (1,500–2,200 m). About 530 species of epiphytes (25 families, 113 genera) were recorded. Orchids were the most important family in terms of species number, followed by ferns. A 1.0 ha plot composed of eight subplots with a total surface of 0.32 ha of montane forest had up to 175 species, showing that these forests rank among the richest worldwide in terms of epiphyte diversity. A mid-elevation peak postulated previously for vascular epiphyte diversity was confirmed. Fallows had 60-70% fewer species than neighboring natural forest. The number of species of orchids, bromeliads, Hymenophyllaceae, and Grammitidaceae were much lower in fallows than in primary forest, but hemiepiphytic aroids, Polypodiaceae, and Aspleniaceae were similar. Reduction of epiphytic species diversity in fallows can be explained by structural characteristics and the young age of the fallow trees, the lack of a dense moss cover, and the drier microclimate in the fallows.
Key words: Andean forests, elevational gradient, secondary vegetation, vascular epiphytes, Bolivia.
Introducción
El bosque montano tropical de los Andes es uno de los ecosistemas más ricos del mundo en lo que se refiere al número de especies (Barthlott et al. 1996). Las epífitas vasculares, incluyendo orquídeas, aráceas, bromeliáceas y helechos, entre otras, son un componente importante de estos bosques, tanto en lo que se refiere a la riqueza de las especies (Gentry & Dodson 1987, Ibisch 1996, Nieder et al. 1999, Krömer et al. 2005), como a su rol en los ciclos de agua y nutrientes (Nadkarni 1984, Coxson & Nadkarni 1995). Actualmente estos bosques están desapareciendo rápidamente, como resultado de la creciente presión humana en la región. Se conoce muy poco sobre el impacto de deforestación a la diversidad de epífitas en bosques montanos y mucho menos sobre la ecología de epífitas en los bosques secundarios (p.e. Hietz-Seifert et al. 1996, Barthlott et al. 2001). Por esta razón, la meta básica de este estudio era comparar la diversidad de epífitas vasculares en el bosque montano maduro y barbechos.
Métodos
Área de estudio
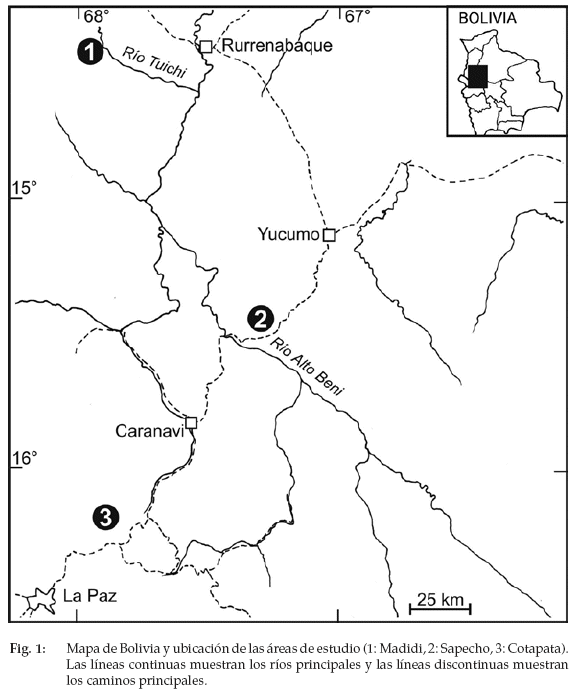
El estudio fue realizado en tres sitios en las laderas orientales húmedas de los Andes en el Departamento de La Paz, Bolivia (Fig. 1). La área de estudio más baja se localiza a 350 m en los alrededores del Río Eslabón (14°27’ S, 67°56’ W) en el Parque Nacional-Área Natural del Manejo Integrado (PN-ANMI) Madidi (Acebey & Krömer 2001). La precipitación anual es aproximadamente de 2.000 mm y la temperatura promedio de 24-26°C (Ribera 1992). El bosque de esta área tiene más de 150 especies de árboles >10 cm DAP por la hectárea (M. Macía com. pers. 2005), con una altura del dosel promedio de aproximadamente 30 m y árboles emergentes que frecuentemente superan 40 m. Las palmeras son de gran importancia en la estructura del bosque, caracterizando el denso estrato intermedio.
La segunda área de estudio se localiza arriba del pueblo de Sapecho (450 m), a lo largo del río Alto Beni hasta 1.200 m en las laderas de la Serranía Marimonos (15° 27’-32’ S, 67° 18’-23’ W). La precipitación anual varía de 1.500 mm en el fondo del valle hasta 2.000 mm en las laderas más altas, mientras que la temperatura promedia oscila entre 24-25°C (Elbers 1995). El bosque natural es un bosque submontano siempreverde o semi-caducifolio que se caracteriza por tener árboles altos de 30-40 m con un estrato de arbustos bien desarrollado. La diversidad de árboles promedio es de cerca de 120 especies por ha (Seidel 1995). Como resultado del crecimiento poblacional, las laderas más bajas de la Serranía Marimonos están cubiertas por un mosaico de campos de cultivo y barbechos de hasta 15 años con una altura del dosel de 12-15 m (Krömer & Gradstein 2003).
La tercera área de estudio se localiza a 1.500-2.200 m en los alrededores de la Estación Biológica Tunquini en el PN-ANMI Cotapata (16°11’-13’ S, 67°51’-54’ W). La precipitación anual media es de 2.500 mm y la temperatura media anual promedia de 13-19°C entre 1.500-2.500 m (Bach et al. 2003, M. Schawe, com. pers. 2005). Las laderas muy inclinadas a estas elevaciones están cubiertas por un bosque montano siempreverde que es de 15-25 m de alto con estratos densos de arbustos y hierbas. La diversidad de árboles es poco conocida pero probablemente más baja que en Sapecho. Como resultado de frecuentes derrumbes naturales y conversión de pequeñas parcelas de bosque para uso agrícola, las laderas más bajas están cubiertas por un mosaico de bosques en diferentes etapas de sucesión que incluyen barbechos de hasta 15 años con una altura del dosel de 8-12 m (Krömer & Gradstein 2003).
Muestreo
El estudio de la diversidad de epífitas vasculares en bosque natural y barbechos de 15 años adyacentes se basó en un método de muestreo representativo en parcelas de 1.0 ha compuesta de ocho subparcelas con una superficie total de 0.32 ha (Gradstein et al. 2003, Krömer 2003). En Madidi se muestreó una parcela de bosque primario (350 m de altitud), en Sapecho un barbecho y cinco parcelas de bosque (500-1.200 m) y en Cotapata dos barbechos y tres parcelas de bosque (1.500-2.200 m). En cada parcela de bosque, se muestrearon ocho árboles maduros del dosel desde la base a la parte exterior de la copa. Se registraron todas las especies de epífitas vasculares dentro de las cinco zonas verticales según Johansson (1974), usando cuerdas y equipo modificado del alpinismo (Single Rope Technique, Perry 1978). Esta técnica permite un inventario casi completo de la diversidad de epífitas del dosel en el bosque (Flores-Palacios & García-Franco 2001).
Debido a que la flora de epífitas en el sotobosque es diferente a la de los árboles del dosel, también se muestrearon epífitas de los arbustos y árboles jóvenes que se encontraban alrededor de cada árbol del dosel muestreado en una subparcela de 20 x 20 m, usando pico de loro y binoculares (Shaw & Bergstrom 1997, Gradstein et al. 2003, Krömer et al. 2007). De la misma manera, se realizaron inventarios en barbechos, que están constituidos generalmente por árboles demasiado frágiles para ser trepados. Los muestreos fueron realizados en ocho subparcelas de 400 m2, los cuales estaban irregularmente distribuidos en cada parcela de 1.0 ha. Se necesitaron aproximadamente ocho horas de trabajo para cada inventario completo de cada subparcela realizado por dos personas (un especialista y un ayudante de campo), incluyendo el muestreo de un árbol y el procesamiento de los especímenes.
Se anotó la presencia y ausencia para todas las especies. Los especímenes colectados fueron depositados en el Herbario Nacional de Bolivia (LPB), con duplicados en los siguientes herbarios: Universidad de Göttingen (GOET), Marie Selby Botanical Gardens, Sarasota (SEL), Missouri Botanical Garden, St. Louis (MO) y herbario Jepson, de la Universidad de California, Berkeley (UC). Para el análisis de los datos se diferenciaron las familias de epífitas neotropicales dominantes - Araceae, Bromeliaceae, Orchidaceae, Piperaceae y Pteridophyta (tratada aquí como una familia por la similitud ecológica de todos los taxa incluidos) - así como todas las otras familias combinadas (en otros).
Resultados
En nueve parcelas (de 0.32 ha cada una) fueron registradas aproximadamente 530 especies de epífitas vasculares en 25 familias y 113 géneros: 89 en bosque piedemonte de Madidi (14 familias, 42 géneros) (Acebey & Krömer 2001), 255 en el bosque submontano de Sapecho (23 familias, 87 géneros) y 292 en el bosque montano de Cotapata (24 familias, 76 géneros) (Krömer 2003). La familia de las orquídeas fue la más rica en especies con aproximadamente 221 especies registradas, seguida por pteridófitas (163), aráceas (43), bromeliás (36), peperomias (34) y las otras familias restantes en conjunto (32). Las comunidades de especies en Sapecho y Cotapata eran notablemente diferentes; sólo 54 especies (11%) ocurrieron en ambas localidades, indicando la alta diversidad beta de las epífitas.
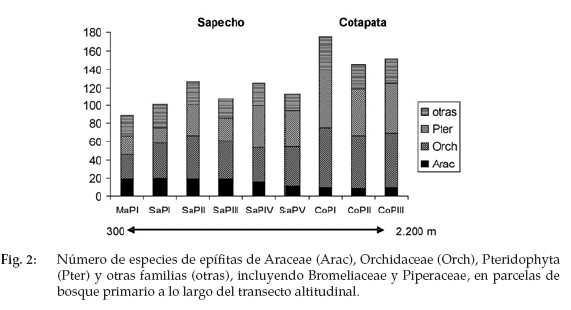
El número de especies (diversidad alfa) aumenta linealmente a lo largo del gradiente altitudinal estudiado desde el bosque piedemonte (89 spp.) pasando por el bosque submontano (101-125 spp.) hasta el bosque medio-montano, donde se alcanzó el valor máximo a una altitud aproximada de 1.600 m (175 spp.); posteriormente este disminuye gradualmente a 150 spp. en 2.200 m de altitud (Fig. 2). Las aráceas muestran una disminución de especies constante a medida que la altitud acrecienta, mientras que las orquídeas y helechos muestran un claro incremento. En dos parcelas localizadas sobre o cerca de crestas a 1.200 m y 1.850 m se registró un número de especies notablemente más bajo.
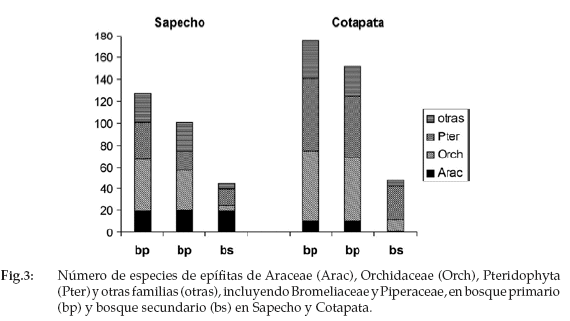
La diversidad de epífitas en barbechos de 15 años mostró una reducción dramática en comparación con la del bosque maduro, sobre todo de orquídeas, bromeliáceas, Hymenophyllaceae y Grammitidaceae. Los barbechos tenían 60-70% especies menos que el bosque natural adyacente (Fig. 3). Sin embargo, la riqueza de las especies no fue disminuida en aráceas hemiepifíticas, Polypodiaceae y Aspleniaceae. En Sapecho, las aráceas fueron el grupo más numeroso de epífitas en los barbechos (43% de todas especies registradas), mientras que en Cotapata el grupo dominante fueron los helechos (ca. 60%). Otras familias, como Cactaceae, Ericaceae y Gesneriaceae, estaban representadas por pocas especies de epífitas en las parcelas de bosque y completamente ausentes en los barbechos.
Discusión
Diversidad de epífitas en el bosque natural
El número de especies total registrado en este estudio es muy alto y sugiere que el número de epífitas vasculares para los Yungas de Bolivia entre 500-2.500 m excede a las 800 especies estimadas por Ibisch (1996). Esto coincide con datos publicados por Vásquez et al. (2003) que registraron para esta ecoregión entre 1.000-3.500 m un total de 903 especies de orquídeas, de las cuales al menos un 80% tiene hábito epifítico. Sin embargo, el número estimado todavía es mucho más alto (hasta el doble), mostrando claramente que los Yungas son el centro de diversidad de orquídeas y epífitas en general, aunque solo cubren un 4% del territorio boliviano. Esta enorme riqueza de orquídeas es el resultado de una intensa especiación debido a la interacción de múltiples factores (Gentry & Dodson 1987, Ibisch 1996, Ackerman 1998).
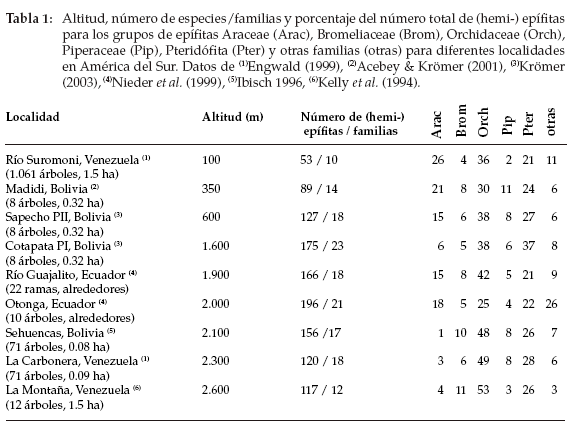
La comparación de nuestros datos con inventarios realizados en otros países andinos a elevaciones y tamaños de parcelas similares mostró que Cotapata se encuentra entre las áreas más ricas en epífitas vasculares del mundo (Tabla 1). Con 175 especies en 0.32 ha, la parcela PI a 1.600 m tiene el mismo número de especies como parcelas inventariadas en otras partes de Bolivia (Ibisch 1996) y Ecuador (Nieder et al. 1999); pero es más rica que en los bosques andinos de Venezuela (Kelly et al. 1994, Engwald 1999). La riqueza de las especies de epífitas vasculares en el bosque submontano de Sapecho es más difícil de evaluar debido a la falta de datos en tipos de bosque similares. Sin embargo, la riqueza de especies es normalmente más baja que en los bosques montanos y significativamente mayor que en bosques de tierras bajas amazónicas o en bosques de piedemonte (ter Steege & Cornelissen 1989, Ek et al. 1997, Engwald 1999, Acebey & Krömer 2001).
Orchidaceae es la familia más importante en cuanto al número de especies y puede contribuir hasta el 50% de la diversidad total (Kelly et al. 1994, Ibisch 1996, Engwald 1999) (Tabla 1). Mucha de esa diversidad es el resultado de géneros neotropicales con varias especies, p.e. Epidendrum, Maxillaria, Pleurothallis y Stelis. Los helechos normalmente son el segundo grupo más grande, con una diversidad muy similar a la de las orquídeas en Cotapata. Sin embargo, la diversidad de los helechos con relación a la de las orquídeas varía en países neotropicales. En Ecuador, la riqueza de las especies de orquídeas es al menos cinco veces mayor que la de helechos (Jørgensen & León-Yánez 1999), mientras que en Bolivia es sólo tres veces más alta (Ibisch 1996). Sugerimos que este es un patrón biogeográfico determinado por la ubicación geográfica de Bolivia en la transición del trópico al subtrópico, es decir, se revela una tendencia a gran escala de una concentración de la diversidad de orquídeas a nivel tropical y un aumento relativo de pteridófitos epífitos extratropical.
De acuerdo a otros estudios, se sabe que la diversidad de epífitas desciende fuertemente por encima de los 2.500 m (Ibisch et al. 1996, Jørgensen & León-Yánez 1999). Justamente en Bolivia el patrón de diversidad de epífitas muestra una curva en forma de campana con el punto máximo a aproximadamente 1.600 m de altitud (Fig. 2). Esto confirma la aseveración de Gentry & Dodson (1987) y Küper et al. (2004) que la curva de números de especies de epífitas vasculares muestra un pico marcado a altitudes intermedias. En nuestro estudio, ambas parcelas localizadas en bosques sobre crestas eran muy diferentes de aquellas sobre las laderas, mostrando números de especies más bajos a consecuencia del tamaño reducido de los árboles individuales.
Las orquídeas y helechos mostraron patrones de diversidad básicamente similares al patrón general (Fig. 2). Sin embargo, la contribución porcentual de ambos grupos a la diversidad total de epífitas mostró diferencias interesantes. Mientras que la contribución de orquídeas permanecía más o menos constante con aproximadamente 30-40% desde tierras bajas hasta aproximadamente los 2.200 m, los valores de pteridófitos aumentaron continuamente, empezando en tierras bajas con proporciones más bajas que las orquídeas y aráceas. En bosques de tierras bajas, las aráceas son casi tan numerosas como las orquídeas representando un cuarto del total de especies de epífitas; pero en bosques montanos, normalmente la riqueza de especies de aráceas es mucho más reducida, a excepción de algunas regiones montañosas en Ecuador (Nieder et al. 1999). Araceae es una familia casi netamente tropical, cuya diversidad máxima no sólo es conocida en tierras bajas, sino también coincide a lo largo de la línea ecuatorial (Benzing 1990, Kessler & Croat 1999). Finalmente, bromeliáceas y Piperaceae, así como el resto de las otras familias normalmente contribuyen con menos del 10% cada una.
Diversidad de epífitas en el bosque natural y en barbechos
La destrucción del bosque podría ser más severa para las epífitas vasculares que para otros grupos de plantas (Turner et al. 1994). En fragmentos del bosque tropical en Singapur, la diversidad de epífitas estaba dos veces más afectada que todas las plantas vasculares en conjunto. Esta dramática disminución de la riqueza de especies de epífitas - a consecuencia de la deforestación - es corroborada por este estudio (Fig. 3). Tanto en barbechos de 15 años en Sapecho (60%) como en Cotapata (70%), la reducción de las especies fue tan severa como en los bosques fragmentados de Singapur y ligeramente más alta que la de los bosques secundarios de 25-50 años en Venezuela, donde Barthlott et al. (2001) encontraron una reducción del 55%.
Las marcadas diferencias en la disminución de especies entre los grupos de epífitas individuales registrados en este estudio, p. ej. en las orquídeas (ca. 90%) y helechos (ca. 45%), también coinciden con los resultados de Singapur (Turner et al. 1994), pero difieren de los resultados de Barthlott et al. (2001), quienes documentaron una reducción de aproximadamente el 60% para ambos grupos en el bosque secundario de La Carbonera en Venezuela. La reducción de especies de Grammitidaceae, Hymenophyllaceae y Bromeliaceae es mucho menor en La Carbonera que la registrada en este estudio. Una menor disminución de estas familias de epífitas en el bosque secundario en La Carbonera puede ser el resultado de una mayor edad de este bosque y la presencia de árboles remanentes. En México, árboles remanentes del bosque natural pueden ser muy ricos en aráceas hemiepifíticas y bromeliáceas, que pueden contribuir considerablemente a la diversidad de hábitats secundarios abiertos (Hietz-Seifert et al. 1996).
La reducción de diversidad de epífitas en los barbechos puede explicarse por los siguientes factores:
a. Características de los árboles hospederos en barbecho, sobre todo su estatura uniforme, corteza lisa y dosel poco ramificado con ramas inclinadas (en lugar de horizontales) que las hacen desfavorables para el establecimiento de epífitas. Los bosques secundarios parecen ofrecer menor número de microhábitats favorables para las epífitas que los bosques primarios cuyos árboles viejos con copas bien desarrolladas proporcionan un mosaico complejo de microhábitats o un mosaico físico (Benzing 1995) que promueve el desarrollo de comunidades ricas de epífitas.
b. El microclima relativamente seco en los barbechos, a causa del dosel más abierto y la exposición a una mayor radiación en los barbechos comparado con el bosque maduro (Acebey et al. 2003). Sin embargo, no todos los grupos de epífitas (p. ej. aráceas hemiepifíticas y helechos xero-tolerantes) son negativamente afectados por la disminución de la humedad relativa del aire.
c. La joven edad de los árboles del barbecho, porque la colonización de los hospederos por parte de las epífitas es un proceso relativamente lento que está relacionado con el tiempo de disponibilidad del sustrato (Dudgeon 1923, Catling et al. 1986, Ibisch 1996) y que se expresa en una fuerte correlación entre el número de especies de epífitas y el tamaño (≅ edad) del árbol.
d. Los reducidos cojines de briofitas epifíticas en los árboles del barbecho, que influencian negativamente a la diversidad de epífitas vasculares, porque estos cojines de musgos suministran un sustrato favorable para la germinación y el establecimiento de estas plantas (Nadkarni 1984, Gradstein 1992, Zotz & Vollrath 2003).
Agradecimientos
Agradecemos al Proyecto de Investigación Agroforestal (PIAF)-El Ceibo, Alto Beni, a la Comunidad de El Chairo y a D. Chairiqui por su ayuda en el trabajo de campo; a T.B. Croat (Araceae), H.E. Luther (Bromeliaceae), M. Kessler (Elaphoglossum), R. Vásquez (Orchidaceae), R. Callejas (Peperomia) y A.R. Smith (Pteridophyta) por las identificaciones; y al personal del Herbario Nacional de Bolivia en La Paz por el apoyo logístico y A. Schmidt-Lebuhn por su ayuda con la elaboración del mapa. Este estudio fue financiado por el Servicio de Intercambio Académico Alemán (DAAD) y el A.F.W. Schimper-Stiftung (becas para T. Krömer).
Referencias
Acebey, A. & T. Krömer. 2001. Diversidad y distribución vertical de epífitas en los alrededores del campamento río Eslabón y de la laguna Chalalán, Parque Nacional Madidi, Dpto. La Paz, Bolivia. Revista de la Sociedad Boliviana de Botánica 3: 104-123.
[ Links ]Acebey, A., S.R. Gradstein & T. Krömer. 2003. Species richness and habitat diversification of bryophytes in submontane rain forest and fallows of Bolivia. Journal of Tropical Ecology 19: 9-18.
[ Links ]Ackerman, J.D. 1998. Evolutionary potential in orchids: patterns and strategies for conservation. Selbyana 19: 8-14.
[ Links ]Bach, K., M. Schawe, S.G. Beck, G. Gerold, S.R. Gradstein & M. Moraes. 2003. Vegetación, suelos y clima en los diferentes pisos altitudinales de un bosque montano de los Yungas, Bolivia – primeros resultados. Ecología en Bolivia 38: 3-14.
Barthlott, W., W. Lauer & A. Placke. 1996. Global distribution of species diversity in vascular plants: towards a map of phytodiversity. Erdkunde 50: 317-327.
[ Links ]Barthlott, W., V. Schmit-Neuerburg, J. Nieder & S. Engwald. 2001. Diversity and abundance of vascular epiphytes: a comparison of secondary vegetation and primary montane rain forest in the Venezuelan Andes. Plant Ecology 152: 145-156.
[ Links ]Benzing, D.H. 1990. Vascular epiphytes: general biology and related biota. Cambridge University Press, Cambridge. 354 p.
[ Links ]Benzing, D.H. 1995. The physical mosaic and plant variety in forest canopies. Selbyana 16: 159-168.
[ Links ]Catling, P.M., Brownell, V.R. & L.P. Lefkovitch. 1986. Epiphytic orchids in a Belizean grapefruit orchard: distribution, colonization, and association. Lindleyana 1: 194-202.
[ Links ]Coxson, D. & N.M. Nadkarni. 1995. Ecological roles of epiphytes in nutrient cycles of forest ecosystems. pp. 495-546. En: Lowman M. & N.M. Nadkarni (eds.). Forest Canopies. Academic Press, San Diego.
[ Links ]Dudgeon, W. 1923. Succession of epiphytes in the Quercus incana forest at Landour, western Himalayas. Preliminary notes. Journal of the Indian Botanical Society 3: 270-272.
[ Links ]Ek, R.C., H. ter Steege & K.C. Biesmeijer. 1997. Vertical distribution and associations of vascular epiphytes in four different forest types in the Guianas. pp. 65-89. En: Ek, R.C. (ed.). Botanical Diversity in the Tropical Rain Forest of Guyana. Tropenbos, Wageningen.
[ Links ]Elbers, J. 1995. Estudio de suelos en la zona de colonización Alto Beni, La Paz, Bolivia. Ecología en Bolivia 25: 37-69.
[ Links ]Engwald, S. 1999. Diversität und Ökologie der vaskulären Epiphyten eines Berg- und eines Tieflandregenwaldes in Venezuela. Books on Demand, Hamburg. 390 p.
[ Links ]Flores-Palacios, A. & J.G. García-Franco. 2001. Sampling methods for vascular epiphytes: their effectiveness in recording species richness and frequency. Selbyana 22: 181-191.
[ Links ]Gentry, A.H. & C.H. Dodson. 1987. Diversity and biogeography of neotropical vascular epiphytes. Annals of the Missouri Botanical Garden 74: 205-233.
[ Links ]Gradstein, S.R. 1992. The vanishing tropical rain forest as an environment for bryophytes and lichens. pp. 234-258. En: Bates, J.W. & A.W. Farmer (eds.). Bryophytes and Lichens in a Changing Environment. Clarendon Press, Oxford.
[ Links ]Gradstein, S.R., N.M. Nadkarni, T. Krömer, I. Holz & N. Nöske. 2003. A protocol for rapid and representative sampling of vascular and non-vascular epiphyte diversity in tropical rain forests. Selbyana 24: 105-111.
[ Links ]Hietz-Seifert, U., P. Hietz & S. Guevara. 1996. Epiphyte vegetation and diversity on remnant trees after forest clearance in southern Veracruz, Mexico. Biological Conservation 75: 103-111.
[ Links ]Ibisch, P. L. 1996. Neotropische Epiphyten-diversität - das Beispiel Bolivien. Martina Galunder-Verlag, Wiehl. 357 p.
[ Links ]Ibisch, P.L., A. Boegner, J. Nieder & W. Barthlott. 1996. How diverse are neotropical epiphytes? An analysis based on the „Catalogue of flowering plants and gymnosperms of Peru“. Ecotropica 2: 13-28.
Johansson, D. 1974. Ecology of vascular epiphytes in West African rain forest. Acta Phytogeographica Suecica 59: 1-136.
[ Links ]Jørgensen, P.M. & S. León-Yánez. 1999. Catalogue of the Vascular Plants of Ecuador. Missouri Botanical Garden Press, St. Louis. 1181 p.
[ Links ]Kelly, D.L., E.V.J. Tanner, E.M. Niclughadha & V. Kapos. 1994. Floristics and biogeography of a rain forest in the Venezuelan Andes. Journal of of Biogeography 21: 223-241.
[ Links ]Kessler, M. & T.B. Croat. 1999. State of knowledge of Bolivian Araceae. Selbyana 20: 224-234.
[ Links ]Krömer, T. 2003. Diversität und Ökologie der vaskulären Epiphyten in primären und sekundären Bergwäldern Boliviens. Cuvillier Verlag, Göttingen. 148 p.
[ Links ]Krömer, T. & S.R. Gradstein. 2003. Species richness of vascular epiphytes in two primary forests and fallows in the Bolivian Andes. Selbyana 24: 190-195.
[ Links ]Krömer, T., M. Kessler, S.R. Gradstein & A. Acebey. 2005. Diversity patterns of vascular epiphytes along an elevational gradient in the Andes. Journal of Biogeography 32: 1799-1809.
[ Links ]Krömer, T., M. Kessler & S.R. Gradstein. 2007. Vertical stratification of vascular epiphytes in submontane and montane forest of the Bolivian Andes: the importance of the understory. Plant Ecology 189: 261-278.
[ Links ]Küper, W., H.Kreft, J. Nieder, N. Köster & W. Barthlott. 2004. Large-scale diversity patterns of vascular epiphytes in Neotropical montane rain forests. Journal of Biogeography 31: 1477-1487.
[ Links ]Nadkarni, N.M. 1984. Epiphyte biomass and nutrient capital of a neotropical elfin forest. Biotropica 16: 249-256.
[ Links ]Nieder, J., S. Engwald & W. Barthlott. 1999. Patterns of neotropical epiphyte diversity. Selbyana 20: 66-75.
Perry, D.R. 1978. A method of access into the crowns of emergent and canopy trees. Biotropica 10: 155-157.
[ Links ]Ribera, M.O. 1992. Regiones ecológicas. pp. 9-72. En: Marconi, M. (ed.). Conservación de la Diversidad Biológica en Bolivia. Centro de Datos para la Conservación, USAID/Bolivia, La Paz.
[ Links ]Seidel, R. 1995. Inventario de los árboles en tres parcelas de bosque primario en la Serranía de Marimonos, Alto Beni. Ecología en Bolivia 25: 1-35.
[ Links ]Shaw, D.S. & D.M. Bergstrom. 1997. A rapid assessment technique of vascular epiphyte diversity at forest and regional levels. Selbyana 18: 195-199.
ter Steege, H. & J.H.C. Cornelissen. 1989. Distribution and ecology of vascular epiphytes in lowland rain forest of Guyana. Biotropica 21: 331-339.
Turner, I.M., H.T.W. Tan, Y.C. Wee, A.B. Ibrahim, P.T. Chew & R.T. Corlett. 1994. A study of plant species extinction in Singapore: lessons for the conservation of tropical biodiversity. Conservation Biology 8: 705-712.
Vásquez, R., P.L. Ibisch & B. Gerkmann. 2003. Diversity of Bolivian Orchidaceae – a challenge for taxonomic, floristic and conservation research. Organisms, Diversity and Evolution 3: 93-102. Electr. suppl.: Appendix 1 (Preliminary list of Bolivian orchid species; http://www.senckenberg.uni-frankfurt.de/odes/03-04.pdf).
Zotz, G. & B. Vollrath. 2003. The epiphyte vegetation of the palm Socratea exorrhiza – correlations with tree size, tree age, and bryophyte cover. Journal of Tropical Ecology 19: 81-90.
Artículo recibido en: Enero de 2005.
Manejado por: Mónica Moraes
Aceptado en: Octubre de 2006.