Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista de la Sociedad Boliviana de Pediatría
versión On-line ISSN 1024-0675
Rev. bol. ped. vol.55 no.1 La Paz 2016
ARTÍCULO DE REVISIÓN
Acinetobacter un patógeno actual
An actual pathogen Acinetobacter
Dr. Jaime Rada Cuentas*
* Coordinador de la Residencia Médica de Pediatría del Hospital Municipal Boliviano Holandés.
Artículo aceptado para su publicación el 11/04/2016
Resumen
Acinetobacter (inmóvil) es un cocobacilo Gram (-) que durante las tres últimas décadas, emerge desde un organismo de patogenicidad cuestionable a un agente infeccioso importante en todos los hospitales del mundo, sobre todo en pacientes internados en Unidades de Cuidados Intensivos (UCI). En casi el 100% de las muestras de suelo y agua se logra cultivar Acinetobacter, también es aislado de muchos alimentos, varios de ellos congelados. En los hospitales por su cualidad de sobrevivir en objetos inanimados húmedos o secos es identificado en el aire, equipamiento nosocomial y material de uso médico. Asimismo, Acinetobacter se desarrolla a partir de numerosas fuentes humanas, incluida la piel, el esputo, la orina, las heces y secreciones vaginales. La transmisión de esta bacteria en los sistemas de salud se produce porque de rutina no se realiza, un apropiado lavado de manos y desinfección del mobiliario de los equipos médicos y superficies hospitalarias en áreas próximas al paciente. Acinetobacter produce el 3 a 7% de las neumonías hospitalarias y el 1 a 2% de las bacteriemias asociadas a catéteres intravasculares, sitios de infección quirúrgica, infecciones del tracto urinario y tiene la capacidad de producir infecciones supurativas en casi cualquier sistema del organismo. Al igual que otras infecciones oportunistas por gramnegativos, los múltiples mecanismos de resistencia han hecho difícil el tratamiento de este agente infeccioso. Por ello, la elección del tratamiento empírico debe basarse de acuerdo a la epidemiología local y en el riesgo que tiene el paciente para adquirir una cepa resistente. Entre las estrategias para evitar la resistencia antimicrobiana, se destaca la prevención de las infecciones asociadas con el personal de salud, optimización del diagnóstico, tratamiento antimicrobiano apropiado y precaución de la transmisión cruzada de patógenos resistentes. Por la habilidad que posee Acinetobacter para sobrevivir durante semanas en condiciones de sequedad, es esencial la desinfección rutinaria del equipo médico y superficies que fueron tocadas por el personal de salud para prevenir la transmisión al paciente susceptible.
Palabras clave:
Rev Soc Bol Ped 2016; 55 (1): 29-48: Acinetobacter, infecciones nosocomiales, resistencia bacteriana.
Abstract
Acinetobacter (still) is a Gram (-) cocobacillus during the last three decades, emerging to from a microorganism of questionable pathogenicity to an important infectious agent in hospitals around the world, especially in patients in intensive care units (ICU). In almost 100% of the samples of soil and water is achieved cultivating Acinetobacter, it is also isolated from many foods, several of them frozen. In hospitals for their quality to survive in wet or dry inanimate objects is identified in the air, nosocomial equipment and medical material. It also develops Acinetobacter from numerous human sources, including skin, sputum, urine, feces, and vaginal secretions. The transmission of these bacteria in health systems occurs because not routine, proper hand washing and disinfection of furniture medical equipment and hospital surfaces in areas near the patient is performed. Acinetobacter produces 3 to 7% of pneumonias and 1 to 2% nosocomial of bacteremia associated with intravascular catheters, surgical sites infection, urinary tract infections and has the ability to produce suppurative infections in almost any organ system. Like other opportunistic gram-negative infections, multiple resistance mechanisms have made it difficult treating this infectious agent. Therefore, the choice of empirical therapy should be based according to local epidemiology and risk having the patient to acquire a resistant strain. Strategies to prevent antimicrobial resistance, preventing associated with health personnel, optimization of diagnosis, appropriate antimicrobial therapy and caution of cross transmission of pathogens resistant infections stands. By Acinetobacter has the ability to survive for weeks in dry conditions, routine disinfection of medical equipment and surfaces that were touched by health personnel to prevent transmission to susceptible patient it is essential.
Key words:
Rev Soc Bol Ped 2016; 55 (1): 29-48: Acinetobacter, nosocomial infections, bacterial resistance.
Introducción
Acinetobacter (inmóvil) es un cocobacilo Gram (-) que durante las tres últimas décadas, emerge desde un organismo de patogenicidad cuestionable a un agente infeccioso importante en todos los hospitales del mundo. 1 Acinetobacter spp., es un agente causal importante de morbilidad y mortalidad infecciosa que afecta sobre todo a pacientes internados en Unidades de Cuidados Intensivos (UCI). A. baumannii es la especie aislada con más frecuencia y la de mayor importancia clínica, en los últimos 20 años.2 Lo más alarmante de este microrganismo, es su habilidad de acumular diversos mecanismos de resistencia antimicrobiana y la emergencia de cepas resistentes a casi todos los antibióticos disponibles en el mercado.1
Acinetobacter fue descrito por primera vez en 1911 como Micrococcus calcoaceticus, desde entonces ha recibido diferentes nombres y recién desde los cincuentas recibe el nombre de Acinetobacter. Su hábitat natural son el agua y el suelo. También, es aislado de comidas, artrópodos y del ambiente. En humanos coloniza la piel, heridas y el tracto respiratorio y gastrointestinal.1
Microbiología
Las especies ahora clasificadas como miembros del género Acinetobacter han sufrido una larga historia de cambios taxonómicos, lo cual ha impedido su estudio adecuado.2
Si bien, el género Acinetobacter se encuentra ubicuo en la naturaleza, con estudios de hibridación ADN-ADN se han identificado al menos 23 especies diferentes (genómicas o "genoespecies") y 11 todavía no poseen un nombre definido (ver tabla 1).3-4 Actualmente, el género Acinetobacter se ubica en la familia Moraxellaceae. Los grupos 1 (A. calcoaceticus), 2 (A. baumannii), 3 y 13, poseen características fenotípicas similares que los sistemas bioquímicos comerciales no fueron capaces de discriminar; por ello, Gerner-Smidt y colaboradores5 sugieren que estas especies conformen el complejo A. calcoaceticus-A. baumannii. Dentro de la especie A. baumannii se han definido, a su vez, 19 bio-tipos, siendo el 1, 2, 6 y 9 los más aislados en las muestras clínicas.5-6
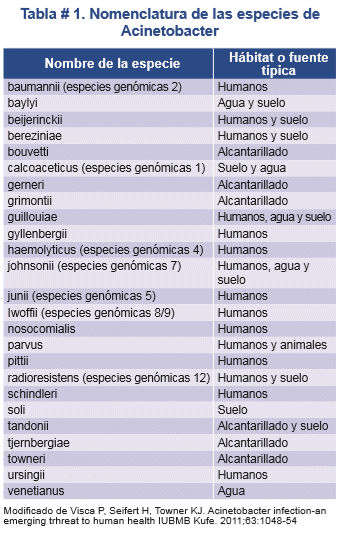
En la práctica hospitalaria habitual, la identificación precisa de las especies es innecesaria y la terminología (p.ej., complejo A. calcoaceticus-A. baumannii) cumple las necesidades tanto de médicos como de microbiólogos.3 Sin embargo, con fines epidemiológicos, se realizan estudios adicionales con pruebas que incluyen: la electroforesis en gel de campo pulsado, los polimorfismos de longitud de fragmentos amplificados (LOFAP), la reacción en cadena de polimerasa de ADN polimórfico amplificado aleatoriamente (RAPD-PCR) o ribotipado, siguen siendo necesarias para la identificación exacta de las cepas.3
Acinetobacter, es un cocobacilo aerobio Gram (-), inmóvil, catalasa positivo, indol y oxidasa-negativos.3-4 Tiene forma de bacilo durante la etapa de crecimiento rápido y de cocobacilo en la fase estacionaria. Generalmente se encuentra encapsulado, es aerobio y con tendencia a retener cristal violeta, por ello suelen ser identificados incorrectamente como cocos grampositivos. La versatilidad para aprovechar una variedad de fuentes de carbono y energía, le permite crecer en medios habituales de laboratorio y sobrevivir en la naturaleza. Las colonias son de 1 a 2 mm, no pigmentadas, pero se caracterizan por ser abombadas y mucoides con superficies que pueden ser lisas o tener depresiones. Su frecuente identificación errónea como Neisseria o Moraxella en la tinción de Gram se aclara fácilmente, mediante la reacción negativa a la oxidasa de Acinetobacter. Su incapacidad para reducir nitrato o desarrollarse en un medio anaeróbico, distingue a Acinetobacter de las enterobacterias. La hemólisis de los eritrocitos, la acidificación de la glucosa, el crecimiento a 44°C y la variabilidad en el uso de las fuentes de carbono son algunas características genotípicas que se utilizaran para distinguir las cepas de Acinetobacter.3
A. baumannii es fenotípicamente indistinguible de A. pitti y A. nosocomialis que se caracterizan por infectar a pacientes previamente sanos. A. lwoffii y A. radioresistans colonizan la piel humana y causan infecciones en el hospedero inmunocomprometido. A. calcoaceticus y A. johnsonii se encuentran en el agua y el suelo. A. baylyi es aislado con frecuencia en los alcantarillados.7,8-11 A.baumannii hace algunos años emerge como un patógeno importante, exhibiendo un incremento constante de su resistencia antimicrobiana.12-14
Epidemiología
En casi el 100% de las muestras de suelo y agua se logra cultivar Acinetobacter. También es aislado de muchas fuentes, como leche pasteurizada, alimentos congelados, vegetales, carne de ave congelada y pescado. En los hospitales fue identificado en el aire nosocomial, humidificadores, agua de grifo, baños de dializado peritoneal, objetos que permiten micciones en la cama (pop. chata y pato), toallas, almohadas, cortinas, piscinas de hidroterapia, catéteres, de angiografía, respiradores mecánicos, bombas de infusión, laringoscopios, duodenoscopios, equipos con control digital, medicación con multidosis, fracción de proteínas plasmáticas y dispensadores de jabón que se comportan como verdaderos reservorios del microorganismo.3-4 Puede sobrevivir en objetos inanimados húmedos o secos del ambiente hospitalario durante semanas o meses. De manera similar a las infecciones por Staphylococcus aureus, el movimiento de los pacientes y personal del nosocomio son los responsables de diseminar la infección y de provocar brotes prolongados.3-4
Acinetobacter se desarrolla a partir de numerosas fuentes humanas, incluida la piel, el esputo, la orina, las heces y secreciones vaginales. Es el microorganismo gramnegativo que con mayor frecuencia el personal hospitalario porta en la piel de forma persistente. Hasta el 25% de los adultos sanos de la comunidad presentan colonización cutánea y el 7% de los adultos y lactantes presentan colonización faríngea transitoria3. Asimismo, coloniza los tubos de traqueostomía de los pacientes internados.3
La resistencia de Acinetobacter a biocidas (p.ej., clorhexidina) se convierte en un problema cuando se realizan diluciones inapropiadas, si el tiempo de exposición es inadecuado o por la presencia de residuos biológicos y/o de Acinetobacter resistente a múltiples fármacos.3
Si bien, Acinetobacter baumannii es reconocido como el agente causal de varias enfermedades nosocomiales severas que incluyen: infecciones de piel y tejidos blandos, infección de heridas, tracto urinario y meningitis secundaria; las infecciones más importantes con elevada mortalidad son la neumonía asociada a ventilador y la bacteriemia.15 Los factores de riesgo para desarrollar una infección nosocomial incluyen: duración de estancia hospitalaria mayor a 5 días,3,16 cirugía preliminar, heridas, infección previa (independiente del uso previo de antibióticos), colonización fecal con Acinetobacter, tratamiento con antibióticos de amplio espectro (cefalosporinas de tercera generación, fluoroquinolonas o carbepenémicos),3-4 catéteres urinarios o intravenosos centrales permanentes, ingreso a una unidad de quemados, estancia prolongada en una UCI, nutrición parenteral, ventilación mecánica e inadecuada aplicación de los protocolos de control de infecciones.3-4
Con menor frecuencia se presentan infecciones por Acinetobacter baumannii adquiridas en la comunidad que incluyen, neumonía en el 85% de los casos y bacteriemia.15 La neumonía adquirida en la comunidad (NAC) es más severa que la nosocomial y -en general- fulminante, falleciendo el 60% de los pacientes.15 Entre los factores de riesgo para adquirir una NAC por Acinetobacter podemos mencionar: al alcoholismo, tabaquismo, a la enfermedad pulmonar crónica, diabetes mellitus y residencia en un país tropical en vías de desarrollo.3
La transmisión de Acinetobacter en los sistemas de salud se produce porque no se realiza de rutina, un apropiado lavado de manos y desinfección del mobiliario de los equipos médicos y superficies hospitalarias en áreas próximas al paciente.17-19 La inadecuada desinfección provoca altos niveles de contaminación ambiental que se asocian directamente con la colonización e infección por Acinetobacter.20
Acinetobacter produce el 3 a 7% de las neumonías hospitalarias y el 1 a 2% de las bacteriemias asociadas a catéteres intravasculares, sitios de infección quirúrgica e infecciones del tracto urinario.20
La prevalencia de los aislamientos clínicos de Acinetobacter varía en cierto grado entre los países y sitios de donde se obtienen las muestras, la misma se ha incrementado -en general- en todo el mundo en las dos últimas décadas.3
El A. baumannii multidrogoresistente fue identificado como un patógeno relevante al provocar infecciones en lesiones traumáticas, de soldados durante los conflictos del Medio Este.21-23 Su establecimiento como un agente causal en infecciones asociadas a los sistemas de salud y la falta de un potente agente antimicrobiano que logre combatirlo, constituye un problema emergente de salud pública.24
Patogenia
A pesar que Acinetobacter spp., es considerado como un agente de baja patogenicidad, ciertas características le permiten aumentar la virulencia de cepas involucradas en infecciones.2
La patogenia de A. baumannii está relacionada con: a) su facultad de adherirse a superficies y células epiteliales humanas, utilizando sus fimbrias; b) sus cadenas de lipopolisacáridos, pese a no conocer el potencial endotóxico del lipopolisacárido de la pared bacteriana en humanos; c) la presencia de lípido A en la membrana celular externa; d) desarrollo de una biopelícula ("biofilm") sobre las superficies y células humanas; e) su capacidad para sobrevivir en medios con limitada concentración de zinc dentro del hospedero; f) su virtud de desarrollarse en un pH ácido y a bajas temperaturas que le permite incrementar su habilidad para invadir tejidos desvitalizados; f) su prolongada viabilidad bajo condiciones de sequedad; g) la producción de bacteriocina que incrementa su sobrevida; h) la presencia de un polisacárido capsular formado por L-ramnosa, D-glucosa, D-ácido glucurónico y D-manosa, que vuelve a la cepa más hidrofílica, disminuyendo su adherencia a hidrocarbonos y ayuda a la bacteria a evadir la fagocitosis, aunque la hidrofobicidad puede ser mayor en cepas de Acinetobacter aisladas de catéteres o aparatos traqueales; i) su cápsula que inhibe la fagocitos; j) la producción de enzimas que pueden dañar tejidos lipídicos, como el butirato y caprilato esterasas, leucin aryl amidasa, gelatinasa y lipasa; k) la producción de sideróforos: l) la producción de aerobactinas y proteínas de la membrana externa dependientes de hierro, por algunas cepas de A. baumannii que le permiten vivir en el cuerpo humano; m) su potencial para adquirir material genético de su entorno para incrementar su sobrevivencia y desarrollar un gran repertorio de mecanismos de resistencia antimicrobiana.2,25-30
Los neutrófilos reclutados juegan un papel preponderante en la respuesta inmune del hospedero contra la infección por Acinetobacter.31-33
Importancia clínica
Acinetobacter spp., tiene la capacidad de producir infecciones supurativas en casi cualquier sistema del organismo.34
Debido a su amplia distribución en la naturaleza y su capacidad para colonizar tejidos sanos o dañados, la interpretación del significado de aislamientos procedentes de muestras clínicas suele ser difícil, poder diferenciar entre una muestra de sangre contaminada y bacteriemia real, suele ser una tarea a veces difícil. El origen más común de las bacteriemias son las infecciones del tracto respiratorio, de heridas quirúrgicas o catéter intravascular, presentando la mayor tasa de bacteriemia nosocomial durante la segunda semana de hospitalización. Asimismo, Acinetobacter puede interpretarse erróneamente en la tinción de Gram, como otros microorganismos gramnegativos que se asocian con mayor frecuencia a síndromes clínicos particulares (p.ej., en LCR, Neisseria meningitidis; en el esputo, Haemophilus influenzae). El complejo A. baumannii es el patógeno aislado con mayor frecuencia y representa el 80% de todos los aislamientos clínicos de esta especie. Sin embargo, la identificación reiterada de especies distintas a A. baumannii (A.ursingii y Acinetobacter cepa RUH) en muestras clínicas, no debería descartarse con la calificación de contaminante.2-3
Vía respiratoria
Acinetobacter con mayor frecuencia infecta el sistema respiratorio debido a la colonización faríngea transitoria que ocurre en personas sanas y la tasa elevada de colonización en los tubos de traqueostomía.34
En niños sanos suele causar bronquiolitis y traqueo-bronquitis adquiridas en la comunidad.35 Se describe neumonía adquirida en la comunidad (NAC) severa por Acinetobacter que se presenta durante los meses de calor y humedad en regiones tropicales.36-38 La NAC en adultos, se presenta -en general- en hospederos con defensas disminuidas (p.ej., alcohólicos, fumadores, con diabetes mellitus, insuficiencia renal o enfermedad pulmonar subyacente).37,39-40Se asocia con una alta incidencia de bacteriemia, síndrome de insuficiencia respiratoria, sepsis, choque y muerte (mortalidad ≥ 50%). La mortalidad de la NAC es más elevada que la infección adquirida en el hospital, aunque se desconocen las razones de esta presentación fulminante. Rara vez, la NAC por especies de Acinetobacter se presenta con imágenes de consolidación y abscesos pulmonares múltiples.37-38
El mayor impacto que ha producido Acinetobacter es haberse constituido como un agente causal importante de la neumonía nosocomial, que se caracteriza por ser de inicio tardío -en especial- en casos asociados a ventilación mecánica, provocando mayor mortalidad y una estancia hospitalaria prolongada.41-43 Los factores predisponentes para desarrollar neumonía nosocomial incluyen: intubación endo-traqueal, traqueostomía, estancia en UCI, cirugía reciente, puntuación de APACHE II alta, enfermedad pulmonar subyacente y el tratamiento previo con antibióticos. Su propagación nosocomial en la UCI se produce a través de los equipos de ventilación mecánica, guantes, colonización del equipo de enfermería y personal de fisioterapia respiratoria, entre otros. Las neumonías nosocomiales por Acinetobacter son con frecuencia multilobulares y puede observarse cavitación, derrame pleural y formación de fístula broncopleural.44
Bacteriemia
Acinetobacter causa del 1% a 2% de todas las bacteriemias y se asocian típicamente a catéteres intravasculares, el 63% son producidas por A. baumannii, 20% por A. nosocomialis y 8% por A. pitti. A. baumannii provoca la mayor mortalidad por bacteriemia.45-47 La bacteriemia nosocomial por Acinetobacter, se asocia con frecuencia a infecciones de las vías respiratorias y el uso de catéteres endovenosos (colonización o infección) y en menor proporción a las infecciones de las vías urinarias, heridas cutáneas y abdominales.40 El choque séptico suele presentarse hasta en el 30% de pacientes con bacteriemia con una tasa de mortalidad del 17-46%.34,48 La producida por especias distintas a A. baumannii tiende a ser menos grave.3
La sepsis suele presentarse tardíamente en neonatos y lactantes hospitalizados por largos períodos de tiempo, con una tasa de mortalidad del 11%, los factores de riesgos que predisponen al desarrollo de bacteriemia en este grupo de pacientes son: el bajo peso al nacer, terapia antibiótica previa, ventilación mecánica y aire ambiental contaminado.2
Genitourinarias
A pesar de colonizar la vía urinaria inferior, Acinetobacter solo es invasivo en raras ocasiones, provocando el 1% de las infecciones del tracto urinario tanto cistitis como pielonefritis, en pacientes con sonda vesical permanente o nefrolitiasis. La mayoría de estas cepas poseen la habilidad de formar "biofilms" en los catéteres urinarios.34,49-50
Infección intracraneal
En pacientes sanos la meningitis por Acinetobacter es infrecuente.51 Suele presentarse -en general- luego de un traumatismo craneoencefálico o intervención neuro-quirúrgica, incluyendo aquellos con tubos de drenaje ventricular. Su incidencia ha disminuido con el uso racional de antibióticos y la implementación de medidas para el control de infecciones.49,52 Hasta un 30% de los pacientes con meningitis presentan un exantema petequial.39
Tejidos blandos
Acinetobacter es un patógeno importante de las heridas traumáticas (p.ej., heridas de guerra), incisiones postoperatorias y quemaduras, debido a su capacidad de desarrollar en tejido dañado o con cuerpos extraños. Las infecciones por Acinetobacter se hicieron patentes recientemente en desastres naturales como terremotos y tsunamis.16,53-54 Puede causar celulitis asociada a catéter venoso permanente que se resuelve con la simple retirada de éste. Se ha descrito fascitis necrosante sinérgica con Streptococcus pyogenes.34
Miscelánea de infecciones
La infección por Acinetobacter puede presentarse en cualquier sitio del organismo. Suele observarse en la esfera oftálmica: conjuntivitis, endoftalmitis,55 úlcera corneal secundaria a contaminación de lentes de contacto blandos y perforación corneal.56 También, puede presentarse endocarditis de válvulas naturales y protésicas,57 osteomielitis, artritis séptica, y abscesos pancreáticos o hepáticos.3
Resistencia bacteriana
Al igual que otras infecciones oportunistas por gramnegativos, el desarrollo de la resistencia antimicrobiana ha hecho difícil el tratamiento de Acinetobacter. A pesar de observarse diferencias importantes en: los patrones de resistencia antimicrobiana según las especies de Acinetobacter, el país o región donde es aislado; la tendencia global es un incremento de su resistencia.3 En la actualidad, los aislamientos de A. baumannii con frecuencia son resistentes a todos los antibióticos disponibles.3,58-59
La habilidad de A. baumannii para adquirir mecanismos de resistencia fue un fenómeno observado a principios de los setentas. El desarrollo extremadamente rápido de resistencia antimicrobiana, se debe al uso masivo de antibióticos en los hospitales y a la gran habilidad que posee A. baumannii para responder en forma rápida a estos desafíos.49 Específicamente, se informa la influencia que tiene el empleo de cefalosporinas de amplio espectro y quinolonas para inducir resistencia.60-62 Uno de los principales problemas, fue la aparición de resistencia a carbepenémicos al adquirir carbapenemasas clase B y D.63-66 El 30% de los Acinetobacter son MDR. Sin embargo, existen diferencias geográficas de resistencia.67-69
Acinetobacter posee múltiples mecanismos de resistencia, estrechamente relacionados con el incremento del tamaño del genoma (ver figura 1).70-71
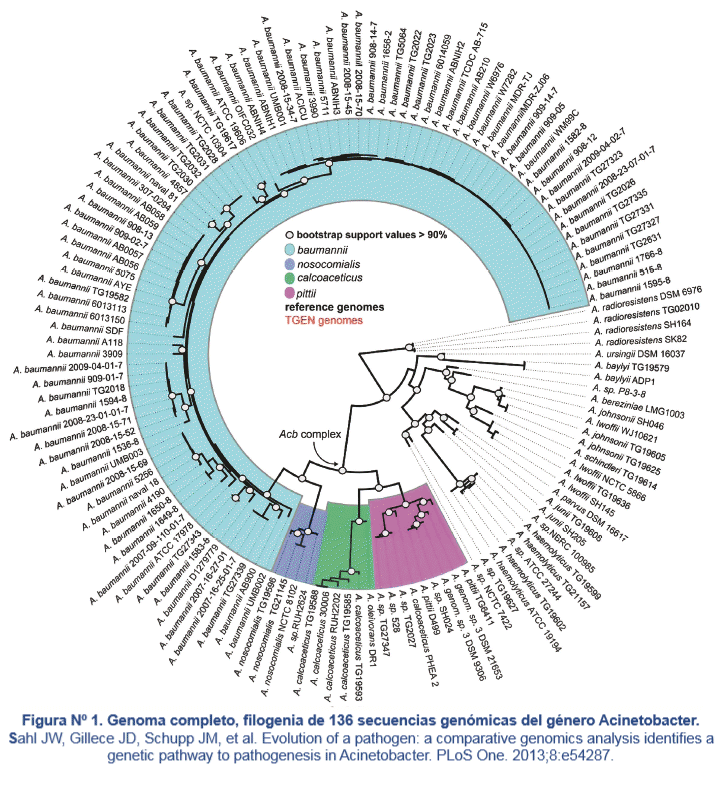
El genoma de A. baumannii contiene varios genes agrupados en islas de resistencia, cuya estructura facilita la adquisición de mecanismos de resistencia de otras especies de bacterias.72 Acinetobacter, tiene mayor probabilidad para adquirir determinantes de resistencia en comparación con otras bacterias, gracias a su estrecha relación con varias especies de su género en el suelo y agua del ambiente que contienen un gran reservorio de genes, responsables de resistencia bacteriana.73
El mecanismo de resistencia antimicrobiana más frecuente de Acinetobacter se lleva cabo mediante la producción de ß-lactamasas. (ver figura 2). El grupo Ambler 1 ß-lactamasas clase C no inducibles son codificadas cromosómicamente, como cefalos-porinasas que hidrolizan a las penicilinas y cefalos-porinas de primera, segunda y tercera generación. El porcentaje de hidrolisis por estas enzimas es menor para cefalosporinas de cuarta generación como el cefepime y carbapenémicos.74-75
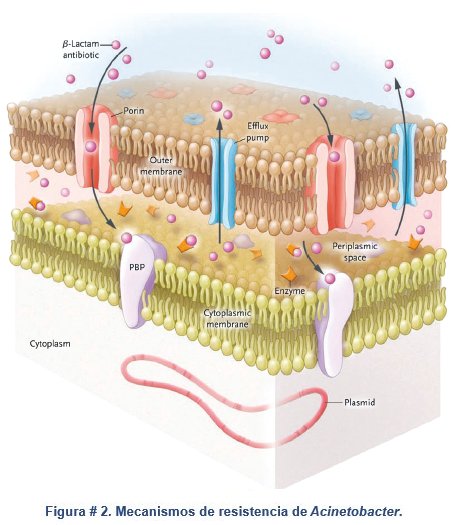
| Al igual que otras bacterias Gram (-), posee una membrana externa y una membrana citoplasmática, un espacio periplásmico donde residen ß-lactamasas (carbapenemasas, ß-lactamasas Ambler clase C, y ß-lactamasas de espectro ampliado). Las proteínas fijadoras de penicilina (PFP), localizadas a nivel de la membrana citoplasmática constituyen el blanco final de los antibióticos ß-lactámicos. Para unirse a ellas en el espacio periplásmico, los antibióticos deben atravesar la membrana externa a través de los canales de porinas (proteínas de la membrana externa). Si bien, los antibióticos ß-lactámicos pueden unirse a las PFP, estos podrían ser expulsados activamente de la estructura bacteriana por las bombas de expulsión. Acinetobacter puede albergar integrones y transposones, elementos genéticos sobre el cromosoma bacteriano o plásmidos que pueden transportar múltiples cajas con genes de resistencia (v.g. ß-lactamasas de espectro ampliado y metalo ß-lactamasas). Modificado de la Referencia 42. |
En 1980 se manifiesta la emergencia y la rápida diseminación mundial de la clase Ambler 2be ß-lactamasas de espectro extendido (BLEE) con una actividad hidrolítica contra las penicilinas y todas las cefalosporinas, induciendo al uso de carbe-penémicos para tratar infecciones por cepas BLEE de Acinetobacter. La subsecuente emergencia de la clase Ambler D, grupo 2d oxacilinasas ha sido la responsable del incremento de resistencia a carbe-penémicos desde el año 2000.76-77 La clase Ambler B, grupo 3 de las metalo-ß-lactamasas que si bien se manifiestan con menor frecuencia también, producen resistencia a carbepenémicos.78-80
La segunda causa más importante de resistencia antimicrobiana de Acinetobacter son las bombas de expulsión que confieren resistencia a antibióticos ß-lactámicos, cloranfenicol, macrólidos, tetraciclinas, tigeciclina, aminoglucósidos y ciertos antisépticos, (ver figura 2)81-82. La presencia de mecanismos de resistencia antimicrobiana adicionales que trabajan en sintonía con las bombas de expulsión limitan las opciones terapéuticas.
En las especies de Acinetobacter, la resistencia a aminoglucósidos está determinada por la presencia de enzimas (fosforilasas, acetilasas o adenilasas) que disminuyen la afinidad a estos antimicrobianos a la subunidad del ribosoma correspondiente.83-84 Sin embargo, se describió el gen armA ubicado en un transposón que codifica una metilasa del ARNr 16S que altera el sitio de acción y por consiguiente genera altos niveles de resistencia a todos los aminoglucósidos.85
La resistencia de Acinetobacter a las fluoroquinolonas es multifactorial, manifestándose ciertas mutaciones que determinan regiones de menor afinidad de las fluoroquinolonas a la DNA girasa y topoisomerasa IV; cuando se combinan con una sub-regulación de la bomba de expulsión A de ABC, se produce la resistencia.86-88
La resistencia a las polimixinas que incluyen a la colistina y polimixina B, se presenta por mutaciones genéticas que codifican a dos componentes del sistema regulador PmrA y PmrB y una reducción de lipopolisacáridos en la pared bacteriana de Acinetobacter, provocando una menor carga negativa con pérdida de la afinidad antimicrobiana.89-90 Similar a la resistencia a carbapenémicos, se ha identificado heteroresistencia de Acinetobacter a polimixinas, observándose la emergencia de resistencia durante el tratamiento.89 Sin embargo, para bien las cepas de A. baumannii resistentes a colistina producen un menor número de infecciones, lo cual potencia lentamente la diseminación de esta panresistencia.91-92
Acinetobacter adquiere el fenotipo multidrogo-resistente (MDR), a través de elementos genéticos mobiles (plásmidos, transposones e integrones).93-95 La presencia de integrones clase I y II se asocia con múltiple resistencia a antibióticos.95-96 La mayoría de ellos es adquirido por contacto con bacterias presentes en su ambiente como las Pseudomonas spp.97-99
Tratamiento
Por el amplio rango de mecanismos de resistencia, la elección del tratamiento empírico debe basarse de acuerdo a la epidemiología local y en el riesgo que tiene el paciente para adquirir una cepa resistente. Antes de iniciar la terapia, debemos considerar que Acinetobacter puede colonizar la piel, faringe, vía digestiva, uretra, conjuntiva y vagina. Por ello, primero tenemos la obligación de considerar, si la cepa aislada en el cultivo se trata de una infección invasiva o solo se trata de una colonización, evitando el sobre uso de antibióticos.3-4 Acinetobacter MDR se define como la resistencia a carbapenémicos o resistencia a tres clases de antimicrobianos100 y pan-resistencia cuando incluye a polimixinas.91-92
Antibióticos ß-lactámicos: cuando Acinetobacter es susceptible, los ß-lactámicos constituyen el tratamiento de elección por su efecto bactericida y amplia distribución en todo el organismo. Estas cepas susceptibles deben ser tratadas con cefalos-porinas de tercera o cuarta generación como la cefotaxime, ceftriaxone o cefepime, porque la presencia de ß-lactamasas intrínsecas inactivan las penicilinas, cefalosporinas de primera y segunda generación.101-103
Carbapenémicos: el imipenem y meropenem constituyen el tratamiento de elección para las infecciones severas por A. baumannii. Si bien, en un inicio aproximadamente el 90% de los aislamientos eran sensibles a carbepenémicos,58,104-105 en los últimos años la susceptibilidad a imipenem a disminuido en Latinoamérica (60.6%) en relación a Europa (85.9%) y Norte América (88.6%).106 La resistencia de A. baumannii a carbapenémicos se produce por varios mecanismos potenciales, incluyendo plásmidos o carbapenemasas codificadas cromosómicamente -en especial- ß-lactamasas clase D (OXA-23, OXA-24 u OXA-58), metalo-ß-lactamasas (ß-lactamasas clase B), bombas de expulsión, alteración en las proteínas fijadoras de penicilina, modificación de cationes o pérdida de proteínas de la membrana externa (porinas).107-108 Más de uno de estos mecanismos de resistencia pueden estar presentes en la misma cepa, confiriéndole un alto nivel de resistencia.
Inhibidores de ß-Lactamasas: El sulbactam posee actividad antimicrobiana intrínseca contra A.baumannii y es el inhibidor de ß-lactamasas más activo.109 La combinación de sulbactam con ampicilina, cefoperazona o penicilinas antipseudomonas no incrementa la actividad antimicrobiana contra A. baumannii.110 La emergencia de cepas de Acinetobacter resistente a carbepenémicos, permitió que los inhibidores de ß-lactamasas surjan como una opción terapéutica. El sulbactam combinado con ampicilina es efectivo para tratar infecciones invasivas como la neumonía, bacteriemia y meningitis.110-112
Aminoglucósidos: Estos antimicrobianos poseen una acción moderada contra A. baumannii.105 En todo el mundo la sensibilidad de Acinetobacter spp. a amikacina es aproximadamente del 60%. Esta actividad es menor en las cepas de A. baumannii MDR en comparación con las que no MDR.69 Si bien las pruebas de sensibilidad muestran cepas de Acinetobacter sensible a aminoglucósidos, su empleo está limitado por su deficiente penetración al tejido pulmonar y sistema nervioso central.113-116
Tigeciclina y minociclina. La minociclina, doxiciclina y en menor escala la tetraciclina han demostrado alto porcentaje de actividad antimicrobiana contra A. baumannii. 117 La tigeciclina es una glicilciclina, derivado semisintético de la minociclina y bacteriostático para A.baumannii.117 Tiene la capacidad de evadir a la mayoría de los mecanismos de resistencia de las tetraciclinas. La tigeciclina combinada con otros antibióticos ha sido empleada con éxito en el tratamiento de Acinetobacter resistente a carbapenémicos. Sin embargo, su volumen de distribución y baja concentración sérica, evita su empleo en la bacteriemia, habiéndose informado el desarrollo de resistencia durante el tratamiento.118-122 La minociclina y derivados de la tetraciclina muestran actividad "in vitro" contra Acinetobacter resistente a carbapenémicos y combinadas con colistina poseen actividad bactericida.123-125
Polimixinas: Son polipéptidos catiónicos que interactúan con el lipopolisacárido de la bacteria gram-negativa. Han demostrado tener actividad bactericida contra A. baumannii105,126-127 y la resistencia contra estos agentes permanece baja incluyendo, cepas MDR y resistentes a carbepenémicos.128-130 Disponemos de dos agentes en este grupo de antimicrobianos: la colistina y polimixina B. Con frecuencia son utilizadas en el tratamiento de infecciones por Acinetobacter resistente a carbapenémicos. Las polimixinas han sido empleadas en el tratamiento de la meningitis nosocomial causada por A. baumannii MDR. Su efectividad clínica solo se alcanza con tratamiento endovenoso. Debido a su inadecuada penetración de la barrera hematoencefálica, colistina ha sido administrada por vía intraventricular o intratecal más colistina endovenosa.131-136
Los informes clínicos de pacientes infectados por A.baumannii resistente a polimixinas son escasos. Sin embargo, su mayor empleo en pacientes críticamente enfermos puede conducir a la emergencia de resistencia.137 La aparición de resistencia se relaciona con el uso previo de colistina que incrementaría la emergencia de resistencia durante la terapia.138 La resistencia innata a colistina es común en ciertas especies de Acinetobacter como el A.junii.139 En áreas con alta prevalencia de Acinetobacter resistente a carbapenémicos y sulbactam, las polimixinas deben ser consideradas como un componente de la terapia empírica en infecciones severas.101
Fluoroquinolonas. Poseen moderada actividad antimicrobiana contra A.baumannii, su sensibilidad global a ciprofloxacina es de 44%.105 Sin embargo, la actividad de fluoroquinolonas contra cepas MDR o resistentes a imipenem es baja.105,133,140
Tratamiento combinado. El conocimiento de las infecciones por A.baumannii es sustentado por estudios realizados "in vitro" o animales. Aunque varias de las combinaciones utilizando colistina, rifampicina, carbapenémicos, sulbactam, minociclina y tigeciclina demostraron resultados promisorios en el laboratorio, la correlación con la evolución clínica está ausente por la falta de estudios controlados apropiados.125,141-146 El tratamiento endovenoso de polimixinas más otros antimicrobianos, como rifampicina para infecciones nosocomiales por A. baumannii MDR produce una favorable respuesta clínica.148,147-151 Sin embargo un estudio multicéntrico aleatorizado en pacientes infectados con A.baumannii MDR tratados con colistina o colistina más rifampicina demostró, que si bien la erradicación microbiológica fue más rápida con el esquema combinado no hubo diferencias en la mortalidad y tiempo de hospitalización.152 Este estudio sugiere que la adición de rifampicina a la colistina cuando tratamos infecciones por Acinetobacter MDR, no está justificada de forma rutinaria y más bien nos muestra la importancia de contar con un estudio aleatorizado que determine si la terapia combinada es más beneficiosa. El uso de colistina en aerosol más colistina endovenosa u otros agentes antimicrobianos en neumonía por A.baumannii MDR brindan una respuesta clínica favorable.153-156 Por los esquemas de tratamiento limitados, el clínico debe optimizar el uso de los antimicrobianos disponibles, usando infusiones prolongadas de antibióticos ß-lactámicos para cepas con sensibilidad intermedia e instilación local de colistina cuando la vía endovenosa proporciona bajas concentraciones tisulares en el sitio de infección.157 Las infusiones intermitentes de antibióticos ß-lactámicos, incrementan el tiempo de concentración de la droga por encima de la MIC.158 La infusión continua permite alcanzar niveles valle altos de ß-lactámicos, que quizá permitan una mejor evolución de las infecciones por Acinetobacter menos sensible.159 Existe ciertos resultados contradictorios por la ausencia de grupos de control, sobre la seguridad y efectividad de la colistina para tratar infecciones por Acinetobacter resistente a carbepenémicos.160-162 La administración de colistina por vía intratecal es efectiva para el tratamiento de infección en el sistema nervioso central por Acinetobacter resistente.163 La colistina en aerosol es segura y posiblemente eficaz para tratar la neumonía causada por Acinetobacter resistente.164-166 Nuevas y prometedoras combinaciones de colistina con antibióticos activos contra Gram-positivos como los glucopéptidos o lipopéptidos han sido estudiados "in vitro" y en vivo.
Finalmente, un triple esquema con colistina, un lipopéptido o glucopéptido y otro agente activo contra A. baumannii MDR como tigeciclina o carbepenémicos deben ser investigados en la práctica clínica. Sin embargo, se necesitan futuras investigaciones que proporcionen datos clínicos evidentes para apoyar estas combinaciones.167
Prevención
Entre las estrategias para evitar la resistencia antimicrobiana, se destaca la prevención de las infecciones asociadas con el personal de salud, optimización del diagnóstico, tratamiento de las infecciones considerando la adecuada elección, dosis y duración del tratamiento antimicrobiano, prevención de la transmisión cruzada de patógenos resistentes. El control de la resistencia antimicrobiana requiere el apoyo de la microbiología clínica, un programa activo de prevención de infecciones y un efectivo proceso de intercambio de información entre los microbiólogos, epidemiólogos y médicos.168
Por la habilidad que posee Acinetobacter para sobrevivir durante semanas en condiciones de sequedad, es esencial la desinfección rutinaria del equipo médico y superficies que fueron tocadas por el personal de salud para prevenir la transmisión al paciente susceptible (ver tabla 2).169-174
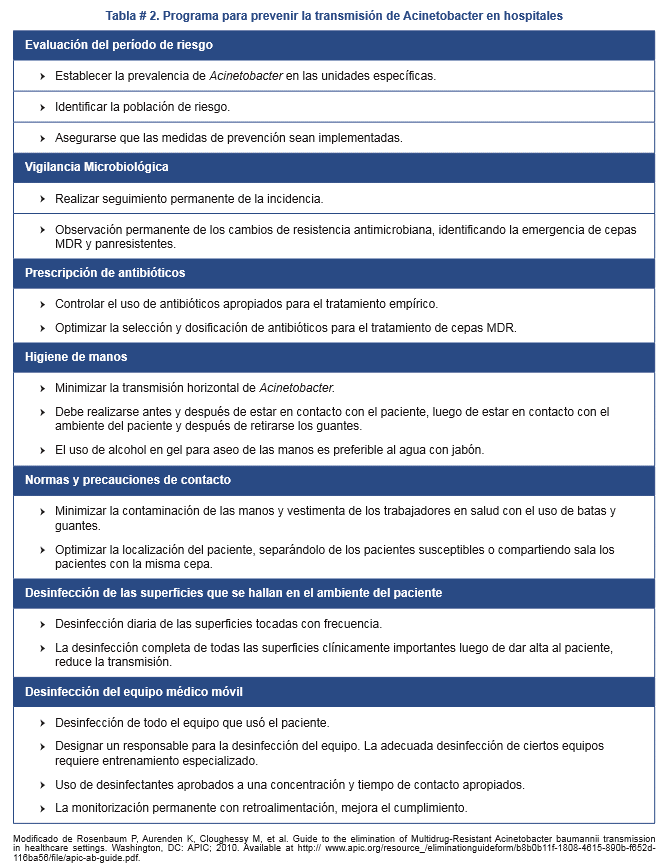
Si bien las medidas de limpieza y desinfección son importantes, el uso de la prueba de bioluminicencia con trifosfato de adenosina es más confiable que la inspección visual.175-176 Clínicamente es relevante considerar la resistencia de microorganismos a los desinfectantes de uso rutinario, la misma no se ha informado en infecciones por Acinetobacter. La disminución de la susceptibilidad se ha identificado en cepas MDR, después que la bacteria ha sido repetidamente expuesta a desinfectantes.177-178
Referencias bibliográficas
1. Muñoz-Price LS, Weinstein RA. Acinetobacter infection. N Eng J Med 2008;358:1271-81. [ Links ]
2. Salazar de Vegasa EZ, Nieves B. Acinetobacter spp.: aspectos microbiológicos, clínicos y epidemiológicos. Rev Soc Venezol Microbiol 2005;25:64-71. [ Links ]
3. Allen DM, Hartman BJ. Género Acinetobacter. En Mandell GL, Bennett JE, Dolin R, ed. Principios y práctica de enfermedades infecciosas. 7ma. Ed. Barcelona: Editorial, DRK edición 2009;vol 2: 2885-9.
4. Phillips M. Acinetobacter species. In Mandell GL, Dolin R, Blaser MJ, eds. Principles and practices of infectious diseases. 8th. Ed. Philadelphia: Imprint Elsevier Inc. 2014;vol 2: 2551--8
5. Gerner-Smidt P. Ribotyping of the Acinetobacter calcoaceticus-Acinetobacter baumannii Complex. J Clin Microbiol 1992; 30: 2680-5. [ Links ]
6. Bouvet P, Grimont P. Identification and biotyping of clinical isolate of Acinetobacter. Ann Inst Pasteur Microbiol 1987; 138: 569-78. [ Links ]
7. Towner KJ. Acinetobacter: an old friend, but a new enemy. J Hosp Infect. 2009;73:355-63. [ Links ]
8. Fournier PE, Richet H. The epidemiology and control of Acinetobacter baumannii in health care facilities. Clin Infect Dis 2006;42:692-9. [ Links ]
9. La Scola B, Raoult D. Acinetobacter baumannii in human body louse. Emerg Infect Dis. 2004; 10:1671-3. [ Links ]
10. Berlau J, Aucken H, Malnick H, Pitt T. Distribution of Acinetobacter species on skin of healthy humans. Eur J Clin Microbiol Infect Dis 1999;18:179-83. [ Links ]
11. Nemec A, Krizova L, Maixnerova M. Genotypic and phenotypic characterization of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex with the proposal of Acinetobacter pittii sp. nov. (formerly Acinetobacter genomic species 3) and Acinetobacter nosocomialis sp. nov. (formerly Acinetobacter genomic species 13TU). Res Microbiol 2011; 162:393-404. [ Links ]
12. Zarrilli R, Pournaras S, Giannouli M, Tsakris A.Global evolution of multidrug-resistant Acinetobacter baumannii clonal lineages. Int J Antimicrob Agents 2013;41:11-19. [ Links ]
13. Sahl JW, Gillece JD, Schupp JM. Evolution of a pathogen: a comparative genomics analysis identifies a genetic pathway to pathogenesis in Acinetobacter. PLoS One 2013; 8:e54287. [ Links ]
14. Diancourt L, Passet V, Nemec A. The population structure of Acinetobacter baumannii: expanding multiresistant clones from an ancestral susceptible genetic pool. PLoS One. 2010;5:e10034. [ Links ]
15. Antunes LC, Visca P, Toener DJ. Acinetobacter baumannii: evolution of a global pathogen. Pathogens Dis 2014;71:292-301. [ Links ]
16. El-Saed A, Balkhy HH, Al-Dorzi HM, Khan R, Rishu A.H, Arabi YM. Acinetobacter is the most common pathogen associated with late-onset and recurrent ventilator-associated pneumonia in an adult intensive care unit in Saudi Arabia. Int J Infect Dis 2013; 17:e696-e701. [ Links ]
17. McGrath EJ, Chopra T, Abdel-Haq N, Preney K, Koo W, Asmar BI, et al. An outbreak of carbapenem-resistant Acinetobacter baumannii infection in a neonatal intensive care unit: investigation and control. Infect Control Hosp Epidemiol. 2011;32:34-41. [ Links ]
18. Markogiannakis A, Fildisis G, Tsiplakou S, Ikonomidis A, Koutsoukou A, Pournaras S, et al. Cross-transmission of multidrug-resistant Acinetobacter baumannii clonal strains causing episodes of sepsis in a trauma intensive care unit. Infect Control Hosp Epidemiol 2008;29: 410-17. [ Links ]
19. Weber DJ, Rutala WA, Miller MB, Huslage K, Sickbert Bennett E. Role of hospital surfaces in the transmission of emerging health care-associated pathogens: norovirus, Clostridium difficile, and Acinetobacter species. Am J Infect Control 2010;38(5 suppl 1):S25-S33. [ Links ]
20. Denton M, Wilcox MH, Parnell P, Green D, Keer V, Hawkey PM, Evans I, Murphy P. Role of environmental cleaning in controlling an outbreak of Acinetobacter baumannii on a neurosurgical intensive care unit. J Hosp Infect. 2004;56:106-110. [ Links ]
21. Murray CK, Yun HC, Roop SA, Hospenthal DR, Gourdine E, Dooley DP. Bacteria recovered from patients admitted to a deployed U.S. military hospital in Baghdad, Iraq. Mil Med 2006;171:821-5. [ Links ]
22. Centers for Disease Control and Prevention. Acinetobacter baumannii infections among patients at military medical facilities treating US service members, 2002-2004. MMWR Morb Mortal Wkly Rep 2004;53:1063-6. [ Links ]
23. Davis KA, Moran KA, McAllister CK, Gray PJ. Multidrug-resistant Acinetobacter extremity infections insoldiers. Emerg Infect Dis 2005; 11:1218-24. [ Links ]
24. BoucherHW, TalbotGH, Benjamin DK Jr, Bradley J, Guidos RJ, Jones RN, Murray BE, Bonomo RA, Gilbert D. 10 x '20 progressdevelopment of new drugs active against gram-negative bacilli: an upda-te from the Infectious Diseases Society of America. Clin Infect Dis 2013;56:1685-94.
25. Penwell WF, Arivett BA, Actis LA. The Acinetobacter baumannii ent A gene located outside the acinetobactin cluster is critical for siderophore production, iron acquisition and virulence. PLoSOne. 2012;7:e36493. [ Links ]
26. Cerqueira GM, Peleg AY. Insights into Acinetobacter baumannii pathogenicity. IUBMB Life. 2011;63:1055-60. [ Links ]
27. Gaddy JA, Actis LA. Regulation of Acinetobacter baumannii biofilm formation. Future Microbiol 2009;4:273-8. [ Links ]
28. Zimbler DL, Penwell WF, Gaddy JA, Menke S, Tomaras A, Connerly P, et al. Iron acquisition functions expressed by the human pathogen Acinetobacter baumannii. Biometals 2009;22:23-32. [ Links ]
29. Kramer A, Schwebke I, Kampf G. How long do nosocomial pathogenspersist on inanimate surfaces?. A systemic review. BMC Infect Dis. 2006;6:130-7. [ Links ]
30. Joly-Guillou M-L. Clinical impact and pathogenicity of Acinetobacter. Clin Microbiol Infect 2005;11:868-73. [ Links ]
31. Tsuchiya T, Nakao N, Yamamoto S, Hirai Y, Miyamoto K, Tsujibo H. NK1.1(+) cells regulate neutrophil migration in mice with Acinetobacter baumannii pneumonia. Microbiol Immunol 2012;56:107-16. [ Links ]
32. Breslow JM. Innate immune responses to systemic Acinetobacter baumannii infection in mice: neutrophils, but not interleukin-17, mediate host resistance. Infect Immun 2011;79:3317-27. [ Links ]
33. Mortensen BL, SkaarEP. Host-microbe interactions that shape the pathogenesis of Acinetobacter baumannii infection. Cell Microbiol 2012;14:1336-44. [ Links ]
34. Glew RH, Moellering RC Jr, Kunz LJ. Infections with Acinetobacter calcoaceticus (Herellea vaginicola): Clinical and laboratory studies. Medicine (Baltimore) 1977;56:79-97. [ Links ]
35. O'Connell CJ, Hamilton R. Gram-negative rod infections: II. Acinetobacter infections in general hospital. N Y State J Med 1981;81:750-3. [ Links ]
36. Chen MZ, Hsueh PR, Lee LN, Lo FH, Lo KF, Ho PL. Severe community-acquired pneumonia due to Acinetobacter baumannii. Chest 2001;120:1072-7. [ Links ]
37. Leung WS, Chu CM, Tsang KY, Lo FH, Lo, KF, Ho PL. Fulminant community-acquired Acinetobacter baumannii pneumonia as a distinct clinical syndrome. Chest 2006; 129:102-9. [ Links ]
38. Ong CW, Lye DC, Khoo KL, Chua GS, Yeoh SF, Leo YS, et al. Severe community-acquired Acinetobacter baumannii pneumonia: an emerging highly lethal infectious disease in the Asia-Pacific. Respirology 2009; 14:1200-5. [ Links ]
39. Goodhart GL, Abrutyn E, Watson R. Community-acquired Acinetobacter calcoaceticus var anitratus pneumonia. JAMA 1977;238:1516-18. [ Links ]
40. Anstey NM, Currie BJ, Hassell M, Palmer D, Dwyer B, Seifert H. Community-acquired bacteremic Acinetobacter pneumonia in tropical Australia is caused by diverse strains of Acinetobacter baumannii, with carriage in the throat of at risk groups. J Clin Microbiol 2002;40:685-6. [ Links ]
41. National Nosocomial Infections Surveillance System. National Nosocomial Infections Surveillance (NNIS) System Reports, data summary from January 1992 through June 2004, issued Oct 2004. Am J Infect Control 2004;32:470-85. [ Links ]
42. Muñoz-Price LS, Weinstein RA. Acinetobacter infection. N Engl J Med 2008;358:1271-81. [ Links ]
43. Lambert ML, Suetens C, Savey A, Palomar M, Hiesmayr M, Morales I, et al. Clinical outcomes of health-care-associated infections and antimicrobial resistance in patients admitted to European intensive-care units: a cohort study. Lancet Infect Dis 2011;11:30-8. [ Links ]
44. Fagon J-Y, Chastre J, Domart Y, Trouillet JL, Gibert C. Mortality due to ventilator associated pneumonia or colonization with Pseudomonas or Acinetobacter species: Assessment by quantitative culture of samples obtained by protected specimen brush. Clin Infect Dis 1996;23:538-42. [ Links ]
45. Wisplinghoff H, Paulus T, Lugenheim M, Stefanik D, Higgins PG, Edmond MB, Wenzel RP, Seifert H. Nosocomial bloodstream infections due to Acinetobacter baumannii, Acinetobacter pittii and Acinetobacter nosocomialis in the United States. J Infect 2012;64:282-90. [ Links ]
46. Tsai HY, Cheng A, Liu CY, Huang YT, Lee YC, Liao CH, Hsueh PR. Bacteremia caused by Acinetobacter junii at a medical center in Taiwan, 2000-2010. Eur J Clin Microbiol Infect Dis 2012;31:2737-2743. [ Links ]
47. Ku SC, Hsueh PR, Yang PC, Luh Kt. Clinical and microbiological characteristics of bacteremia caused by Acinetobacter lwoffii. Eur J Clin Microbiol Infect Dis. 2000;19:501-505. [ Links ]
48. Seifert H, Strate A, Pulverer G. Nosocomial bacteremia due to Acinetobacter baumannii. Clinical features, epidemiology, and predictors of mortality. Medicine (Baltimore). 1995;74:340-39. [ Links ]
49. Gaynes R, Edwards JR; National Nosocomial Infections Surveillance System. Overview of nosocomial infections caused by gram-negative bacilli. Clin Infect Dis. 2005;41: 848-54. [ Links ]
50. Pour NK, Dusane DH, Dhakephalkar PK. Bio-film formation by Acinetobacter baumannii strains isolated from urinary tract infection and urinary catheters. FEMS Immunol Med Microbiol 2011;62:328-38. [ Links ]
51. Chang WN, Lu CH, Huang CR, Chuang YC. Community-acquired Acinetobacter meningitis in adults. Infection 2000;28:395-7. [ Links ]
52. Allen DM, Wong SY. Acinetobacter: A perspective. Singapore Med J 1990;31:511-14. [ Links ]
53. Maegele M, Gregor S, Steinhausen E, et al. The long-distance tertiary air transfer and care of tsunami victims: Injury patterns and microbiologic and psychologic aspects. Crit Care Med 2005;33:1136-40. [ Links ]
54. Oncul O, Keskin O, Acar HV, Kucukardali Y, Evrenkaya R, Atasoyu EM, et al. Hospital-acquired infections following the 1999 Marmara earthquake. J Hosp Infect 2002;51:47-51. [ Links ]
55. Peyman GA, Vastine DW, Diamond JG. Vitrectomy and intraocular gentamicin management of Herellea endophthalmitis after incomplete phacoemulsification. Am J Ophthalmol 1975;80: 764-5. [ Links ]
56. Wand M, Olive GM, Mangiaracine AB. Corneal perforation and iris prolapse due to Mima polymorpha. Arch Ophthalmol 1975;93:239-41. [ Links ]
57. Gradon JD, Chapnick EK, Lutwick LI. Infective endocarditis of a native valve due to Acinetobacter: Case report and review. Clin Infect Dis 1992;14:1145-8. [ Links ]
58. Van Looveren M, Goossens H: Antimicrobial resistance of Acinetobacter spp. in Europe. Clin Microbiol Infect 2004; 10:684-704 [ Links ]
59. Levin AS: Treatment of Acinetobacter spp. infections. Expert Opin Pharmacother 2003;4:1289-96. [ Links ]
60. Mahgoub S, Ahmed J, Glatt AE. Underlying characteristics of patients harboring highly resistant Acinetobacter baumannii. Am J Infect Control 2002;30:386-90 [ Links ]
61. Kopterides P, Koletsi PK, Michalopoulos A, Falagas ME. Exposure to quinolones is associated with carbapenem resistance among colistin-susceptible Acinetobacter baumannii blood isolates. Int J Antimicrob Agents 2007;30(5):409-14 [ Links ]
62. Livermore D: The zeitgeist of resistance. J Antimicrob Chemother 2007;60(Suppl. 1):59-61. [ Links ]
63. Landman D, Quale JM, Mayorga D, Adedeji A, Vangala K, Ravishankar J, et al. Citywide clonal outbreak of multiresistant Acinetobacter baumannii and Pseudomonas aeruginosa in Brooklyn, NY: the preantibiotic era has returned. Arch Intern Med 2002;162,1515-20 [ Links ]
64. Zarrilli R, Crispino M, Bagattini M, Barretta E, DiPopolo A, Triassi M, et al. Molecular epidemiology of sequential outbreaks of Acinetobacter baumannii in an intensive care unit shows the emergence of carbapenem resistance. J Clin Microbiol 2004;42:946-53 [ Links ]
65. Yum JH, Yi K, Lee H et al.Molecular characterization of metallo-ß-lactamase-producing Acinetobacter baumannii and Acinetobacter genomospecies 3 from Korea: identification of two new integrons carrying the bla (VIM-2) gene cassettes. J Antimicrob Chemother 2002;49:837-40 [ Links ]
66. Van Looveren M, Goossens H: Antimicrobial resistance of Acinetobacter spp. in Europe. Clin Microbiol Infect 2004; 1:684-704 [ Links ]
67. Halstead DC, Abid J, Dowzicky MJ. Antimicrobial susceptibility among Acinetobacter calcoaceticus-baumannii complex and Enterobacteriaceae collected as part of the Tigecycline Evaluation and Surveillance Trial. J Infect 2007; 55: 49-57. [ Links ]
68. Gales AC, Jones RN, Forward KR, Linares J, Sader HS, Verhoef J. Emerging importance of multidrug-resistant Acinetobacter species and Stenotrophomonas maltophilia as pathogens in seriously ill patients: geographic patterns, epidemiological features, and trends in the SENTRY Antimicrobial Surveillance Program (1997-1999). Clin Infect Dis 2001; 32 (suppl2): S104-13. [ Links ]
69. Gales AC, Jones RN, Sader HS. Global assessment of the antimicrobial activity of polymyxin B against 54.731 clinical isolates of Gram-negative bacilli: report from the SENTRY antimicrobial surveillance programme (2001-2004). Clin Microbiol Infect 2006; 12:315-21. [ Links ]
70. Sahl JW, Gillece JD, Schupp JM. Evolution of a pathogen: a comparative genomics analysis identifies a genetic pathway to pathogenesis in Acinetobacter. PLoS One 2013;8:e54287. [ Links ]
71. Rice LB. Challenges in identifying new antimicrobial agents effective for treating infections with Acinetobacter baumannii and Pseudomonas aeruginosa. Clin Infect Dis. 2006;43(suppl 2):S100-S105. [ Links ]
72. Fournier PE, Vallenet D, Barbe V. Comparative genomics of multidrug resistance in Acinetobacter baumannii. PLoS Genet 2006;2:e7. [ Links ]
73. Bonomo RA, Szabo D. Mechanisms of multidrug resistance in Acinetobacter species and Pseudomonas aeruginosa. Clin Infect Dis. 2006;43(suppl 2):S49-S56 [ Links ]
74. Jacoby GA. AmpC beta-lactamases. Clin Microbiol Rev 2009;22:161-82. [ Links ]
75. Heritier C, Poirel L, Nordmann P. Cephalosporinase over-expression resulting from insertion of ISAba1 in Acinetobacter baumannii. Clin Microbiol Infect 2006;12:123-30. [ Links ]
76. Poirel L, Bonnin RA, Nordmann P. Genetic basis of antibiotic resistance in pathogenic Acinetobacter species. IUBMB Life 2011;63:1061-7. [ Links ]
77. Higgins PG, Dammhayn C, Hackel M, Seifert, H. Global spread of carbapenem-resistant Acinetobacter baumannii. J Antimicrob Chemother 2010;65:233-8. [ Links ]
78. Walsh TR, Toleman MA, Poirel L, Nordmann P. Metallo-beta-lactamases: the quietbefore the storm? Clin Microbiol Rev 2005; 18:306-25. [ Links ]
79. Ghazawi A, Sonnevend A, Bonnin RA, Poirel L, Nordmann P, Hashmey R, et al. NDM-2 carbapenemase-producing Acinetobacter baumannii in the United Arab Emirates. Clin Microbiol Infect 2012;18:E34-E36. [ Links ]
80. Nordmann P, Poirel L, Walsh TR. The emerging NDM carbapenemases. Trends Microbiol 2011;19:588-95. [ Links ]
81. Coyne S, Courvalin P, Perichon B. Efflux-mediated antibiotic resistance in Acinetobacter spp. Antimicrob Agents Chemother 2011;55:947-53. [ Links ]
82. Peleg AY, Adams J, Paterson DL. Tigecycline efflux as a mechanism for nonsusceptibility in Acinetobacter baumannii. Antimicrob Agents Chemother 2007;51:2065-9. [ Links ]
83. Zavascki AP, Carvalhaes CG, Picão RC. Multidrug-resistant Pseudomonas aeruginosa and Acinetobacter baumannii: resistance mechanisms and implications for therapy. Expert Rev Anti Infect Ther 2010;8:71-93. [ Links ]
84. Nemec A, Dolzani L, Brisse S, vandenBroek P, Dijkshoorn L. Diversity of aminoglycoside-resistance genes and their association with class 1 integrons among strains of pan-European Acinetobacter baumannii clones. J Med Microbiol 2004;53(pt 12): 1233-40. [ Links ]
85. Doi Y, Adams JM, Yamane K, Paterson DL. Identification of 16S rRNA methylase-producing Acinetobacter baumannii clinical strains in North America. Antimicrob Agents Chemother 2007;51:4209-10. [ Links ]
86. Lopes BS, Amyes SG. Insertion sequence disruption of adeR and ciprofloxacin resistance caused by efflux pumps and gyrA and parC mutations in Acinetobacter baumannii. Int J Antimicrob Agents 2013;41:117-21. [ Links ]
87. Vila J, Ruiz J, Goñi P. Mutation in the gyrA gene of quinolone-resistant clinical isolates of Acinetobacter baumannii. Antimicrob Agents Chemother 1995;39:1201-3. [ Links ]
88. Vila J, Ruiz J, Goñi P. Quinolone-resistance mutations in the topoisomerase IV parC gene of Acinetobacter baumannii. J Antimicrob Chemother 1997;39:757-62. [ Links ]
89. Adams MD, Nickel GC, Bajaksouzian S, Lavender H, Murthy A. Jacobs MR, et al. Resistance to colistin in Acinetobacter baumannii associated with mutations in the PmrAB two-component system. Antimicrob Agents Chemother 2009;53:3628-34.
90. Cai Y, Chai D, Wang R, Liang, B.; Bai, N. Colistin resistance of Acinetobacter baumannii: clinical reports, mechanisms and antimicrobial strategies. J Antimicrob Chemother 2012;67:1607-15. [ Links ]
91. Lopez-Rojas R, Domínguez-Herrera J, McConnell MJ, Docobo F, Smani Y, Fernandez M. et al. Impaired virulence and in vivo fitness of colistin-resistant Acinetobacter baumannii. J Infect Dis 2011;203:545-8. [ Links ]
92. Rolain JM, Roch A, Castanier M, Papazian L, Raoult D. Acinetobacter baumannii resistant to colistin with impaired virulence: a case report from France. J Infect Dis 2011;204:1146-7. [ Links ]
93. Segal H, Thomas R, Gay EB: Characterization of class 1 integron resistance gene cassettes and the identification of a novel IS-like element in Acinetobacter baumannii.Plasmid 2003 ;49:169-78 [ Links ]
94. De Vries J, Wackernagel W: Integration of foreign DNA during natural transformation of Acinetobacter spp. by homology-facilitated illegitimate recombination. Proc Natl Acad Sci USA 2002;99:2094-9. [ Links ]
95. Poirel L, Menuteau O, Agoli N, Cattoen C, Nordmann P: Outbreak of extended-spectrum ß-lactamase VEB-1-producing isolates of Acinetobacter baumannii in a French hospital. J Clin Microbiol 2003;41:3542-7. [ Links ]
96. Ruiz J, Navia MM, Casals C, Sierra JM, Jimenez De Anta MT, Vila J: Integron-mediated antibiotic multi-resistance in Acinetobacter baumannii clinical isolates from Spain. Clin Microbiol Infect 2003; 9:907-11. [ Links ]
97. Oh JY, Kim KS, Jeong YW, Cho JW, Park JC, Lee JC: Epidemiological typing and prevalence of integrons in multiresistant Acinetobacter isolates. APMIS 2002; 110:247-52. [ Links ]
98. Gallego L, Towner KJ: Carriage of class 1 integrons and antibiotic resistance in clinical isolates of Acinetobacter baumannii from northern Spain. J Med Microbiol 2001; 50:71-7. [ Links ]
99. Gombac F, Riccio ML, Rossolini GM, Lagatolla C, Tonin E, MontiBragadin C, Lavenia A, Dolzani L. Molecular characterization of integrons in epidemiologically unrelated clinical isolates of Acinetobacter baumannii from Italian hospitals reveals a limited diversity of gene cassette arrays. Antimicrob Agents Chemother 2002;46:3665-8. [ Links ]
100. Falagas ME, Koletsi PK, Bliziotis IA: The diversity of definitions of multidrug-resistant (MDR) and pan-drug-resistant (PDR) Acinetobacter baumannii and Pseudomonas aeruginosa. J Med Microbiol 2006; 55:1619-29. [ Links ]
101. Towner KJ. Acinetobacter: an old friend, but a new enemy. J Hosp Infect 2009;73:355-63. [ Links ]
102. Rodriguez-Martinez JM, Nordmann P, Ronco E, Poirel L. Extended-spectrum cephalosporinase in Acinetobacter baumannii. Antimicrob Agents Chemother2010;54:3484-8. [ Links ]
103. Tian GB, Adams-Haduch JM, Taracila M, Bonomo RA, Wang HN, Doiet Y. Extended-spectrum AmpC cephalosporinase in Acinetobacter baumannii: ADC-56 confers resistance to cefepime. Antimicrob Agents Chemother 2011;55:4922-5. [ Links ]
104. Gales AC, Jones RN, Forward KR, Linares J, Sader HS, Verhoef J. Emerging importance of multidrug-resistant Acinetobacter species and Stenotrophomonas maltophilia as pathogens in seriously ill patients: geographic patterns, epidemiological features, and trends in the SENTRY Antimicrobial Surveillance Program (1997-1999). [ Links ]
105. Gales AC, Jones RN, Sader HS. Global assessment of theantimicrobial activity of polymyxin B against 54 731 clinical isolates of Gram-negative bacilli: report from the SENTRY antimicrobial surveillance programme (2001-2004). Clin Microbiol Infect 2006; 12:315-21. [ Links ]
106. Reinert RR, Low DE, Rossi F, Zhang X, Wattal C, Dowzicky MJ. Antimicrobial susceptibility among organisms from the Asia/Pacific Rim, Europe and Latin and North America collected as part of test and the invitro activity of tigecycline. J Antimicrob Chemother 2007;60: 1018-29. [ Links ]
107. Poirel L, Nordmann P. Carbapenem resistance in Acinetobacter baumannii: mechanisms and epidemiology. Clin Microbiol Infect 2006; 12: 826-36. [ Links ]
108. Gomes Chagas TP, Rangel Carvalho K, De Oliveira Santos IC, D'Alincourt Carvalho-Assef AP, Dutra Asensi M. Characterization of carbapenem-resistant Acinetobacter baumannii in Brazil (2008-2011): country wide spread of OXA-23-producing clones (CC15 and CC79). Diagn Microbiol Infect Dis 2014; 79: 468-72. [ Links ]
109. Rafailidis PI, Ioannidou EN, Falagas ME. Ampicillin/sulbactam: current status in severe bacterial infections. Drugs 2007; 67: 1829-49 [ Links ]
110. Corbella X, Ariza J, Ardanuy C. Efficacy of sulbactam alone and in combination with ampicillin in nosocomial infections caused by multiresistant Acinetobacter baumannii. J Antimicrob Chemother 1998; 42: 793-802. [ Links ]
111. Smolyakov R, Borer A, Riesenberg K, Schlaeffer F, Alkan M, Porath et al. Nosocomial multi-drug resistant Acinetobacter baumannii bloodstream infection: risk factors and outcome with ampicillin-sulbactam treatment. J Hosp Infect. 2003;54:32-38.
112. Jimenez-Mejias ME, Pachón J, Becerril B, Palomino-Nicás J, Rodriguez-Cobacho A, Revuelta M. Treatment of multidrug-resistant Acinetobacter baumannii meningitis with ampicillin/sulbactam. Clin Infect Dis 1997;24:932-5. [ Links ]
113. Akers KS, Chaney C, Barsoumian A, Beckius M, Zera W, Yu, X, et al. Aminoglycoside resistance and susceptibility testing errors in Acinetobacter baumannii-calcoaceticus complex. J Clin Microbiol. 2010; 48:1132-8. [ Links ]
114. Vidal L, Gafter-Gvili A, Borok S, Fraser A, Leibovici L, Paul M. Efficacy and safety of aminoglycoside monotherapy: systematic review and meta-analysis of randomized controlled trials. J Antimicrob Chemother 2007;60:247-57. [ Links ]
115. Panidis D, Markantonis SL, Boutzouka E, Karatzas S, Baltopoulos G. Penetration of gentamicin into the alveolar lining fluid of critically ill patients with ventilator-associated pneumonia. Chest 2005;128:545-52. [ Links ]
116. Jung S, Yu JK, Shin SH, Park KG, Jekarl DW, Han K, et al. False susceptibility to amikacin by VITEK 2 in Acinetobacter baumannii harboring armA. Ann Clin Lab Sci 2010;40:167-71. [ Links ]
117. Karageorgopoulos DE, Falagos ME. Current control and treatment of multidrug-resistant Acinetobacter baumannii infections. Lancet Infect Dis 2008;8:751-62. [ Links ]
118. Karageorgopoulos DE, Kelesidis T, Kelesidis I, Falagas ME. Tigecycline for the treatment of multidrug-resistant (including carbapenem-resistant) Acinetobacter infections: a review of the scientific evidence. J Antimicrob Chemother 2008;62: 45-55. [ Links ]
119. Muralidharan G, Micalizzi M, Speth J, Raible, D, Troy S. Pharmacokinetics of tigecycline after single and multiple doses in healthy subjects. Antimicrob Agents Chemother 2005;49: 220-9. [ Links ]
120. Hornsey M, Loman N, Wareham DW, Ellington MJ, Pallen MJ, Turton JF, et al. Whole-genome comparison of two Acinetobacter baumannii isolates from a single patient, where resistance developed during tigecycline therapy. J Antimicrob Chemother 2011;66:1499-1503.
121. Chan JD, Graves JA, Dellit TH. Antimicrobial treatment and clinical outcomes of carbapenem-resistant A cinetobacter baumannii ventilator-associated pneumonia. J Intensive Care Med 2010;25:343-8. [ Links ]
122. Mullangi PK, Pankey GA. Tigecycline in critical care. Crit Care Clin 2008;24:365-75 [ Links ]
123. Hawley JS, Murray CK, Griffith ME, McElmeel ML Fulcher LC, Hospenthal D.R, Jorgens JH. Susceptibility of Acinetobacter strains isolated from deployed U.S. military personnel. Antimicrob Agents Chemother 2007;51:376-8. [ Links ]
124. Bishburg E, Bishburg K. Minocyclinean old drug for a new century: emphasis on methicillin-resistant Staphylococcus aureus (MRSA) and Acinetobacter baumannii. Int J Antimicrob Agents 2009;34:395-401. [ Links ]
125. Liang W, Liu XF, Huang J. Activities of colistin and minocycline-based combinations against extensive drug resistant Acinetobacter baumannii isolates from intensive care unit patients. BMC Infect Dis 2011;11:109. [ Links ]
126. Henwood CJ, Gatward T, Warner M, James D, Stockdale MW, Spence RP, et al. Antibiotic resistance among clinical isolates of acinetobacter in the UK, and in vitro evaluation of tigecycline (GAR-936). J Antimicrob Chemother 2002;49: 479-87. [ Links ]
127. Insa R, Cercenado E, Goyanes MJ, Morente A, Bouza E. In vitro activity of tigecycline against clinical isolates of Acinetobacter baumannii and Stenotrophomonas maltophilia. J Antimicrob Chemother 2007; 59: 583-5. [ Links ]
128. Song JY, Kee SY, Hwang IS, Yamaguchi H, Abe S. In vitro activities of carbapenem/sulbactam combination, colistin, colistin/rifampicin combination and tigecycline against carbapenem-resistant Acinetobacter baumannii. J Antimicrob Chemother 2007; 60: 317-22. [ Links ]
129. Coelho JM, Turton JF, Kaufmann ME, Glover J, Woodford N, Warner M, et al. Occurrence of carbapenem-resistant Acinetobacter baumannii clones at multiple hospitals in London and southeast England. J Clin Microbiol 2006;44: 3623-7. [ Links ]
130. Scheetz MH, Qi C, Warren JR, Postelnick MJ, Zembower T, Obias A, et al. In vitro activities of various antimicrobials alone and in combination with tigecycline against carbapenem-intermediate or resistant Acinetobacter baumannii. Antimicrob Agents Chemother 2007; 51: 1621-6. [ Links ]
131. Falagas ME, Bliziotis IA, Tam VH. Intraventricular or intrathecal use of polymyxins in patients with Gram-negative meningitis: a systematic review of the available evidence. Int J Antimicrob Agents 2007; 29: 9-25. [ Links ]
132. Ng J, Gosbell IB, Kelly JA, Boyle MJ, Ferguson JK. Cure of multiresistant Acinetobacter baumannii central nervous system infections with intraventricular or intrathecal colistin: case series and literature review. J Antimicrob Chemother 2006; 58: 1078-81. [ Links ]
133. Jimenez-Mejias ME, Pichardo-Guerrero C, Marquez-Rivas FJ, Martin-Lozano D, Prados T, Pachon J. Cerebrospinal fluid penetration and pharmacokinetic/pharmacodynamic parameters of intravenously administered colistin in a case of multidrug-resistant Acinetobacter baumannii meningitis. Eur J Clin Microbiol Infect Dis 2002; 21: 212-14. [ Links ]
134. Katragkou A, Roilides E. Successful treatment of multidrugresistant Acinetobacter baumannii central nervous system infections with colistin. J Clin Microbiol 2005; 43: 4916-17. [ Links ]
135. Paramythiotou E, Karakitsos D, Aggelopoulou H, Sioutos P, Samonis G, Karabinis A. Post-surgical meningitis due to multiresistant Acinetobacter baumannii. Eff ective treatment with intravenous and/or intraventricular colistin and therapeutic dilemmas. Med Mal Infect 2007; 37: 124-25. [ Links ]
136. Guardado AR, Blanco A, Asensi V, Perez F, Rial JC, Pintado V, et al. Multidrugresistant acinetobacter meningitis in neurosurgical patients with intraventricular catheters: assessment of different treatments.J Antimicrob Chemother 2008; 61: 908-13. [ Links ]
137. Rafailidis PI, Ioannidou EN, Falagas ME. Ampicillin/sulbactam: current status in severe bacterial infections. Drugs 2007; 67: 1829-49 [ Links ]
138. Hawley JS, Murray CK, Jorgensen JH. Colistin heteroresistance in acinetobacter and its association with previous colistin therapy. Antimicrob Agents Chemother. 2008;52: 351-2. [ Links ]
139. Nemec A, Dijkshoorn L. Variations in colistin susceptibility among different species of the genus Acinetobacter. J Antimicrob Chemother. 2010;65:367-9. [ Links ]
140. Halstead DC, Abid J, Dowzicky MJ. Antimicrobial susceptibility among Acinetobacter calcoaceticus-baumannii complex and Enterobacteriaceae collected as part of the Tigecycline Evaluation and Surveillance Trial. J Infect 2007; 55: 49-57. [ Links ]
141. Hornsey M, WarehamDW. Invivo efficacy of glyco-peptide-colistin combination therapies in a Galleria mellonella model of Acinetobacter baumannii infection. Antimicrob Agents Chemother. 2011;55:3534-7 [ Links ]
142. Tripodi MF, Durante-Mangoni E, Fortunato R, Utili R, Zarrilli R. Comparative activities of colistin, rifampicin, imipenem and sulbactam/ampicillin alone or in combination against epidemic multidrug-resistant Acinetobacter baumannii isolates producing OXA-58 carbapenemases. Int J Antimicrob Agents. 2007;30:537-40. [ Links ]
143. Pachón ME, Docobo F, Jiméne ME, Ibanez J, Garcia A, Pichardo C, et al. Efficacy of rifampin, in monotherapy and in combinations, in an experimental murine pneumonia model caused by panresistant Acinetobacter baumannii strains. Eur J Clin Microbiol Infect Dis. 2011;30:895-901. [ Links ]
144. Bassetti M, Repetto E, Righi E, Boni S, Diverio M, Molinari MP, et al. Colistin and rifampicin in the treatment of multidrug-resistant Acinetobacter baumannii infections. J Antimicrob Chemother 2008;61: 417-20. [ Links ]
145. Petrosillo N, Ioannidou E, Falagas ME. Colistin monotherapy vs. combination therapy: evidence from microbiological, animal and clinical studies. Clin Microbiol Infect. 2008;14:816-27. [ Links ]
146. Shields RK, Kwak EJ, Potoski BA. High mortality rates among solid organ transplant recipients infected with extensively drug-resistant Acinetobacter baumannii: using in vitro antibiotic combination testing to identify the combination of a carbapenem and colistin as an effective treatment regimen. Diagn Microbiol InfectDis. 2011;70: 246-52. [ Links ]
147. Motaouakkil S, Charra B, Hachimi A, et al. Colistin and rifampicin in the treatment of nosocomial infections from multiresistant Acinetobacter baumannii. J Infect 2006; 53: 274-78. [ Links ]
148. Petrosillo N, Chinello P, Proietti MF, Cecchini L, Masala M, Franchi C, et al. Combined colistin and rifampicin therapy for carbapenem-resistant Acinetobacter baumannii infections: clinical outcome and adverse events. Clin Microbiol Infect 2005; 11: 682-3. [ Links ]
149. Kasiakou SK, Michalopoulos A, Soteriades ES, Samonis G, Sermaides GJ, Falagas ME. Combination therapy with intravenous colistin for management of infections due to multidrug-resistant Gram-negative bacteria in patients without cystic fibrosis. Antimicrob Agents Chemother 2005; 49: 3136-46. [ Links ]
150. Ouderkirk JP, Nord JA, Turett GS, Kislak JW. Polymyxin B nephrotoxicity and efficacy against nosocomial infections caused by multiresistant Gram-negative bacteria. Antimicrob Agents Chemother 2003; 47: 2659-62. [ Links ]
151. Sobieszczyk ME, Furuya EY, Hay CM, Pancholi R DellaLatta P, Hammer SM, et al. Combination therapy with polymyxin B for the treatment of multidrug-resistant Gramnegative respiratory tract infections. J Antimicrob Chemother 2004;54: 566-69.
152. Durante-Mangoni E, Signoriello G, Andini R, Mattei A, De Cristoforo M, Murino P et al. Colistin and rifampicin compared with colistin alone for the treatment of serious infections due to extensively drug-resistant Acinetobacter baumannii: a multi-center, randomized clinical trial. Clin Infect Dis 2013;57:349-58. [ Links ]
153. Berlana D, Llop JM, Fort E, Badia MB, Jodar R. Use of colistin in the treatment of multiple-drug-resistant Gram-negative infections. Am J Health Syst Pharm 2005; 62: 39-47. [ Links ]
154. Michalopoulos A, Fotakis D, Virtzili S, Vletsas C, Raftopoulou S, Mastora Z, et al. Aerosolized colistin as adjunctive treatment of ventilator-associated pneumonia due to multidrug-resistant Gram-negative bacteria: a prospective study. Respir Med 2008; 102: 407-12. [ Links ]
155. Falagas ME, Kasiakou SK, Kofteridis DP, Roditakis G, Samonis G. Effectiveness and nephrotoxicity of intravenous colistin for treatment of patients with infections due to polymyxin-only susceptible (POS) Gram-negative bacteria. Eur J Clin Microbiol Infect Dis 2006; 25: 596-9. [ Links ]
156. Michalopoulos A, Kasiakou SK, Mastora Z, Rellos K, Kapaskelis AM, Falagas ME. Aerosolized colistin for the treatment of nosocomial pneumonia due to multidrug resistant Gram-negative bacteria in patients without cystic fi brosis. Crit Care 2005; 9: R53-59. [ Links ]
157. Peleg AY, Hooper DC. Hospital-acquired infections due to gram-negative bacteria. N Engl J Med 2010;362:1804-13. [ Links ]
158. Cooper TW, Pass SE, Brouse SD, Hall RG. Can pharmacokinetic and pharmacodynamic principles be applied to the treatment of multidrug-resistant Acinetobacter? Ann Pharmacother 2011;45 (2):229-40 [ Links ]
159. Roberts JA, Kirkpatrick CM, Roberts MS, Robertson TA, Dalley AJ, Lipman, J. Meropenem dosing in critically ill patients with sepsis and without renal dysfunction: intermittent bolus versus continuous administration? Monte Carlo dosing simulations and subcutaneous tissue distribution. J Antimicrob Chemother 2009;64:142-50. [ Links ]
160. Dalfino L, Puntillo F, Mosca A, Monno R, Spada ML, Coppolecchia S, et al. High-dose, extended-interval colistin administration in critically ill patients: is this the right dosing strategy? Apreliminary study. Clin Infect Dis 2012;54:1720-6. [ Links ]
161. Plachouras D, Karvanen M, Friberg LE, Papadomichelakis E, Antoniadou A, Tsangaris I, et al. Population pharmacokinetic analysis of colistin methane-sulfonate and colistin after intravenous administration in critically ill patients with infections caused by gram-negative bacteria. Antimicrob Agents Chemother 2009;53:3430-6. [ Links ]
162. Kalin G, Alp E, Coskun R. Use of high-dose IV and aerosolized colistin for the treatment of multidrug-resistant Acinetobacter baumannii ventilator-associated pneumonia: do we really need this treatment? J Infect Chemother 2012;18:872-7. [ Links ]
163. Khawcharoenporn T, Apisarnthanarak A, Mundy LM. Intrathecal colistin for drug-resistant Acinetobacter baumannii central nervous system infection: a case series and systematic review. Clin Microbiol Infect. 2010;16:888-94. [ Links ]
164. Celik IH, Oguz SS, Demirel G, Erdeve O, Dilmen U. Outcome of ventilator-associated pneumonia due to multidrug-resistant Acinetobacter baumannii and Pseudomonas aeruginosa treated with aerosolized colistin in neonates: a retrospective chart review. Eur J Pediatr 2012;171:311-6. [ Links ]
165. Lu Q, Luo R, Bodin L, Yang J, Zahr N, Aubry A, et al. Efficacy of high-dose nebulized colistin in ventilator-associated pneumonia caused by multidrug-resistant Pseudomonas aeruginosa and Acinetobacter baumannii. Anesthesiology 2012;117:1335-47. [ Links ]
166. Arnold HM, Sawyer AM, Kollef MH. Use of adjunctive aerosolized antimicrobial therapy in the treatment of Pseudomonas aeruginosa and Acinetobacter baumannii ventilator-associated pneumonia. Respir Care 2012;57: 1226-33 [ Links ]
167. Claeys KC, Fiorvento AD, Rybak MJ. A Review of Novel Combinations of colistin and lipopeptide or glycopeptide antibiotics for the treatment of multidrug-resistant Acinetobacter baumannii. Infect Dis Ther (2014) 3:69-81 [ Links ]
168. Fraimow HS, Tsigrelis C. Antimicrobial resistance in the intensive care unit: mechanisms, epidemiology, and management of specific resistant pathogens. Crit Care Clin 2011; 27:163-205. [ Links ]
169. Hong KB, Oh HS, Song JS. Investigation and control of an outbreak of imipenem-resistant Acinetobacter baumannii infection in a pediatric intensive care unit. Pediatr Infect Dis J 2012;31:685-90. [ Links ]
170. Denton M, Wilcox MH, Parnell P, Green D, Keer V, Hawkey PM, et al. Role of environmental cleaning in controlling an outbreak of Acinetobacter baumannii on a neurosurgical intensive care unit. J Hosp Infect 2004;56:106-10. [ Links ]
171. Otter JA, Yezli S, French GL. The role played by contaminated surfaces in the transmission of nosocomial pathogens. Infect Control Hosp Epidemiol. 2011;32:687-99. [ Links ]
172. Jawad A, Heritage J, Snelling AM. Influence of relative humidity and suspending menstrua on survival of Acinetobacter spp. on dry surfaces. J Clin Microbiol 1996;34: 2881-7. [ Links ]
173. Jawad A, Seifert H, Snelling AM, Heritage J, Hawkey PM. Survival of Acinetobacter baumannii on dry surfaces: comparison of outbreak and sporadic isolates. J Clin Microbiol 1998;36:1938- 41. [ Links ]
174. Kramer A, Schwebke I, Kampf G. How long do nosocomial pathogens persist on inanimate surfaces? A systematic review. BMC Infect Dis. 2006;6:130. [ Links ]
175. Cooper RA, Griffith CJ, Malik RE, Obee P, Looker N. Monitoring the effectiveness of cleaning in four British hospitals. Am J Infect Control 2007;35:338-41. [ Links ]
176. Corbella X, Pujol M, Argerich MJ, Ayats J, Sendra M, Pena C, et al. Environmental sampling of Acinetobacter baumannii: moistened swabs versus moistened sterile gauze pads. Infect Control Hosp Epidemiol 1999;20:458-60.
177. Kawamura-Sato K, Wachino J, Kondo T, Ito H, Arakawa Y. Reduction of disinfectant bactericidal activities in clinically isolated Acinetobacter species in the presence of organic material. J Antimicrob Chemother 2008;61:568-76. [ Links ]
178. Kawamura-Sato K, Wachino J, Kondo T, Ito, H.; Arakawa, Y. Correlation between reduced susceptibility to disinfectants and multidrug resistance among clinical isolates of Acinetobacter species. J Antimicrob Chemother 2010;65:1975-83. [ Links ]














