Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista de la Sociedad Boliviana de Pediatría
On-line version ISSN 1024-0675
Rev. bol. ped. vol.53 no.1 La Paz 2014
ACTUALIZACIÓN
L-Asparaginasa, un arma de doble filo pero de vital importancia
L-Asparaginase, a weapon with a double edged, but with a vital importance
Dr.: David Ballón Cossío*
* Médico de Unidad de Oncología. Hospital del Niño "Dr. Ovidio Aliaga Uría". La Paz
Correspondencia: Dr. David Ballón, correo electrónico: eido.dbc@hotmail.es
Conflicto de intereses: ninguno que declarar.
Articulo recibido el 8/2/14 y que fue aceptado para su publicación el 23/03/14.
Introducción
La L-asparaginasa (L-ASP) es una enzima que hidroliza la asparagina en amonio y ácido aspártico y la glutamina en ácido glutámico y amonio1,2. Aunque la función es simple y la asparagina es un aminoácido no esencial, tiene repercusión importante en el tratamiento de la leucemia, considerándosela como un elemento central en el tratamiento de la leucemia linfoblástica aguda (LLA) pediátrica1-3,5, además puede utilizarse como esquemas de terapia en linfomas no Hodgkin o leucemia mieloblastica aguda6. En general la L-ASP tiene menores efectos adversos que los reportados por otros quimioterápicos, pero los eventos secundarios a esta enzima son de importancia para la modificación de las terapias y posibles efectos a largo plazo en los pacientes. Las dosis varían según el protocolo utilizado entre 5,000 UI/m2 a 25,000 UI/m2. Aunque la mayoría de los protocolos administran este medicamento en fases de inducción y reinducción, se intenta prolongar su utilización incluso en otras fases, que pueden presentar efectos como mielosupresión3.
Efectos positivos en las terapias
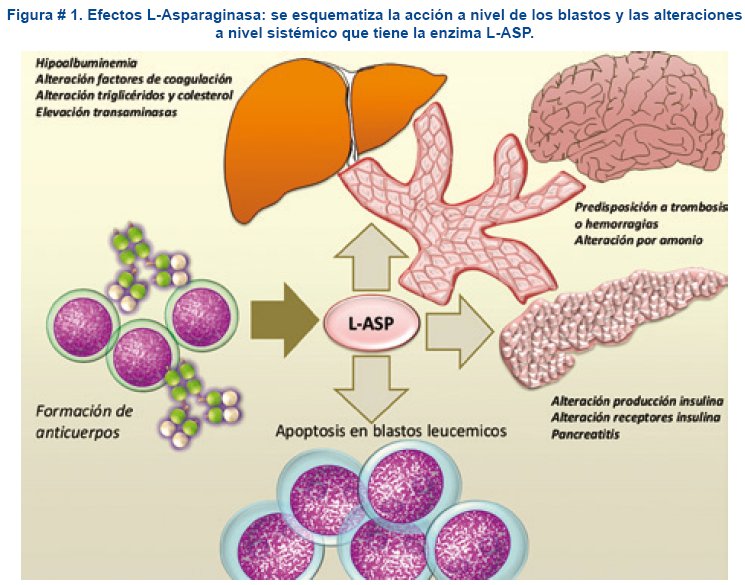
El motivo por el cual es tan importante esta acción de L-ASP se debe a que la mayoría de las células blasticas de la LLA, no posee la enzima para sintetizar la asparagina, dependiendo casi exclusivamente de la que se encuentra en la sangre, así vemos que los blastos que presentan la translocación TEL-AML1 o blastos con hiperdiploidias (ambos factores de buen pronóstico) son muy susceptibles a esta deplesión, pero las LLA- de células T y los que poseen la translocación BCR-ABL son menos sensibles a los efectos de esta enzima7-9. Al contrario muchos de los tejidos contienen la asparagina-sintetasa, evitando que los efectos de la L-ASP sean intensos en el cuerpo4. La asparagina es un aminoácido importante para formar proteínas, motivo por el cual cuando disminuye este aminoácido los blastos entran en apoptosis1, aunque esta disminución de asparagina para activar la apoptosis es aceptado, hay factores que tiene importancia en la respuesta y pueden incluso modificarla, así vemos que la producción de asparagina por la células mesenquimales de la medula ósea producen un efecto protector para los blastos8. Hay blastos de LLA que contienen la enzima para sintetizar asparagina, motivo por el cual es una razón para la resistencia a este medicamento. La depleción de asparagina también influyen a nivel del sistema nervioso central (SNC), considerándose un medicamento profiláctico para la recaída del SNC a pesar que no traspasa la barrera hematoencefalica, pero esta depleción sistémica también afectara a los blastos en el SNC7,9. Ver figura #1.
Actualmente hay disponible tres formas de esta enzima, la producida por Escherichia coli, la producida por Erwinia chrysanthemi y una forma sintética, la L-asparaginasa pegilada de E. coli que contiene cadenas de polietilen glicol (PEG-ASP)1,5,9. En el caso de la PEG-ASP la ventaja mas grande, es que la vida media es mayor, por tanto produce una mayor reducción de asparagina y las reacciones a esta enzima son menores por tener cadenas de carbohidratos que imitan a las proteínas sintetizadas en el cuerpo. Se puede monitorizar la actividad de la L-ASP, la misma que debe ser mayor a 100 U/L para obtener una hidrólisis completa en el plasma1, lamentablemente no está disponible en muchos centro esta cuantificación. La L-ASP se recomienda que se administre por vía intramuscular con lidocaína, debido a que la administración por vía endovenosa produce mayor efectos de hipersensibilidad y tóxicas en los pacientes4. Es importante la administración de L-ASP a pesar de las toxicidades leves a moderadas, debido a que la sobrevida libre de eventos de los pacientes es mayor si pueden tolerar todas o cerca a todas las dosis de los protocolos, modificándose esta sobrevida a los 5 años de un 90% a un 76% de los pacientes, siendo un factor de riesgo actualmente la falta de administración de este medicamento7.
Efectos negativos en las terapias
Reacciones de hipersensibilidad: se considera como un evento tóxico de mayor frecuencia, debido a que producirá reacciones inmunitarias, induciendo la formación de anticuerpos que irán a inactivar la enzima administrada, que por lo general se acompaña de reacciones alérgicas clínicas cuando el número de anticuerpos ya es elevado. Esta reacción inmunitaria con formación de anticuerpos producirá una inactivación de la enzima que incluso puede ser de forma silenciosa1,5,9. Este evento se incrementa cuando el número de administraciones es mayor. Las reacciones van desde leves alergias como eritema en el sitio de inyección, urticaria, broncoespasmo hasta reacciones anafilácticas en un 20 a 40%5-17. Los anticuerpos se reportan en un 30 a 70% de los pacientes pediátricos que reciben L-ASP de E. coli, siendo menores estas reacciones con la PEG-ASP y mucho menor con la L-ASP proveniente de Erwinia1,5. El mayor problema con esta reacción es que hay una mayor inactivación de la enzima, pero las reacciones adversas aumentaran conforme continúe la administración de L-ASP1. La única manera de continuar con este esquema de terapia es el cambio de L-ASP producida de E. coli a la producida por Erwinia o a la PEG-ASP1.
Inhibición de síntesis de proteínas: esta acción es la más extendida de L-ASP y con mayor repercusión desde el punto de vista del paciente y las terapias. Se pueden observar alteraciones en la coagulación (trombosis, hemorragias), hipoalbuminemia, elevación de enzimas hepáticas, pancreatitis e hiperglicemia1,2. Estos eventos se incrementan en porcentaje cuando se asocia con otros medicamentos, como los corticoides, vincristina, daunorrubicina, o asociados a otros factores como el sexo, edad, índice de masa corporal etc.
Las trombosis por L-ASP puede ser a nivel de las venas periféricas o centrales, son eventos severos, pero poco frecuentes, presentándose típicamente con una media de 3 semanas del inicio de la fase de inducción6,8,9. Aunque las alteraciones en la coagulación producidas por L-ASP más glucocorticoides son desde predisposición a sangrados o trombosis, se vio que hay una predisposición a los estados de hipercoagulabilidad17-19. A pesar de las alteraciones que produce L-ASP como la disminución de los niveles de antitrombina III, plasminogeno, proteína
C, proteína S, disminución de la actividad fibrinolítica, alterando el tiempo de protrombina y tiempo de tromboplastina parcial y tiempo de sangrado; no hay un factor claro para este evento. Se reporta trombosis en 1 a 2 % de paciente con LLA6,9,19. Actualmente se asocia los eventos trombóticos al uso de prednisona, a la presencia de catéter venoso central y en menor medida trombofilias10 y se producen generalmente en el SNC o extremidades superiores8. El evento más frecuente es la trombosis venosa de seno sagital, que clínicamente va desde cefaleas, vómitos, alteraciones del estado mental, déficit motor a convulsiones. Actualmente la tomografía y la resonancia magnética, son los métodos para el diagnostico, con o sin contraste o con venografía19.
La hiperglicemia por L-ASP se presenta en un 10 a 15 % de los pacientes con LLA y se la define como la elevación de glucosa >200 mg/dl en una determinación o mas, o >140 mg/dl en dos ocasiones. La hiperglicemia es por reducción de producción de insulina por las células pancreáticas y disminución de funcionalidad de los receptores de insulina12,15. La hiperglicemia es un evento que tiene influencia en las etapas de neutropenia y se vera mas con la asociación de glucocorticoides por el efecto sinérgico que tienen. La elevación de glicemia predispondrá a las infecciones, aumentando los porcentajes de mortalidad y al aumentar las suspensiones en las terapias aumentara el riesgo de recaídas15. Se observara hiperglicemias en la fase de inducción por la administración de corticoides y L-ASP12.
El grupo de riesgo para estas elevaciones se vio que son niños mayores de 10 años, pacientes obesos (>20% del peso ideal), pacientes hispanos, mujeres y pacientes con antecedentes personales o familiares de diabetes. Esta complicación remite al detener la L-ASP y los corticoides12. Aun así debe vigilarse debido a que puede producir cetoacidosis o coma hiperosmotico no cetosico. Se debe vigilar esto, con la monitorización de glucosa en sangre y orina. La modificación de la dieta y el aumento de la actividad física ayudaran a la reducción de la glicemia12. El uso de insulina en este evento será en caso de síntomas de diabetes, o la falta de respuesta a la restricción de líquidos y glucosa.
La pancreatitis debida a L-ASP, se la considera cuando hay una elevación mayor a tres veces el valor de lipasa, amilasa, e imágenes a la radiografía de abdomen, tomografía o ultrasonido, asociado a signos y síntomas17. Se reporta entre 1 a 18% de paciente con LLA, con mayor incidencia en pacientes mayores a 10 años y con una media de presentación de 12 días después de la administración para la aparición de este cuadro con la utilización de E. coli16,17. Este evento esta en relación con la administración de prednisona, dexametasona y daunomicina. No hay una relación clara entre la dosis, la duración ni el tipo de L-ASP para la aparición de este evento. Aunque la mayoría de los casos de pancreatitis son leves, un 2% son severos16. Aun así una gran parte de los pacientes vuelve a recibir la L-ASP, por lo menos con una resolución de síntomas de 72 horas16,17.
La hipoalbuminemia es un efecto frecuente de la L-ASP pero tiene una influencia indirecta en la toxicidad vista por los glucocorticoides, al disminuir esta proteína y producir mayor niveles de la dexametasona (unión a proteínas en un 80%) y aumentando también la metabolización de este medicamento, produciendo de esta manera mayor toxicidad y menos efectos anti-leucémicos. Este efecto se observa con mayor intensidad en los pacientes que son de alto riesgo al recibir dosis más altas de L-ASP. Un efecto interesante observado es que los valores normales de albumina en los pacientes con LLA presentan inactivación por anticuerpos18.
Otras reacciones por L-ASP son: la hidrolisis producida por L-ASP que aumenta los niveles a amonio mayor a 80 ug/dl en el primer día y 3 días después de la administración en todos los pacientes, que puede sobrepasar el ciclo de la urea y puede producir anorexia, irritabilidad, letárgia, vómitos, incluso cambios menores en el electroencefalograma, convulsiones, por la elevación que puede llegar a ser siete veces más que el valor normal. Aun así puede observarse elevación del amonio sin aumento ninguna clínica2.
La hipertrigliceridemia (>200 mg/dl) e hipercolesterolemia secundaria a L-ASP por lo general son elevaciones transitorias y se relaciona a la administración de dexametasona más L-ASP, la cual puede remitir rápidamente omitiendo este corticoide. El mecanismo aun no es bien entendido, pero parece deberse a la elevación de síntesis de lipoproteínas de muy baja densidad y disminución de actividad de la lipoproteína lipasa11,13. Aunque esta elevación puede pasar desapercibida por ser mayormente asintomática se presenta en un 33-67 %. Es adecuado vigilar estos valores porque niveles > a 1,000 mg/dl predisponen a la pancreatitis inducida por tri-glicéridos, pero aun así. Esté valor que se reporta en 19 % hay pocos reportes de pancreatitis11, pero se asocia a síntomas neurológicos por aumento de la viscosidad. Otras terapias como la disminución de grasas en la dieta, fibratos, aumentando líquidos endovenosos y plasmaferesis también reducen los niveles de triglicéridos13,14.
Referencias
1. Schrey D, Speitel K, Lanvers-Kaminsky C, Gerss J, Morucke A, Boos J. Five Year Center Study of aspraginase therapy within the ALL-BFM 2000 trial. Pediatric Blood Cancer 2011;57:378-84. [ Links ]
2. Steiner M, Attaraschi A, Kastner U, Dworzak M, Haas OA, Gadner H, Mann G. Distinct fluctuantions of ammonia levels during asparaginasa therapy for childhood acute leukemia. Pediatric Blood Cancer 2007;49:640-2. [ Links ]
3. Merryman R, Stevenson KE, Gostic WJ, Neuberg D, O'Brian J, Sallan SE, et al. Asparaginase associated myelosuppression and effect on dosing of other chemotherapeutic agents in childhood acute lymphoblastic leukemia. Pediatric Blood Cancer 2012;59:925-7. [ Links ]
4. Albertsen BK, HAsle H, Clausen N, Schroder H, Jakobsen P. Pain intensity and bioavailability of intramuscular asparaginasa and local anesthetic: a double blinded study. Pediatric blood cancer 2005;44:255-8. [ Links ]
5. Wang B, Relling MV, Storm MC, Woo MH, Ribeiro R, Pui CH, Hak LJ. Evaluation of immunologic cross reaction of astiasparaginase antibodies in acute lymphoblastic leukemia (ALL) and lymphoma patients. Leukemia 2003;17:1583-8. [ Links ]
6. Eguiguren JM, Pui CH. Bone Marrow necrosis and thrombotic complications in childhood acute lymphoblastic leukemia. Med Pediatr Oncol 1992;20:58-60. [ Links ]
7. Woo MH, Hak LJ, Storm MC, Gajjar AJ, Sandlund JT, Harrison PL, et al. Cerebroespinal fluid asparagine concentrations after Escherichia coli asparaginasa in children with acute lymphoblastic leukemia. J Clin Oncol 1999;17:1568-73. [ Links ]
8. Tong WH, Pieter R, Hop WCJ, Lanvers-Kaminsky C, Boos J, van der Sluis M. No evidence of increased asparagine levels in the bone marrow of patients with acute lymphoblastic leukemia during asparaginasa therapy. Pediatric Blood Cancer 2013;60:258-61. [ Links ]
9. Van den Berg H. Asparaginase revisited. Leukemia & lymphoma 2011;52:168-78. [ Links ]
10. Qureshi A, Mitchell C, Richards S, Vora A, Goulden N. asparaginase related venous thrombosis in UKALL 2003 re-exposure to asparaginasa is feasible and safe. Br. J. Harmatol 2009;149:410-3. [ Links ]
11. Cohen H, Bielorai B, Harats D, Toren A, Pinhas-Hamiel O. Conservative treatment of L-asparaginase-associated lipid abnormalities in children with acute lymphoblastic leukemia. Pediatric Blood Cancer 2010;54:703-6. [ Links ]
12. Baillargeon J, Langevin AM, Mullins J, Ferry R, DeAngulo G, Thomas PJ, et al. Transient hyperglycemia in Hispanic children with acute lymphoblastic leukemia. Pediatric Blood Cancer 2005 ;45:960-3. [ Links ]
13. Tong WH, Pieters R, Van der Sluis IM. Successful management of extreme hypertriglyceridemia in a child with acute lymphoblastic leukemia by temporalily omitting dexamethasone. Pediatric Blood Cancer 2012;58:317-8. [ Links ]
14. Salvador C, Meister B, Crazzolara R, Kropshofer G. Management of hypertriglyceridemia in children with acute lymphoblastic leukemia under persistent therapy with glucocorticoids and L-asparaginase during induction chemotherapy. Pediatric Blood Cancer 2010;59:711. [ Links ]
15. Roberson JR, Raju S, Shelso J, Pui CH, Howard SC. Diabetic ketoacidosis during therapy for pediatric acute lymphoblastic leukemia. Pediatric Blood Cancer 2008 ;50:1207-12. [ Links ]
16. Knoderer HM, Robarge J, Flockhart DA. Predicting Asparaginase associated pancreatitis. Pediatric Blood Cnacer 2007;49:634-9. [ Links ]
17. Kearney SL, Dahlberg SE, Levy DE, Voss SD, Sallan SE, Silverman LB. Clinical course and outome in children with acute lymphoblastic leukemia and asparaginasa-associated pancreatitis. Pediatric Blood Cancer 2009;53:162-7. [ Links ]
18. Yang L, Panatta JC, Cai X, Yang W, Pei D, Cheng C, et al. Asparaginase may influence dexamethasone pharmacokinetics in acute lymphoblastic leukemia. J. Clin. Oncol. 2008;26(12):678. [ Links ]
19. Wani NA, Kosar T, Pala NA, Qureshi UA. Sagittal sinus thrombosis due to L-asparaginase. J Pediatri Neurosci 2010;5:32-5. [ Links ]














