Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista de la Sociedad Boliviana de Pediatría
On-line version ISSN 1024-0675
Rev. bol. ped. vol.51 no.1 La Paz 2012
ACTUALIZACION
Documento de consenso del síndrome de apneas-hipopneas durante el sueño en niños (versión completa)
Consensus document on sleep apnea-hypopnea syndrome in children (full version)
Dr.: María Luz Alonso-Álvarez, Teresa Canet, Magdalena Cubell-Alarco, Eduard Estivill, Enrique Fernández-Julián, David Gozal, María José Jurado-Luque, María Amalia Lluch-Roselló, Francisco Martínez-Pérez, Milagros Merino-Andreu, Gonzalo Pin-Arboledas, Nuria Roure, Francesc X. Sanmartí, Óscar Sans-Capdevila, Francisco Segarra-Isern, Miguel Tomás-Vila y Joaquín Terán-Santos
Artículo reproducido con permiso de los autores y que fue publicado en Archivos de Bronconeumología 2011; 47 (Sup 15): 2-18
a Unidad Multidisciplinar de Sueño, CIBERES, Complejo Asistencial Universitario de Burgos, Burgos, España
b Servicio de Neurofisiología Clínica, Hospital Virgen de los Lirios de Alcoy, Alicante, España
c Psicología, Centro Psicológico MCA, Valencia, España
d Clínica del Son Estivill, USP Institut Universitari Dexeus, Barcelona, España
e Unitat del Son Estivill de Capio, Hospital General de Catalunya, Barcelona, España
f Servicio de Otorrinolaringología, Hospital Universitario, Departamento de Cirugía, Universidad de Valencia, Valencia, España. Presidente de la Comisión de Roncopatía y Trastornos Respiratorios del Sueño de la SEORL
g Department of Pediatrics and Comer Children's Hospital, Pritzker School of Medicine, The University of Chicago, EE.UU.
h Unidad Multidisciplinar de Sueño, Hospital Universitari Vall d'Hebron, Barcelona, España
i Pediatría de Atención Primaria, Centro de Salud Ingeniero Joaquín Benlloch, Valencia, España
j Servicio de Neurofisiología Clínica, Hospital Universitario Puerta de Hierro, Majadahonda, Madrid, España
k Unidad Pediátrica de Trastornos del Sueño, Hospital Universitario La Paz, Madrid, España
l Unidad Valenciana del Sueño, Hospital Quirón, Valencia, España
m Unidad de Epilepsia y Sueño Pediátrica, Neuropediatría, Hospital Universitari Sant Joan de Déu, Barcelona, España
n Neuropediatría, Hospital Universitari i Politècnic La Fe, Valencia, España
Avalado por:
Sociedad Española de Neumología y Cirugía Torácica (SEPAR)
Sociedad Española de Sueño (SES)
Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP)
Asociación Española de Pediatría de Atención Primaria (AEPap)
Sociedad Española de Otorrinolaringología (SEORL)
Definición, epidemiología, fisiopatología
El síndrome de apneas-hipopneas del sueño (SAHS) en la infancia es un trastorno respiratorio del sueño, caracterizado por una obstrucción parcial prolongada de la vía aérea superior y/u obstrucción intermitente completa que interrumpe la ventilación normal durante el sueño y los patrones normales del mismo. Se asocia habitualmente con síntomas que incluyen el ronquido y trastornos del sueño1. El SAHS infantil tiene una entidad clara con perfiles muy diferenciados con respecto al del adulto en lo referente a etiología, presentación clínica y tratamiento. Es por este motivo que la Academia Americana de Medicina del Sueño separa de forma clara ambas entidades y las incluye en apartados diferentes en su clasificación2.
El SAHS es una patología altamente prevalente en la edad infantil, que afecta entre un 2 y un 4% de niños con edades comprendidas entre los 2 y los 6 años 1. Respecto al ronquido, las cifras alcanzan del 7 al 16,7% de 6 meses a 13 años y del 5 al 14,8% en adolescentes3,4.
Para entender la fisiopatología del SAHS hay que tener presente que durante la inspiración se produce una presión negativa que favorece el colapso de los tejidos hacia el interior que se contrarresta por la acción de los músculos dilatadores de la faringe. Existen factores predisponentes en la infancia que alteran esta función de la musculatura faríngea, tanto anatómicos, que provocan un aumento de la resistencia de la vía aérea, como neurológicos, que impiden el funcionamiento normal de los músculos dilatadores. La hipertrofia amigdalar y adenoidea, las malformaciones craneofaciales, la obesidad, las enfermedades neurológicas como la parálisis cerebral infantil, las enfermedades neuromusculares, el reflujo gastroesofágico y la obesidad son algunos de los factores de riesgo que con mayor frecuencia se presentan en la infancia.
Así, se entiende que el SAHS es un cuadro comórbido de diferentes trastornos crónicos en la infancia, algunos de ellos muy prevalentes. Solo por citar un ejemplo, entre un 30 y un 45% de niños con síndrome de Down pueden presentar SAHS5, un 27% de niños con discapacidad psíquica cumple criterios para ser evaluados formalmente en busca de SAHS6 y hasta un 50% de los niños remitidos para valoración por sospecha de SAHS presenta obesidad7.
Las repercusiones médicas del SAHS incluyen alteraciones cardiovasculares, como alteraciones en la función ventricular y elevaciones discretas de la presión arterial, además del retraso pondoestatural. Desde el punto de vista neuroconductual está plenamente demostrado que pueden presentar problemas de aprendizaje, con disminución del rendimiento escolar, labilidad emocional, fenotipos conductuales que se han venido en denominar trastorno de déficit de atención con hiperactividad-like y, en definitiva, situaciones que afectan a la calidad de vida del niño y de su familia8.
Podemos decir por tanto que el SAHS constituye un problema preferente de salud pública infantil por varios motivos. En primer lugar, por la elevada prevalencia del trastorno. En segundo lugar, porque se comporta como trastorno comórbido de diferentes procesos crónicos. En tercer lugar, porque su existencia empeora el curso de diferentes entidades a las que se asocia. Por ejemplo, hay trabajos que demuestran que la presencia de SAHS en niños epilépticos puede influir en la refractariedad al tratamiento de dicha epilepsia9. Por último, los trastornos del sueño en general y el SAHS en particular influyen de forma clara en la calidad de vida del niño y también en la de sus cuidadores en el caso de los niños con discapacidad.
El conocimiento del SAHS en la infancia ha estado muy limitado hasta hace relativamente poco tiempo. Desde hace unos años ha habido un esfuerzo considerable por parte de diferentes colectivos científicos en la difusión de conocimientos en torno de esta entidad. Habitualmente, el pediatra de atención primaria es el objetivo al que van dirigidas las guías clínicas publicadas, pero no debemos olvidar que el manejo diagnóstico y terapéutico del SAHS es claramente multidisciplinar. Diferentes especialistas (pediatras, otorrinolaringólogos, neumólogos, neurofisiólogos) están implicados en el proceso asistencial de los niños afectados de trastornos respiratorios relacionados con el sueño.
Comorbilidad del síndrome de apneas-hipopneas del sueño.
Consecuencias cardiovasculares del SAHS en la población pediátrica Estudios epidemiológicos han demostrado que los trastornos respiratorios durante el sueño (TRS) son muy frecuentes en la población pediátrica y, del mismo modo que en los adultos, también están asociados a riesgo cardiovascular10.
Desde hace dos décadas existe un interés creciente por los TRS en la edad pediátrica, justificado por las graves consecuencias que pueden provocar en diferentes sistemas. Por otra parte, el aumento de la prevalencia de la obesidad y el sobrepeso en la población infantil contribuye a un incremento de la incidencia del síndrome de apneashipopneas del sueño (SAHS) en los niños y también, de forma directa e indirecta, del riesgo vascular. La hipoxia intermitente secundaria a cada evento respiratorio y la obstrucción de las vías aéreas superiores provocan una serie de fenómenos que son causantes de las complicaciones cardiovasculares: incremento de la actividad simpática, disfunción endotelial, generación de radicales libre e incremento de la presión de la arteria pulmonar con disfunción cardíaca derecha. A continuación, se detallan todos estos fenómenos.
Disfunción autonómica
La función autonómica se manifiesta a diferentes niveles:
1. Tono arterial: la hipoxia intermitente provocada por las apneas e hipopneas se acompaña de cambios significativos de la presión intratorácica y de una alteración de la función autonómica, consistente en un incremento de la respuesta adrenérgica y del tono basal simpático, y de una disminución del tono y actividad vagales. En adultos con SAHS existe una elevación de la concentración basal de norepinefrina y catecolaminas urinarias y este fenómeno también se ha objetivado en los niños, en los cuales se ha relacionado su concentración con la gravedad del SAHS11. Por otra parte, la activación simpática que existe en estos pacientes, y de forma independiente a su edad, provoca cambios en el tono arterial, que se han objetivado con pruebas no invasivas como la velocidad de la onda de pulso, la tonometría de pulso arterial (pulse arterial tonometry) y el tiempo de tránsito de pulso (pulse transit time o PTT en inglés), que analizamos a continuación12,13:
- Velocidad de la onda de pulso: este parámetro, predictor del riesgo vascular, mide el tiempo que tarda una pulsación en recorrer una cierta distancia. La velocidad de la onda de pulso depende de la distensibilidad arterial y en el SAHS disminuye la distensibilidad y aumenta la velocidad de la onda de pulso.
- Tonometría de pulso arterial: estímulos térmicos o respiratorios incrementan el tono arterial aunque, en niños con SAHS, se ha observado que este fenómeno está muy exagerado como respuesta a un incremento del tono simpático.
- PTT: el PTT es el intervalo que tarda un pulso generado en el corazón hasta su llegada a territorios periféricos y también depende de la distensibilidad o rigidez de la pared arterial. El PTT es un marcador directo del arousal secundario a los eventos respiratorios obstructivos porque cada apnea-hipopnea se acompaña de un incremento de la presión arterial.
2. Frecuencia cardíaca: el control autonómico de la función cardíaca determina la frecuencia del latido y su variación en condiciones de reposo o como respuesta a diferentes estímulos de tal forma que este parámetro (la variabilidad de la frecuencia cardíaca) permite evaluar cuantitativamente la función del sistema nervioso autónomo y del control cardiovascular latido a latido. Se ha demostrado que, en niños con SAHS, existe un predominio simpático con incremento del tono adrenérgico y disminución de la actividad vagal que provoca un aumento y una variabilidad de la frecuencia cardíaca14,15.
3. Presión arterial sistémica: las alteraciones de la función autonómica parecen ser la causa principal del incremento del tono arterial y, consecuentemente, de la aparición de hipertensión arterial (HTA) en los niños con SAHS. La relación entre ambos trastornos es conocida desde hace décadas, pero los primeros estudios solo incluían a niños con HTA definida con los mismos criterios que en adultos (presión arterial sistólica superior a 140 mmHg y/o presión arterial diastólica superior a 80 mmHg).
Solo desde 1998 se están considerando las cifras en función de la edad y el peso pero, en todo caso, se ha observado que existen diferencias significativas entre los grupos control y los niños con TRS, quienes presentan cifras de presión arterial (PA) más elevadas con una relación directa entre los valores de la PA y el índice de apneas-hipopneas16.
Los registros ambulatorios de la PA realizados en niños con un TRS han permitido objetivar otros fenómenos como las variaciones de la PA diastólica, la ausencia de la caída nocturna de la PA (nocturnal dipping) y el marcado incremento de la PA matutina17.
No debemos olvidar la coexistencia de obesidad/sobrepeso, HTA sistémica y SAHS, cuya prevalencia se incrementa de forma paralela en la población infantil. En niños con SAHS se obtienen cifras de PA significativamente superiores en los pacientes obesos respecto de aquellos en los que el índice de masa corporal se encuentra dentro de límites normales18.
Como ya hemos visto, existe una disfunción autonómica provocada por el SAHS en la población pediátrica aunque en la actualidad se desconocen sus consecuencias a largo plazo. Probablemente, la hipoxia intermitente provoque una disregulación autonómica con reducción mantenida del tono vagal, incluso en ausencia del estímulo.
Cambios en la función y en la pared ventricular
El incremento de la PA es un factor conocido de modificación de la pared ventricular que se manifiesta con hipertrofia, aumento de grosor de la pared interventricular, reducción de la fracción de eyección en ambos ventrículos y alteración del diámetro de la aurícula izquierda. La presencia de SAHS no solo contribuye a exagerar estos fenómenos, sino que también es capaz, por sí sola, de inducir una remodelación cardíaca y disfunción ventricular en adultos.
En niños con SAHS también se han observado estos cambios y los signos de disfunción cardíaca podrían detectarse incluso antes de que aparezcan manifestaciones clínicas. Cuando se comparan niños sanos, niños con ronquido habitual sin apneas y niños con SAHS, se encuentran diferencias significativas en estos parámetros y la intervención quirúrgica (adenoamigdalectomía) resuelve o minimiza las anomalías de la pared ventricular. Sin embargo, a pesar de que existe una disfunción de la contractilidad cardíaca en pacientes pediátricos con SAHS, no se ha descrito una mayor incidencia de fallo cardíaco19,20.
Cor pulmonale
En el SAHS, los episodios repetidos de hipoxia e hipercapnia secundarios a los eventos respiratorios durante el sueño, provocan incremento de la resistencia vascular en la arteria pulmonar e hipertensión pulmonar que se resuelve, en pacientes adultos, tras instaurar tratamiento con CPAP21. En los niños, aunque el cor pulmonale puede ser la primera manifestación del SAHS, esta complicación es menos frecuente.
Daño endotelial: inflamación sistémica y aterogénesis La relación entre daño endotelial y complicaciones cardiovasculares graves es conocida desde hace años pero, recientemente, también se ha implicado al SAHS en esta asociación22 y se ha visto que su tratamiento puede revertir estas lesiones. Los mecanismos que pueden estar implicados en la afectación vascular endotelial son14,22-24:
1. Cambios en la producción de sustancias vasoactivas (incremento de endotelina, reducción del óxido nítrico) en respuesta a la hipoxemia intermitente, que provocan vasoconstricción e HTA.
2. Incremento de mediadores de adherencia inflamatorios, que inducen un estado de hipercoagulabilidad.
3. Activación simpática con daño endotelial directo.
4. Susceptibilidad genética, que podría ser un factor determinante en el caso de los niños con antecedentes familiares de enfermedad cardiovascular.
En adultos y en la población pediátrica existen claras evidencias de la asociación entre el SAHS y la aterosclerosis, en la que existe participación de fenómenos inflamatorios sistémicos22,23. Por otra parte, se piensa que el estrés oxidativo secundario a la hipoxia intermitente y a los arousals o microdespertares que ocurren durante el sueño puede conducir a una activación de los linfocitos T, probablemente de forma similar al fenómeno objetivado en la aterogénesis24. En adultos y niños conTRS, como respuesta a una activación de la respuesta inflamatoria y de la aterogénesis, existe una mayor expresión de moléculas de adhesión en monocitos circulantes25. Por otra parte, la expresión de interleucina (IL) 1 y 6 y del factor de necrosis tumoral alfa (TNF-α) está relacionada con la presencia de SAHS y también con la gravedad del trastorno, que mejora tras la instauración del tratamiento26,27. Aunque en los niños los resultados son contradictorios, se ha descrito una elevación de la concentración plasmática matutina de TNF-α relacionada con la fragmentación del sueño provocada por los eventos respiratorios28.
La proteína C reactiva (PCR) es, al mismo tiempo, un marcador de inflamación sistémica y un factor de aterosclerosis. La PCR puede incrementarse en los niños con SAHS y, aunque también existen resultados contradictorios respecto a este hecho, sí se ha objetivado una reducción de la PCR tras adeno-amigdalectomía29.
Por último, no debemos olvidar la relación entre el SAHS y los estados de hipercoagulabilidad. Se sabe que la p-selectina es un marcador de activación plaquetaria y su incremento en adultos con SAHS contribuye a la formación de placas de aterosclerosis y de trombos. Aunque en niños con SAHS existen menos datos, se ha observado que existe un incremento del fibrinógeno matutino30 (fig. 1).
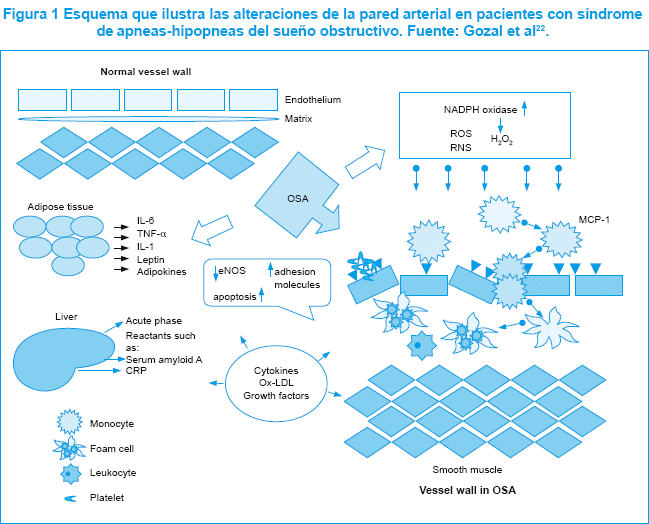
El SAHS induce un mecanismo oxidativo mediante la activación de la NADPH-oxidasa y la formación de peróxido de hidrógeno (H2O2). Además, el SAHS incrementa la liberación de citocinas (IL-1, IL-6 y TNF-α). En el hígado se incrementa la formación de reactantes de fase aguda y PCR. Los monocitos circulantes inducen la expresión de moléculas de adhesión en la superficie endotelial, disminuyen la actividad de la sintetasa endotelial del óxido nítrico y se activa la apoptosis en la superficie endotelial. A su vez, estas células endoteliales activan la formación de trombos.
Conclusión
El SAHS en la población pediátrica está asociado a una importante morbilidad que afecta, fundamentalmente, al sistema nervioso central y al sistema cardiovascular, con disfunción autonómica con arritmias cardíacas e HTA, remodelación de la pared ventricular y afectación endotelial. La magnitud del daño de los órganos diana está determinada, fundamentalmente, por la gravedad del SAHS y es posible que este trastorno, iniciado en la etapa infantil, sea el detonante de una cascada de eventos que determinen un inicio más precoz de algunos fenómenos que normalmente aparecerían en la edad adulta. El reconocimiento temprano de la existencia de un SAHS evitaría estas consecuencias y la eventual mortalidad en algunos casos.
Complicaciones endocrinometabólicas del síndrome de apneashipopneas durante el sueño en la edad pediátrica
El síndrome de apneas-hipopneas durante el sueño (SAHS) infantil se ha convertido no solo en una entidad relativamente prevalente, sino también en una enfermedad asociada a múltiples comorbilidades que pueden alcanzar implicaciones hasta la edad adulta.
Los mecanismos fisiopatológicos subyacentes del daño sobre los órganos diana empiezan a ser dilucidados, e implican vías inflamatorias y oxidativas.
Los niños han representado clásicamente un buen modelo clínico para estudiar la relación entre los trastornos respiratorios durante el sueño y el metabolismo glucídico, con una limitada comorbilidad coexistente31.
Sin embargo, la susceptibilidad individual, así como las condiciones ambientales y el estilo de vida (actividad física e intelectual, dieta), desempeñan un importante papel en la variabilidad fenotípica. Precisamente por este motivo y por los cambios comportamentales y dietéticos de la población infantil durante las dos últimas décadas en las que ha aumentado el porcentaje de obesidad y el sedentarismo, el fenotipo clásico considerado hasta hace relativamente pocos años está siendo progresivamente sustituido por un patrón similar al que encontramos en la edad adulta, hasta el punto de proponerse la creación de dos tipos32, tal y como se realizó en su momento con la diabetes mellitus: el primero de ellos, asociado a hipertrofia linfoadenoidea en ausencia de obesidad (tipo I), y otro asociado fundamentalmente a obesidad y con menor hiperplasia amigdalar (tipo II), discutiéndose la creación de un tercer tipo que incluiría a niños afectados de malformaciones craneofaciales o alteraciones neuromusculares.
Retraso del crecimiento
A pesar de que este problema presentaba una incidencia desproporcionadamente alta en los primeros casos descritos, hoy en día se considera que menos del 5% de los pacientes con SAHS presenta retraso ponderoestatura33. De estos, incluso aquellos con obesidad presentan ganancia ponderal al ser tratados34.
Se han propuesto diversos mecanismos para explicar las alteraciones del crecimiento en el SAHS, entre los que se encuentran la disminución de niveles de factor de crecimiento insulínico tipo 1, sus proteínas de unión e incluso la liberación de hormona del crecimiento35.
Síndrome metabólico
El término "síndrome metabólico" se ha empleado para describir la conjunción de resistencia insulínica, dislipemia, hipertensión y obesidad en la que se encuentra implicado el tejido adiposo disfuncionante, no habiéndose definido aún unos criterios de consenso de dicha entidad en la edad pediátrica36. Sin embargo, el riesgo de presentarlo se encuentra próximo al 50% en niños obesos, porcentaje que aumenta proporcionalmente al índice de masa corporal. Este y los niveles elevados de insulina en ayunas durante la infancia han demostrado ser los mayores factores predictores de desarrollar un síndrome metabólico en la edad adulta37.
El papel etiológico de los trastornos respiratorios durante el sueño sobre el metabolismo infantojuvenil sigue sin conocerse con seguridad38.
Mientras que en adultos, tanto la obesidad como el SAHS han sido identificados como importantes factores de riesgo de padecer síndrome metabólico, en la población infantil parece encontrarse determinado por el grado de obesidad (relacionado con la resistencia insulínica) y la dislipemia (con elevación de los niveles plasmáticos de triglicéridos y reducción de los niveles en plasma de las lipoproteínas de alta densidad), mientras que el SAHS no parece contribuir de forma tan significativa39. Sin embargo, aunque no parece inducir resistencia insulínica en pacientes pediátricos no obesos, sí puede desempeñar un papel predominante en caso de obesidad.
En la población general, existe una asociación entre los trastornos respiratorios durante el sueño y la existencia de síndrome metabólico.
Algunos estudios40 han encontrado un incremento de 6,49 veces la probabilidad de desarrollar un síndrome metabólico en relación con los niños que no presentan trastornos respiratorios durante el sueño. En la muestra, el 25% de los niños presentaba sobrepeso y un 19% había desarrollado un síndrome metabólico.
En muestras clínicas de niños obesos41, se ha encontrado una correlación entre los trastornos respiratorios durante el sueño y los niveles de insulinemia en ayunas, independientemente del índice de masa corporal, en los cuales la resistencia insulínica y la dislipemia parecen encontrarse determinadas fundamentalmente por el grado de adiposidad corporal, más que por la gravedad del trastorno respiratorio durante el sueño42. De hecho, en niños no obesos con SAHS el grado de severidad de este no ha demostrado ser un predictor significativo de la resistencia insulínica o de los valores del índice HOMA43.
Uno de los temas emergentes es el aumento de la producción y liberación, por parte del tejido adiposo, de adipoquinas pro y antiinflamatorias, sustancias que están implicadas en muchas de las manifestaciones clínicas de esta patología, como la diabetes44, hipertensión arterial o enfermedad cardiovascular25,45, y cuyo principal factor determinante de un incremento de los niveles de las mismas sería la obesidad.
En una primera etapa, el tejido adiposo se vuelve resistente a la acción de la insulina debido a la acción de alguna de estas adipoquinas, como el factor de necrosis tumoral alfa (TNF-α), las interleucinas 1 y 6 (IL-1, IL-6), la leptina o la resistina.
En una segunda etapa aparece dicha resistencia en otros tejidos y se produce un aumento tanto en los niveles de glucosa como de insulina.
Dicho aumento, junto con los altos niveles de adipoquinas que se producen, conduce a la aparición de diferentes efectos adversos, entre los que se encuentran un aumento del estrés oxidativo, disfunción endotelial, aumento de la presión arterial y alteraciones del metabolismo lipoproteico, todos ellos con efectos adversos en la salud.
Entre la multitud de adipoquinas existentes destaca la leptina, que desempeña un importante papel en la regulación del apetito, el sueño, la homeostasis metabólica e incluso el control respiratorio. A diferencia de los pacientes adultos, la elevación de los niveles de leptina circulante no se ha correlacionado con el grado de obesidad de los pacientes pediátricos con SAHS, sino que parece estar relacionada con la alteración respiratoria y la hipoxemia asociada46. El comportamiento de otras adipoquinas estudiadas, como la adiponectina (cuyos niveles se encuentran reducidos en niños obesos, presenten o no SAHS), requiere nuevos estudios para determinar su implicación47.
Así, se podría concluir que el SAHS puede provocar alteraciones significativas de la homeostasis lipídica y de la inflamación sistémica; la presencia de obesidad concomitante es la causa de una alteración de la regulación glucémica secundaria a cambios en la sensibilidad a la insulina, independientemente del índice de masa corporal48.
Entre la obesidad y la apnea parece crearse un "círculo vicioso" en el que ambas se favorecen mutuamente: la obesidad aumenta la apnea del sueño y esta provoca somnolencia y reduce la actividad del niño, por lo que se favorece el aumento de peso.
De forma similar a lo que sucede en la edad adulta, la coexistencia de obesidad y SAHS aumenta considerablemente el riesgo de presentar alteraciones metabólicas40, así como esteatosis hepática no alcohólica49, lo que constituye un factor predictivo independiente para la diabetes tipo 2 y se asocia a dislipemia.
El síndrome metabólico es más frecuente entre adolescentes que a edades más tempranas y afecta fundamentalmente a varones con sobrepeso, de forma similar a lo que sucede en la edad adulta. Se ha correlacionado con mayores índices de apnea-hipopnea, desaturaciones más severas y una menor eficiencia del sueño que en los niños que no presentan dicho síndrome50. En cambio, no se han encontrado diferencias significativas en el índice de alertamientos corticales (arousals), el porcentaje de sueño de ondas lentas, el tiempo total de sueño medio o en la roncopatía habitual.
Efectos del tratamiento
Hasta el momento se han reunido pocos datos acerca de los efectos del tratamiento del SAHS en las alteraciones metabólicas en la población infantil.
La adenoamigdalectomía en ambos grupos, obesos y no obesos, se ha acompañado de una mejoría significativa del perfil lipídico, la proteína C reactiva y la apolipoproteína B, lo que estaría apoyando el mecanismo patogénico del SAHS en la homeostasis lipídica y las vías inflamatorias sistémicas, independientemente del grado de adiposidad. Se han descrito leves mejorías de las cifras de las lipoproteínas de alta densidad plasmáticas en niños adenoamigdalectomizados, sin cambios significativos en los niveles de insulina.
El aumento de los niveles de leptina y de los marcadores de actividad nerviosa simpática observados en pacientes con SAHS en relación con los de roncadores simples mostraba un descenso tras el tratamiento con presión positiva continua en la vía respiratoria durante 3 meses50. Sin embargo, no se ha demostrado ningún efecto del tratamiento sobre la resistencia insulínica, los niveles de insulinemia o los valores del índice HOMA51.
A pesar del creciente desarrollo de la investigación en este campo, se hace evidente la necesidad de un mayor conocimiento de las interacciones entre los trastornos respiratorios durante el sueño y sus consecuencias metabólicas con la obesidad52-54
Conclusión
Aunque no se ha establecido una relación clara entre niños no obesos con SAHS y alteraciones metabólicas, parece claro que la presencia de SAHS en un niño obeso pueda amplificar sus alteraciones metabólicas, y que la interrelación entre SAHS y obesidad es más compleja que simplemente su suma. La asociación demostrada entre el síndrome metabólico, el sobrepeso y las alteraciones ventilatorias durante el sueño sugiere la necesidad de realizar estudios de cribado en aquellos niños en los que se detecta una de las tres entidades.
Trastornos neurocognitivos, conductuales, depresivos y excesiva somnolencia diurna del síndrome de apneas-hipopneas durante el sueño en la edad pediátrica
Las alteraciones conductuales y neurocognitivas, junto con los síntomas depresivos y la somnolencia excesiva diurna en la niñez, pueden deberse a un trastorno respiratorio durante el sueño (TRS).
Trastornos neurocognitivos: inatención, hiperactividad, bajo rendimiento escolar
La odds ratio (OR) para las alteraciones neuroconductuales en niños roncadores es de 2,93 (intervalo de confianza del 95%)55.
Se ha sugerido que la comorbilidad entre el trastorno de déficit de atención con hiperactividad (TDAH) y problemas respiratorios durante el sueño es alta (23 %)56. El mecanismo por el cual el problema respiratorio puede contribuir al déficit de atención es desconocido.
En los niños con problemas respiratorios durante el sueño se triplica la frecuencia de alteraciones de la conducta y problemas de atención57.
En los niños que presentan hiperactividad y que no reúnen los criterios diagnósticos del TDAH, la Academia Americana de Pediatría recomienda, tras una exhaustiva evaluación, la realización de una cuidadosa historia de sueño y, si presentan ronquido, la realización de un estudio nocturno de sueño1.
El rendimiento escolar resulta afectado en los niños con TRS58. Los niños con bajo rendimiento académico tienen más probabilidades de haber roncado durante la niñez temprana y de requerir una adeno-amigdalectomía por el ronquido, en comparación con sus compañeros con rendimiento escolar superior, de manera que la morbilidad neurocognitiva asociada a los TRS puede ser solo parcialmente reversible, esto es, puede desarrollarse una "deuda de aprendizaje" en estos trastornos ocurridos durante la niñez temprana y perjudicar el rendimiento escolar posterior59.
El papel desempeñado por la susceptibilidad interindividual, junto con las condiciones ambientales y la forma de vida, puede explicar gran parte de la variación en el fenotipo. Hay que tener en cuenta que el fenotipo del SAHS pediátrico ha cambiado; hemos ido del paciente que presenta hipertrofia amigdalar sin obesidad asociada al prototipo de un paciente con una hipertrofia amigdalar leve o moderada, y con un biotipo obeso que es muy similar al del paciente adulto. Por esta razón, se propone el uso de los términos tipo I y el tipo II en SAHS en niños, para tener en cuenta las diferencias clínicas y las manifestaciones de la patología60.
Asimismo, se ha observado que casi la mitad de los niños con SAHS (47%) ha tenido problemas conductuales61, aumentando la correlación si se añade al SAHS otro trastorno del sueño. Sin embargo, hay que tener en cuenta que otros factores, como la obesidad, la falta de horas de sueño y tener otros trastornos del sueño asociados, también determinan el comportamiento de estos niños56.
Un metaanálisis que analizó 61 estudios62 puso en evidencia la correlación entre trastorno respiratorio en niños y déficits en el comportamiento, la regulación emocional, el comportamiento escolar, la atención selectiva, la atención sostenida y el mantenimiento de alerta. Hay también evidencia de que el trastorno respiratorio tiene una mínima asociación con el humor, la expresión lingüística, la percepción visual y la memoria de trabajo. Los resultados han sido escasos para extraer conclusiones sobre la inteligencia, la memoria y algunos aspectos de la función ejecutiva.
Posteriormente a este metaanálisis, se realizó un estudio prospectivo de casos y controles con 20 niños en cada grupo de entre 3 y 12 años, que valoraba otros aspectos neurocognitivos y conductuales. Se aplicó un cuestionario a los padres preguntando sobre el sueño de los niños, problemas respiratorios, alteraciones de conducta y neurocognitivas. Se realizó una polisom-nografía nocturna completa, batería de pruebas psicológicas validadas y exploración otorrinolaringológica. Los resultados muestran que en el 75% de los casos los parámetros de atención, memoria, estructuración espacial y ansiedad están afectados. La atención directa está alterada en el 45,5% de los niños, la hiperactividad en el 30,8% de los casos y el déficit de atención en el 53,8%. La comparación entre casos y grupo control mostraba una diferencia estadísticamente significativa en atención, memoria y estructuración espacial. Todos los parámetros están más alterados si se miden con las pruebas psicológicas que por la valoración (cuestionario) de los padres63.
Otro metaanálisis de 55 estudios64 alertó del impacto negativo de la hipoxia crónica o intermitente en el desarrollo, el comportamiento y el rendimiento escolar. Deben tenerse en cuenta todas las situaciones que puedan exponer a los niños a la hipoxia, ya que los efectos nocivos se han observado incluso cuando las desaturaciones son pequeñas.
Síntomas depresivos: irritabilidad, fatiga, ánimo depresivo y falta de interés por las actividades diarias
Algunos autores65 han demostrado que los niños que eran roncadores, sin importar la severidad del índice de apneas-hipopneas (IAH) o la presencia de obesidad, tenían peor calidad de vida y más síntomas depresivos que los niños que no eran roncadores. La mala calidad del sueño debida al SAHS podía traducirse en fatiga durante el día con mayores problemas de concentración, irritabilidad, humor depresivo y disminución del interés por las actividades diarias. Estos síntomas diurnos pueden ocasionar dificultades en otros aspectos de la vida del niño, como la relación con la familia y sus compañeros, o la participación en actividades físicas y deportivas.
Los niños que son evaluados por problemas conductuales o afectivos frecuentemente presentan somnolencia diurna. La etiología de esta somnolencia es diversa pero incluye una higiene de sueño inadecuada, SAHS y trastorno del retraso de fase, entre otros66.
Según los resultados de la escala el Child Behavior Checklist, los niños roncadores (el 22 frente al 11%) presentan más síntomas de internalización, especialmente síntomas ansioso-depresivos, y mayor reactividad emocional que los no roncadores, mientras que no se encuentran diferencias significativas en la escala de síntomas de externalización. En las pruebas que miden atención auditiva y conocimiento lingüístico (CI verbal), los roncadores contestaron peor que los no roncadores67. Cuando en estos niños se trata adecuadamente el SAHS, mejora su calidad de vida68.
Excesiva somnolencia diurna
En 1995 un estudio que evaluó a niños con SAHS, observó que solo un 7% de esos niños presentaba síntomas compatibles con excesiva somnolencia diurna (ESD)28.
Los niveles del factor de necrosis tumoral alfa (TNF-α) (citocina inflamatoria implicada en la ESD) están aumentados en los niños con SAHS, particularmente en los casos más severos, y se correlacionan principalmente con el IAH, con la fragmentación del sueño y el índice de masa corporal. Además, el tratamiento quirúrgico del SAHS causa reducciones significativas de los niveles TNF-α con prolongaciones recíprocas en la latencia de sueño28.
En algunos estudios se observa un acortamiento de la latencia de sueño en los niños con SAHS, pero es infrecuente la ESD, que tiende a desarrollarse en los casos más intensos o en los pacientes obesos69.
La probabilidad de ESD en los niños obsesos (SAHS tipo II) es mayor que para los no obesos (SAHS tipo I), sea cual sea el nivel de severidad del SAHS70,71.
En otros estudios, sin embargo, sí hay más síntomas diurnos de ESD, como dificultad para despertarse, cansancio matutino o somnolencia diurna (OR = 6,3), o mayor probabilidad de quedarse dormidos mientras miraban la televisión (OR = 1,8) y en lugares públicos (OR = 2,1), en roncadores que en no roncadores72.
Conclusión
Si bien mediante una encuesta clínica es difícil detectar la presencia de ESD en el niño con TRS, sí son frecuentes las alteraciones de conducta (irritabilidad, agresividad), neurocognitivas (memoria, inteligencia general, funciones ejecutivas, etc.) y del estado de ánimo.
Diagnóstico del síndrome de apneas-hipopneas durante el sueño en edad pediátrica
Las evidencias sobre las consecuencias clínicas del síndrome de apneas-hipopneas durante el sueño (SAHS) pediátrico (morbilidad cardiovascular, neurocognitiva, alteración del medro, etc.)73-78 cada vez son más abrumadoras, de manera que, actualmente, la actitud expectante y conservadora frente a los trastornos respiratorios del sueño (TRS) en la infancia no está justificada; su prevalencia y sus consecuencias en la calidad de vida del niño y su entorno obligan a un diagnóstico y tratamiento temprano.
Por otro lado, la situación actual de presión asistencial debería condicionar los objetivos a corto plazo en cuanto al diagnóstico del SAHS pediátrico; estos deberían ser, entre otros, incrementar el poder de sospecha diagnóstica en asistencia primaria (AP), facilitando métodos de cribado y aproximación diagnóstica al alcance de la mayoría de la población, coordinando y racionalizando todos los medios disponibles de manera que permitieran identificar de forma eficiente el mayor porcentaje posible de población de riesgo que debería ser objeto de especial control y seguimiento tanto en AP como en las unidades de sueño.
Todo ello, con el reconocimiento de que la prueba de referencia para el diagnóstico del SAHS es la polisomnografía (PSG) nocturna1,55,79,80 pero, al mismo tiempo, siendo conscientes de que parece evidente que en nuestro medio es impracticable realizar una PSG nocturna al 2-3% de la población infantil.
Por esta razón, existe un interés creciente en el perfeccionamiento de técnicas o test de cribado, así como en el desarrollo de herramientas más simples que permitan alcanzar resultados diagnósticos fidedignos, reservando las técnicas más complejas y/o costosas (PSG, poligrafía respiratoria) para aquellos niños en los que las pruebas simples no aporten un diagnóstico de certeza o para aquellos otros en los que el resultado de las técnicas complejas puede condicionar la terapia (p. ej., ventilación no invasiva frente a tratamiento quirúrgico).
La necesidad de incrementar la eficiencia diagnóstica obliga a potenciar los esfuerzos en el diagnóstico o en la sospecha diagnóstica del SAHS de manera temprana en aras a disminuir los costes adicionales o indirectos de los TRS81:
- Los niños con SAHS son frecuentadores de los servicios sanitarios tanto de AP como hospitalaria. El diagnóstico correcto conlleva un descenso de esta hiperfrecuentación.
- Disminución del uso de servicios paralelos: los niños con SAHS presentan con frecuencia problemas de conducta y aprendizaje que condicionan la necesidad de terapias y evaluaciones cognitivo- conductuales o farmacológicas. El diagnóstico temprano ocasiona una disminución del uso de estos servicios.
- El diagnóstico y tratamiento precoz del SAHS ocasiona una disminución de la comorbilidad asociada (obesidad, alteraciones cardiovasculares, etc.).
Este grupo de trabajo, por motivos de claridad expositiva, propone analizar la metodología diagnóstica del SAHS en dos compartimentos teóricos, el correspondiente a AP y el correspondiente a asistencia hospitalaria. Somos conscientes de que en muchos puntos esta división artificial es superada por la realidad y que ambos estratos no deberían tener solución de continuidad, pues en muchas ocasiones se superponen y complementan.
Pautas diagnósticas en asistencia primaria
Desde el punto de vista clínico la evaluación de un niño con sospecha clínica de SAHS en AP debería incluir la historia clínica y exploración completa, así como unas valoraciones específicas82.
Algunas premisas previas
- El diagnóstico de sospecha de los TRS se debería iniciar desde los primeros controles de salud incluidos en el programa del niño sano. Así, la Academia Americana de Pediatría recomienda que en los controles de salud se investigue el sueño en todos los niños1. Si el niño presenta ronquido y síntomas o hallazgos clínicos sugestivos de SAHS, se iniciará la escalada diagnóstica específica de TRS.
- Es importante reconocer que la exploración clínica rutinaria y la historia clínica de manera aislada, no son métodos suficientes y fiables para el diagnostico del SAHS en un niño roncador. Su poder predictivo positivo es del 55,8%. En general, la evaluación clínica per se tiene una alta sensibilidad pero una baja especificidad, lo que ocasionaría la presencia de muchos falsos positivos. Añadir un cuestionario específico sobre la apnea del sueño incrementa las posibilidades diagnósticas (de un 26% por historia clínica a un 53% usando un cuestionario específico)83.
Algoritmo diagnóstico en asistencia primaria y en la unidad de sueño (figs. 2 y 3)

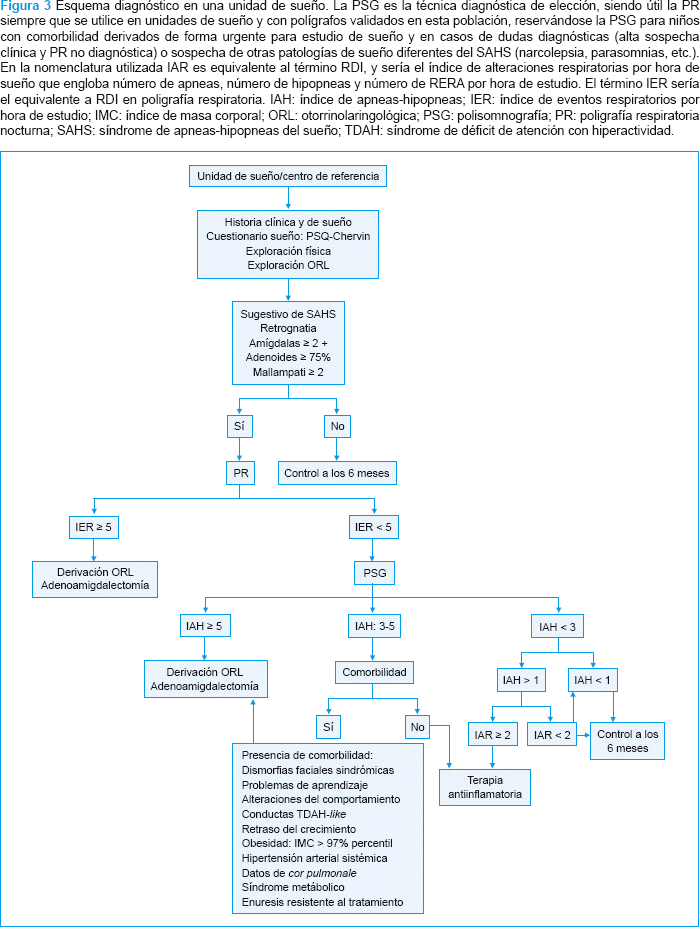
Asistencia primaria
Cribado rutinario en los controles de salud frente a la presencia de trastornos del sueño.
Historia y anamnesis
Importante destacar:
1. Antecedentes familiares: investigar la existencia de otros casos de SAHS en la familia. El SAHS tiene un componente genético evidente. Asimismo, valorar situaciones medioambientales o socioeconómicas desfavorables (p. ej., hábito tabáquico familiar)84.
2. Eventos relacionados con el sueño y la respiración del niño: investigar la posición habitual durante el sueño: el cuello hiperextendido, posición prona con las rodillas debajo del tórax, posición semisentado o necesitando varias almohadas. Se trata de posiciones inconscientes que realiza el niño durante el sueño buscando una mejor ventilación. Algunos síntomas incrementan la probabilidad de que un niño que ronca presente SAHS85,86:
- La observación familiar de apnea (odds ratio [OR] = 3,3).
- Respiración bucal diurna frecuente (OR = 3,7).
- Preocupación paterna sobre la respiración del niño (OR = 4,4).
- Dificultad respiratoria durante el sueño (OR = 5,4).
- Despertares frecuentes durante el sueño en un niño que previamente dormía bien.
- Aparición de cambios escolares o conductuales.
- Presencia de enuresis secundaria.
3. La excesiva somnolencia diurna no es predictiva de la presencia de SAHS en los niños pequeños87.
4. Incluir en la historia el test PSQ de Chervin para TRS. Consta de 22 preguntas orientadas a los TRS. Es el referente en la sospecha de SAHS para niños entre 2 y 18 años de edad, según se acordó en el Consenso Nacional del Síndrome de Apnea del Sueño. Su línea de corte del 33% tiene una sensibilidad del 0,85 y una especificidad del 0,87. Ha sido traducido y validado en lengua española88,89.
Exploración clínica
Valorar especialmente:
1. La anatomía craneofacial y de vías respiratorias altas: evaluar la presencia de respiración bucal no coincidente con procesos catarrales y la presencia de hipertrofia adenoamigdalar así como la anatomía craneofacial (hipertrofia adenoamigdalar, retrognatia, Mallampati)90-93.
Es importante tener en cuenta que el grado de hipertrofia adenoamigdalar no está linealmente correlacionado con la presencia de SAHS: adenoides y amígdalas de pequeño tamaño no la excluyen si los otros síntomas están presentes.
2. Exploración cardiopulmonar: evaluar el posible desplazamiento del impulso máximo, soplo sugestivo de regurgitación tricúspide, observación del trabajo respiratorio, presencia de cianosis, descripción del patrón y frecuencia respiratoria, variabilidad de la frecuencia cardíaca94. En la mayoría de las situaciones estos datos no son significativos.
3. Somatometría y cambios recientes en ella (en ambos sentidos).
Los niños obesos representan un grupo de riesgo especial, incluso tras la adenoamigdalectomía, y requieren un seguimiento diferenciado.
Pruebas complementarias
1. Radiografía lateral de faringe: su utilidad es muy controvertida. La radiografía realizada en vigilia difícilmente predice el grado de obstrucción real y aún menos la obstrucción que se produciría durante el sueño95.
2. Índice de Brouillette96,97: en la mayoría de las ocasiones no es capaz de distinguir entre ronquido habitual con o sin presencia de SAHS, de manera que no constituye una prueba útil para distinguir pacientes roncadores con y sin SAHS.
3. Vídeo domiciliario: la observación del esfuerzo respiratorio nocturno puede aportar muchos datos. Sivan et al 98 desarrollaron una prueba para valorar el vídeo realizado en el hogar durante media hora por los padres en niños de 2 a 6 años de edad y obtuvieron una sensibilidad y una especificad del 89 y el 77%, respectivamente. Su punto de corte predice el 55% de los casos de TRS. Para que el vídeo reúna las condiciones idóneas debemos solicitar a los padres:
- Una duración de media hora, buscar posición decúbito supino, interesan mucho los movimientos del tórax: sin ropa (ni de cama ni pijama) de cintura para arriba, correcto funcionamiento del audio (dada la importancia de los ruidos respiratorios); el mejor momento de la grabación: de 5 a 5 h 30 min (mayor porcentaje de sueño REM) o cuando los padres observen que los ruidos respiratorios son más intensos.
Indicaciones de derivación a una unidad de sueño y/o otorrinolaringológica ante sospecha de TRS/ SAHS según las disponibilidades de nuestro medio y la certeza diagnóstica:
- Según clínica, exploración y pruebas complementarias descritas previamente: si la prueba de Chervin y/o el vídeo domiciliario confirman la sospecha de presencia de TRS/SAHS.
- Según criterios diagnósticos mostrados en la figura 2.
Criterios diagnósticos
Consideraremos la presencia de criterios mayores y criterios menores para el establecimiento de una estrategia diagnóstico-terapéutica:
Criterios mayores:
- Problemas de aprendizaje.
- Se duerme en clase (> 1 vez/semana).
- Conductas de síndrome de déficit de atención con hiperactividad-like.
- Presión arterial > percentil (PC) 85 para la talla.
- Enuresis resistente al tratamiento.
- Índice de masa corporal > PC 97% para la edad.
- Índice de Mallampati > 2 + hipertrofia adenoidea.
Criterios menores:
- Hipercolesterolemia para la edad.
- Otitis medias recurrentes y/o infecciones de vías altas recurrentes.
- Asma/rinitis alérgica.
- Historia familiar (1 progenitor o 3 familiares cercanos).
- Historia de prematuridad.
Cuando un niño roncador habitual presenta 4 criterios mayores o 3 criterios mayores + 2 criterios menores, el niño debe remitirse a una unidad de sueño.
Pauta diagnóstica en la unidad de sueño
Las herramientas diagnósticas en esta etapa son:
1. Nasofibroscopia con endoscopio flexible: permite valorar la permeabilidad de las fosas nasales, la presencia de hipertrofia adenoidea, la permeabilidad de las coanas y la presencia de alteraciones laríngeas91.
2. Poligrafía respiratoria (PR): los sistemas portátiles o de PR (niveles III y IV de la ASDA)99 son sistemas diseñados inicialmente para su utilización en el domicilio y que típicamente incluyen la medida de variables cardiorrespiratorias pero no de variables neurofisiológicas; los polígrafos a utilizar deben registrar: flujo oronasal (generalmente medido con termopar/termistor y/o cánula nasal), esfuerzo respiratorio (torácico y/o abdominal), saturación de oxígeno por pulsioximetría, posición corporal, ronquido y frecuencia cardíaca); otra variable que suelen incorporar es el electromiograma tibial (2 electrodos en el tibial anterior) para evaluar los movimientos periódicos de piernas. Son técnicas no vigiladas y que no permiten intervención durante su realización. Se realiza, al igual que la PSG, durante el horario de sueño nocturno. Son muchos los polígrafos respiratorios que existen en el mercado y algunos de ellos han sido validados por las unidades de sueño que los utilizan.
El sueño debe ser espontáneo, no inducido farmacológicamente, y habitualmente se realiza entre las 22 h y las 8 h del día siguiente. Los criterios de análisis de los registros deberán ser los mismos en todos los polígrafos en cuanto a todas las variables que registren y según criterios de la American Association of Sleep Medicine (AASM)80.
La PR presenta algunas limitaciones que es necesario conocer:
1. No detecta los microdespertares electroencefalográficos, por lo que no permite diagnosticar el síndrome de resistencia aumentada de la vía aérea superior. Frente a ello, algunos estudios han relacionado la presencia de microdespertares electroencefalográficos con otras variables, como la disminución del tiempo de tránsito de pulso, el aplanamiento del asa del flujo inspiratorio o la disminución de la amplitud de las bandas seguido de una hiperventilación.
2. Al no registrar variables neurofisiológicas que nos permiten registrar el tiempo de sueño, utiliza el tiempo en la cama como denominador de los distintos índices (apneas, hipopneas, desaturaciones), lo que puede producir falsos negativos al ser el tiempo en la cama mayor que el tiempo de sueño real.
A pesar de estas limitaciones, la American Thoracic Society (ATS) reconoce que la PR sería una técnica prometedora y requiere investigación al respecto. Varios autores sugieren que el empleo de criterios clínicos, junto con una exploración minuciosa de la vía aérea superior, un vídeo doméstico y una PR con un equipo validado es una buena alternativa para el diagnóstico de certeza de niños con sospecha clínica de SAHS100,101. Hay pocos estudios realizados con PR en niños y los que hay se realizaron en población de alta probabilidad de SAHS, con escaso número de pacientes y sin comparar simultáneamente con la PSG, obteniéndose resultados discordantes102,103.
Recientemente se ha publicado un estudio en 53 niños con sospecha clínica de SAHS, a los cuales se les ha realizado simultáneamente PSG y PR en el laboratorio de sueño104. Considerando como diagnóstico de SAHS la presencia de índice de apneas/hipopneas obstructivo (IAHo) ≥ 3 en PSG e índice de eventos respiratorios (IER) ≥ 3 en PR, la coincidencia diagnóstica fue del 84,9%. La diferencia de medias entre IAHo e IER no fue significativa (0,7 ± 5,4; p = 0,34). El coeficiente de correlación intraclase entre el IAHo y el IER fue de 89,4 (intervalo de confianza [IC] del 95%, 82,4-93,7; p < 0,001). Para el diagnóstico de SAHS se consideraron los valores de IAH obstructivo ≥ 1, ≥ 3 y ≥ 5, calculándose las curvas ROC para cada uno de ellos, siendo 4,6 el mejor IER para los tres valores de IAH obstructivo considerados con un área bajo la curva de eficiencia diagnóstica superior al 85% y una especificidad de hasta el 91,7%. Por tanto, una PR hospitalaria es una alternativa válida para el diagnóstico del SAHS en el niño y se considera una técnica de cribado adecuada para el estudio del SAHS en la infancia.
Su principal indicación sería el estudio de pacientes con alta o baja probabilidad de padecer un SAHS, mientras que los pacientes con probabilidad media y aquellos con comorbilidad asociada deberían realizarse una PSG completa, al igual que aquellos con resultados negativos en la PR, pero con alta sospecha clínica de presentar un SAHS.
Al mismo tiempo, se abre la puerta a la necesidad de validar su realización en el domicilio del propio niño, sobre todo cuando en los últimos años se están comercializando polígrafos extraordinariamente portátiles que permiten su uso en el domicilio.
3. PSG nocturna: la PSG nocturna realizada en el laboratorio de sueño sigue siendo la técnica de referencia1,55,79,80 para el diagnóstico de SAHS en los niños. En 2007, la AASM80 publica las reglas para la codificación de las variables neurofisiológicas y cardiorrespiratorias de la PSG, tanto en adultos como en niños.
La PSG nocturna consiste en el registro continuo y supervisado del estado de vigilia y de sueño espontáneo, no inducido farmacológicamente, mediante el registro de:
a. Variables neurofisiológicas: electroencefalograma, electrooculograma, electromiograma tibial y submentoniano. Permite la valoración de los estadios de sueño y la arquitectura de sueño.
b. Variables cardiorrespiratorias con registro de:
b. 1. Flujo oro-nasal: para la valoración de eventos respiratorios: apneas, hipopneas y limitaciones al flujo, mediante termosensores (termopar/termistor) o cánulas nasales.
b.2. Esfuerzo respiratorio: para la clasificación de los eventos respiratorios en centrales, obstructivos o mixtos mediante bandas piezoeléctricas torácicas y abdominales o pletismografía de impedancia.
b.3. Valoración del intercambio gaseoso: saturación de oxígeno por pulsioximetría (SatO2) y medida del CO2 espirado o transcutáneo.
b.4. Frecuencia cardíaca.
b.5. Ronquido.
b.6. Posición corporal: permite el análisis de la ocurrencia de eventos respiratorios en relación con la posición corporal.
b.7. Electromiografía de los músculos tibiales anteriores: permite el análisis de la presencia o no de movimientos mioclónicos de las piernas durante la vigilia y/o sueño asociados o no a eventos respiratorios.
Dada la edad de los pacientes, requiere un entorno específico adecuado y adaptarse al horario de los niños, requiriendo además personal entrenado tanto en la realización de la técnica como en su interpretación.
Consideraciones técnicas, basadas en la AASM80:
1. El sensor utilizado para detectar la ausencia de flujo para la identificación de las apneas es el termopar o termistor oronasal.
2. El sensor utilizado para la identificación de las hipopneas es la cánula de presión nasal.
3. El sensor aceptado para la detección de esfuerzo respiratorio es el catéter esofágico o la pletismografía de impedancia calibrada o sin calibrar.
4. El sensor para la detección de saturación de oxígeno es la pulsioximetría.
5. Para valorar la hipoventilación alveolar se acepta la monitorización de CO2 transcutáneo o el end-tidal CO2.
Los criterios diagnósticos utilizados en el adulto no pueden utilizarse en los niños y debe tenerse en cuenta, en especial, la diferencia en el criterio de la duración del evento respiratorio y el índice total de estos, que se considera diferente en los niños. El criterio de pausas respiratorias ≥ 10 s para definir un evento respiratorio en los adultos no es correcto en niños, ya que períodos más cortos son capaces de producir descensos de la SatO2 y aumentos de la PaCO2. Hoy en día sabemos que un índice de apneas de 1 es estadísticamente significativo, pero no sabemos cuál es el nivel clínicamente significativo. Al valorar la PSG es preciso tener en cuenta que las apneas centrales son frecuentes en los niños y solo se consideran patológicas si duran más de 20 s o se acompañan de desaturaciones.
En el año 2006 se publican los valores polisomnográficos de normalidad en niños105 y la AASM80 en 2007 publica los criterios para la identificación de apneas y su clasificación, de hipopneas, de limitaciones al flujo, hipoventilación nocturna y de respiración periódica en niños, expuestos en la tabla 1.
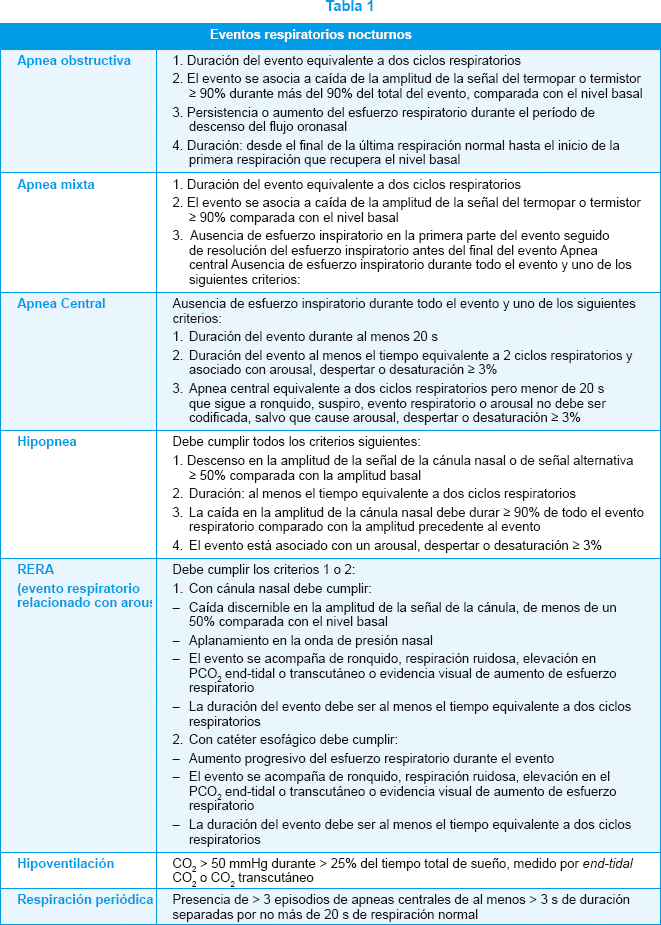
Efecto laboratorio
En un estudio reciente en que se realizaban 2 PSG a un grupo de niños se comprobó que el estudio del primer día identificó correctamente el 84% de los casos con SAHS, y que los casos no detectados en la primera noche fueron aquellos que tenían un IA en el límite de la normalidad106.
Clasificación diagnóstica del síndrome de apneas-hipopneas del sueño en niños
La International Classification of Sleep Disorders considera por consenso el diagnóstico de SAHS en niños cuando hay uno o más eventos respiratorios por hora de sueño. Sobre la base de los conocimientos actuales, teniendo en cuenta los valores de normalidad polisomnográficos publicados en niños, en el año 2005 se publican los criterios diagnósticos de SAHS en niños107.
Estos criterios diagnósticos, a pesar de ser los más recientemente publicados y los únicos que clasifican el grado de gravedad del SAHS en niños, son previos a las normas de codificación publicadas por la AASM en 200780. Actualmente, es necesaria la valoración de los eventos respiratorios, apneas, hipopneas y RERA definidos según la AASM80 para la indicación de tratamiento.
El Grupo de Consenso Español de Síndrome de Apneas/Hipopneas durante el sueño acepta un índice de apneas obstructivas entre 1 y 3 como línea de corte de normalidad108.
Los criterios polisomnográficos que se vienen utilizando son los que se recogen en la tabla 2.
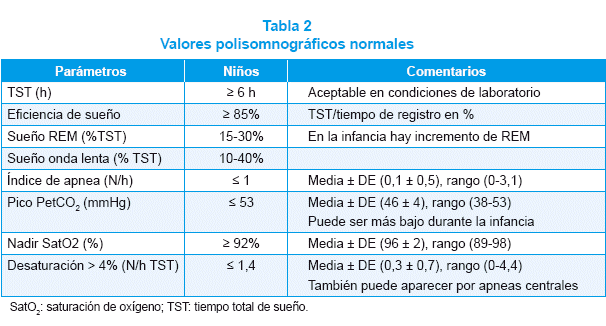
En relación con la gravedad del SAHS, según la PSG esta se clasifica en:
- SAHS leve: IAH < 5.
- SAHS moderado: IAH de 5 a 10.
- SAHS grave: IAH > 10.
Hay que tener en cuenta que los valores de IAH no pueden predecir con precisión la gravedad de la desaturación de oxígeno en pacientes pediátricos con SAHS y viceversa.
Las indicaciones generales de la realización de una PSG en niños con sospecha de SAHS son109:
- Diferenciar el ronquido no acompañado de TRS del ronquido acompañado de TRS.
- Para diagnóstico de SAHS.
- Determinar la intensidad del TRS.
- Clarificar el diagnóstico cuando los síntomas y los factores de riesgo no concuerdan.
- Realizar cribado en niños con altas probabilidades de SAHS (trisomía 21, acondroplasia, etc.).
- Determinar la intensidad de los TRS en niños con riesgo quirúrgico.
- Determinar el nivel de presión positiva (CPAP) necesario.
- Determinar la presencia de SAHS residual después del tratamiento (quirúrgico u otra opción de tratamiento realizado); si persisten síntomas subjetivos, factores de riesgo o previo al tratamiento era un SAHS grave.
- Para diagnóstico de hipoventilación alveolar central congénita.
- Para determinar hipoventilación durante el sueño en enfermedades neurológicas o de la pared torácica.
Los inconvenientes de la PSG son:
- No está disponible en todos los hospitales.
- Es cara y precisa personal especializado.
En Tucson, han realizado estudios polisomnográficos domiciliarios con registros válidos en más del 90% de los niños de entre 5 y 12 años110.
El subcomité para el estudio de SAHS en niños de la AAP concluye que la PSG nocturna es el método más fiable para el diagnóstico de SAHS en niños, aunque los criterios no están validados; subraya que la demora diagnóstica puede acarrear secuelas graves y apoya el desarrollo de una pauta de diagnóstico, cuyos objetivos son:
- Considerar el diagnóstico de SAHS para evitar secuelas por parte de los pediatras.
- Evitar intervenciones quirúrgicas en pacientes que no tienen consecuencias adversas.
- Evaluar a los pacientes de mayor riesgo de complicaciones quirúrgicas.
Esquema diagnóstico-terapéutico
Dada la elevada prevalencia del SAHS en niños y la comorbilidad que conlleva, el tratamiento, en su mayoría quirúrgico con un riesgo derivado de la propia cirugía, la no correlación a veces de la exploración otorrinolaringológica (tamaño de amígdalas) y la posibilidad de que pese al tratamiento quede patología residual, pensamos que se podría usar la PR como primera técnica de diagnóstico con la finalidad de tener un diagnóstico del SAHS cuantificado. La PR podría utilizarse en la extensa población infantil susceptible de SAHS y de esta forma disminuir el infradiagnóstico, reservándose la PSG para niños con comorbilidad derivados de forma urgente para estudio de sueño y en casos de dudas diagnósticas o sospecha de otras patologías de sueño diferentes del SAHS.
Tratamiento del síndrome de apneas-hipopneas del sueño en los niños
El tratamiento de elección del síndrome de apneas-hipopneas durante el sueño (SAHS) en los niños es quirúrgico (adenoamigdalectomía)1,55,108,111-113. Uno de los mayores problemas en niños es a quién y cuándo tratar. Está aceptado que los niños con SAHS grave o con riesgo de serias complicaciones como cor pulmonale o fracaso del crecimiento deben tratarse siempre, requiriendo tratamiento urgente los niños que presenten fracaso cardiorrespiratorio o hipoxemia grave independientemente de la edad. También existe acuerdo en no tratar quirúrgicamente a los niños con ronquido habitual; sin embargo, el tratamiento en los niños con alteraciones poli-somnográficas leves es controvertido.
Tratamiento quirúrgico
Adenoamigdalectomía
Tradicionalmente la adenoamigdalectomía ha sido el tratamiento de elección para los trastornos respiratorios del sueño (TRS) en el niño. Consigue la normalización del cuadro respiratorio nocturno, de la sintomatología diurna y la reversión en muchos casos de las complicaciones cardiovasculares, alteraciones neurocognitivas, retraso en el crecimiento y enuresis.
La eficacia de la adenoamigdalectomía es de aproximadamente el 78% de los casos de SAHS infantil112,113; sin embargo, esta eficacia es variable en los estudios publicados y así recientemente se publi ca un estudio multicéntrico en el que la tasa de curación es de solo un 27,2%114.
El riesgo posquirúrgico pediátrico oscila entre el 0 y el 1,3%; sin embargo, en los niños con SAHS se han encontrado tasas de entre el 16-27%108 con mayor incidencia de complicaciones de la vía respiratoria, recomendándose monitorización en el postoperatorio en los casos de mayor riesgo: edad menor de 3 años, anomalías craneofaciales, retraso de crecimiento, obesidad, parálisis cerebral, cor pulmonale o graves alteraciones en el estudio polisomnográfico previo a la intervención quirúrgica. La American Academy of Pediatrics55 recomienda en estos casos hospitalización y monitorización continua con pulsioximetría durante al menos la primera noche del tratamiento quirúrgico, pudiéndose utilizar la presión positiva continua en la vía aérea (CPAP) en el período perioperatorio para estabilizar a los pacientes antes de la cirugía y para tratamiento de las complicaciones postoperatorias.
En cuanto al seguimiento, todos los niños deben reevaluarse clínicamente después de la cirugía, debiéndose realizar estudio de sueño (polisomnografía [PSG] o poligrafía respiratoria [PR]) posquirúrgico en los niños que fueran SAHS graves en el preoperatorio, o cuando persistan factores de riesgo o síntomas de SAHS.
La última revisión de la Cochrane113 nos muestra la ausencia actual de estudios doble ciego en el tratamiento del SAHS infantil y concluye que la literatura disponible sobre los efectos de la adenoamigdalectomía en el SAHS pediátrico presenta problemas metodológicos que incluyen la falta de aleatorización y controles, así como variaciones en las definiciones y variables tenidas en cuenta; a pesar de todo ello las evidencias disponibles actualmente, provenientes de ensayos no aleatorios y trabajos no controlados, sugieren que la adenoamigdalectomía es un tratamiento eficaz en el SAHS infantil. Así pues, la adenoamigdalectomía sigue siendo hoy en día el tratamiento de elección del SAHS infantil y los clínicos deben seguir realizándola en niños con SAHS significativo y asegurarse de sus beneficios en cada caso concreto; por tanto, ante la ausencia y necesidad actual de estudios de calidad, la cirugía debe realizarse como parte de un completo enfoque clínico.
Técnicas de amigdalectomía
Hay varias técnicas para realizar la amigdalectomía y su respectiva efectividad es aún materia de debate115,116. los resultados quirúrgicos, incluidos la resolución del síndrome de apneas-hipopneas, dolor postoperatorio y tiempo de recuperación, difieren en los diferentes procedimientos. Actualmente, se carece de datos provenientes de ensayos controlados aleatorios que apoyen un método de amigdalectomía sobre otro115,116, dependiendo en gran medida de la experiencia del equipo en cada una de las técnicas quirúrgicas.
Otros procedimientos quirúrgicos
La septoplastia, uvulofaringopalatoplastia, epi-glotoplastia, glosopexia y cirugía maxilomandibular, se realizan con poca frecuencia pero pueden estar indicadas en casos seleccionados.
La traqueotomía, aunque es eficaz en el tratamiento del SAHS tanto infantil como en el adulto, dadas sus importantes consecuencias físicas y psíquicas, actualmente está en desuso y solo se realizaría si las alteraciones anatómicas presentadas fueran imposible de corregir con otras técnicas y no se pudiesen realizar otros tratamiento menos agresivos, debiéndose en estos casos realizar tratamiento con CPAP o ventilación mecánica no invasiva (VMNI) como puente en espera de cirugía o incluso como tratamiento definitivo.
Presión positiva continua en la vía aérea superior
La utilización de CPAP fue desarrollada por Sullivan en 1981 y consiste en una turbina que transmite una presión predeterminada de aire a través de una mascarilla nasal o facial adaptada a la cara del paciente, fijada con un arnés. El sistema genera constantemente un flujo y transmite una presión a la vía aérea superior, evitando su colapso tanto estático (apneas) como dinámico (hipopneas) durante el sueño. La CPAP corrige las apneas obstructivas, mixtas y en ocasiones las centrales, elimina las hipopneas y suprime el ronquido. Evita la desaturación de oxígeno, los despertares electroencefalográficos (arousal) secundarios a los eventos respiratorios y normaliza la arquitectura del sueño. La CPAP no es un tratamiento curativo, lo cual implica que su aplicación debe ser continuada; por ello, obtener un adecuado cumplimiento resulta imprescindible. En el tratamiento con CPAP es fundamental:
- Adecuada indicación del tratamiento con CPAP.
- Adecuada preparación del paciente para la utilización de la CPAP.
- Adecuado control y seguimiento de los pacientes.
La CPAP constituye la segunda línea de tratamiento del SAHS en la infancia117, ya que la mayoría de los niños con SAHS mejora con la adenoamigdalectomía, quedando un pequeño grupo de pacientes que requerirán tratamientos adicionales o en los que el CPAP será la primera opción. Generalmente, suelen ser niños con obesidad, alteraciones craneofaciales o enfermedades neuromusculares añadidas a la hipertrofia adenoamigdalar o sin hipertrofia adeno-amigdalar.
La presión óptima en los pacientes con SAHS es la mínima presión que más efectivamente previene las consecuencias adversas del SAHS, al mismo tiempo que cause menor disconfort y menor riesgo de complicaciones, requiriéndose para ello estudios de titulación de presión de CPAP con el objetivo de encontrar la presión adecuada que normalice la respiración y el sueño fisiológico118. La titulación de presión de CPAP en niños es necesario realizarla con PSG nocturna que permita comprobar la desaparición de los eventos respiratorios y el ronquido, la normalización de la SatO2 y de los valores de CO2, así como una adecuada estructura del sueño. Es necesaria la realización de controles periódicos puesto que son niños en crecimiento y los requerimientos en presión y el ajuste de la mascarilla cambian con el crecimiento y el desarrollo del niño.
La BiPAP, presión positiva continua binivel, está fundamentalmente indicada en pacientes con hipoventilación. Los estudios realizados para valorar CPAP/BiPAP en niños con SAHS sin hipoventilación, fundamentalmente encaminados a valorar la tolerancia y el cumplimiento, no encuentran ventajas en la BiPAP con respecto a la CPAP117. Por tanto, la BiPAP estaría indicada en niños con SAHS e hipoventilación y fundamentalmente en niños con patología concomitante crónica (enfermedad neuro-muscular, síndromes polimalformativos, etc.).
Recientes investigaciones han demostrado la efectividad de una cánula nasal de alto flujo y baja presión para el tratamiento del SAHS119, requiriéndose más investigaciones al respecto.
Efectos secundarios del tratamiento con presión positiva continua en la vía aérea superior
En general, los efectos secundarios inmediatos suelen ser: irritación o erosión local, conjuntivitis, sequedad nasal o faríngea, rinorrea, aerofagia, epistaxis, etc. Como complicación se ha descrito la hipoplasia facial del tercio medio de la cara por un largo uso y la compresión continuada de la mascarilla. Es aconsejable el uso de humidificadores y el tratamiento efectivo de las alergias y/o rinitis.
Control y seguimiento de los niños tratados con presión positiva continua en la vía aérea superior
Se debe realizar el seguimiento de estos pacientes regularmente durante los 3 primeros meses para evaluar la adaptación a la mascarilla y los posibles efectos adversos120: 1 semana, 15 días, 1 mes, 2 meses, 3 meses y posteriormente, debido al rápido crecimiento craneofacial en los niños, debe evaluarse cada 6 meses. Se debe realizar una visita anual para evaluar la posibilidad de deficiencia del crecimiento maxilar120. Se debe prestar especial atención al tamaño de la máscara (con necesidad de cambio aproximadamente cada 6 meses según el período evolutivo), así como a los puntos de sujeción, siendo aconsejable disponer de dos mascarillas con diferentes puntos de presión.
Oxigenoterapia
Los estudios que han evaluado el efecto del tratamiento con oxígeno en niños con SAHS demuestran mejoría de la saturación de oxígeno pero no se observa modificación ni en el número ni en la duración de las apneas obstructivas; en cambio, en algunos individuos se observaba aumento de los niveles de CO2 con el suplemento de oxígeno; por ello no se debe administrar oxígeno a los niños con SAHS si no es asociado a monitorización cardiorrespiratoria o en presencia de soporte ventilatorio.
Tratamiento conservador
En todo niño obeso, la dieta es una de las primeras medidas terapéuticas, aunque, al igual que en el adulto, la pérdida de peso y la terapia posicional, es poco efectiva.
La obesidad puede producir SAHS al aumentar la presión crítica, ya sea por efecto directo sobre la propia vía aérea superior (VAS), provocando un estrechamiento de la misma debido al depósito de tejido adiposo, o por efecto indirecto sobre los músculos dilatadores faríngeos, disminuyendo su capacidad contráctil. Aunque la mayoría de los adultos con SAHS son obesos, los niños con SAHS frecuentemente presentan peso normal o incluso fracaso de crecimiento; sin embargo, la obesidad puede aumentar el riesgo de SAHS en los niños. En los últimos años, con el aumento de la incidencia de la obesidad en la infancia, se está observando un aumento de la incidencia de SAHS en niños obesos. En niños obesos con SAHS siempre es necesario indicar tratamiento dietético y pérdida ponderal, aunque incluso en niños obesos con hipertrofia adenoamigdalar la primera opción de tratamiento es la adenoamigdalectomía121.
Tratamiento farmacológico
La inflamación de la mucosa nasal está presente en los niños con SAHS, en los cuales la causa más frecuente del SAHS es la hipertrofia adenoamigdalar. El tratamiento de las rinitis alérgicas se realiza con corticoides tópicos nasales, objetivándose una disminución de la inflamación de la mucosa. El tratamiento con corticoides tópicos sobre la hipertrofia adenoidea produce mejoría de los síntomas de obstrucción nasal en niños con hipertrofia adenoidea moderada-grave y disminución del tamaño adenoideo122. Por tanto, los corticoides tópicos nasales pueden ser un tratamiento en niños con SAHS leve, con hipertrofia adenoidea moderada-grave y predominancia de síntomas nasales. Sin embargo, los efectos a largo plazo aún no son conocidos, requiriéndose estudios a largo plazo.
Los antagonistas de receptores de los leucotrienos actuarían como agentes antiinflamatorios y, por tanto, reduciendo el volumen total del tejido linfoideo en la vía aérea superior, conduciendo a una mejoría de los TRS en los niños123.
Tratamiento ortodóntico
Pocos estudios han evaluado el papel del tratamiento ortodóncico-ortopédico.
La patogenia del SAHS infantil es un proceso dinámico, siendo la conjunción de factores anatómicos y funcionales la que lleva a un desequilibrio de la VAS traducido en colapso de la VAS y, por tanto, alteración de la respiración y de la ventilación normal durante el sueño124. Ciertas anomalías esqueléticas craneofaciales ocasionan estrechamiento y obstrucción de la VAS. Aunque los tratamientos ortopédicos no obtienen resultados inmediatos, su utilización en edades tempranas puede mejorar el desarrollo de las características craneofaciales y, por tanto, disminuir el riesgo de desarrollar SAHS en edad adulta108. En una revisión realizada por la Cochrane125, se concluye que no existen pruebas suficientes para declarar que los aparatos bucales o los aparatos ortopédicos funcionales sean efectivos para el tratamiento del SAHS en los niños. Sin embargo, el tratamiento ortodóntico puede ser útil en el tratamiento de los niños con anomalías craneofaciales que constituyan factores de riesgo del SAHS126.
Ante un niño con SAHS, es necesaria una adecuada exploración esquelética, y en caso de presencia de anomalías esqueléticas craneofaciales, considerar la opción de tratamiento ortodóncico-ortopédico.
Estrategia terapéutica
El tratamiento del SAHS en el niño puede mejorar con el conocimiento de los factores etiopatogénicos. El SAHS en el niño no es consecuencia de una única causa, sino de la asociación de diferentes factores etiopatogénicos: mecánicos, neurológicos, genéticos, etc. El problema fundamental es el desconocimiento actual de la historia natural de la apnea del sueño127,128. Hoy sabemos cuáles son los valores de normalidad, pero aún desconocemos cuál es la estrategia terapéutica a seguir. Esto es debido, en parte, a que a pesar de que el tratamiento de elección del SAHS en la infancia es la adenoamigdalectomía, no existen estudios controlados y aleatorizados en este sentido y tampoco conocemos los resultados a largo plazo de dicho tratamiento. Parece razonable no basarnos únicamente en niveles patológicos de índice de apneas-hipopneas (IAH), sino, además, tener en cuenta otros factores, como son la clínica y la comorbilidad, para establecer una adecuada estrategia, tanto diagnóstica como terapéutica129,130. En este sentido, y basándonos en los criterios actuales de diagnóstico y los niveles de normalidad, se plantea una estrategia terapéutica que tenga en cuenta la asociación de valores de PSG, clínica y comorbilidad o consecuencias demostradas del SAHS (fig. 3).
Para establecer indicación de tratamiento, consideraremos una serie de variables:
- IAH por hora de sueño.
- IAR: índice de alteraciones respiratorias: índice de apnea + hipopnea + RERA obstructivo/h de sueño.
- IER: índice de eventos respiratorios obstructivos en la PR.
- SatO2 min: saturación de oxígeno mínima.
- % TST PetCO2 > 50 mmHg: porcentaje de tiempo total de sueño con CO2 transcutáneo o end-tidal por encima de 50 mmHg.
- Síntomas: teniendo en cuenta los síntomas mostrados en el árbol de decisión.
- Comorbilidad: teniendo en cuenta la comorbilidad mostrada en el árbol de decisión.
- Hipertrofia adenoamigdalar.
En cada caso, podremos considerar más de una opción de tratamiento. Teniendo en cuenta la alteración predominante, las variables previamente mencionadas y el árbol de decisión, podemos establecer los siguientes grupos de tratamiento, siempre considerando cada caso concreto de forma individualizada:
1. Derivación a otorrinolaringología e indicación de adenoamigdalectomía:
la presencia de síntomas y/o comorbilidad y alguna de las siguientes variables:
- IER(enPR)>5.
- IAH (PSG) > 3.
- IAH < 3 con IAR > 2.
- SatO2 mínima < 85% y % TST PetCO2 > 50 mmHg durante > 25% TTS.
Cuando el IER (en PR) < 5, con presencia de síntomas y/o comorbilidad, es indicación de PSG.
2. Terapia antiinflamatoria (corticoides tópicos y antileucotrienos): cuando no exista SatO2 mínima< 85% ni PETCO2 > 50 mmHG durante > 25% TTS, en las siguientes circunstancias:
- IAH (PSG): 3-5 sin comorbilidad.
- IAH (PSG): 1-3 con IAR > 2.
- Podría considerarse en caso de indicación quirúrgica y tiempo de espera quirúrgico > 4 meses.
3. Tratamiento con CPAP:
- Presencia de un SAHS residual después de una intervención quirúrgica.
- SAHS asociado a otras patologías (p. ej., síndromes malformativos, síndrome de Down, enfermedades neuromusculares, obesidad), en el período de espera a tratamiento quirúrgico, ante SAHS residual o persistente después de tratamiento quirúrgico o ante imposibilidad o contraindicación de tratamiento quirúrgico.
- En el período prequirúrgico para estabilizar la vía aérea en niños con aumento de riesgo quirúrgico.
- En el intervalo de crecimiento craneofacial y dental hasta la intervención quirúrgica definitiva.
4. Control evolutivo en el plazo aproximado de 6-12 meses.
- IAH (PSG): 1-3 con IAR < 2.
- IAH (PSG) < 1.
5. En los casos concretos de hipoventilación, que cursen con desaturaciones de oxígeno y PET CO2 elevado, estaría indicado tratamiento quirúrgico y/o tratamiento con VMNI.
6. Tratamiento ortodóncico-ortopédico: valorar su indicación en los casos que presenten alteraciones craneofaciales.
Control postratamiento
En cuanto al seguimiento, todos los niños deben reevaluarse clínicamente después de la cirugía, debiéndose realizar estudio de sueño posquirúrgico109 en los niños que fueran SAHS grave en el preoperatorio y en aquellos en que, aunque no sean SAHS grave, persistan factores de riesgo o síntomas de SAHS:
- Si clínicamente presentan mejoría sintomática, en los casos de SAHS grave o con factores de riesgo, sería recomendable control polisomnográfico en el plazo de 6 meses.
- Si presentan sintomatología clínica persistente a pesar de tratamiento quirúrgico, se realizará PSG independientemente de la gravedad del SAHS.
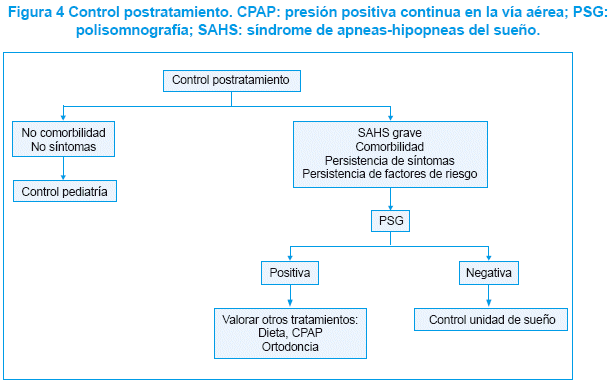
Agradecimientos
Queremos expresar nuestro agradecimiento a todos los miembros de las sociedades científicas integrantes de este documento por las sugerencias, comentarios y aportaciones que lo han hecho posible.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. American Academy of Pediatrics. Clinical practice guideline: Diagnosis and management of child-hood obstructive sleep apnea syndrome. Pediatrics 2002; 109:704-12. [ Links ]
2. American Academy of Sleep Medicine. International classification of sleep disorders. 2nd ed. En: Diagnostic and coding manual. Westchester: American Academy of Sleep Medicine; 2005.
3. Teculescus DB, Cailluier I, Perrin R, Rebstock E, Rauch A. Snoring in French preschool children. Pediatr Pulmonol. 1992;13:239-44. [ Links ]
4. Delasnerie-Laupetre N, Patois E, Valatx JL, Kaufmann F, Alperovitch A. Sleep, snoring and smoking in high school students. J Sleep Res. 1993;2:138-42. [ Links ]
5. Miguel-Diez J, Villa-Asensi JR, Alvarez-Sala JL. Prevalence of sleep-disordered breating in children with Down syndrome. Polygraphic finding in 108 chidren. Sleep. 2003 ;25:1006-9. [ Links ]
6. Tomás Vila M, Beseler Soto B, Benac Prefasi M, Cardona Ferrer C, Pascual Olmos MJ, Lozano Campos I. Trastornos del sueño en niños y adolescentes con incapacidad psíquica. Análisis comparativo entre alumnos escolarizados en centros ordinarios y centros de educación especial de la Comunidad Valenciana. An Pediatr (Barc). 2008;69:335-41. [ Links ]
7. Gozal D, Simakajornboon N, HolbrookCR. Secular trends in obesity and parenterally reported daytime sleepiness among children referred to a pediatric sleep center for snoring and suspected sleep-disordered breathing (SDB). Sleep. 2006;29:A74. [ Links ]
8. Sans-Capdevila O, Gozal D. Consecuencias neuro-biológicas del síndrome de apnea del sueño infantil. Rev Neurol. 2008;47:659-64. [ Links ]
9. Kotagal P, Yardi N. The relationship between sleep and epilepsy. Semin Pediatr Neurol. 2008;15:42-9. [ Links ]
10. Bhattacharjee R, Gozal D. Cardiovascular disease and sleep disordered breathing: are children vulnerable? Sleep. 2009;32:1251-2. [ Links ]
11. Snow A, Serpero L, Sans Capdevila O, et al. Urinary catecholamines in pediatric obstructive sleep apnea: effect of obesity. Sleep. 2008 (A0184). [ Links ]
12. Kwok KL, Ng DK, Cheung YF. BP and arterial distensibility in children with primary snoring. Chest. 2003;123:1561-6. [ Links ]
13. Brietzke SE, Katz ES, Roberson DW. Pulse transit time as a screening test for pediatric sleep-related breathing disorders. Arch Otolaryngol Head Neck Surg. 2007;133:980-4. [ Links ]
14. Kheirandish-Gozal L, Bhattacharjee R, Gozal D. Autonomic alterations and endothelial dysfunction in pediatric obstructive sleep apnea. Sleep Med. 2010;11: 714-20. [ Links ]
15. Liao D, Li X, Rodriguez-Colon SM, Liu J, Vgontzas AN, Calhoun S, Bixler EO. Sleepdisordered breathing and cardiac autonomic modulation in children. Sleep Med. 2010;1 1:484-8. [ Links ]
16. Zintzaras E, Kaditis AG. Sleep-disordered breathing and blood pressure in children: a meta-analysis. Arch Pediatr Adolesc Med. 2007;161:172-8. [ Links ]
17. Amin RS, Carroll JL, Jeffries JL, Grone C, Bean JA, Chini B, et al. Twenty-four-hour ambulatory blood pressure in children with Sleepdisordered breathing. Am J Respir Crit Care Med. 2004;169:950-6. [ Links ]
18. Li AM, Au CT, Sung RY, Ho C, Ng PC, Fok TF, et al. Ambulatory blood pressure in children with obstructive sleep apnoea -a community based study. Thorax. 2008;63:803-9. [ Links ]
19. Amin RS, Kimball TR, Kalra M, Jeffries JL, Carroll JL, Bean JA, et al. Left ventricular function in children with sleep-disordered breathing. Am J Cardiol. 2005;95: 801-4. [ Links ]
20. Gorur K, Doven O, Unal M, Akkus N, Ozcan C. Preoperative and postoperative cardiac and clinical findings of patients with adenotonsillar hypertrophy. Int J Pediatr Otorhinolaryngol. 2001;59:41-6. [ Links ]
21. Arias MA, García-Río F, Alonso-Fernández A, Martínez I, Villamor J. Pulmonary hypertension in obstructive sleep apnoea: Effects of continuous positive airway pressure: A randomized, controlled cross-over study. Eur Heart J. 2006;27:1106-13. [ Links ]
22. Gozal D, Kheirandish-Gozal L. Cardiovascular morbidity in obstructive sleep apnea. Oxidative stress, inflammation, and much more. Am J Respir Crit Care Med. 2008;17:369-75. [ Links ]
23. Gozal D, Kheirandish-Gozal L, Serpero LD, Sans Capdevila O, Dayyat E. Obstructive sleep apnea and endothelial function in school-aged nonobese children: effect of adenotonsillectomy. Circulation. 2007;116:2307-14. [ Links ]
24. De la Peña M, Barceló A, Barbe F, Piérola J, Pons J, Rimbau E, et al. Endotelial function and circulating endothelial progenitor cells in patients with sleep apnea syndrome. Respiration. 2008;76:28-32. [ Links ]
25. Sans Capdevila O, Kheirandish-Gozal L, Dayyat E, Gozal D. Pediatric obstructive sleep apnea. Complications, management, and long-term outcomes. Proc AmThorac Soc. 2008:274-82. [ Links ]
26. Kaditis AG, Alexopoulos EI, Kalampouka E, Hatzi F, Karadonta I, Kyropoulos T, et al. Nocturnal change of circulating intercellular adhesion molecule 1 levels in children with snoring. Sleep Breath. 2007; 11:267-74. [ Links ]
27. Kataoka T, Enomoto F, Kim R, Yokoi H, Fujimori M, Sakai Y, et al. The effect of surgical treatment of obstructive sleep apnea syndrome on the plasma TNF alpha levels. Tohoku J Exp Med. 2004;204:267-72. [ Links ]
28. Gozal D, Serpero LD, Kheirandish-Gozal L, Capdevila OS, Khalyfa A, Tauman R. Sleep measures and morning plasma TNF-alpha levels in children with sleepdisordered breathing. Sleep. 2010;33:319-25. [ Links ]
29. Kheirandish-Gozal L, Capdevila OS, Tauman R, Gozal D. Plasma reactive protein in nonobese children with obstructive sleep apnea before and after adenotonsillectomy. J Clin Sleep Med. 2006;2:301-4. [ Links ]
30. Kaditis AG, Alexopoulos EI, Kalampouka E, Kostadima E, Angelopoulos N, Germenis A, et al. Morning levels of fibrinogen in children with sleep disordered breathing. Eur Respir J. 2004;24:790-7. [ Links ]
31. Lévy P, Bonsignore MR, Eckel J. Sleep, sleep-disordered breathing and metabolic consequences. Eur Respir J. 2009;34:243-60. [ Links ]
32. Dayyat E, Kheirandish-Gozal L, Gozal D. Childhood obstructive sleep apnea: one or two distinct disease entities? Clin Sleep Med. 2007;42:374-9. [ Links ]
33. Freezer NJ, Bucens IK, Robertson CF. Obstructive sleep apnoea presenting as failure to thrive in infancy. J Paediatr Child Health. 1995;31:172-5. [ Links ]
34. Roemmich JN, Barkley JE, D'Andrea L, Nikova M, Rogol AD, Carskadon MA, et al. Increases in overweight after adenotonsillectomy in overweight children with obstructive sleep-disordered breathing are associated with decreases in motor activity and hyperactivity. Pediatrics. 2006;117:e200-8. [ Links ]
35. Nieminen P, Lopponen T, Tolonen U, Lanning P, Knip M, Lopponen H. Growth and biochemical markers of growth in children with snoring and obstructive sleep apnea. Pediatrics. 2002;109:e55. [ Links ]
36. Tresaco B, Bueno G, Pineda I, Moreno LA, Garagorri JM, Bueno M. Homeostatic model assessment (HOMA) index cut-off values to identify the metabolic syndrome in children. J Physiol Biochem. 2005;61:381-8. [ Links ]
37. Weiss R, Dziura J, Burgert TS, Tamborlane WV, Taksali SE, Yeckel CW, et al. Obesity and the metabolic syndrome in children and adolescents. N Engl J Med. 2004;350:2362-74. [ Links ]
38. Verhulst SL, Rooman R, Van Gaal L, De Backer W, Desager K. Is sleep-disordered breathing an additional risk factor for the metabolic syndrome in obese children and adolescents? Int J Obes. 2009;33:8-13. [ Links ]
39. Tauman R, O'Brien LM, Ivanenko A, Gozal D. Obesity rather than severity of sleepdisordered breathing as the major determinant of insulin resistance and altered lipidemia in snoring children. Pediatrics. 2005;116:e66-73. [ Links ]
40. Redline S, Storfer-Isser A, Rosen CL, Johnson NL, Kirchner HL, Emancipator J, et al. Association between metabolic syndrome and sleep-disordered breathing in adolescents. Am J Respir Crit Care Med. 2007;176:401-8. [ Links ]
41. De la Eva RC, Baur LA, Donaghue KC, Waters KA. Metabolic correlates with obstructive sleep apnea in obese subjects. J Pediatr. 2002;140:654-9. [ Links ]
42. Waters KA, Sitha S, O'Brien LM, Bibby S, De Torres C, Vella S, et al. Follow-up on metabolic markers in children treated for obstructive sleep apnea. Am J Respir Crit Care Med. 2006;174:455-60. [ Links ]
43. Kaditis AG, Alexopoulos EI, Damani E, Karadonta I, Kostadima E, Tsolakidou A, et al. Obstructive sleep-disordered breathing and fasting insulin levels in nonobese children. Pediatr Pulmonol. 2005;40:515-23. [ Links ]
44. Verhulst SL, Schrauwen N, Haentjens D, Rooman RP, Van Gaal L, De Backer WA, et al. Sleep-disordered breathing and the metabolic syndrome in overweight and obese children and adolescents. J Pediatr. 2007;150:608-12. [ Links ]
45. Ortega RM. Obesidad, resistencia a la insulina y aumento de los niveles de adipoquinas. Nutrición hospitalaria: órgano oficial de la Sociedad Española de Nutrición Parenteral y Enteral. 2009;24:415-21. [ Links ]
46. Katagiri H, Yamada T, Oka Y. Adiposity and cardiovascular disorders: disturbance of the regulatory system consisting of humoral and neuronal signals [review]. [Published erratum appears in Circ Res. 2007;101:e79.] Circ Res. 2007;101: 27-39. [ Links ]
47. Tauman R, Serpero LD, Capdevila OS, O'Brien LM, Goldbart AD, Kheirandish-Gozal L, et al. Adipokines in children with sleep disordered breathing. Sleep. 2007;30:443-9. [ Links ]
48. Gozal D, Sans Capdevila O, Kheirandish-Gozal L. Metablic alterations and systemic inflammation in obstructive sleep apnea among nonobese and obese prepubertal children. Am J Respir Crit Care Med. 2008; 177:1142-9. [ Links ]
49. Kheirandish-Gozal L, Sans Capdevila O, Kheirandish E, Gozal D. Elevated serum aminotransferase levels in children at risk for obstructive sleep apnea. Chest. 2008;133:92-9. [ Links ]
50. Nakra N, Bhargava S, Dzuira J, Caprio S, Bazzy-Asaad A. Sleep-disordered breathing in children with metabolic syndrome: the role of leptin and sympathetic nervous system activity and the effect of continuous positive airway pressure. Pediatrics. 2008;122:e634-42. [ Links ]
51. Apostolidou MT, Alexopoulos EI, Damani E, Liakos N, Chaidas K, Boultadakis E, et al. Absence of blood pressure, metabolic, and inflammatory marker changes after adenotonsillectomy for sleep apnea in Greek children. Pediatr Pulmonol. 2008;43:550-60. [ Links ]
52. Kohler MJ, Van den Heuvel CJ. Is there a clear link between overweight/obesity and sleep disordered breathing in children? Sleep Med Rev. 2008;12:347-61. [ Links ]
53. Spruyt K, Gozal D. Mr. Pickwick and his child went on a field trip and returned almost empty handed... What we do not know and imperatively need to learn about obesity and breathing during sleep in children! Sleep Med Rev. 2008; 12:335-8. [ Links ]
54. Arens R, Muzumdar H. Childhood obesity and obstructive sleep apnea syndrome. J Appl Physiol. 2010;108:436-44. [ Links ]
55. American Academy of Pediatrics. Technical report: diagnosis and management of childhood obstructive sleep apnea syndrome. Pediatrics. 2002;109:e69-89. [ Links ]
56. Owens J.A, Mehlenbeck R, Lee J, King MN. Effect of weight, sleep duration and comorbid sleep disorders on behavioral outcomes in children with sleep-disordered breathing. Arch Pediatr Adolesc Med. 2008;162:313-21. [ Links ]
57. Friedman BC, Hendeles-Amitai A, Kozminsky E, Leiberman A, Friger M, Tarasiuk A, et al. Adenotonsillectomy improves neurocognitive function in children with obstructive sleep apnea syndrome. Sleep. 2003;26:999-1005 [ Links ]
58. Beebe DW, Ris MD, Kramer ME, Long E, Amin R. The association between sleep disordered breathing, academia grades and cognitive and behavioral functioning among overweight subjects during middle to late childhood. Sleep. 2010;33: 1447-56. [ Links ]
59. Gozal D, Pope D. Ronquido durante la niñez temprana y rendimiento académico a los 13-14 años. Pediatrics (ed. esp.). 2001;51:427.
60. Dayyat E, Kheirandish-Gozal L, Sans Capdevilla O, Maarafeya MM, Gozal D. Obstructive sleep apnea in children: relative contributions of body masss index and adenotonsillar hypertrophy. Chest. 2009; 136:137-44. [ Links ]
61. Byars K, Apiwattanasawee P, Leejakpai A, Tangchit-yongsiva S, Simakajornboom N. Behavioral sleep disturbances in children clinically referred for evalutation of obstructive sleep apnea. Sleep Med. 2011;12:163-9. [ Links ]
62. Beebe DW. Neurobehavioral morbidity associated with disordered breathing during sleep in children: a comprehensive review. Sleep. 2006;29:1115-34. [ Links ]
63. Esteller E, Barceló M, Segarra F, Piñeiro Z, Pujol A, Matiño E, et al. Alteraciones neurognitivas y conductuales en los trastornos respiratorios del sueño infantil. Acta Otorrinolaringol Esp. 2009;60:325-31. [ Links ]
64. Bass JL, Corwin M, Gozal D, Moore C, Nishida H, Parker S, et al. The effect of chronic or intermittent hypoxia on cognition in childhood: a review of the evidence. Pediatrics. 2004;114:805-16. [ Links ]














