Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista de la Sociedad Boliviana de Pediatría
versión On-line ISSN 1024-0675
Rev. bol. ped. v.46 n.1 La Paz 2007
ARTICULO ORIGINAL
Adherence to treatment of anemia with microencapsulated ferrous fumarate
Drs.: C. Cinthya Urquidi B.*, Héctor Mejía S.**, Claudia Vera A.***
* Médico Epidemiologo./ claudiacinthya@gmail.com
** Pediatra. Hospital del Niño “Dr. Ovidio Aliaga U.” La Paz, Bolivia
*** Médico Cirujano. Centro de Iniciativa para el Desarrollo y Promoción en Salud
Artículo recibido 14/2/07 y fue aprobado para publicación 18/4/07
Resumen
Objetivos: evaluar según el porcentaje de respuesta, la adherencia al tratamiento de la anemia con microgránulos de fumarato ferroso.
Diseño: ensayo clínico aleatorio controlado.
Intervención: gotas de sulfato ferroso y microgránulos de fumarato ferroso.
Métodos: 124 niños con valores de hemoglobina menores a 13.7 g/dL y de 6 a 24 meses de edad ingresaron al estudio, fueron aleatorizados en dos grupos, el grupo control con sulfato ferroso y el grupo experimental de los microgránulos con fumarato ferroso. Se midió los niveles de hemoglobina antes y después del tratamiento y otras variables de cumplimiento.
Resultados: el porcentaje de niños que pasaron al estado no anémico en el grupo fumarato ferroso fue de54% y en el grupo control 22% (p< 0.05). El porcentaje de respuesta positiva al tratamiento en el grupo fumarato fue de 91% y en el grupo control del 71% (p< 0.05). La media de hemoglobina final del grupo experimental fue de 13.5 g/dL y de 12.6 g/dL en el control (p< 0.05). El porcentaje de cumplimento fue significativamente en el grupo experimental fue de 78% y en el control del 55%, (p< 0.05).
Conclusiones: el uso del fumarato ferroso microencapsulado, produce una reducción significativa de la prevalencia de anemia en una población pediátrica de alto riesgo por presentar mejor adherencia a este. La aplicación de la nueva intervención en los programas de salud, aumentaría en un 33% los beneficios obtenidos por el nuevo suplemento.
Rev. Soc. Bol. Ped. 2007;46 (1): 3-11: Anemia, deficiencia de hierro, adherencia, fumarato ferroso.
Abstract
Objective: to evaluate the adherence to treatment of anemia through the percentage of response with ferrous fumarate, in comparison to ferrous sulfate drops after two months of treatment.
Study Design: randomized controlled clinical trial.
Intervention: ferrous sulfate drops and microencapsulated ferrous fumarate sprinkles.
Methods: 128 Children (age-6-24 months) were enrolled and randomized to ferrous sulfate drops group or ferrous fumarate group. Capillary blood samples taken at the baseline and final visits were obtained from a finger prick in order to asses hemoglobin values. Compliance was also measured.
Results: successful treatment of anemia (hemoglobin > 13.6 g/dL) occurred in 54 % of the sprinkles group and in 22% of the drops group (p<0.05). The positive response to treatment was higher in the experimental group (91%) than the control group (71%) (p<0.05). The rate of compliance was 55 % in the control group and 76 % in the experimental group. The mean hemoglobin levels increases significantly in each group from baseline to the final visit.
Conclusion: the use of microencapsulated ferrous fumarate increased the adherence to treatment and reduced the rates of anemia significantly in high risk pediatric population. The implementation of the new intervention by programs health would enhance over 33% the benefits.
Key Word:
Rev. Soc. Bol. Ped. 2007;46 (1): 3-11: Anemia, iron deficiency, adherence, ferrous sulfate, ferrous fumarate.
La Organización Mundial de la Salud (OMS) junto con la Fundación para Niños de las Naciones Unidas(UNICEF) estima que el número de niños afectados con anemia ferropénica excede los 750 millones, especialmente en países en desarrollo, siendo una de las principales causas de las altas tasas de morbimortalidad infantil. Varios estudios han demostrado que este tipo de anemia se encuentra estrechamente relacionada con una depresión tanto motora como mental en el desarrollo del niño, la cual puede ser irreversible.a,b,c,d,e
Aunque la diversificación y fortificación de alimentos han demostrado ser efectivos en países, los hábitos alimenticios y el grado de pobreza de varios países en desarrollo, como ocurre en Bolivia, dejan fuera del alcance el consumo de estos alimentos.f
La principal estrategia en Bolivia, para el control y tratamiento de la anemia, es la suplementación con hierro. A pesar de todos los esfuerzos realizados para la mejora de la adherencia y cumplimiento del tratamiento, el desagradable sabor metálico, la tinción dental y el disconfort abdominal que deja el sulfato ferroso después de su ingesta, sigue siendo la principal barrera para alcanzar las metas trazadas por los diferentes programas y sobre todo, es la principal barrera que encuentran los padres para lograr que sus niños puedan ingerir el suplemento5.
Según la Encuesta Nacional de Salud y Demografía del 2003 (ENDSA), 8 de cada 10 niños bolivianos presenta algún grado de anemia. Es evidente, por la alta prevalencia, que las estrategias implementadas no han sido satisfactorias. De cualquier modo, existe evidencia de que las gotas de sulfato ferroso son poco efectivas en el tratamiento de la anemia ferropénica, particularmente debido al incumplimiento del régimen terapéutico por su desagradable sabor metálico, por los efectos adversos gastrointestinales y la tinción dental producida por el hierro .g,h,i,j,k
En respuesta a una reunión de la UNICEF, donde se determinó que la prevención y control de anemia era una prioridad en países en desarrollo, un grupo de investigadores del Hospital del Niño de Toronto, desarrollaron una nueva forma de suplementación en polvo en base de fumarato ferroso y otros micro nutrientes como zinc, vitamina C, D, A y ácido fólico. Varios estudios clínicos y comunitarios se han conducido para determinar la eficacia, seguridad, biodisponibilidad y la aceptabilidad de los microgránulos. En todos los casos, los microgránulos de fumarato ferroso han demostrado ser tan eficaces como las gotas de sulfato ferroso. 7,11
El propósito de este trabajo, es evaluar la aceptación y tolerancia a los microgránulos de fumarato ferroso microencapsulado en relación a las gotas de sulfato ferroso, en circunstancias similares a las de un programa de intervención, dado que este micronutriente fortificador será introducido en el Programa Nacional de Alimentación y Nutrición para la prevención y control de la anemia en niños menores de 2 años.
El estudio se llevó a cabo entre los meses de Julio y Diciembre del 2005, en tres centros de salud dependientes del Ministerio de Salud de la ciudad de La Paz: Centro Materno Infantil Bella Vista, Villa Nuevo Potosí y el Centro de Salud Chasquipampa, donde la población concurrente presenta un nivel socioeconómico homogéneo.
La población de estudio fueron los niños entre 6 mese y 2 años de edad que consultan estos centros. Solo niños con valores menores a 13.6 g/dL (punto de corte para la altura)1 fueron elegibles. Otros criterios de inclusión fueron: residentes del área de jurisdicción del centro, iniciación de alimentación complementaria. No se incluyeron aquellos niños con evidencia clínica de desnutrición severa, enfermedad aguda grave que comprometa el estado general y aquellos provenientes de zonas de alto riesgo de malaria o niños febriles.
Previo el ingreso al estudio, los niños recibieron atención médica integral para descartar otras patologías. Además, contaron con el consentimiento informado por parte de uno de los padres. Los niños cumplieron con los criterios de inclusión, recibieron tratamiento acuerdo al programa tradicional. Los niños que continuaron anémicos pese a cumplir el tratamiento, fueron remitidos a un centro de tercer nivel para descartar otras causas de anemia. A los niños anémicos que no cumplieron con el tratamiento, se les proporcionó el tratamiento contrario. El proceso de reclutamiento se realizó en el horario de mayor consulta en los centros de salud, de 8:00 a.m. a 2:00 p.m., este proceso duró aproximadamente dos semanas hasta completar la muestra.
Los niños fueron asignados aleatoriamente a dos grupos; al grupo fumarato ferroso (experimental) y sulfato ferroso (control). Como no fue posible ni conveniente el cegamiento de los padres ni del profesional de salud, se diseñó un proceso de aleatorización en base a los días de consulta, donde se asignó un tipo de tratamiento a cada día de la semana de forma alterna, esta asignación era desconocida por los padres, así se evitó la contaminación entre grupos. Como el tipo de muestreo realizado fue de casos consecutivos, se dejó al azar la asistencia de cada niño al centro de salud. Ampos grupos por igual recibieron: información y educación acerca de la anemia, sus consecuencias y modo de uso, dosis, posibles efectos adversos y duración del tratamiento.
El esquema de tratamiento para el grupo experimental fue de 1 gramo (1 sobre) diario por 60 días, donde cada sobre contiene 12.5 mg de Fumarato Ferroso, 5 mg de Cinc, 30 mg de vitamina C, 300 μg. de vitamina A y 160 μg. de Acido Fólico. Para el grupo control el esquema fue según normas del programa implementado: Dosis de 20 gotas/ día durante 60 días en niños de 6 meses a 1 año de edad y de 25 gotas de Sulfato Ferroso día en niños de 1 a 2 años de edad con un total de tres frascos. Cada 20 gotas (1 ml) de Sulfato Ferroso, 1 contiene 125 mg de Sulfato Ferroso, 0.25 mg de ácido fólico y 30 mg de Acido Ascórbico.
Se realizó 2 monitoreos, cada 30 días, para completar el esquema de tratamiento, recolectar algunos datos demográficos, variables de adherencia, medición final de hemoglobina.
Para la medición de adherencia se utilizó una combinación de métodos indirectos. Se tomaron muestras de sangre capilar con técnicas estandarizadas para la determinación de los niveles de hemoglobina, las muestras fueron procesadas con el Sistema Fotómetro B-Hemoglobin HemoCue Portable. Para la medición de las otras variables, se utilizó el recuento de dosis restantes y un cuestionario que evaluara la aceptabilidad del tratamiento.
Sobre los datos de un estudio anterior, donde la proporción de niños no anémicos después del tratamiento con sulfato ferroso es de 0.64 y 0.90 con fumarato ferrosom. Con un - unilateral de 0.05 y poder de 90%, se estimó una muestra de 48 niños por grupo. Se estima que las pérdidas en el seguimiento en la conclusión del estudio serían del 30%n por lo que un total de 62 niños por grupo fueron reclutados.
Los datos previamente codificados fueron introducidos a una hoja de cálculo Excel (2003). Para el análisis, se utilizó el paquete estadístico para Windows SPSS 12.0. Los resultados se analizaron por el principio de “intención de tratar” lo que entrega una visión menos sesgada de la real magnitud del efecto de la intervención.
Debido a la ausencia de normalidad y homocedasticidad de las variables cuantitativas y análisis de variables cualitativas, se utilizó estadística no paramétrica para grupos pareados e independientes: Para la comparación de medias se usó las pruebas de Mann-Whitney y Rango de Signos de Wilcoxon, para proporciones se utilizó la prueba de X2 y la prueba de Mc. Nemar. Para las celdas menores a 5, se utilizó la Prueba exacta de Fisher.
Se realizó el tamizaje de anemia a un total de 144 niños de los cuales el 86.8% (125 niños) presentaban concentraciones de hemoglobina menores a 13.6 g/dL. Solo un niño no contó con consentimiento informado de uno de sus padres.
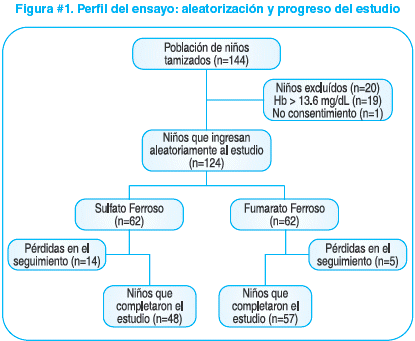
Los 124 niños fueron asignados aleatoriamente a los dos grupos conforme acudían a consulta al centro de salud y al día correspondiente de tratamiento. Las pérdidas en el seguimiento fueron del 15%, 14 niños en el grupo control, 5 en el experimental; esto se debió a que no se encontraron sus domicilios. Hubo un abandono ya que el inicio del tratamiento coincidió con un cuadro diarreico. Previo al análisis, se exploró los datos de aquellos casos perdidos con el principio del “peor de los casos”, el resultado del análisis no cambió significativamente el resultado final, por lo que las pérdidas no fueron incluidas en el análisis. Finalmente, un total de 105 niños terminaron con el protocolo de investigación y se incluyeron en el análisis. (Figura #1)
No hubo diferencia significativa entre grupos en cuanto a la media de hemoglobina, edad y medidas antropométricas. Aunque el género no estaba tan equitativamente distribuido en ambos grupos, tampoco hubo una diferencia significativamente importante. Cuadro # 1.
Después del tratamiento, el porcentaje de respuesta en el grupo control fue de 20.8% y de 54.4% en el grupo experimental, la diferencia de proporciones estimada entre ambos grupos (0.34, IC 95% 0.16, 0.51) fue estadísticamente significativa (p < 0.01). Como este intervalo no incluye el 0, podemos estar 95% seguros que esta diferencia existe.
El porcentaje estimado de niños que respondieron positivamente al tratamiento (aumento de Hb ≥ 1 g/dL) en el grupo experimental fue de 91% (52/57) y de 71% (34/48) en el grupo control. La diferencia entre estas proporciones (0.20, IC95% 0.04,0.26) fue estadísticamente significativa (p=0.007,).
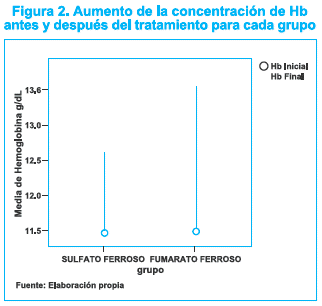
En el grupo experimental, la hemoglobina aumentó un promedio estimado de 2 g/dL después del tratamiento (p= 0.00001, IC95% 1.7 – 2.4) y en el grupo control el aumento fue de 1.1 g/dL (p= 0.00001, IC95% 0.7 – 1.6). Figura # 2.
La media estimada final de hemoglobina en el grupo experimental, fue de 13.5 ± 1.4 g/dL y de 12.6 ± 1.2 g/dL en el grupo control. La diferencia entre estas medias (0.93, IC 95% 0.46, 1.41) fue estadística-mente significativa (p< 0.01).
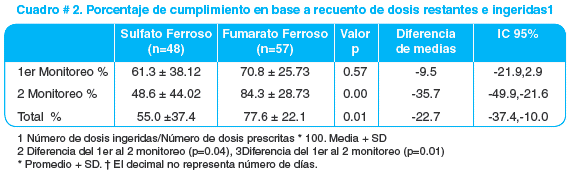
En el primer monitoreo, el porcentaje de cumplimiento promedio para el grupo experimental fue de 70.8% y de 61.1% en el grupo control. En el segundo monitoreo, el cumplimiento en el grupo experimental fue de 84.3% y de 48.6% en el grupo control. En total, el porcentaje promedio de cumplimiento para el grupo experimental fue de 77.6% y de 55.0% en el grupo control. Cuadro # 2.
En el grupo control hubo un 67% (32/48) reporte de problemas en el uso del suplemento y de 28% (16/57) en el grupo experimental, en el primer monitoreo (IC 95% 23,55). En el segundo monitoreo fue de 73% en grupo control y de 16% en el experimental (IC 95% 41,73). La diferencia entre el segundo y primer monitoreo en el reporte de problemas en el grupo control fue de 6% (p=0.629) y de -12% en el grupo experimental (p=0.092).
El “escupir el suplemento” fue el problema más reportado en el primer monitoreo, 38% (18/48) en el grupo control y 23% (12/57) en el experimental (IC95% -1,31) el niño “mantenía la boca cerrada” 25% grupo control (12/48) y 12% (7/57) en el experimental (IC95% -3,29), “llanto y gestos” en tercer lugar por igual. En el segundo monitoreo, en un 46% se reportó “escupía la comida” en el control y en 11% en el experimental (IC95% 19,55), 38% que el niño “mantenía la boca cerrada” en el control y 5% en el experimental (IC95% 17,49), se reportó en un 21% la presencia de “llanto” en el grupo control y de 2% en el experimental (IC95% 3,35).
En el momento del primer monitoreo, el reporte de efectos colaterales fue de 67% en el grupo control y de 56% en el experimental (p=0.271). Para el segundo monitoreo, el reporte para el grupo control fue de 83 y de 75% en el experimental (p=0.322). El efecto más reportado fue estreñimiento.
En el 1er monitoreo al 50% de las madres les pareció “Fácil” el uso de las gotas de sulfato ferroso, al 8% “Muy Fácil” y al 31% le pareció “Difícil”; por otro lado, al 60% de las madres les pareció “Fácil” el uso de los microgránulos de fumarato ferroso, al 30% “Muy Fácil” y al 10% le pareció “Difícil”. Para el segundo monitoreo, al 38% de las madres les pareció “Fácil” el uso de las gotas y “Difícil” al 44%; en el grupo experimental, al 51% (29/57) de las madres les pareció “Fácil” el uso de los microgránulos, al 44% “Muy Fácil” y al 5% “Difícil”.
En el grupo experimental en el primer monitoreo, el 51% de las madres notaron algún cambio en la comida donde los microgránulos fueron mezclados, ya sea en olor, color o sabor. Para el segundo monitoreo la percepción del cambio en la comida fue del 25%. El tipo de comida más utilizado fue la sopa (38.6%), seguida de la papilla (33.3%) y el segundo plato (19.3%), algunas (8.8%) madres utilizaron jugos para la mezcla de los microgránulos.
El aumento relativo del beneficio fue del 0.41 (IC95% 0.17,0.58), lo que significa que la suplementación con microgránulos de fumarato ferroso aumentó en un 41% el beneficio relativo de pasar al estado no anémico que con el uso del suplemento convencional. El aumento absoluto del beneficio fue del 0.32 (IC95% 0.14,0.50), con lo que el 32% de los niños experimentaron un evento favorable en base al uso de los microgránulos. El número necesario de pacientes a tratar para producir el beneficio es de 3 (IC95%2,7). Se estimó un beneficio relativo de 2.4 (mayor que 1), esto quiere decir que la frecuencia de niños que aumenten sus niveles de hemoglobina hasta pasar al estado no anémico, aumentará en 2.4 veces más con el uso del nuevo tratamiento.
En el caso de la terapia con hierro, donde la adherencia es importante, se recomienda la evaluación de la tolerancia en base a la combinación de métodos directos (determinación del fármaco o su metabolito) e indirectos como el recuento de medicación sobrante e información aportada por el propio paciente, debido a las limitaciones de cada uno estos métodos utilizados por sí solos. Por tal motivo, para evaluar la adherencia, se utilizó los niveles de hemoglobina como un marcador indirecto de la ingesta de hierro (ya que ésta responde rápidamente a la suplementación), junto al recuento de dosis restante.o,p,q
Con los resultados obtenidos en este estudio, existe evidencia suficiente para rechazar la hipótesis de nulidad que sustenta que la adherencia al nuevo tratamiento es igual o menor al convencional. El porcentaje estimado de niños que incrementaron sus niveles de hemoglobina hasta alcanzar un estado “no anémico” en el grupo experimental (54%) fue significativamente mayor que en el grupo control (21%). Estos resultados no se pueden comparar con el primer estudio realizado por Zlotkin et alr, donde la diferencia en el porcentaje entre grupos fue del 2%, ya que el protocolo del mencionado estudio no fue diseñado para medir la efectividad sino eficacia del tratamiento; el diseño, requería el máximo cumplimiento del suplemento para alcanzar el objetivo. En otro estudio realizado en nuestro medio13, se implementó un método recordatorio para maximizar la tasa de cumplimiento, alcanzando una tasa de curación del 91%; una desventaja fue la falta de un grupo control, por lo que no sabríamos si la tasa de respuestas con las gotas de sulfato ferroso sería tan alta bajo el mismo método recordatorio, que no se asemeja a las condiciones de la vida real y no refleja el impacto de un programa de salud en curso donde el tratamiento prescrito no es monitorizado estrictamente.
Después del tratamiento, hubo un porcentaje de niños que continuaron anémicos. Una posible explicación es la coexistencia de déficit de otros micronutrientes como la vitamina A; se ha demostrado que esta juega un rol importante en la movilización del hierro de reserva para el proceso de hematopoyesiss La mezcla del suplemento con alimentos ricos en inhibidores de la absorción del hierro pudo haber sido también otra causa.t En lugares donde la parasitosis intestinal es frecuente y la prevalencia de anemia es alta, la presencia de parásitos intestinales puede ser una causa importante de anemia; por tal motivo, se recomienda la administración de un antiparásitario junto con la suplementación de hierro y se ha demostrado que la respuesta es aún mayor con esta combinación.u,v
Pese al escaso monitoreo, una vez más queda demostrada la eficacia de los microgránulos.ll Ambos grupos presentaron un aumento significativo de los niveles de hemoglobina; sin embargo, el aumento fue mayor en el grupo experimental. Cuando las reservas de hierro están bajas, las células de la mucosa intestinal en un mecanismo de compensación y regulación, duplican el proceso de absorción, por lo que al mínimo de hierro ingerido, mínimo absorbido.w,x
El promedio de cumplimiento del tratamiento, también fue significativamente mayor en el grupo con fumarato ferroso (78%) que en el grupo control (55%); este dato se aproxima al obtenido en un estudio donde se evaluó la efectividad de la libre administración de los microgránulos en niños del área rural de Bangladeshy. Aunque el resultado obtenido por el presente estudio refleje un buen porcentaje de cumplimiento, este no alcanzó al 100% y es más, un 19% de los niños del grupo experimental, se encontraban entre los 6 y 7 meses de edad, de los cuales la mayoría recién se encontraba iniciando su alimentación complementaria, por lo que varios de los niños aún no recibían alimentación complementaria diariamente. Además, en ambos grupos el reporte de efectos colaterales fue similar dentro de estos, el estreñimiento y las deposiciones liquidas; debido a esto, varias madres admitieron haber suspendido el tratamiento por un par de días.
El reporte de problemas en el uso del suplemento fue significativamente mayor en el grupo control, El más frecuente, fue el hecho que el niño se rehusaba a ingerir el alimento. En el tratamiento experimental, el hierro se encuentra encapsulado, esto para evitar su oxidación al contacto con alimentos y así camuflar su sabor metálico, una de las principales recomendaciones para el uso de los microgránulos fue mezclarlos en alimentos espesos y relativamente tibios para evitar la dilución del hierro. Pese a estas recomendaciones, varias madres admitieron haber usado la sopa como vehiculo de los microgránulos. Por tal motivo, se reportó en un 33% cambio en el sabor de la comida, este problema disminuyó significativamente para el segundo monitoreo. Sin embargo, el reporte de problemas en el grupo control fue mayor por rechazo al sabor metálico. Si bien en el momento del primer monitoreo se redujo y se dividió la dosis a dos veces al día, el reporte de los problemas no cambió significativamente para la visita final.
Hubo un solo caso en que la madre se rehusó a continuar con el protocolo, ya que su niño presentó deposiciones liquidas persistentes después del consumo de los microgránulos. Según el reporte de otros estudios. En algunos niños de 6 a 7 meses, quienes no habían sido expuestos antes a alimentación complementaria, habrían presentado deposiciones liquidas, incluso diarrea moderada, limitándose a un par de días de evolución y sin deshidratación. No se tiene una seguridad del origen de las deposiciones líquidas, pero puede deberse al cambio de la flora intestinal asociada con la administración de hierro a la dieta, o posiblemente al efecto del acido ascórbico en el peristaltismo intestinal.z,aa,ab
En Tanzania, se concluye que la adherencia no solo está relacionada con los efectos colaterales, si no también al aspecto y su frecuencia de dosis.ac Varias madres encontraron más difícil el uso de las gotas ya sea a su aspecto, sabor o a que se dividió la dosis en el día. Hubo algunos problemas también en el uso de los microgránulos; probablemente por ser un tratamiento nuevo y estaba siendo mal administrado, pero al final la mayoría de las mamás admitieron que el uso del nuevo suplemento era más fácil.
La implicación clínica de esto nos señala, que la implementación de la nueva intervención logró reducir la prevalencia de la anemia en más del 30%, es decir, que de cada 3 niños tratados con microgránulos por lo menos uno aumentaría sus niveles de hemoglobina, hecho que no sucedería con el suplemento convencional.
Gracias a una mejor adherencia a los microgránulos de fumarato ferroso, estos pueden ser un tratamiento tanto eficaz como efectivos los beneficios obtenidos por este, son mucho mayores que el suplemento convencional. Para tener una idea global de la adherencia al tratamiento bajo la influencia de otros factores como zonas endémicas de malaria, o estados socioeconómicos más altos y diferentes grupos etarios; futuros estudios comunitarios son necesarios.
Al Programa Nacional de Nutrición, Servicio Departamental de Salud, Micronutriente Initiative, Universidad Mayor de San Andrés-Facultad de Medicina Unidad de Postgrado y a todo el personal de los tres centros de salud.
Referencias
a WHO/UNICEF/UNU, ed. Iron deficiency anemia, assessment, prevention and control: a guide for programme managers. WHO/NHD/01.3. Geneva: WHO, 2001. [ Links ]
b UNICEF/WHO, ed. Prevention and Control of Iron Deficiency Anaemia in Women and Children: Report of the UNICEF/WHO Regional Consultation. UNICEF/WHO Geneva 1999. [ Links ]
c Grantham-McGregor S, Ani C. A review of studies on the effect of iron deficiency on cognitive development in children. J Nutr 2001; 131:5649-68. [ Links ]
d Pollitt E. Iron deficiency and cognitive function. Ann Rev Nutr 1993;13:521-37. [ Links ]
e Lozoff B, Jimenez MD, Hagen J, Mollen E, Wolf AW. Poorer behavioral and developmental outcome more than 10 years after treatment for iron deficiency in infancy. Pediatrics 2000;105:E51. [ Links ]
f Grantham-McGregor S, Ani C. A review of studies on the effect of iron deficiency on cognitive development. PLoS Med 2005 2(1): e1. [ Links ]
g Nestel P, Alnwick D. Iron/multi-micronutrient supplements for young children. Summary and conclusions of consultation held at UNICEF, Copenhagen. Washington, DC: International Life Sciences Institute, 1997. [ Links ]
h INACG. Efficacy and effectiveness of interventions to control iron deficiency and iron deficiency anemia. International Nutritional Anemia Consultative Group. Washington, DC: International Life Sciences Institute, 2004. [ Links ]
i Galloway R, McGuire J. Determinants of compliance with iron supplementation: supplies, side effects, or psychology? Soc Sci Med 1994;39:381-90. [ Links ]
j Schauer C, Zlotkin S. Home fortification with micronutrient sprinkles-a new approach for the prevention and treatment of nutritional anemias. Paediatr Child Health 2003;8:87- 90. [ Links ]
k Zlotkin SH, Christofides AL, Hyder SM, Schauer CS, Tondeur MC, Sharieff W. Controlling iron deficiency anemia through the use of home-fortified complementary foods. Indian J Pediatr 2004; 71(11):1015-19. [ Links ]
l Dirren H, Logman MHGM, Barclay DV, Freire WB. Altitude correction for hemoglobin. Eur J Clin Nutr 1994;48:625–32.
m Cataudella J, Castagna L, Zlotkin S. Microencapsulated Ferrous Fumarate Sprinkles in the Treatment of Iron Deficiency Anaemia in Infants and Young Children in Bolivia. (Tesis de Grado) Mayo 2003. [ Links ]
n Lazcano P.E, Salaz. M, Guitierrez.C, Anglés A, Hernandez A. Viramonetes JL. Ensayos clínicos alaeatorizados: variantes, métodos de aleatorización. Análisis, consideraciones éticas y regulación. Sal Pub de Mex 2004: 46:559-84. [ Links ]
o Bangsberg DR, Hecht FM, Clague H, Charlebois ED, Ciccarone Chesney M. Provider assessment of adherence to HIV antiretroviral therapy. J Acquir Immune Defic Syndr 2001;26:435-42. [ Links ]
p Yadrick M, Kenny M, Winterfeldt E. Iron, copper, and zinc status: response to supplementation with zinc or zinc and iron in adult females. Am J Clin Nutr 1989; 49:145-50. [ Links ]
q Freire WB. Hemoglobin as a predictor of response to iron therapy and its use in screening and prevalence estimates. Am J. Clin Nutr 1989; 50: 1442-9. [ Links ]
r Zlotkin SH, Arthur P, Antwi KY, Yeung G. Treatment of anemia with microencapsulated ferrous fumarate plus ascorbic acid supplied as sprinkles’ to complementary (weaning) foods. Am J Clin Nutr 2001; 74:791–95.
s Suharno D, West C, Muhila L, Karyadi D, Hautvast J. Supplementation with vitamin A and iron for nutritional anaemia in pregnant women in West Java, Indonesia. Lancet 1993; 342:1325-8. [ Links ]
t Claire F M, Swiss Federal Institute of Technology Zurich: Optimizing the absorption of fortification iron (Tesis doctoral). Diss ETH No. 15113; 2009. [ Links ]
u Stoltzfus, R. J., Kvalsvig, J. D., Chwaya, H. M., Montresor, A., Albonico, M., Tielsch, J. M., Savioli, L. & Pollitt, E. Effects of iron supplementation and anthelmintic treatment on motor and language development of preschool children in Zanzibar: double blind, placebo controlled study. Br. Med. J.2001; 323:1389-93. [ Links ]
v INACG. Efficacy and effectiveness of interventions to control iron deficiency and iron deficiency anemia. International Nutritional Anemia Consultative Group. Washington, DC: International Life Sciences Institute, 2004. [ Links ]
w Charlton R, Bothwell T. Iron absorption. Ann Rev Med 1993; 34:55-68. [ Links ]
x Allen, L. H., Rosado, J. L., Casterline, J. E., Lopez, P., Munoz, E. & Martinez, H. Lack of hemoglobin response to iron supplementation in anemic Mexican preschoolers with multiple micronutrient deficiencies. Am J Clin Nutr 2000; 7:1485-94. [ Links ]
y Hospital for Sick Children Scientific Retreat. The effectiveness of fl exible administration of sprinkles in anemic and non anemic infants and young children in rural Bangladesh. 2004 [ Links ]
z Zlotkin S, Antwi KY, Schauer C, Yeung G. Use of microencapsulated iron (II) fumarato sprinkles to prevent recurrence of anemia in infants and young children at high risk. Bulletin of World Health Organization 2003; 81:108-15 [ Links ]
aa Zlotkin S, Christofides A, Schauer C, Asante KP, Owusu-Agyei S. Home fortification using sprinkles containing 12.5 mg of iron successfully treats anemia in Ghanaian infants and young children. FASEB J 2004;343-52. [ Links ]
ab Sprinkles Global Health Initiative. It has been noted that some infants develop a change in their stool consistency (loose stool or constipation) and colour when they start taking Sprinkles. Why does this happen? Is it of any significance? Disponible en: http://www.supplefer.com/about_sprinkles/faqs.html [ Links ]
ac Charlote E, Ekstrom M, Kavishe F, Habicht JP, Frongillo E, Rasmussen K, Hemed L. Adherence to iron supplementation during pregnancy in Tanzania: determinants and hematologic consequences. Am J Clin Nutr 1996; 64:368-74. [ Links ]