Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Boliviana de Pediatría
versión On-line ISSN 1024-0675
Rev. bol. ped. v.42 n.3 La Paz ago. 2003
ARTICULOS DEL CONO SUR - CHILE
Evolución neurosensorial en recién nacidos de muy bajo peso de nacimiento a los 2 años de edad corregida
Neurosensory evaluation of very low birth weight babies at a corrected age of 2 years
Drs.: Angélica Alegría O.*, Enrica Pittaluga P.*, Patricia Mena N.*, Luis Schlack P. ***, Marcelo Díaz M.****, María Vergara S.**, Ivonne D'apremont O.*, Elisa Jiménez A.*.
* Médico. Unidad de Neonatologa, Hospital Sotero del Ro.
** Psicloga, Hospital Stero del Ro.
*** Médico. Unidad de Neurologa Infantil, Hospital Stero del Ro.
**** Fonoaudiologo, Hospital Stero del Ro.
(1) Artículo original de Chile. Publicado en la Revista de la Sociedad Chilena de Pediatria 2002; 73(4): 348-56 y que fue seleccionado para su reproducción en la VIII Reunión de Editores de Revistas Pediátricas del Cono Sur. Brasil 2003
Resumen
Objetivo: El propósito de nuestro estudio fue conocer el déficit neurosensorial a los 2 años de edad corregida (EC) en niños con antecedentes de muy bajo peso de nacimiento (MBPN) en control en el policlínico de seguimiento del Servicio de Recién Nacidos del Hospital Dr. Sótero del Río, Santiago, Chile.
Método y participantes: 254 RN de 268 sobrevivientes de un total de 424 RNMBPN nacidos entre 1994 a 1996 fueron seguidos prospectivamente por un equipo multidisciplinario, que realiza evaluación clínica, neurológica, auditiva y psicomotora. Del grupo en seguimiento: 181 niños, que representa el 71% del grupo, completan adecuadamente los controles.
Resultados: Treinta y dos por ciento (59/181) de los niños tiene una evaluación neurosensorial anormal a los 24 meses de EC; 13% (24/181) presenta anormalidad neurosensorial severa: 6,6% (12/181) parálisis cerebral, 6% coeficiente del desarrollo mental menor de 70,3% sordera neurosensorial severa bilateral y 1 presentó ceguera. La mitad de los niños con parálisis cerebral presentan además otra secuela severa. Los factores asociados significativamente con evolución neurosensorial anormal fueron peso de nacimiento menor de 1 000 g, hemorragia intraventricular grados 3 y 4, convulsiones, apneas y ductus. En análisis de regresión logística, la apnea fue significativa e independientemente asociada a evolución neurosensorial anormal.
Palabras Claves:
Rev Chil Pediatr 2002; 73(4): 348-56: RNMBPN, pretérmino, seguimiento, neurosensorial, parálisis cerebral, factores prenatales y postnatales).
Summary
Objective: to report the neurosensory disabilities at an corrected age (CA) of 24 months of very low birth weight (VLBW) babies born between 1994 and 1996 in the Neonatal Unit of the Sótero del Río Hospital, Chile.
Patients and methods: 254 infants of 268 survivors (95%) from a total of 424 VLBW babies were prospectively followed-up with clinical, neurological, sensory and psychomotor evaluations. 181 children (71%) have completed the 2 year study.
Results: 32% (59/181) had an abnormal neurological examination at 24 months, 13% (24/181) had severe disabilities, 6.6% (12/181) cerebral palsy, 6% had a Bayley Mental Developmental Index of less than 70, 3% had severe neurosensory impairment and 1 was blind. About half of the children with cerebral palsy had another disability. Risk factors for severe deficits included a birth weight of less than 1 000gm, intraventricular haemorrhage grade 3-4, seizures, apnoea and a patent ductus. Using a multiple logistic regression analysis to adjust for neurological outcome, apnoea was a high risk factor.
Key words:
Rev Chil Pediatr 2002; 73(4): 348-56: VLBW, follow-up, neurosensory, cerebral palsy, pre and postnatal factors).
Introducción
La mortalidad del recién nacido de muy bajo peso de nacimiento (RNMBPN) ha disminuido en los últimos años, gracias a los avances del cuidado intensivo neonatal, la ampliación del uso de corticoides prenatal y el uso postnatal de surfactante(1,2). Con una mayor sobrevida, los estudios se han dirigido a evaluar la morbilidad neonatal y sus consecuencias. Las llamadas morbilidades mayores que se describen en este grupo de RNMBPN y que afectan el desarrollo posterior son: daño hipoxico o hemorrágico cerebral severo, retinopatía del prematuro, displasia broncopulmonar, infecciones nosocomiales y enterocolitis necrosante. Los problemas postnatales derivados son múltiples: en el ámbito de crecimiento y desarrollo se consideran anormalidades neurológicas mayores a la presentación de parálisis cerebral, ceguera uni o bilateral, sordera y coeficiente del desarrollo menor a 70. El mayor número de niños que sobreviven, cada vez con menor edad gestacional, puede aumentar el riesgo de secuela pulmonar, neurológica, cognitiva y/o sensorial. Además de disminuir la mortalidad es importante conocer las secuelas y los factores asociados de manera de modificar las prácticas clínicas de riesgo e iniciar un tratamiento precoz para minimizar los efectos secundarios de las secuelas. En la experiencia internacional el aumento en la sobrevida no se ha acompañado de un incremento en la incidencia de morbilidad médica y la tasa de parálisis cerebral permanece estable aunque el número absoluto de niños con parálisis cerebral ha aumentado debido al aumento de niños sobrevivientes(3-5).
Los pacientes que tienen más secuelas del período neonatal se rehospitalizan con mayor frecuencia en servicios de pediatría y son controlados por múltiples especialidades pediátricas, lo cual induce a pensar que la sobrevida del RNMBPN esté altamente asociada a secuelas y compromiso neurosensorial posterior.
Con el objetivo de pesquisar precozmente alteraciones neurológicas, sensoriales y describir los factores de riesgo asociado, se realizó un estudio de seguimiento, prospectivo y protocolizado en la población de RNMBPN egresado vivos de la Unidad de Neonatología del Hospital Dr. Sótero del Río entre los años 1994-1996.
Material y Método
Los RNMBPN nacidos entre los años 1994-1996, egresados vivos del hospital Dr. Sótero del Río e ingresados a seguimiento, fueron controlados siguiendo un calendario de citaciones preestablecido por un equipo de profesionales multidisciplinario.
Para todas las evaluaciones se estimó la edad corregida (EC) calculadas con: edad postnatal real en semanas _ (40 - edad gestacional). La edad gestacional se determinó por ecografía precoz, y en ausencia de ésta con la fecha de última regla, confirmada con la evaluación de Ballard modificado(6).
El control clínico por neonatólogo fue mensual hasta los 6 meses, bimensual de 6 a 12 meses, trimestral desde los 12 a 24 meses de edad corregida (EC). En cada control se evaluó antropometría, estado nutricional, estado general, morbilidad; se entregó indicaciones de alimentación, estimulación y tratamiento.
El control por neurólogo se realizó a las 40 semanas, a los 3, 8, 14, 24 meses de EC según pauta preestablecida basada en Dubowitz(7) y Amiel Tyson(8), clasificando el examen en normal o anormal. Las anormalidades fueron clasificadas como: alteración del tono, síndrome convulsivo, síndrome piramidal y parálisis cerebral.
El otorrinolaringólogo realizó otomicroscopía e impedanciometría previo a los potenciales evocado auditivo (PEA) efectuados a los 6 meses de EC. El PEA anormal, fue repetido en un plazo cercano a los dos meses.
El control fonoaudiológico se realizó a los 4, 10, 18 y 24 meses con escala Early Language Milestone, que evalúa el lenguaje en tres áreas: expresiva, comprensiva y visual(9). Se consideró retraso del lenguaje si el puntaje global estaba bajo el percentil(5).
El desarrollo psicomotor se evaluó por enfermera a los 6, 12, 18, 24 meses de EC, aplicando la escala de Evaluación de Soledad Rodríguez de 0-24 meses, validada para RNMBPN(10).
La psicóloga aplicó el test de desarrollo motor y mental de Bayley II a los 12 y 24 meses de EC(11).
El oftalmólogo evaluó con fondo de ojo a las 4-6 semanas de vida y 40 semanas de EC, la frecuencia de los controles entre ambas fechas dependió del grado de retinopatía diagnosticado según clasificación internacional de retinopatía del prematuro(12).
En base a estas evaluaciones de desarrollo cada niño se clasificó como:
Normal: ausencia de compromiso motor, de alteración visual y/o auditiva, coeficiente del desarrollo según Bayley mayor de 85.
Anormal moderado: presencia de uno o más de los siguientes criterios: coeficiente de desarrollo mayor de 70 y menor de 85, alteración auditiva unilateral, retraso del lenguaje, síndrome convulsivo, alteración del tono sin parálisis cerebral.
Anormal severo: presencia de uno de los siguientes criterios: coeficiente de desarrollo menor de 70, ceguera, sordera bilateral y parálisis cerebral.
La evolución a los 2 años EC se relacionó con los antecedentes prenatales y los diagnósticos del periodo neonatal. Entre los factores prenatales se consideraron los antecedentes de: síndrome hipertensivo, colestasia intrahepática del embarazo, infección ovular, uso prenatal de corticoides y ruptura prematura de membranas.
Entre los factores postnatales se analizó el test de Apgar a los 5 minutos (mayor o menor a 3), sexo, edad gestacional (mayor o menor a 30 semanas), peso de nacimiento, días de hospitalización, días de ventilación mecánica, presencia de displasia broncopulmonar (DBP: definida como cambios radiológicos pulmonares y dependencia de oxígeno a las 36 semanas de EC), ductus arterioso permeable, infección connatal, apnea significativa (apnea que requiere estimulación para recuperarse o traslado a UCI), hemorragia intraventricular según clasificación de Papile(13) y síndrome convulsivo.
Toda la información obtenida fue traspasada a una base de datos. El análisis estadístico comparó los datos con el test de X2, análisis univariado y de regresión logística.
Resultados
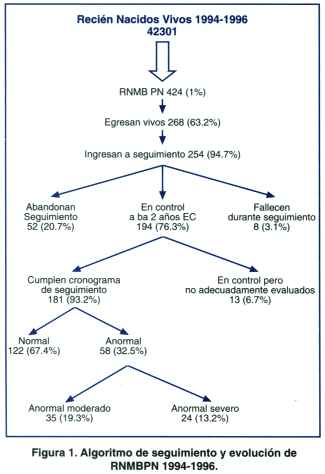
Entre 1994 y 1996 nacieron en el hospital Dr. Sótero del Río 43 302 recién nacidos, de ellos el 1% (424 niños) correspondió a RNMBPN. La tasa mortalidad especifica del MBPN fue de 36,8%, egresando vivos 268 niños y se ingresaron 254 al programa de seguimiento. El 76,3% de los niños completó el seguimiento a los dos años, de los cuales se excluyeron 13 (6,7%), por no cumplir con la evaluación programada. Se obtuvo un diagnostico neurosensorial en 181 niños, que constituyeron el 67,8% de los egresados vivos. En la figura 1 se describe un algoritmo de seguimiento y evolución.
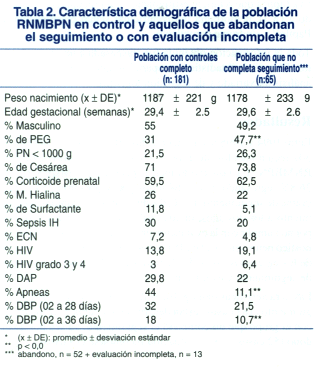
Las características demográficas del grupo que completó el seguimiento (181 casos) están descritas en la tabla 1, comparadas con el grupo que no completó el seguimiento, ya sea por abandono (52 casos) o por evaluación incompleta (13 casos).
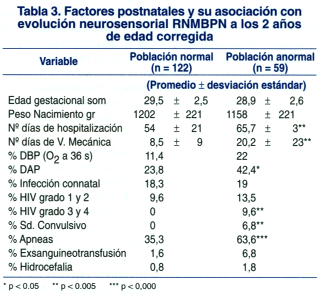
En la tabla 2 se describen los antecedentes de los niños clasificados como normales y los anormales a los dos años.
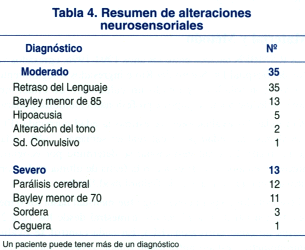
En la tabla 3 se describen los diagnósticos según severidad. El 50% de los niños con parálisis cerebral presentaron otra secuela asociada: 3 tienen un coeficiente de desarrollo bajo 70, un niño sordera, uno ceguera y uno síndrome convulsivo.
El diagnostico de parálisis cerebral se presentó en el 6,6% de los pacientes en seguimiento, en 7 casos como displejia espástica, 2 con tetraplejia, 2 con hemiparesia y uno con hemiplejia.
Se analizó como variaba el examen neurológico en el transcurso del tiempo, el 72% de los niños considerados normales al año, es igualmente considerado normal a los 2 años de edad corregida, pero 25% de los niños considerados normales cambian a anormal moderado debido a retraso del lenguaje. Siete pacientes catalogados con alteración del tono muscular en el primer año, en evaluación por el equipo multidisciplinario son considerados normales a los 2 años de EC.
Los casos de parálisis cerebral fueron todos confirmados a los dos años y tenían diagnóstico de alteración del tono entre las 40 semanas y los 8 meses de EC.
El 90,6% de los pacientes evaluados hasta los 2 años de EC tenían fondo de ojo realizado en el período intrahospitalario. Este fue normal en 82,9% (136 niños) y anormal en 17% (28 niños), con retinopatía grado I en 15 casos, retinopatía grado II en 12 y 1 niño con retinopatía grado III.
A todos los niños se les realizó evaluación fonoaudiológica. En 37 niños se realizó potenciales auditivos evocados (PEA), 3 de ellos presentaron sordera neurosensorial (1,7% del grupo en seguimiento) y en 14 se confirmo hipoacusia de causa mixta: central y periférica.
El análisis de correlación entre los factores prenatales estudiados y la evolución neurosensorial anormal a los 2 años, no mostró ninguna asociación significativa. El análisis de los factores postnatales mostró asociación significativa entre la evolución neurosensorial anormal a los 2 años EC y peso de nacimiento menor a 1 000 g, mayor número de días de hospitalización, mayor número de días de ventilación mecánica, mayor % de ductus arterioso persistente, hemorragia intracraneana grado III y IV, apneas y síndrome convulsivo (tabla 2).
El grupo que finalizó el estudio presentó mayor porcentaje de apneas y dependencia de oxígeno a las 36 semanas de edad corregida al comparar con el grupo que abandona seguimiento o no son suficientemente evaluados.
Al realizar el análisis de regresión logística se encontró que la probabilidad de examen neurosensorial anormal a los 2 años de EC está asociada en forma significativa e independiente solamente con apnea, OR: 3,21 (1,57 < OR < 6,6).
Discusión
La primera dificultad en los estudios de seguimiento es mantener la adhesividad al programa, en nuestro caso, pese a citaciones repetidas un quinto de los pacientes que ingresan al seguimiento dejan de asistir en un plazo de 2 años. Los niños que abandonan el seguimiento pueden estar menos o mas afectados, pero los datos demográficos muestran que los niños no evaluados tienen menos factores de riesgo para las alteraciones neurosensoriales analizadas: menor incidencia de apneas, menor incidencia de DBP (tabla 1). En esta población, de bajo nivel socioeconómico, los pacientes no tienen acceso a otra forma de atención y la actividad del seguimiento es realizada con un enfoque de médico tratante integral, por lo cual los pacientes inasistentes tienden a tener menos problemas. Aún así, si suponemos el peor de los casos, que los que abandonan el seguimiento y los que no están completamente evaluados están todos afectados, encontramos un 49,5% de los egresados vivos con una evaluación considerada normal a los dos años. Si bien la evaluación a los 2 años es precoz, no detecta alteraciones de aprendizaje, déficit atencional o problemas conductuales, hay un buen diagnóstico de los trastornos neurológicos motores y problemas sensoriales mayores.
La parálisis cerebral es una de las causas mas comunes de discapacidad grave en la niñez. Este síndrome, no progresivo, de discapacidad motora es 70 veces mas frecuente en los RNMBPN que en la población de niños de peso de nacimiento normal(14). Se ha descrito que la corioamnionitis clínica aumenta en 2,7 veces el riesgo de tener déficit neurológico y se ha asociado infección materna con parálisis cerebral, pero son estudios retrospectivos de poblaciones con parálisis cerebral(15-17). Por otro lado, habría una importante relación entre infección intrauterina y enfermedad de la sustancia blanca, que incluye la leucomalacia periven-tricular y el ensanchamiento ventricular(18). La infección perinatal junto con otros factores de riesgo como desprendimiento de placenta, isquemia cerebral y la muerte de uno de los gemelos, podría desencadenar una cascada inflamatoria de citokinas que pueden determinar daño en un cerebro que se está desarrollando(19,20). Se ha postulado una predisposición genética a la coexistencia de respuesta inflamatoria y su asociación a parálisis cerebral(21). En general los estudios de seguimiento coinciden en que la frecuencia de parálisis cerebral aumenta a menor edad gestacional y menor peso de nacimiento(22). La incidencia de parálisis cerebral representa 6,6% de los pacientes en seguimiento. La cifra es similar a otras series clínicas(23,24). Hack en un seguimiento de RNMBPN en edad escolar, describe 9% de parálisis cerebral para menor de 750 g y 6% para el grupo de 750-1 499 g de peso al nacer(25).
El seguimiento oftalmológico se limitó a los problemas de retina, registrándose un caso de ceguera en todo el grupo, no se evaluaron alteraciones de refracción y no se analizaron las alteraciones de convergencia que son frecuentes en este grupo de niños; Powls señala una incidencia de 9,5%-25% de estrabismo en RNMBPN, con una alta asociación con retinopatía del prematuro y 27% de miopía en niños que presentan el antecedente de RPP(26).
Para algunos autores la incidencia de sordera es hasta 15 veces mayor que en los RN de término. Se ha demostrado que mientras más tarde se haga el diagnostico y se retrase el tratamiento, más difícil es la adquisición del lenguaje(27). En nuestro grupo, la incidencia de sordera es casi 17 veces más que la descrita para RN de término. Si bien en sólo el 19% de los niños en control se realizó PEA, este examen se realizó en todo paciente en que se planteó alteración auditiva. La hipoacusia grave o profunda se ha asociado significativamente a la coexistencia de menor peso de nacimiento, presencia de hemorragia intracraneana, ventilación mecánica por más de 10 días, exposición agentes ototóxicos, hiperbilirrubi-nemia y sepsis(28-30). Las cifras internacionales describen una incidencia de 1-3 por cada 1 000 RNV, cifra que aumenta dramáticamente a 2-4% en los RN dados de alta de unidades de cuidados intensivos neonatales.
El grupo con retraso del lenguaje requiere mayor estudio y seguimiento para poder determinar si el retraso corresponde a un problema cognitivo o si depende de influencia ambiental.
Estudios de cuociente intelectual (CI) en niños de MBPN describen mayor incidencia de CI subnormal (CI 70-84) y deficiente (< 70) a menor peso de nacimiento: 8-13% de los menores de 1 000 g y 20% de los menores de 750 g tienen inteligencia subnormal25. Nosotros no evaluamos coeficiente intelectual, sólo coeficiente de desarrollo a los 2 años y encontramos 6% (11 niños) con coeficiente de desarrollo menor de 70.
La mayoría de los factores postnatales que se encontraron asociados a evolución neurosensorial anormal, están descritos en otros estudios de seguimiento. La hemorragia intraventricular grado III y IV están claramente asociada a evolución neurológica anormal(11,17,31,32). La DBP se ha asociado a alteraciones del neurológicas, además de alteraciones cognitivas y motoras(32,33). En nuestro estudio, la incidencia global de DBP fue de 32% considerando criterio de requerimiento de oxígeno a los 28 días y de 18% con criterio de oxígeno a las 36 semanas de EC. El grupo con examen neurológico anormal presentó el doble de incidencia de DBP (usando criterio de oxígeno a las 36 semanas), 22% vs 11,4% del grupo con evolución normal pero esta diferencia no es estadísticamente significativa.
La asociación de apneas con compromiso neurológico ha sido reportada en algunos estudios. Dos mecanismos para esta asociación pueden citarse: uno es que la apnea con bradicardia prolongada produce hipoperfusión y daño hipoxico-isquémico cerebral; la otra posibilidad es que la apnea está reflejando una mayor inmadurez del SNC, como lo muestra la menor velocidad de conducción del tronco cerebral por menor mielinización en niños con apneas. La presencia de apneas sería un marcador de inmadurez y de mayor vulnerabilidad frente a las diferentes noxas del período perinatal(34-37).
En Chile nacen alrededor de 280 000 niños al año, de los cuales entre el 0,8 y 0,9% es menor de 1 500 g, si aplicamos una sobrevida de 60%, egresarían vivos 1 473 niños. Según nuestros datos se puede estimar alrededor de 100 niños con parálisis cerebral y 25 niños con sordera cada año en el país, asociado a MBPN, que requieren un programa de diagnóstico y rehabilitación precoz.
La mantención de programas de seguimiento con alta adherencia y los recursos para recuperar la información de la evolución, el desarrollo de redes de información y análisis centralizado como el actual programa de Seguimiento del Ministerio de Salud y la relación con los eventos perinatales es fundamental para el avance de las prácticas clínicas neonatológicas y la mejoría de la calidad de la sobrevida al mediano plazo.
Agradecimientos
A Sr. Luis Villarroel del P., M Sc. Estadística. Instructor Asociado Salud Pública Universidad Católica de Chile quien colaboró en los análisis estadísticos; Dra. Iturra, Oftalmóloga del Hospital; Dr. Andrés Rosenblut, Otorrinolaringólogo del Hospital; Médicos del Servicio de Neonatología y Neurología del Hospital Sótero del Río; Médicos y tecnólogos del Instituto de Rehabilitación Infantil de Santiago, quienes realizaron los potenciales evocados auditivos.
Referencias
1. Long W, Coorbert A, Cotton R, et al: A controlled trial of synthetic surfactant in infants weighting 1250 o more with respiratory distress syndrome. The American Exosurf neonatal Study Group 1 and Canadian Exosurf neonatal Study. N Engl J Med 1991; 325: 1696-703. [ Links ]
2. Collaborative European Multicenter Study group: Surfactant replacement therapy for severe neonatal respiratory distress syndrome: An international randomized clinical trial. Pediatrics 1988; 82: 683-91. [ Links ]
3. Hack M: Follow-up for high risk neonatal. En Neonatal-Perinatal Medicine Diseases of the Fetus and Infant, Fanaroff Avroy., Martin Richard. editores. Sixth Edition. Vol 2, Chapter 38: 952-7. [ Links ]
4. O'Shea T, Preisser J, Klinepeter K: Trends in mortality and Cerebral Palsy in a Geographically based cohort of very low birth weight neonates born between 1982 to 1994. Pediatrics 1998; 101: 642-7. [ Links ]
5. Stevenson D, Wright L: Very low birth weight outcomes of the National Institute of Child Health and Human Development Neonatal Research network, January 1993 through December 1994. Am J Obstet Gynecol 1998; 179: 1632-9. [ Links ]
6. Ballard JL, Khoury JC, Wedig K et al: New Ballard Score, expanded to include extremely premature infants. J Pediatr 1991; 119: 417-23. [ Links ]
7. Dubowitz L, Dubowitz V, Goldberg C: Clinical assesment of gestational age in the newborn infants. J Pediatr 1970; 77:1. [ Links ]
8. Amiel-Tison C, Grenier A: Valoración neurológica del recién nacido y del lactante, diciembre 1981, 1 edición español Toray-Masson Barcelona. [ Links ]
9. Caplan J, Gleason JR: Quantifyng language development from birth to 3 years using the early language milestone scale Pediatrics 1990; 86 (6): 955-62. [ Links ]
10. Rodríguez S, Arancibia V, Undurraga C: Escala de evaluación del desarrollo psicomotor: 0-24 meses, 1986, 3ª Edición, Santiago Chile. [ Links ]
11. Bayley N: Bayley Scales of Infant Development 1993, 2nd ed. San Antonio, Texas. Psychological Corporation, 1993. [ Links ]
12. An international classification of retinopathy of pre-maturity. Pediatrics 1984; 74: 127-33. [ Links ]
13. Papile A, Burstein J, Burstein R: Incidence and evolution of subependimal and intraventricular hemorrhage. J Pediatr 1978; 92: 529-34. [ Links ]
14. Cummins SK, Nelson KB, Grether JK: Cerebral palsy in four northen California counties, births 1983 through 1985. J Pediatr 1993; 123: 230-7. [ Links ]
15. Dammann O, Allred EN, Veelken N: Increased risk of spastic diplegia among very low birth weight children after preterm labor or prelabor rupture of membrane. J Pediatr 1998; 132: 531-5. [ Links ]
16. Nelson KB, Ellenberg JH: Predictors of low and very low birth weight and relation of these to cerebral palsy. JAMA 1985; 254: 1473-9. [ Links ]
17. Leonard CH, Clyman R, Piecuch R: Effect of medical and social risk factors on outcome of prematurity and very low birth weight. J Pediatr 1990, 116: 620-6. [ Links ]
18. Dammann O, Levinton A: Maternal intrauterine infection, cytokines and brain damage in the preterm newborn. Pediatr Res 1997; 42: 1-8. [ Links ]
19. G_mez R, Romero R, Edwin SS: Pathogenesis of preterm labor and preterm premature rupture of membranes associated with intraamniotic infection. Infect Dis Clin North Am 1997; 11: 135-76. [ Links ]
20. O'Shea M, Damman O: Antecedents of cerebral palsy in very low-birth weight infants. Clin Perinatol 2000; 27: 285-301. [ Links ]
21. Damman O, Durum SK, Levinton A: Modification of the infection-associated risks of preterm birth and white matter damage in the preterm newborn by polymorphisms in the tumor necrosis factor-locus?. Pathogenesis 1998; 2: 1-7. [ Links ]
22. Hack M, Klein N, Taylor H: Long-term develop-mental outcomes of low birth weight infants. Packard Foundation publication: The Future of Children 1995; 5: 176. [ Links ]
23. Sommerfelt-K: Long term outcome for non handi-capped low birth weight infants. Eur J Pediatric 1998; 657: 1-3. [ Links ]
24. Fernández Carrocera LA, Pe_uela Olaya MA: Crecimiento y alteraciones del neurodesarrollo en el recién nacido de alto riesgo. Academia Mexicana de Pediatría A.C. Libro 1999; 1. [ Links ]
25. Hack M, Taylor HG, Klein N: School-age outcomes in children with birth weights under 750 g. N Engl J Med 1994; 331: 753-9. [ Links ]
26. Powls A, Botting N, Cooke RW: Visual impairment in very low birthweight children. Arch Dis Child 1997; 76: 82-7. [ Links ]
27. Kennedy CR: The assessment of hearing and brainstem function. Eyre Ja. The neurophysiological examination of the newborn infant. London: Mac Keith Press 1992; 79-92.
28. Garza S, Poblano A, Robledo G: Potenciales provocados auditivos en ni_os con riesgo neonatal de hipoacusia. Rev Panam Salud Pública 1997; 2: 119-24. [ Links ]
29. Bergman I, Hisch RP, Fria JL, Shapiro SM: Cause of hearing loss in the high risk premature infant. J Pediatr 1985; 106: 95-101. [ Links ]
30. Arnold J, Radkowski D: Hearing loss in the newborn infant. In Neonatal-Perinatal Medicine Diseases of the Fetus and Infant. Fanaroff Avroy, Martin Richard editors. 6 Edition. Vol 2, Chapter 39: 958-63.
31. Allan WC, Vohr B, Makuch R: Antecedents of cerebral palsy in a multicenter trial of indomethacin for intraventricular hemorrage Arch Pediatr Adolesc Med 1997; 151: 580-5. [ Links ]
32. Barrera Reyes RH, Fernández Carrocera LA: Neurodesarrollo al año en pacientes con Displasia Brocopulmonar. Bol Med Hosp Infant Mex 1995; 52: 572-81. [ Links ]
33. Singer L, Yamashita T, Lilien L: A longitudinal study of developmental outcome of infants with broncho-pulmonary dysplasia and very low birth weight. Pediatrics 1997; 100: 987-93. [ Links ]
34. Koons AH, Mojica N, Jadeja N, et al: Neurodevelop-mental outcome of infants with apnea of prematurity. Am J Perinatol 1993; 10: 208-11. [ Links ]
35. Ramackers VT, Casaer P, Daniels H: Cerebral hyperperfusion following episodes of bradycardia in the preterm infant. Early Hum Develop 1993; 34: 199-208. [ Links ]
36. Perlman J: Neurobehavioral deficits in premature graduates of intensive care. Potential medical and neonatal environmental risk factors. Pediatrics 2001; 108: 1339-48. [ Links ]
37. Handerson-Smart DJ, Pettigrew AG, Cambell DJ: Clinical apnea and brain-stem neural function in preterm infants. N Engl J Med 1983; 308: 353-7. [ Links ]