En el año 1861, Walcott realiza por 1era vez una nefrectomia parcial, esta se realizó de manera accidental al realizar una cirugía de quistes hepáticos. Simon realiza otro caso en 1869 en un intento de tratamiento de una fístula urinaria. Czerny 1887, fue el primero en realizar una nefrectomia parcial con la intención de curar un tumor de riñón1-7.
Vermooten 1950, define la nefrectomia parcial moderna para el tratamiento de tumores renales. En 1981 se inició la era actual de la nefrectomia parcial para el tratamiento de lesiones tumorales de riñón. Las indicaciones para una nefrectomia parcial se dividen en tres categorías: indicaciones absolutas, indicaciones relativas y las electivas8-11. Las indicaciones absolutas; tumor en riñón único, tumores en ambos riñones y tumores renales en pacientes con insuficiencia renal. Las indicaciones relativas: tumores renales y enfermedad benigna del otro riñón, enfermedades crónicas que predispongan a insuficiencia renal a largo plazo o tumores en síndromes genéticos de origen hereditario; las indicaciones electivas, tumores renales pequeños, totalmente exofíticos sin otra enfermedad.
Se tienen escalas que nos pueden ayudar a predecir la complejidad y dificultad del manejo de estos tumores, entre los que tenemos los puntajes de nefrometría que más se utilizan, RENAL (Radio, Exofítico / Endofítico, proximidad al sistema colector, anterior-posterior y localización en relación con los polos del riñón; aspectos preoperatorios y tamaños utilizados para la clasificación anatómica [PADUA]; índice de centralidad) que está basado en las características de las imágenes preoperatorias han sido implementados para definir la complejidad quirúrgica10. La puntuación RENAL es la mayormente utilizada, teniendo como parámetros de puntaje: bajo riesgo 4 - 6, riesgo intermedio 7 - 9, alto riesgo 10 - 12 puntos.
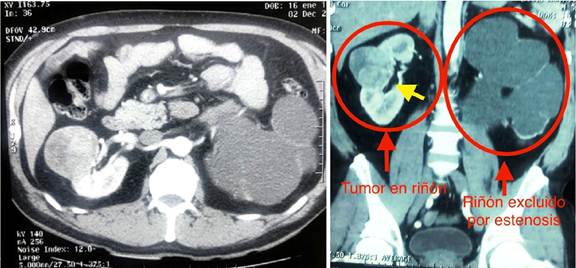
Figura 1. Urotomografia contrastada: se observa riñón izquierdo excluido, con perdida total de su función, con riñón derecho con tumor de 10 x 8 cm de diámetro
Presentamos el caso de paciente con indicación absoluta, con tumor de alta complejidad, RENAL 12xh (alta complejidad) resuelta por laparoscopia12,13,14.
Presentación del caso
Paciente masculino de 52 años de edad, acude a consulta por presentar eventos de hematuria macroscópica, formadora de coágulos filiformes, para lo cual acudió a varios centros de atención primaria, recibiendo tratamiento médico para infecciones de vías urinarias y crecimiento prostático obstructivo, sin mejoría, por lo que se derivó a consulta médica en nuestra unidad, realizándose estudios de gabinete, con ecografía de vías urinarias, documentando crecimiento prostático obstructivo grado III, hidronefrosis izquierda severa y tumor renal derecho, por lo que se decide realizar estudios complementarios, con hemograma, función renal, examen general de orina, urocultivo, documentando enfermedad renal crónica con creatinina de 1,8 mg/dl, urea 42 mg/dl, el resto de estudios dentro de parámetros normales, ameritando con estos resultados, preparación con hidratación y valoración por nefrología, para realizar una urotomografía contrastada, y determinar con este estudio la anatomía de las vías urinarias, el tamaño del tumor, localización y relación con otras estructuras, además de evaluar el riñón izquierdo que presentaba hidronefrosis en estudio previo (Figura 1).
Se documenta mediante tomografía contrastada trifásica, la presencia de tumor solido en riñón derecho dependiente del polo superior, de 10 x 8 cm de diámetro, con realce a la aplicación de contraste, con el riñón contralateral con hidronefrosis severa secundaria a probable estenosis ureteropielica izquierda, con pelvis renal con dilatación severa, con pérdida de la totalidad del parénquima renal, sin captación ni eliminación del medio de contraste, no se observa datos dilatación ureteral, ni ganglios retroperitoneales, la tomografía de tórax dentro de parámetros normales. Con lo que se concluye el diagnóstico de tumor renal derecho T2bN0M0, exclusión renal izquierda secundaria a estenosis ureteropiélica, enfermedad renal crónica KDIGO 3a y crecimiento prostático obstructivo.
Con estos resultados, de decide programar cirugía para extracción del tumor renal derecho, al ser el paciente monorreno, se tiene como mejor opción quirúrgica la nefrectomía parcial derecha laparoscópica, se hace el cálculo de dificultad técnica mediante la escala RENAL Score, obteniendo un puntaje de 10ah, lo que nos marca una cirugía de alta complejidad, con riesgo de tener la necesidad de realizar una nefrectomía radical por la alta complejidad del procedimiento, se comenta con el paciente y se decide proceder con la cirugía preservadora de nefronas mediante nefrectomía parcial por abordaje laparoscópico.
La cirugía se realizó en posición de Israel Bergman izquierda, colocación de sonda Foley 16 Fr, se procede a colocar tres trocares de trabajo: a nivel paraumbilical de 10 mm y otro de 10 mm a nivel de línea clavicular media a dos centrimetros de la cresta iliaca antero-superior, otro de 5 mm en línea media clavicular a nivel subcostal (Figura 2). Se liberan adherencias, se incide fascia de Told, se diseca y separa colon, se accede a retroperitoneo, se identificó el uréter y se disecó en sentido cefálico, se localizó hilio renal, el cual se diseco en su totalidad, con el objetivo de tener un buen control vascular en caso necesario, se procedió a disecar grasa perirrenal, se localiza tumor renal, se limpia borde del tumor, y se procede a incidir capsula renal a nivel del borde renal, con un margen de 1 cm del borde visible, se realizar corte de parénquima renal con energía bipolar, se procede a seccionar por completo el tumor, se realiza el procedimiento sin isquemia, (Figura 3) se cauteriza lecho quirúrgico, se procede a cierre de colectores con Vicryl 2-0, surgete continuo, en plano profundo, se coloca Gelfoam hemostático en lecho quirúrgico, y se afronta bordes de parénquima renal con crómico 1, se corrobora adecuada hemostasia, se procede a dejar drenaje en lecho, y se extrae pieza quirúrgica, se realiza el procedimiento sin complicaciones, con un sangrado estimado de 300 ml, se deja al paciente en reposo absoluto, y con control de la función renal, se observa ligera elevación de la creatinina a las 24 hrs, llegando a 2 mg/dL, sin necesitar apoyo dialítico, con posterior recuperación de la función renal a niveles basales a las 72 hrs de la cirugía.
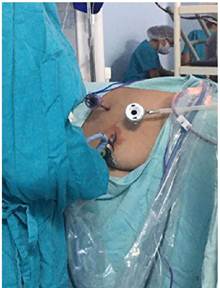
Figura 2. La imagen corresponde a la posiciòn del paciente y localizaciòn de los trocares de laparoscopia.
El resultado histopatológico reporta: carcinoma renal de células claras, grado nuclear Furhman 2, bordes quirúrgicos negativos que distan a 0,8 cm del borde tumoral, sin datos de extensión tumoral al tejido adiposo peritumoral. Tamaño del tumor 10 cm x 7 cm (Figura 4).
A los doce meses de seguimiento con tomografía de control, sin datos de recurrencia local, sin datos de actividad tumoral en el estudio de control, con función renal conservada, doce meses posteriores a la cirugía con creatinina 1.6 mg/dL, aun con controles y con adecuada evolución.
Discusión
La nefrectomía parcial por abordaje laparoscópico es una técnica que imita los pasos de la cirugía por abordaje abierto. En 1993, en animales McDougall et al,15 describe por 1era vez una nefrectomía parcial por abordaje laparoscópico. El mismo año, Fueron Wienfield et al16, realizan la 1era nefrectomía parcial por abordaje laparoscópico en humanos y en Cleveland Clinic realizan la primera nefrectomía parcial retroperitoneal además que se indica que la cirugía conservadora de nefronas está indicada de manera absoluta en pacientes monorrenos, con tumores bilaterales y pacientes con insuficiencia renal crónica17.
El número de diagnóstico de estas lesiones, se ha incrementado durante los últimos años, esto debido al mayor uso de imágenes radiológicas, muchas veces con el objetivo de estudio de otras patologías12.
El límite de tamaño de los tumores que se pueden tratar por laparoscopia, se ha ido incrementando de manera progresiva y directa con base en la experiencia adquirida de los cirujanos urólogos laparoscopistas, actualmente ideales hasta 7 cm de diámetro18,19. Por otro lado, en la actualidad, no existen contraindicaciones en cuanto a la localización de la lesión para su tratamiento con cirugía. El tipo de abordaje depende del criterio del urólogo y de la anatomía de la lesión14,20. En nuestro caso nosotros realizamos el cierre de los colectores con sutura con poliglactina u otro tipo de sutura de tipo absorbible, sintética, y entrelazada, para afrontar el parénquima usamos hilo catgut crómico 1, mediante puntos simples, previa colocación de un hemostático absorbible y con la aplicación de Gelfoam (Gelatina de Piel Porcina Purificada) en el lecho quirúrgico.
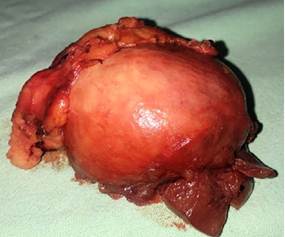
Figura 4. Pieza quirúrgica completa, con borde quirúrgico de parénquima renal sano, evidenciando extracción completa de tumor renal.
La reproductibilidad de los abordajes urológicos mediante laparoscopia se ha incrementado alrededor del mundo y prácticamente convirtiéndose en el estándar para el manejo de estas patologías. Estas cirugías permiten heridas pequeñas, una exposición quirúrgica amplificada todo esto permite reproducir los pasos de la cirugía por abordaje abierto, reduce sangrado, reduce el dolor y el tiempo de internamiento, además de una menor convalecencia postoperatoria y mejor resultado estético en el paciente.
Conclusión
La nefrectomía parcial es el manejo ideal para tumores renales pequeños que están localizados en la corteza renal y en los extremos polares del riñón o con un riñón contralateral sin función; pero tenemos el dilema cuando se presentan en pacientes con función renal baja o tumores localizados cerca del hilio renal de más > 5 cm se debe tomar los riesgo de intentar realizar este procedimiento, el abordaje por vía laparoscópica es excelente opción con excelentes resultados, con menor riesgo de complicaciones, y menor sangrado que cirugía abierta.