La infección causada por el nuevo coronavirus (Covid-19), denominada en un principio como novel coronavirus 2019 (2019 n Cov) y posteriormente Síndrome Agudo Respiratorio Severos 2 (SARS CoV-2), llegó a declararse una pandemia desde marzo de 2020 por la Organización Mundial de la Salud (OMS)1 El SARS CoV-2 en niños, mostró tasas de infección más bajas y cuadros clínicos menos severos1. En un estudio en 70 000 casos encontraron que menos del 1% eran pediátricos, menos severos y clínicamente distintos a los adultos, el año 2021 estudios posteriores realizados en la región Latinoamericana confirmaron la información previa, pero describieron formas más graves de COVID-19, donde cerca al 13 % de los pacientes ingresaron a la Unidad de Cuidados Intensivos Pediátricos por Infecciones Respiratorias Agudas Graves (IRAG) y Síndrome Inflamatorio Multisistémico Pediátrico (MIS-C), afectando principalmente a menores niveles socioeconómicos2.
Gran parte de la evidencia disponible sobre los cuadros graves por COVID-19, tanto en estudios observacionales como experimentales, provienen de población adulta3, a pesar de que los niños presentan manifestaciones y características diferentes4. Aunque los pacientes pediátricos no suelen presentar síndrome de dificultad respiratoria aguda (SDRA) y con menor frecuencia presentan neumonías. Existen datos que sugieren que la incidencia y gravedad van en aumento, principalmente en presencia de ciertos factores de riesgo como: neoplasias, cardiopatías, diabetes, inmunocompromiso, síndrome de Down asma severo y otros5. El diagnóstico molecular para virus respiratorios es rápido, sensible, específico y puede ser de utilidad en el manejo clínico oportuno de pacientes pediátricos con factores de riesgo o gravedad clínica, además se debe considerar el papel de los niños como portadores de la enfermedad, y su capacidad de transmitir a otras personas de su entorno6.
La edad pediátrica se caracteriza por la gran actividad y respuesta innata frente a agentes virales, ya sea por interacción con los virus vivos atenuados de las vacunas o con la interacción/competición de agentes virales comunes a esa edad6,7 esto permite mecanismos locales de control cruzado con otros virus en las barreras físicas (mucosa respiratoria), de esta manera se limita el crecimiento de SARS CoV-28, consiguientemente la gravedad de la enfermedad9. Existen virus como el rinovirus, virus sincitial respiratorio (VSR) y virus de la influenza (FLU), que son frecuentes en niños y podrían brindar protección cruzada frente a Covid-197 o por otra parte llegar a producir coinfección, principalmente en niños que pudiesen tener enfermedades de base 10.
Finalmente mencionar, que no se cuenta con datos acerca de la caracterización de otros virus respiratorios causantes de IRAG desde el inicio de la pandemia por Covid-19 en Bolivia y tampoco tras el desconfinamiento ante las medidas adoptadas en nuestro país, por lo que la información que aporta este estudio sobre la vigilancia epidemiológica a través de un diagnóstico diferencial en población hospitalizada, es de gran utilidad para mostrar la situación de las infecciones respiratorias agudas graves en medio de una pandemia, contribuyendo a fortalecer la toma de decisiones y optimizar los servicios de salud que se ofrecen a esta población en lo que respecta a un problema recurrente de morbilidad y mortalidad en el hospital pediátrico de referencia en Cochabamba.
El presente estudio tuvo como objetivo evaluar el comportamiento epidemiológico de SARS-CoV-2, VSR y FLU como responsables de infección respiratoria aguda grave en población internada en el Hospital del Niño Manuel Ascencio Villarroel del departamento de Cochabamba.
Materiales y métodos
Se realizó un estudio observacional, prospectivo, transversal. La población de estudio incluyó a 41 pacientes pediátricos que fueron internados con infección respiratoria aguda grave, sospechosa de etiología viral, en el Hospital Manuel Ascencio Villarroel, durante junio 2021 a junio 2022. Los criterios de inclusión fueron: menores de 5 años de edad, cuadro clínico compatible con Infección Respiratoria Aguda Grave (IRAG), de acuerdo a la definición de la OMS: fiebre o historia de fiebre, tos, dificultad para respirar y necesidad de hospitalización1. Dentro de los criterios de exclusión se encuentran los pacientes pediátricos mayores de 5 años de edad a la fecha de internación, que estuvieran bajo tratamiento antiviral en el momento de su internación, niños con agente etiológico previamente identificado o pacientes con datos clínicos de menor severidad a neumonía grave o de manejo ambulatorio.
Se realizó la recolección de muestras de secreciones respiratorias a través de aspirados nasofaríngeos tomadas por el personal médico del servicio de infectología del Hospital del Niño Manuel Ascencio Villarroel (HNMAV), bajo protocolo establecido, para que estas muestras puedan emplearse para la detección molecular de virus respiratorios en estudio: Virus SARS CoV-2, VSR, FLU A y B. Las muestras fueron conservadas a 4°C y trasladadas dentro de las 24 horas, al laboratorio de Biología Molecular de la Facultad de Cs. Farmacéuticas y Bioquímicas de la Universidad Mayor de San Simón (UMSS), para su procesamiento. Se realizó la extracción de ácidos nucleicos virales por el método de columna, empleando el kit de extracción comercial con N° de catálogo: 52906 correspondiente a QIAamp® VIRAL RNA MINI KIT de la línea Qiagen. Posteriormente, para la detección molecular por reacción en cadena de la polimerasa en tiempo real multiple (RT-qPCR) de los siguientes virus respiratorios: SARS CoV-2, VSR, FLU A y B, se empleó el kit comercial de la marca Seegene N° catalogo RV10259X : Allplex SARS CoV-2/FluA/FluB/RSV Assay, empleando un termociclador de la línea BIORAD CFX-96.
El kit comercial Allplex SARS CoV-2/FluA/FLuC/RSV Assay, es un ensayo de PCR en tiempo real múltiple que permite la amplificación y detección simultanea de ácidos nucleicos objetivo en los genes S, RdRP y N de SARS CoV-2, Virus de la influenza tipo A (Flu A), Virus de la influenza tipo B (Flu B) y Virus Sincitial Respiratorio (VSR) con dos controles internos (Endogeno IC y exogeno IC). Para realizar la detección y amplificación múltiple, brindando mayor exactitud en una sola reacción, este ensayo emplea las tecnologías patentadas DPO, TOCE y MuDT. La presencia de secuencias de genes específicos en la reacción se informa como un valor de Ct a través del software de análisis de Seegene Viewer, a través del cual se realizó la interpretación de resultados de las pruebas moleculares.
Para evitar que el producto de amplificación actúe como contaminante potencial, se utiliza el sistema Uracilo-ADN glicosilasa (UDG)-dUTP en el ensayo. El Sistema UDG- dUTP se utiliza a fin de eliminar los amplicones sobrantes usando escisiones por UDG de residuos de uracilo desde el ADN, mediante la escisión del enlace N-glicosílico.
Para el análisis de la población de estudio, se empleó la información disponible en las historias clínicas de los pacientes, también se usó como herramienta de recolección de datos la ficha epidemiológica frente a SARS CoV-2 /Covid-19, dispuesta por el Ministerio de Salud, Bolivia.
La ficha epidemiológica para SARS CoV-2 / Covid-19 incluye los siguientes aspectos:
Datos clínicos: sintomático o asintomático, presencia de tos seca, dolor de garganta, fiebre, dificultad respiratoria, mialgias, malestar general, cefalea, perdida y/o disminución del olfato, perdida y/o disminución del gusto.
Estado actual del paciente al momento de la notificación: estable/leve, critico/grave, fallecido.
Diagnóstico clínico: Síndrome gripal/IRA/Bronquitis, IRAG/Neumonía u otro.
Datos de hospitalización y/o aislamiento.
Enfermedad de base o condiciones de riesgo: diabetes, enfermedad renal crónica, hipertensión arterial, enfermedad oncológica, enfermedad cardiaca, enfermedad respiratoria.
En cuanto al análisis estadístico, los datos epidemiológicos se registraron en una base de datos creada en Microsoft Office - Excel 2019. Los análisis estadísticos se realizaron utilizando el software SPSS versión 25. Con los resultados obtenidos se calcularon porcentajes para la valoración de las frecuencias de las variables cualitativas y se calculó la media para las cuantitativas.
Consideraciones éticas: el estudio contó con la aprobación del Comité de Bioética del HNMAV, que al ser un estudio observacional y no interferir en el manejo estandarizado de la infección respiratoria aguda grave, requirió solamente de un consentimiento informado al momento de la hospitalización, donde se especifica la aceptación de padres o tutores para la realización de pruebas diagnósticas según los protocolos institucionales, además mencionar que se entregó los resultados de las pruebas de PCR (Panel viral respiratorio) para beneficio del paciente, el mismo no tuvo ningún costo para el paciente ni para la institución de salud.
Resultados
Fueron internados entre junio de 2021 a junio de 2022 un total 41 pacientes de hasta 5 años con IRAG. Respecto a los hallazgos moleculares, 51,2 % de la población en estudio, dio un resultado positivo para alguna infección viral por SARS-CoV-2, VSR o FLU, detección que fue realizada por RT-qPCR en tiempo real múltiple. En cuanto a la frecuencia de circulación de virus respiratorios en la población con infección viral estudiada, se obtuvo que el agente más frecuente, con el 47,6 % (n=10) fue el VSR seguido de SARS- CoV-2 con el 42,9 % (n=9); sin embargo, no se detectaron casos positivos para el virus de la Influenza A ni B. Finalmente con el 9,5 % (n=2) se detectó coinfección entre SARS-CoV-2 y VSR; estas coinfecciones se presentaron en pacientes entre los 4 y 5 años de edad. En cuanto al umbral de ciclos o cycle threshold (Ct) obtenido en la ejecución de la RT-qPCR, valor que está relacionado con la carga viral, a menor valor de Ct, correspondería a una mayor carga viral. Se observa en la Figura 1 su distribución de acuerdo al grupo etario y la estratificación del riesgo de contagiosidad11 encontrándose que en el 80,9% de los pacientes con infección viral positiva diagnosticados por una RT-qPCR presentaron un Ct menor a 30 para el agente viral detectado en el momento del diagnóstico ver Figura 1.
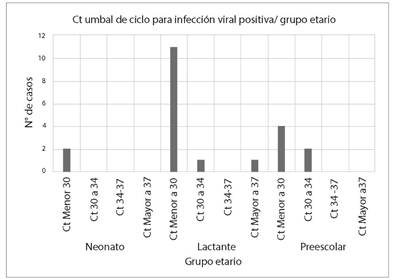
Nota: El gráfico muestra la distribución por grupos etarios donde se considera a neonatos (0 a 28 días), lactantes (28 días a 2 años) y niños en edad preescolar (3 a 5 años).
Figura 1 Distribución del resultado de Ct por RT-qPCR para el agente viral responsable (VSR y/o SARS-CoV-2) y su distribución por grupos etarios en pacientes con infección viral internados en el Hospital Manuel Ascencio Villarroel.
En cuanto a algunas características epidemiológicas, podemos mencionar que las semanas epidemiológicas donde se registró un mayor número de casos positivos en los pacientes de estudio, fueron entre las semanas 23 y 28, coincidentes con los meses de junio y julio, encontrándose el 57,14% de la totalidad de casos en este periodo. El tiempo de demora en acceder a los servicios de salud desde el inicio de los síntomas, fue: el 63 % (n=26) dentro de los 3 primeros días, el 24,4 % (n=10) entre 4 a 7 días y 12,2 % (n=5) después de 1 semana. En cuanto al nexo probable de contagio, el 37,5 % es desconocido, el 31,3 % indica que fue el padre o la madre, el 6,3 % el cuidador y el 25 % es otro contacto diferente. A pesar de que no se obtuvo ningún caso para infección viral por el virus de la Influenza en la población de estudio, el 93,8 % refiere que el paciente no cuenta con la vacuna frente a la misma.
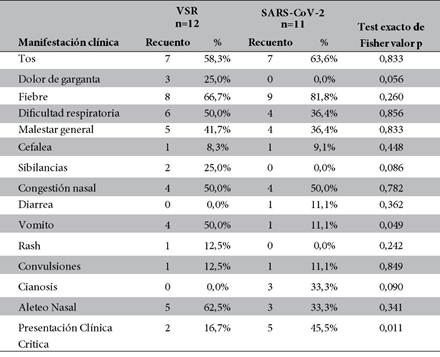
Tabla 1 Manifestaciones clínicas reportadas en pacientes internados en el Hospital del Niño Manuel Ascencio Villarroel, según agente etiológico viral.
Dentro de las características clínicas reportadas, la edad media fue de 19,9 meses, encontrándose pacientes desde cuatro días de edad hasta los cinco años. El 51,2% de la población fue femenino y 48,8 % masculino, con una relación 1:1, distribuidos según grupo etario de la siguiente manera: 33,3 % (n=7) menores de 6 meses, el 23,8 %(n=5) de 6 a 12 meses, el 14,3 % (n=3) entre 13 a 24 meses y el 28,6% (n=6) entre 2 a 5 años.
Los síntomas en pacientes con infección viral en el momento de la internación, fueron principalmente fiebre con el 76,2 % y tos con el 61,9 %. El 42,9% presentó dificultad respiratoria (Figura 2). No hubo reporte de casos de pérdida o disminución del olfato o gusto. Por otra parte, durante la hospitalización el 87,5 % presentó una temperatura normal durante el desarrollo de la enfermedad; el 12,5 % presentó sibilancias; el 68,8 % presentó una frecuencia cardiaca normal; el 25 % presentó taquicardia y solo el 6,3 % presentó bradicardia (signo de severo compromiso cardiopulmonar, secundario a una hipoxia prolongada). El 18,8 % presento cianosis; el 31,+3 % presentó taquipnea y el 12,5 % presentó convulsiones (Figura 2).
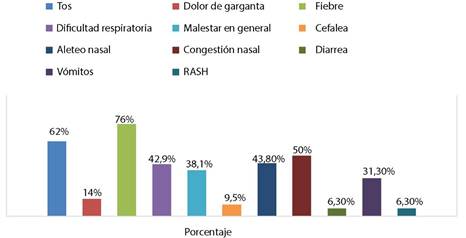
Figura 2 Manifestaciones clínicas reportadas en pacientes internados en el Hospital del Niño Manuel Ascencio Villarroel con un resultado positivo para infección viral
Clínicamente no existen diferencias significativas entre la presentación clínica de IRAG causado por VSR y SARS- CoV-2; buscando algún patrón clínico específico para el agente etiológico viral en cuadros graves, no se puede diferenciar el agente viral solo con métodos clínicos, siendo necesario el apoyo laboratorial. En cuanto a los pacientes que requirieron ingresar a terapia intensiva (cuadro critico), se observó que existe una relación entre pacientes con cuadros críticos (p=0,011) y la etiología asociada al COVID-19 (Tabla 1).
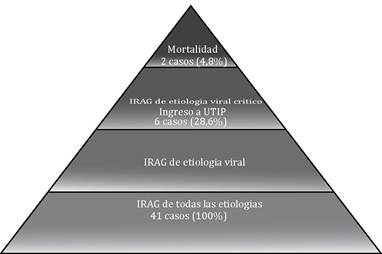
En cuanto al estado de salud en el momento de la internación, los pacientes con infección viral confirmada el 71,4 % ingreso con un estado estable y el 28,6 % con un estado crítico/grave. Hubo casos aislados de pacientes con desnutrición crónica, enfermedad cardiaca, síndrome Down, enfermedad oncológica o enfermedad renal. En cuanto al tiempo de internación de los pacientes, el 62,5% fue de 4 a 7 días, el 31,3 % fue internado por más de una semana, y el 6,3 % menos de 3 días. El 14,3% (n=3) de los pacientes con infección viral ingreso a terapia intensiva. Dos pacientes con infección viral de la presente población, fallecieron ambos por COVID-19, uno de ellos presentó coinfección viral SARS- CoV-2/ VSR (Figura 3).
Discusión
Dentro de las principales causas de muerte a nivel mundial, la neumonía y las otras infecciones respiratorias agudas graves, ocupan el cuarto lugar y representan el grupo de mayor mortalidad dentro de las enfermedades transmisibles de acuerdo a la Organización mundial de la Salud. El 15 % de las muertes en niños menores de 5 años se atribuyen a la neumonía, como principal causa de mortalidad infantil12.
Revisando los datos epidemiológicos del HNMAV, antes y durante la pandemia por COVID-19, entre 2016 y 2019, las neumonías graves o muy graves (IRAG) se ubicaban entre las tres principales causas de morbilidad, alcanzando hasta 157 casos por año (2016). No obstante, en la gestión 2020 se registraron solo 28 casos de IRAG, coincidiendo con la cuarentena rígida a causa de la pandemia por COVID-19, ubicándose en ese momento en el sexto lugar dentro de las causas de morbilidad, Ahora bien, en la gestión 2021, se contaba con el registro de 66 pacientes hospitalizados por este diagnóstico. Asimismo, dentro de las principales causas de muerte en los pacientes hospitalizados, se evidenció que la IRAG se encuentra entre el primer y segundo lugar en las gestiones 2016 a 2020 y en 2021 respectivamente13, lo que es compatible con los reportes internacionales12,13.
Antes del inicio de la pandemia por COVID-19, diversos estudios sobre la circulación de virus respiratorios en todo el mundo, mostraban al VSR como uno de los principales causantes de IRAG en niños hospitalizados, no obstante, ante la circulación del SARS-CoV-2, se ha generado un impacto sobre la circulación habitual de los virus respiratorios7. En nuestro estudio no hemos detectado ningún caso de infección por el virus de la Influenza, a pesar de que una gran mayoría de la población estudiada no contaba con la vacuna en el momento de la internación. Sin embargo, ha sido reportado que después de iniciada la pandemia por COVID-19, Los casos de infección por el virus de la influenza se ha mantenido por debajo de los niveles esperados en diferentes partes del mundo, inclusive de acuerdo a un informe presentado por la OMS, este refiere que en África y el Sur de Asia, el reporte de casos del virus de la Influenza, ha correspondido a casos aislados o incluso no se han presentado14.
Asimismo, en un centro pediátrico de referencia nacional en Argentina, se encontró en 2020, que el Rinovirus fue el principal agente viral detectado en población con IRAG y no el VSR, como lo había sido en 2019. En 2020, el SARS-CoV-2 fue el segundo agente predominante, no registrándose en ese año ningún caso de Infección respiratoria aguda baja por VSR ni FLU14, a diferencia de la población del presente estudio donde el VSR, en el periodo de estudio, aún es el principal agente viral identificado, seguido de SARS-CoV-2.
En cuanto a las manifestaciones clínicas de IRAG por SARS-Cov-2, un estudio realizado en Colombia, en pacientes hospitalizados, a pesar de buscar síntomas de disgeusia y anosmia no se encontraron casos15, al igual que en nuestro estudio, mencionando que dichos síntomas, en la población pediátrica en etapas de desarrollo preverbal (menores de 2 años), es difícil de determinar. Las manifestaciones gastrointestinales como el vómito y diarrea mostraron 17% y 22% de frecuencia respectivamente16 y aunque en nuestra población de estudio se reportó vómitos en el 31,3 % y diarrea en el 6,3%, esto confirma que la sintomatología respiratoria es más frecuente que la gastrointestinal. Por otra parte mencionar que otros síntomas extra respiratorios de importancia son las convulsiones que afectan hasta el 12,5% de nuestros pacientes, muchas veces de manera primaria, es decir sin una causa identificable (hipoxia, desequilibrios del medio interno), estos síntomas son más frecuente en la infección por SARS-CoV-2, que por otros virus respiratorios17.
En la pandemia por el virus de la Influenza A H1N1 que aconteció en 2009, los niños fueron uno de los grupos etarios más afectados, incluso el Virus Sincitial Respiratorio dejo de ser el principal agente viral responsable de infecciones respiratorias durante los periodos de mayor circulación pandémica10,14,15. sin embargo la afectación de la población pediátrica por COVID-19 en esta pandemia iniciada el 2020 ha mostrado características diferentes.
En cuanto a las coinfecciones virales , estudios realizados en Italia y Argentina, solo encontraron coinfecciones por SARS- CoV-2 con Rinovirus y CoV-NL6319,20, a diferencia de nuestro estudio donde se encontró coinfecciones entre SARS-CoV-2 y VSR, terminando una de ellas en la muerte del paciente.
Dentro de las limitaciones del presente estudio, podemos mencionar que por costos de las pruebas moleculares en el momento que se inició este estudio, solo se pudo realizar la adquisición de un panel respiratorio para 4 agentes virales : VSR, FLU A, FLU B y SARS-CoV-2 , asimismo por las características particulares de los pacientes en estudio y el tiempo de recolección de las muestras (1 año), se contó con un número reducido de pacientes, siendo estos resultados una estimación de la situación en población pediatría en cuanto a este tipo de infecciones respiratorias agudas graves y ser estos resultados propios para la población pediátrica del HNMAV estudiada.
En la población pediátrica estudiada podemos concluir que tras el desconfinamiento después del inicio de la pandemia por COVID-19 se encontró como agentes causantes de IRAG al VSR y a SARS-CoV-2, no se encontraron casos por FLU; las manifestaciones clínicas respiratorias en estos cuadros graves son similares y no permiten diferenciar entre agentes causales, por lo que la identificación molecular del agente infeccioso es clínicamente relevante. Los IRAG virales son cuadros la gravedad variable pero la probabilidad de requerir UTIP y de mortalidad es considerable.
Ante el retorno a las actividades presenciales, el comportamiento en la circulación de virus respiratorios, puede estar sujeta a cambios, siendo necesario una vigilancia epidemiológica constante en nuestro país, especialmente en población pediátrica, incluyendo datos como la incidencia, tasas de morbilidad, mortalidad, detección y contención de brotes de nuevas variantes de virus respiratorios, atendiendo la co-circulación de SARS-CoV-2, Virus de la Influenza, Virus Sincitial respiratorio y la detección oportuna de otros virus respiratorios emergentes. Finalmente, resaltar que ante la emergencia sanitaria que se ha vivido tras el inicio de la pandemia por COVID-19 y el fortalecimiento de los laboratorios con la implementación del diagnóstico molecular en hospitales, se ha notado la importancia de realizar la vigilancia epidemiológica de virus respiratorios empleando técnicas de biología molecular, principalmente por la alta sensibilidad, especificidad, tiempo de entrega de resultados, los mismos que sin duda representan importantes ventajas para contar con un diagnóstico oportuno en pacientes con cuadros clínicos graves donde es de fundamental importancia anticipar las posibles complicaciones de estas infecciones, ofreciendo estas pruebas moleculares una relación costo- beneficio considerable.