La saliva se ha utilizado cada vez más en las últimas décadas para evaluar la salud humana. Esta es una mezcla integrada de secreciones de las glándulas salivales, células epiteliales orales descamadas, líquido crevicular gingival y diferentes microorganismos. También contiene una gran cantidad de proteínas como inmunoglobulinas, mucinas y enzimas, así como metabolitos, hormonas y electrolitos1-4. Esta composición permite la detección de patógenos y también la cuantificación de biomarcadores proporcionando información sobre el sistema inmunológico, inflamatorio, endocrino y metabólico del individuo4. En algunos casos, su valor para detectar cambios fisiológicos es similar o superior al suero, por lo tanto, la saliva parece ser un fluido de enorme potencial en la evaluación de la salud, especialmente debido a la información clínica que puede proporcionar y al carácter no invasivo de su recogida. Además, puede realizarse por personas sin formación particular y sin mayores requisitos en términos de equipo o comodidades1.
La detección de SARS CoV-2 en saliva se informó por primera vez en Hong Kong, por To, Tsang, Yip, en 2020 en pacientes con infección por Covid-19, en este estudio, las muestras de saliva analizadas en serie mostraron disminuciones en los niveles de ARN de SARS CoV-2 después de la hospitalización y durante la recuperación del paciente5. Cheng y colaboradores (2020) también informaron una carga viral de SARS CoV-2 alta de hasta 5,9 x 106 copias/mL en la saliva de un paciente6, y Zhang et al. (2020) mostraron que el 53,3% de pacientes después de varios días de tratamiento portaban aun el virus7. Estudios con tamaños de muestra pequeños fueron los primeros en detectar consistentemente al nuevo coronavirus en saliva. Posteriormente, mas reportes han demostrado que el SARS CoV-2 se puede detectar de manera eficiente en la saliva3,5,8-12.
El uso de saliva presenta varias ventajas sobre el hisopado nasofaríngeo. La saliva, al poder ser recolectada por uno mismo evita la exposición de los trabajadores de la salud a pacientes potencialmente contaminados y, por lo tanto, reduce el riesgo de contaminación por SARS CoV-210,13-15.
Además, también reduce la necesidad de personal de salud y tiempos de espera para recolección de muestras, lo que evita concentraciones de personas y disminuye la probabilidad de transmisión del virus. Por otro lado, es fácilmente aceptado por los pacientes ya que no es invasiva ni dolorosa como la toma de muestra nasofaríngea, se puede utilizar para muestreos seriados y en estudios a gran escala o epidemiológicos, siendo especialmente ventajoso en poblaciones como los niños. Es fácil, rápido y económico de recolectar, lo que permite pruebas generalizadas1.
En Bolivia no existen estudios reportados que relacionen la detección de SARS CoV-2 a partir de muestra de saliva y de hisopado nasofaríngeo (HNF), en este sentido este trabajo tiene por objetivo determinar la concordancia entre dos tipos de muestras; muestras de HNF y muestras de saliva obtenidas en un mismo paciente, para detectar al SARS CoV-2 por RT- PCR.
Material y métodos
Este estudio de tipo descriptivo transversal, se realizó entre enero y marzo de 2021 durante la segunda ola de Covid-19 en la ciudad de Cochabamba, Bolivia. Fue aprobado por el Comité de Ética e Investigación del Hospital Clínico Viedma (HCV) y de la Facultad de Medicina de la Universidad Mayor San Simón (UMSS), siguiendo las directrices de Helsinki. Todos los pacientes firmaron un formulario de consentimiento informado antes de la inclusión. Los criterios de inclusión para la selección de los pacientes fueron los siguientes: sintomáticos respiratorios con dos o más síntomas sugerentes de Covid-19. Se excluyeron pacientes con una evolución sintomática sugerente de Covid-19 de más de 15 días.
La población de pacientes que cumplieron los criterios arriba mencionados fueron 9 mujeres y 21 hombres, la edad de los pacientes osciló entre 21 y 85 años. Los síntomas comunes fueron: tos (18%), dolor de cabeza (17%), disnea (14%), mialgia (12%), dolor de garganta (7%) y fiebre (6%). El 40% de los pacientes llegaron en urgencias, el 60% consultó al médico internista, y el promedio de evolución de los síntomas fue de 10 días.
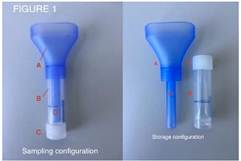
Las muestras de HNF y saliva fueron recolectadas por el mismo personal técnico del laboratorio de la institución, siguiendo procedimientos operativos estandarizados. La toma de muestra de saliva se obtuvo con dispositivos de recolección pasivo de saliva (Figura 1). Estos dispositivos fueron amablemente proporcionados por el Dr. Cyril Gueydan de la Universidad Libre de Bruselas (ULB). La recolección de saliva se realizó en pacientes que no se cepillaron los dientes, comieron o bebieron momentos antes del muestreo. Después de una explicación sobre los objetivos del proyecto y sobre el uso del dispositivo recolector de saliva, se solicitó a cada participante de auto-recolectar pasivamente su muestra de saliva, depositando aproximadamente 1 ml directamente en el dispositivo de recolección que contenía 1 ml de medio de transporte e inactivación del virus (VTM Life Science Park, ShenZhen, China). Paralelamente se tomó una muestra nasofaríngea utilizando hisopos de dacrón provistos con el mismo kit de VTM, que posteriormente fué depositado en el mismo medio de transporte de inactivación. Las muestras fueron identificadas y almacenadas a -20 °C hasta la extracción de ARN y su procesamiento por RT-PCR.
El ARN viral se extrajo a partir de 300 μL de muestras de HNF y muestras de saliva, utilizando el kit de purificación de ARN total (Norgen Biotek Thorold, ON, Canadá) de acuerdo con las instrucciones del fabricante. La amplificación del ARN diana del SARS CoV-2 se realizó mediante RT- PCR utilizando un termociclador QuantStudio 5 y el kit de ensayo V1 TaqMan™ 2019 nCoV (Applied Biosystems, Foster City, CA, E.E.U.U.). Las secuencias objetivo del SARS CoV-2 amplificadas fueron: el gen Orf 1ab (ORF), el gen de la proteína Spike (S), el gen de la nucleocápside (N) y la ARNasa P humana como control interno. La RT-PCR se realizó en un volumen final de 25 μL. Para cada gen objetivo evaluado, la mezcla total contenía 6,25 μL de Master Mix (4X), 1,25 μL de 2019-nCoV Orf 1ab, proteína S o N, (20X), 1,25 de ensayo RNaseP y 11,25 μL de grado RT-PCR agua y 5 μL de plantilla de ARN. Las condiciones de RT-PCR fueron las siguientes: un ciclo a 50°C durante 5 min. (paso de transcripción inversa), seguido de un ciclo a 95°C durante 20 segundos. (etapa de activación inicial) seguida de 40 ciclos de 95°C durante 3 seg. y 60°C durante 30 seg. Se usó agua libre de ARNasa como control no objetivo (NTC); el control positivo consistió en el kit de control V1 TaqMan™ 2019 nCoV (Applied Biosystems, Foster City, CA, EE. UU.). La RNAsa P humana se amplificó en paralelo con los genes diana específicos del SARS CoV- 2 como control interno (IC) para el procedimiento de extracción y recuperación de ARN. Para la interpretación de los resultados, las muestras con un Cycle Threshold (Ct) ≤ 37 para al menos uno de los tres genes diana mencionados anteriormente se consideraron positivas para la infección por SARS CoV-2. Las muestras se consideraron negativas para la infección por SARS CoV-2 cuando el Ct era ≥ 38 para todos los genes diana. Todas las ejecuciones de RT-PCR se validaron observando la amplificación de IC para cada muestra. Los controles negativos y positivos también validaron las ejecuciones de RT-PCR.
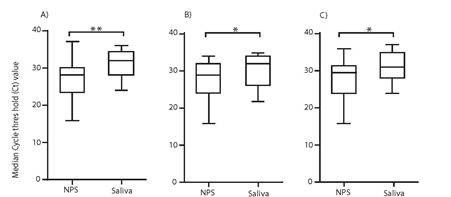
Figura 1 La carga viral (mediana de Cts) para las muestras de saliva es significativamente más alta que para las muestras de HNF para todos los genes estudiados. a) ORFla, b) N (nucleocápside) y c) gen S (proteínas de pico). La diferencia estadística se probó utilizando la prueba t pareada p*≤ 0,05 p **≤ 0,01.
Resultados
La detección por RT-PCR de SARS CoV-2 en HNF y saliva se realizó en 30 pacientes y se confirmó el diagnóstico de Covid-19 en base al resultado en una u otra muestra en 19 de 30 pacientes (63%). Asumiendo que la detección del SARS CoV-2 por RT-PCR en muestras de HNF representa el "estándar de oro", la detección del virus en la saliva mostró una sensibilidad analítica general del 83,3 %. El SARS CoV- 2 se detectó en 15 de 30 pacientes tanto en HNF como en muestras de saliva. Sin embargo, tres muestras que dieron positivo en HNF dieron negativo en saliva, y una muestra que dio negativo en HNF, dio positivo en saliva. La concordancia entre HNF y saliva por RT-PCR según el coeficiente kappa de Cohen, fue de 0,730 (IC del 95 %: 0,486 - 0,974), clasificada como buena (Tabla 1).
Tabla 1 Concordancia entre HNF y saliva por rRT-PCR según kappa de Cohen
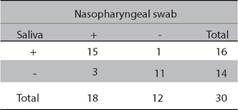
Coeficiente de kappa de Cohen: 0,730 (IC 95% : 0,486 - 0,974 )
Los valores de Ct de los tres genes diana (ORF, N y S) del SARS CoV-2, que fueron positivos para ambas muestras (HNF y saliva), se compararon por separado mediante la prueba t pareada. Los CTs de las muestras de HNF fueron significativamente más bajos que los CTs de las muestras de saliva para los genes ORF (p = 0,007), N (p = 0,0325) y S (p = 0,0323). Estos datos muestran que las muestras de HNF presentaban una carga viral más alta que la muestra de saliva (Figura 1).
Discusión
Cuando estalló la pandemia de Covid-19, la OMS recomendó el uso de hisopado nasofaríngeos o faríngeos para la detección de la etiología del SARS CoV-2 de Covid-1920. La recogida de HNF provoca molestias por su procedimiento de recogida invasivo, además existen riesgos considerables para los trabajadores de la salud durante la recolección de estas muestras. La saliva es una muestra alternativa, no invasiva, y parece confiable, ya que la viabilidad y la idoneidad de la saliva frente a las NPS para la detección del SARS CoV-2 ha sido reportada11.
El SARS CoV-2 puede estar presente en la saliva ya que se informó que las células epiteliales de la cavidad oral han mostrado una expresión abundante de ACE2 (enzima convertidora de angiotensina 2), un receptor que juega un papel clave en la entrada del SARS CoV-2 en las células, por lo tanto, las células ACE2 positivas en las glándulas salivales también se consideran células diana del SARS CoV-2, donde puede duplicarse, lo que convierte a la saliva en una muestra ideal para la detección viral4.
El hisopado nasofaríngeo es el método de muestreo de referencia recomendado en el diagnóstico de Covid-19, sin embargo, también se aceptan otras muestras como hisopado orofaríngeo (OPS), líquido de lavado bronco alveolar (BALF), esputo, hisopado nasal, aspiración o lavado para detectar SARS CoV-218. Desafortunadamente, la recolección de tales especímenes presenta grandes desventajas. De hecho, los procedimientos de recolección son invasivos, pueden causar algún grado de incomodidad o dolor para los pacientes y requieren trabajadores de la salud competentes con equipos de protección y bioseguridad para evitar riesgos de contaminación debido al contacto cercano con los pacientes19. Estos sistemas de recolección también pueden inducir tos y estornudos, generando aerosol, aumentando el riesgo de transmisión viral. El esputo se ha propuesto como muestra no invasiva del tracto respiratorio inferior, sin embargo, su dificultad para obtenerla ha sido descrita en el caso de SARS CoV, un virus con muchas similitudes con el Covid-19, especialmente en las primeras etapas de la infección, cuando no hay tos y sólo hay tos seca1.
Varios estudios que comparan el uso de muestras de hisopado nasofaríngeo y saliva para el diagnóstico laboratorial de Covid-19 reportan en general una buena concordancia entre estos dos tipos de muestras6,9,12,20-22. Los resultados de nuestro estudio muestran una concordancia de 0,730 considerada buena cuando se compara ambos tipos de muestra. En cuanto a la variabilidad de sensibilidad analítica, los valores informados en saliva puede oscilar entre el 53 y el 100%9,15-18. En nuestro estudio la sensibilidad para la detección de SARS CoV-2 por RT-PCR en muestras de saliva fue del 83,3% . Esta concordancia y sensibilidad es similar a la reportadas por Pasomsub et. al9, Plantamura et.al16 y Landry et.al17, aunque la sensibilidad es ligeramente inferior a la encontrada por Kendal et.al23.
La literatura actual sugiere que la carga viral encontrada en la saliva es adecuada para un diagnóstico confiable24. A pesar de la evidencia alentadora, la adopción de pruebas de saliva a gran escala sigue obstaculizada por la falta de estandarización del método de recolección y procedimientos analíticos. Los dispositivos disponibles para recolectar saliva pueden ser muy diferentes, lo que podría afectar la sensibilidad de detección. Algunos métodos incluyen la absorción de saliva en una almohadilla del cual el fluido tiene que ser eluido mecánicamente o babeando en un tubo de ensayo. En cualquier caso, el grado de viscosidad, que varía entre sujetos, puede dificultar el procesamiento posterior, interferir con el pipeteo, causando contaminación e impactando en la eficiencia de la extracción de ARN12.
Varios estudios investigaron la presencia de SARS CoV-2 en fluidos orales en diferentes etapas de la infección por RT-PCR, comparando la sensibilidad de detección de virus en saliva y en hisopados nasofaríngeos15. Según Plantamura et.al. (2021) la diferencia de sensibilidad entre HNF y saliva no solo podría estar relacionada con el curso de la infección, sino también el tipo de muestra de saliva proporcionada durante el muestreo (obtención de saliva pasiva o saliva mezclada con esputo) y por último por la dificultad de extraer el material genético en muestra con moco. La calidad de la muestra, los genes objetivos y la variabilidad del procedimiento para recolectar y preparar las muestras de saliva pueden también afectar la sensibilidad de detección SARS CoV-220,25-27.
La saliva es una muestra en la que se detecta con alta sensibilidad SARS CoV-2 en individuos sintomáticos y en etapas tempranas de aparición de síntomas21, y también existe una mayor tasa de detección en saliva entre 3 y 5 días después del inicio de los síntomas22, ya que la carga viral de SARS CoV-2 y la presencia de ARN viral en la primera semana después del inicio de los síntomas es mayor, luego disminuye con el tiempo25. En este estudio observamos tres resultados discordantes en muestras de saliva, que fueron negativas para SARS CoV-2 y positivas para HNF, probablemente esta diferencia este más relacionada con el período de recolección de la muestra ya que dos de las tres muestras discordantes se recolectaron 20 días después del inicio de los síntomas, lo que podría explicar la discordancia observada. Como en otros reportes26-28, también observamos que la saliva tiene valores medios de CT más altos que la muestra de HNF cuando comparamos de valores los CT en muestras emparejadas de HNF y saliva (Figura 1), sugiriendo que la carga viral en saliva es más baja que en HNF. Sin embargo se ha reportado valores de Ct más bajos en saliva que en HNF en muestras con resultados concordantes20. Con respecto a la contaminación de las muestras de saliva con esputo, creemos que este factor no ha influenciado los resultados obtenidos, ya que, por una parte, las muestras fueros obtenidas de forma pasiva, y por otra parte se ha descrito que el esputo proporciona tasas significativamente más altas de detección de ARN del SARS CoV-2 que en muestras de HNF29, lo que no es nuestro caso, ya que los valores de CT en saliva siempre fueron mayores que en muestras de HNF.
Una gran limitación de nuestro estudio es el pequeño número de sujetos incluidos en la muestra. A este respecto, cabe resaltar que los primeros estudios reportados el 2020 analizando la saliva fueron realizados en un número de muestras reducido, estos resultados que mostraron su eficacia como muestra alternativa fueron luego corroborados con estudios que incluyeron mayor población muestral. En nuestro caso una limitante mayor fue la cantidad de dispositivos recolectores de saliva disponibles, además de la difícil adherencia de pacientes al estudio.
Consideramos que los resultados de este estudio contribuyen a mejorar la evidencia de que las pruebas en saliva pueden representar una alternativa a las muestras de HNF en entornos comparables a la situación boliviana, donde las instituciones de salud han enfrentado saturación de sus recursos humanos y técnicos con un impacto directo en la calidad de la atención. También este tipo de muestra disminuiría el rechazo de las personas a tomas consecutivas, facilitando entre otros aspectos estudios epidemiológicos. Estos resultados incentivan a considerar el uso de la saliva como una buena alternativa para la recolección de muestras para el diagnóstico de Covid-19 en nuestro medio. Se recomienda más estudios para estandarizar diferentes métodos o dispositivos de recolección de muestras de saliva para la detección de SARS CoV-2 y para su uso en la detección de otros virus respiratorios.