Un estimado de 65 340 americanos serán diagnosticados con cáncer renal y 14,970 morirán por esta enfermedad en Estados Unidos en el 20181. El carcinoma de células renales (RCC) compromete aproximadamente el 3,8% de todos los nuevos canceres diagnosticados, con una media de edad al diagnóstico de 64 años. Aproximadamente 90% de los estos tumores son RCC, y aproximadamente 80% de estas son de células claras2,3. Otras menos comunes incluyen el papilar, cromófobo, por traslocación y conductos de Bellini.
El tabaquismo y la obesidad son los factores principales para su desarrollo, existen algunos tipos hereditarios de RCC como la enfermedad de von Hippel-Lindau (VHL), siendo esta la más frecuente. VHL es causado por una mutación autosómica dominante en el gen VHL, que predispone el desarrollo de RCC y otras lesiones vasculares proliferativas4,5. El análisis de la base de datos SEER indica que la incidencia de RCC está en incremento en un 0,7% cada año, y las muertes van en descenso en un 0,9% cada año del 2005 al 20146.
La supervivencia a cinco años para el RCC localizado se incrementó de 88,4% (durante el 1992-1995) a 92,6% (durante 2007-2013) y para enfermedad avanzada de 7,3% a 11,7% respectivamente7.
Los factores pronósticos más determinantes para la supervivencia a los cinco años son el estadio del tumor, el grado histológico, la extensión local del tumor, la presencia de ganglios positivos y la evidencia de metástasis a distancia8. El RCC metastatiza en primer lugar al pulmón, luego a ganglios linfáticos, hueso, hígado, glándula adrenal, y cerebro5.
El manejo quirúrgico actual estándar de los tumores renales pequeños es la cirugía conservadora de nefronas, que fue informada por primera vez por Czerny en 18909. Las directrices recomiendan la nefrectomía parcial como el tratamiento quirúrgico preferido en pacientes con una masa renal T110,11. Históricamente, la nefrectomía parcial se reservó para pacientes seleccionados, incluidos pacientes con riñón solitario, enfermedad renal crónica preexistente (ERC) o tumores renales bilaterales12. Sin embargo, la evidencia sugiere que la nefrectomía parcial es equivalente en términos de resultados oncológicos y superior en las mediciones de calidad de vida, incluido la pérdida de todo el riñón y la función renal a largo plazo13-15. La comparación de términos de pacientes tratados con nefrectomía parcial versus nefrectomía total/radical para tumores ≤ 5 cm informó tasas equivalentes de supervivencia cáncer específico y recidiva local a los nueve años de seguimiento16. La morbilidad perioperatoria es levemente más alta luego de una nefrectomía parcial comparada con la extirpación completa del riñón por varias complicaciones, incluyendo hemorragia (3,1% vs. 1,2%), pérdida de orina (4,4% vs 0%) y necesidad de reoperación (4,4% vs 2,4%)17.
Un ensayo prospectivo aleatorizado que comparó nefrectomía parcial con nefrectomía total en 541 pacientes con masas renales pequeñas (<5 cm), encontró inesperadamente una mayor supervivencia global en el grupo de nefrectomía total (81% frente a 76%, respectivamente, p <0,05) en un seguimiento medio de 9,3 años18, Sin embargo, las muertes cardiovasculares fueron más frecuentes en pacientes sometidos a nefrectomía parcial, a pesar de la menor carga de ERC. Este ensayo (Organización Europea para la Investigación y Tratamiento del Cáncer [EORTC] 30 904)18.
Los abordajes quirúrgicos mínimamente invasivos (MIS), son cada día más utilizados para la nefrectomía parcial y la nefrectomía radical, que incluyen abordajes laparoscópicos y asistidos por robot19. Con respecto a la nefrectomía parcial abierta versus MIS, los resultados oncológicos y los resultados de la función renal fueron equivalentes, con menor pérdida de sangre pero tiempos operatorios más largos observados en abordajes laparoscópicos20-22. Puntajes de nefrometría (Radio, Exofítico / Endofítico, proximidad al sistema colector o sinusal, anterior/posterior y ubicación en relación con las líneas polares (RENAL); aspectos preoperatorios y dimensiones utilizados para la clasificación anatómica (PADUA); índice de centralidad) basado en las características de imagen preoperatorias de los SRM han sido ampliamente implementados para categorizar objetivamente la complejidad operativa de la nefrectomía parcial23-25. La puntuación RENAL es la más ampliamente utilizada y ha permitido la estandarización en la notificación de los resultados y las complicaciones después de una nefrectomía parcial26. Spaliviero et al han propuesto un nuevo método de nefrometría llamado complejidad arterial. Se necesita más investigación para validar este sistema de puntuación en un modelo multiinstitucional27. Los determinantes más importantes de la función renal postoperatoria son la función renal preoperatoria, el volumen de parénquima renal preservado y el daño vascular al parénquima no maligno.
El primer factor se relaciona con la enfermedad renal subyacente y no es modificable, mientras que el volumen del parénquima remanente está en gran parte determinado por las características tumorales no mutables17. Se ha puesto mucho énfasis en minimizar la lesión isquémica al tejido no maligno al disminuir el tiempo de fijación o al realizar las técnicas de pinzamiento selectivo o fuera de pinzamiento28. Minimizar el tiempo de isquemia se acepta como el factor clave, y muchos estudios sugieren que un tiempo de isquemia más prolongado (> 30 minutos) da como resultado una función renal deficiente dentro de los primeros 3 a 6 meses después de la operación. Castañeda et al compararon de forma retrospectiva los resultados funcionales renales a los 6 meses y 1 año después de la operación y no encontraron diferencias en el pinzamiento de la arteria renal principal versus el pinzamiento selectivo frente a los métodos sin pinzamiento29.
La necesidad de preservar la función renal se demostró en un estudio poblacional de más de 1 millón de pacientes, que mostró una incidencia elevada de eventos cardiovasculares y mortalidad con empeoramiento de las etapas de la ERC30. El resultado óptimo multiparamétrico de la cirugía ahorradora de nefronas se ha definido como el margen quirúrgico negativo, la ausencia de complicaciones perioperatorias y el tiempo de isquemia caliente de 25 minutos o menos31. La nefrectomía parcial (NP) involucra de manera intencional la resección de una parte normal y sano del parénquima renal involucrando el tumor33-34. La enucleación de tumor renal (ER) es una alternativa de preservación de nefronas, en esta técnica el tumor renal es disecado del parénquima normal a través de un plano avascular a lo largo de la pseudocápsula de tumor fibroso37-45. ER minimiza así la cantidad de parénquima renal normal escindido con el tumor37-41. Estudios recientes han confirmado que la ER puede optimizar la preservación del parénquima vascularizado cuando se compara con SPN38. Sin embargo, la mayoría de los estudios no han podido demostrar una significancia estadística funcional que de una ventaja para ER37-41. Otras ventajas de ER incluyen un menor tiempo operatorio y menor pérdida de sangre38-42. La ER puede facilitar el enfoque de manejo con isquemia cero en comparación con la PN37-38.
Los estudios más recientes han informado menores tasas de márgenes quirúrgicos positivos y mejores condiciones locales controlar con ER en comparación con NP37,43-45.
Material y métodos
Se realizó un estudio retrospectivo, observacional y comparativo de pacientes sometidos a nefrectomía parcial laparoscópica en el periodo comprendido entre Julio de 2019 a Noviembre de 2021, en dos centros hospitalarios: Hospital Obrero Nº2 y Clínica Los Ángeles de la ciudad de Cochabamba, Bolivia. Todas las cirugías fueron realizadas por el mismo cirujano. Se incluyeron pacientes con diagnóstico clínico, radiológico y de tumor renal cT1 y cT2 que cumplieran con los siguientes parámetros: expediente clínico completo, y con al menos un seguimiento de dos meses para valorar complicaciones.
Se incluyeron todos los pacientes sometidos a nefrectomía parcial o enucleación laparoscópica, con diagnóstico confirmado de tumor renal.
Para su análisis se agruparon, según el abordaje, en dos grupos: parcial y enucleación, donde se compararon; edad, IMC, el tamaño del tumor, y su RENAL score, tiempo quirúrgico, sangrado transoperatorio, días de hospitalización, complicaciones postoperatorias, y bordes quirúrgicos.
El análisis estadístico realizado fue la prueba de t de Student y U-Mann Whitney para las variables cuantitativas con distribución normal y libre, respectivamente, y una Chi2 de Fisher para las variables dicotómicas, considerando una p<0,05 como significativa. Se utilizó el SPSS versión 20 (IBM, Chicago, IL).
Consideraciones éticas: el estudio fue aprobado por el Comité de Ética del Hospital Obrero Nº2 y Clínica Los Ángeles, de la ciudad de Cochabamba, Bolivia. Al ser un estudio descriptivo y retrospectivo, no se requirió consentimiento informado.
Resultados
Se evaluaron un total de 17 expedientes; se excluyeron tres, debido a que ameritaron cirugía radical. Por su localización y hallazgos transoperatorios, 14 expedientes cumplieron los criterios de inclusión, de los cuales seis fueron por abordaje parcial grupo I y ocho por enucleación grupo II. La media de edad fue de 47,7 (± 7,6) vs 54,2 (± 7,3), el IMC de 27,1 (23,8-31) vs 28 (24,6-30,1), para los grupos I y II respectivamente.
El RENAL score en global de todos los pacientes fue de baja a moderada, se realizó un análisis por separado, en el grupo I, la distribución fue complejidad baja 2 (33,3%), moderada 1 (16,7%) y alta 3 (50%), en el grupo II, baja complejidad 5 (62,5%), moderada 2 (25%), alta complejidad 1 (12,5%).
La mediana del tamaño del tumor para los del grupo I fue de 7,2 (2,5-10) para el grupo II fue de 3,21-5,7, todos los tumores fueron menores de 10 cm, con una clasificación cT1 hasta cT2, todos evaluados mediante tomografía, ninguno de los casos presentó metástasis o actividad ganglionar, todos contaban con laboratorios completos y dentro de parámetros normales.
La localización del tumor en general fue de predominio derecho 9 (64,2%), realizando el análisis por separado en el grupo I, el lado derecho fueron 5 (83,3%), izquierdo 1 (16,6%), en el grupo II, fueron del lado derecho 5 (62,5%), izquierdo 3 (37,5%).
En cuando a los bordes quirúrgicos, dos (14,2%) casos salieron con bordes positivos, en el análisis por separado, para el grupo I, uno (16,6%), para el grupo II, uno (12,5%), con reporte histopatológico para ambos de carcinoma de células cromófobo, con positividad focal en el margen quirúrgico, los cuales se mantienen en vigilancia, sin evidenciar recurrencia, sin ameritar hasta este momento algún otro tipo de manejo quirúrgico, y por el estirpe celular con buen pronóstico.
En cuanto al tipo histológico, ocho (5,1%) pacientes del total de los operados, tienen el diagnóstico de carcinoma de células claras, dos (14,2%) son carcinomas cromófobos, los cuales son del grupo II, cuatro casos salieron con reporte histopatológico benigno, por grupos dos (33,3%) vs 3 (37,5%) respectivamente, de estos para los del grupo I, los reportes fueron, un amgiomiolipoma, un oncocitoma, para el grupo II, fueron un quiste renal simple y dos oncocitomas renal.
El grado histológico más frecuente fue el grado 2, con seis casos en general, seguido por el grado histológico 3, ningún paciente presento grado 1 o 4 (Tabla 1).
Tabla 1: Características demográficas de los pacientes con abordaje por nefrectomía parcial (grupo I) y enucleación (grupo II) laparoscópica
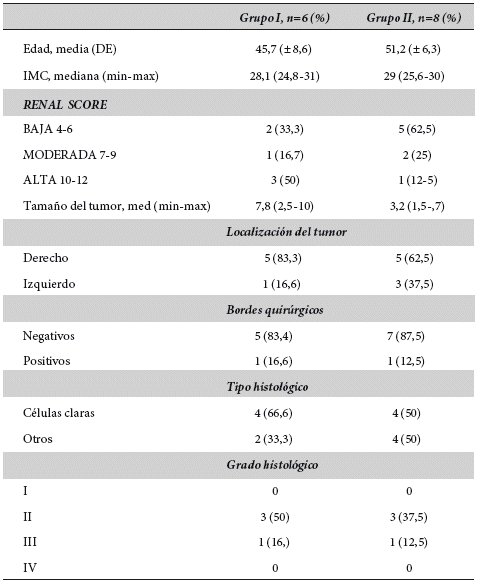
Como complicación hubo fuga urinaria en un paciente del Grupo I, con tumor de 10 cm, el cual se controló mediante colocación de catéter JJ, bajo sedación. El tiempo quirúrgico y sangrado transoperatorio fueron de: 187 (80-360) y 155 (120-225) minutos; 210 (120-300) y 76 (20-150) mL para el Grupo I y II, respectivamente. Los días de estancia hospitalaria fueron cuatro (2-7) y tres (2-3) días para el Grupo I y II respectivamente; ninguno de los pacientes presentó sangrado postoperatorio o nefrectomía posterior a la cirugía (Tabla 2).
Tabla 2 Análisis bivariado entre pacientes sometidos a nefrectomía parcial vs enucleación
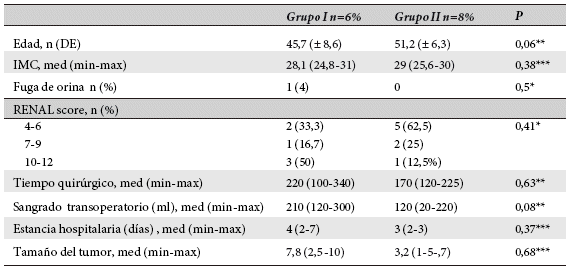
Med= Mediana, +x2 ; **t de Student, ***U-Mann Whitney
De los dos pacientes que se excluyeron del estudio, uno en el que se decidió terminar el procedimiento en nefrectomía radical, debido a que durante la evaluación de sus estudios y comorbilidades, presentaba alto riesgo de complicaciones postoperatorias, y datos de infiltración del tumor a seno renal, el otro caso que terminaron en nefrectomía radical, fue debido a los hallazgos transoperatorios, en los que se evidenciaba infiltración extensa del tumor a seno renal, presentando alto riesgo de dejar bordes positivos, decidiendo realizar procedimiento radical.
Se encontraron dos estudios donde se comparan ambos abordajes con variables similares a la nuestras, encontrando que son muy parecidos a nuestros resultados, en cuanto al tiempo quirúrgico, sangrado y éxito oncológico (Tabla 3).
Discusión
La nefrectomía parcial laparoscópica es una técnica que trata de reproducir todos y cada uno de los pasos de la cirugía abierta. McDougall et al5, describen por primera vez la nefrectomía parcial laparoscópica en animales en 1993. Fueron Wienfield et al6, quienes realizaron la primera nefrectomía parcial laparoscópica transperitoneal en humanos en 1993 y el grupo de Cleveland Clinic quien efectuó la primera nefrectomía parcial laparoscópica retroperitoneal. Según Uzzo y Novick la cirugía conservadora está indicada de manera imperativa en monorrenos, tumor renal bilateral e insuficiencia renal severa7.
La cirugía de preservación de nefronas es reconocida como efectiva para el tratamiento del carcinoma de células, cuando es necesaria la preservación de la función renal. También es cada vez más reconocido como un tratamiento efectivo para tumores pequeños, descubiertos incidentalmente, incluso cuando el riñón contralateral es normal6,11.
El número de estos tumores ha aumentado en los últimos años debido al mayor uso de técnicas de imágenes radiológicas no invasivas12, El límite de tamaño tumoral ha ido aumentado de manera progresiva con la experiencia de los cirujanos laparoscopistas hasta los 7 cm8. Por otro lado, no existen contraindicaciones absolutas en cuanto a la localización tumoral para la realización de la cirugía conservadora de nefronas. El único impedimento lo marca la habilidad y la experiencia de los distintos grupos de trabajo9. El tipo de abordaje utilizado dependerá de las preferencias del cirujano y de la anatomía de la lesión. Nosotros utilizamos el abordaje transperitoneal y todos nuestros abordajes son zero isquemia para todos los casos4,10. No utilizamos de manera rutinaria la colocación de catéter ureteral preoperatorio o catéter JJ transoperatorio, aunque sí la consideramos indicada en los casos en los que se evidencia invasión de la vía urinaria en las pruebas de imagen o de manera postoperatoria en los casos con apertura confirmada de la vía urinaria, realizamos el cierre de los colectores con material de sutura con poliglactina 910 u otro tipo de sutura absorbible, sintética, multifilamentosa y entrelazada, y en plano superficial para afrontar el parénquima usamos catgut crómico 1, puntos simples, previa colocación de un hemostático absorbible de celulosa oxidada, terminando con la aplicación de Gelfoam (Gelatina de Piel Porcina Purificada) en el lecho quirúrgico.
Presentamos nuestros resultados en un grupo de pacientes, tratados durante dos años en dos Instituciones de Salud: Clínica Los Ángeles y Hospital Obrero Nº2; comparando con las principales series publicadas9,11,14,18,25-29, los márgenes positivos oscilan entre el 0 y el 8%, siendo la media del 1,46% en nuestra serie tenemos un porcentaje de 14,2% el cual se acerca al promedio reportado en la literatura mundial (Tabla 3). Los resultados obtenidos en nuestro medio, son muy similares. La posibilidad de márgenes positivos será mayor en grupos con poca experiencia. Evidentemente, en centros donde se realicen cirugías de tumores cada vez más grandes y complejos, también pueden aumentar los márgenes positivos. Las complicaciones más frecuentes son la hemorragia perioperatoria, que sucede en el 10,77% y la fístula urinaria que se produce en el 4,76%, en nuestra serie solo tuvimos un caso con fuga urinaria, en un tumor grande, en paciente monorreno funcional, el cual se manejó con colocación de catéter JJ guiado por ureteroscopica y fluoroscopia, además de permanecer con sonda transuretral y drenajes por 10 días, remitiendo la fuga, sin necesitar otro tipo de intervención, ninguno de nuestros pacientes presentó sangrado en el seguimiento postoperatorio.
La factibilidad de los procedimientos urológicos mediante abordajes laparoscópicos ha detonado su utilización alrededor del mundo. Estos procedimientos permiten incisiones mínimas, una exposición quirúrgica adecuada que permite reproducir los gestos de la cirugía abierta, reducen el sangrado, el dolor y, en muchos casos, los días de internamiento. La menor convalecencia y mejor resultado estético se consideran ventajas adicionales.
El tiempo quirúrgico y el sangrado transoperatorio en nuestra serie fueron comparables a los resultados reportados en la literatura. Debe considerarse que el tamaño del grupo estudiado, el tipo de análisis retrospectivo y comparativo, son limitantes de este estudio. Sin duda, se requieren más estudios comparativos con mayor número de pacientes que permitan establecer definitivamente los beneficios del abordaje laparoscópico, para el tratamiento de los tumores renales pequeños.
Conclusiones
La nefrectomía parcial laparoscópica es una técnica mínimamente invasiva que reproduce los pasos de la cirugía abierta. Nuestra serie inicial alcanza buenos resultados quirúrgicos y oncológicos, similar a otras series descritas. No cabe duda que resulta necesario aumentar esta experiencia en lo que respecta al número de pacientes y al tiempo de seguimiento para poder afianzar los resultados obtenidos.
El abordaje laparoscópico es factible y seguro, presenta las ventajas de la cirugía de mínima invasión, requiere de un mayor número de pacientes para obtener conclusiones definitivas, y así poder en un futuro definir este tipo de abordaje como el Gold Standar para el manejo de esta patología.















