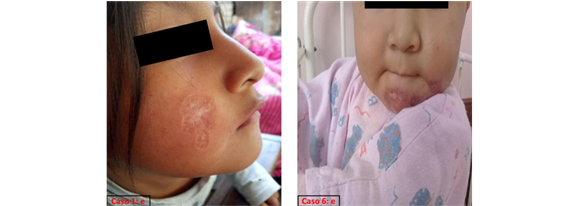
La leishmaniasis tegumentaria americana, es una enfermedad muy frecuente en varones adultos, que por motivos laborales invaden el habitad natural de vectores y reservorios, posibilitando la transmisión en humanos1,2. En los últimos años se ha incrementado el número de casos en niños como resultado de la domesticación del vector en áreas selváticas con asentamientos humanos2,3. Es muy posible que la información de la totalidad de enfermos no sea real, en parte por el deficiente sistema de información4.
De las cinco especies de leishmania presente en Bolivia, L. braziliensis, es responsable del 85% de los casos5 atendidos en la consulta médica. La evolución a la cronicidad depende principalmente del estado inmunológico del paciente y las variaciones genéticas de los parásitos de leishmania, importantes para el desarrollo de resistencia a los medicamentos6,7.
En Bolivia la aplicación de los medicamentos y el seguimiento en pacientes con leishmaniasis deben ser realizados el personal de salud. Según protocolo del Ministerio de Salud, existen medicamentos de primera línea (antimoniales) cuyo tratamiento es ambulatorio durante todos los días de administración, siendo 20 días en leishmaniasis cutánea (LC) o de 30 días en leishmaniasis mucosa (LM), salvo situaciones especiales donde requiera la evaluación especializada. Los antimoniales son las drogas anti leishmaniasis de primera línea desde hace más de 70 años, están disponibles en el mercado bajo la forma de estibogluconato de sodio y el antimoniato de meglumina, hoy en dia la resistencia a los antimoniales es un problema creciente principalmente con las especies de Leishmania. La Anfotericina B es medicamento para tratamiento de segunda línea debido a que su manejo requiere de cuidado por los efectos adversos16
En Latinoamérica, el tratamiento de la leishmaniasis se realiza con compuestos de antimonio, con una tasa de curación entre 70 y 85%, dependiendo de factores asociados al parasito y al huésped8. Se emplea la anfotericina B, con una tasa de curación de 90-95%, sobre todo en casos de falla terapéutica a los compuestos de antimonio8.
En Bolivia no existe registro, previo a este documento, sobre el empleo de anfotericina B en pacientes pediátricos, en ese sentido, el interés con la presente serie de casos es comunicar la experiencia del empleo de anfotericina B liposomal en pacientes pediátricos que no curaron con la terapia de compuestos antimoniales.
Presentación de los casos
Fueron internados en el Hospital de Niños Manuel Asencio Villarroel de la ciudad de Cochabamba para recibir Anfotericina B liposomal, seis pacientes pediátricos con leishmaniasis cutánea que no curaron con el empleo de compuestos de antimonio (Glucantime®) intramuscular a la dosis 20mg/Kg peso 20 días (Tabla 1).
Como datos epidemiológicos tenemos que el lugar probable de infección, de cinco de ellos fue en los Yungas (Norte y Sud) del departamento de La Paz y uno en la población de Nicolás Suarez en el departamento de Pando, lugares donde se encuentra el vector que transmite la enfermedad. La distribución por edad de los pacientes fue: uno de 10 meses, cuatro entre 3 y 5 años y uno de 7 años respectivamente; cinco de sexo femenino y uno de sexo masculino. El diagnóstico se realizó en las ciudades de La Paz y Cochabamba.
Tabla 1 Antecedentes clínicos y tratamientos previos con Glucantime® de pacientes pediátricos con leishmaniasis cutánea. Datos presentados como frecuencias (%).
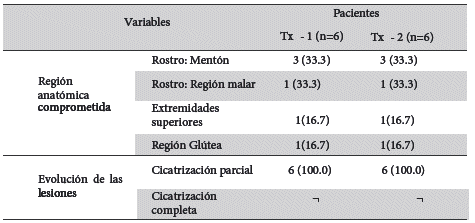
Tx - 1 y Tx - 2= Primer y segundo tratamientos con Glucantime ® (20 mg/kg/Peso/día por 20 días)
La clínica de presentación inicial consistía en úlceras o cicatrización incompleta de las mismas, en diferentes regiones anatómicas del cuerpo, después de recibir dos ciclos de tratamiento con Glucantime® (Antimoniato de meglumina), con intervalos de tres meses entre tratamiento. (Tabla 1). Antes de iniciar el tratamiento, de todas las úlceras se obtuvo amastigotes de Leishmania spp. mediante el raspado del borde de las lesiones9.
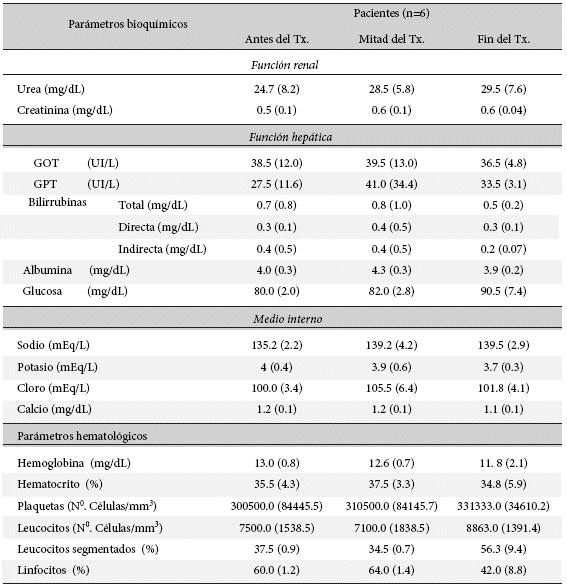
Previo al inicio del tratamiento con anfotericina B liposomal se procedió a la evaluación del estado nutricional mediante el uso de tablas nutricionales de la OMS10, encontrándose los pacientes en rango normal de nutrición. Se realizó la determinación de pruebas de función renal, hepática y exámenes complementarios (Tabla 2), al inicio, mitad de tratamiento y al final del mismo. En todos los momentos estos parámetros se encontraban dentro del rango considerado normal en pediatría.
Para la administración de Anfotericina B liposomal entre 2 a 3 mg/kg/día11-14 (promedio de 2,5 mg/Kg/ día), se tomó como referencia la edad del paciente, el lugar y el diámetro de la úlcera. La dosis acumulada alcanzada por paciente fue entre 30 a 58 mg/kg, con un promedio de 42 mg/Kg. La aplicación del medicamento fue hospitalaria por vía endovenosa entre 14 a 20 días y un promedio de 18 días.
La cicatrización de las úlceras cutáneas fue progresiva desde el inicio del tratamiento hasta lograr una completa curación (Figura 1).
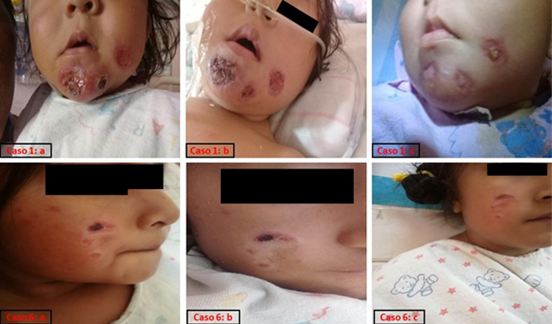
Figura 1 Evolución de las úlceras cutáneas por leismania de los pacientes pediátricos 1 y 6 durante el tratamiento con Anfotericina B liposomal. a=inicio del tratamiento; b=en algún momento durante el tratamiento; c=al final del tratamiento.
El control de posibles efectos adversos al medicamento se evaluó antes, durante y después del tratamiento mediante evaluación clínica, bioquímica y hematológica (Tabla 2), encontrándose todos ellos dentro de valores pediátricos normales.
Tabla 2 Evaluación de la función renal y hepática y otros parámetros, bioquímico / hematológicos de los pacientes pediátricos con leishmaniasis cutánea durante el tratamiento con Anfotericina B liposomal. Datos presentados como Promedio (DS).
Antes de iniciar el tratamiento, las lesiones tenian una media de diametro de 25 mm, el primer mes de control post tratamiento, presentan un diámetro menor a 10 mm, pero a los tres meses post tratamiento la cicatrización fue completa en todas las úlceras (Figuras 2a y 2b).
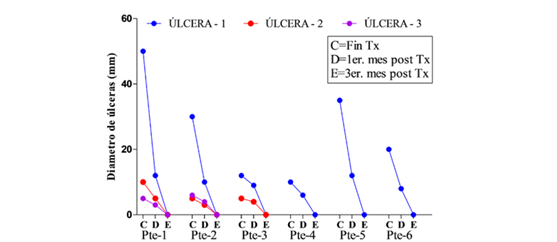
Figura 2a Seguimiento clínico de las úlceras cutáneas por leismania de pacientes pediátricos desde El momento de finalizacion del tratamiento con anfotericina B liposomal hasta los tres meses post tratamiento. Datos del diámetro en mm presentados de forma individual por cada paciente. Pte.=Paciente.
Discusión
En Bolivia, la infección por leishmania en niños es reportado con menor frecuencia15, probablemente como consecuencia de las falencias del sistema de reporte de casos4. Aunque los mismos responden satisfactoriamente al tratamiento con Glucantime®(Antimoniato de meglumina)8 , llamó la atención, la falta de respuesta a la aplicación de dos series del tratamiento con Glucantime® en los seis niños atendidos en el Hospital de Niños Manuel Asencio Villarroel de la ciudad de Cochabamba que se presenta en este reporte de casos y que tuvieron que ser tratados con anfotericina B, identificado como de segunda línea de acuerdo con la normativa boliviana16.
El empleo de anfotericina B desoxicolato y liposomal está documentado en población adulta que presentan falla terapéutica, La dosis oscila entre 1 a 3 mg/kg peso8,17,18 en periodos de administración variables. A pesar de ello, se recomienda evaluar en cada país, la dosis a emplear tomando encuentra aspectos clínicos y epidemiológicos además de las características inherentes a las cepas de leishmania circulantes a nivel local17.
La administración de anfotericina B a pacientes pediátricos que presentan falla terapéutica al Glucantime®, de acuerdo con experiencias previas, se aplica en dosis variables de 0,5 a 1 mg/Kg peso/día cuando se emplea Anfotericina B desoxicolato18 y entre 2 a 5 mg/Kg peso/día, si se emplea Anfotericina B liposomal11, la mayor dosis de este último responde a su tolerabilidad por parte de los pacientes. La administración de anfotericina B liposomal, descrita en este reporte de casos, es la primera experiencia documentada en Bolivia del empleo de este medicamento en pediatría para la resolución de leishmaniasis post falla terapéutica al tratamiento con Glucantime®.
La dosis diaria administrada a los pacientes, osciló entre 2 y 3 mg/Kg peso día de acuerdo a la edad de los niños, como dosis empíricas, las mismas que se encuentra dentro del rango de dosis administradas por otros autores11,12,13,19.
En el presente reporte de casos, no se encontró ningún efecto adverso de la administración de las dosis de Anfotericina B señaladas previamente, sobre la función renal, hepática, cardiaca ni tampoco otras manifestaciones adicionales como fiebre, escalofríos o vómitos que sugieran una posible acción toxica del medicamento en las dosis empleadas. Tales hallazgos son similares a los reportados en estudios previos11-13,19. Por tanto, se puede asumir que hubo buena tolerabilidad a la anfotericina B en estos niños con leishmaniasis, sin embargo, se deberá continuar con la evaluación de las dosis empadas en un número mayor de niños para tener mayor certeza sobre la tolerabilidad del medicamento en las dosis empleadas.
Con las dosis empleadas de anfotericina B liposomal en los seis pacientes se pudo observar una respuesta clínica favorable a partir del séptimo día de aplicación, la cual se hace más evidente al primer mes post tratamiento y la remisión completa es perceptible a los tres meses posteriores a la conclusión del tratamiento. Los reportes previos de otros autores, no indican un seguimiento post tratamiento sin embargo señalan proceso de remisión de las ulceras a la conclusión del tratamiento con anfotericina B liposomal, aplicada en diferentes dosis y tiempos11,19. Tal situación, sugiere que se logra la curación clínica de las ulceras por leishmania por acción de la anfotericina B independientemente del tiempo y dosis empleadas siempre y cuando se alcance una dosis acumulada que resulte tolerable para el paciente y que no supere el umbral señalado por los estudios de farmacocinética (pico máximo entre 83 y 100 µg/ml) para una dosis diaria de anfotericina liposomal de 10mg/Kg peso20,21, límite al que no se llegó en la presente serie de casos, cuya dosis máxima fue de 3 mg/Kg peso/día y que se encuentra en el rango de dosis administradas por otros autores11-13,19. Así mismo, la dosis acumulada en la presente serie de casos se encuentra próxima a 50mg/Kg peso11 y muy por debajo de la dosis acumulada de 1g/Kg peso19 reportadas previamente en el tratamiento de leishmaniasis cutánea en niños en los cuales se alcanzó la cicatrización de sus ulceras.
La norma Boliviana de tratamiento de la leishmaniasis cutánea indica el empleo de anfotericina B liposomal en casos de falla terapéutica a los compuestos de antimonio[16], sin embargo, las dosis de anfotericina B señaladas en dicha norma no hace diferenciación entre población adulta y población pediátrica con leishmaniasis recidivante posterior al tratamiento con Glucantime®, se tomó en cuenta artículos de revisión que fueron escasos, también se acudió al vademécum pediátrico donde se obtuvo un rango de 2 a 3 mg/kg/día. Además tomamos en cuenta la severidad de la lesión y la edad de estos pacientes pediátricos con leishmaniasis cutánea recidivante del Hospital del Niño Manuel Ascencio Villarroel. Los pacientes evolucionaron de forma favorable sin presentar efectos secundarios, por lo cual la información obtenida en la presente reporte de casos se constituye en la primera experiencia de aplicación de este medicamento en población pediátrica en Bolivia.
Conclusión
Los resultados obtenidos en la presente serie de casos, permiten concluir que la Anfotericina B liposomal dio resulto eficaz en el tratamiento de leishmaniasis cutánea post tratamiento con Glucantime® de los seis pacientes pediátricos, evidenciándose el proceso de remisión de las úlceras a partir del séptimo día de tratamiento y la completa cicatrización a los tres meses posteriores al tratamiento.
La dosis empleada (2 a 3 mg/Kg peso/día) resulto ser segura y tolerable para los niños, ya que la evaluación permanente no evidenció la aparición de signos compatibles con posible daño renal, hepatico, cardiaca ni otras manifestaciones como fiebre, escalofríos o vómitos que sugieran una posible acción toxica del medicamento.
Si bien, la norma boliviana referente al tratamiento de la leishmaniasis no diferencia la dosis de anfotericina B para población adulta y población pediátrica, la experiencia desarrollada en el hospital pediátrico Manuel Asencio Villarroel, se constituye en la primera experiencia documentada y puede servir como referencia para futuros tratamientos con anfotericina B liposomal en población pediátrica en Bolivia.