Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Gaceta Médica Boliviana
versão On-line ISSN 1012-2966
Gac Med Bol vol.43 no.1 Cochabamba ago. 2020
Artículo de Revisión
Uso de plasma convaleciente en pacientes con COVID-19
Use of convalescent Plasma in COVID-19 patients
Nelson M. Nina Garcia1, Guiselle Alejandra Cussi Coronel 2
1Especialista en Hematología y Hemoterapia, Hospital de Especialidades Materno Infantil, La Paz, Bolivia.
Recibido el 30 de abril de 2020.
Aceptado el 15 de junio de 2020.
Resumen
La enfermedad por coronavirus 2019 (COVID-19) representa una de las mayores pandemias a las que el mundo se enfrenta y está produciendo una crisis sanitaria global. Hasta la fecha no se disponen de terapias o vacunas aprobadas para esta enfermedad. Se están estudiando varias opciones terapéuticas y desarrollando vacunas. El plasma convaleciente constituye una opción terapéutica interesante contra COVID-19, ya que sutilizó con éxito en otros brotes virales en el pasado. Esta terapia se consiste en la recolección de plasma de individuos recuperados de la enfermedad viral que desarrollaron anticuerpos. Es considerada la única estrategia a corto plazo, para conferir inmunidad inmediata a individuos susceptibles. En esta revisión se aborda los posibles mecanismos de acción del plasma convaleciente, damos una vista panorámica de los primeros estudios realizados en COVID-19, así como como los procedimientos necesarios para implementar esta terapia.
Palabras clave: COVID-19, SARS-CoV-2, plasma convaleciente
Abstract:
Coronavirus 2019 disease (COVID-19) represents one of the largest pandemics the world is facing and is producing a global health crisis. To date, there are no approved therapies or vaccines for this disease. Various therapeutic options are being explored and vaccines are being developed. Convalescent plasma is an interesting therapeutic option against COVID-19, as it has been successfully used in other viral outbreaks in the past. This therapy consists of collecting plasma from individuals recovered from the viral disease who developed antibodies. It is considered the only short-term strategy to confer immediate immunity to susceptible individuals. This review addresses the possible mechanisms of action of convalescent plasma, we give a panoramic view of the first studies carried out on COVID-19, as well as the necessary procedures to implement this therapy.
Keywords: COVID-19, SARS-CoV-2, convalescent plasma
A finales de diciembre de 2019, se notificaron casos de neumonía inexplicada en Wuhan, China. Efectuados los análisis respectivos se concluyó que el agente causal de estos casos era un nuevo coronavirus1. La Organización Mundial de la Salud (OMS) denominó a la enfermedad causada por este virus como COVID-19 (enfermedad por coronavirus 2019). Asimismo, el Comité Internacional de Taxonomía de Virus nombró a este nuevo agente como Coronavirus 2 del Síndrome Respiratorio Agudo Grave (SARS-CoV-2)1.
A medida que los casos se incrementaban en el lugar de origen y áreas circundantes, también se empezaron a registrar casos en otras partes del mundo. Esto conllevó a que la OMS inicialmente declare a COVID-19 como una emergencia de salud pública de interés internacional y el 11 de marzo se declaró oficialmente como pandemia2. En Bolivia los primeros casos de COVID-19 se registraron en marzo de 2020 (departamentos de Oruro y Santa Cruz), actualmente se reportan casos en los nueve departamentos, siendo Santa Cruz el departamento más afectado3.
La transmisión del SARS-CoV-2 es principalmente por contacto cercano, probablemente también por aerosoles, sin embargo, se sugieren otras vías de transmisión que son motivo de estudio1. La expresión clínica de COVID-19 es variable siendo el aparato respiratorio el sitio más afectado, sin embargo, la afección de otros órganos también es posible4. La enfermedad puede expresarse como formas leves o incluso formas graves que amenazan la vida, esta última en función a ciertos factores de riesgo4.
A la fecha no existen tratamientos ni vacunas específicas para esta enfermedad, por lo que es un área de intensa investigación5. El tratamiento en general es sintomático, así como el manejo respectivo de las complicaciones.
En el escenario actual y ante el constante incremento de casos en todo el mundo, se necesitan estrategias de tratamiento urgentes, que sean factibles y eficaces para enfrentar la enfermedad, en especial en aquellos casos graves. Recientemente se ha sugerido el uso de plasma convaleciente (PC) de pacientes recuperados de COVID-19 como una estrategia de tratamiento en algunos casos, tal como sucedió en epidemias previas causadas por otros agentes virales6. Los resultados iniciales de este tratamiento en pacientes con COVID-19, demostraron efectividad en términos de mejoría clínica, reducción de carga viral, menores complicaciones, así como una reducción en la mortalidad7,8.
El tratamiento con PC es accesible en diversos entornos del mundo, siendo relativamente segura en relación a efectos colaterales. Considerado que aún no contamos con medicamentos aprobados para esta enfermedad, podría convertirse en una estrategia terapéutica para algunos pacientes o ser parte del tratamiento convencional. Siguiendo esta línea, en Bolivia a través del Programa Nacional de Sangre se inició el protocolo de tratamiento con PC para casos de COVID-19 desde el mes de mayo de 20209.
La presente revisión describe los aspectos generales del tratamiento con PC en COVID-19, mecanismos subyacentes, resultados, así como procedimientos necesarios para instaurar esta estrategia terapéutica.
Antecedentes Históricos
El uso de productos sanguíneos convalecientes data de finales de 180010. Una de las primeras enfermedades en las que se demostró su efectividad fue la gripe española (1918–1920)10. Según análisis posteriores, los productos sanguíneos convalecientes redujeron la mortalidad hasta en un 21%6.
Posteriormente durante la epidemia de SARS-CoV-1 de 2003, se utilizó PC en varios pacientes. El tratamiento resulto en una menor mortalidad y un menor tiempo de estancia hospitalaria6,11.
Durante la pandemia por el virus de la Influenza A H1N1 de 2009 también se utilizó PC en pacientes con enfermedad grave, demostrándose un impacto favorable en la mortalidad y la disminución de la carga viral6. Además, esta modalidad de tratamiento fue bien tolerada, no reportándose complicaciones relacionadas a la misma6.
En 2014 la OMS recomendó el tratamiento empírico con PC durante los brotes de Ebola y más recientemente también fue utilizado en pacientes con Síndrome Respiratorio del Medio Oriente (MERS-CoV)6, 11.
Fundamento y Mecanismo de acción
Para comprender de mejor manera el fundamento de esta modalidad de tratamiento, debemos comprender primero a que nos referimos cuando hablamos de PC. Zhang et al. 11 considera al PC, como aquel que fue recolectado de un paciente que sobrevivió a una enfermedad infecciosa y que por lo tanto desarrolló anticuerpos (Ac).
En este sentido el tratamiento con PC es una forma de inmunización pasiva a corto plazo, que permite la transferencia de anticuerpos neutralizantes (NAbs por sus siglas en inglés) contra un patógeno específico a un paciente que cursa con la infección. Estos anticuerpos tienen la capacidad neutralizar al agente patógeno y por consiguiente reducir los eventos fisiopatológicos deletéreos en el paciente12.
En la mayoría de las enfermedades virales el punto máximo de la viremia se alcanza antes que el paciente desarrolle la suficiente cantidad de Ac, como consecuencia ciertos pacientes susceptibles, desarrollan complicaciones mayores tal como sucede en la infección por SARS-CoV-26. En este sentido la introducción de Ac específicos contenidos en el PC pueden mejorar los resultados del paciente.
Los mecanismos que comentamos explican el efecto antiviral del PC. Sin embargo, se han sugerido otros mecanismos atribuibles al tratamiento. Recientemente, Rojas et al.13 realizaron una revisión para explicar los posibles mecanismos del PC en COVID-19. Sugieren como otro efecto de importancia es la inmunomodulación, la cual se produciría mediante varios mecanismos que comentaremos a continuación13 : Mecanismos F (ab´) 2, sugieren que el PC puede inhibir ciertos autoanticuerpos, estos podrían jugar un papel en COVID-19, pudiendo ser responsables de algunas complicaciones como la trombosis mediada por anticuerpos antifosfolípido. Asimismo, este mecanismo podría interferir la cascada del complemento, la cual también estaría implicada en la fisiopatología de la enfermedad.
Mecanismos en Fc (fragmento cristalizable), sugieren que el PC puede producir la saturación de FcRn (receptor para el Fc neonatal), la cual tendría efectos sobre ciertos anticuerpos que podrían jugar un papel en la patogénesis. Asimismo, los receptores Fcγ tienen importancia en la inhibición y modulación de células inmunes, al respecto también proponen mecanismos a este nivel.
Efectos en las células dendríticas, sugieren que el PC puede mejorar las propiedades antiinflamatorias de estas células, considerando que la respuesta inflamatoria juega un papel importante en esta enfermedad.
Efectos en los linfocitos T y B, sugieren que el PC podría modular el equilibrio y la sobrevida de diferentes poblaciones de linfocitos T. También sugieren efectos a nivel de los linfocitos B.
Efectos en otras células, sugieren que el PC podría evitar la migración de las células inmunes hacia el tejido pulmonar.
Por lo arriba mencionado, el PC ejercería efectos antivirales mediante NAbs específicos, pero además destacan los posibles mecanismos inmunomoduladores descritos a diferentes niveles, los cuales que podrían interferir en la fisiopatología de COVID-19 y por consiguiente prevenir el desarrollo de complicaciones.
Primeros estudios del uso plasma convaleciente en COVID-19
Los primeros reportes del uso del PC en pacientes con COVID-19 son en su mayoría series de casos, sin embargo son estudios muy valiosos, debido que nos proporcionan las primeras experiencias del uso de esta modalidad de tratamiento aplicada a esta enfermedad, además son el punto de partida para el desarrollo de los protocolos actuales.
Considerando su importancia, al comentar cada uno de estos estudios se describirán algunos aspectos metodológicos y resultados más destacables.
Uno de los primeros reportes corresponde a Shen et al 7. En su estudio describen el tratamiento con PC aplicado a cinco pacientes con COVID-19 crítico en un Hospital de Shenzhen, China. Los donantes seleccionados se encontraban asintomáticos durante al menos durante diez días, con pruebas para SARS-CoV-2 negativas (por RT-PCR), además de presentar títulos de anticuerpos específicos para SARS-CoV-2 de 1:1000 (por ELISA) y un título de NAbs mayor a 40. Los pacientes recibieron dos transfusiones de PC con un volumen de 200 a 250 ml.
Los autores destacan la mejoría de varios parámetros clínico-laboratoriales entre los que destacan la puntuación SOFA (Sequential Organ Failure Assessment); cociente de presión arterial de oxígeno/fracción inspiratoria de oxígeno (PaO2/FiO2), con mejoría sustancial a los 12 días; normalización de la temperatura; disminución de los marcadores inflamatorios (PCR, IL-6, procalcitonina); reducción de la carga viral; incremento de los títulos de anticuerpos IgG e IgM y de los NAbs7. También describen la resolución gradual de las lesiones pulmonares en los estudios de imagen, que en algunos pacientes ya fue evidente al tercer día después del tratamiento7.
Duan et al.8 reportaron una serie de diez pacientes con COVID-19 con criterios de enfermedad grave tratados con PC en Wuhan, China. Siete de ellos tenían prueba positiva para SARS-CoV-2 antes de la transfusión. Los donantes seleccionados se encontraban afebriles por más de 3 días, sin ningún síntoma respiratorio, además de tener 2 pruebas negativas para SARS-CoV-2 por reacción en cadena de la polimerasa en tiempo real (RT-PCR) con intervalo de 1 día. Los pacientes recibieron una transfusión de 200 ml de PC inactivado con actividad de neutralización > 1: 640.
El tratamiento resultó en mejoría de varios parámetros clínico-laboratoriales: los síntomas mejoraron entre 1 a 3 días; hubo remisión de la linfopenia; reducción de los niveles de marcadores inflamatorios; mejoría de la función hepática y remisión de las lesiones pulmonares en estudios de imagen 8. Además, en cinco pacientes se observó un aumento de los títulos de NAbs y en los siente pacientes con prueba positiva previa para SARS-CoV-2 se observó la negativización 8.
Otro estudio también realizado en Wuhan, reportó una serie de seis pacientes con COVID-19 en estado crítico o que presentaban evolución desfavorable a pesar del tratamiento estándar14. Los donantes seleccionados se encontraban afebriles menos durante al menos 3 días, sin ningún síntoma respiratorio, con 2 pruebas consecutivas para SARS-CoV-2 negativas por RT-PCR y luego de 3 semanas desde el inicio de la enfermedad. Los pacientes recibieron la transfusión de 200 ml de PC, posterior a la misma en cinco pacientes se observó la resolución de las lesiones pulmonares en estudios de imagen.
En Corea se reportaron dos pacientes con COVID-19 con criterios de gravedad, mayores de 60 años con síndrome de distrés respiratorio agudo (SDRA)15. Los pacientes recibieron dos transfusiones de PC (250 ml) cada 12 horas. Ambos pacientes presentaron mejoría significativa de los parámetros clínico-laboratoriales, así como independencia de la ventilación mecánica. La prueba para SARS-CoV-2 fue negativa en ambos pacientes posterior a la transfusión (día 20 y 26)15.
Zeng et al.16 describieron los resultados de veintiún pacientes mayores de 60 años con COVID-19 que fueron ingresados a la unidad de cuidados intensivos. Seis de los pacientes fueron tratados con PC y al resto se lo considero como grupo control. Este estudio más allá de valorar los resultados del tratamiento, analizó el aclaramiento viral.
La mortalidad en el grupo de tratamiento fue 5/6 y en el grupo control fue 14/15. El 100% de los pacientes tratados con PC tenía SARS-CoV-2 indetectable en comparación con un 21,4% en el grupo control (p = 0,005), además era evidente un mayor tiempo de sobrevida en el grupo tratado16.Este estudio denota la efectividad del PC en términos de aclaramiento viral, sin embargo y como lo sugieren los autores, esta modalidad de tratamiento debería ser instaurada antes de que el paciente pase a un estado crítico.
Un aspecto en el que coinciden todos los estudios comentados es que, el uso de PC estuvo limitado a pacientes con COVID-19 grave o crítico y en algunos casos fue estrategia terapéutica elegida ante la no mejoría clínica. Destacamos que casi todos los estudios reportaron resultados favorables. Además, en general el tratamiento fue bien tolerado ya en ningún estudio se reportaron reacciones adversas significativas.
Regulación
El tratamiento con PC en pacientes con COVID-19 es una estrategia terapéutica emergente ante la actual pandemia. En este sentido hacemos notar que al momento de escribir el presente artículo, aun no es un tratamiento aprobado por las entidades regulatorias correspondientes, debido a la falta aún de ensayos clínicos.
En los Estados Unidos, la Food and Drug Administration (FDA) autorizó el uso del PC para COVID-19 como un producto de investigación mediante tres vías: ensayos clínicos, acceso ampliado y como un nuevo medicamento de investigación (IND por sus siglas en ingles) de emergencia en un solo paciente17.
Asimismo, en una publicación de la International Society of Blood Transfusion (ISBT)18, se sugiere que el uso clínico del PC debe manejarse como una terapia experimental y por consiguiente cumplir con todas las normas éticas y legales. Esta instancia recomienda también que, dada la naturaleza experimental las muestras de donantes y pacientes deberían almacenarse para estudios posteriores.
En Bolivia de forma consistente con las regulaciones mencionadas, el tratamiento con PC para COVID-19 se autorizó como tratamiento experimental sujeto a evaluación de seguridad y eficacia, siendo regulado por el Programa Nacional de Sangre9.
Selección de donantes
La selección de donantes es el paso fundamental para iniciar un protocolo de tratamiento con PC para COVID-19. Para este efecto se requiere de registros nacionales u hospitalarios y la sensibilización necesaria a la población para promover la donación.
Uno de los problemas con lo que se enfrenta en varias partes del mundo, especialmente durante el reporte de los primeros casos, es la falta de pacientes recuperados. Otro problema que surge es la falta interés para la donación, desde nuestro punto de vista este es un problema muy común en nuestro país. Remarcamos que la donación de PC por un paciente recuperado debe ser un acto voluntario y altruista9.
Los criterios para la selección para los donantes de PC en el caso de COVID-19, fueron definidos recientemente con base a los estudios desarrollados a la fecha y según las instituciones correspondientes (Tabla 1)18,19. Al igual que para una donación estándar, se debe efectuar la evaluación clínica del donante, se sugiere además el registro de datos relacionados con el diagnóstico y el curso de la enfermedad para estudios posteriores18.
Tabla 1: Criterios para la selección del donante de plasma convaleciente para el tratamiento de COVID-1919, 20

Recolección y procesamiento del PC
Según las recomendaciones vigentes la recolección de PC debe realizarse únicamente por aféresis, no aconsejándose el uso de sangre entera como aporte de PC18. El procedimiento de aféresis será realizado según protocolo estándar, en establecimientos de salud certificados y por personal calificado 9,18,19. El volumen a recolectarse debe estar en relación a los parámetros del donante, se sugiere recolectar un volumen entre 200 a 600 ml de plasma18.
Una vez obtenido el PC, este debe someterse a un proceso de reducción de patógenos18.Cuando sea factible debe determinarse los títulos totales de Ac y NAbs18,19. Se considera que los NAbs se correlacionan mejor con la eficacia, aunque esta prueba no es de fácil acceso en varios entornos 20.
Es interesante comentar que, los títulos de anticuerpos en pacientes convalecientes están en relación con la carga viral inicial. Considerando este aspecto se ha sugerido que los pacientes que tuvieron mayor sintomatología desarrollan mayores títulos de anticuerpos19. Se requieren más estudios para tomar en cuenta esta consideración durante la selección del donante.
Zhang et al.21 evaluaron los niveles de Ac en seis donantes recuperados de COVID-19, cinco de ellos tenían títulos altos de Ac y eran elegibles para los criterios utilizados en su estudio. Esto sugiere que probablemente la mayoría de los donantes que cumplen los criterios de selección establecidos presentarían títulos altos de Ac.
Destacamos sin embargo que, a la fecha no existe un nivel óptimo recomendado de Ac en el PC para asegurar su eficacia.
En relación a la probable viremia en el PC, según los criterios sugeridos para la selección del donante, esta no existiría, sin embargo se sugiere la detección de SARS-CoV-2 en el plasma recolectado antes de la transfusión19.
Como se mencionó previamente al ser un tratamiento experimental deben almacenarse las muestras del suero del donante para futuras investigaciones.
El PC recolectado debe dividirse en alícuotas de 200 a 250 ml, además de ser correctamente etiquetada, precisando el nombre del producto y especificando que se trata de un tratamiento experimental9,18.Puede hacerse uso inmediato de la unidad o ser criopreservado según normas estándar18. El intervalo entre donación por aféresis en general es de 2 semanas y no menor a 7 días18,19.
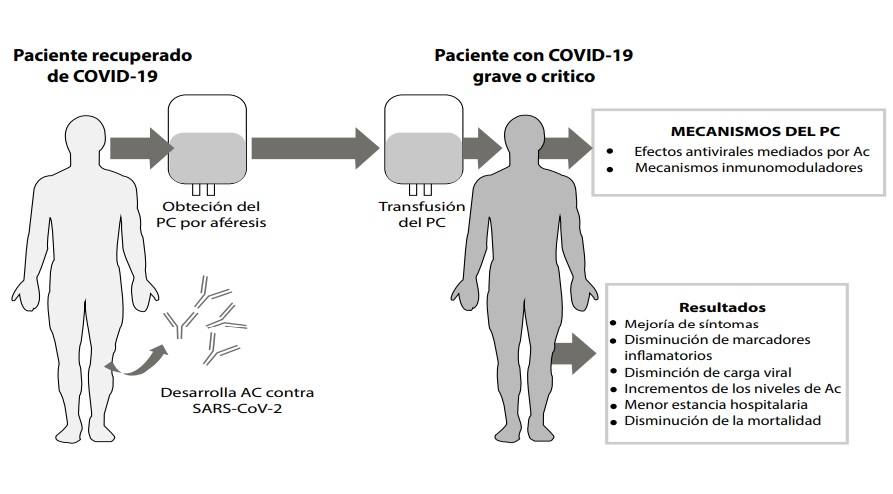
Figura 1: Fundamentos y resultados del plasma convaleciente en pacientes con COVID-19
Selección del paciente, administración y dosis
Actualmente no existen recomendaciones para la selección del paciente con COVID-19 candidato a ser tratado con PC. En los estudios realizados a la fecha, el tratamiento se efectuó principalmente en pacientes enfermedad grave o critica.
La FDA, para facilitar la solicitud de IND sugiere seguir los criterios de elegibilidad de Protocolo Nacional de Acceso Ampliado para Tratamiento, que son los siguientes 17:
1. COVID-19 confirmado por laboratorio
2. COVID-19 grave o con peligro inminente de vida, por ejemplo:
a. Enfermedad grave se define como uno o más de los siguientes: dificultad respiratoria (disnea); frecuencia respiratoria ≥ 30/min; saturación de oxígeno ≤ 93%; PaO2/FiO2 <300; infiltrados
pulmonares> 50% en 24-48 horas.
b. Enfermedad potencialmente mortal se define como uno o más de los siguientes: insuficiencia respiratoria; shock séptico; disfunción o falla orgánica múltiple
En Bolivia, siguiendo con los lineamientos mencionados se plantea el tratamiento para casos graves y críticos de COVID-199.
Aun no existe evidencia suficiente que apoye el uso de PC en fases más tempranas, sin embargo, considerando los mecanismos de acción y la fisiopatología de la enfermedad, podríamos suponer mayores beneficios si el tratamiento se instaura en fases más tempranas. Zeng et al.16 también sugirieron que el tratamiento podría ser más beneficioso en etapas tempranas de la enfermedad, tras evidenciar un aclaramiento viral importante después de tratamiento, sin embargo, a pesar de este hallazgo y al ser pacientes en etapas muy avanzadas, la mortalidad fue alta. Se requieren más estudios que definir la etapa óptima para indicar el tratamiento con PC en pacientes con COVID-19.
El proceso de transfusión es el mismo al efectuado con el plasma fresco congelado (PFC), respetando la compatibilidad ABO y según normas establecidas a nivel nacional9. En relación a la dosis, las recomendaciones sugieren administrar 200 a 400 ml como dosis única y una o dos dosis adicionales en función a la gravedad y la tolerancia del paciente7,18. El tiempo de administración como sucede con el PFC es de 10-20 ml/Kg/hora22, se debe considerar un mayor tiempo de administración en pacientes con riesgo de sobrecarga circulatoria.
Reacciones adversas
Como sucede con cualquier hemocomponente, la transfusión de PC supone el riesgo de reacciones adversas como: reacciones febriles no hemolíticas, reacciones alérgicas, infecciones asociadas a la transfusión, reacciones hemolíticas y aquellas más graves como la lesión pulmonar aguda relacionada a la transfusión (TRALI) o la sobrecarga circulatoria asociada a la transfusión (TACO)23.
Hacemos énfasis en TRALI y TACO al ser las reacciones adversas más severas y pueden poner en riesgo la vida24. Se describieron varios factores de riesgo para estas complicaciones, entre las que destacan: ventilación mecánica, balance hídrico positivo, shock, edad avanzada, disfunción cardiaca entre otras23,24. Varios de los factores mencionados pueden estar presentes en pacientes con COVID-19 grave o crítico.
Se debe prestar la atención suficiente para identificar de manera oportuna estas complicaciones. Si bien en la mayoría de los pacientes con COVID-19 graves y críticos puede ser difícil de identificar estas complicaciones, se debe sospechar ante cualquier deterioro súbito de los parámetros respiratorios o inestabilidad hemodinámicas posteriores a la transfusión. Tanto el TRALI como el TACO habitualmente se presentan dentro de las 6 horas después de la transfusión24.
En el escenario actual dentro de un protocolo de PC para COVID-19, el donante debe ser preferentemente de sexo masculino o una mujer sin antecedentes de embarazos ni abortos, este es un factor que disminuye la probabilidad de TRALI9. En el caso del TACO sugerimos identificar los factores de riesgo y considerar un mayor tiempo de infusión con un control estricto del balance hídrico.
En relación al riesgo de transmisión del SARS-CoV-2, no se considera un agente relevante de transmisión a través de transfusiones, solo el 1% de los pacientes sintomáticos tendría el ARN de virus en la sangre20. Como indicamos previamente algunas recomendaciones sugieren la detección del ARN virus en el plasma recolectado antes de la transfusión18.
Un estudio reciente, evaluó 5 000 pacientes hospitalizados con COVID-19 grave o potencialmente mortal que recibieron PC25. La incidencia de todos los eventos adversos graves en las primeras cuatro horas después de la transfusión fue menor al 1% y una tasa de mortalidad reportada del 0.3%. De treinta y seis eventos adversos graves reportados, solo dos se consideraron estar relacionados directamente con la transfusión.
En consecuencia, si bien existe el riesgo de reacciones adversas asociadas a la transfusión de PC en pacientes con COVID-19, los estudios disponibles a la fecha concluyen que la incidencia es muy baja.
Conclusiones
COVID-19 representa uno de los retos más grandes para la medicina en los últimos años y probablemente la mayor crisis de salud mundial. Aun no se disponen de tratamientos y vacunas específicas para la enfermedad.
El PC es una estrategia terapéutica que se ha utilizado en otras enfermedades virales en el pasado, demostrando resultados positivos. Los primeros estudios que evaluaron este tratamiento en paciente con COVID-19 especialmente críticos, muestran que tiene un impacto positivo en la recuperación de los pacientes; reducción de la carga viral y reducción de la mortalidad. Además, en general no se reportaron efectos adversos significativos.
El tratamiento con PC es una medida terapéutica que ante la emergencia de un nuevo agente viral como sucede con el SARS-CoV-2, puede convertirse en una estrategia de tratamiento de disponibilidad inmediata.
Reconocemos que aún no se puede llegar a una conclusión definitiva sobre la efectividad, dosis óptimas y el momento ideal del tratamiento con PC en pacientes con COVID 19. Se requieren con urgencia resultados de ensayos clínicos aleatorizados, muchos de los cuales están en curso.
Referencias bibliográficas
1. Wang LS, Wang YR, Ye DW, Liu QQ. A review of the 2019 Novel Coronavirus (COVID-19) based on current evidence. Int J Antimicrob Agents 2020:105948
2. Cucinotta D, Vanelli M. WHO Declares COVID-19 a Pandemic. Acta Biomed. 2020;91(1):157‐160. [ Links ]
3. Ministerio de Salud. Guía para el manejo del COVID-19. Versión mayo de 2020. La Paz: Unidad de epidemiologia DGSS; 2020
4. Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, He JX et al. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med. 2020; 382(18):1708-1720. [ Links ]
5. Rismanbaf A. Potential Treatments for COVID-19; a Narrative Literature Review. Arch Acad Emerg Med. 2020;8(1):e29. [ Links ]
6. Chen L, Xiong J, Bao L, Shi Y. Convalescent plasma as a potential therapy for COVID-19. Lancet Infect Dis. 2020;20(4):398‐400. [ Links ]
7. Shen C, Wang Z, Zhao F, Yang Y, Li J, Yuan J, et al. Treatment of 5 Critically Ill Patients With COVID-19 With Convalescent Plasma. JAMA. 2020;323(16):1582‐1589. [ Links ]
8. Duan K, Liu B, Li C, Zhang H, Yu T, Qu J et al. Effectiveness of convalescent plasma therapy in severe COVID-19 patients. Proc Natl Acad Sci. 2020;117(17):9490-9496. [ Links ]
9. Programa Nacional de Sangre del Ministerio de Salud. Obtención y uso del plasma hiperinmune obtenido por plasmaferesis en pacientes con COVID-19. Version mayo 2020. La Paz: Programa Nacional de Sangre – DGSS; 2020
10. Brown BL, McCullough J. Treatment for emerging viruses: Convalescent plasma and COVID-19. Transfus Apher Sci. 2020;102790. [ Links ]
11. Zhang J, Xie B, Hashimoto K. Current status of potential therapeutic candidates for the COVID-19 crisis. Brain Behav Immun. 2020;S0889-1591(20)30589-4. [ Links ]
12. Alzoughool F, Alanagreh L. Coronavirus drugs: Using plasma from recovered patients as a treatment for COVID-19. Int J Risk Saf Med. 2020;31(2):47‐51. [ Links ]
13. Rojas M, Rodríguez Y, Monsalve DM, Acosta-Ampudia Y, Camacho B, Gallo JE, Rojas-Villarraga A, et al. Convalescent plasma in Covid-19: Possible mechanisms of action. Autoimmun Rev. 2020:102554. [ Links ]
14. Ye M, Fu D, Ren Y, Wang F, Wang D, Zhang F, et al. Treatment with convalescent plasma for COVID-19 patients in Wuhan, China. J Med Virol [Internet] 2020 [citado el 20 de mayo de 2020];10.1002/jmv.25882. Disponible en: https://onlinelibrary.wiley.com/doi/full/10.1002/jmv.25882
15. Ahn JY, Sohn Y, Lee SH, Cho Y, Hyun JH, Baek YJ, et al. Use of Convalescent Plasma Therapy in Two COVID-19 Patients with Acute Respiratory Distress Syndrome in Korea. J Korean Med Sci. 2020;35(14):e149. [ Links ]
16. Zeng QL, Yu ZJ, Gou JJ, Li GM, Ma SH, Zhang GF, et al. Effect of Convalescent Plasma Therapy on Viral Shedding and Survival in COVID-19 Patients. J Infect Dis. 2020; 222 (1):38-43. [ Links ]
17. Food and Drug Administration. Recommendations for Investigational COVID-19 Convalescent Plasma [Internet]. FDA. 2020 [citado el 2 de mayo de 2020]. Disponible en: https://www.fda.gov/vaccines-blood-biologics/investigational-new-drug-ind-or-device-exemption-ide-process-cber/recommendations-investigational-covid-19-convalescent-plasma.
18. Epstein J, Burnouf T. Points to consider in the preparation and transfusion of COVID-19 convalescent plasma. Vox Sang [Internet] 2020 [citado el 25 de mayo de 2020];10.1111/vox.12939. Disponible en: https://onlinelibrary.wiley.com/doi/full/10.1111/vox.12939
19. Tiberghien P, de Lamballerie X, Morel P, Gallian P, Lacombe K, Yazdanpanah Y. Collecting and evaluating convalescent plasma for COVID-19 treatment: why and how?. Vox Sang [Internet] 2020 [citado el 25 de mayo de 2020];10.1111/vox.12926. Disponible en: https://onlinelibrary.wiley.com/doi/full/10.1111/vox.12926
20. Bloch EM, Shoham S, Casadevall A, et al. Deployment of convalescent plasma for the prevention and treatment of COVID-19. J Clin Invest. 2020;130(6):2757-2765. [ Links ]
21. Zhang L, Pang R, Xue X, Bao J, Ye S, Dai Y, et al. Anti-SARS-CoV-2 virus antibody levels in convalescent plasma of six donors who have recovered from COVID-19. Aging. 2020;12(8):6536-6542. [ Links ]
22. Robinson S, Harris A, Atkinson S, Atterbury C, Bolton-Maggs P, Elliott C et al. The administration of blood components: a British Society for Haematology Guideline. Transfus Med. 2018;28(1):3‐21. [ Links ]
23. Pandey S, Vyas GN. Adverse effects of plasma transfusion. Transfusion. 2012;52 Suppl 1(Suppl 1):65S‐79S.
24. Delaney M, Wendel S, Bercovitz RS, Cid J, Cohn C, Dunbar NM, et al. Transfusion Reactions: Prevention, Diagnosis, and Treatment. Lancet. 2016;388(10061):2825-2836. [ Links ]
25. Joyner JM, Wright RS, Fairweather D, Senefeld JW, Senefeld J, Bruno K, Klassen S, et al. Early safety indicators of COVID-19 convalescent plasma in 5,000 patients. medRxiv [Internet]. 2020 [citado el 20 mayo de 2020]. Disponible en: https://www.medrxiv.org/content/10.1101/2020.05.12.20099879v1.