Serviços Personalizados
Journal
Artigo
Indicadores
Links relacionados
Compartilhar
Gaceta Médica Boliviana
versão On-line ISSN 1012-2966
Gac Med Bol vol.42 no.1 Cochabamba jun. 2019
Caso Clínico
Antimoniato de meglumine perilesional en leishmaniasis cutánea con falla terapéutica sistémica: serie de casos
Perilesional meglumine antimonate in cutaneous leishmaniasis with systemic therapeutic failure: series of cases
Ernesto Rojas Cabrera1,a, Aleida Verduguez-Orellana1,b,c, Marisol Córdova Rojas1,b, Miguel Guzmán-Rivero1,d
1Centro Universitario de Medicina Tropical (CUMETROP), Facultad de Medicina, Universidad Mayor de San Simón. Cochabamba, Bolivia.aMédico especialista en Medicina Tropical, bMaster en Inmunología, cMaster en Epidemiologia clínica, dPhDBioquímica pura y aplicada.*Correspondencia a: Ernesto Rojas Cabrera. Correo electrónico: ernesto.rojas.cabrera@gmail.com
Recibido el 09 de abril de 2019.
Aceptado el 06 de mayo de 2019.
Resumen
En Bolivia, los medicamentos utilizados para el tratamiento de la leishmaniasis cutánea son los antimoniales, de aplicación sistémica en dosis/kg peso, los cuales provocan efectos adversos por la aplicación en largos periodos y grandes volúmenes. La aplicación perilesional de antimonio tiene similar eficacia terapéutica que la sistémica. Sin embargo, no se cuenta con información documentada respecto a la eficacia del tratamiento perilesional en pacientes con falla terapéutica, posterior al tratamiento sistémico. El objetivo de esta serie de casos fue evaluar el tratamiento perilesional con glucantime®, en pacientes con leishmaniasis cutánea y falla terapéutica, posterior a un primer ciclo de tratamiento sistémico con antimoniales. El estudio se realizó con once pacientes con leishmaniasis cutánea con falla terapéutica, posterior a la administración de un primer ciclo de tratamiento sistémico con glucantime® procedentes de la zona tropical de Bolivia. Se consideró como falla terapéutica la persistencia de la lesión y presencia de parásitos obtenidos de los bordes de la lesión. La intervención perilesional consistió en la aplicación día por medio de glucantime® en cinco sesiones. La inoculación se realizó sobre el borde de la lesión y la dosificación del medicamento se calculó multiplicando el área de la lesión por el factor 0.008. Todos los pacientes presentaron dolor local durante el momento de inoculación del medicamento, así como también presentaron un ligero agrandamiento del área de la lesión después de la primera aplicación del medicamento En las siguientes inoculaciones se observó la reducción progresiva del área de la lesión hasta su completa cicatrización.
Palabras claves: leishmaniasis cutánea, falla terapéutica, tratamiento perilesional, efectos adversos
Abstract
In Bolivia, the drugs used for the treatment of cutaneous leishmaniasis are the antimonials by systemic application in doses / kg/weight, which cause adverse effects due to the applications in long periods and large volumes. The perilesional application of antimony has similar therapeutic efficacy than the systemic one. However, there is no documented information regarding the efficacy of perilesional treatment in patients with therapeutic failure after systemic treatment. The aim of this series of cases was to evaluate the perilesional treatment with Glucantime®, in patients with cutaneous leishmaniasis and therapeutic failure, after a first cycle of systemic treatment with antimonials. The study was conducted with eleven patients with cutaneous leishmaniasis and therapeutic failure, after the administration of a first cycle of systemic treatment with Glucantime®. from the tropical zone of Bolivia. The persistence of the lesion and the presence of parasites at the edge of the lesion were considered as therapeutic failure. The perilesional intervention consisted in the application past one day of glucantime® in five sessions. The inoculation was performed on the edge of the lesion and the dosage of the medication was calculated by multiplying the area of the lesion by the factor 0.008. All the cases presented local pain during the time of inoculation of the drug, as well as a slight enlargement of the area of the lesion after the first inoculation of the drug. In the following inoculations the progressive reduction of the area of the lesion was observed until its complete healing.
Keywords: cutaneous leishmaniasis, therapeutic failure, perilesional treatment, adverse effects
La leishmaniasis cutánea en Bolivia constituye la forma clínica más frecuente1 y es un importante problema de salud pública en el país2. Los medicamentos recomendados para el tratamiento de esta enfermedad son escasos3,4 y su eficacia terapéutica es variable5. La aplicación sistémica de antimoniales en dosis/kg peso por vía intramuscular es la más habitual6-8, sin embargo, tienen el inconveniente de producir efectos adversos que van de moderados a severos por la toxicidad del medicamento9-11, debido a los largos periodos de aplicación (20 días) y grandes volúmenes de medicamento que deben ser aplicados diariamente. Otro aspecto asociado a este inconveniente, es el costo elevado de los medicamentos para pacientes de los países en vías de desarrollo12,13. Alternativamente, estudios previos han evaluado la aplicación perilesional de fármacos con antimonio con similar eficacia terapéutica que la aplicación sistémica, tomando como criterios la ausencia de efectos adversos severos y el menor tiempo de aplicación en comparación a los 20 días de la aplicación sistémica14-18.Sin embargo, no se cuenta con información previamente documentada respecto a la aplicación perilesional de antimoniato de meglumine en pacientes con leishmaniasis cutánea que muestran falla terapéutica posterior al tratamiento sistémico, cuya falla podría responder a factores asociados al parásito como al paciente19, entre otros, pero que no están completamente dilucidados. En este sentido, el objetivo de la presentación de esta serie de casos fue evaluar el tratamiento perilesional con antimoniato de meglumine, en pacientes con leishmaniasis cutánea y falla terapéutica, posterior a un primer ciclo de tratamiento sistémico con antimoniales, con el propósito de establecer alternativas terapéuticas seguras y de bajo costo.
En la presente serie de casos, fueron incluidos once pacientes con diagnóstico de leishmaniasis cutánea con falla terapéutica, posterior a la administración de un primer ciclo de tratamiento sistémico con antimoniato de meglumine (glucantime®), en dosis 20mg/kg peso, por 20 días. Los pacientes fueron atendidos en el Centro Universitario de Medicina Tropical (CUMETROP) de la Facultad de Medicina, Universidad Mayor de San Simón entre abril de 2013 y enero de 2018. Para la inclusión de los pacientes al estudio, se consideró como falla terapéutica la persistencia de la lesión inicial con un diámetro igual o menor a 3 x 3 cm (900 mm2), presencia de úlcera satélite o cicatrización incompleta, además de la confirmación por laboratorio de la presencia de parásitos obtenidos del borde de la o las lesiones, posterior a los cuarenta y cinco días de concluida la administración intramuscular de glucantime® (20mg/kg -peso por 20 días).
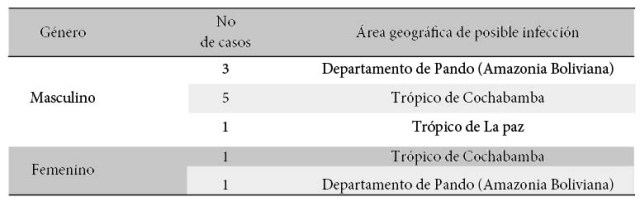
Todos los pacientes eran residentes de la zona tropical de Bolivia. La tabla 1, muestra la distribución del número de pacientes por género y área geográfica de probable infección. La edad de los pacientes estaba comprendida en el rango de 21 y 38 años con una media de 28 años.
Tabla 1. Distribución de los casos según género y área geográfica de procedencia
Antecedentes clínico terapéuticos
Al inicio del primer tratamiento (sistémico), los pacientes presentaban una sola lesión cutánea en las extremidades superiores o inferiores (Tabla 2), clínicamente compatible con leishmaniasis y confirmado por los hallazgos de laboratorio de formas amastigotes y promastigotes mediante exámenes parasitológicos a partir de raspado y/o aspirado del borde interno de la lesión20,21. El periodo transcurrido entre la aparición de la lesión y el inicio del primer tratamiento con glucantime® (20mg/kg-peso/día por 20 días) administrado por vía intramuscular fue variable (entre 3 y 27 meses). Concluida la última aplicación del medicamento, diez de los casos presentaron persistencia de la lesión activa con diámetro variable. Solo uno de los casos presentó una lesión satélite observado durante los controles posterior a la conclusión del tratamiento. Sin embargo, en ninguno de los casos se encontró linfangitis y/o adenopatías, que de haberse presentado hubieran sido excluidos del tratamiento perilesional.
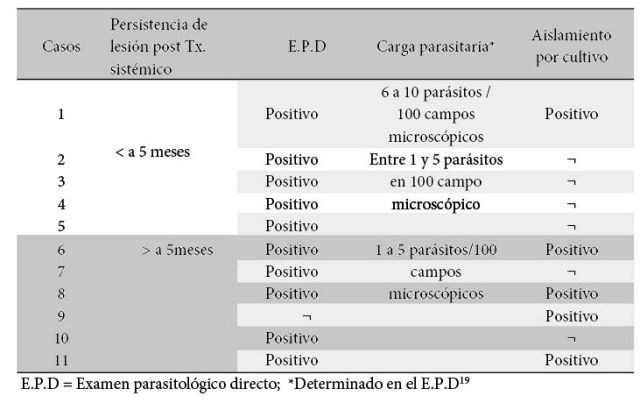
Tabla 2. Resultados de laboratorio antes del tratamiento perilesional
Intervención terapéutica con antimonio perilesional
Todos los casos antes de la aplicación del tratamiento perilesional tenían parásitos en las lesiones (determinados por técnicas de laboratorio) independientemente de la antigüedad que tenía la lesión, después de haber concluido el tratamiento sistémico (Tabla 2).
La intervención perilesional consistió en la aplicación de glucantime® en cinco sesiones, aplicados día por medio. La cantidad de medicamento administrado en cada sesión fue calculada multiplicando el área de la lesión por el factor 0.00818.
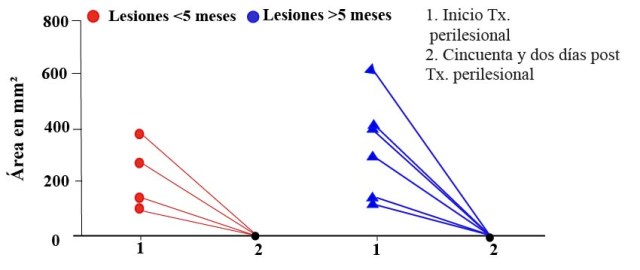
La inoculación se realizó sobre el borde de la lesión en cada punto cardinal con una jeringuilla para aplicación de insulina. El área de las lesiones previas a la intervención perilesional fue variable, pero todas llegaron a la cicatrización completa a los cincuenta y dos días posterior a la última aplicación (Figura 1).
Figura 1. Área de la lesión de cada paciente antes de iniciar el tratamiento perilesional con Glucantime® (1) y después de un
mes de concluido el tratamiento (2) con la cicatrización completa de las lesiones en todos los casos.
Hallazgos
En todos los casos se presentó como efecto no deseado, dolor local durante la aplicación del medicamento, que desapareció tan pronto se concluyó con la inoculación. Así mismo en nueve de los 11 casos se presentó un ligero aumento del área de la lesión después de la primera aplicación del medicamento reducción progresiva posterior.
Finalmente se realizó un seguimiento clínico mensual durante los siguientes cuatro meses después de la última aplicación perilesional. Durante ese periodo de tiempo no se observó cambios clínicos que sugieran recidivas o reactivación de la lesión (Figura 2).
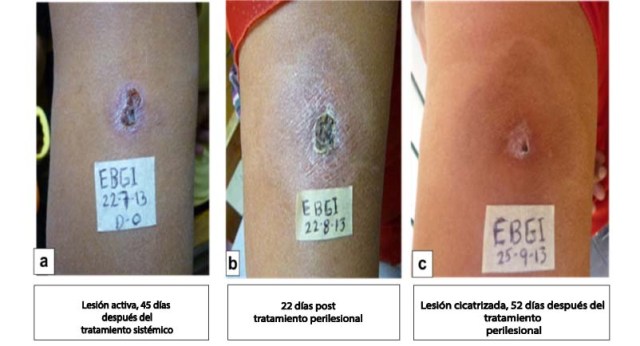
Figura 2. Seguimiento clínico y evaluación del proceso de cicatrización post tratamiento.
a= Post tratamiento sistémico; b,c= post tratamiento perilesional en dos momentos diferentes
Discusión
El tratamiento de la leishmaniasis cutánea en Bolivia, consiste en la aplicación sistémica de antimonio6-8, como tratamiento de primera línea22. Diversos reportes demostraron efectos de toxicidad cardiaca, renal y hepática provocadas por el antimonio9,11,25, con una tasa de curación entre el 70 y 90% en países de Latinoamérica5,9-11, esto depende mayoritariamente de la especie de leishmania implicada en el desarrollo de la enfermedad5. El tratamiento perilesional con antimoniales, de acuerdo con diversos reportes tiene una tasa de curación variable entre 42% y 90 %, en función del tamaño de las ulceras; el número de las mismas, así como también de la especie de leishmania implicada en la infección14-18. En pacientes bolivianos con una única lesión cutánea se alcanzó una tasa de curación de 70%18. El tratamiento perilesional aplicado a los once casos del presente reporte alcanzó 100% de cicatrización de las úlceras y sin evidencias de recaída hasta seis meses después de concluido el tratamiento, probablemente porque los pacientes recibieron un primer tratamiento sistémico con antimonio con el cual no alcanzaron la cicatrización completa, lo cual fue considerado como falla terapéutica23,24. Sin embargo, es necesario realizar otros estudios que permitan clarificar estos aspectos. Los efectos adversos por la aplicación perilesional reportados en este estudio, fueron principalmente dolor local durante el tiempo de inoculación del medicamento de manera similar a lo reportado previamente por otros estudios que señalan al dolor local como el efecto adverso más frecuente con este tipo de tratamiento14-18, así mismo en este estudio se observó en todos los casos un agrandamiento de la ulcera después de la primera aplicación que podría ser una reacción alérgica local de corta duración, que fue desapareciendo gradualmente hasta la tercera aplicación. El tratamiento perilesional aplicado a estos once casos constituye una estrategia de tratamiento ante la falla terapéutica del tratamiento sistémico en un primer ciclo y es el primer reporte en este sentido, pues las investigaciones previas sobre el uso del tratamiento perilesional fue evaluado como alternativa al tratamiento sistémico por la ausencia de efectos cardio y hepatotóxicos así como también por su bajo costo y la mayor adherencia de los pacientes al tratamiento que en promedio es de nueve días frente a 20 días del tratamiento sistémico.
La aplicación perilesional de antimoniales en estos pacientes mostró cicatrización completa a los 52 días post tratamiento perilesional (figura 2) en todos los casos, efectos adversos locales y una buena adherencia al tratamiento. Este reporte debería considerarse como una evaluación piloto para desarrollar futuras investigaciones en este campo para contar con alternativas de tratamiento seguro, de bajo costo y con alta adherencia para los pacientes con falla terapéutica al tratamiento sistémico con antimoniales pentavalentes.
Referencias bibliográficas
1. García AL, Parrado R, Rojas E, Delgado R, Dujardin JC, Reithinger R. Leishmaniasis in Bolivia: comprehensive review and current status. Am J Trop Med Hyg. 2009,80(5):704-711. [ Links ]
2. Rojas E, Parrado R, Delgado R, Reithinger R, García AL. Leishmaniasis in Chaparé Bolivia. Emerg Infect Dis. 2009,15(4):678-680. doi: 10.3201/eid1504.081257. [ Links ]
3. Berman JD. Chemotherapy for leishmaniasis: biochemical mechanisms, clinical efficacy, and future strategies. Rev Infect Dis. 1988, 10 (3):560–586.
4. Murray H, Berman J, Davies C, Saravia N. Advances in leishmaniasis. Lancet 2005, 366:1561–77.
5. Shing S, Sivakumar R. Challenges and new discoveries in the treatment of leishmaniasis. J Infect Chemother. 2004, 10(6):307-315. [ Links ]
6. Organización Panamericana de la Salud (OPS). Manual de procedimientos para vigilancia y control de las leishmaniasis en las Américas. OPS; 2019. Disponible en: http://iris.paho.org
7. Hepburn NC. Cutaneous leishmaniasis: current and future management. Expert Rev Anti Infec Ther. 2003,1(4):563–70.
8. Gonzalez U. Cochrane reviews on neglected diseases: the case of cutaneous leishmaniasis. Cochrane Database Syst Rev. 2013,3: ED000055. doi:10.1002/14651858.ED000055.
9. Ezzine Sebai N, Mrabet N, Khaled A, Zeglaoui F, Krafi M, Fazaa B, Kamoun MR. Side effects of meglumine antimoniate in cutaneous leishmaniasis: 15 cases. Tunis Med. 2010,88(1):9-11. [ Links ]
10. Shanehsaz S M, Ishkhanian S. Therapeutic and adverse effects of standard-dose and low-dose meglumine antimoniate during systemic treatment of Syrian cutaneous leishmaniasis patients. J Pakistan Assoc Dematol. 2014,24(2):115-121. [ Links ]
11. Oliveira AL, Brustoloni YM, Fernandes TD, Dorval ME, Cunha RV, Bóia MN. Severe adverse reactions to meglumine antimoniate in the treatment of visceral leishmaniasis: a report of 13 cases in the southwestern region of Brazil. Trop. Doct. 2009,39:180–182. doi:10.1258/td.2008.080369.
12. Desjeux P. Leishmaniasis: Current situation and new perspectives. Comp Immunol Microbiol Infect Dis. 2004, 27(5):305-318. doi: 10.1016/j.cimid.2004.03.004. [ Links ]
13. Blum J, Lockwood DN, Visser L, Harms G, Baileye MS, Caumes E, Clerinx J, van Thiel P, Morizot G , Hatz C, Buffet P. Local or systemic treatment for New World cutaneous leishmaniasis, Re-evaluating the evidence for the risk of mucosal leishmaniasis. Inter Health. 2012,4 (3): 153–163
14. Alkhawajah AM, Larbi E, Al-Gindan Y, Abahussein A, Jain S. Treatment of cutaneous leishmaniasis with antimony: intramuscular versus intralesional administration. An Trop Med Parasitol. 1997, 91(8):899-905. [ Links ]
15. Asilian A, Sadeghinia A, Faghihi G, Momeni A. Comparative study of the efficacy of combined cryotherapy and intralesional meglumine antimoniate (Glucantime) vs. cryotherapy and intralesional meglumine antimoniate (Glucantime) alone for the treatment of cutaneous leishmaniasis. Int J Dermatol. 2004, 43(4):281-3. [ Links ]
16. Faghihi G, Tavakoli-kia R. Treatment of cutaneous leishmaniasis with either topical paromomycin or intralesional meglumine antimoniate. Clin Exp Dermatol. 2003,28:13-16. [ Links ]
17. Sadeghian G, Nilfroushzadeh MA, Iraji F. Efficacy of local heat therapy by radiofrequency in the treatment of cutaneous leishmaniasis, compared with intralesional injection of meglumine antimoniate. Clin Exp Dermatol. 2007,32:371-374. [ Links ]
18. Soto J, Rojas E, Guzman M, Verduguez A, Nena W, Maldonado M, Cruz M, Gracia L, Villarroel D, Alavi I, Toledo J, Berman J. Intralesional antimony for single lesions of bolivian cutaneous leishmaniasis. Clin Infect Dis. 2013,56(9):1255-60. [ Links ]
19. Rojas R,Valderrama L, Valderrama M, Varona MX, Ouellette M, Saravia NG. Resistance to Antimony and Treatment Failure in Human Leishmania (Viannia) Infection. J Infect Dis. 2006,193:1375-1383. [ Links ]
20. Torrico Rojas MC, Parrado R, Garcia AL. Manual de normas y procedimientos técnicos para leishmaniasis. (Documento técnico) Ministerio de Salud, Bolivia 2010.
21. Bermúdez H, Solano M, Torrico-Rojas M C, Carballo-Montero M, Lafuente-Covarrubias O, Lara-Arias M P, Paredes Torrico P. Diagnóstico de leishmaniasis utilizando medio de cultivo TSTB en pacientes del trópico de Cochabamba. Gac Méd Bol. 2005,28(2):31 – 35.
22. Bolivia, Ministerio de salud. Norma nacional y manual de procedimientos técnicos de leishmaniasis. Ministerio de Salud, 2015. www.sns.gob.bo
23. Arevalo J, Ramirez L, Adaui V, Zimic M, Tulliano G, Miranda-Verástegui C, Lazo M, Loayza-Muro R, De Doncker S, Maurer A, Chappuis F, Dujardin JC, Llanos-Cuentas A. Influence of Leishmania (viannia) species on the response to antimonial treatment in patients with american tegumentary leishmaniasis. J Infect Dis. 2007,195(12):1846-1851. [ Links ]
24. David CV, Craft N. Cutaneous and mucocutaneous leishmaniasis. Dermatol Ther. 2009,22(6):491-502. doi: 10.1111/j.1529-8019.2009.01272.x. [ Links ]
25. Hepburn NC, Siddique I, Howie AF, Beckett GJ, Hayes PC. Hepatotoxicity of sodium stibogluconate in leishmaniasis. Trans. R. Soc. Trop. Med. Hyg. 1994, 88:453–455. doi:10.1016/0035-9203(94)90432-4.