Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta Médica Boliviana
versión On-line ISSN 1012-2966
Gac Med Bol vol.38 no.2 Cochabamba dic. 2015
ARTÍCULO ORIGINAL
Efecto del calcio nixtamalizado en la recuperación del crecimiento en niños con malnutrición crónica dentro de un manejo integral
Eífect of nixtamalized calcium within a comprehensive management in the recovery of growth in children with chronic malnutrition
Sevilla Paz Soldán Ricardo1,a, Antezana Valera Amalia2.a, Zalles Cueto Lourdes3,a, Erostegui Carlos1,a, Castellón Terrazas Silvia2,a
1 Instituto de Investigacones Biomédica (IIBISMED), Facultad de Medicina, UMSS
2 Carrera Biologia, Facultad de Ciencias y Tecnología, UMSS
3 Laboratorio de Investigación Médica (LABIMED), Facultad de Medicina, UMSS
4 LABIMED. Facultad de Medicina-UMSS a Docente investigador
* Correspondencia a: Ricardo Sevilla Paz Soldán Correo electrónico: rsevillap55@hotmail.com
Recibido el 28 de agosto de 2015. Aceptado 15 de septiembre de 2015.
Resumen
Objetivos: valorar el efecto de calcio de maíz nixtamalizado sobre el crecimiento de niños con malnutrición crónica. Previa determinación de características fisicoquímicas, se elaboraron papillas para niños, 63 niños ingresaron al estudio. Métodos: estudio descriptivo controlado y seguimiento longitudinal, fueron incluidos 21 niños con retardo del crecimiento leve a moderado, quienes conformaron el grupo estudio (GE) y se beneficiaron de un esquema integral (clínica, laboratorio, antropometría, psicología, educación, nutrición). E grupo control fue también de 21 niños (GC) y recibió solo zinc como placebo. Ambos grupos fueron comparados con 21 niños sanos (GS) del mismo contexto social. Resultados: los niños del GE mejoraron ZT/E en promedio -1,1 ± 0,7 DS vs -2,5 ± 1,0 del GC (p<0,001) vs. GS 0,13 ± 0,14DS. La respuesta inmunitaria medida por ecografía del timo expresado en mm2fueen GE: 609,5 ± 123,6 DS vs. GC: 471,54 i 93,42DS (p<0,001) vs GS: 545,2 ± 0,8 DS. El desarrollo psicomotor en porcentaje: MF:GE: 97,8 ± 2,9 DS vs .GC: 90,9 ± 5,0 DS (p<0,01) vs.GS 99,5 ± 2,1 DE; MG: GE: 95,8 ± 2,9 vs GC: 80,6 ± 4,6 DS vs (p<0,01) GS: 97,6 ± 5,3DS; DLGE: 95,6 ± 4,1 vs. GC: 82,5 ± 4,8 DE (p<0,001) vs. GS 98,8 ± 5,4 DE; GPS: GE: 96,6 ± 4,8vs. GC: 80,6 ± 4,6 (p<0,001) vs. GS: 99,7 ± 1,0 DS. Asimismo el calcio iónico incrementó en GE: 5,1 ± 0,5 DE vs. GC: 4,1 ± 0,2 DE (p<0,001); GE: 25 hidroxi vitamina D se incrementó 52,5 ± 6,2 ng/ml. En el GE PTH llego a 21,5 ± 5,6 pg /mi y \¡ calcitonina ingresó dentro umbrales esperados 12,2 ± 1,5 pg /mi. Conclusiones: la recuperación del crecimiento de niños es mejor con calcio nixtamalizado dentro de un manejo integral.
Palabras claves: malnutrición crónica, recuperación integral, calcio nixtamalizado.
Abstract
Objective: to assesst effect of corn calcium nixtamalized about the growth of children with chronic malnutrition. Previous determinatiorj of physicochemical characteristics, were prepared porridge for children , 63 children enrolled to the study. Method: descriptive study controlled and longitudinal follow-up work, were included 21 children with slight to modérate delayed growth, who formed the studj group (GE ) and benefited from a comprehensive scheme (clinical, laboratory, anthropometry, psychology, education, nutrition ).Tha control group was also 21 children (GC) and they just received zinc received like placebo. Both groups were compared with 21 health) children (GS) in the same social context. Results: GE children improved ZT/Eon average-1.1 ±0.7 vs.-2.5 ± 1.0DSGC( p<0,001 ) vs.GS 0.13 ±0,14DS.Theimmuneresponsemeasured by ultrasound thymus was expressed in mm2 in the GE group: DSvs. 609.5 ± 123.6GC 471.54 ± 93,42DS ( p<0,001 ) vs GS: 545.2 ± 0.8 DS. Psychomotor development in percentage: MF : GE : 97.8 ± 2.9 vs DS .GC: 90.9 ± 5.0 DS ( p<0,01 ) vs.GS 99.5 ± 2.1 SD; MG : GE : GC 95.8 ± 2.9 vs 80.6 ± 4.6 vs DS ( p<0,01 ) GS: 97.6 ± 5,3DS ; DL : GE : 95.6 ± 4.1 vs. GC: 82.5 ± 4.Í DE ( p<0,001 ) vs. GS: 98.8 ± 5.4 SD; GPS : GE : 96.6 ± 4,8vs . GC: 80.6 ± 4.6 ( p<0,001 ) vs. GS: 99.7 ± 1.0 DS. Also calcium ion GE increasec 5.1 ± 0.5 SD vs. GC: 4.1 ± 0.2 (P < 0.001 ); GE : 25 hydroxy vitamin D was increased 52.5 ± 6.2 ng / mi. In the GE PTH carne to 21.5 ± 5.6 pe /mi and calcitonin entered within expected thresholds 12.2 ± 1.5 pg / mi. Conclusions: the recovery of growth in children is better with calcium nixtamalized within a integrated management.
Keywords: chronic malnutrition, comprehensive recovery, calcium nixtamalized.
El retardo en crecimiento en niños es una patología habitualmente nutricional, inherente a la propia pobreza y ausencia de verdaderas políticas de salud, siendo común en los países en desarrollo. La prevalencia según el Ministerio de Salud de Bolivia llega al 16% en niños menores de 5 años, sin embargo por consulta externa del Hospital del Niño Manuel Ascencio Villarroel son atendidos hasta 50% de niños con algún grado de desnutrición crónica13.
En la atención a niños y mujeres gestantes en el sistema de salud, se trata patologías específicas y no se toma en cuenta el retardo en el crecimiento "in útero". Esta patología es de por sí grave, por afectar al tejido óseo, sistema nervioso, inmunitario, endocrinológico y otros tejidos, por lo que es necesario un abordaje integral desde el inicio de la vida puesto que al momento de la fecundación, el espermatozoide lleva calcio en la parte terminal de su ADN, el cual coadyuva al "fogonazo" que se produce en este instante. Luego de ello existe una lluvia de cromosomas que se van juntando para llegar a una intensa multiplicación celular4 y el niño pueda crecer adecuadamente.
Investigaciones recientes muestran que cuando no se lleva en forma organizada un programa integral como el AIEPI C (atención integral de enfermedades prevalentes de la infancia) muestran como una falla en los resultados5.Por el contrario, la desarrollada en Bolivia con el CLAPSEN permitió la recuperación y reprogramación casi completa de los sistemas orgánicos afectados por la malnutrición5. Está claro que la nutrición y el entorno que rodea al niño o niña son importantes para su crecimiento.
Siguiendo el funcionamiento del cuerpo humano, apreciamos la importancia de la relación cerebro - hipotálamo -hipófisis y su coordinación en la expresión de las diferentes hormonas, su importancia también fue relevada con el uso de alimentos ricos en calcio a nivel de la neurotransmisión6, receptores celulares, comunicación entre células dentro de un entorno donde nace, crece y se desarrolla el niño7.
Así, la estimulación de receptores acoplados a proteínas G, captan la señales externas de la superficie celular, generando la transmisión intracelular de las señales por medio de la interacción proteína-proteína y la ejecución de la respuesta a través de una modificación de la actividad de los genes. Estos genes situados en el núcleo de las células, controlan la herencia de padres a hijos y existe la predisposición a una alteración del crecimiento que será trasmitida, también es necesario conocer que los genes controlan las funciones de las células, determinando qué sustancias, estructuras, enzimas y qué productos químicos participan, pero estos también son modulados por el medio y entorno donde vive el niño o niña7-8. El calcio actúa en el control hormonal, neurotransmisión, inmunomodulación, y en la contracción del músculo. Las células de la glándula pituitaria anterior, con sus receptores específicos para hormonas liberadoras individuales, generalmente responden a través de vías de señalización dependientes de Ca2+, IP3, y PKC (proteína quinasa C), que estimulan la exocitosis de hormonas de las células de la glándula hipofisaria. Estas hormonas hipofisarias son llevadas a través de la circulación sistémica a los tejidos dianas localizados en todo el cuerpo, generando actividades biológicas únicas.
Por otra parte existe un alto contenido del calcio y fosforo en el tejido óseo, el 99% del calcio del cuerpo humano se encuentra en el hueso y representan el 65% de su peso, y más de la mitad del contenido de magnesio de todo el cuerpo se encuentra en este8. Sin embargo, para que la función del calcio sea adecuada necesita de otros nutrientes como fosforo, vitamina D, potasio, iodo, zinc, magnesio y otras vitaminas como la vitamina A, vitamina C7.
Igualmente el calcio tiene una capacidad multifuncional como segundo mensajero en diferentes grupos celulares del sistema inmunitario que incluyen linfocitos T y B, macrófagos, mastocitos, etc.911. El calcio en el espacio extracelular se encuentra solo en 1%, es el principal sustrato para la mineralización de cartílago, hueso y varias formas de secreción endocrina y exocrina.
Al igual que el calcio, la vitamina D demuestra efectos importantes en la multiplicación celular; crecimiento de tejidos, mediador en la respuesta inmunitaria entre ellas a los linfocitos B, linfocitos T, complemento son referidos por diferentes investigaciones1113. Los osteoblastos o células formadoras del hueso poseen receptores nucleares para lau~5 (OH)2 D3, lo que justifica que la vitamina D es esencial para la regulación de la salud ósea, al regular también la función del osteoblasto1416.
Una vez en el interior de la célula el linfocito T o B es activado por su receptor y por proceso de co-estimulación, se produce el reclutamiento y activación de un grupo de proteínas tirocinasas, unidas a otras proteínas adaptadoras que llevan a la fosforilación y activación de la fosfolipasa C-"y (PLCyl en linfocitos T y PLCy2 en linfocitos B). Esta enzima, a su vez, hidroliza el fosfatidilinositol-3, 4-bifosfato (PIP2) de la membrana celular a 2 segundos mensajeros el fostatidil 3 inositol (IP3), y el diacilglicerol (DAG). El IP3 se desplaza y se une a su receptor ubicado en la membrana del retículo endoplásmico (RE), causando la salida del Ca2+ almacenado en su interior y la activación de otras señales intracelulares.17,20
Sin embargo, el agotamiento rápido del Ca2+ en el RE llevaría a una respuesta a este ion de corta duración. Para facilitar la prolongación de las respuestas celulares, se debe activar otra vía de entrada del Ca2+, denominada SOCE, la cual fue descubierta por búsquedas a gran escala de ARN de interferencia. La (SOCE por su sigla en inglés, store operated calcium entry) actúa a través de canales CRAC y su mecanismo de activación depende de la interacción de dos moléculas reguladoras21. Un sensor del Ca2+ en el RE o molécula de interacción estromal (STIM-1, del inglés stromal interaction molecule). Una subunidad poro del canal CRAC (Orail).
Su distribución en los espacios intra y extracelular hace que para su utilización y movilización se requiera de bombas, proteína G y canales especializados, y la influencia del estado de despolarización o repolarización celular. Además, la cantidad y la duración del flujo de Ca2+ van a determinar el tipo y la duración de sus efectos en la señalización intracelular.
Los recientes descubrimientos en relación con la entrada de Ca2+ dependiente de depósito han abierto nuevos caminos en la investigación, y cómo este catión dirige el destino celular, en especial en los linfocitos T y B. Esta revisión se centra principalmente en las funciones del Ca2+ en los grupos celulares y su implicación en autoinmunidad.
Se ha investigado su papel en la proliferación celular y la progresión del ciclo celular en las células HEK293, 48 horas, .previa privación de suero, y un tratamiento de 24 horas con hidroxiurea 1 mM o con 10 M RO-3306 un inhibidor de quinasa 1 dependiente de ciclina, bloqueo del ciclo celular inducida en G1, S y G2 / M, respectivamente. Fue monitorizada la amplitud SOCE; la tensión de células enteras, se redujo notablemente (60-70%) en todas las condiciones, con plena reversibilidad dentro de 4 horas, deprimiendo el canal Orai y STIM-1. RNA resultó en una gran inhibición de SOCE (70-80%), mientras que siSTIM2 tuvo un efecto menor, pero significativo (30%). El tiempo de duplicación de la población de células no se vio afectada en las células STIM1 (18 horas, la misma que en las células de control), pero se incrementó tanto en las células Orail (29 horas) y en siSTIM2 (23 horas), incluso cuando se combina con siSTIMl. Esto sugiere que STIM1 no juega ningún papel en la proliferación celular en las células HEK293 mientras STIM2 está involucrado tanto en SOCE y la proliferación celular en estas células. En este sentido varios estudios profundizan actualmente la importancia de la señalización del calcio, describiéndose mutaciones y roles de las diferentes proteínas intervinientes21,33.
Lo mencionado reafirmalanecesidad de encarar el problema nutricional de retardo en el crecimiento de origen nutricional con un objetivo común, recuperar el funcionamiento celular para un óptimo crecimiento de los tejidos afectados; por lo que el presente estudio evalúa la recuperación del retardo en crecimiento de los niños menores de cinco años, con el uso de calcio nixtamalizado en la alimentación diaria, con un abordaje integral.
Material y métodos
Este estudio es descriptivo, longitudinal prospectivo y controlado. Fue realizado en el servicio de consulta externa del Hospital del Niño Manuel Ascencio Villarroel de Cochabamba, Bolivia. De 750 niños valorados en seis meses, 70 ingresaron al estudio, divididos en tres grupos: 21 conformaron el grupo estudio (GE), 21 el grupo control (GC), y 21 niños sanos (GS) A todos se les realizó seguimiento, excepto a tres niños en el GS, dos en el GC y dos en el GE, por lo que fueron separados del estudio, quedando un total de 63. Los niños ingresaron al grupo estudio previo consentimiento firmado por los padres, delante testigo. Los criterios para la inclusión de niños fueron: retardo en crecimiento leve o moderado para el indicador T/E (OMS-2006), sin infecciones graves, anemia ni hipotiroidismo.
En cuanto al manejo nutricional, a los niños del grupo estudio (GE) se les dio un aporte de calcio nixtamalizado dos veces al día según demanda, que contenía 40 g de maíz nixtamalizado, 20 g de manzana o pina, y agua hasta una cantidad suficiente para completar a 200 ce. Adicionalmente se dio, vitaminas y minerales en jarabe, y se brindó el cuidado de recuperación integral nutricional aplicando la estrategia CLAPSEN (Clínica, Laboratorio, Antropometría, Psicología y Nutrición. Con actividades basadas en la buena alimentación, orientación nutricional y estimulación del desarrollo)34.
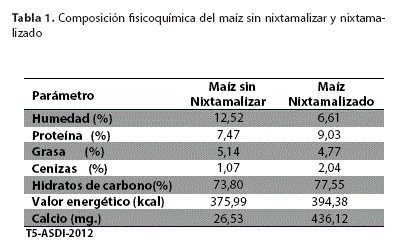
El calcio nixtamalizado fue preparado con maíz, "variedad cubano amarillo" producido en el valle de Cochabamba, provincia de Cliza, luego de ser cocido por una hora con hidróxido de calcio al 2%, se mantuvo en remojo durante 12 horas, para luego está sometido a un proceso de secado y molido, posteriormente se preparó en forma de papillas (Tabla 1) para finalmente ser envasado y administrado a los niños con retardo en crecimiento previas pruebas fisicoquímicas en la que se constató un incremento de concentración de 26 mg/100 g de calcio sin nixtamalizar hasta 436 mg/100 g en el maíz nixtamalizado al igual que hicieron otros autores35. Además se valoró la composición de diferentes papillas y se realizaron pruebas de degustación, la administración fue en dos tiempos de comida durante el día por espacio seis semanas.
El grupo GC recibió zinc a la dosis estándar de 2 mg/ kg/día, no recibió calcio nixtamalizado ni recibió manejo integral. El grupo GS recibió dieta habitual, con aporte nutricional normal para la edad cumpliendo las características de adecuación, suficiencia, densidad, variedad, volumen y respeto de horarios, dentro de un entorno propicio para su crecimiento y desarrollo. A los pacíentnes del GC y del GS se les citó para comprobar la ausencia de patología y realizarse la evaluación bioquímico-inmunonutricional a las seis semanas.
A todos los niños que ingresaron al estudio, tomaron peso, talla, perímetro cefálico, perímetro braquial, pliegue cutáneo, y ecografía de la superficie del timo. Asimismo se tomaron muestras sanguíneas para la determinación de calcio iónico, vitamina D3, y las hormonas calcitonina y paratohormona (PTH).
Los resultados fueron procesados por SPSS.statisticsl9, utilizándose la prueba de t de student para valorar diferencias entre grupos.
Resultado
El promedio de edad fue de 22 ± 13,3 meses; 56,2 % fueron del sexo masculino y 43,7% del sexo femenino. El promedio de talla de los niños del GE fue al ingreso de 77,5 ± 10,1 DS y al egreso 82,7 ± 9,4 DS, mientras que para el grupo control al inicio del estudio fue de 75,5 ± 6,7 DS y al egreso 75,5 ± 6,7 DS. En el grupo de niños sanos, la talla de ingreso fue 83,7 ± 12,6 y al egreso 85,3±12,5.
Se calculó el incremento de la talla en los tres grupos: el grupo estudio mejoró 5,2 ± 2 cm, el grupo control no tuvo incremento en talla y el grupo de niños sanos 1,6 cm.
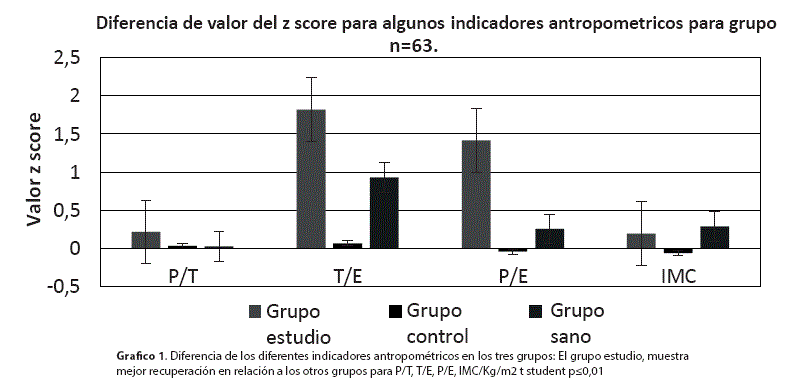
Se calculó el puntaje Z para los parámetros peso talla (ZP/T), talla edad (ZT/E), peso edad (ZP/E) y el índice de masa corporal/kg/m2 (ZIMC), para cada grupo, y se calculó la diferencia entre la semana 0 al ingreso al estudio y la sexta semana, encontrándose disminución de z score para el grupo estudio.
Estas diferencias expresadas como reducción se multiplicaron por -1 para visualizar la magnitud de mejoría y se encontró que el grupo estudio tenía mejoría sustancial respecto al grupo control y al de niños sanos, cuyos valores fueron significativos por prueba de T de Student p<0,5; **p<0,01 (Gráfico 1).
La variación del perímetro cefálico ZPC en el GE al ingreso fue de -0,93 ± 1,2 DS y al egreso -0,86 ± 0,7 DS; la del CG -1,1 ± 0,3 DS al ingreso y 0,3 ± 0,9 al egreso, y la del GS:-1,1 ± 0,6 DS al ingreso y 0,6 ± 0,7 DS al egreso. El indicador pliegue cutáneo ZPCT al ingreso para GE fue 0,38 ± 1,4 DS y al egreso 1,6 ± 2,2 DS (p<0,05*), con diferencia significativa. La variación del perímetro braquial ZPB fue al ingreso para el GE -1,3 ± 1,5 DE, y al egreso 1,5 ± 5,6 DS, para el GC -0,7 ± 0,8 DS al ingreso y -1,0 ± 0,7 DE al egreso y para GS -0,96 ± 0,7 DS : al ingreso y -0,7 ± 0,6 DS al egreso.
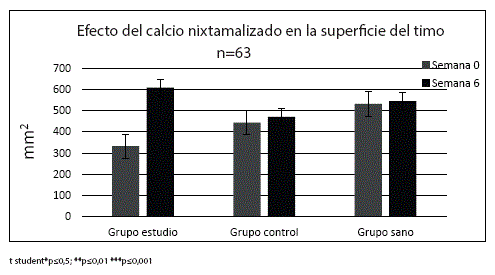
Por otro lado, la respuesta inmunitaria, medida por ecografía del timo, también mejoró. Para el GE fue de 609,5 ± 123,6 DS (mm2), y para el GC 471,54 ± 93,42 DS mm2 (p<0,001) (Gráfico 2).
El gráfico 2 muestra el efecto del calcio nixtamalizado y el manejo integral sobre la superficie del timo. Véase que el crecimiento en porcentaje del timo del grupo estudio es bastante mayor que el del grupo control y del grupo sano.
Los parámetros bioquímico-nutricionales, particularmente el calcio, hormona paratiroidea, vitamina D3, y la calcitonina fueron relevantes. El calcio iónico se incrementó significativamente en el GE de 2,1 mg/dl ± 0,6 DS al inicio a 5,1 + 0,5 DS al terminar el estudio, mientras que en el GC no tuvo variación (4,1 ± 0,2 DS) y en el GS se mantuvo dentro lo normal. En el GE, los valores sanguíneos de 25 hidroxivitamina D se incrementaron a 52,5 ± 6,2 ng/ml, a la vez que la hormona paratiroidea llego a 21,5 ± 5,6 pg/ml y la calcitonina ingresó dentro los umbrales esperados 12,2 ±1,5 pg/ml (Gráfico 3).
El gráfico 3 muestra los valores laboratoriales de calcio, vitamina D3 y hormonas paratiroidea y calcitonina medidos en niños de los tres grupos en la semana 0 y semana 6. Los cuatro parámetros mejoraron en los niños del GE, mientras que para el GC no hay diferencia, y para el GS tampoco hay diferencia pero sus valores son normales.
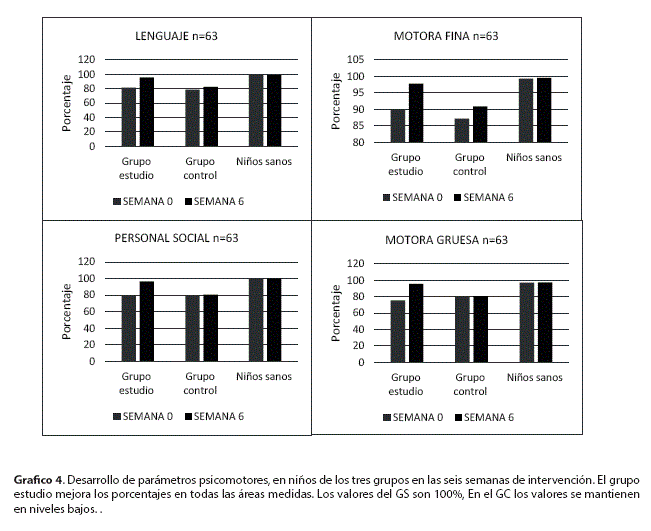
El progreso del desarrollo psicomotor expresado en porcentaje en las diferentes áreas fue mayor en el grupo estudio (Gráfico 4). Los valores encontrados son los siguientes: motor fino GE: 97.8 ± 2,9 DS, GC: 90,9 ± 5,0 DS (p<0,01) y GS: 99,5 ± 2,1 DS; motor grueso: GE, 95,8 ± 2,9 DS, GC, 80,6 ± 4,6 (p<0,01) y GS, 97,6 ± 5,3 DS. DL: GE: 95,6 ± 4,1 vs. GC: 82,5 ± 4,8 DS.(p<0,001) vs. GS:9 8,8 ± 5,4 DS; GPS: GE:96,6 ± 4,8 vs .GC: 80,6 ± 4,6. (p<0,001) vs. GS: 99,7 ± 1,0 respectivamente.
Grafico 2. Efecto del calcio nixtamalizado y del manejo integral sobre la superficie del timo. Véase que el crecimiento en porcentaje del timo del grupo estudio es bastante mayor que el del grupo control y del grupo sano.
Discusión y Conclusión
El presente trabajo muestra que es posible la recuperación del retardo del crecimiento leve y moderado con el aporte de calcio nixtamalizado dentro de un manejo integral.
El proceso de nixtamalización del tipo de maíz utilizado "Cubano Amarillo" induce cambios estructurales, químicos, funcionales y nutricionales. Uno de los aspectos más importantes al ser descascarillado el maíz, la penetración de agua caliente y acarrea iones de calcio, afecta la pared celular e induce gelatinización parcial del almidón, y aumento de la insolubilidad de las proteínas, reduce la fibra dietética insoluble y aumenta la fibra dietética soluble, así mismo, favorece la disponibilidad de la niacina que no es biodisponible en el maíz, lo cual evita el desarrollo de pelagra, como demostraron varios estudios35.
Al repercutir en el crecimiento, se vio en el estudio, que repercute también en la respuesta inmunitaria y en el desarrollo psicomotor. Efectos favorables de la nixtamalización también fueron reportados en Guatemala con el uso de la "INCAPARINA"36.
El estudio identifica el efecto favorable de una estrategia de intervención integral, con orientación nutricional, estimulación del desarrollo psicomotor, aporte de alimentario se administra zinc, hierro, magnesio, vitamina A, iodo complementado con vitamina D y vitaminas hidrosolubles con aportes mínimos necesarios32.
El resultado fue evidente en el crecimiento, desarrollo y respuesta inmunitaria aunque no llega a lo ideal, pero el progreso es tangible.
Asimismo permite reflexionar sobre los tratamientos puntales con el zinc, que por si sólo podría recuperar el crecimiento, hecho que no vimos en el trabajo. El calcio por si sólo tampoco lo realizaría a pesar de su importancia por las múltiples funciones que realiza en el organismo humano, por tanto el manejo integral es de suma importancia.
El hecho de mejorar los niveles de calcio e hidroxivitamina D, aparentemente promueven el restablecimiento de la calcitonina y PTH, lo que permite inferir que la presencia de calcio produce una mejor señalización celular, responsable del crecimiento, respuesta inmunitaria y desarrollo psicomotor de niños incluidos en el GE, sin embargo es necesario tener en cuenta la influencia de algunas proteínas intracelulares, aspecto no medido en el estudio.

Un aspecto importante que puede influenciar este crecimiento, es la genética. Seguramente la deficiencia de calcio disminuye la expresión de algunos genes, los cuales se activan al aumentar la concentración de calcio, y tienen su efecto particular en el crecimiento y desarrollo, aspectos que son de interés y deberían ser estudiados.
El valor del efecto nutricional del calcio dentro de un entorno familiar y estimulante, mostrado en este estudio, es esencial; no obstante, los avances en la biología molecular cada vez más detallados, deberían permitirnos en el futuro contar con un alimento o una técnica de preparación de alimentos que puedan coadyuvar en el tratamiento de niños con retardo en crecimiento, y ajustar los aportes que son necesarios para el mantenimiento de la buena salud celular, tal como se aprecia en el presente estudio.
Conflictos de interés: los autores declaramos que no existe conflicto de intereses.
Referencias bibliográficas
1. Sevilla R, Erostegui C, Zalles L. Modelo de atención integral del niño en riesgo nutricional menor de 5 años estrategia Mochila Nutricional s. Santivañez. Cochabamba-Bolivia.2015. [ Links ]
2. Banco Mundial Perfil Nutricional del país Antropometría de la niñez www.globalnutritionreport.org. 2014. [ Links ]
3. Laura Manzaneda La mitad de los pacientes se encuentran en estado crónico con secuelas en su desarrollo cognitivo y físico. CADA ANO ATIENDEN A MIL NIÑOS POR DESNUTRICIÓN. Los tiempos Cochabamba Bolivia Sección B local Bl Octubre 2015. [ Links ]
4. "Molecular changes during egg activation". AR Krauchunas, MF Wolfher.Curr Top Dev Biol. 2013 ; 102: 267-292. [ Links ]
5. David Mukunya, Samuel Kizito, Tonny Orach, Regina Ndagire, Emily Tumwakire, Godfrey Zari Rukundo, Ezekiel Muperel and Sarah Kigulil Knowledge of integrated management of childhood illnesses community and family practices (C-IMCI) and association with child undernutrition in Northern Uganda: a cross-sectional study BMC Public Health 2014, 14:976 doi:10.1186/1471-2458-14-976 [ Links ]
6. Sevilla Paz Soldán, Ricardo, Zalles Cueto, Lourdes and Sevilla Encinas Gerard. Efecto de un esquema de monitoreo y tratamiento nutricional en niños desnutridos graves, aproximación a una óptima señalización celular. Gac Med Bol, Dic 2012, vol.35, no.2, p.62-66. ISSN 1012-2966 [ Links ]
7. Sevilla Paz Soldán Ricardo Nutrición en la comunicación- Señalización celular y en la incógnita de la interacción humana Cochabamba Bolivia pp.896 2014 [ Links ]
8. Gil Ángel Tratado de Nutrición Bases fisiológica y bioquímicas de la Nutrición 2a Edición Ed. Panamericana pp.964.2010 [ Links ]
9. Oh-hora M, Rao A. Calcium signaling in lymphocytes. Curr Opin Immunol. 2008; 20:250-8. [ Links ]
10. Shulze-Luehrmann J, Ghosh S. Antigen-receptor signaling to nuclear factor kappa B.Immunity.2006;25:701-15. [ Links ]
11. Holick ME Vitamin D deficiency. N Engl J Med. 2007;357:266-81 [ Links ]
12. Bischoff-Ferrari HA, Giovannucci E, Willett WC, Dietrich T, Dawson-Hughes B. Estimation of optimal serum concentrations of 25-hydroxyvitamin D for múltiple health outcomes. Am J Clin Nutr. 2006;84:18-28. [ Links ]
13. Liu PT, Stenger S, Li H, Wenzel L, Tan BH, Krutzik SR, et al. Toll-like receptor triggering of a vitamin D-mediated human antimicrobial response. Science. 2006;311:1770-3. [ Links ]
14. Gombart A, O'Kelly J. Regulation of the CAMP geneby 1,25 (OH)2 D3 in various tissues. J Steroid Biochem Mol Biol. 2007; 103:552-7. [ Links ]
15. Peleg S, Nguyen C, Woodard BT, Lee JK, Posner GH. Differential use of transcription activation function 2 domain of the vitamin D receptor by 1,25- Dihydroxyvitamin D3 and its A ring-modified analogs. Molecular Endocrinology 1998;12:525-35 [ Links ]
16. Li, W, Llopis, J, Whitney M, Zlokarnik, G & Tsien, R Y (1998). Cell-permeant caged InsP3 ester shows that Ca2+ spike frequency can optimize gene expression. Nature, 392: 936-41. [ Links ]
17. Lage R, Dieguez C; Vidal-Puig A, López M AMPK: a metabolic gauge regulating whole-body energy homeostasis. Trend mol Med 2008; 14:539-49 [ Links ]
18. Craske, M, Takeo, T, Gerasimenko, O, Vaillant, C, Torok, K, Petersen, O H & Tepikin, A V.) Hormone-induced secretory and nuclear translocation of calmodulin: oscillations of calmodulin concentration with the nucleus as an integrator Proc. Nati. Acad. Sci. 1999. USA 96: 4426-4431. [ Links ]
19. Amaia Vela Desojol, Gustavo Pérez de Nanclares, Gema Graul, Aníbal Aguayo, Amaia Rodríguez, Itxaso Rica HIPOPARATIROIDISMO Rev Esp Endocrinol Pediatr 2013;4 Suppl(l):119-128 | Doi. 10.3266/Rev Esp Endocrinol Pediatr.pre2013.Mar. 161 [ Links ]
20. Putney JW. A model for receptor-regulated calcium entry. Cell Calcium. 1986; 7:1-12. [ Links ]
21. Parekh AB, Putney JW. Store-operated calcium channels. Physiol Rev. 2005; 85:757-810. [ Links ]
22. Luik RM, Wu MM, Buchanan J, Lewis RS. The elementary unit of store-operated Ca2+ entry: Local activation of CRAC channels by STIM1 at ER-plasma membrane junctions. JCellBiol.2006;174:815-25. [ Links ]
23. Macian F. NFAT proteins: key regulators of T-cell development and function. Nat RevImmunol.2005;5:472-84. [ Links ]
24. Patrick J. Shaw, Stefan Feske Physiological and pathophysiological functions of SOCE in the immune system. Front Biosci .2012 January 1; 4: 2253-2268. [ Links ]
25. Cullen PJ, Lockyer PJ. Integration of calcium and Ras signaling. Nat Rev Mol Cell Biol.2002;3:339-48. [ Links ]
26. Stathopulos PB, Li GY, Plevin MJ, Ames JB, Ikura M. almacenados Ca 2+oligomerización inducida por el agotamiento de la interacción del estroma molécula 1 (STIM1) a través de la región EF-SAM: un mecanismo de iniciación para capacitiva Ca2+ entrada.. J Biol Chem 2006; 281:. 35855-35862 [ PubMed ] [ Links ]
27. Zhang SL, et al. STIM1 es una Ca 2 + sensor que activa los canales CRAC y migra desde el Ca 2+ tienda para la membrana plasmática. Naturaleza. 2005; 437 :. 902-905 [ PMC libres artículo ] [ PubMed ] [ Links ]
28. Picard C, McCarl CA, Papólos A, et al.STIMl mutation associated with a syndrome of immunodeficiency and autoimmunity. N Engl J Med. 2009; 360: 1971-80. [ Links ]
29. Skibinska-Kijek A , Wisniewska MB, Gruszczynska-Biegala J, et al.Immunolocalization of STIM1 in the mouse brain. Acta Neurobiol Exp (Wars). 2009; 69: 413-28. [ Links ]
30. Byun M, Abhyankar A, Lelarge V, et al.Whole-exome sequencing-based discovery of STIM1 deficiency in a child with fatal classic Kaposi sarcoma. J Exp Med. 2010; 207: 2307-12. [ Links ]
31. Beyersdorf NI, Braun A, Vógtle T, Varga-Szabo D, Galdos RR, Kissler S, Kerkau T, Nieswandt B STIMl-independent T cell development and effector function in vivo. J Immunol. 2009 Mar 15;182(6):3390-7. doi: 10.4049/jimmunol.0802888. [ Links ]
32. Cheng KT1, Liu X, Ong HL, Swaim W, Ambudkar ISPLoS Biol Local Ca2+ entry via Orail regulates plasma membrane recruitment of TRPC1 and controls cytosolic Ca2+ signáis required for specific cell functions.. 2011 Mar;9(3):el001025. doi: 10.1371/journal. pbio.1001025. Epub 2011 Mar 8. [ Links ]
33. Guan-Hung Kuo, 1 Shu-Wei Chang, 1 and Pei-Ju Tsai 1 Ca2+ Signaling in Cytoskeletal Reorganization, Cell Migration, and Cáncer Metástasis Biomed Res Int. 2015;: 409245. [ Links ]
34. Sevilla R, Zalles L, Belmonte G, Chevalier P, Parent Gérard, Katherine Hilderbrand, Kolsteren Patrick. "CLAPSEN" a global approach to the management of severe malnutrition in Bolivia. Cahiers detudes et de recherches francophones / Santé. 2000;10(2):97-102. [ Links ]
35. Silvia Cristina Pérez Solé Revisión de los alcances de la investigación existente sobre alimentos que participan en la síntesis de neurotransmisores en base a su contenido de aminoácidos y cofactores del nacimiento a los 24 meses, Tesis de grado pp72 Guatemala Febrero Agosto2014. [ Links ]
36. Bressani Ricardo Nixtamalización de maíz Publicación INCAP PCE/041 En Agroindustria rural, recursos técnicos y alimentación. Boucher F, Muchnik J, Eds. San José Costa Rica, Serie agroindustrial rural CIRAD-CIID-IICA Nol, Julio 1995, pp.64-82 [ Links ]
37. CASTILLO, V.K.C et al. Efecto de la concentración de hidróxido de calcio y tiempo de cocción del grano de maíz (Zea mays L.) nixtamalizado, sobre las características fisicoquímicas y Teológicas del nixtamal. ALAN [online]. 2009, vol.59, n.4 [citado 2015-06-04], pp. 425-432 [ Links ]
38. Jorge L. Rosado, I.B. M.Sc, Ph.D., Rafael Camacho-Solís, M.C., Héctor Bourges, M.C., Ph.D. Adición de vitaminas y minerales a harinas de maíz y de trigo en México Salud Publica Mex 1999;41:130-137. [ Links ]