Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta Médica Boliviana
versión impresa ISSN 1012-2966versión On-line ISSN 2227-3662
Gac Med Bol v.37 n.2 Cochabamba dic. 2014
Artículo Original
Terapia secuencial para la erradicación de Helicobacter pylori: ¿superior a la triple terapia estándar?
Sequential therapy for Helicobacter pylori eradication: ¿superior to triple standard therapy?
Daniela Torrico Guillen1,a, Karen Claros Espinoza1,a, Bethzi Valdez Guzmán1,b
1Hospital Obrero N°2 - Caja Nacional de Salud, Cochabamba, Bolivia. aResidente de Medicina Interna; bGastroenteróloga. *Correspodencia a: Karen Griselda Claros Espinoza. Correo electrónico: porsiescribes@hotmail.com
Recibido el 19 de junio de 2014.
Aceptado 9 de julio de 2014.
Resumen
Objetivos: establecer la eficacia de la terapia secuencial como tratamiento primario para la erradicación de Helicobacter pylori en comparación con la triple terapia estándar.
Métodos: estudio prospectivo, aleatorizado, abierto, basado en población, incluyéndose pacientes mayores de 15 años que acuden a consulta externa de Gastroenterología del Hospital Obrero Nro. 2 (Cochabamba, Bolivia) de junio a diciembre del 2013. Se definieron dos brazos de estudio: Triple terapia estándar (Omeprazol, Claritromicina, Amoxicilina durante 10 días) y Terapia secuencial (Omeprazol y Amoxicilina por 5 días, seguido de Omeprazol, Claritromicina y Tinidazol por 5 días).
Resultados: se incluyeron en el análisis 200 pacientes. Existió un claro predominio del sexo femenino y edad mayor a 40 años entre los afectados. El porcentaje de erradicación fue del 36% en grupo de terapia estándar y 80% en la terapia secuencial (valor p < 0,001), con una diferencia absoluta del 44% a favor de la terapia secuencial.
Conclusiones: la terapia secuencial fue superior a la triple terapia estándar para la erradicación de helicobacter pylori.
Palabras claves: helicobacter pylori, agentes antibacterianos, terapia secuencial.
Abstract
Objectives: to establish the efficacy of sequential therapy as primary treatment for the eradication of Helicobacter pylori compared with standard triple therapy.
Methods: prospective, randomized, open, based on population study, including patients older than 15 years attending outpatient Gastroenterology Department on Hospital Obrero Nro. 2 (Cochabamba, Bolivia) from june to december 2013. Study has two arms: standard triple therapy (Omeprazole, Clarithromycin, Amoxicillin for 10 days) and sequential therapy (Omeprazole and Amoxicillin for 5 days followed by Omeprazole, Clarithromycin and Tinidazole for 5 days).
Results: we included 200 patients in the study. There was a clear predominance of females and more than 40 years among the affected age. The eradication rate was 36% in the standard therapy group and 80% in the sequential therapy (p <0.001), with an absolute difference of 44% for sequential therapy.
Conclusions: the sequential therapy was superior to standard triple therapy for the eradication of Helicobacter pylori.
Keywords: Helicobacter pylori, antibacterial agents, sequential therapy.
Se estima que más de la mitad de la población mundial está infectada por Helicobacter pylori (HP)1, que se ha relacionado con diferentes enfermedades, entre ellas cáncer gástrico2-4. Como en todos los procesos infecciosos, la meta del tratamiento es la eliminación de la bacteria a través de la anti-bioticoterapia. Sin embargo, debido a mutaciones genéticas y otras modificaciones en la estructura bacteriana la resistencia a los antibióticos es considerada actualmente como la principal causa de fracaso terapéutico5.
En poblaciones con resistencia a claritromicina menor al 20% se recomienda el uso de la Triple Terapia Estándar (TTE) como tratamiento de primera línea, consistente en un inhibidor de la bomba de protones (IBP) + dos antibióticos (claritromicina más amoxicilina o metronidazol). Mientras que si la resistencia a claritromicina es mayor puede iniciarse el tratamiento con terapia cuádruple (con bismuto), secuencial, concomitante o una terapia híbrida6.
Además se ha reportado poblaciones con mayor resistencia a metronidazol (18-22%, hasta 82%) a claritromicina (4-12%)1,7, pudiendo ser resistencia primaria8 o relacionada a exposición previa a antibióticos utilizados en el tratamiento9. En Bolivia no existen estudios publicados en cuanto al perfil de resistencia del H. pylori.
El objetivo del presente trabajo es establecer la eficacia del esquema secuencial (cuádruple terapia secuencial sin bismuto) como tratamiento primario para la erradicación de HP en comparación con la triple terapia (basada en IBP + claritro-micina + amoxicilina) en pacientes de Gastroenterología del Hospital Obrero Nro. 2 en el período de junio a diciembre del 2013. Se plantea la hipótesis de superioridad de la terapia secuencial (TS) para la erradicación de HP.
Material y métodos
Población de estudio, reclutamiento y elegibilidad
Se realizó un estudio prospectivo, aleatorizado, abierto, basado en población, incluyéndose pacientes hombres y mujeres mayores de 15 años que acuden a consulta externa de Gastroenterología del Hospital Obrero Nro. 2 en Cochabamba, Bolivia; durante el período de junio a diciembre del 2013. Se excluyeron los pacientes menores de 15 años y aquellos que recibieron previamente terapia para erradicación de HP, antecedente de alergia a alguno de los medicamentos del esquema de tratamiento propuesto, ingesta de inhibidores de bomba de protones por lo menos 2 semanas antes de ingresar al estudio. Los participantes fueron sometidos a gastroduodenoscopía y biopsia gástrica. Aquellos pacientes con diagnóstico histo-patológico de HP fueron incluidos en el estudio.
Ramdomización
Los pacientes con resultado positivo para HP y con los demás criterios de inclusión, fueron ramdomizados de forma secuencial en dos grupos: a) grupo TTE (omeprazol 20 mg BID + amoxicilinalg BID + claritromicina 500 mg BID por 10 días) o b) grupo TS (omeprazol 20 mg BID + amoxicilina lg BID por cinco días, seguido de omeprazol 20 mg BID + claritromicina 500 mg BID + tinidazol lg BID por cinco días). La medicación fue suministrada por el seguro del hospital en el caso de la TTE, mientras que el costo del tinidazol fue cubierto por el paciente en la TS. A todos los pacientes se les recomendó evitar la ingesta de bebidas alcohólicas, alimentos ricos en grasa y realizar interconsulta con nutricionista.
Una vez concluido el tratamiento, tras 6-8 semanas, los pacientes fueron sometidos a control por gastroduodenoscopía y nueva biopsia gástrica y/o resultado de antígeno para HP en heces, de acuerdo con la valoración clínica del médico tratante.
Consideraciones estadísticas
Nuestra hipótesis fue que la TS es superior a la TTE en la erradicación de HP
El análisis fue realizado por protocolo. Se excluyeron del análisis final aquellos pacientes que no concluyeron tratamiento y quienes no realizaron endoscopía digestiva alta de control post tratamiento y/o el test de antígeno en heces. La comparación entre ambos grupos se realizó por medio de la prueba del chi cuadrado para variables nominales y comparación de medias para muestras no relacionadas para variables cuantitativas. Análisis secundarios fueron realizados en relación con la edad, sexo y comorbilidades. Se determinaron intervalos de confianza del 95% y valor de p, siendo significativo un valor menor a 0,01. No se realizó análisis multivariado para los datos secundarios. Todos los análisis estadísticos fueron realizados con el programa SPSS® 19 a partir de una base de datos de Excel® 2010.
Un total de 1 809 pacientes acudieron a consulta externa de Gastroenterología en el Hospital Obrero Nro. 2 en el período de junio a diciembre del 2013, fueron incluidos en el estudio 364 (20%) pacientes confirmados de infección de HP por histopatología de biopsia gástrica y/o duodenal. Se excluyeron del estudio 129 pacientes en la primera fase debido al antecedente de uso de inhibidores de bomba de protones en las dos semanas previas al estudio, fracaso terapéutico en tratamiento de erradicación previo o antecedente de alergia a algún principio activo de los medicamentos utilizados. Los 238 pacientes restantes fueron ramdomizados de forma aleatoria simple al grupo TTE (117 pacientes) o TS (121 pacientes). Ingresaron al análisis 200 pacientes que completaron el protocolo de estudio (100 del grupo TEE y 100 de TS), excluyéndose del análisis final 17 pacientes del grupo TTE y 21 de TS por estudios o controles incompletos (análisis por protocolo) (Fig. 1).

Figura 1. Esquema de distribución de los pacientes en el estudio.
Resultados
El 15,9% de los pacientes no retornaron a control o no completaron los estudios necesarios, obteniéndose un 84,1% de cumplimiento de seguimiento entre los participantes (ingesta del 100% de la medicación indicada), siendo levemente superior en el grupo de TTE (valor p 0,55). No se estudiaron los motivos del incumplimiento al tratamiento por parte de los pacientes.
Las características de los participantes fueron similares en ambos brazos del estudio (Tabla 1). Predominando las pacientes de sexo femenino, mayores de 40 años en ambos grupos. Los hallazgos endoscópicos y patológicos tampoco mostraron diferencias estadísticamente significativas en cuanto a su dis-
Tabla 1. Características generales de los pacientes incluidos en el estudio.
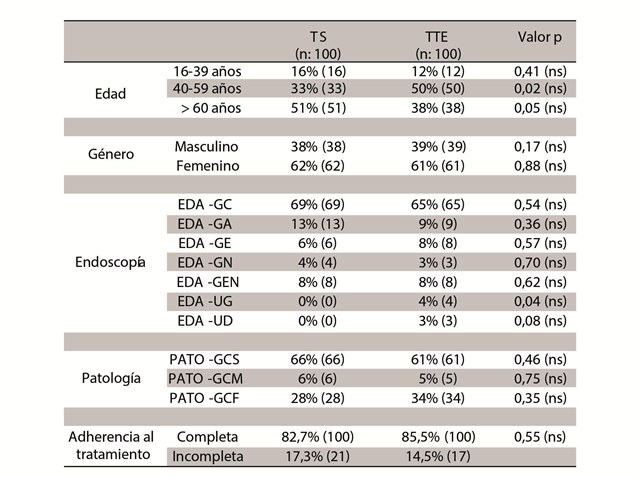
TTE: Triple Terapia Estándar, TS: Terapia Secuencial, EDA-GC: gastritis crónica, EDA-GA: gastritis aguda, EDA-GE: gastritis erosiva, EDA-GN: gastritis nodular, EDA-GEN gastritis enantematosa, EDA-UG: úlcera gástrica, EDA-UD: úlcera duodenal, PATO-GCS: gastritis crónica superficial, PATO-GCM: gastritis crónica moderada PATO-GCF: gastritis crónica folicular.(ns): no significativo, valor de p mayor a 0,01.
tribución en ambas terapias. Siendo el hallazgo endoscópico más frecuente la gastritis crónica en ambas terapias y el hallazgo patológico más frecuente en ambos grupos fue la gastritis crónica superficial.
En el análisis por protocolo, el porcentaje de erradicación en el grupo TTE fue de 36% (IC 95%: 26,5%-45,4%), siendo superada ampliamente por la TS con el 80% (IC 95%: 72,187,8). Esta diferencia fue estadísticamente significativa (valor p <0,01).(Fig.2)

Figura 2. Erradicación de H. pylori por terapia secuencial y triple terapia (expresado en porcentajes)
Evidenciándose un aumento absoluto de la tasa de erradicación del 44% (IC95%: 34,2%-53,7%) en el grupo de TS (Tabla 2). En el análisis secundario, la superioridad de la TS se mantuvo presente en todos los grupos, distribuidos por edad y sexo (Tabla 3).
Tabla 2. Comparación en la tasa de erradicación de H. Pylori con los esquemas
TTE y TS.
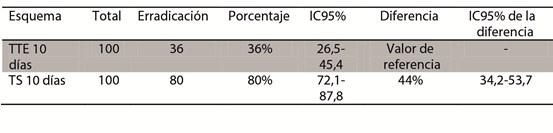
TTE: Triple Terapia Estándar. TS: terapia secuencial.
Tabla 3. Comparación en la tasa de erradicación de H. pylori con los esquemas TTE y TS

Discusión
Diversos estudios se han realizado en torno a la superioridad de la terapia cuádruple, administrada, tanto de forma secuencial como concomitante en comparación con la triple terapia estándar, encontrándose la superioridad de la primera en la mayoría10-12 o al menos equivalencia en la tasa de erra-dicación13. En el presente estudio, se evidenció por una parte la baja efectividad de TTE (36%) en la población estudiada, mucho menor a la reportada en otros estudios10,11,17. Por otra parte la efectividad alcanzada por la TS (80%) no supera el 90% encontrado en otros estudios que utilizaron un esquema similar al nuestro (cuádruple terapia secuencial sin bismu-to)13, 14, estando más cercana a lo deseable.
Cada vez son más las poblaciones que requieren una intervención más agresiva en cuanto al esquema antibiótico para afrontar el manejo del paciente con HP sin tratamiento previo, según indican las revisiones y guías actuales15,17-20, principio apoyado por los hallazgos de nuestro estudio, aunque en algunas poblaciones persiste una baja resistencia a los esquemas actuales16.
A pesar de no existir datos publicados sobre la resistencia antimicrobiana de H. pylori en Bolivia, nuestros resultados permiten sospechar una tasa de resistencia a claritromicina superior al 20%, además de la posible asociación con resistencia a metronidazol, lo que debe ser constatado por medio de estudios epidemiológicos y microbiológicos adecuados.
Conflictos de interés: los autores declaramos que no existe conflicto de intereses.
Referencias
1. Sáenz R. Organizaciones Mundiales de Gas-troenterología (WGO) y Endoscopia Digestiva (OMED) renuevan autoridades en Londres 2009. Una revisión somera de la participación de Chile en esta historia. Publicación Oficial de la Sociedad Chilena de Gastroenterología. 2010; 21(1): 47-56.
2. Uemura N, Okamoto S, Oichiro S, Matsumura N, Yamaguchi S, Yamakido M, et al. Helicobacter pylori infection and the development of gastric cancer. N England J Med 2001; 345(11): 784-789.
3. Seoane A, Bessa X, Alameda1 F., Munné A., Gallen M., Navarro S., et al. Role of Helicobacter pylori in stomach cancer after partial gastrectomy for benign ulcer disease. Rev EspEnferm Dig 2005; 97(11): 778-785.
4. Nomura A, Stemmermann G. N, Chyou P, Kato I, Pérez G. I, Blaser M J. Helicobacter pylori infection and gastric carcinoma among Japanese Americans in Hawaii. N England J Med 1991; 235(16): 1132-36.
5. Megraud F, Antibiotic resistance in Helicobacter pylori infection. Br Med Bull 1998; 54(1): 207216.
6. Malfertheiner P, Megraud F., O’Morain C., Atherton J., Axon A. T. R., Bazzoli F, et al. Management of Helicobacter pylori infection: theMaastricht IV/ Florence Consensus Report. Gut 2012;61:646-664.
7. Fallore C. Review: Epidemilogy of the antibiotic resistance of helicobacter pylori in Canada. Can J Gastroenterol 2000; 14(10): 879-882.
8. Oleastro M, Cabral J, Magalhaes-Ramalho P, Sande-Lemos P, Paixao E, Benoliel J, et al. Primary antibiotic resistance of Helicobacter pylori strains isolated from Portuguese children: a prospective multicentre studyover a 10 year period. J Antimi-crob Chemother. 2011 0ct;66(10):2308-11.
9. Megraud F, Coenen S, Versporten A, Kist M, Lopez-Brea M, Hirschl AM, et al. Helicobacter pylori resistance to antibiotics in Europe and its relationship to antibiotic consumption. Gut 2013;62:34-42.
10. Basu P, Rayapudi K, Pacana T, Shah NJ, Krish-naswamy N, Flynn M. A Randomized Study Comparing Levofloxacin, Omeprazole, Nitazoxanide, and Doxycycline versus Triple Therapy for the Eradication of Helicobacter pylori. Am J Gastroenterol 2011; 106:1970-1975.
11. Lahbabi M, Alaoui S, El Rhazi K, et al. Sequential therapy versus standard triple-drug therapy for Helicobacter pylori eradication: result of the HPFEZ randomised study.Clin Res Hepatol Gastroenterol. 2013 Sep;37(4):416-21. Abstract disponible en:
http://www.ncbi.nlm.nih.gov/pub-med/23168228.
12. De Francesco V, Zullo A, Hassan C, Della Valle N, et al. The prolongation of triple therapy for Helicobacter pylori does not allow reaching therapeutic outcome of sequential scheme: a prospective, randomised study. Dig Liver Dis. 2004 May;36(5):322-6.Abstract disponible en: http://www.ncbi.nlm.nih.gov/pubmed/15191200
13. Greenberg E, Anderson G, Morgan D, Torrez J, Chey W, Bravo LD, et al. A Randomised Trial of empiric 14-day Triple, five-day Concomitant, and ten-day Sequential Therapies for Helicobacter pylori in Seven Latin American Sites. Lancet. 2011 August 6; 378(9790): 507-514.
14. De Francesco V, Zullo A, Margiotta M, Ma-rangi S, Burattini O, Berlocos P, et al. Sequential treatment for Helicobacter pylori does not share the risk factors of triple therapy failure. Aliment PharmacolTher 2004; 19: 407-414.
15. Gong EJ, Yun SC, Jung HY, Lim H, Choi KS, Ahn JY, et al. Meta-Analysis of First-Line Triple Therapy for Helicobacter pylori Eradication in Korea: Is It Time to Change?.J Korean Med Sci 2014; 29: 704-713.
16. Fock K M, Katelaris P, Sugano K, et al. Second Asia-Pacific Consensus Guidelines for Helicobacter pylori infection. J GastroenterolHepatol 2009;24: 1587-1600.
17. Gisbert JP, Calvet X. The Effectiveness of Standard Triple Therapy for Helicobacter pylori Has Not Changed Over the Last Decade, But it is Not Good Enough.Aliment PharmacolTher 2011; 34:1255-1268.
18. O’Connor A, Gisbert JP, McNamara D, O’Moraim C. Treatment of Helicobacter pylori Infection 2011. , Helicobacter 2011; 16 (Suppl. 1): 53-58.
19. Tepes B, O’Connor A, Gisbert JP, et al. Treatment of Helicobacter pylori infection 2012. Helicobacter 2012; 17 (Suppl. 1): 36-42.
20. Gatta L, Vakil N, Vaira D, Scarpignato C. Global eradication rates for Helicobacter pylori infection: systematic review and meta-analysis of sequential therapy. BMJ 2013;347:f4587.














