Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta Médica Boliviana
versión impresa ISSN 1012-2966versión On-line ISSN 2227-3662
Gac Med Bol v.28 n.2 Cochabamba 2005
TRABAJO ORIGINAL
DIAGNÓSTICO DE LEISHMANIASIS UTILIZANDO MEDIO DE CULTIVO TSTB EN PACIENTES DE TROPICO DE COCHABAMBA
* Hernán Bermúdez, ** Marco Solano, ** Mary Cruz Torrico Rojas, *** Mauricio Carballo Montero, *** Omar Lafuente Covarrubias, *** María del Pilar Lara Arias, *** Paola Paredes Torrico
* Médico Lab. Parasitología LABIMED CUMETROP, IIBISMED
** Bioquímico, IIBISMED
*** Estudiantes de la Facultad de Medicina UMSS.
RESUMEN
Se realizó un estudio prospectivo, analítico y experimental para determinar el porcentaje de sensibilidad de un nuevo medio de cultivo para el diagnóstico de Leishmania, denominado TSTB (Torrico-Solano-Torrico-Bermúdez). Se obtuvieron las muestras por aspirado de úlceras con sospecha clínica de Leishmaniasis de pacientes provenientes del trópico de Cochabamba.
Los objetivos planteados fueron determinar el porcentaje de sensibilidad del cultivo ya mencionado y analizar el crecimiento de parásitos de Leishmania.
Como resultados se obtuvo un 90% de sensibilidad mediante este método diagnóstico y una mínima contaminación por hongos (mohos y levaduras); además, un cambio de coloración en el medio de cultivo debido al crecimiento y multiplicación de los parásitos por consumo de los nutrientes.
Palabras claves: Leishmania, Diagnóstico, Cultivo, Aspirado.
ABSTRACT
A prospective, analytic and experimental study was realized, in which we tried to determine the percentage of sensitive of a new culture medium for the diagnosis of Leishmania, denominated Torrico-Solano-Torrico-Bermudez (TSTB). Samples were obtained by a piration of ulcers with clinical suspicion of Leishmaniasis from patients proceeding from the tropical area of Cochabamba.
The objectives planted were to determine the percentage of sensitive of the mentioned culture and to analyze the growth of the parasites of Leishmania.
As a result, a 90 % of positivity was obtained with this diagnostic method, with a minimum contamination by fungus (moss and yeast); further more, a change in the colour of culture medium was observed, because of the growth and multiplication of the parasites by consumption of the nutrients.
Key words: Leishmania, Diagnosis, Culture, Aspiration.
INTRODUCCION
Los parásitos del género Leishmania son organismos unicelulares pertenecientes al reino Protozoa, orden Kinetoplastida, familia Trypanosomatidae, se divide en dos subgéneros: (Leishmania y Viannia), el subgénero Leishmania se divide a su vez en cinco complejos; donovani, trópica, major, aethiopica y mexicana; el complejo Viannia en braziliensis y guyanenss.
Los complejos braziliensis, mexicana y donovani son los principales agentes de la leishmaniasis en muchas áreas tropicales y subtropicales de América, donde los humanos son solo huéspedes accidentales en el ciclo de vida del parásito. Los protozoarios flagelados de este género son capaces de producir un amplio espectro de enfermedades en los humanos que van desde algunas infecciones asintomáticas a horribles lesiones desfigurantes del rostro como el caso de la leishmaniasis mucosa (espundia), o a la fatal forma visceral de la enfermedad.
En 1989 la Organización Mundial de la Salud (OMS) ha estimado que existen aproximadamente 12 millones de personas infectadas en todo el mundo y 350 millones con riesgo de contraer la enfermedad: constituyéndose en un importante problema de salud pública.1
En la naturaleza todas las especies de Leishmania son transmitidas por la picadura de un insecto flebotomino hembra infectada. Estos parásitos tienen dos distintos estadios en su ciclo de vida; una forma móvil flagelada que vive extracelularmente en el tracto digestivo del insecto vector llamado promastigote y una forma no flagelada que se encuentra intracelularmente en el sistema fagocítico mononuclear del huésped vertebrado, el amastigote.2
Existen medios de cultivo monofásicos (líquidos) que son de difícil aplicación y uso en las áreas endémicas de los países pobres, debido a su costo y a la necesidad de importación lo que dificulta su aprovechamiento. Los medios de cultivo bifásicos entre ellos el más conocido es el NNN constituyen los medios más empleados para el cultivo de parásitos. Con este medio se consiguió una positividad del 23 % en pacientes del área endémica boliviana.
El uso de la inoculación en hámsters para el diagnóstico de Leishmania solo presenta un 60 % de éxito en la positividad y no basta con hacer un simple frotis del lugar clínicamente positivo, es necesario cultivar.
Las especies de Leishmania obtenidas como amastigotes de los huéspedes vertebrados mamíferos, crecen y se multiplican en cultivos axénicos a temperatura ambiente (22° a 26° C) como promastigotes3, forma similar a aquella encontrada en el insecto vector 4-5, permaneciendo invariable su capacidad de infección cuando es inoculado en huéspedes susceptibles6 aunque dicha capacidad va disminuyendo a medida que el número de subcultivos va en aumento7.
En América especies de Leishmanias pueden ser cultivados en medios de cultivo definidos tales como Schneider Drosophyla Médium; Glucosa, Suero bovino fetal, Lactosa y Hemoglobina (GLSH10%); y medios adaptados de formulaciones utilizadas en el cultivo in vitro de células mamíferas8-9-10 o en medios de cultivo semi-definidos bifásicos como Tobie sangre de conejo al 15% (TSL 15%); medio NNN (Novy, Mac Neal y Nicolle), USMARU y Evans modified Tobie's médium1-2.
Los objetivos planteados fueron determinar el porcentaje de sensibilidad del cultivo ya mencionado y analizar el crecimiento de parásitos de Leishmania.
MATERIALES Y METODOS
Diseño Metodológico:
Tipo de estudio: Estudio prospectivo, analítico y experimental
Población y Muestra:
Población: Personas que viven o vivieron en el trópico de Cochabamba donde se han reportado casos de leishmaniasis, quienes tienen úlceras cutáneas con sospecha clínica de esta patología, que representan un número total de 84 pacientes de los cuales se obtuvieron 108 muestras.
Muestra: 29 pacientes, de quienes se obtuvieron 36 muestras, que presentan úlceras cutáneas con sospecha clínica de leishmaniasis que provienen del trópico cochabambino y con prueba de Intradermo Reacción de Montenegro (IDRM) positiva.
Método e instrumentos de recolección de datos
Preparación del medio de cultivo TSTB
Cuatro gramos de agar base sangre N° 2 (DIFCO cod. 0696-17) fueron disueltos en 100 ml de agua destilada y esterilizada en autoclave (Webeco GMBH) a 121 °C de temperatura y 1 atmósfera de presión durante 15 minutos, posteriormente el medio estéril fue enfriado en baño maría a 50 °C. En el interior de una campana de flujo laminar vertical de bioseguridad clase II. (LABCONCO Cat. N° ) se añadió 15 ml de sangre de conejo desfibrinada al medio de cultivo y 1 ml de una mezcla de antibióticos (penicilina G sódica 3.000 UI y Sulfato de estreptomicina 3.000 ug).
Dos a 2,5 ml de la mezcla así preparada fue distribuida en tubos de 10 ml con tapa rosca y se dejó enfriar en soportes con un ángulo de 25°. El medio así preparado se conservó hasta el momento de utilizar en un refrigerador a 4 °C, por no más de 15 días.
Dos tubos fueron colocados en una incubadora a 37° C para control de esterilidad. 3 tubos fueron inoculados con promastigotes de leishmania como control de calidad de los medios de cultivo.
Aislamiento del parásito
Previo lavado de las úlceras se realizó una limpieza de la zona elegida con solución salina (ClNa al 0,85 %) a la cual se agregó 3.000 UI de penicilina G sódica y 3.000 ug de sulfato de estreptomicina (ATBPS).
Se cargó una jeringa de 3 ml (NIPRO o TERUMO) con 1,5 ml de ATBPS, y se cambió la aguja por una de 23 G X 1". Introduciendo la aguja en el sitio elegido comenzando de la parte sana de la piel y llegando hasta la proximidad del borde de la lesión haciendo rotar la jeringa tres veces mientras se está dentro de la piel, esto cortará pequeñas piezas de tejido con los bordes de la aguja. Se aspiró tanto fluido tisular y piezas de tejido cómo fue posible, jalando y soltando el émbolo con suavidad. Posteriormente se saco la jeringa y se inoculó 0,5 ml en un tubo con medio de cultivo.
Se repitió este procedimiento con los otros dos tubos y se rotularon para incubarlos entre 22 y 25°C en una incubadora refrigerada (FISHER SCIENTIFIC. Cat. N° 11-679-304R). La lectura de los tubos se realizó cada 7 días durante 21 días. Para la lectura de los tubos y los subcultivos se utilizó una campana de flujo laminar vertical (LABCONCO) de bioseguridad clase II.
Con una pipeta Pasteur estéril se mezcló el sobrenadante del tubo y se realizó un subcultivo en un medio de cultivo fresco, colocando una gota en un portaobjetos y cubriendo con un cubreobjetos de 20 x 20 mm y se observó en un microscopio (OLYMPUS CH-30).
RESULTADOS
De los 29 pacientes (36 muestras) que fueron seleccionados de acuerdo a los criterios de inclusión, 26 (90%) fueron positivos por cultivo en agar TSTB y 3 (10%) fueron negativos, obteniendo un alto porcentaje de positividad (Cuadro y Gráfica N° 1).
CUADRO 1
| SENSIBILIDAD EN EL DIAGNOSTICO DE Leishmania sp. POR CULTIVO EN AGAR TSTB DE ASPIRADO DE MUESTRA CON JERINGA EN PACIENTES DEL TROPICO DE COCHABAMBA ENERO-JULIO DE 2003 COCHABAMBA - BOLIVIA |

| Fuente: IIBISMED - CUMETROP - LABIMED |
GRAFICO 1
| SENSIBILIDAD EN EL DIAGNOSTICO DE Leishmania sp POR CULTIVO EN AGAR TSTB DE ASPIRADO DE MUESTRA CON JERINGA EN PACIENTES DEL TROPICO DE COCHABAMBA ENERO-JULIO DE 2003 COCHABAMBA-BOLI VIA |
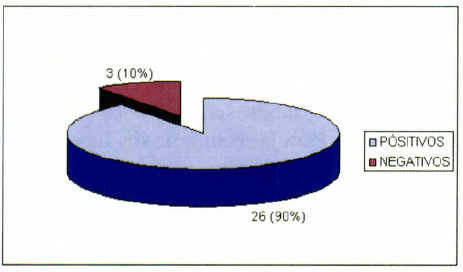
| Fuente: IIBISMED-CUMETROP- LABIMED. |
De las 36 muestras obtenidas de los 29 pacientes, 33 fueron positivas y 3 fueron negativas. En la primera lectura, de las 33 muestras positivas: 18 (54.5 %) tuvieron crecimiento de parásitos en los 3 tubos de cultivo 7 (21%) solo en 2 tubos de cultivo. 4 (12%) en un solo tubo de cultivo. 4(12 %) no presentaron crecimiento de parásitos, los cuales dieron resultados positivos en la segunda lectura (Cuadro y Grafica N° 2).
CUADRO 2
| NUMERO DE MUESTRAS CON CRECIMIENTO DE Leishmania EN AGAR TSTB DE ACUERDO AL NUMERO DE TUBOS DE CULTIVO EN LOS QUE SE OBSERVARON LOS PARASITOS ENERO-JULIO DE 2003 COCHABAMBA-BOLJVIA |
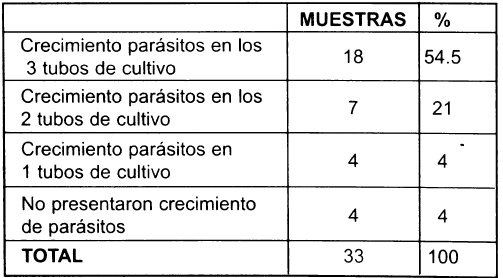
| Fuente: IIBISMED-CUMETROP- LABIMED. |
GRAFICA 2
| NUMERO DE MUESTRAS CON CRECIMIENTO DE Leishmania EN AGAR TSTB DE ACUERDO AL NUMERO DE TUBOS DE CULTIVO EN LOS QUE SE OBSERVARON LOS PARASI TOS ENERO-JULIO DE 2003 COCHABAMBA - BOLIVIA |
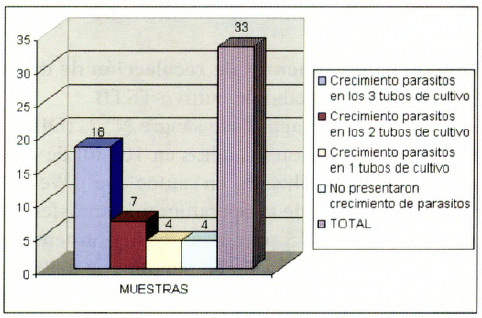
Del total de muestras analizadas solo 3 (7 %) presentaron contaminación con hongos (mohos y levaduras) en uno o dos de la serie de tres tubos utilizados para el cultivo.
En cuanto al análisis del crecimiento de los parásitos en el medio de cultivo se observó a los 7 a 10 días, un cambio de coloración en la fase sólida del cultivo, previamente rojo, que adoptó una coloración pardo rojizo o pardo oscuro comenzando desde la base del tubo hasta alcanzar el nivel de la fase líquida, debido al consumo de los nutrientes del medio TSTB por los parásitos en multiplicación. La solución salina (Fase Líquida) cuya coloración era cristalina adquirió un aspecto ligeramente opalescente o turbio como consecuencia de la multiplicación de los parásitos. Estos cambios se observaron en la clasificación "c" y "d" de la siguiente escala basada en el siguiente criterio: Negativo (-), si no se observan parásitos en 1000 campos microscópicos examinados; a, menos de 1 parásito por campo en 100 campos microscópicos examinados; b, 1 parásito por campo en 50 campos microscópicos examinados; c, de 1 a 10 parásitos por campo en 20 campos microscópicos examinados; y de más de 10 parásitos por campo en 10 campos microscópicos examinados.
DISCUSION Y CONCLUSIONES
Las lesiones cutáneas producidas por especies de Leishmania en el trópico de Cochabamba presentan una amplia variedad de formas clínicas, de las cuales solo el 64 % de las lesiones cutáneas son leishmaniásicas y el restante son debidas a etiologías diferentes20, por esta razón el diagnóstico clínico de leishmaniasis es complicado porque la existencia de algunas lesiones cutáneas producidas por otros microorganismos pueden mimetizar esta patología, por tanto, debe realizarse la confirmación parasitológica de la infección. Entre los métodos de diagnóstico parasitológico por cultivo la técnica de aspirado presenta mejores ventajas que la técnica de biopsia debido a que existe menor probabilidad de contaminación, es un procedimiento menos traumático y se puede obtener muestras de distintos lugares alrededor de la lesión, mejorando así la sensibilidad del aislamiento. En nuestro estudio la sensibilidad fue de 90 % similar a la obtenida en los estudios de Ramírez et. al. (90.4%)21 y mayor que la descrita por Romero et. al. (41,7%)22 Estos resultados se deben a la técnica de toma de muestra por aspirado en tres sitios diferentes de las lesiones cutáneas y cultivo en tres tubos, utilizando un medio semidefinido (TSTB) para el desarrollo de Leishmania.
El rango de contaminación por hongos (mohos y levaduras) de nuestro estudio fue bajo (7%) en comparación a la proposición original de 28,6% (Marzochi et al. 1993)23 y comparable al resultado de 2,9% obtenido por Romero et. al22., debido a la técnica aspiratoria empleada y la reducción de la exposición del medio de cultivo durante la inoculación. Es digno de expresar que no hubo contaminación con bacterias gracias a la elevada concentración de antibióticos en el medio de cultivo, propuesta por el grupo de trabajo de LABIMED (IBISMED, Facultad de Medicina UMSS - Cochabamba, Bolivia) debido a la resistencia de las bacterias de la zona. Cabe recalcar que no se contaminaron ninguno de los tres tubos de cada paciente y se logró un diagnóstico certero con los tubos no contaminados.
En relación a la sensibilidad del cultivo utilizado en esta investigación constatamos que se muestra superior al de otros medios como el NNN. En cuanto a la especificidad, esta es del 100% puesto que es imposible obtener promastigotes (falsos positivos) en pacientes no leishmaniásicos.
Por los motivos anteriormente indicados recomendamos la utilización del medio TSTB en los laboratorios de investigación con infraestructura para cultivos axénicos de Leishmania spp. no solo en nuestro país sino también a nivel internacional.
BIBLIOGRAFIA
1. Organización Mundial de la Salud (OMS) 1990. Lucha contra las Leishmaniasis: serie de informes técnicos 793. Ginebra. [ Links ]
2. Evans,D.A., 1993. In Vitro Cultivation and Biological Cloning of Leishmania, p.29-41. In John E. Hyde (ed.), Protocols in Molecular Parasitology. Humana Press. Totowa, New Jersey. U.S.A. [ Links ]
3. Torrico MC, De Doncker S, Arevalo J, Le Ray D, Dujardin JC. In vitro promastigote fitness of putative Leishmania (Viannia) braziliensis/Leishmania (Viannia) peruviana hybrids. Acta Trop. 1999 Jan 15;72( 1 ):99-110. [ Links ]
4. Bates, P.A., 1993. Axenic culture of leishmania amastigotes. Parasitol. Today 9: 143-146.
5. Pan, A. A., 1984. Leishmania mexicana: Serial Cultivation of intracellular stage in a cell - free medium. Exp. Parasitol. 58: 72-80.
6. Keithly, J. S., 1976. Infectivity of Leishmania donovani amastigote and promastigote for golden hamsters. J. Protozool. 23: 244-245.
7. Da Silva, R. P. and Sacks, D. L., 1987. Infect. Immunol. 55: 2802-2806.
8. Koech, D. K., íha, D.W., Ho, M., and Wuamachi, A.N., 1987. Contnbution of adherent cells and serum components to immune supression in Kenyan visceral leishmaniasis. Am. J. Trop. Med. Hyg. 36 : 501-504.
9. Gastes, M., Cabrera, M., Trujillo, D. and Convit, J. 1988. T-cell subpopulation, expression of Interleukin-2 and gamma interferon in human ameriean eutaneous leishmaniasis. J. Clin.Microb. 26: 1207-1213.
10. Rey, J. A., Travi, B.L. Valencia, A. Z., and Saravia, N.G., 1990. Infectivity of the subespecies of Leishmania braziliensis complex in vivo and in vitro. Am J. Trop. Med. Hyg. 43: 623-631.
11. Dimier-David L, David C, Ravisse P, Bustillos R, Revollo S, Lyevre P, Muñoz M, Vargas F, Dedet JP. Parasitological diagnosis of mucocutaneous leishmaniasis due to Leishmania b. braziliensis in Bolivia. Rev Soc Bras Med Trop. 1991 Oct-Dec;24(4):231-4. [ Links ]
12. Aviles H, Belli A, Armijos R, Monroy FP, Harris E. PCR detection and identification of Leishmania parasites in clinical specimens in Ecuador: a comparison with classical diagnostic methods. J Parasitol. 1999 Apr;85(2): 181-7 [ Links ]
13. Weigle KA, Labrada LA, Lozano C, Santrich C, Barker DC. PCR-based diagnosis of acute and chronic eutaneous leishmaniasis caused by Leishmania (Viannia). J Clin Microbiol. 2002 Feb;40(2):601-6. [ Links ]
14. Weigle KA, de Davalos M, Heredia P, Molineros R, Saravia NG, D'Alessandro A. Diagnosis of eutaneous and mucocutaneous leishmaniasis in Colombia: a comparison of se ven methods. Am J Trop Med Hyg. 1987 May:36(3):489-96. [ Links ]
15. Silveira TG, Teodoro U, Lonardoni MV, Guilherme AL, Toledo MJ, Ramos M, Arraes SM, Bertolini DA, Spinoza RP, Barbosa OC. Epidemiologic aspeets of Cutaneous Leishmaniasis in an endemic area of the state of Parana, Brazil. Cad Saude Publica. 1996 Apr; 12(2): 141-147. [ Links ]
16. Medeiros AC, Rodrigues SS, Roselino AM., Comparison ofthe specifícity of PCR and the histopathological detection of leishmania for the diagnosis of American cutaneous leishmaniasis. Braz J Med Biol Res. 2002 Apr;35(4):421-4. [ Links ]
17. Gontijo B, de Carvalho M de L. American cutaneous leishmaniasis Rev Soc Bras Med Trop. 2003 Jan- Feb;36( 1 ):71 -80. Epub 2003 Apr 22. [ Links ]
18. de Brujin MH, Labrada LA, Smyth AJ, Santrich ( Barker DC. A comparative study of diagnosis by the polymerase chain reaction and by current clinical methods using biopsies from Colombian patients with suspected leishmaniasis. Trop Med Parasitol. 1993 Sep;44(3):201-7.
19. Desjeux P, Mollinedo S, Le Pont F, Paredes A, Ugarte G. Cutaneous leishmaniasis in Bolivia. A study of 185 human cases from Alto Beni (La Paz Department). Isolation and isoenzyme characterization of 26 strains of Leishmania braziliensis braziliensis [corrected], Trans R Soc Trop Med Hyg. 1987;81(5):742-6. [ Links ]
20. Bermudez, H. y Zapata, M. E. - 1997. Etiología y características epidemiológicas y clínicas de las úlceras cutáneas del trópico de Cochabamba. UMSS, DUI, OMS. Informe final, Curso de Diplomado en Investigación en Salud. 49 pp.
21. J Clin Microbiol. 2000 Oct;38( 10):3768-73. Diagnosis of cutaneous leishmaniasis in Colombia: the sampling site within lesions influences the sensitivity of parasitologic diagnosis. Ramirez JR, Agudelo S, Muskus C, Alzate JF, Berberich C, Barker D, Velez ID.
22. Mem Inst Oswaldo Cruz. 1999 Jul-Aug;94(4):505-8. Sensitivity of a vacuum aspiratory culture technique for diagnosis of localized cutaneous leishmaniasis in an endemic area of Leishmania (Viannia) braziliensis transmission. Romera GA, Sampaio RN, Macedo V, Marsden PD. Núcleo de Medicina Tropical, Universidades de Brasilia, Brasilia, DF, 70919-970, Brasil, gromero@unb.br
23. Marzochi MCA, Teixeira PC, Marzochi KBF, Conceicao NF, Coutinho W, Brito DB 1993. Vacuum aspiratory puneture system for Leishmania culturing, isolation and transport, preliminary report. Rev Inst Med Trop Sao Paulo 35: 301-303.














