Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta Médica Boliviana
versión impresa ISSN 1012-2966versión On-line ISSN 2227-3662
Gac Med Bol v.28 n.1 Cochabamba 2005
CASO CLÍNICO
SARCOMA DE ESTROMA EXTRAGASTROINTESTINAL RETROPERITONEAL
*Tito Grágeda Soto,*Jorge Sandoval C.,*Víctor Hugo Gonzáles M.,**lvonne Salcedo S.
* Médico Servicio de Cirugía, Patología y Oncología del Hospital Elizabeth Seton Caja Petrolera de Salud Cochabamba.
** Médico Interno Hospital Elizabeth Seton Caja Petrolera de Salud Cochabamba.
INTRODUCCION
Los tumores del estroma gastrointestinal (GIST) son neoplasias mesenquimatosas comunes del estómago e intestino delgado, siendo menos frecuentes en otras partes del tracto digestivo.
El poder diferenciarlos del leiomioma, leiomiosarcoma, schwannoma, liposarcoma retroperitoneal, tumor desmóide, carcinoide con morfología fusocelular y metástasis de melanoma o carcinoma fusocelular es sumamente necesario, dado que estas son patologías más frecuentes y la mayoría de estos tumores puede ser caracterizada a través de la información clínica y de la microscopía de rutina.
La ubicación de los GIST tiene lugar en cualquier localización del tracto gastrointestinal tubular y en algunas localizaciones extragastrointestinales, aunque es mayoritariamente gástrica (50-60%), intestino delgado (20-30%), intestino grueso (10%), esófago (5%), y (5%) en otras ubicaciones; este antecedente es un importante factor pronóstico independiente del tamaño tumoral, la tasa mitótica y la edad del paciente. Aunque no se ha comprobado fehacientemente, los localizados en el intestino delgado parecen ser los que tienen peor pronóstico.
Generalmente son lesiones protruidas, con frecuente ulceración central y tienen el antecedente clínico de haber debutado con episodios de hemorragia digestiva. El tamaño es notable dado que no pocos de ellos son de más de 4 cm y algunos se extienden como reloj de arena alcanzando la subserosa exhibiendo franca invasión del resto de los tejidos.
En la histopatología convencional se describen 2 patrones morfológicos, uno fusocelular y otro epitelioideo. Las determinaciones Inmunohistoquímicas con c-Kit (CD117) positivas, pueden facilitar la distinción dado que es muy raro que los GIST sean CD117(-). El 2530% de los GIST son malignos y se acompañan de metástasis y/o la invasión de órganos o estructuras adyacentes al momento del diagnóstico. El comportamiento del resto de estos tumores es bastante errático e impredecible.
El pleomorfismo se aprecia en las variantes epitelioides y le confiere un mal pronóstico, de la misma forma que la aneuploidía, en consecuencia ante la presencia de pacientes portadores de un GIST se enfatiza la cautela diagnóstica del patólogo y el seguimiento a largo plazo de éstos, dado que necesitan ser evaluados constantemente y por tiempo indefinido, existiendo la confianza que con los avances de la biología molecular se obtenga una mejor apreciación pronostica.
CASO CLINICO
Paciente de sexo femenino de 69 años consulta por presentar cuadro clínico caracterizado por sensación de plenitud y cambio en su hábito intestinal de aproximadamente un mes de evolución, alternando estreñimiento con periodos de evacuaciones laxas. Además acusa dolor abdominal en flanco izquierdo, irradiado al dorso, no refiere pérdida de peso, el apetito conservado y tiene un IK del 100%. Al examen físico en abdomen se palpa una masa ovoide que ocupa el hipocondrio y flanco izquierdos de aproximadamente 15x18 cm de longitud, poco móvil, de consistencia dura, con una prolongación hacia el epigastrio.
Los exámenes de laboratorio solicitados estaban dentro de rangos normales incluyendo el Antigeno Carcino Embrionario CEA de 2.3 ng/ml.
El ultrasonido muestra imagen tumoral de 12.0 x 8.5 cm, sugerente de estar localizado en las paredes del colon descendente, con disminución del diámetro e invasión extramural del lado medial, metástasis en el lóbulo hepático derecho y crecimiento ganglionar a nivel retroperitoneal. (imágenes 1-2).
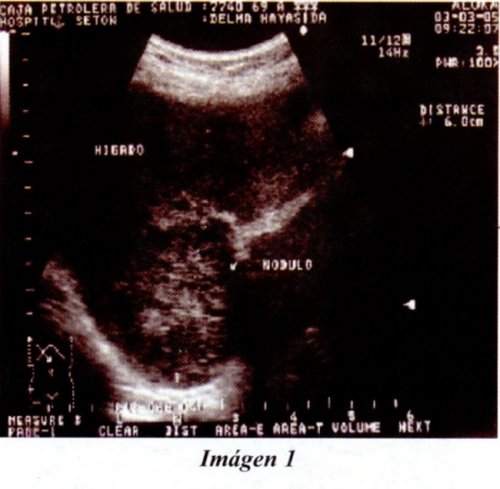
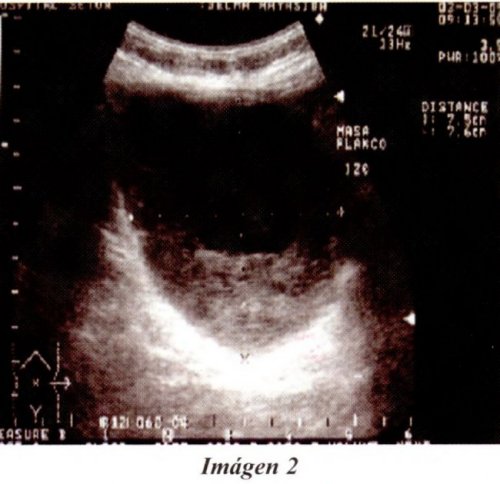
La Tomografía Computarizada Contrastada de abdomen muestra: Extensa lesión tumoral nodular heterogénea, en topografía del colon descendente, con múltiples focos mestastásicos en ambos lóbulos del hígado y múltiples ganglios paraaorticos. (Imágenes 3 y 4).
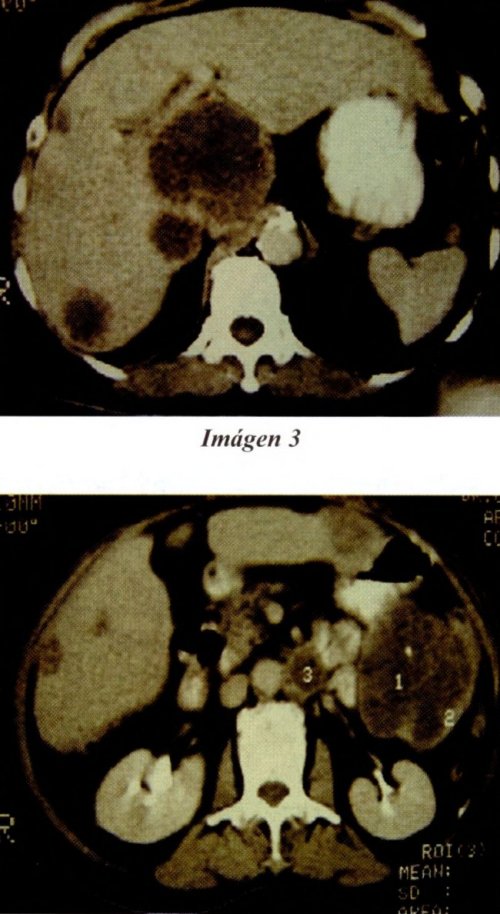
En el periodo preoperatorio la impresión diagnóstica considera tumor abdominal, posible neoplasia de colon. La paciente es sometida a cirugía con los siguientes hallazgos: líquido ascítico libre en escasa cantidad, hígado con múltiples metástasis pequeñas y grandes en ambos lóbulos y adenopatías mayores a 2 cm. en hilio hepático. Tumor primario retroperitoneal sólido quístico de 18 x 15 cm. que desplaza el estómago hacia anterior y está fijo a la pared posterior del colon transverso próximo al ángulo esplénico en una longitud de 7cm cubierto superficialmente por epiplón gastrocolico, se palpan adenopatías periaórticas menores a un centímetro. El procedimiento realizado fue una colectomía parcial (Segmento del transverso, ángulo esplénico y parte del colon descendente).
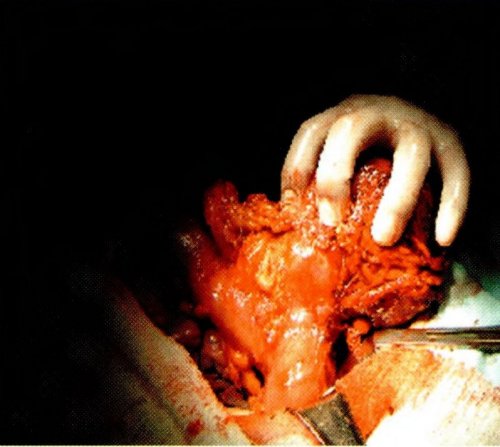
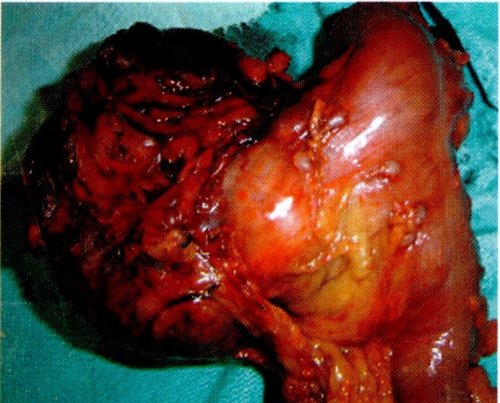
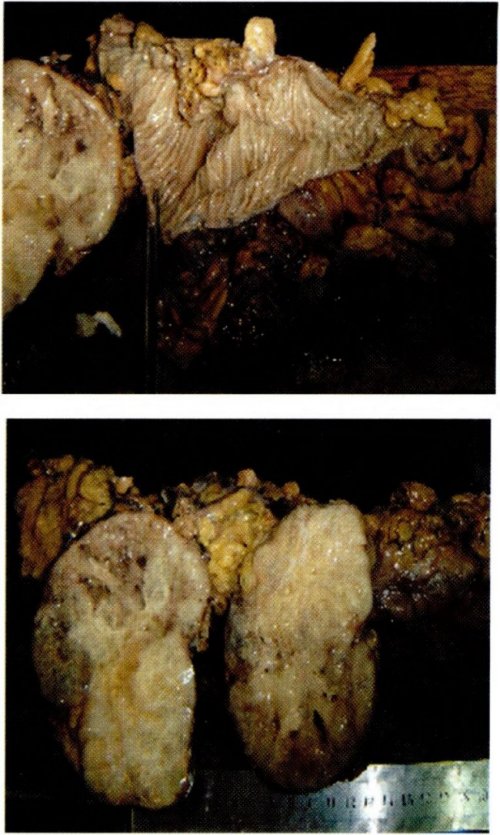
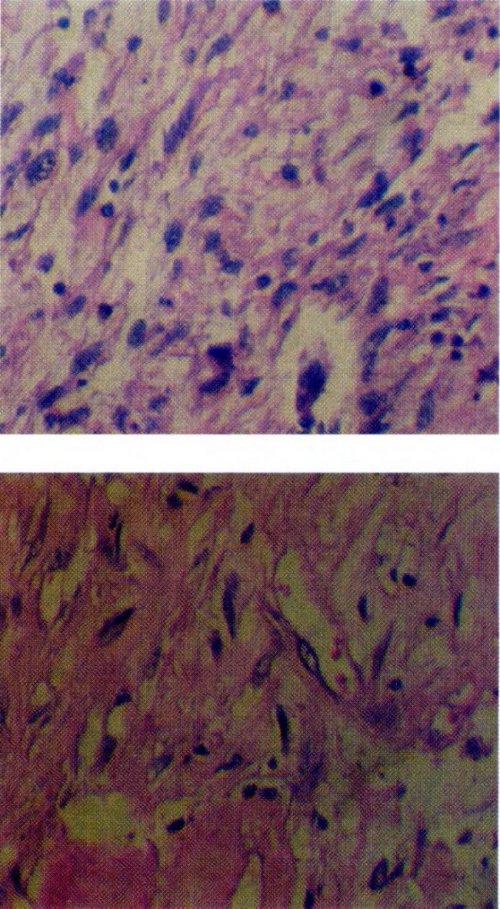
La evolución postoperatoria fue satisfactoria tolerando la vía oral adecuadamente y restableciéndose el tracto gastrointestinal en forma precoz, el alta fué al quinto día con seguimiento ambulatorio.
ANALISIS
Los GIST son tumores mesenquimatosos c-Kit (+) del tracto gastrointestinal existen evidencias de que la expresión de KIT y las mutaciones que resultan de su activación como mecanismo oncogénico cmcial en la mayor parte de los GIST se deben a que las células intersticiales de Cajal (CIC) requieren de esta proteína para su desarrollo y actividad funcional normal. Refuerza lo anterior el hecho de que en los síndromes de GIST, los familiares poseen mutaciones de ganancia de función de KIT en la línea germinal e hiperplasia de las células intersticiales de Cajal, lo cual sirve como un marcador fenotípico nuevo y confiable para los GIST.
Las mutaciones señaladas anteceden a las aberraciones citogenéticas y por lo tanto acontecen muy precozmente en el desarrollo del 90-95% de los GIST, determinando la proliferación de los tumores avanzados. Investigaciones recientes han determinado que el estado de la mutación de KIT es el factor predictivo más importante en la respuesta del paciente tratado con Imatinib (inhibidor específico de la tirosina kinasa), con un 80% de éxito en tumores con una mutación del exón 11 y sólo de 9% en tumores con mutación no identificable, con lo cual la terapia de los GIST presenta un nuevo enfoque de tratamiento, especialmente cuando los tumores estromales gastrointestinales son c-Kit (CD117)(+) de tipo maligno y/o inoperables.
En consecuencia, es altamente recomendable el uso de c-Kit (CD117) con el objetivo de confirmar el diagnóstico de GIST, como lo es el que cada nuevo lote de anticuerpos y sus diluciones, sea estandarizado usando controles positivos y negativos apropiados para lo cual es necesario que en el acto operatorio de resección del tumor se incluya también parte de la mucosa intestinal normal (epitelio) para poder utilizar a los mastocitos que son células positivas para c-Kit- como control positivo interno de la inmunorreacción.
BIBLIOGRAFIA
1) Strickland L, Letson GD, Muro-Cacho CA. Gastrointestinal stromal tumors. Cáncer Control. 8, 252-261, 2001.
2) Miettinen M, Sarlomo-Rikala M, Lasota J. Gastrointestinal stromal tumors: recent advances in understanding of their biology. Hum Pathol. 30, 1213-1220, 1999.
3) Chan JKC..Mesenchymal tumors of the gastrointestinal tract: a paradise for acronyms (STUMP, GIST, GANT, and now GIPACT). Implications of the c-kit in genesis, and yet another of many emerging roles of the intersticial cell of Cajal in the pathogenesis of gastrintestinal disease. Adv. Anat. Pathol. 6, 19-40, 1996.
4) Kindblom I-G., Remotti H., Aldenborg F., et al.. Gastrointestinal pacemaker cell tumor (GIPACT). Gastrointestinal stromal tumors show phenotypic characteristics of the intersticial cells of Cajal. Am.J.Clin.Pathol. 152, 1259-1269, 1998.
5) Sircar K., Hewlett BR., Huizinga JD., et al.. Intersticial cells of Cajal as precursors of gastrointestinal stromal tumors. Am.J. Surg.Pathol. 23, 377-389, 1999.
6) Wang L, Vargas H, French SW. Cellular origin of gastrointestinal stromal tumors: a study of 27 cases. Arch Pathol Lab Med. 124, 1471-1475, 2000.
7) Sakurai S., Fukasawa T., Chong JM., et al.. C-kit gene abnormalities in gastrointestinal stromal tumors (tumors of intersticial cell of Cajal). Jpn. J. Cancer Res. 90, 1321-1328, 1999.
8) Hagger R., Finlayson C., Jeffrey I., et al.. Role of the intersticial cells of Cajal in the control of gut motility. Br. J. Surg. 84, 445-450, 1997.
9) Miettinen M., Sarlomo-Rikala M., Lasota J.. Gastrointestinal stromal tumours. Ann. Chir. Gyn. 87, 278-281, 1998.
10) Miettinen M, Lasota J. Gastrointestinal stromal tumors-definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnosis. Virchows Arch. 438,1-12, 2001.
11) Robbins S.. Patología estructural y funcional. 6a ed., Interamericana, México, 1980. Cp. 21. pp: 871-950. [ Links ]














