INTRODUCCIÓN
Los metales pesados descargados en ambientes fluviales como contaminantes no tratados, provocan un grave problema ambiental al entrar en la cadena de consumo acuoso por organismos, animales y humanos quienes resienten diversas enfermedades y trastornos. Las altas concentraciones de metales pesados en la cuenca del río Tambo se deben a las afloraciones geotermales volcánicas y vertimientos de aguas contaminadas de las mineras de la Compañía de Minas Buenaventura S.A.A. y Minera Aruntani S.A.C 1.
En la cuenca del río Tambo que tiene sus orígenes desde las quebradas Margaritani y Apostoloni, así como en los ríos que afluyen, Queullijahuire, Aruntaya, Titire y la quebrada de Acosiri, se han cuantificado las concentraciones de cadmio que varían en un intervalo de 0,015 a 0,21 mg/L. Estos valores sobrepasan los Estándares de Calidad Ambiental para Agua 9), (10. Cabe mencionar que estas aguas se utilizan para consumo humano, bebida de animales, el riego de cultivos y acuicultura.
La concentración máxima permitida de Cadmio (II) en agua potable es de 0,003 mg/L. Esto fue establecido por la Organización Mundial de la salud (OMS) (11). El estándar de calidad ambiental (ECA) para el Cadmio es de 0,005 mg/L en aguas destinadas para consumo humano, según el Decreto Supremo N° 004-2017- MINAM. Así mismo, la FAO/OMS en 1972 estableció que el cadmio puede ingerirse como máximo semanalmente en un rango máximo de 0,4-0,5 mg por persona y en el agua hasta 10 mg/L. Esto, debido a su toxicidad que produce disfunción renal y trastornos pulmonares, neurológicos, sobre el sistema cardiovascular, reproductor y carcinogenicidad.
El objetivo del presente estudio es evaluar la capacidad de muestras de diatomita para remover iones Cadmio (II) presentes en muestras de agua obtenidas del río Tambo (cerca de la zona de Punta de Bombón, en Perú). El cadmio residual en las muestras de agua será medido después de un proceso de quimisorción y filtración del agua utilizando diatomita. Diatomita son rocas de caparazones de diatomitas fosilizadas, compuestas en un 60% de sílice (SiO2) 2), (3 y tienen la función de filtrar el cadmio del agua. Este trabajo pretende contribuir al cuidado y balance del medio ambiente fluvial en el Perú.
EXPERIMENTAL
Procedimiento de toma de muestra
Se delimitó el punto de muestreo, según accesibilidad, en la zona de Punta de Bombón, Puente COSTANERA NORTE, en Perú, con coordenadas 17°08'45,6"S 71°47'50,2"W. Se registró en campo los parámetros de pH y temperatura. Se tomaron muestras puntuales de agua superficial en frascos de plástico PET para la medición del parámetro de Cadmio. Se tomaron 5 muestras de volumen de 300 mL, sin la adición de preservantes, asegurando la cadena de frío mediante el uso de un recipiente refrigerado con hielo (cooler con ice pack).
Recolección de diatomita
La diatomita se encuentra en estado natural, y por estudios previos realizados por Caballero y Zuni mencionados en su tesis 8, se tomaron las muestras de diatomita en el sector de Subín, ubicado en el departamento de Moquegua, Perú, con Coordenadas UTM WGS 84-19K, Este: 264776 y Norte: 8161297.
Procesado de las muestras
En laboratorio, las muestras de diatomita fueron lavadas con agua destilada, eliminando impurezas disueltas en ellas, así como también las que precipitaron. Las muestras fueron secadas bajo sombra durante una semana. Posteriormente, se molió en morteros de porcelana. Luego, la diatomita fue tamizada con tamices ASTM #8, #20 y #100 respectivamente. Se recolectó la fracción pasante del tamiz ASTM #100 para ser utilizada en la activación química. Se pesaron y recolectaron en bolsas herméticas dos muestras de 1 kg cada una.
Activación química de la diatomita
En un vaso de precipitado se colocaron 50 g de diatomita tamizada y se añadieron 300 mL de ácido nítrico al 5% de concentración para su activación, de acuerdo a Moreno et al. 4. Posteriormente, la suspensión se calentó llevándola a ebullición durante 2 horas. Se dejó decantar y enfriar la mezcla. Una vez enfriada, se lavó con abundante agua destilada para eliminar el excedente de ácido presente en la muestra. Se decantó para eliminar el agua. El sólido húmedo se secó en una estufa a una temperatura de 50 °C por 24 horas. Se molió en mortero de porcelana. Se recolectó la fracción separada por tamiz ASTM #100 y se colocó en bolsa hermética. Luego, se procedió a determinar la porosidad de la diatomita utilizando un microscopio de barrido.
Análisis estadístico
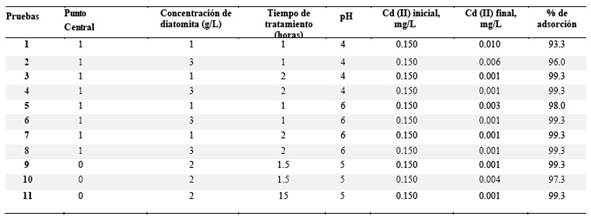
Se realizó el diseño factorial 2k con 3 puntos centrales. Se consideraron 3 factores, con un bloque y se realizaron 11 pruebas en total incluyendo los 3 puntos centrales. En la tabla 1, se puede observar las variables de la investigación. Se pudo obtener el modelo de la concentración final de Cadmio II en la muestra de agua después de su tratamiento con diatomita a partir del diseño factorial.
Proceso de remoción de cadmio con el Sistema Batch.
Se tomó la cantidad de diatomita de acuerdo a la matriz experimental mostrada en la tabla 2. Se realizaron ensayos con tres niveles de concentración de diatomita por litro de agua en evaluación, realizando las siguientes pruebas:
a) 1 gramo de diatomita por 1L de agua en estudio: Muestras: 1, 3, 5, 7
b) 2 gramos de diatomita por 1L de agua en estudio: Muestras: 9, 10, 11
c) 3 gramos de diatomita por 1L de agua en estudio: Muestras: 2, 4, 6, 8
Adsorción del cadmio (II) por diatomita
En un vaso de precipitado se añadió una cantidad de muestra de agua del Río Tambo y de la diatomita activada de acuerdo al diseño factorial. Los tiempos de agitación fueron de 1, 1,5 y 2 horas de acuerdo al diseño. Luego de la agitación, se obtuvo una mezcla sólido-líquido. Se filtró la mezcla en papel filtro Whatman N° 40. Se retuvieron los sólidos y se llevaron a caracterizar mediante Microscopia Electrónica de Barrido (SEM). Luego del filtrado, se procedió a determinar la concentración de Cd (II) por el método 200.7 de la EPA, y por étodo espectrométrico de emisión atómica de plasma acoplado inductivamente, para el análisis de trazas de agua y desechos.
Análisis de la diatomita y su adsorción de cadmio
Aplicando el método Echlin 5, se llevó las muestras al microscopio electrónico de barrido, análisis para el cual se fijó la muestra en cinta de carbono en plataformas de metal denominadas “stub”. Se realizó el metalizado por “sputter” mediante el bañado en oro (1 minuto y 30 segundos; a 18 miliamperios mA). Luego, se realizó la observación en el Microscopio Electrónico de Barrido (SEM) a alto vacío (INSPECT S50) según la metodología propuesta por Lux (Microscopia electrónica ultraestructura y citología vegetal). Se obtuvieron imágenes a aumentos de 100x, 500x, 1000x y 5000x. Los parámetros utilizados para el filamento fueron los siguientes: abertura 4-5, distancia de trabajo de 10 mm y una intensidad energía eléctrica de 8-10 kilovoltios (kV).
Figura 1. Muestras metalizadas de diatomitas con oro para caracterizar mediante el Microscopio Electrónico de Barrido (SEM)
Análisis factorial
Para realizar el análisis factorial y obtener la ecuación de regresión de remoción del Cd (II) se utilizó el método factorial con 3 réplicas y el análisis de varianza.
Análisis mediante espectrofotometría de absorción atómica:
Para la cuantificación de Cadmio se utilizó el ICP-OES-Perkin Elmer Optima 8000. Se siguió el método 200.7 de la EPA titulado “Determinación de metales y elementos traza en agua y residuos por plasma de acoplamiento inductivo a espectrometría de emisión atómica”. Las muestras de agua antes y después de su tratamiento con diatomitas fueron nebulizadas y el aerosol resultante fue transportado a la antorcha de plasma de argón inducido por radiofrecuencia. Los instrumentos midieron los espectros de emisión de líneas atómicas característicos por espectrometría. Los espectros se dispersaron mediante un espectrómetro de rejilla y las intensidades de los espectros de línea se monitorearon a longitudes de ondas específicas mediante un dispositivo fotosensible. Las fotocorrientes del dispositivo fotosensible fueron procesadas y controladas por un sistema informático.
RESULTADOS Y DISCUSIÓN
Resultados de la matriz
Los resultados de laboratorio usando la técnica de espectrofotometría de absorción atómica para la medición de Cd (II) se detallan en la tabla 2. También se muestran los valores de las variables en base al modelo del diseño experimental. Se visualiza un alta adsorción de Cadmio (II) por la diatomita, mostrando la eficiencia del método empleado en función a la matriz experimental.
En la tabla 2, se puede observar también los valores iniciales de las concentraciones reales de cadmio en las aguas muestreadas y a su vez la disminución de dichos valores después del tratamiento con diatomitas 7), (8.
En la imagen SEM de la diatomita natural (Fig. 2A) se observa las frústulas activadas químicamente con microtubos entre tamaños de 6.312 μm y 4.730 μm de forma céntrica, antes de la adsorción. También se puede observar los microporos de la diatomita, en los laterales de los microtubos, con diámetros alrededor de 1 μm. Asimismo, en las partículas de diatomitas se visualiza que existe una acumulación de microcristales tanto en el microtubo, como en la superficie después de la adsorción de cadmio (II) (Fig. 2B). Según Chang et. Al 6, este proceso de quimisorción es producido en gran medida por intercambio iónico entre los iones de cadmio II y los de Mg II y Ca II presentes en la diatomita. Pero también, en menor medida, existirá el atrapamiento del cadmio en los microporos de la diatomita 6.
Resultados del análisis de varianza ANOVA
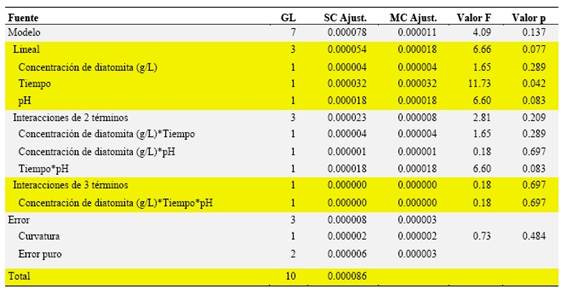
La tabla 3 muestra los resultados del análisis factorial 2K con 3 factores que son el pH, el tiempo de tratamiento y la concentración de diatomita.
El factor b (tiempo) influye grandemente en el porcentaje de adsorción de Cd (II) con un nivel de significancia del 5%. Por otro lado, se acepta la hipótesis nula para la concentración de diatomita y pH, así como las interacciones dobles y triples. Es decir, que las interacciones no tienen efecto significativo sobre él porcentaje de adsorción del Cd (II), habiéndose obtenido el valor de Efecto B (Tiempo) = 0.042.
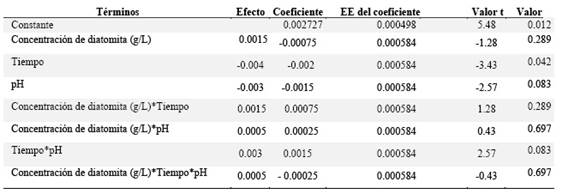
Estimación de los efectos de factores e interacciones
La Tabla 4 muestra los efectos de los factores que tienen influencia en la variable de respuesta. Esto significa que el factor Tiempo presenta un mayor efecto cuando cambia de un nivel inferior de 1 hora a uno superior de 2 horas y disminuyendo la concentración de cadmio (II) en 0.004 mg/L. Cuando el pH cambia sus niveles de (-) a (+), la variable respuesta disminuye en 0.003. Cuando los niveles de concentración de diatomita cambian del nivel inferior al superior, la concentración (mg/L) de Cadmio disminuye en 0.0015. Este efecto de los factores principales se ve reflejado en la Interacción triple, Concentración de diatomita, Tiempo y pH que indica que la variable medida disminuye en 0.0005 mg/L de Cadmio, lo cual no sucede cuando se presentan interacciones dobles.
Gráficas factoriales
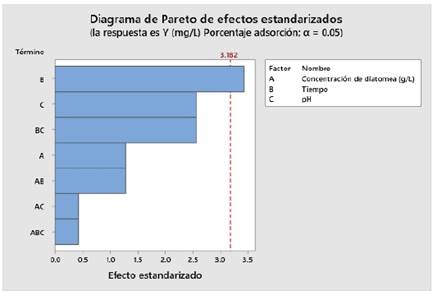
Gráficas de efectos estandarizados y diagrama de Pareto de efectos estandarizados
Los factores que no atraviesan la línea recta vertical segmentada roja en la Fig. 3, no tendrán efecto significativo en la variable de respuesta. El efecto B que es el tiempo, tiene mayor efecto significativo sobre la variable respuesta y no tiene efecto significativo de los otros factores principales A y C. Las Interacciones dobles y triples tampoco tienen un efecto sobre la variable respuesta según la tabla 4 de Coeficientes codificados. Los resultados muestran que el valor t indica que la concentración de la diatomita no es significativa.
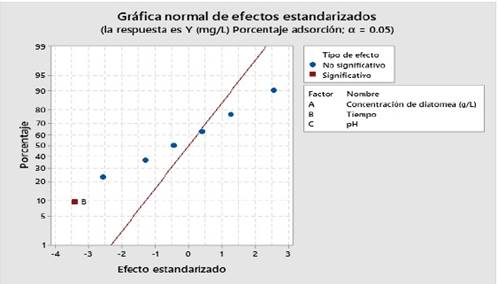
Grafica normal de Efectos estandarizados.
En la figura 4, se presenta una línea recta oblicua segmentada roja de referencia, los factores que están alejados de esta línea no tienen significancia.
Diseño del modelo matemático y ecuación de regresión para la remoción del Cd
En la tabla 5, R-cuad. nos indica que el 90.51% de los datos están representados por este modelo.
Ecuación de regresión en unidades no codificadas
Del análisis del diseño experimental se obtuvo el modelo matemático para la adsorción del Cd.
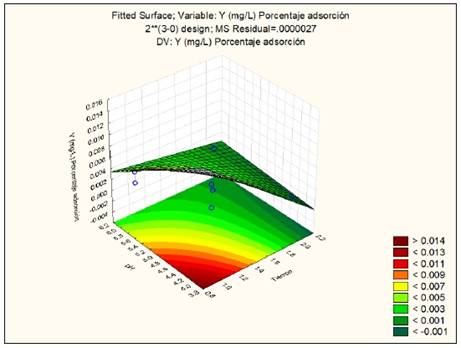
La figura 5 muestra la gráfica de superficie de respuesta donde el color rojo representa cuantificación de la variable Cd (mg/L) entre 0.014 y 0.009. Por otro lado, el color verde representa combinaciones de Tiempo y pH con valores menores a 0.005 mg/L de Cadmio. Por tanto, la región de interacción más favorable es a mayor tiempo y pH entre 4 a 6, siendo indistinto cualquier concentración de diatomita (g/L).
CONCLUSIÓN
El objetivo de la investigación es el estudio de remoción de iones de cadmio (II) de muestras de agua colectadas del Rio Tambo. Para esto, la diatomita resultó ser eficiente en el uso de microfiltros para la remoción de cadmio presente en cuerpos de aguas contaminadas con dicho metal.
Se determinó que los niveles reales de concentración inicial de iones de cadmio (II) en el río Tambo en el momento de la colecta de las muestras, tenían un valor de 0,150 mg/L. Según los resultados del análisis de laboratorio, se redujo la concentración de cadmio (II) en un 98,6 ± 0.9% utilizando las diatomitas. Es decir, se constató una concentración final de cadmio II de 0.002 ± 0.001 mg/L.
La activación de cualidad filtrante de la diatomita fue realizada con ácido nítrico al 5%, facilitando así una mayor adsorción de contaminantes del cuerpo de agua.
Con el uso de la matriz del diseño experimental en estos primeros estudios, y considerando una concentración de cadmio inicial en el agua de 0.15 mg/L, se logró disminuir los niveles iniciales de cadmio (II), presentes en las muestras colectadas. Después del tratamiento, dichos valores no sobrepasaron el valor de 0,005 mg/L de agua destinada para consumo humano según según el Decreto Supremo N° 004-2017- MINAM.
La diatomita demostró ser un buen filtro para la descontaminación de aguas con metales pesados, como es el caso del cadmio. Según el análisis de varianza, los coeficientes codificados con el diagrama de Pareto indican que el tiempo influye bastante en la adsorción de Cadmio (II) frente a la Diatomita.












 uBio
uBio