Revista Boliviana de Química
versión On-line ISSN 0250-5460
Rev. Bol. Quim v.37 n.5 La Paz dic. 2020
DOI: 10.34098/2078-3949.37.5.4
ARTÍCULOS ORIGINALES COMPLETOS
Thermochemical conversion and microstructural analysis of self-reducing
briquettes made of husk resulting from lamination coming from the
forming process of steel in hot (Mill scale), and recycled graphite
Conversion termoquímica y análisis microestructural de briquetas auto-reductoras
hechas de cáscarilla resultante de la laminación proveniente del proceso de
conformado del acero en caliente (Mill scale), y grafito reciclado
Edwin Urday Urday*, Marcelo Rodríguez Valdivia, Giancarlo Sánchez Chávez
Escuela Profesional de Ingeniería de Materiales, Facultad de Ingeniería de Procesos FIP, Universidad Nacional San
Agustín de Arequipa UNSA, Av. Independencia s/n-Pab. Ing. Materiales, phone +5154200037,
Arequipa, Perú, materiales@unsa.edu.pe, http://fip.unsa.edu.pe/ingmateriales/
* Correspondent author: eurday@unsa.edu.pe
Received 07 02 2020 Accepted 11 26 2020 Published 12 30 2020
Abstract
This paper shows the results of an investigation carried out to recycle the husk resulting from lamination coming from the (Mili Scale) forming process of steel in hot, in order to explore the possibility of obtaining sponge iron with a high metallic content. The experimentation consisted of forming self-reducing briquettes by mixing iron-oxide and graphite, and conducting them to a self-reducing process, varying the temperature from 900 to 1050°C for a minimum period of 30 min. expandable to 90 min, depending of the case. The husk and the reduced producís obtained were characterized by applying mineralogical analysis techniques using fluorescence and X-ray diffraction, and chemical and mineralogical composition using scanning electrón microscopy (SEM). In the reduced producís the amount of mass loss and the change in the proportion of real weight were determined. Additionally, the determination of the degree of metallic conversión was possible by means of the analytical technique of the analysis of metallic Fe and total Fe for each sample. The results showed that at the conditions: [90 min - 1050°C -13% of graphite, the degree of metal conversión is equal to 99.9%], and for: [30 min - 1050°C - 20.7% of graphite, a 95% of metal conversión is reached], and for: [90 min - 1050°C - 20.7% of graphite, a 94.4% of metal conversión is reached]. In the case of the máximum degree of metal conversión, the formation of iron could be observed from the coalescing of metal points (whiskers) that leads to formation of dense and compact phases.
Keywords: Self-reducing briquettes, Husk, Lamination, Metal conversión.
Resumen
Este artículo presenta los resultados de la investigación sobre reciclado de la cascarilla resultante de la laminación proveniente del proceso de conformado del acero en caliente, con el fin de explorar la posibilidad de obtener hierro esponjoso con un alto contenido metálico. La experimentación consistió en formar briquetas auto-reductoras mezclando óxido de hierro y grafito llevándolas a un proceso de auto-reducción variando la temperatura de 900 a 1050°C por el lapso mínimo de 30 min. extensible a 90 min., dependiendo del caso. La cascarilla y los productos reducidos obtenidos fueron caracterizados aplicando técnicas de análisis mineralógico mediante fluorescencia y difracción de rayos X, y de composición química mediante microscopía electrónica de barrido (SEM). En los productos reducidos, se determinó la cantidad de masa perdida y el cambio en la proporción de peso real. Adicionalmente, la determinación del grado de conversión metálica fue posible mediante la técnica analítica del análisis del Fe metálico y Fe total para cada muestra. Los resultados mostraron que en las condiciones: [90 min -1050°C - 13% de grafito, se alcanza un grado de conversión metálica igual al 99.9%], y para [30 min - 1050°C -20.7% de grafito, un 95% de conversión metálica se observa] y para [90 min - 1050°C - 20.7% de grafito, un 94.4% de conversión metálica se observa]. Para el caso del máximo grado de conversión metálica, se pudo observar la formación de hierro a partir del coalescimiento de puntos metálicos (whiskers) que conlleva a crear fases densas y compactas.
Palabras clave: Briquetas auto-reducto ras, Cascarilla, Laminación, Conversión metálica.
INTRODUCCIÓN
La industria siderúrgica constituye una actividad económica estratégica para el desarrollo de un país por su diversidad de procesos productivos que comprende, y la variedad de productos terminados que ofrece. Estos encuentran su aplicación en los sectores de la construcción, metalmecánica, minera, entre los más importantes. Como todo proceso productivo, implica la generación de grandes cantidades de residuos de carácter no metálico que contaminan el medio ambiente y que en dependencia del tipo de proceso utilizado pueden generar cerca de 500 kg de residuos sólidos de diferente naturaleza por tonelada de producto terminado [1]. Uno de estos residuos es la cascarilla de laminación, la cual representa cerca del 2% del total de acero laminado producido [2,3]. Por lo tanto, existe la preocupación de reutilizar estos desechos con la perspectiva de contar con materia prima con alto contenido de hierro [4] y considerando el control ambiental.
Desde la década de los 80s el interés por usar aglomerados reductores como materia prima para la fabricación de acero, ha crecido grandemente debido entre otras, a las siguientes ventajas [5]:
-Utiliza residuos como: finos de mineral, finos de carbón, etc., de bajo costo.
-El proceso de reducción es rápido, debido al contacto íntimo entre el reductor y las partículas de óxido
-Reciclar residuos siderúrgicos y obtener hierro esponja mediante un proceso de reducción a alta temperatura a bajo costo y amigable con el medio ambiente.
-La cascarilla de laminación es una capa de óxido de hierro que se forma en los materiales ferrosos que se enfrían después de ser procesados por laminado en caliente. Esta cascarilla contiene óxidos de Hierro (II) y hierro (III) con un contenido de 70% de hierro [6].
Algunos procesos comerciales de reciclaje como RHF (horno rotatorio), Inmetco, Fastmelt [7] son utilizados para tratar residuos sólidos o finos de mineral de hierro, los cuales son mezclados con material de carbón de bajo costo para producir briquetas y pellets [8], en los que el elemento reductor del óxido de hierro ya este contenido en su composición. Estos procesos se basan en la tecnología de la auto-reducción (reducción carbonotérmica) que consiste esencialmente en emplear aglomerados de óxidos de hierro mezclados con un agente reductor carbonoso en cantidad suficiente como para realizar su reducción completa [9]. Las reacciones químicas [10,11] resultantes por efecto de la temperatura permiten la reducción gaseosa de los óxidos de hierro (1) y la gasificación del carbón mediante la reacción de Boudouard (2).
FexOy(s) + CO (g) = FexOy-i(s) + CO2(g) (1)
C(s) + CO2(g) = 2CO (g) (2)
El presente estudio se ha dividido en dos fases. En la primera se ha caracterizado la cascarilla de laminación mediante determinación del tamaño de partícula, análisis mineralógico al difractómetro de rayos X, análisis de composición química y morfológico mediante microscopía electrónica de barrido (SEM). Asimismo, se fabricaron briquetas auto-reductoras en verde con diferente composición de mezcla para las pruebas de reducción.
En la segunda fase, se realizaron pruebas de reducción carbonotérmica (conversión termoquímica) determinándose la cantidad real de pérdida de masa considerando los pesos de las briquetas antes y después del proceso de reducción. Asimismo, se determinó el grado de conversión metálica empleando técnicas analíticas de determinación de Fe total y Fe metálico. Los resultados obtenidos, los cuales son coincidentes con los reportados en la literatura, permiten considerar positivamente la aplicación de este proceso a nivel industrial debido a su justificación técnico-económica.
EXPERIMENTAL
Materiales y métodos
La cascarilla fue obtenida de una empresa de la localidad de Arequipa, que se dedica a la fabricación de perfiles y barras de acero laminadas en caliente. Como material reductor, se utilizó residuos de electrodos de grafito provenientes de una fábrica de acero localizada en la ciudad de Pisco del departamento de lea. Ambos materiales fueron sometidos a un proceso de molienda para conseguir tamaños de partícula apropiados que permitan un íntimo contacto entre ellas. Como agente aglomerante se utilizó silicato de sodio por su habilidad de proporcionar una fijación rápida y un fuerte secado, así como la de suministrar una capa resistente al agua.
Caracterización de cascarilla de laminación
Muestras de cascarilla de laminación fueron analizadas utilizando un difractómetro de rayos X Siemens D 5000 usando las siguientes condiciones operativas: unfiltered CuK radiation, 40 KV, 30 mA, step size = 0.02°, tiempo de cuenta 2 s por cada paso. El análisis químico y la identificación morfológica se llevó a cabo empleando un microscopio electrónico LEO Evo 50 VP dotado de un dispositivo EDS con programa de cálculo por microanálisis semi cuantitativo INCA Energy 300 Oxford.
Preparación de briquetas auto-reductoras
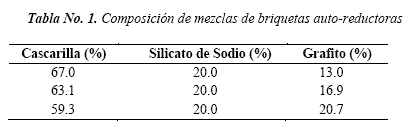
Se formaron briquetas usando un formador metálico con un diámetro interno de aproximadamente 25.4mm. Se prepararon diferentes mezclas constituidas por cascarilla de laminación, grafito y silicato de sodio. La Tabla No. 1, presenta las composiciones de mezclas utilizadas para las diferentes muestras. A fin de obtener buena plasticidad de las mezclas y facilitar la formación de las briquetas se añadió agua en una cantidad determinada. Las briquetas así conformadas y en verde, se llevaron a secado a temperatura ambiente durante tres días. La Figura No.1, muestra los materiales y las briquetas en verde.
Pruebas de reducción carbonotérmica
Se colocaron briquetas auto-reductoras en un contenedor de acero inoxidable y se cubrieron completamente con carbón mineral granulado a fin asegurar la presencia de gases reductores. A continuación, el contenedor fue colocado en un horno de resistencias eléctricas Veb Electro Bad Frankenhausen con dispositivo de control digital de temperatura de 0 hasta 1100°C. Las pruebas de reducción se llevaron a cabo siguiendo lo establecido en una matriz experimental factorial a dos niveles, considerando como variables independientes la temperatura (900, 975 y 1050°C), tiempo de reducción (30, 45 y 90min.) y cantidad de grafito (13, 16.9 y 20.7%). Bugdayci et. al [6], reportan haber empleado tiempos de reducción similares en pruebas realizadas a escala laboratorio.
Caracterización de los productos de la reducción carbonotérmica
Variación en la masa
Considerando el peso de las muestras antes y después del proceso de reducción, es posible determinar la cantidad real de peso que se pierde por efecto de la gasificación del material reductor (grafito) y el oxígeno perdido por parte de los óxidos de hierro. La cantidad de masa perdida (ΔM) se calcula mediante la siguiente ecuación (1):
ΔM=(Mi-M2)/Mi x 100 % (1)
Donde:
Mi : masa de muestra antes de la reducción (g)
M2: masa de muestra después de la reducción (g)
Asimismo, se analizó el cambio en la proporción de peso real (Pf/Pi) para cada muestra y según las condiciones de prueba a las que fueron sometidas. Donde: Pf = peso final de muestra reducida y Pi = peso inicial de muestra no reducida.
Grado de conversión metálica
El grado de conversión metálica se determina conociendo los contenidos de Fe metálico y Fe total. Para la estimación del contenido de Fe total, se tomó porciones de material de briquetas en verde y con mezclas: 67% de cascarilla+ 13% grafito + 20% silicato de sodio y 59.3% cascarilla + 20.7% de grafito + 20% de silicato de sodio. Para el cálculo del Fe metálico, se tomó material de las briquetas sometidas a reducción carbonotérmica. En ambas determinaciones, se utilizó la técnica analítica de titulación con dicromato de potasio [12].
El grado de conversión metálica (GCM) se calcula aplicando la ecuación (2):
GCM = (% FemetàlicoX Peso despuès / % Fetotal X Peso antes) X 100 (2)
donde :
GCM = Grado de Conversión metálica (%)
% Femetàlico = Contenido de Fierro metálico
% Femetàlico = Contenido de Fierro total
Peso antes = Peso de briqueta antes de la reducción (g)
Peso despuès = Peso de briqueta después de la reducción (g)
Reactivos
Determinación del Fe total:
HC1 (p.a.), solución de ClHg2 al 5%, solución sulfo-fosfórica, solución indicadora de difenilamina sulfonato de sodio, solución de K2Cr2O7 0.1N
Determinación del Fe metálico:
Solución de SO4Cu al 4%, H2SO4 (p.a), polvo metálico de Zn (p.a.), solución sulfo-fosfórica, solución de K2Cr207 0.1N.
Análisis morfológico mediante microscopía electrónica de barrido
El análisis se llevó a cabo sobre la superficie transversal de la briqueta auto-reductora correspondiente a cada prueba, haciéndose un barrido desde el centro hacia el exterior de la misma. Debido a la existencia de hierro reducido en todas las muestras, no fue necesario realizar una deposición superficial de oro para hacerlas conductoras. En todos los casos, se utilizó detector de electrones secundarios (SE) y una alimentación de tensión al filamento de 20 KV para la obtención de imágenes con buen contraste y resolución.
RESULTADOS Y DISCUSIÓN
Difracción de rayos X- Cascarilla
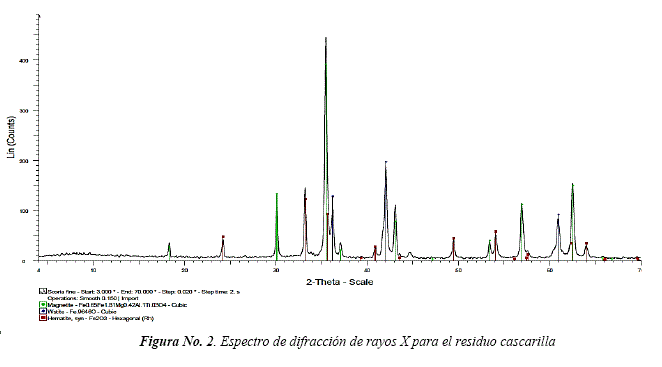
El análisis puso en evidencia la presencia de especies mineralógicas de óxidos de hierro como wustita (FeO), magnetita (Fe3O4) y hematita (Fe2O3); siendo la magnetita la fase predominante y de mayor cantidad. La Figura No. 2, muestra el espectro de intensidad para un barrido en muestra de cascarilla.
La Tabla No. 2, presenta los contenidos porcentuales de las fases mineralógicas calculadas a partir de las áreas debajo de los espectros. Se destaca la presencia de magnetita (Fe3O4) como óxido en mayor proporción (57.36%). Gaballah et. al, [13], reporta la presencia de los mismos óxidos de hierro además de cuarzo y hierro metálico para una cascarilla de laminación procedente de plantas egipcias.
Análisis químico
La Tabla No. 3, muestra la composición elemental porcentual del residuo cascarilla donde se puede apreciar que el mayor contenido corresponde al elemento Fe. La presencia de elementos como Cu, Mg y Al corresponden a elementos contaminantes externos.
Tamaño de partícula de cascarilla y grafito
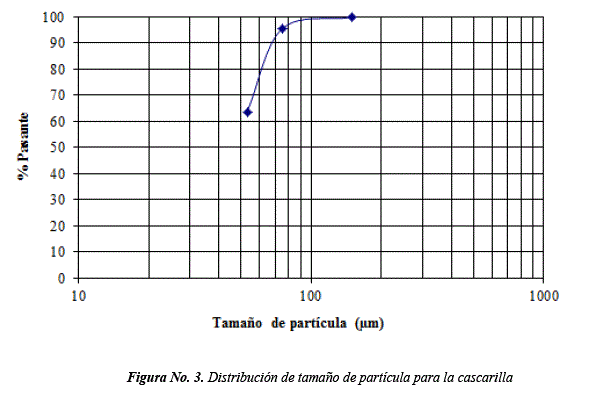
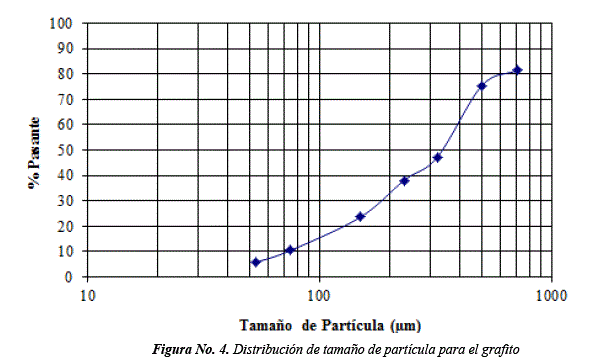
Las Figuras No. 3 y 4, muestran las gráficas de distribución de tamaño de partícula correspondientes a la cascarilla y al grafito.
Se obtuvieron clases granulométricas dimensionales de 150 hasta 53 um para la cascarilla y 710 hasta 53 um para el grafito respectivamente. Los tamaños de partícula conseguidos son similares a los sugeridos en la literatura consultada [14].
Análisis morfológico por SEM - cascarilla
La Figura No. 5, presenta formaciones cristalinas con hábito cristalino cúbico-hexaoctaedral correspondiente a la Wustita (FeO), trigonal-hexagonal de Hematita e isométrico-hexoctahedral que corresponde a la magnetita, en muestra de cascarilla [15].
Pruebas de reducción carbonotérmica
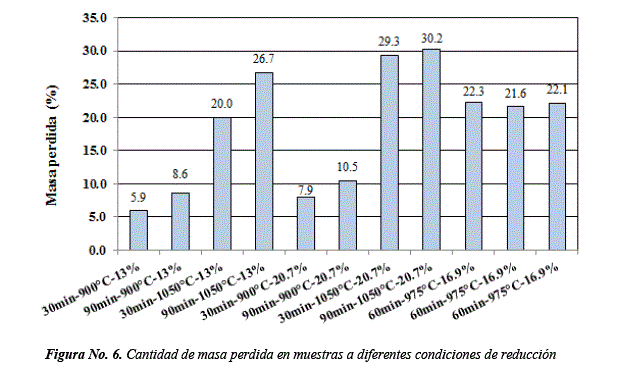
Cantidad de masa perdida (ΔM)
En la Figura No. 6, se presenta cantidad de masa perdida (ΔM), para muestras reducidas a diferentes condiciones de prueba.
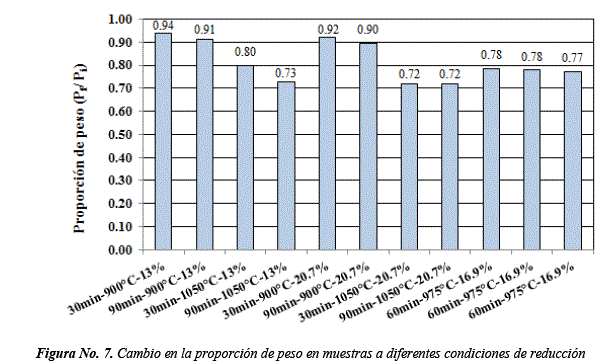
Cambio en la proporción de peso real (Pf/Pi)
En la Figura No. 7, se muestra el cambio en la proporción de peso real (Pf/Pi), para las diversas condiciones de ensayo consideradas en el diseño experimental.
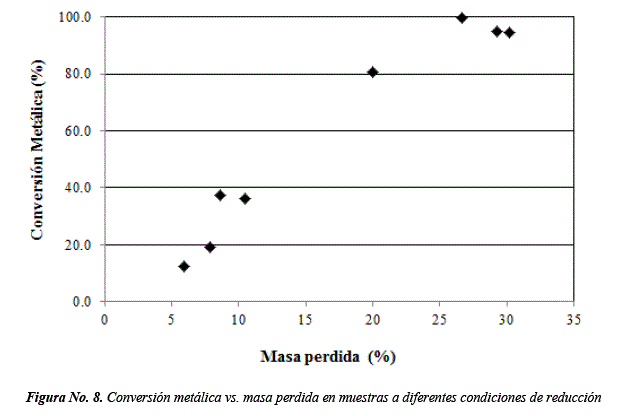
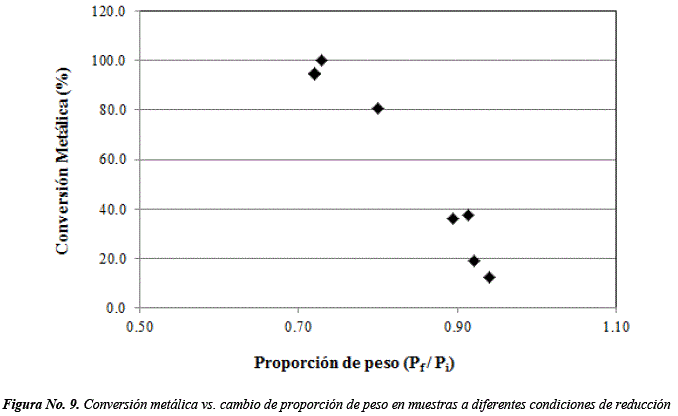
Relación del Grado de conversión metálica con la masa perdida y el cambio de proporción de peso
Las Figuras No. 8 y 9, presentan la relación existente entre el grado de conversión metálica con la pérdida real de masa y el cambio en la proporción de peso para cada prueba.
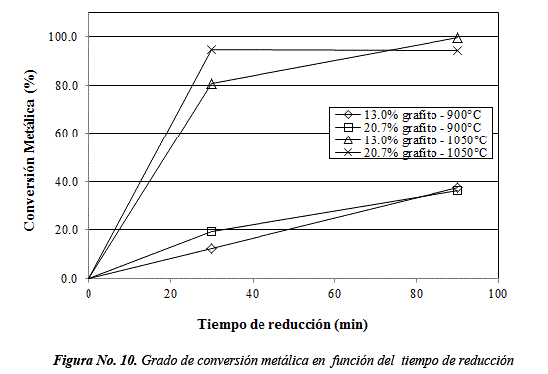
Efecto del tiempo de reducción sobre el grado de conversión metálica
La Figura No. 10, muestra el efecto del tiempo de reducción sobre el grado de conversión metálica para pruebas a 900 y 1050°C con cantidades de grafito de 13.0 y 20.7%.
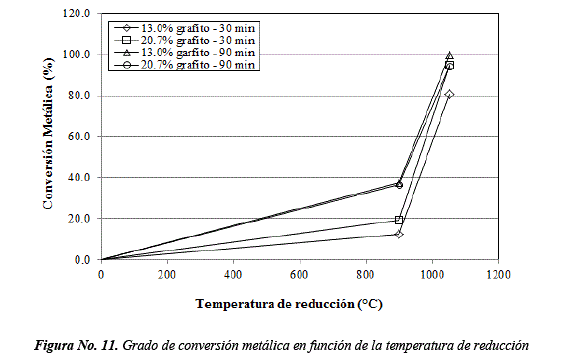
Efecto de la temperatura de reducción sobre el grado de conversión metálica
En la Figura No. 11, se muestra el efecto de la temperatura de reducción en el grado de conversión metálica para pruebas con 30 y 90 min. y cantidades de 13.0 y 20.7% de grafito.
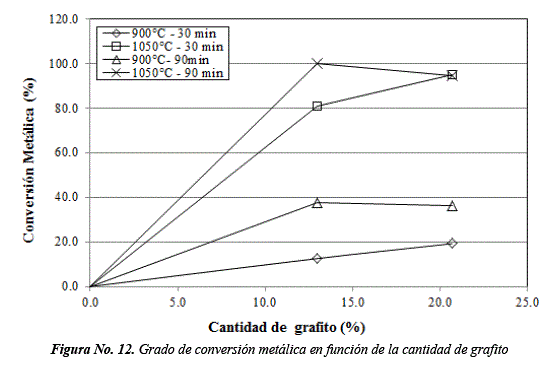
Efecto de la cantidad de grafito sobre el grado de conversión metálica
La Figura No. 12, muestra el cambio en el grado de conversión metálica por efecto de la cantidad de grafito para pruebas a 900 y 1050ºC por 30 y 90 min.
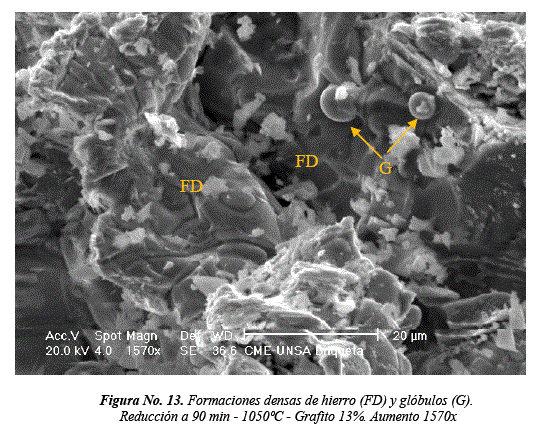
Análisis morfológico por SEM - briquetas reducidas
Las Figuras No. 13, 14 y 15, presentan las imágenes al SEM correspondientes a las muestras que presentaron mayores grados de conversión metálica, 99.9%, 95.0% y 94.4% respectivamente.
Materiales
El análisis de los resultados de la experimentación efectuada evidenció que:
La cascarilla de laminación y el grafito, después del proceso de molienda, presentan dimensiones adecuadas como para establecer un contacto íntimo entre partículas, condición que muchos autores consideran necesaria para el proceso de auto-reducción. El grado de reducción es directamente dependiente del tamaño de partícula, así, a menor tamaño corresponde un mayor grado de reducción. Esto se basa en el hecho de que, las partículas finas de óxido reaccionan más rápidamente que aquellas gruesas, debido al mejor contacto con las partículas de grafito.
Los resultados de difracción de rayos X, indican fases mineralógicas de óxidos de hierro como FeO, Fe2Ü3 y Fe3Ü4, sin presencia de compuestos minerales que corresponden a sulfuras, carbonates u otros que son comunes en minerales de hierro. Este hecho puede favorecer las reacciones de reducción al no encontrar impurezas. Hernández Buitrago et. al., [16], proponen que las posibles reacciones de reducción para estos óxidos en el rango de 700 a 1200°C serían según las reacciones:
Fe2O3(s) + CO(g) = 2Fe3O4(s) + CO2 (3)
Fe3O4(s) + CO = 3FeO(s) + CO2 (4)
FeO + CO(g) = Fe(s) + CO2(g) (5)
Por otro lado, Park, H., [17], explica que en la reducción; el Fe2O3 se convierte primeramente en FeO (el Fe3O4 es una fase intermedia formada por una reacción rápida) y seguidamente producto de una reducción adicional el FeO se reduce a Fe.
El silicato de sodio incorporado como aglomerante permite brindar buena resistencia mecánica a las briquetas, reduciendo considerablemente el tiempo de curado no superando las 48 horas para obtener productos en verde manipulables. Dankwah, J.R, [18], llevó a cabo la producción de pellets tomando un tiempo de curado superior de 72 horas empleando como aglomerante resina epóxica.
Reducción carbonotérmica
La Figura No. 16, muestra las briquetas auto-reductoras después del proceso de reducción carbonotérmica a 1050°C por 90 miny con una cantidad de grafito de 13.0%.
La mayor cantidad de masa perdida se presenta cuando la temperatura, el contenido de material reductor y el tiempo son altos. Este comportamiento se debe a la ocurrencia de reacciones de reducción del Fe2O3 a FeO y luego de FeO a hierro metálico. La pérdida de peso está asociado al aumento de moles de C reactivo y también a la alta temperatura que incrementa la velocidad de difusión y acelera las reacciones químicas [19].
Con respecto a la pérdida real de masa (ΔM), para un 26.7% de masa perdida, corresponde un grado de conversión metálica igual a 99.9%, mientras que para 29.3 y 30.2 son de 95.0 y 94.4% respectivamente. Los valores de pérdida real de masa obtenidos son cercanos a aquellos reportados para el caso de un proceso de auto-reducción completa [9].
A menor proporción de disminución de peso (Pf/Pi), la conversión metálica aumenta. Así, cuando Pf/Pi es igual a 0.73 se alcanza 99.9% de conversión metálica, mientras que para 0.72 corresponde 95.0 y 94.4%. Un indicio físico del grado de conversión de óxido a hierro metálico, está dado por ΔM y Pf/Pi que reflejan la pérdida de masa causada por la gasificación del carbono y la remoción del oxígeno contenido en el óxido durante el proceso de reducción
A 1050°C, el grado de conversión metálica se incrementa de 99.9 a 94.4%. De 900 a 1050°C, el grado de conversión aumenta 2.66 veces cuando se adiciona 13% de grafito y 2.5 veces con 20.7% de grafito en la mezcla. A altas temperaturas existe una concentración de gases reductores que promueve el equilibrio según la reacción de Boudouard, formando alta densidad de núcleos de hierro por una buena difusión [9]. Se puede afirmar que a esta temperatura y con 90 min. de reducción, el material reductor alcanza la gasificación completa no teniendo influencia en el proceso.
El grado de conversión metálica se ve incrementado cuando la temperatura es alta. A las condiciones de prueba de 90 min - 1050°C - 13% de grafito, 30 min. - 1050°C - 20.7% de grafito y 90 min - 90 min - 20.7% de grafito; llega a valores de 99.9, 95.9 y 94.4%, respectivamente. El proceso de reducción es más eficiente e incrementa el grado de conversión a altas temperaturas debido a una alta transferencia de calor y a la presencia de una atmósfera rica en gases de CO que evita la re-oxidación del material reducido [20]. Jiang, X, et. al, [21], en su investigación de reducción de pellets auto-reductores, concluyen haber conseguido un grado de conversión metálica de 97.6% el cual se encuentra entre los valores de 94.4% y 99.9% obtenidos por el presente estudio.
A medida que se incrementa el tiempo de reducción de 30 a 90 min., el grado de conversión metálico también aumenta. Es notoria la interacción de las demás variables (temperatura y cantidad de grafito), así, a valores altos y tiempos prolongados se consigue altos grados de conversión. Este comportamiento se debe presumiblemente a una rápida difusión del gas reductor y a una buena interacción con los diferentes óxidos presentes [22,23].
El mayor grado de conversión metálica es alcanzado cuando se usa 13% de reductor y el tiempo de reducción es 90 min. En estas condiciones, se mejora la conversión en 2.6 veces cuando se experimenta con temperaturas altas. Valores próximos a los obtenidos, son reportados en la literatura revisada [17].
Las formaciones densas y compactas de hierro se presentan a 1050°C, 90 min. y 13% de grafito. Se establece una secuencia en la morfología de hierro metalizado en función de la temperatura: A 900°C, se inicia la metalización mediante la formación de filamentos y agregados sintetizados de hierro, continuando progresivamente hasta 1050°C con formaciones de whiskers y capas densas compactas con ausencia de porosidad [23]. La formación de whiskers y glóbulos de hierro [10] ocasiona hinchamiento y un aumento del volumen en las briquetas auto-reductoras. Coincidentemente, Al-Kelesh, H., [24] identifica granos pequeños esféricos que crecen para formar clusters sintetizados. Al formarse capas metalizadas densas y compactas, hay una contracción con la consiguiente reducción de su volumen.
CONCLUSIONES
La conversión termoquímica a diferentes condiciones de prueba de briquetas producidas con cascarilla de laminación y grafito revelaron las siguientes conclusiones:
El alto contenido de óxidos (henatita, magnetita y wustita) en la cascarilla de laminación, representa una ventaja para el proceso de reducción no existiendo presencia de impurezas tales como azufre, fósforo, sílice, etc., que puedan interferir. Emplear tamaños de partícula en el rango de 75 a 5 um para el caso del óxido de hierro, y de 150 a 53 um para el grafito favorece la obtención de altos grados de conversión metálica. El silicato de sodio, usado como elemento aglomerante, confiere una alta resistencia mecánica en verde a la vez que asegura un buen contacto entre partículas de óxido y el material reductor (grafito).
La temperatura de reducción viene a constituir la variable más importante e influyente en el proceso de auto-reducción. Con su incremento en el proceso, se incrementan el cambio en la proporción de peso (Pf/Pi) y la pérdida real de masa (ΔM).
El mecanismo de crecimiento de hierro metálico sigue cuatros etapas: a) filamentos, b) agregados sintetizados, c) whiskers, d) formaciones densas metalizadas.
Cuando la auto-reducción se realiza a una temperatura de 1050°C y 90 min, se forma hierro a partir del coalescimiento de puntos metalizados (whiskers) que conlleva a crear fases densas y compactas.
Para condiciones de prueba a 90 min - 1050°C - 13% de grafito y 30 min - 1050°C - 20.7% y 90min - 1050°C - 20.7%, corresponden grados de conversión de 99.9, 95.0 y 94.4% respectivamente.
Los resultados obtenidos en este trabajo, demuestran la factibilidad de producir hierro esponja a partir de residuos de la industria siderúrgica (cascarilla de laminación y grafito). Esta alternativa tecnológica permite su reciclaje a bajo costo, con mínimas necesidades operacionales y alta compatibilidad ambiental.
RECONOCIMIENTOS
Los autores agradecen al Centro de Microscopía Electrónica de la Universidad Nacional de San Agustín de Arequipa, por la realización del análisis y su aporte con las imágenes de microestructuras al SEM.
REFERENCIAS
1. Davydenko, A., Karasev, A., Glaser, B., Jonsson P. 2019, Direct Reduction of Fe, Ni and Cr from Oxides Waste Products used in Briquettes for Slag Foaming in EAF, Journal Materials, 12(3434), 2-9. DOI: http://dx.doi.org/10.3390/ma12203434 [ Links ]
2. Murthy, Y., Agrawal, A., Pandey, A., 2017, Characterization of Mill Scale for Potential application in Construction Industry, Indian Journal of Engineering., 14 A(35), 71-76. https://www.academia.edu/30649327/Characterization_of_Mill_Scale_for_Potential_Application_in_Construction_Industry [ Links ]
3. Annunziata Branca, T., Coll, V., Algermissen, D., Granbom, H. 2020, Reuse and Recycling of By-Products in the Steel Sector: Recent achievements Paving the way to Circular Economy and Industrial Symbiosis in Europe, Journal Metals, 10(345), 2-18. DOI: http://dx.doi.org/10.3390/met10030345 [ Links ]
4. Mousa, E., Lundgren, M., Sundqvist, L., Erik-From, L., Robles, A., Friberg, H. 2019, Reduced carbon consumption and CO2 emission at the Blast Furnace by use of Briquettes containing Torrefied Sawdust, Journal of Sustainable Metallurgy, 5, 391-401. DOI: https://doi.org/10.1007/s40831-019-00229-7 [ Links ]
5. Dutta, S.K. 2017, Iron ore-coal composite pellets/briquettes as new feed material for iron and steemaking, Material Science & Engineering International Journal,1(1), 10-13. DOI: 10.15406/mseij.2017.01.00003 [ Links ]
6. Buğdaycı, M., Turan, A., Murat Alkan, M., Demirci F. & Yucel, O. (2014, February) A comparative Study on the Reduction of Mill Scale from continuous Casting Process. Paper presented to The 5th International Symposium on High-Temperature Metallurgical Processig, California, USA. Recuperado de DOI: https://doi.org/10.1002/9781118887998.ch62 [ Links ]
7. Dasgupta, S., Sallem, S., Srirangam P., Auniger M., Roy, G., 2020, A Computational Study on the Reduction Behavior of Iron Ore/Carbon composite Pellets in Both Single and Multi-layer Bed Rotary Hearth Furnace, Metallurgycal and Materials Transactions B, 51B, 818-826. DOI: https://doi.org/10.1007/s11663-020-01778-z [ Links ]
8. Ahmed, H., Perssons, A., Sundqvist, L. & Byorkman, B. (2014, September) Utilization of Steelmaking Industry Materials in Producing Direct Reduced Iron. Lecture presented at European Steel Environment & Energy Congress (ESEC), Teesside University, UK. Recuperado de: https://www.researchgate.net/publication/280090746_Utilization_of_Steelmaking_Industry_Waste_Materials_in_Producing_Direct_Reduced_Iron [ Links ]
9. Covcevich, M., Zymila, V., Osorio, E., Faria Vilela, A.C. 2014, Carbon Gasification in Self-reducing Mixtures, ISIJ International, 54(12), 2687-2696. DOI: http://dx.doi.org/10.2355/isijinternational.54.2687 [ Links ]
10. Guo, D., Hu, M., Pu, Ch., Xiao B., Hu, Z. 2015, Kinetics and mechanisms of direct reduction of iron ore-biomass composite pellets with hydrogen gas, International Journal of Hidrogen Energy, 40, 4733-4740. DOI: http://dx.doi.org/10.1016/j.ijhydene.2015.02.065 [ Links ]
11. Kowitwarangkul, P., Babich, A., Senk, A. 2014, Reduction Kinetics of Self-Reducing pellets of Iron Ore, AISTech, 611-622. https://www.researchgate.net/publication/286575723_Reduction_kinetics_of_self-reducing_pellets_of_iron_ore [ Links ]
12. Mohassab, Y., Elzohiery, M., Chen, F., Yong Sohn, H. 2016, Determination of Total Iron Content in Iron Ore and DRI: Titrimetric Method versus ICP-OES Analysis, The Minerals, Metals & Materials Society, 125-133. DOI: https://doi.org/10.1002/9781119274742.ch15 [ Links ]
13. Gaballah, N.M., Zikry, A.F., Khalifa, M.G., Farag, A.B., El-Hussiny, N.A. 2014, Kinetic Reduction of Mill Scale via Hydrogen, Science of Sintering, 46, 107-116. DOI: 10.2298/SOS1401107G [ Links ]
14. Man, Y., Feng, J., Ge, Q., Li, F. 2014, Effect of particle size on reduction behavior in iron ore-coal composite pellets, Journal of Chemical and Pharmaceutical Research, 6(7), 2484-2490. https://www.jocpr.com/articles/effect-of-particle-size-on-reduction-behavior-in-iron-orecoal-composite-pellets.pdf [ Links ]
15. Rocha Lemos, L., Freitas Seabra, S., Andrade de Castro, L., 2015, Reduction disintegration mechanism of cold briquettes from blast furnace dust and sludge, Journal of Materials Research and Technology, 4(3), 278-282. DOI: http://dx.doi.org/10.1016/j.jmrt.2014.12.002 [ Links ]
16. Hernández Buitrago, L., Daza Prada, I., Amaral-Labati, G., Bebeduce Neto, F., Lenz e Silva, F.B. 2018, Microstructural, thermochemestry and mechanical evaluation of self-reducing pellets using electric arc furnace (EAF) dust containing zinc for Waelz process, Revista Matéria, 23(2), 1-14. DOI: https://doi.org/10.1590/s1517-707620180002.0343. [ Links ]
17. Park, H., Sahajwalla, V. 2014, Effect of Alumina and Silica on the reaction Kinetics of Carbon Composite Pellets al 1473 K, ISIJ International, 54(1), 49-55. DOI: http://dx.doi.org/10.2355/isijinternational.54.49 [ Links ]
18. Dankwah, J.R. 2018, Waste Epoxy Modified Iron Oxide-Polymer Composite Pellets: Green Strength development and Oxide reactivity in Ironmaking Technology, Ghana Mining Journal, 18(2), 48-55. DOI: https://dx.doi.org/10.4314/gm.v18i2.6 [ Links ]
19. Man, Y., Feng, F.X., Chen, Y.M., Zhou, J.Z. 2014, Weight loss and direct reduction characteristics of iron ore-coal composites pellets, Journal of Iron and steel Research International, 2-11. DOI: https://doi.org/10.1016/S1006-706X(14)60188-6 [ Links ]
20. Jiang, X., Ding, G., Guo, H., Gao, Q., Shen, F. 2018, Carbonothermic Reduction of ore-coal Composite Pellets in a Tall Pellets Bed, Minerals, 8(550), 2-15. DOI: http://dx.doi.org/10.3390/min8120550 [ Links ]
21. Farahat, R., Eissa, M., Megahed, G., Baraka, A. 2010, Reduction of mill scale generated by steel processing, Journal of Steel and Related Materials, 88-92. https://www.researchgate.net/publication/288874180_Reduction_of_mill_scale_generated_by_steel_processing [ Links ]
22. Abdel Hamid, E.M., Amin, Ah.K., Sibak, H.A., Abadir, M.F. 2018, Kinetics of Reduction of El-Dekheila Pellets Fine Waste and Mill Scale Briquettes using Hydrogen, International Journal of Applied Engineering Research, 13(6), 3954-3965. DOI: http://www.ripublication.com [ Links ]
23. Covcevich Bagatini, M., Zymls, V., Osorio, E., Faria Vilela, A.C. 2011, Characterization and reduction Behavior of Mill Scale, ISIJ International, 51(7), 1072-1079. DOI: https://doi.org/10.2355/isijinternational.51.1072 [ Links ]
24. Al-Kelesh, H., Nasr, M.I. 2019, Reduction Behavior of Low Iron Ore at Reducing Conditions Simulating Different Zones of Blast Furnace, Materials Research, 22(2), 1-8. DOI: http://dx.doi.org/10.1590/1980-5373-MR-2018-0891 [ Links ]
25. Eissa, M., Ahmed, A., El-Fawkhry, M. 2015, Conversion of Mill Scale waste into Valuable Products via Carbothermic Reduction, Journal of Metallurgy, , 1-10. DOI: http://dx.doi.org/10.1155/2015/926028 [ Links ]












 uBio
uBio