Revista Boliviana de Química
versión On-line ISSN 0250-5460
Rev. Bol. Quim vol.35 no.4 La Paz 2018
FULL ORIGINAL ARTICLE
The conservation of the agricultural use bacteria Azospirillum Brasilense by microencapsulation
Conservación por microencapsulación de bacterias de uso agrícola: Azospirillum Brasilense
José L. Hernández Mendoza1, Paula L. Hinojosa López2, Ángel Salazar Bravo1, Jesús Gerardo García Olivares1, Guadalupe Concepción Rodríguez Castillejos2, Jesús Di Cario Quiroz Velásquez1*
1 Laboratorio de Biotecnología Experimental Centro de Biotecnología Genómica del Instituto Politécnico Nacional. Boulevard del Maestro s/n esq. Elias Pina, Col. Narciso Mendoza, Cd. Reynosa, Tamaulipas México, C.P. 88710.
2Unidad Multidisciplinaria Reynosa Aztlán de la Universidad Autónoma de Tamaulipas. Calle 16 y Lago de Chápala S/N, Aztlán, 88740 Reynosa, Tamps. Phone: 01 899 921 3340 phone +59122772269.
*Corresponding author: jqu¡roz@¡pn.mx
Received 09 17 2018 Accepted 10 22 2018 Published 10 30 2018
ABSTRACT
Microencapsulation is performed to protect or provide a cover for substances that are easily alterable, with the objective to mask flavors, store chemicals and transform products of traditional use into smart products, capable of changing under environmental conditions. In this work the process of encapsulation of the bacterium Azospirillum brasilense was evaluated. Different concentrations of sodium alginate and calcium chloride were used to achieve better yields, stability and viability. The best conditions to form a microcapsule were the combination of 2% alginate and 1M calcium chloride. Five years later the encapsulated bacteria underwent reléase, used the LB médium and germinating maize seeds. Bacteria were found viable, suggesting that the encapsulation of bacteria, or other microorganisms that associate with plants, as serving as agricultural inoculants.
Keywords: Microparticles alginate polymer conservaron, recuperation.
RESUMEN
La microencapsulación es un método que se emplea para proteger o proporcionar una cubierta a sustancias inestables, para enmascarar sabores, almacenar sustancias y transformar productos de uso tradicional en desarrollos tecnológicos avanzados. En este trabajo se evalúo la encapsulación de la bacteria Azospirillum brasilense como un método para conservar por largos períodos de tiempo bacterias no esporuladas. Se utilizaron diferentes concentraciones de alginato de sodio y concentraciones de cloruro de calcio para lograr mejores rendimientos, estabilidad y viabilidad. Los resultados mostraron que el alginato en bajas concentraciones produce solamente láminas delgadas que por lo general queda adheridas al sustrato empleado para secarlas y se pierden. Por el contrario, las mejores condiciones para formar una microcápsula uniforme, que húmeda es de aproximadamente 1 mm de diámetro, fue una combinación de alginato al 2% y Cloruro de Calcio al 1M. Las microcápsulas se secaron y se conservaron en seco, en frasco ámbar a temperatura ambiente. Cinco años después se sometieron microesferas a liberación de la bacteria lo cual se logró en medio de cultivo y junto a semillas en imbibición. Después de esto, se estima que la encapsulación es un método que puede servir para encapsular bacterias que puedan servir como inoculantes agrícolas.
INTRODUCCIÓN
La microencapsulación es una tecnología de empaquetamiento de sustancias químicas y materiales biológicos, que está conformada por partículas con una membrana polimérica [1]. La encapsulación de microorganismos permite el aislamiento físico y proporciona protección contra factores de medio ambiente o físico-químicos del suelo, permitiendo la liberación gradual del agente encapsulado [2]. Además, estas microcápsulas ofrecen la posibilidad de recuperar el agente ya que constituye un micro-entorno interno adecuado para las bacterias [3]. Los encapsulados pueden ser utilizados en la industria farmacéutica, alimenticia, medica, y agrícola [2,3,4]. El alginato ha sido uno de los polímeros más utilizado en la microencapsulación; pues forma una matriz altamente versátil, biocompatible y no tóxica para los componentes activos, células o microorganismos sensibles al calor, pH, oxígeno y luz, entre otros factores [5].
El alginato es un polímero natural compuesto de ácido D-manurónico y ácido L-glucurónico, y puede extraerse de diferentes macroalgas [6] así como de varias bacterias [7]. Las principales ventajas del alginato en el proceso de microencapsulado es su naturaleza no tóxica, su biodegradabilidad, su capacidad de liberar de manera lenta los agentes encapsulados y su bajo costo [2,3,8,9]. El alginato ha sido también utilizado en la encapsulación de microalgas para el tratamiento de aguas residuales [2,10]. El horizonte del uso de esta tecnología continúa en franca expansión en campos como la farmacología, la industria alimenticia y los probióticos entre otros [2,5,11,12].
La inoculación bacteriana en plantas está destinada a la promoción del crecimiento vegetal a través de la fijación biológica de nitrógeno y la liberación de hormonas vegetales, entre ellas, el ácido indol acético [13]. Este incremento en el sistema radicular favorece la absorción de agua y minerales [14]. El uso de los microorganismos ya inmovilizados y usados como biofertilizantes o bioplaguicidas han tenido gran aceptación entre los sistemas agrícolas [15]. Bashan[16] encapsuló Azospirillum brasilense y Pseudomona ñuorescencens que posteriormente fueron inoculadas en plantas de trigo en condiciones de campo. El inóculo se recuperó y sus poblaciones cuantitativamente fueron comparables a las poblaciones de bacterias inoculadas en turba que es la forma de comercialización de productos con esta bacteria.
Azospirillum brasilense es un bacilo móvil, gram negativo, de vida libre que se encuentra en el suelo [17]. Investigaciones recientes han demostrado algunas propiedades de A. brasilense como la producción de ácido indol acético, hormona vegetal de promoción del crecimiento vegetal y que aumenta la adaptabilidad de las plantas al habitat de la rizósfera [8,13], Azospirillum es considerado como uno de los géneros de rizobacterias promotoras del crecimiento vegetal más estudiados en los últimos 30 años, debido a su capacidad de mejorar significativamente el crecimiento y desarrollo, así como el rendimiento de numerosas especies vegetales de interés agrícola [10,19]. Esta bacteria muestra efectos benéficos en la planta debido a su capacidad de fijar nitrógeno, solubilizar fosfatos y producir sustancias promotoras del crecimiento en plantas, incluyendo fitohormonas y sideróforos [14,20]. Por las virtudes de Azospirillum brasilense antes mencionadas, se fijó el objetivo del presente trabajo en la evaluación de la eficacia del método de conservación bacteriana de encapsulación en alginato de calcio.
RESULTADOS, DISCUSIÓN
El alginato en su forma de sal sódica del ácido algínico (NaC6H7O)n (additive E-401), que es un forma purificada de la substancia original obtenida de las paredes de las algas cafés (Macrocystis pyrifera), interactúa con iones de calcio (CaCU) formando uniones donde el calcio hace de puente iónico entre los grupos carboxilo del alginato que es un copolímero de bloques homopoliméricos de residuos de β-D-mannuronato y su 5-epímero α-L-guluronato enlazados
en 1→4. Dicho intercambio de iones y la interacción con el copolímero permiten la formación de microcápsulas. [21,22]. En el proceso, la concentración de alginato toma un papel preponderante en la formación de las microcápsulas, ya que en la concentración más baja no se consolidan y al filtrarlas quedan adheridas al papel filtro como una película delgada. Solo en la concentración de 2% se formaron partículas que al secarse permanecen y son manejables. El pH aparentemente no tiene efecto en la formación de las microcápsulas ya que independientemente del mismo, las partículas no pierden sus propiedades o forma. Resultados similares han sido reportados para microencapsulados con glibenclamida [2,23].
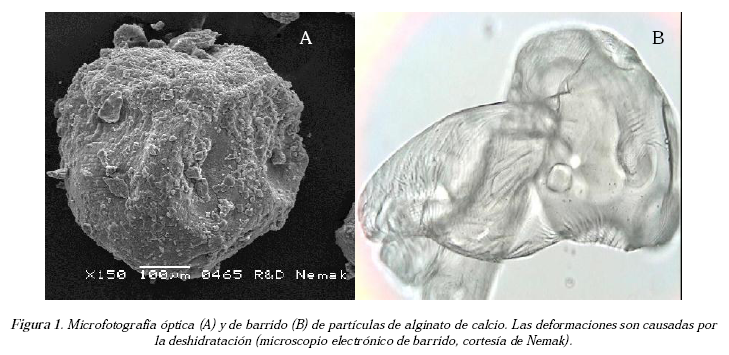
Las partículas del microencapsulado se formaron idealmente en una mezcla de alginato al 2% y cloruro de calcio 1M. En esta condición las partículas se produjeron mejor con una presión promedio de 10 Lb/Pulg2, donde no se fusionaron o adhirieron entre ellas, conservando su forma y su facilidad de manipulación (Figura 1B).
La concentración de cloruro de calcio no es determinante en el proceso y a 0.1 M, las microcápsulas requieren permanecer por más tiempo en la solución, mientras que a 1M, 15 minutos es suficiente. En esta concentración media, se observó la formación de filamentos, partículas con pliegues y contorno irregulares (Figura 1A). Estas condiciones no se consideran las mejores en el proceso de microencapsulación. En esta concentración el alginato está desorganizado, sin estructura, en forma de película delgada, con algunos espacios, pero nada definido como partícula pues se deforma al secarse. El alginato se adhiere al papel y se pierde.
En cuanto a la recuperación de la bacteria, al introducirse micropartículas en agua, estas no se disolvieron durante los 6 meses que estuvieron en observación. De la misma manera, al tomarse una muestra del agua, no se recuperaron colonias, por lo que se determina que no hay liberación de la bacteria encapsulada.
Por otra parte, al colocarse las microcápsulas en medio de cultivo, al cabo de 72 h se observa que hay formación de colonias de A. brasilense, por lo que se confirma que la bacteria permanece viva en las microcápsulas y es una forma de conservación de la cepa. Resultados similares han sido reportados al usar las microcápsulas de alginato [15].
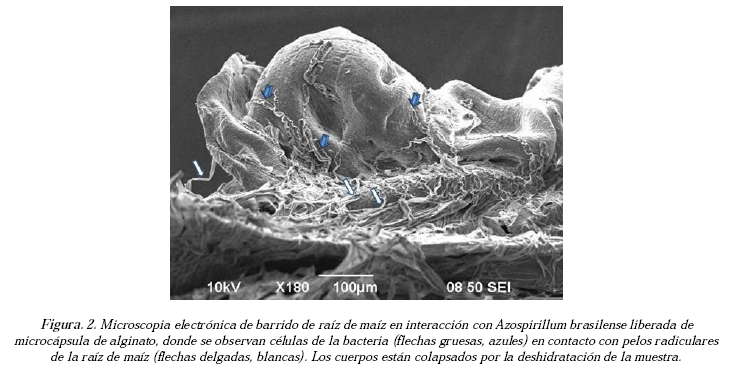
Al colocarse las microcápsulas de alginato junto a semillas de maíz en germinación, a simple vista no se observa la liberación de A brasilense, por lo que las muestras se deshidrataron para llevarlas a microscopía electrónica de barrido. Como resultado de éstas observaciones, se detectaron células bacterianas sobre la partícula de alginato adherida a raicillas de maíz. En esta misma imagen se pueden observar pelos radiculares en contacto con las células bacterianas (Figura 2).
Debido al gran potencial que presenta este proceso, se ha desarrollado en diferentes campos como en el área alimenticia y de la salud [2,5,21,24]. Homayouni et al. [25] evaluaron la inmovilización de bacterias probióticas con la finalidad de aumentar su supervivencia, los autores encontraron que la adición de cloruro de calcio a la mezcla de almidón y bacterias produjo una inmediata reticulación y con ello la formación de perlas de hidrogel, comprobándose la efectividad del uso de cloruro de calcio para la inmovilización de microorganismos. Las técnicas de microcencapsulación de bacterias están siendo utilizadas para diferentes alimentos como el queso adicionado con probióticos (L. acidophilus); en un estudio se evaluó la estabilidad de estas microcápsulas por 182 días en condiciones de refrigeración. Se encontró que el número de células viables se redujo en menor tiempo en el queso con bacterias libres; lo que demostró que las microcápsulas de alginato y almidón aumentan la tasa de supervivencia bacteriana [24]. En otro estudio llevado a cabo por Cruz et al. [26] se evaluó la microencapsulación de la microalga Chlorella vulgaris y de A. brasilense como agentes de tratamiento de aguas residuales; elaboraron perlas de polivinilpirrolidona, alcohol polivinílico o carboximetilcelulosa adicionadas con alginato y cloruro de calcio con la finalidad de aumentar su resistencia. Se encontró que, aunque las perlas iban perdiendo resistencia, permanecían estables el tiempo suficiente para eliminar la mayor parte de los contaminantes. De la misma manera, Lupo et al. [5] presentaron el uso de dicha técnica con diferentes probióticos.
En el presente trabajo se empleó una bacteria que no forma esporas de resistencia, con lo cual es potencialmente más susceptible de deshidratarse. Dada la importancia de la agricultura en nuestro país, se buscan nuevas alternativas para alargar la vida de anaquel; en ese sentido los inoculantes son una alternativa económica y efectiva para obtener resultados favorables en agricultura. El proceso de combinación de concentraciones fue muy rápido y sin mayores exigencias ya que una de las principales características de los componentes (alginato de sodio y cloruro de calcio) es la facilidad e inocuidad del proceso, sin influencia alguna de factores medioambientales.
Los resultados obtenidos permitieron demostrar la estabilidad de las partículas en agua (debido a su hidroinsolubilidad) sin difusión bacteriana alguna ni formación de colonias. Por otra parte, cuando las partículas se colocan en las cajas con agar LB se logró, tras una evolución temporal, recuperar bacterias del medio y comprobar la formación de colonias.
Finalmente, cuando las partículas se colocaron en el medio de germinación de semillas de maíz (Pioneer 30P49), fue posible recuperar la bacteria después de las 24 horas pos-inoculación (Fig. 2).
La microencapsulación puede tener diferentes usos [21]. Es por ende importante llevar a cabo investigaciones sobre la factibilidad del proceso en otros ámbitos e.g. la utilización de otro tipo de bacterias, o en áreas de impacto como la salud, en tal sentido es importante poner énfasis en la liberación bacteriana prolongada [2,23] además de en la extensión del tiempo de vida y en la vida de anaquel.
EXPERIMENTAL
Se analizaron cuatro variables: concentración de alginato de sodio (2%, 1.5%, 1%), concentración de cloruro de calcio (0.1 y 1 molar), pH (6,7 y 8) y finalmente la recuperación de la bacteria tiempo después del almacenamiento.
El alginato comercial (Alginic acid sodium salt Sigma-Aldrich A2158) tiene una presentación de polvo humectable de color claro y sin olor a temperatura ambiente. Se pesan 20 gr de alginato comercial, se agrega lentamente agua caliente (1000 mL a 55° C) y se agita hasta disolución. El cloruro de calcio (Caledon Número de catálogo 2520-1) se disuelve a temperatura ambiente. Los compuestos ya preparados se esterilizan a 121°C por 15 min.
La bacteria es una cepa nativa de suelo agrícola cultivado con sorgo y conservada en glicerol al 86%. Se creció en caldo Luria Bertani (USBological Life Sciences) a 27°C y con agitación a 200 RPM hasta tener una riqueza de 1x106UFC/mL-1. Posteriormente la suspensión bacteriana se mezcló con el alginato de sodio a temperatura ambiente y se agitó hasta homogenizar la muestra. Estas preparaciones fueron empleadas para encapsulamiento. Por otra parte, se preparó un lote de alginato, solo sin la bacteria para ser empleado como control. Todo el alginato empleado en los diferentes experimentos fue esterilizado (120°C y 15Lb/Pulg2).
Para el proceso de encapsulación, el alginato solo o mezclado con la bacteria, se colocó en un recipiente y se acopló con un sistema de compresión (10 lb/Pulg2) para expulsar muestras de material a través de una puntilla de micropipeta (T-300, Axygen) mismas que se depositaron en un crisol de 2 L con 1.5 L de cloruro de calcio, agitado con un magneto (200RPM) por espacio de 15 min. Después las microesferas fueron recuperadas por filtración usando papel Whatman No. 1 y se dejaron secar a temperatura ambiente (26°C ± 2°C) durante 24h. Se realizaron observaciones de las microcápsulas por microscopía óptica y electrónica de barrido (Nikon modelo Alphaphoto YS).
Las partículas permanecieron almacenadas a temperatura ambiente, en frasco ámbar cerrado y en obscuridad por 5 años, al cabo del mismo se sometieron a diferentes pruebas entre ellas, la disolución directa en agua desionizada, la siembra en agar e inoculando plántulas de maíz. Para el primer caso, las partículas (200mG) fueron colocadas en tubos de ensayo con agua desionizada y 48 horas después se realizó la observación y toma de muestra para siembra en agar LB. Los ensayos de recuperación directa se realizaron colocando micropartículas de alginato en placas de agar LB, mismas que se incubaron a 27° C por 48 horas. En el caso de la inoculación de plántulas de maíz, se colocaron las partículas en semillas de maíz germinando y 72 horas después se tomaron muestras para siembra en agar y para microscopía electrónica de barrido. En todos los casos el parámetro considerado fue la recuperación de la bacteria.
CONCLUSIONES
Se demostró que la microencapsulación con alginato de sodio y cloruro de calcio es un método adecuado para la conservación temporal, literalmente 5 años, de microorganismos, a saber, la bacteria de aplicaciones agrícolas, Azospirillum brasilense.
RECONOCIMIENTOS
Se agradece el financiamiento del presente trabajo al Instituto Politécnico Nacional (IPN) a través de proyectos SIP. José Hernández-Mendoza agradece por ser becario del COFAA-IPN, EDI-IPN y SNI. Guadalupe Concepción Rodríguez-Castillejos agradece al SNI. Paula Hinojosa-López, estudiante de QFB agradece a la Universidad Autónoma de Tamaulipas Unidad Aztlán por la correspondiente cobertura.
REFERENCIAS
1. Parra-Huertas, R.A. 2010, Microencapsulación de Alimentos, Rev. Fac. Nal. Agr., 63, 5669-5684. [ Links ]
2. Charles-Navarro, D., Bocanegra-García, V., Palos, I., Rivera, G., Esquivel-Ferriño, P., Gracia-Vásquez, S., Ortiz-Andrade, R., Jesús Quiroz-Velásquez, J., Hernández-Mendoza, J.L. 2010, Encapsulation and reléase characteristics of glibenclamide loaded calcium-alginate beads, Quím. Nova, 33, 1435-1439. [ Links ]
3. Bashan, Y., Hernández, J.P., Leyva, L., Bacilio, M. 2002, Alginate Microbeads as inoculant carrier for plant Growth- promoting bacteria, Biol. Fértil. Soils, 35, 359-368. [ Links ]
4. Rathore, S., Desai, P., Liew, C, Chan, L., Heng, P. 2013, Microencapsulation of microbial cells, J. FoodEng., 116, 369-381. [ Links ]
5. Lupo, B., González, C, Alicia, M. 2012, Microencapsulación con alginato en alimentos. Técnicas y aplicaciones, Revista Venezolana de Ciencia y Tecnología de Alimentos, 3, 130-151. [ Links ]
6. Rahelivao, M., Andriamanantoanina, H., Heyraud, A., Rinaudo, M. 2013, Structure and properties of three alginates from Madagascar seacoast algae, FoodHydrocolloid, 32, 143-146. [ Links ]
7. Hay, I., Reliman, Z., Ghafoor, A., Rehm, B. 2010, Bacterial biosynthesis of alginates, J. Chem. Technol. Bíotechnol, 85, 752-759 [ Links ]
8. Kitamikado, M., Yamaguchi, K., Tseng, C, Okabe, B. 1990, Methods Designed to Detect Alginate-Degrading Bacteria, Appl. Environ. Microbio!, 56, 2939-2940. [ Links ]
9. Chan, E.S., Wong, S.L., Lee, P.P., Lee, J.S., Ti, T.B., Zhang, Z., Poncelet, D., Ravindra, P., Phan, S.H., Yim, Z.H. 2011, Effects of starch filler on the physical properties of lyophilized calcium-alginate beads and the viability of encapsulated cells, Carbohydr. Polym, 83, 225-232. [ Links ]
10. Bashan, Y., Holguin, G., Bashan, L. 2004, Azospirillum-plant relationships: physiological, molecular, agricultural, and environmental advances (1997-2003), Can. J. Microhiol, 50, 521-577. [ Links ]
11. Avendaño-Romero, G.C., López-Malo, A., Palou, E. 2013, Propiedades del alginato y aplicaciones en alimento, Temas Selectos de Ingeniería de Alimentos, 7, 87-89. [ Links ]
12. Campos, D.C., Acevedo, F., Morales, E., Aravena, J., Amiard, V., Jorquera, M.A., Inostroza, N.G., Rubilar, M. 2014, Microencapsulation by spray drying of nitrogen-fixing bacteria associated with lupin nodules, World J. of Microhiol Biotechnol, 30, 2371-2378. [ Links ]
13. Hernández, J.L., Quiroz, J.D., Moreno, V.R., Mayek, M. 2008, Biosíntesis de ácido antracnílico y ácido indolacético a partir de triptófano en una cepa de Azospirillum brasilense nativa de Tamaulipas, México, Avances en Investigación Agropecuaria, 12, 57-67. [ Links ]
14. Dalla Santa, O.R., Soccol, C.R., Ronzelli, P., Fernández Hernández, R., Alvarez, G.L.M., Dalla Santa, H.S., Pandey, A. 2004, Effects of inoculation of Azospirillum sp. in maize seeds under field conditions, J. Food, Agrie, and Environ, 2 (1), 238-242, [ Links ]
15. Bashan, L., Bashan, Y. Plant growth-promoting bacteria andgreen microalgae: a convenient model for hasic studies ofplant-hacterium interactions. In: Azospirillum sp.: cell physiology, plant interactions and agronomic research in Argentina ed by Cassan, F. D., García de Salamone, I., 2008, Asociación Argentina de Microbiología, Buenos Aires, Argentina, 37-48. [ Links ]
16. Bashan, Y. 1986, Migration of the Rhizosphere Bacteria Azospirillum brasilense and Pseudomona Fluorescens Towards Wheat Roots in the Soil, J Gen Microbio, 132, 3407-3414. [ Links ]
17. Lin, S., Shen, F., Young, L., Zhu, Z., Chen, W., Young, C. 2012, Azospirillum formosense sp. nov., a diazotroph from agricultural soil, Int. J. Syst. Evol. Microbio!., 62, 1185-1190. [ Links ]
18. Fibach-Paldi, S., Burdman, S., Okon, Y. 2011, Key physiological properties contributing to rhizosphere adaptation and plant growth promotion abilities of Azospirillum brasilense, Microbiol. Lett., 326, 99-108. [ Links ]
19. Villa-Castro, L., Mayek-Pérez, N., García-Olivares, J.G., Hernández-Mendoza, J.L. 2014, Efecto de la inoculación en maíz con cepas nativas de Azospirillum sp, Avances en Investigación Agropecuaria., 18, 33-38. [ Links ]
20. Sivasakthivelan, P., Saranraj, P. 2013, Azospirillum and its Formulations: A Review, Int JMicrohiol Res., 4, 275-287. [ Links ]
21. Ortíz, J., Bravo, J.A., Vila, J.L. 2018, Molecular kitchen chemistry; Bolivian traditional gastronomy; molecular chuflay, Rev. Bol. Quim,, 35(1), 1-5. [ Links ]
22. https://en.wikipedia.org/wiki/Alginic acid, access date 09/17/2018.
23. Padrón-Pérez, C. Tesis de grado, Maestría en Análisis Clínicos, Análisis del proceso de microencapsulación de Metformina y Glibenclamida por gelificación iónica y validación del método por HPLC para su determinación. Universidad Autónoma de Tamaulipas. Unidad Aztlán, pp 73.
24. Mirzaei, H., Pourjafar, H., Homayouni, 2012, A. Effect of calcium alginate and resistant starch microencapsulation on the survival rate of Lactohacíllus acídophílus La5 and sensory properties in Iranian white brined cheese, Food Chem., 132. 1966-1970. [ Links ]
25. Homayouni, A., Ehsani, M., Azizi, A., Yarmand, M., Razavi, S. 2007. Effect of lecithin and calcium chloride solution on the microencapsulation process yield of calcium alginate beads, Irán Polym J, 16, 597-606. [ Links ]
26. Cruz, I., Bashan, Y., Hernández, G., Bashan, L. 2013, Biological deterioration of alginate beads containing immobilized microalgae and bacteria during tertiary wastewater treatment, Appl Microhiol Biotechnol, 97, 9847-9858. [ Links ]












 uBio
uBio