Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista Boliviana de Química
On-line version ISSN 0250-5460
Rev. Bol. Quim vol.33 no.5 La Paz Dec. 2016
ARTÍCULOS ORIGINALES
Chemical and mineralógica!. Characterization of Machu Rumi, a clay with geofagic uses by residents of Chimpajilahuata Community of Azángaro district, Puno, Perú
Heber Nehemias Chui Betancur1,*, Dwight Roberto Acosta Najarro2, Paula Ofelia Olivera de Lescano3, Godofredo Huamán Monroy1
*Corresponding author: heberchui@gmail.com
Abstract
Machu Rumi, or an oíd stone with geofagy applications used by members of the Chimpajilahuata community of Azángaro district in Puno, Perú, was chemically and mineralogically characterized. The samples were analyzed by means of the use of X-ray fluorescence (XRF), X-Ray Diffraction (XRD) and Scanning Electron Microscopy (SEM) whose elemental abundance was: Fe 11%, Al 4%, Ti 4080 ppm, Ca 814 ppm, and Zn 220 ppm, and other elements with low concentration such as V, Cr, Mn, Ni and Sr. Also, the main crystalline phases were identified by X-ray Diffraction and reported as: Quartz (SiO2), Clinochlore [Mg3 Al Mn2 Al Si3Oio(OH)8], Goethite [Fe+3O(OH)]; and Chamosita [(Mg5.036Fe4.964) AI2.724 (SÍ5.70 AI2.30 O20) (OH)i6]. Goethite presence was common in the layers 2, 3, 5 and 6; this clay mineral is considered a very effective reducing agent, capable of removing inorganic as well as organic arsenic. The topology sheet samples were observed across the micrographs obtained by scanning electrón microscopy.
Keywords: Machu Rumi, Geofagy, Clay, XRF, XRD, Chimpajilahuata.
Resumen
Spanish title: Caracterización química y mineralógica del Machu Rumi de uso geoíágico por los habitantes de la comunidad de Chimpajilahuata del distrito de Azángaro, Puno, Perú. En el presente artículo se describe la caracterización química y mineralógica del Machu Rumi (Piedra antigua con aplicaciones geofágicas por los integrantes de la comunidad de Chimpajilahuata del distrito de Azángaro, Puno, Perú). Las muestras fueron analizadas por la técnica de Fluorescencia de Rayos X (FRX), Difracción de Rayos X (DRX), y Microscopía Electrónica de Barrido (SEM) cuya abundancia elemental fue: Fe 11%, Al 4%, Ti 4080ppm, Ca 814 ppm, y del Zn con 220ppm, seguida de otros elementos de baja concentración como el V, Cr, Mn, Ni y Sr. Asimismo, se reportan las principales fases cristalinas identificadas por la técnica de Difracción de Rayos X como: cuarzo (SiO2), Clinochlore [Mg3 Mn2 Al Si3 Al O10 (OH)8], goetita [Fe+3 O (OH)]; y la chamosita [(Mgs.oseFe4.964) AI2.724 (SÍ5.70 AI2.30 O20) (OH)i6], la presencia de Goethita es común en las capas 2, 3, 5 y 6; este mineral de arcilla es considerado un reductor muy eficaz con capacidad de remover arsénico inorgánico así como orgánico. La topología laminar de las muestras fue observada a través de las micrografías obtenidas por Microscopía Electrónica de Barrido.
INTRODUCCIÓN
La cultura peruana es una rica mezcla de costumbres y tradiciones ancestrales [8,11] entre ellas, la ingesta de arcillas: machu rumi, ch'aqo, ch'aqu, chaco, ch'ako, ch'aquo, chhacco, ch'akko, chachakko, o también p'asa según denominaciones sinónimas en lengua quechua. Esta tradición se conoce en la cultura Uru (propia del Lago Titicaca) como qhiqhiche y en la cultura Aymara de Bolivia y del norte de Chile como upi. Las mismas son utilizadas para proveer de complementos minerales, contrarrestar componentes perjudiciales en la dieta (como las fitotoxinas) y/o para ciertos tratamientos médicos [3].
La Geofagia es el consumo deliberado de tierra, una costumbre ancestral practicada por muchas comunidades en el mundo [4,9,17]. En Perú se han encontrado reportes científicos referidos al consumo de arcilla en el altiplano, tal es el caso de ch'aqo, estudiado por Quispe et al. [15], quién reportó principalmente minerales correspondientes al grupo de las esmectitas (montmorillonita, nontronita, volkonskoita y vermiculita) y minerales correspondientes al grupo de los tectosilicatos (cuarzo, cristobalita, albita y ortoclasa). Además, se identificó en todas las muestras la presencia de microfósiles de diatomeas pertenecientes a la orden Pernales. La ingesta de arcilla es una práctica común de mujeres y niños en Nigeria, esas arcillas contienen fases cristalinas como la Montmorillonita, Chabazite-Na, Diaspore, Faujasite-Na, y Lizardite-IM, muestras colectadas cerca de Bauchi, Benue, Gombe, Kogi, Nasarawa, Osun y Plateau. Los análisis incluyeron Difracción de Rayos X (XRD) y ICP-OES para determinar los elementos químicos: Al, As, Cr, Cu, Fe, Pb, Se y Zn. También, los resultados de este análisis indican que metales como Pb y Se tienen concentraciones elevadas, las cuales no son recomendadas para el consumo humano y pueden contribuir a deteriorar la salud mediante malformaciones congénitas en recién nacidos y diferentes tipos de cáncer [1]. En la muestras de arcilla comestible de nombre Sikor, estudiadas en la universidad de Montfort Ucrania, se reportó la presencia de arsénico y otros elementos tóxicos, que fueron caracterizados mediante inducción de plasma (ICP-MS) encontrándose las concentraciones siguientes As (3.8-13.1 mg kg-1), Pb (21-26.7 mg kg-1) y Cd (0.09-0.4 mg kg-1), además de menores concentraciones de Mn, Fe y Zn, las cuales representan un potencial adverso para la salud, principalmente las debidas al As, Pb y Cd [2,16].
En la Universidad de California se analizaron 7 arcillas africanas que fueron colectadas en sitios arqueológicos ocupados por el Homo erectus y posteriormente por el Homo sapiens, cuyas costumbres incluyeron la geofagia. Estas arcillas comestibles fueron analizadas por Fluorescencia de Rayos X (FRX) cuyos resultados muestran la siguiente composición elemental; Ca, Cu, Fe, Mg, Mn y Zn. En lo referente al análisis mineralógico, se utilizó la técnica de Difracción de Rayos X (DRX) mediante la cual se identificaron fases cristalinas en cantidades significativas como la Kaolinita, Montmorillonita y la Sardinia, evidentemente, dichas arcillas contribuyeron con calcio a la dieta de las mencionadas comunidades [9].
Esta investigación tuvo por objeto caracterizar química y mineralógicamente la muestra llamada Machu Rumi, colectada de la comunidad de Chimpajilahuata del distrito de Azángaro provincia de Azángaro Puno Perú. El arsenal analítico empleado incluyó principalmente: Fluorescencia de Rayos X con energía dispersiva y Difracción de Rayos X. Este estudio constó de dos partes: 1. La caracterización de elementos químicos típicos y sus respectivas concentraciones con la finalidad de identificar elementos que pondrían en riesgo a la salud y 2. Identificación de fases cristalinas presentes en la muestra de investigación.
EXPERIMENTAL
Materiales y métodos Área de estudio
La muestra constituye una roca llamada Machu rumi, (que en el idioma quechua significa piedra vieja) es rígida por el exterior y que al quebrarla por la mitad dentro de ella existe polvo (fig. 1) con seis capas (análogo a un huevo). La geofagia del polvo tendría propiedades curativas sobre los intensos dolores abdominales, según los pobladores de la comunidad de chimpajilahuata del distrito de azángaro, Puno, Perú. La muestra fue colectada de la comunidad de chimpajilahuata con coordenadas geográficas: 14°55'15.1"Sy 70°13'27.9"O.
Trabajo en laboratorio
La roca tiene aproximadamente 12 cm de diámetro en promedio, cuya capa externa es de 2.3 cm en promedio, al partir la roca (Machu rumi) por la mitad, en el interior se pudo observar 6 capas de polvo (fig. 1), y se obtuvo muestras de cada capa, las cuales han sido estudiadas por Fluorescencia de Rayos X y la Difracción de Rayos X.
Las muestras en polvo, fueron directamente extraídas en espectrocapsulas sin ninguna preparación adicional, numeradas en forma creciente de afuera hacia el centro (fig. 1), se sometió al análisis por Fluorescencia de Rayos X con energía dispersiva, cuyas condiciones de análisis fueron: Fuente de Excitación Tubo de Rayos (Gd) con set de blancos secundarios, este equipo tiene un sistema modular de espectroscopia de Rayos X, constituido por un detector semiconductor de Si(Li) de 167 eV de resolución para 5.89 KeV de energía. Para la toma de datos se utilizó el Analizador Multicanal PCAII The Nucleus, y para la evaluación de espectros, la determinación cualitativa y los cálculos cuantitativos, se utilizó el Quantitative X-Ray Analysis Software (QXAS).
Las muestras en polvo, se colelactaron directamente a las capsulas pre-establecidas por el equipo de Difracción de Rayos X (DRX), a fin de estudiar las fases cristalinas, este equipo cuenta con un Difractómetro Bruker Miniflex II, con los siguientes parámetros de medición: paso angular de 0.04°, fuente de radiación Cu-Ka![]() , ángulos de 4o a 80° y 30 kV de voltaje de aceleración. Las microfotografias fueron obtenidas por medio de la Microscopía Electrónica de Barrido, JEOL JSM-5600LV (Jeol, Tokyo, Japan) Scanning Electron Microscope (SEM) operado a 15 keV.
, ángulos de 4o a 80° y 30 kV de voltaje de aceleración. Las microfotografias fueron obtenidas por medio de la Microscopía Electrónica de Barrido, JEOL JSM-5600LV (Jeol, Tokyo, Japan) Scanning Electron Microscope (SEM) operado a 15 keV.
RESULTADOS Y DISCUSIÓN
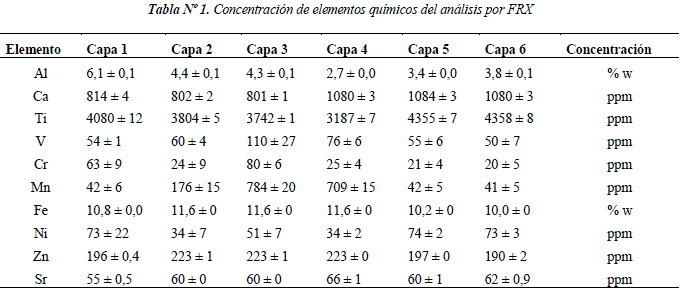
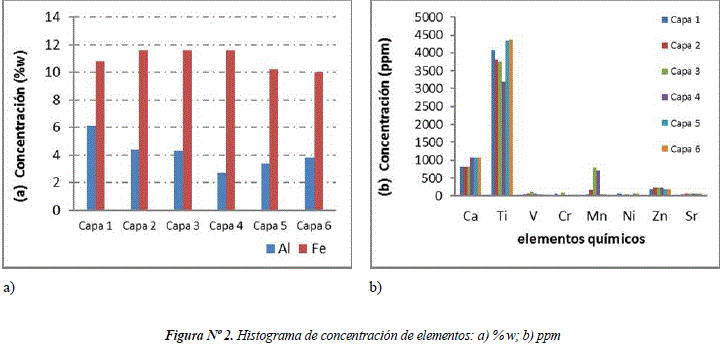
Del análisis por FRX (tabla 1) se pudo observar que los elementos químicos con mayor abundancia fueron: Fe (10,96%w en promedio en las 6 capas analizadas, con una desviación estándar (DE) igual a 0.74%w) y Al (4.1 l%w en promedio en las 6 capas analizadas, DE = 1.15%w), siendo estos elementos más abundantes en las capas exteriores. Los elementos químicos con menor concentración son Ti (3921 ppm en promedio en las 6 capas analizadas, DE = 444.78ppm) y Ca (943.5 ppm en promedio en las 6 capas analizadas, DE = 151.06ppm), la concentración de Ti es ligeramente mayor en las capas 1, 5 y 6; mientras que la concentración de Ca aumenta en las capas interiores (fig. 2a y 2b). Los elementos considerados traza son Mn > Zn > V > Sr > Ni > Cr.
En las muestras de polvo estudiadas por capas, los elementos químicos con mayor concentración fueron Ca, Fe, Al, y Zn, elementos esenciales para el buen funcionamiento de nuestro organismo. El núcleo de las capas internas (son la que tiene aplicaciones geofágicas por los pobladores de la comunidad de Chimpajilahuata) tiene mayor concentración de Ca que las otras capas, lo que sugiere que la geofagia del machurumi contiribuiría a la geofagia benéfica, al no encontrarse elementos químicos como el Pb, Cd y Se, (ausentes en el Machurumi). Investigaciones similares con tierras comestibles de Nigeria, desarrollada por Agene et al. y Momoh et al. [1,13], se reportó la presencia de Ca, Fe, y Zn, esenciales para el funcionamiento de nuestro cuerpo, pero a su vez se encontró elementos contaminantes como el Pb y Se, que son considerados elementos contaminantes que puede contribuir a deteriorar la salud. Del mismo modo [9], reportes sobre arcillas africanas con función geofágica generados en la Universidad de California, mencionan la presencia de elementos Fe, Ca y Zn los cuales contribuyen a funciones nutricionales. El Al en nuestro organismo es el responsable de bajar el nivel de la acidez estomacal, el Mn es un elemento es un mineral traza esencial para todos los seres vivos conocidos, pero en cantidades mayores puede causar un síndrome de intoxicación en los mamíferos, con daños neurológicos que a veces son irreversibles [10]. Un estudio relacionado con los suplementos mineralógicos como una función geofágica en arcillas africanas menciona elementos como Al, Mn y Ti en baja concentración como en el presente estudio, a diferencia de las arcillas africanas el Machu rumi no contiene elementos químicos contaminantes como el Pb, As, Cu [9].
En el análisis de las fases cristalinas se encontró que el Cuarzo y el Clinochlore son minerales que están presentes en las 6 capas internas del Machu rumi (tabla 2), estos minerales también fueron reportados por Browman [3] y Quispe et al. [15], siendo el cuarzo una fase cristalina muy común en arcillas comestibles y se le atribuye la limpieza intestinal. Por lo que hace sugerir que el Machu rumi contribuye a la limpieza estomacal de los consumidores. La presencia de Goethita es común en las capas 2, 3, 5 y 6; este mineral de arcilla es considerado un reductor muy eficaz, y puede remover tanto arsénico inorgánico como orgánico [14]. Estudios mineralógicos muestran que la goethita es una absorbente para el arsénico de naturaleza orgánica e inorgánica [12]. Por lo tanto, la goethita presente en el Machu rumi podría ser un componente que ayuda a remover arsénico del organismo que lo consuma. Cabe señalar que no hay presencia de este mineral en tierras comestibles similares que hayan sido estudiadas, lo que significa que es una tierra muy particular. Además, en nuestro estudio se reporta la presencia de la aleación de Hierro Cobalto solamente en la capa 1 que es la más externa (Los pobladores de Chimpajilahuata manifiestan que consumen la capa central con fines medicinales), siendo un mineral característico del Machu rumi.
La Chamosita, Clinochlore son minerales del grupo de los silicatos con estructuras laminares (fig. 3a y 3b), subgrupo filosilicatos y dentro de éstos pertenece a los clorhidratos; es un alumino - silicato de magnesio, hierro y aluminio, con otros posibles elementos [5,6,15]. En el estudio referido a la caracterización del ch'aqo se reporta minerales de arcilla que se encuentran dentro del grupo de los silicatos y se le atribuye a estos minerales de arcilla de proporcionar Al, Fe, Mn al organismo mediante intercambio catiónico [15].
CONCLUSIONES
Los elementos químicos con mayor abundancia son: Fe (10,96%w en promedio, DE = 0.74%w) y Al (4.ll%w en promedio, DE = 1.15%w), siendo estos elementos más abundantes en las capas exteriores. Los elementos químicos con menor concentración son Ti (3921 ppm DE = 444.78 ppm) y Ca (943.5 ppm en promedio, DE = 151.06 ppm), la concentración de Ti, es ligeramente mayor en las capas 1, 5 y 6; mientras que la concentración de Ca aumenta en las capas interiores. Los elementos considerados traza son Mn > Zn > V > Sr > Ni > Cr. Ca, Fe, Al, y Zn, elementos esenciales para el buen funcionamiento de nuestro organismo.
Los elementos químicos con mayor concentración son Ca, Fe, Al, y Zn, elementos esenciales para el buen funcionamiento de nuestro organismo. La capa más interna, es la que tiene aplicaciones geofágicas por los pobladores de la comunidad de Chimpajilahuata, evidencia mayor concentración de Ca que las otras capas, por lo que sugiere que la geofágia del machurumi contiribuiría a la geofágia benéfica.
En el análisis de fases cristalinas se encontró que el Cuarzo y el Clinochlore son minerales que están presentes en las 6 capas internas del Machu rumi, estos minerales también fueron reportados por Browman [3] y Quispe et al. [15], siendo el cuarzo una fase cristalina muy común en arcillas comestibles y se le atribuye la limpieza intestinal [7]. Lo que sugiere que el Machu rumi contribuye a la limpieza estomacal de los consumidores.
Se detectó la presencia de Goethita en las capas 2, 3, 5 y 6; este mineral de arcilla es considerado un reductor muy eficaz. Estudios mineralógicos muestran que la goethita es una absorbente para el arsénico de naturaleza orgánica e inorgánica [12]. Por lo tanto, la goethita presente en el Machu rumi podría ser un componente que ayude a remover arsénico del organismo. Cabe señalar que no hay presencia de este mineral en tierras comestibles similares que hayan sido estudiadas en diversas partes del mundo, lo que significa que es una tierra muy particular.
RECONOCIMIENTOS
Los autores agradecen el apoyo del Instituto de Física de la UNAM, el Instituto Peruano de Energía Nuclear (IPEN), y el apoyo del CONCYTEC que hizo posible la realización de una estancia científica, a través de la movilización nacional e internacional, IV convocatoria.
NOTA
1 Instituto de Investigaciones de la Universidad Nacional de Altiplano de Puno Av. Sesquicentenario s/n, Ciudad Universitaria, teléfono 051 367516, Puno, Perú, heberchui@gmail.com
2 Instituto de Física, Universidad Autónoma de México, Circuito de la Investigación Científica, Ciudad Universitaria, CP 04510, Teléfono: +52(55)56-65-72-63, Ciudad de México, México
3 Centro Nuclear RACSO, Instituto Peruano de Energía Nuclear, Av. Canadá 1470 Teléfono: 226-0030, San Borja Lima Perú
REFERENCIAS Y BIBLIOGRAFÍA ADICIONAL*
1. Agene J., Lar A., Mohammed O., Gajere N., Dang B., Jeb N., Ogunmola K. 2014, American Journal of Human Ecology. 3, 1-9. [ Links ]
2. Al-Rmalli S., Jenkins R., Watts M, Haris P. 2010, Environmental Health. 9, 1-8. [ Links ]
3. Browman D. 2004, Estudios Atácamenos. 28, 133-141. [ Links ]
4. Bunnell J., Finkelman R., Centeno J., Selinus O. 2007, Geological Acta: an international earth science journal. 5(3), 273- 281. [ Links ]
5. Dominy N., Davoust E., Minekus M. 2003, The Journal of Experimental Biology. 207, 319-324. [ Links ]
6. Gallaga Y, Determinación y análisis de fórmulas estructurales de esmectitas del estado de Guanajuato, Ed. Guanajuato, 2002, Guanajuato, México, pp 45-53. [ Links ]*
7. Hrachová J. 2006, Materials Letters. 61, 3361-3365. [ Links ]
8. Jiménez L. 2006, Pensar Iberoamérica. 10, 121-134. [ Links ]
9. Johns J., Duquette M, 1991, American Society for Clinical Nutrition. 53, 448-456. [ Links ]
10. Kawai K., Saathoff E., Antelman G, Msamanga G, Fawzi W. 2009, The American Society of Tropical Medicine and Hygiene. 80(1), 36-43. [ Links ]
11. Kroeber L, Collier D. The archaeology and pottery of Nazca, Edición, 1ra edición, 1998, Lima Perú, pp. 259-282 [ Links ]
12. Mcrae, C. Evaluation of reactive materials for in situ treatment of arsenic III, arsenic V and Selenium VI using permeable reactive barriers: laboratory study, 1ra edición, 1999, Waterloo, Canadá, pp 65-74. [ Links ]
13. Momoh A, Davies T., Akinsola H., Iweriabor B., Mashao M. 2012, International Journal of Current Research. 4, 129-134. [ Links ]
14. Nikolaidis P., Dobbs G., Lackovic J. 2003, Water Research. 37, 1417-1425. [ Links ]
15. Quispe J., Medina J., Aranibar J. 2007, Acta Microscópica. 16(2), 226-228. [ Links ]
16. Shinondo C, Mwikuma G 2010, Medical Journal of Zambia. 35(2), 48-52*. [ Links ]
17. Weiss P. 1943, Perú indígena. 5(12), 12-21. [ Links ]
* Sin llamada en el texto