Revista Boliviana de Química
versión On-line ISSN 0250-5460
Rev. Bol. Quim vol.33 no.5 La Paz dic. 2016
ARTÍCULOS ORIGINALES
Encapsulation, characterization and thermal stability of anthocyanins from Zea Mays L. (Purple Corn)
Evelyn V. Mendoza Sillerico1,2, Cecilia K. Curi Borda2, Virginia J. Rojas Mercado1, Juan A. Alvarado Kirigin2,*
*Corresponding author: jaalvkir@gmail.com
Abstract
The optimal conditions for encapsulation of anthocyanin extract from Zea mayzs L. (purple corn) by using, a mixed design, was investigated. This study determined the best mixture ratio of Maltodextrin and Arabic gum as encapsulant agents and the effect of the inlet temperature on the response variables: yield, moisture and total anthocyanins concentration. The physico-chemical and morphological characterization of the obtained encapsulates was performed. The heat effect at temperatures of 45°, 60° and 75°C on the concentration of total anthocyanins was also evaluated as well as the color variation of the encapsulates at room temperature in a two-month-period.
Keywords: Zea mays L., Maíz morado, Antocianinas, Encapsulación, Secado por aspersión.
Resumen
Spanish title: Encapsulación, caracterización y estabilidad térmica de antocianinas de Zea mays L (maíz morado). En el presente trabajo se investigaron las condiciones óptimas para la encapsulación del extracto de antocianinas del marlo de Zea mayz L. (maíz morado) mediante un diseño mixto, determinándose las mejores proporciones de maltodextrina y goma arábiga en la mezcla encapsulante y el efecto de la temperatura de entrada sobre las variables respuesta: rendimiento, humedad y antocianinas totales. A partir de los encapsulados obtenidos, se realizó su caracterización fisicoquímica y morfológica. Finalmente, se evaluó el efecto de la temperatura en la concentración de antocianinas totales en condiciones extremas de almacenamiento, a tres diferentes temperaturas: 45°, 60° y 75 °C y la variación de color a temperatura ambiente en un periodo de dos meses.
INTRODUCCIÓN
Actualmente se presta un gran interés al uso y consumo de los colorantes naturales en la industria alimentaria, cosmética y farmacéutica reemplazando a los colorantes sintéticos debido a su naturaleza química, inocuidad y funcionalidad. El maíz morado es una variedad pigmentada del Zea mays L. cultivada en Bolivia, cuyos granos y marlo presentan coloración morada. Los compuestos mayoritarios responsables de dicho color fueron identificados como: pelargonidina 3-O-![]() -D-glucósido, peonidina 3-O-
-D-glucósido, peonidina 3-O-![]() -D-glucósido y cianidina 3-3-O-
-D-glucósido y cianidina 3-3-O-![]() -D-6-malonilglucósido. [1]
-D-6-malonilglucósido. [1]
La estabilidad de las antocianinas depende de la combinación del medio ambiente y factores químicos. Los factores que afectan la estabilidad son: la temperatura, pH, luz, oxígeno, enzimas, la presencia de copigmentos, iones metálicos, ácido ascórbico, dióxido de sulfuro y azúcares [2].
Para prolongar la estabilidad de las antocianinas se puede utilizar la técnica de encapsulación mediante secado por aspersión (spray drying), que es uno de los procesos más antiguos y más utilizados para encapsular agentes activos. Es un método de bajo costo y su eficiencia de operación es comparablemente mayor que la de otros tipos de secadores [3] para producir un producto seco y estable. Investigaciones de la encapsulación de antocianinas mediante secado por aspersión muestran que la utilización de maltodextrina conjuntamente con goma arábiga [4] produce encapsulados con un rendimiento de 14, 9 % y con una pérdida de 1.5 % de antocianinas.
EXPERIMENTAL
Las muestras de marlos de maíz morado utilizadas en la investigación fueron recolectadas del Municipio de Sorata de las comunidades de Chajlaya, Cuñapata, Tahana, San Isidro, Quehuaya y Villa "Siempre Unidos" del departamento de La Paz, Bolivia; éstas fueron identificadas mediante comparación con especímenes voucher que se hallan depositados en el Herbario Nacional de Bolivia (LPB) al momento de esta investigación.
Extracción y cuantiñcación de antocianinas
La materia prima fue pulverizada a un tamaño de partícula de 2 mm utilizando un cernidor con tamaño de poro de 20 Mesh. La extracción se realizó con una mezcla de etanol al 60% acidificado con 0,5% de HC1 en una relación soluto - solvente de 1:10 [4], a una temperatura de 50 °C [5] y un tiempo de extracción de 3 hr [7]. El número óptimo de extracciones para lograr la máxima eficiencia fue de 2 con una agitación de velocidad media. El extracto obtenido se filtró y se concentró a una temperatura de 40°C. Se determinó el contenido de antocianinas totales expresado como cianidina-3-glucósido mediante el método de pH diferencial de acuerdo a Giusti & Wrolstad [8] utilizando un espectrofotómetro UV-VIS.
Encapsulación mediante secado por aspersión
El extracto fue mezclado con el agente encapsulante (maltodextrina y goma arábiga) en una relación 1:1, agitándose a una velocidad constante durante 20 minutos. La mezcla fue secada mediante el Spray dryer YC- 015, el mismo que funciona según el principio de flujo co-corriente y utiliza para la atomización una boquilla a presión de dos fluidos. La temperatura de entrada fue de 120 a 130 °C con flujo constante de alimentación de 7 mL/min. El polvo fue recolectado en frascos al abrigo de la luz y almacenado en un desecador para su posterior análisis. A partir de los resultados se realizó un análisis de varianza (ANOVA) mediante el software Design Expert v.7.0, considerando valores dep ![]() 0,05 significativos. El análisis mixto usado contempló el factor de análisis de temperatura de entrada y componentes de mezcla, donde las variables de respuesta fueron: rendimiento, humedad y concentración de antocianinas totales.
0,05 significativos. El análisis mixto usado contempló el factor de análisis de temperatura de entrada y componentes de mezcla, donde las variables de respuesta fueron: rendimiento, humedad y concentración de antocianinas totales.
Caracterización de los encapsulados
Se determinó el porcentaje de humedad mediante la balanza de humedad Moisture Analyzer MAC modelo 110/ WH utilizándose 0,5 g de muestra. La actividad de agua se determinó mediante el equipo Rotronic Hygropalm modelo HP22-A2. Se realizó un análisis colorimétrico mediante colorímetro CHROMA METER CR-400 midiendo los valores de luminosidad (L*, negro-blanco), croma (a*, verde-, rojo+) y tono (b*, azul-, amarillo+). Los valores de L*, a* y b* se usaron para calcular: la cromaticidad (C), índice de oscurecimiento (IO), ángulo hue (h°) y la perdida de color resultante del proceso de secado, utilizando las siguientes fórmulas:
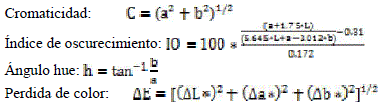
Donde ![]() E es la diferencia de color en general;
E es la diferencia de color en general; ![]() L es la variación de L* de coordenadas;
L es la variación de L* de coordenadas; ![]() a es la variación de la coordenada a*;
a es la variación de la coordenada a*; ![]() b es la variación de la coordenada b*.
b es la variación de la coordenada b*.
Se realizó un análisis morfológico con el mejor tratamiento del diseño experimental mediante un microscopio óptico marca OPTIKA B-350 italy también con un microscopio electrónico de barrido JEOL JSM-T108.
Estabilidad térmica
Se realizaron ensayos de estabilidad térmica de las antocianinas encapsuladas en condiciones extremas de almacenamiento a 45°, 60° y 75 °C. Se llenaron tubos a cabalidad con las muestras, que posteriormente, fueron calentadas en un digestor por un tiempo total de 6 hr. La variación de la concentración de antocianinas fue medida a través del método de pH-diferencial cada media hora, utilizando un espectrofotómetro UV-VIS. Además, se evaluó la vida de anaquel al abrigo de la luz a temperatura ambiente (20°C) por un periodo de 60 días, registrándose los cambios de color cada 4 días mediante el colorímetro CHROMA METER CR-400.
RESULTADOS Y DISCUSIÓN
Caracterización de los encapsulados de antocianinas
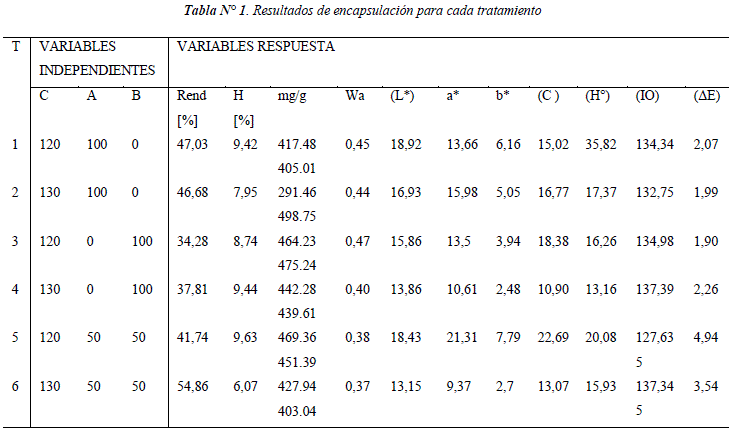
La tabla N° 1 muestra los resultados obtenidos en cada uno de los tratamientos de las 8 combinaciones y 2 réplicas, donde A es la concentración de maltodextrina, B es la concentración de goma arábiga y C es la temperatura de entrada. Así mismo se presenta la caracterización fisicoquímica de todos los polvos encapsulados obtenidos y los resultados de las mediciones colorimétricas.
El análisis de varianza (ANOVA) muestra la existencia de diferencias significativas p![]() 0,0001 en el modelo experimental planteado para cada una de las variables de respuesta y sus coeficientes de correlación: Rendimiento = + 46.26A + 36.04 B + 28.61 AB (R2= 0.9381); Humedad = + 8.71 A + 9.08 B - 4.17 AB - 0.76 AC (R2= 0.9320); Antocianinas Totales = + 453.21A + 455.34B - 65.36 AB + 41.89 AC - 14.40 BC (R2= 0.9489). Los valores de R-Squared obtenidos por el programa para cada variable respuesta indican que los modelos de regresión funcionan correctamente.
0,0001 en el modelo experimental planteado para cada una de las variables de respuesta y sus coeficientes de correlación: Rendimiento = + 46.26A + 36.04 B + 28.61 AB (R2= 0.9381); Humedad = + 8.71 A + 9.08 B - 4.17 AB - 0.76 AC (R2= 0.9320); Antocianinas Totales = + 453.21A + 455.34B - 65.36 AB + 41.89 AC - 14.40 BC (R2= 0.9489). Los valores de R-Squared obtenidos por el programa para cada variable respuesta indican que los modelos de regresión funcionan correctamente.
De acuerdo al esquema de color CIELAB, los datos obtenidos en la Tabla N° 1 se localizan en el primer cuadrante, donde los valores de ángulo hue (h°) están entre 13,45 a 35,98, indicando un color rojo- púrpura y con un índice de oscurecimiento (IO) de 126,75 a 138,04 que muestran una alta intensidad de color. Los valores de cromaticidad de 9,2 a 22,75 indican un color brillante asociado a una luminosidad (L) de 12,48 a 19,45. El ![]() E entre 1,16 a 5,25 indica la estabilidad de color en el polvo encapsulado comparado con el color del extracto original de antocianinas.
E entre 1,16 a 5,25 indica la estabilidad de color en el polvo encapsulado comparado con el color del extracto original de antocianinas.
Las partículas poseen morfologías no homogéneas, de múltiples tamaños que oscilan entre 1-15 ![]() como se muestra en la Figura N° 1.
como se muestra en la Figura N° 1.
En la Figura N° 2, se aprecia las diferentes partículas que presentan formas esféricas y esferas irregulares con concavidades.
Estabilidad térmica Evaluación colorimétrica
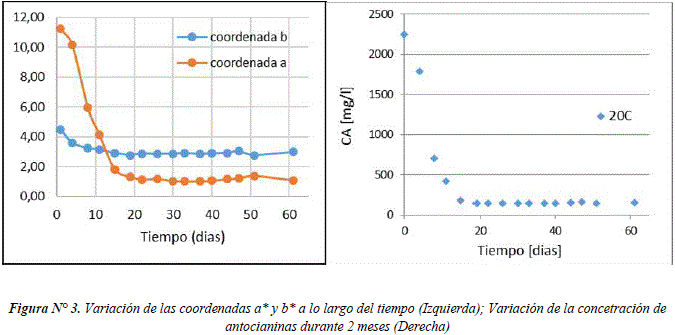
En la Figura N°3 se observan a la izquierda los valores de las coordenadas a* y b* obtenidos a partir de las mediciones de la permanencia del color realizadas por triplicado durante los dos meses. A la derecha, se obseva la variación de la concentración de antocianinas a lo largo del tiempo obtenida a partir del producto de la concentración inicial de antocianinas y el porcentaje de permanencia de la cromaticidad calculada para cada punto a partir de los valores de a* y b* con respeco a la cromaticidad inicial.
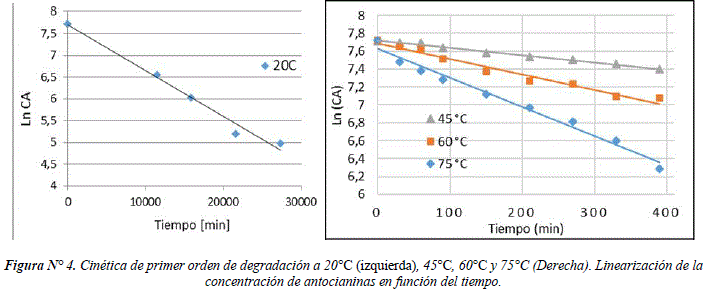
Por otro lado, se obtuvieron las curvas de degradación de las antocianinas encapsuladas a 45°, 60° y 75°C durante 6 horas. A partir de estos datos, se determinó que la cinética de degradación de las antocianinas es de primer orden mediante su respectiva linearización como se muestra en la Figura N° 4.
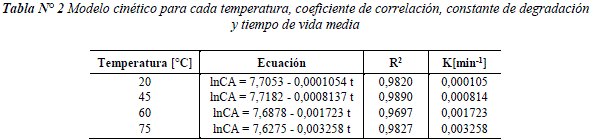
La ecuación que describe esta cinética de primer orden para cada temperatura está dada por: lnCt - lnco = -kt, donde: ct - es la concentración de antocianinas a un tiempo de reacción t, co - es la concentración inicial de antocianinas y k - es la constante de degradación. Dichas constantes, así como el tiempo de vida media calculado para cada temperatura se determinan con base en la ecuación ![]() y se presentan en la Tabla 2.
y se presentan en la Tabla 2.
Modelo de la ecuación de Arrhenius
Las constantes de degradación (k) para cada temperatura se ajustaron al modelo de Arrhenius (Figura N° 5), obteniéndose la Ecuación:
![]()
donde E es la energía de activación (cal/mol), R es la constante universal de los gases (1,987 cal/mol K) y T es la temperatura absoluta en K.
![]()
La energía de activación para la degradación del encapsulado es igual a 53,3 KJ/mol y el tiempo de vida media calculado a partir del ajuste a la ecuación de Arrhenius y la ecuación ![]() es igual a 4,1 días a 20°C, 17,5 horas a 45°C, 7,0 horas a 60°C y 3,1 horas a 75°C.
es igual a 4,1 días a 20°C, 17,5 horas a 45°C, 7,0 horas a 60°C y 3,1 horas a 75°C.
CONCLUSIONES
Mediante el proceso de extracción se determinó el contenido de antocianinas totales en la harina de marlo de maíz morado. El proceso de extracción mostró que después de una segunda extracción se obtuvo una concentración de antocianinas de 104 mg antocianinas totales/g de harina de marlo y el rendimiento de extracción acumulado (eficiencia de extracción) fue de 87,9 %. Esto muestra que sólo son necesarias dos extracciones para obtener la mayor cantidad de antocianinas del marlo. Gracias a que el colorante es obtenido de la harina de marlo de maíz morado, se puede lograr un buen aprovechamiento de los desechos de la materia prima utilizada para obtener otros productos como el api.
A través del diseño mixto se determinó que las condiciones más adecuadas para el secado por aspersión incluyen una temperatura de entrada de 130 °C y una mezcla de encapsulante con 50 % de maltodextrina y 50 % de goma arábiga. El rendimiento obtenido de 54.87 % de antocianinas encapsuladas es 4 veces mayor al rendimiento reportado de 14.9 % por Villacrez Y. [4]. La concentración final promedio de antocianinas en el tratamiento 6 es de 415,49 mg/ g de encapsulado. Este valor representa una pérdida del 16,90 % de antocianinas con respecto a la concentración inicial del 50% de antocianinas contenida en los sólidos totales antes del proceso de encapsulado.
Se puede apreciar que los encapsulados obtenidos son microbiológicamente estables debido a su bajo contenido de humedad 6,25 % y actividad de agua de 0,353. La excelente colorimetría obtenida en el polvo se pudo verificar a través de su cromaticidad (C) 16,944 y ángulo hue (h°) 18,41.
En función a los resultados obtenidos de la ecuación de Arrhenius, la energía de activación para la degradación del encapsulado es igual a 53,3 KJ/mol y las antocianinas se degradan rápidamente por encima de 45°C. Por otro lado, a 20°C, después del 80% de degradación de las antocianinas, el color del encapsulado ha cumplido su tiempo de vida útil dando como resultado un color no característico (coordenadas L=6,00, a*=4,14 y b*=3,14). Este porcentaje de degradación equivale a 9 días a 20°C, sin embargo, este periodo puede ser extendido hasta 33 días a 4°C lo que implica que el colorante puede ser utilizado en productos refrigerados como jugos y helados manteniendo una coloración apropiada.
RECONOCIMIENTOS
The authors gratefully acknowledge the financial support of the Sweedish International Development Cooperation Agency (SIDA) during the development of this research work.
NOTA
1 Department of Chemical Engineering, Research and Development Institute of Chemical Processes IIDEPROQ, Universidad Mayor de San Andrés UMSA, Calle Andrés Bello s/n, Ciudad Universitaria Cota Cota, Phone 59122774412, La Paz, Bolivia
2 Department of Chemistry, Research Institute of Chemical Sciences IIQ, Universidad Mayor de San Andrés UMSA, P.O. Box 303, Calle Andrés Bello s/n, Ciudad Universitaria Cota Cota, Phone 59122792238, La Paz, Bolivia
REFERENCIAS
1. Cuevas, E., Antezana, A. Y Winterhalter, P, 2008. Análisis y Caracterización de Antocianinas en diferentes variedades de Maíz Boliviano(Zea mays). Cochabamba, Bolivia. Universidad Mayor San Simón de Cochabamba, pp. 7. [ Links ]
2. Hutchings, B. Food Color and Appearance, Blackie Academic & Professional, 1994, New York, pp. 132. [ Links ]
3. Masters, K. Spray Drying in Practice. Charlottenlund, Denmark: Spray Dry Consult International Aps., 2002. [ Links ]
4. Villacrez Yepez, J.L. 2013, Desarrollo de microencapsulados por Spray Drying a partir de frutos de Mora de Castilla (Ruhus glaucus Benth). Bogotá, Colombia : Universidad Nacional de Colombia, Facultad de Ciencias, Departamento de Química, [ Links ].
5. Fernandez, J. Determinación de antocianinas en el maíz morado, Perú: s.n., 2005. [ Links ].
6. Acevedo Castillo, A.R. 2003, Efecto de la temperatura y un copigmento en la estabilidad de antocianinas de la col morada en una bebida. Cholula, Puebla, México: Universidad de las Américas Puebla, Departamento de Ingeniería Química y Alimentos, [ Links ].
7. Camaño, H., Arrazola, G. Obtención y estabilización de antocianinas de berenjena (Solanum melongena L.) mediante microencapsulación y su evaluación como compuesto funcional.. Córdoba: s.n., 2013 [ Links ]
8. Giusti, M., Wrolstad, R.E. Caracterización y medición de antocianinas por espectroscopia UV-Visible.. Oregon, 2000. [ Links ]












 uBio
uBio