Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista Boliviana de Química
On-line version ISSN 0250-5460
Rev. Bol. Quim vol.31 no.2 La Paz Dec. 2014
ARTICULO ORIGINAL
ELECTROCHEMICAL BEHAVIOR OF LiFePO4 / C IN FUNCTION OF PARTICLE SIZE, SYNTHESIZED BY THE HYDROTHERMAL ROUTE![]()
Max Vargas1, Diego J. Cuscueta2, Jaime Villca1, Waldo Yapu1, Mario Blanco3, Cesario Ajpi1, Fabián Benavente1, Saúl Cabrera1,*
*Corresponding author: saulcabreram@hotmail.com
1Department of Chemistry, Instituto de Investigaciones Químicas IIQ, Laboratorio de Ciencia de Materiales, Universidad Mayor de San Andrés UMSA, P.O. Box 303, Tel. 59122795878, La Paz, Bolivia
2 Instituto Balseiro-UNCu, Centro Atómico Bariloche-CNEA, CONICET. Av. Bustillo 9500 - 8400, Bariloche, Río Negro, Argentina
3Department of Geology, Instituto de Investigaciones Geológicas y del Medio Ambiente IIGMA, Laboratorio de Caracterización Estructural de Minerales, Universidad Mayor de San Andrés UMSA, Campus Universitario, Calle Andrés Bello s/n, Cota-Cota, Tel. 59122793392, La Paz, Bolivia
ABSTRACT
LiFePO4 material was prepared by hydrothermal method at a temperature of 170°C, using Li2CO3, LiAc, LiOH as precursors for lithium, and FeSO45H2O and H3PO4 as precursors for Fe and P, the solution pH was set according to the lithium precursor used. The structural characterization was carried by XRD, SEM, TEM technics. A single crystalline phase was identified and a particle size ranged between 20 and 0.5um was observed for the different lithium precursors. The electrochemical characterization shows a discharge capacity of 130 mAh/g for the LiOH lithium precursor synthetized material. ![]() Original Spanish title:Comportamiento electroquímico de LiFePO4/C en función del tamaño de partícula, sintetizado por la ruta hidrotermal
Original Spanish title:Comportamiento electroquímico de LiFePO4/C en función del tamaño de partícula, sintetizado por la ruta hidrotermal
Keywords: Cathode, Solid-Solid Reaction, pyrolytic, atrane, Synthesis of Materials.
RESUMEN
Se preparó LiFePO4/C por la ruta Hidrotermal a una temperatura de 170 °C, utilizando Li2CO3, LiAc, LiOH, como precursores de litio y FeSO45H2O y H3PO4como precursores de Fe y P, se adecuo el pH de la solución según el precursor de litio. La caracterización estructural se llevó a cabo mediante las técnicas de difracción de rayos X, microscopía electrónica de barrido y transmisión, identificando una sola fase cristalina y tamaños de partícula entre 20 hasta 0.5um para los distintos precursores utilizados. La caracterización electroquímica mostró una capacidad de descarga de 130 mAh/g para el electrodo sintetizado utilizando LiOH como precursor de Litio.
INTRODUCCION
Con el desarrollo de nuevos dispositivos electrónicos, la sociedad se ha vuelto cada vez mas dependiente de la energía eléctrica y con el consecuente uso de dispositivos portátiles viene la necesidad de energía portátil [1]. La aplicación de las baterías incluye su uso en teléfonos móviles, ordenadores portátiles o reproductores de MP3 y otros, a futuro cercano su aplicación en EV, y HEV. [2].
El fosfato de hierro litio (LiFePO4) es un material cátodo altamente utilizado para baterías Ion Litio, de la misma manera en Bolivia, se pretende utilizarlos para el desarrollo de baterías, bajo el Plan de Industrialización de los Recursos Evaporíticos del salar de Uyuni, es así que un estudio profundo de sus propiedades estructurales y electroquímicas son relevante, tanto para el campo académico como industrial [3].
El fosfato de hierro Litio (LFP) es un material de tipo olivino con la estructura triphylite, el primer reporte de caracterización electroquímica de este material fue desarrollado por Padhi et. al en 1997 [4], en la cual se describe la extracción e inserción electroquímica de litio en la red cristalina, logrando una capacidad de 100 a 110 mAh/g, menor al valor teórico de 170 mAh/g, muchos estudios se han realizado para incrementar la capacidad del material y mejorar la difusión de ion litio en la estructura del electrodo, centrada a su capacidad de inserción y desinserción molar de los iones Li, según la ecuación:
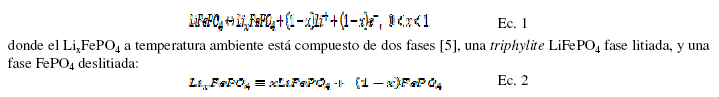
El LiFePO4 vs Li/Li+ presenta un potencial de equilibrio de 3,4 V [6], pese a que es ligeramente inferior al de LiCoO2 donde continua representando una alternativa altamente potencial para su comercialización. [7, 8]. Las ventajas de LiFePO4 como material catódico son principalmente su baja toxicidad y económicamente atractivo [9,10, 11]. Este material catódico puede ser sintetizado por varios métodos como sol-gel, hidrotermal, spray pirolisis, reacción en estado sólido, entre los más utilizados [9-14].
En este trabajo se realizó la síntesis de LiFePO4/C utilizando diferentes precursores de partida como fuentes de litio para el control de tamaño de partícula.
RESULTADOS, DISCUSION
Caracterización estructural, DRX, SEM, TEM
En la figura N° 1 se presenta los difractogramas de rayos X de las muestras de LiFePO4, /C sintetizadas por la ruta hidrotermal (Anexo I), los picos característicos coinciden con el patrón (N° 96- 210-0917 de la base de datos libre COD), el cambio de precursor no muestra señales adicionales en los espectros, por lo que los productos obtenidos presentan una buena similitud estructural.
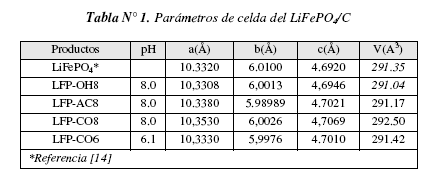
En la tabla N°1 se muestran los parámetros de las celdas, obtenidos por refinamiento de los espectros de difracción, se identifica que todos los productos presentan similar parámetros de celda, incluso el sintetizado a pH = 6.0, donde se tiene la presencia adicional de HPO42-, en función a sus constantes de estabilidad.
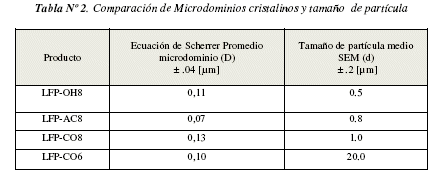
En las microimágenes de barrido (Figura N° 2) se observar la forma y tamaño de las partículas obtenidas, el tamaño promedio de las partículas, calculadas de una veintena de imágenes, muestra que existe un incremento desde 0.5 hasta 1 ¡am, conforme cambia el tipo de precursor de partida de la fuente de Li utilizado, para las síntesis hidrotermales a pH 8. Así mismo, la disminución del pH de síntesis a 6, produce un cambio brusco en el tamaño pasando del orden de 1 a 20 ¡am (Tabla N° 2). Con el incremento de tamaño se identifica con mayor claridad el hábito cristalino, identificándose claramente planos muy bien definidos.
En esta tabla N° 2 puede observarse, como el tamaño de partícula va incrementando a medida que cambia el tipo de precursor de litio, a las síntesis realizadas a pH de 8, esta cambio en el tamaño, permite proponer que el proceso de crecimiento de las partículas es dependiente del isopotencial superficial de las partículas, que son dependientes de la presencia de diferentes contra iones aniónicos, los cuales regulan en el tamaño de las mismas. Sin embargo, para el caso del precursor de Li2CO3 a pH de 6.01 se muestra un gran incremento del tamaño debido a que existen las especies biácidas de fosfato, que podrían favorecer la existencia de puentes de hidrogeno intermedios en el proceso de síntesis.
Las imágenes TEM de la figura N° 3 permiten apreciar, en a) el recubrimiento de una partícula cristalina de LiFePO4 con carbono, el cual se encuentra en estado amorfo, con un espesor de recubrimiento de aproximadamente de 5nm, y en b) el diámetro promedio de las partículas de LiFePO4 aproximadamente 500 nm, para el producto sintetizado con precursor de LiOH, detallando la morfología y la disposición de las partículas luego de la síntesis.
Proceso carga-descarga del LFP/C
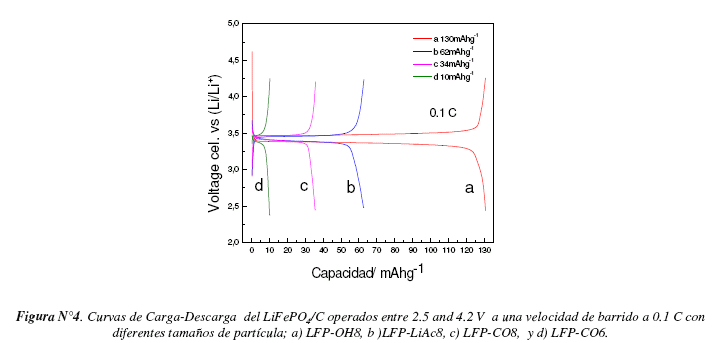
En la figura N° 4 se muestran las curvas de carga-descarga de los materiales catódicos de LiFePO4/C obtenidos a partir de los diversos tipos de precursores. Las capacidades de descarga fueron obtenidas a una velocidad de 0.1 C, donde se observa una capacidad de carga de 130, 62, 34 y 10 mAh/g a partir de los productos obtenidos por los precursores de LiOH, LiAc, Li2CO3 respectivamente, utilizando como potenciales de corte vs Li/Li+ 2.5 y 4.2 V.
El tamaño de partícula y morfología son fundamentales en las propiedades electroquímicas, donde se observa que cuando se tiene un tamaño de partícula de 20|im, la capacidad es baja debido a que los iones litio tienen que difundirse dentro de las partículas distancias muy grandes [14], a su vez esto también se ve influenciado con la morfología, ya que la dirección del proceso de migración del ion litio no es favorecida, porque se ve un crecimiento en las direcciones de los planos (200) y (020) generándose una inadecuada orientación de difusión.
Para el caso de la muestra preparada a partir de LiOH, se obtiene la mayor capacidad de descarga (130mAh/g) en consistencia con el menor tamaño de partícula, siendo la distancia de difusión de los iones Li en el seno del material menores, adicionalmente se identifica un crecimiento cristalino preferencial en el plano (020), dando a una morfología adecuada, que favorece la difuuion del litio.
La tasa de retención del material de la capacidad inicial a 0.1C fue del 81.3% a partir del precursor de LiOH, dando como resultado una buena aproximación en el comportamiento electroquímico.
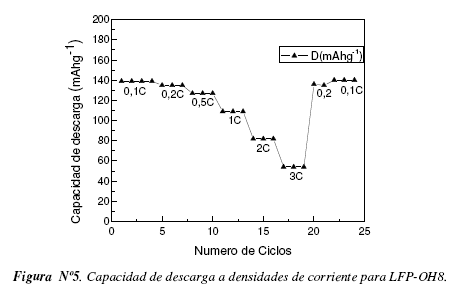
La Figura N° 5, muestra la disminución de la capacidad a distintas densidades de corriente desde 0.1 a 3C, para el material obtenido con precursor de hidróxido de litio. Este material presenta un comportamiento relativamente estable a velocidades de descarga bajas desde 0.1 a 0.5C. Por otra parte a velocidades de descarga mayores de 1 a 3C, se observa una disminución de la capacidad más acentuada. Posteriormente se realizó la descarga a velocidades bajas entre 0.2 a 0.1C, encontrando una buena reversibilidad de la capacidad.
CONCLUSIONES
Se sintetizó en forma exitosa el material LiFePO4 por el método hidrotermal a partir de diferentes precursores de Litio y variación de pH, realizándose su recubrimiento con carbono. Estos parámetros de síntesis son determinantes
en el tamaño y morfología de las partículas finales obtenidas, donde se favorece diferentes planos de crecimientos cristalinos de la fase tipo LiFePO4. Estos parámetros determinan la capacidad de carga en el material catódico, donde a menor tamaño y una orientación de crecimiento en el plano adecuado favorecen una alta capacidades de carga, principalmente por el menor recorrido en los procesos de difusión de los iones litio en el seno de las partículas. El producto obtenido a partir de LiOH a pH 8, presentan una morfología tipo ovoide, con un tamaño promedio de 500 nm con una alta capacidad de descarga electroquímica de 130 mAh/g a 0.1C, así como una muy buena reversibilidad carga/descarga.
SECCION EXPERIMENTAL
Síntesis del LiFePO4
El material LiFePO4 fue preparado mediante el proceso hidrotermal que consistente en una mezcla de hierro (II) a partir de FeSO4 7H2O (Sigma-Aldrich), fosfato a partir de H3PO4(85% en peso) y diferentes precursores de Litio, denominándose a los productos LFP-OH8 a partir de LiOH, LFP-AC8, a partir de LiAc, y LFP-CO8, a partir de Li2CO3 (99.9% Sigma-Aldrich),
Los precursores de partida fueron disueltos en agua destilada como primer paso y posteriormente se realizó una mezcla de las tres disoluciones, el pH de la solución fue ajustada a pH 8, el volumen de la mezcla fue de 120 ml y colocados en un vaso de teflón de alta densidad (volumen interno 125 ml) para luego llevarlos a un auto clave de acero inoxidable, por un t=18h, T= 170°C.
Adicionalmente, para la muestra preparada con Li2CO3-, se varió el pH de 8 a 6 obteniéndose el producto (LFP-CO6). Después de la filtración, las muestras fueron secadas a 60°C durante 4 h en vacío.
Recubrimiento con carbón
Las muestras obtenidas de LiFePO4 fueron recubiertos con carbono utilizando como precursor de carbono al almidón. El carbón recubierto fue del orden del 5% en peso en relación al LiFePO4. La mezcla de almidón y LiFePO4 fueron homogenizados con acetona, y secado a 50 °C por 30 min., la mezcla fue calcinada a 750 ° C durante 3 h en una atmósfera reductora al 10% H2/Ar con una velocidad de flujo 200 ml/min.
Caracterización cristalográfica y morfológica
Las muestras preparadas se caracterizaron por difracción de rayos X (DRX) mediante un difractómetro Panalitycal-Empyrean con radiación Cu-K y detector PIXcel3D. La caracterización morfolófica se realizó con un microscopio electrónico de barrido (SEM) FEI Nova Nano 230 y un microscopio electrónico de transmisión Phillips CM200UT operado a 200keV.
Medidas electroquímicas
La evaluación electroquímica se realizo en una celda de dos electrodos usando láminas de litio metálico como contra electrodo. El electrodo de trabajo fue preparado mediante la mezcla del material activo LiFePO4/C, Carbón Aditivo Super C65 y Polyvinylidene fluoride (PVDF) como aglutinante en N-methyl-2-pyrrolidone (NMP) en relación 8:1:1. La mezcla fue depositada en una lámina de Aluminio y cortada de forma circular de área 1 cm2 y secado a 80°C por 24h. El electrolito se preparo a una concentración de 1M de LiPF6 disuelto en una mezcla de carbonato de etileno (EC) y carbonato dimetilo (DMC) en una relación 1:1 v/v. Las celdas electroquímicas fueron ensambladas en atmosfera inerte de Ar, y las medidas electroquímicas fueron realizadas mediante proceso galvanostático de carga-descarga con un potencial de corte entre 2.4-4.2 V a 0.1 C (1C=170mA/g).
REFERENCIAS
1. Linden, D. & Reddy, T. B. (eds) Handbook of Batteries, 3rd edn (McGraw-Hill, 2002). [ Links ]
2. Poizot, P., Laruelle, S., Grugeon, S., Dupont, L. & Tarascon, J.-M. Nature 407, 496-499 (2000). [ Links ]
3. Cabrera S., Benavente F., Vargas M., Perspectivas en el Procesamiento de Materiales-Electrodos para Baterias Ion Litio en Bolivia, Revista Boliviana de Química, Vol. 29, N°l, 2012. [ Links ]
4. A. K. Padhi, K. S. Nanjundaswamy, and J. B. Goodenough, "Phospho-olivines as positive-electrode materials for rechargeable lithium batteries," J. Electrochem. Soc. 144 (1997) 1188-1194. [ Links ]
5. J. Graetz, C. C. Ahn, R. Yazami, and B. Fultz, "Highly reversible lithium storage in nanostructured silicon," Electrochem. Solid-State Lett. 6 (2003) A194-A197. [ Links ]
6. J. Graetz, C. C. Ahn, R. Yazami, and B. Fultz, "Nanocrystalline and thin film germanium electrodes with high lithium capacity and high rate capabilities," J.Electrochem. Soc. 151 (2004) A698-A702. [ Links ]
7. K. Mizushima, P. C. Jones, P. J. Wiseman, and J. B. Goodenough, "LixCoO2 (0 < x < 1) A New Cathode Material for Batteries of High-Energy Density," Mater. Res. Bull. 15 (1980) 783-789. [ Links ]
8. K. Amine, H. Yasuda, and M. Yamachi, "Olivine LiCoPO4 as 4.8V electrode material for lithium batteries," Electrochem. Solid-State Lett. 3 (2000) 178-179 [ Links ]
9. M. Koltypin, D. Aurbach, L. Nazar, and B. Ellis, "On the stability of LiFePO4 olivine cathodes under various conditions (electrolyte solutions, temperatures)," Electrochem. Solid-State Lett. 10 (2007) A40-A44 [ Links ]
10. K. Amine, J. Liu, and I. Belharouak, "High-temperature storage and cycling of C-LiFePO4/graphite Li-ion cells," Electrochem. Comm. 7 (2005) 669-673 [ Links ]
11. R. Yazami and P. H. Touzain, "A reversible graphite-lithium negative electrode for electrochemical generators," J. Power Sources 9 (1983) 365-371 [ Links ]
12. M. Holzapfel, H. Buqa, W. Scheifele, P. Novak, and F. M. Petrat, "A new type of nano-sized silicon/carbon composite electrode for reversible lithium insertion," Chem.Comm. (2005) 1566-1568 [ Links ]
13. A. S. Andersson, B. Kalska, L. Haggstrom, and J. O. Thomas, "Lithium extraction/insertion in LiFePO4: an x-ray diffraction and M'ossbauer spectroscopy study," Solid State Ionics 130 (2000) 41-52 [ Links ]
14. Rahul Malik, Damian Burch, Martin Bazant, and Gerbrand Ceder, "Parti cle Size Dependence of the Ionic Diffusivity", American Chemical Society 10, 4123-4127 [ Links ]