Revista Boliviana de Química
versión On-line ISSN 0250-5460
Rev. Bol. Quim v.28 n.2 La Paz 2011
ARTICULO ORIGINAL
EVALUACIÓN DE LA TOXICIDAD AGUDA A DOSIS FIJAS DEL EXTRACTO DE WERNERIA DACTYLOPHYLLA (PUPUSA)
Juan Antonio Ávila Illanes,1 Grace Ruiz Pinell,1 Claudia Tórrez Choque,1 Patricia Mollinedo Portugal,2 José Luis Vila Castro,2 Marco Bugiardini,2 Michel Sauvain,3 Eduardo Gonzáles,1 José A. Bravo2
1Instituto de Investigaciones Fármaco Bioquímicas (IIFB), Facultad de Ciencias, Farmacéuticas y Bioquímicas, Universidad Mayor de San Andrés. Av. Saavedra Nº 2224, Miraflores, La Paz, Bolivia.
2Instituto de Investigaciones en Productos Naturales (IIPN), Carrera de Ciencias Químicas, Universidad Mayor de San Andrés, Calle Andrés Bello y Calle 27 Cota Cota, Edificio FCPN, 2º piso, La Paz- Bolivia.
3Institut de Recherche pour le Développement, Avenida Honorio Delgado 430, Urb. Ingeniería San Martín de Porres 34, Lima, Perú
Keywords: Acute toxicity, Swiss mice, Werneria dactylophylla
ABSTRACT
A study was conducted to evaluate the potential toxic effect of a lyophilized aqueous extract of Werneria dactylophylla (Pupusa) recognized for their important pharmacological properties. For its development we used the fixed dose procedure, using a limit dose of 2000 mg / kg and 5000 mg / kg of body weight, administered by orogastric route for 14 days performing observations. The selected animals were female albino Swiss mice weighing between 18 and 20 g. Results demonstrated the safety of the plant with no signs or symptoms of toxicity observed. Body weight behaved according to the growth curve of the species and there were no gross abnormalities in the studied organs, allowing to say that the LD50 is above 5000 mg / kg, considering the product as nontoxic as the Williams criterion. The methodology and experimental design was conducted along the lines described by the standard EPA (Environmental Protection Agency) 870.1100, OECD 425 (Organization for Economic Trade and Development), which covers the 24 most developed nations of the world, for applying the method of Acute Toxicity Class (CTA).
Corresponding author: juan_antonio_avila@hotmail.com
RESUMEN
Se realizó un estudio con el objeto de evaluar el posible efecto tóxico de un extracto acuoso liofilizado de Werneria dactylophylla (Pupusa) reconocida por sus importantes propiedades farmacológicas. Para el desarrollo del mismo se utilizó el procedimiento de dosis fijas, utilizando dosis límite de 2000 mg/Kg y 5000 mg/Kg de peso corporal, administradas por vía orogástrica, realizándose observaciones durante 14 días. Los animales seleccionados fueron ratones Swiss albinos hembras con un peso comprendido entre 18 y 20 g. Los resultados demostraron la inocuidad de la planta al no observarse signos ni síntomas de toxicidad. El peso corporal se comportó acorde a la curva de crecimiento de la especie y no se apreciaron alteraciones macroscópicas en los órganos estudiados, todo lo que permite afirmar que la DL50 se ubica por encima de 5000 mg/Kg, considerándose el producto como no tóxico según el criterio de Williams. La metodología y el diseño experimental se llevó a cabo siguiendo la orientación descrita por la norma EPA (Agencia de Protección Ambiental) 870.1100, OECD 425 (Organización Económica para el Comercio y Desarrollo), que abarca las 24 naciones más desarrolladas del mundo, para la aplicación del método de las Clases de Toxicidad Aguda (CTA).
INTRODUCCION
La validación científica de las plantas medicinales hoy en día toma gran importancia una vez detectada su actividad biológica dentro del desarrollo de un nuevo fármaco, porque no podemos limitarnos a la sabiduría popular, la seguridad y eficacia de una planta ya que cada parte de ella tiene numerosas sustancias capaces de producir efectos tóxicos.1 2 Werneria dactylophylla de nombre vernáculo Pupusa (familia Asteraceae, tribu Senecionae) está conformada por 40 especies distribuidas geográficamente en los países de Argentina, Bolivia, Colombia, Chile, Ecuador, Perú y Venezuela, son hierbas pigmeas perennes de uso ancestral como remedio para la inflamación de las amígdalas, asma, bronquitis aguda, contra heridas infectantes y un importante reporte es el uso para el mal de altura (soroche) como sustituto de la coca para la hipoxia de la altura.3 4 5 El presente estudio tuvo como objetivo obtener información sobre la toxicidad aguda oral en ratones hembras del extracto acuoso elaborado a partir de la Werneria, así como determinar los signos de toxicidad retardada tras la administración por vía orogástricaa dosis límite del producto.
SECCION EXPERIMENTAL
Material Vegetal
Planta colectada al pie del cerro Huayna Potosí, Milluni región del departamento de La Paz a 4960 metros de altura. La clasificación taxonómica de la planta fue realizada por el Herbario Nacional de Bolivia y depositado con el número de código VCM-1. Extracto acuosos liofilizado de Werneria dactylophylla, fue elaborado por el Instituto de Investigaciones en Productos Naturales (IIPN,UMSA)
Modelo biológico
Se emplearon ratones Swiss albinos hembras, sanas con un peso de 18 – 20 g, provista por el bioterio de la Facultad de Ciencias Farmacéuticas y Bioquímicas de la Universidad Mayor de San Andrés. Se formaron cuatro grupos de tres animales cada uno: dos tratados y dos controles. Los animales agrupados se mantuvieron durante el ensayo (14 días) con alimentación peletizada y agua ad libitum, a una temperatura de 20 ± 2º C, un fotoperíodo de 12 horas luz / 12 horas oscuridad y una humedad relativa entre 30 y 70 %.
Diseño experimental
Para el ensayo se empleó el test límite, metodología y diseño experimental descrito por las normas EPA (Agencia de Protección Ambiental) 870.1100, OECD 425 (Organización Económica para el Comercio y Desarrollo.6 7 La sustancia administrada fue de 2000 mg/mL y 5000 mg/mL de peso del producto a evaluar disuelto en agua destilada, mediante cánulas por vía orogástrica a una dosis por única vez, los volúmenes de administración no excedieron los 100 µl. El alimento fue retirado 12 horas antes de comenzar el experimento y vuelto a suministrar 3 horas después de la administración. Durante el período de ensayo los animales fueron observados individualmente durante los primeros 30 minutos, con especial atención durante la primera, 2 horas, 4 horas, 6 horas, 24 horas, 48 horas, 7 días hasta los 14 días del experimento. Se controló y observó los cambios de comportamiento, signos y síntomas de toxicidad de los animales y mortalidad mediante la tabla de Irwing. La evaluación incluyó la relación que puede existir entre los ratones tratados y grupo control que recibió el vehículo (agua destilada). Las observaciones están dirigidas a la determinación de: muerte y tiempo de ocurrencia de la misma, signos y síntomas de toxicidad: Ataxia, parálisis de patas anteriores y posteriores, alarma, piloerección, equilibrio, palidez, erección de la cola, actividad motora, reflejo corneal, analgesia . El test de la chimenea está dirigido para evaluar actividad neuromuscular, incluyendo su inicio y duración. Se controló el peso vivo de los animales en los días 1, 7 y 14 días del experimento como uno de los parámetros demostrativos de toxicidad. Al finalizar el experimento se procedió al sacrificio de los animales por inhalación de éter etílico para el estudio anatomopatológico macroscópico del cerebro, estómago hígado, bazo, pulmones, riñones, e intestinos.
RESULTADOS, DISCUSION
Comportamiento del peso corporal
La administración del producto no afectó el incremento de peso de los animales tratados a las dosis de 2000 mg/Kg y 5000 mg/Kg respecto al grupo control, comportandose dentro de los parámetros establecidos del modelo biológico, lo cual fue corroborado mediante el análisis estadistico de los datos. Como se puede apreciar en la Figura 1-2
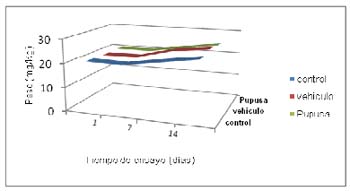
Fig. 1 Comportamiento del peso corporal tras el tratamiento con una dosis administrada de 2000 mg/kg
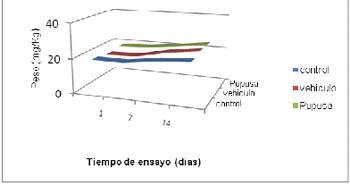
Fig. 2 Comportamiento del peso corporal tras el tratamiento con una dosis administrada de 5000 mg/kg
No hubo diferencias significaticas (p>0.05) entre las pendientes de las curvas de ganacias de peso corporal obtenidas de los tratados y los controles.
Signos clínicos
La evaluación de los signos clínicos incluyo la reacción entre los ratones tratados y no tratados durante todo el ensayo. Las observaciones clínicas durante el período de ensayo no arrojaron alteraciones en los diferentes sistemas estudiados. Todos los parámetros evaluados permanecieron normales en los animales, como el reflejo postural normal, respuesta habitual a los estímulos nociceptivos, consumo de alimento y agua como corresponde a su especie a la dosis de 2000 mg/kg y 5000 mg/kg. La supervivencia fué de un 100 por ciento, siendo esto un indicador de que la DL50 del producto por vía oral es superior a 5000 mg/Kg de peso corporal.
Exámen anatomopatológico macroscópico
El estudio del exámen anatomopatológico macroscópico de los órganos cerebro, estómago hígado, bazo, pulmones, riñones, e intestinos, buscando posibles signos de toxicidad, no evidenciaron alteraciones patológicas en los órganos analizados. El peso corporal constituye uno de los parámetros y principal indicadores de posibles trastornos orgánicos en los estudios de toxicidad. En este estudio no se observaron variaciones en la ganancia de peso corporal de los animales a las dosis de 2000 mg/Kg y 5000 mg/Kg.. Las observaciones realizadas durante todo el ensayo en los diferentes signos clínicos mostraron que en los animales tratados, a las dosis evaluadas, no se provocaron alteraciones clínicas ni produjeron mortalidad. Los estudios macroscópicos no tuvieron lugar a modificaciones en los órganos examinados ni se observaron alteraciones clínicas. El estudio de toxicidad aguda oral del producto evidencia que en nuestras condiciones experimentales la DL50 es superior a 5000 mg/kg.
CONCLUSIONES
El producto se clasifica como no tóxico a una dosis de 5000 mg/kg, según la tabla de Williams publicada en el Manual de Técnicas de Investigación CYTED 1995 para productos naturales administrados por vía orogástrica a dosis única por vía oral en ratones Swiss albinos hembras, lo cual avala los resultados obtenidos.
BIBLIOGRAFÍA
1. Morón FJ: Plantas medicinales y medicamentos herbarios. En: Morón FJ, Levy M. Farmacología general. La Habana : Editorial Ciencias Médicas; 2002.p. 195-205. [ Links ]
2. Morón, F, Villán J, Martínez M.J. REv. Cubana Med. Gen. 1991;7;276-84 [ Links ]
3. Lock Sing, O.,R.,Diversidad Química del Género Werneria. Rev. Soc. Quim. Perú v. 72 n. 1Lima ene/mar. 2006 [ Links ]
4. Cabrera, A.,L. Las Especies Argentinas del Género Werneria (Compositae, In: Notas del Museo de La Plata, Tomo XIII, botánica, Nº 60, Instituto del museo de la Universidad Nacional de La Plata, república Argentina, 27de julio 1948. pp 49-61 [ Links ]
5. Bonilla et al. Contribución al estudio químico biológico de la Werneria dactylophylla, rev. Soc. quim. Perú, 57,182-188,1991 [ Links ]
6. OECD. Guideline no. 420 Acute oral toxicity – fixed Dose Procedure. Francia : Guideline for Testing of Chemicals, Inc.; 2007 (Actualizado 26 Jun 2007); citado 18 Nov 010) . Disponible en: http:// www.oecd.org [ Links ]
7. OECD. Organization for Economic Cooperation and Development. Guidelines for testing of chemicals. Guideline no. 420: Acute oral toxicity class method, Paris; 2002; 5-6. [ Links ]
8. Repetto M. Toxicología Fundamental. Toxicología Experimental. Toxicidad Aguda. Tercera Edición. Editado por ENPSES-MERCIE GROUP, España; 2002; 295-298 [ Links ]












 uBio
uBio 

