Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista Boliviana de Química
On-line version ISSN 0250-5460
Rev. Bol. Quim vol.28 no.2 La Paz 2011
ARTICULO ORIGINAL
FOTOCROMISMO EN FIBRA DE POLIAMIDA
Willy J. Rendón P.
Instituto de Investigaciones en Productos Naturales (IIPN), Instituto de Investigaciones Químicas (IIQ), Carrera de Ciencias Químicas, Facultad de Ciencias Puras y Naturales , Universidad Mayor de San Andrés, 2º piso Edificio FCPN Campus Universitario Calle 27 y Calle Andrés Bello Cota Cota, La Paz - Bolivia
Keywords: Reacción de Stenhousen, colorante, teñido, fotocromismo
ABSTRACT
The polyamide fibber presents a good affinity for Stenhousens products, particularly when fixed with Cibatex. It shows a relevant photochromic activity when applying sun light-radiation, provoking a colour change from roseate to violet.
Corresponding author: willyjrendon@yahoo.com
RESUMEN
La fibra de poliamida presenta buena afinidad por el producto de Stenhousen, especialmente fijada con Cibatex y muestra marcada actividad fotocrómica, cuando es sometida a una radiación de luz solar, produciendo el cambio de color rosado a violeta.
INTRODUCCION
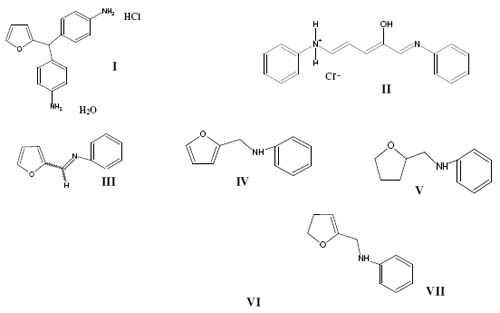
J. Stenhousen publicó en 1870 la reacción, entre el furfural, anilina y ácido clorhídrico, en medio alcohólico, dando un producto de color rosado intenso. (1). Varios investigadores estudiaron las reacción de Stenhousen, reportando moléculas como I donde asumen ésta estructura por la similitud con los colorantes derivados del trimetilmetano, posteriormente la estructura II fue propuesta (2) por Zincke y Millhousen, así también se propusieron las estructura III (3) el furfuriledeno-anilina, y la N-furfuril-anilina IV (4), N-tetrafurfuril-anilina V, N,N-dietil-anilina VI y el N-dihidrofurfuril-anilina VII.
El producto de color rosado intenso que presenta la reacción de Stenhousen entre la anilina y el furfural en medio ácido, motivo a varios investigadores la búsqueda útil de éste producto, entre los que se encuentra el método de análisis colorimétrico, para la determinación del contenido y evaluación del furfural, proveniente de la hidrólisis de pentosas de residuos vegetales, refinado de petróleo y bebidas alcohólicas (5,6,7,8). Cuando usaron el método analítico colorimétrico para la determinación de furfural y de acuerdo con la Norma Boliviana notaron que las lecturas de absorbancia variaban por efecto de la radiación de la fuente del equipo (espectrofotómetro), mostrando una variación en los valores de absorbancia, unas veces incrementándose y otras reduciéndose, durante el proceso de las lecturas en el espectrofotómetro. Las soluciones sometidas a fenómenos físicos de temperatura y luminosidad, mostraban una decoloración de la solución de rosado a incoloro, esto les indujo a realizar un estudio de estabilidad del compuesto coloreado proveniente de la reacción de Stenhousen y tener mayor confianza en las lecturas de los valores de absorbancia, logrando estabilizar y sensibilizar el producto coloreado, para ello usaron bajas temperaturas y la N,N-dimetilformamida, bajo estas condiciones les permitió realizar lecturas de absorbancia más confiables (9), éste método fue comparado con el método volumétrico del clorhidrato de la hidroxilamina dando una correlación del 0,999. (10). El producto de la reacción de Stenhousen usado como colorante en solución acuosa presentó buena afinidad con las fibras de poliamida, tiñendo de color rosado intenso la que permitió diferenciar la fibra de poliamida de otras. (11). La gran importancia y uso técnico que tienen los fenómenos termocrómicos y fotocrómicos, inducen a los químicos, buscar moléculas con sensibilidad a las propiedades físicas como la luz y la temperatura; Ya que estas propiedades son de interés técnico y usados en dispositivos para el control de temperatura, en satélites, elementos de memoria en computadoras, cremas protectoras de las radiaciones solares para proteger de la radiación UV que son causantes de la destrucción celular, acelerando el envejecimiento y participando en la generación del cáncer cutáneo (12,13), también en la elaboración de fibras textiles, así como de filtros ópticos para control en fase líquida o sólida y cuyas transiciones son estudiadas por resonancia del spin electrónico (ESR) (14, 15).
SECCION EXPERIMENTAL.
Preparación del producto de la reacción de Stenhousen.- Se mezcla 10 ml. de furfural con 20 ml de anilina y 30 ml de ácido acético, la mezcla se deja en reposo por 24 horas en condiciones naturales, al cabo de la cual se añade una cantidad suficiente de cloruro de sodio hasta saturación de la solución acuosa, momento en la que el producto de la reacción de Stenhousen precipita un sólido de color guindo.
Teñido de la fibra.- Se pesa 0,130 g de poliamida limpia y seca. Se preparan las siguientes soluciones, una solución compuesta de 0,02 ml de furfural/ ml de solución acuosa, 0,04 ml de anilina/ ml de solución acuosa y 0,06 ml de ácido acético/ ml de solución acuosa (la que constituye la solución acuosa de la sal de acetato de anilina), y 0,05 g de sal/ ml de solución acuosa. La solución de teñido está constituida por 5 ml de solución acuosa de furfural, 5 ml de solución acuosa de acetato de anilina y diluida a un volumen de 20 ml con agua a la que se añadió 5 ml de solución salina, toda la solución se mantiene reaccionando por 4 h. A temperatura ambiente. La fibra de poliamida 0,130 g es sumergida en la solución coloreada y se deja por 45 min., agitando constantemente y a la temperatura ambienten de 17ºC., luego se procede al fijado.
Fijado del colorante.- Se prepara la solución de ácido acético usando 0,35 ml de ácido acético /ml de solución acuosa, en 5 ml de ésta solución se sumerge la fibra teñida por el tiempo de 10 min. y a temperatura ambiente, luego se disuelve 2 gotas de cibatex / 10 ml de agua y ésta mezcla se añade a la solución acética donde se encuentra la fibra, y se la mantiene por especio de 10 min. después del proceso de fijado se procede al lavado con agua y detergente, para luego proceder al secado en condiciones ambientales.
Intensificación del color.- Para intensificar el color sobre la fibra es suficiente tratar la fibra teñida con unas gotas de ácido sulfúrico.
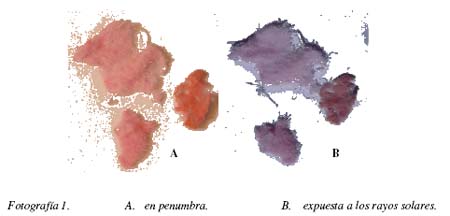
Fenómeno del fotocromismo.- Una vez teñida de rosado la fibra de poliamida, ésta es sometida al efecto de la radiación solar, el color rosado de la fibra cambia de inmediato a violeta como puede observarse en la fotografía 1., una vez pasado el efecto de la radiación el color de la fibra vuelve al color original cuando es llevado nuevamente la fibra a penumbra.
RESULTADOS, DISCUSIÓN
La reacción de Stenhousen usada ampliamente como método de análisis del furfural, presenta el fenómeno fotocrómico y termocrómico en solución acuosa, así como en fase sólida, el producto es de fácil precipitación, añadiendo cloruro de sodio al producto de la reacción, la precipitación de la sustancia coloreada es debido a la fuerza iónica de la sal de sodio, el producto coloreado es soluble en agua, lo que demuestra la elevada polaridad del compuesto. El uso del producto cibatex permite fijar el colorante en la fibra, esto produce una mayor durabilidad del color ante los efectos de la radiación luminosa solar, aunque no de manera óptima como uno quisiera, ya que el colorante pierde el color con el tiempo, sin embargo mantiene el color rosado en la fibra de poliamida por muchos años en completa oscuridad. El cambio de color rosado a violeta, como muestra la imagen fotográfica, constata el cambio de color, debido a la radiación solar, manifestando claramente la propiedad fotocrómica del producto de la reacción de Stenhousen adherida a la fibra de poliamida. El uso del ácido sulfúrico en el teñido de la fibra eleva el tono del color rosado, esto permitiría desarrollar un nuevo método analítico cuantitativo del furfural por reflexión.
RECONOCIMIENTOS
A la Carrera de Ciencias Químicas, por el apoyo que brinda a la realización de los trabajos de Investigación.
REFERENCIAS
1. WILLIAM M. FOLEY, JR., GUY E. SANFORD AND HERBERT MCKENNIS, JR. J. Am. Chem. 74; 5489-5491 (1952). [ Links ]
2. RICHARD W. DRISKO AND HERBERT MCKENNIS, JR; J.Am. Chem. Soc., 74; 2626-2628 (1952). [ Links ]
3. DE CHALMOT; JLACBF; JUSTUS LIEBIG.; Ann. Chem; 271; 1892; 12.
4. KLYUYEV M.V.; NASIBULIN A.A.; ABDULLAYEV M.G.; PECHAM; Pet.Chem USSR (Engl. Transt); EN; 34; 5; 1994.; 399-406.; Neftekhimiya.; RU. 34.; 5.; 1994.; 413-420. [ Links ]
5. R.S.STILLING, Y B BROWING.; Ind. And Eng. Chem.; Analytical Edition; Vol 12; 499-502. (1940). [ Links ]
6. O.I.MILNER AND DAVID LIDERMAN.; Ind. And Eng. Chem.; Analytical Edition.; Vol 27; 1922-1823. (1955). [ Links ]
7. R.B. HARRISON.; Analyst.; 88 (1049.; 644-646 (1963).; C.A.59; 12184H. [ Links ]
8. D.G.N.T.; Norma Boliviana 206-77.; Determinación de ésteres, metanol, aldehídos, furfural y alcoholes superiores en bebidas alcohólicas destiladas.; La Paz- Julio; 1977. [ Links ]
9. RENDÓN P.W.; Rev. Bol. Quím.; Vol 6.; 9-12.; 1986. [ Links ]
10. DUCHEN U.E.P.; RENDÓN P. W.; Trabajo Teórico Experimental,; UMSA,; La Paz Bolivia; 1986. [ Links ]
11. RENDÓN P.W.; Rev. Bol. Quím.; Vol.; 26.; 27-29.; 2009 . [ Links ]
12. TESTAR SEVILLA GEORGINA,; BALFAGÓN COSTA ALBERTO,; Afinidad: Revista de Química Teórica y aplicada,; Vol. 64, Nº 527,; 2007. [ Links ]
13. GACEN J.; Boletín Intertex. (U.P.C.).; Nº 119.; págs 59-65.; 2001. [ Links ]
14. METZ F.I., SERVOSS W.C. AND WELSH F.E.; J.Phys. Chem 66, 2446 (1962). [ Links ]
15. COHEN M.D. AND SCHMIDT G.M.J.; J.Phys. Chem 66, 2442 (1962). [ Links ]
16. Auletta C. Acute Systemic Toxicity Testing. In: Product Safety Evaluation Handbook: Ed. Gad S.C.; Ed. Marcel Dekker, Inc. U.S; 1999; 43-86. [ Links ]
17. Gámez R, Más R, Noa M, Menendez R. Acute and oral subchronic toxicity of D-003 in rats. Toxicol Letters 2000; 118:31-41. [ Links ]
18. OECD. Organization for Economic Cooperation and Development. Guidelines for testing of chemicals. Guideline no. 420: Acute oral toxicity class method, Paris; 2002; 5-6. [ Links ]
19. Repetto M. Toxicología Fundamental. Toxicología Experimental. Toxicidad Aguda. Tercera Edición. Editado por ENPSES-MERCIE GROUP, España; 2002; 295-298 [ Links ]
20. Gonzales Eduardo, Ávila Juan A., Arias Juan L., Torrico Bernardo, Contribución al estudio de la plunbagina determinación de la dosis letal media, Biofarbo; Vol. IV; 1995; 63-66. [ Links ]














