Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista Boliviana de Química
versión On-line ISSN 0250-5460
Rev. Bol. Quim v.27 n.1 La Paz ago. 2010
ARTICULO ORIGINAL
Actividad antifUngica IN VITRO de extractos polares de plantas del genero baccharis sobre fitopatOgenos
Silvia Martíneza,b,c, Enrique Terrazasc, Teresa Alvarezc, Oscar Mamanib, José Vilaa, Patricia Mollinedoa
aInstituto de Investigaciones en Productos Naturales (IIPN), bÁrea de Bioorgánica del Instituto de Investigaciones Químicas (IIQ), Universidad Mayor de San Andrés, Campus Universitario, Edifico de la F.C.P.N., Calle27, Cota-Cota cInstituto de Investigaciones Fármaco-Bioquímicas (IIFB), Universidad Mayor de San Andrés, Avenida Saavedra 2224, 2º piso, Miraflores
Keywords: Fitopatógenos, biocontroladores, Aspergillus niger, Phytophthora palmivora, Baccharis sp, in Vitro.
ABSTRACT
Researching for natural alternatives to control plant diseases, polar extracts were made of Baccharis genus plants. The inhibitory effect of polar extracts in Vitro was evaluated, as mycelia growth inhibition against phyyopathogenic fungi: Phytophthora palmivora and Aspergillus niger. The results have shown a significant effect of the extracts of B. latifolia on reducing the growth of pathogenic fungi.
Corresponding author: sssilmar92@gmail.com
INTRODUCCION
Las plagas y enfermedades constituyen la principal limitante de la producción agrícola. Su control se ha basado, en el uso de productos químicos sintéticos, muchos de los cuales han producido, como efecto secundario, problemas de desequilibrio ambiental, de salud humana y el surgimiento de plagas y enfermedades más agresivas y resistentes a ellos. Existe referencia de una alta incidencia de enfermedades y diversos cuadros clínicos por intoxicación en la población, como también se detectan elevados niveles de pesticidas en cosechas y personas. Como consecuencia, se buscan otras alternativas. Una de ellas es el uso de derivados botánicos para el control de plagas y enfermedades. Las plantas, en su evolución han desarrollado mecanismos de defensa contra insectos, hongos, bacterias y otros organismos nocivos y los metabolitos secundarios producidos por ellas constituyen una de esas barreras. Las especies del género Baccharis son utilizadas tradicionalmente para el control o tratamiento de varias dolencias, contusiones, inflamaciones, también como desinfectante y antimicrobiano. Se destaca la presencia de Flavonoides, Diterpenos y Triterpenos donde los Flavonoides, son conocidos por conferir resistencia frente al ataque de microorganismos.
RESULTADOS, DISCUSION
Las medidas del diámetro de crecimiento se muestran en la Figura 1 para Aspergillus niger y en la Figura 3 para Phytophthora palmivora, mientras que el porcentaje de inhibición se representa en la Figura 2 para Aspergillus niger y en la Figura 4 para Phytophthora palmivora.
Aspergillus niger
La velocidad de crecimiento (Figura 1).del control negativo Aspergillus niger es de 0,4355 mm/hora. El extracto etanólico de Baccharis latifolia BLE, crece a una velocidad de 0,1657 mm/h y para BLMA de 0,2143 mm/h. La velocidad de crecimiento del extracto acuoso de Baccharis genistelloides de La Paz BGLPA es de 0,253 mm/h. Del porcentaje de inhibición (Tabla 1 y Figura 2), se puede ver que los extractos de Baccharis genistelloides de La Paz acuoso BGLPA y de Baccharis latifolia etanólico BLE y el de polaridad media BLMA, son los que presentan un porcentaje de inhibición por encima del 50% luego de 240 horas de realizadas las mediciones diarias del diámetro de crecimiento, mientras que el Control negativo C(-) Aspergillus niger creció hasta llegar al 74% en ese mismo lapso de tiempo. Con los cual se puede considerar que BLMA y BGLPA son extractos que a la concentración de 50 mg/mL inhiben el crecimiento in Vitro de Aspergillus niger. De la misma manera BLE inhibe a una concentración de 20 mg/mL.
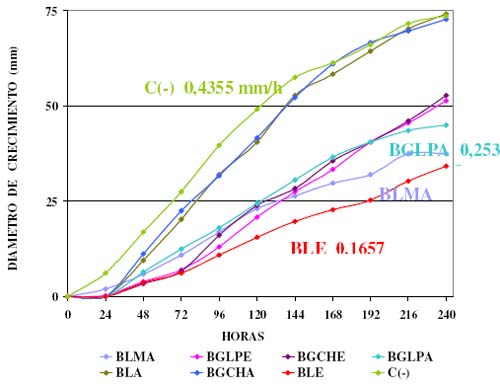
Figura 1. Cinética del crecimiento con Extractos Polares del género Baccharis sobre Aspergillus niger Control negativo c(-).
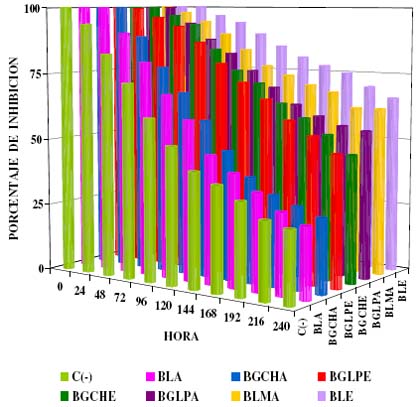
Figura 2. Porcentaje de Inhibición de Extractos polares del género Baccharis sobre Aspergillus niger Control negativo c(-).
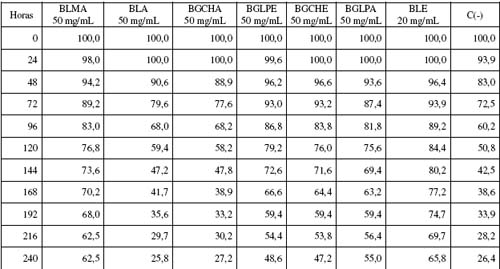
Tabla 1. Porcentaje de inhibición de extractos polares del género Baccharis sobre Aspergillus niger Control negativo c(-).
Con los resultados obtenidos se puede observar que BLE es el extracto que inhibe y mantiene la inhibición de Aspergillus niger a lo largo del tiempo hasta 65,8 %. Esta buena actividad, posiblemente este relacionado a que el extracto contiene algunos compuestos poco polares que pueden estar presentes además de los polares y tienen buena difusión en el medio sólido. Por otro lado Baccharis presenta triterpenos y flavonoides que según el uso tradicional tienen actividad como antisépticos o antimicrobianos. Este efecto explicaría la baja actividad contra este hongo al actuar los otros extractos del mismo género de Baccharis tanto acuosos como etanólicos como BLMA, BGLPA los que presentan un porcentaje de inhibición por encima del 50%, a su vez BGLPE, BGCHE valores poco menores al 50% de inhibición.
Phytophthora palmivora
En la Figura 3, la velocidad de crecimiento para el Control negativo C(-) Phytophthora palmivora es de 0,1816 mm/hora, en comparación al extracto etanólico BLE de Baccharis latifolia que crece a 0,0028 mm/hora. Lo cual indica que existe inhibición del desarrollo del hongo en el lapso de los diez días de realizada la evaluación in Vitro. En la Tabla 2 y Figura 4 vemos que el porcentaje de inhibición desarrollado frente al Control negativo C(-) Phytophthora palmivora del extracto etanólico de Baccharis latifolia BLE llega a 98,8% a lo largo de las 240 horas. Estos resultados muestran que el extracto etanólico es más efectivo para inhibir a Phytophthora palmivora, mientras que el resto de los extractos inhibe solamente en un 25% hasta el décimo día de evaluación. El efecto inhibitorio posiblemente se deba a que como el proceso de extracción se realizó con etanol, que puede extraer tanto compuestos polares como poco polares. Se puede considerar que la mezcla de estos compuestos podría actuar produciendo un efecto sinérgico en la inhibición del crecimiento del hongo fitopatógeno Phytophthora palmivora.
Conclusiones
De las dos especies del género Baccharis, solamente Baccharis latifolia presenta actividad inhibitoria frente a los dos fitopatógenos Aspergillus niger y Phytophthora palmivora. Se puede considerar en especial el extracto etanólico BLE a 20 mg/mL que inhibe a los dos hongos en un 65,8% y 98,8% respectivamente. Por otro lado, Baccharis genistelloides de La Paz (50 mg/mL) presenta inhibición alrededor del 50% solamente frente a Aspergillus niger con los extractos etanólicos y acuosos. Podemos considerar que estos tipos de extractos tienen un gran potencial como controladores de hongos fitopatógenos, por lo cual se recomienda realizar los estudios sobre plantas con estas enfermedades y continuar el estudio con estos y otros fitopatógenos. Además pueden servir como agentes selectivos para el control biológico de las enfermedades en plantaciones y de esta manera mejorar el rendimiento de las cosechas y reducir los gastos en la compra y uso de pesticidas, evitando de esta manera los efectos secundarios tanto en el medioambiente como en las personas.
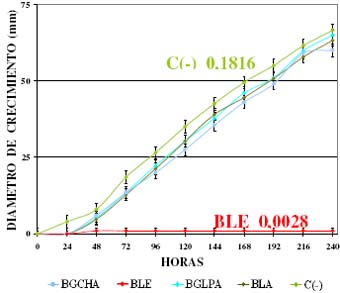
Figura 3. Porcentaje de Inhibición de extractos polares del género Baccharis sobre Phytophthora palmivora Control negativo c(-).
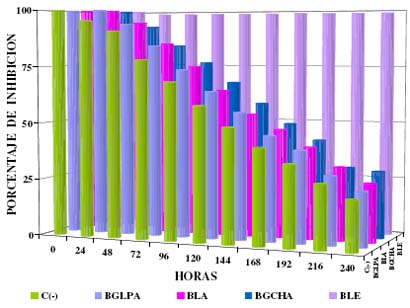
Figura 4. Porcentaje de Inhibición de Extractos polares del género Baccharis sobre Phytophthora palmivora Control negativo c(-).
Tabla 2. Porcentaje de inhibición de extractos polares del género Baccharis sobre Phytophthora palmivora Control negativo c(-).

SECCION EXPERIMENTAL
La evaluación de la actividad inhibitoria de los extractos se realizó in Vitro mediante el método de difusión en agar en pozo central. Los extractos se agregaron al medio Agar Papa Dextrosa después de esterilizar en autoclave, obteniendo una concentración final de 20 y 50 mg/mL y se dispensaron en placas Petri. Luego de 1 hora se inoculan con una suspensión de 1x106 U.F.C./mL de Phytophthora palmivora como de Aspergillus niger y se incuban a 25 ±2ºC. Se midió el diámetro en milímetros de la zona de crecimiento del hongo en cuatro direcciones cada día tomando como resultado el valor promedio de estas mediciones y se compara con la del Control Negativo C(-) para determinar el porcentaje de inhibición de cada uno de los extractos.
Material
Plantas
Se realizó la extracción con etanol (E) y agua destilada (A) de Baccharis latifolia (BL), Baccharis genistelloides (BG), concentrando hasta obtener extracto libre de solvente. Se denominaran según sea el caso con sus siglas y adicionando la sigla del solvente utilizado. Para BL se tiene un extracto de Polaridad media Acuoso denominado BLMA Solamente para B. Genistelloides se adicionaran las siglas LP de La Paz. y CH de Cochabamba. Esta etapa se desarrolló en el Área de Bioorgánica del Instituto de Investigaciones Químicas. Para la evaluación antifúngica se utilizó 20mg/mL y 50 mg/mL de cada extracto.
Hongos
La evaluación de la actividad inhibitoria in Vitro se realizó con cepas de los hongos Phytophthora palmivora QK08 y Aspergillus niger qs07 en el Área de Microbiología de la colección del Instituto de Investigaciones Fármaco-Bioquímicas de la Facultad de Ciencias Farmacéuticas y Bioquímicas.
REFERENCIAS
1.Ramírez Legarreta M. R., et.al., Impacto ambiental del uso de plaguicidas en Huertos de manzano del Noroeste de Chihuahua, México, Rev. Méx. Fitopatología 2002; 20(2):168-173 [ Links ]
2.Ramírez J. A., Plaguicidas: Clasificación, uso, toxicología y medición de la exposición, Arch. Prev. Riesgos Labor. 2001; 4(2):67-75 [ Links ]
3.Yengle María, et.al., Practicas de utilización de plaguicidas en agricultores en el distrito de Huaral-Peru, 2005, Rev. Peruana de Epidemiología 2008;12(1):1-6 [ Links ]
4.Martínez Calbimonte Sergio Diego, Análisis del Cultivo del Cacao San Ignacio de Mojos-Beni, Informe de Viaje, Marcial Consultores, Centro de Investigación y Promoción del Campesinado CIPCA, Diciembre 2005 [ Links ]
5.Pierre Francis, et.al., Residuos de Plaguicidas Organoclorados y Organofosforados en el cultivo de la Cebolla en la Depresión de Quíbor, Venezuela, Bioagro 2007;19 (2):69-78 [ Links ]
6.Aldana-Madrid M.L., et.al., Insecticide residues in Stored Grains in Sonora, Mexico: Quantification and toxicity Testing, Bulletin of Environmental Contamination and Toxicology 2008; 80(2): 93-96 [ Links ]
7.Ramírez-Vasquez N., Betancur Maria E., Ruiz John D., López Carlos, Restrepo Luis F., Zapata Mauren, Validación de un método analítico para la determinación de Fention en Leche Bovina, Actual. Biol. 2006;28(85):115-124 [ Links ]
8.Loaiza J.E., Rivera G., Potencial biocida de extractos de Gliricidia sepium contra patógenos del cultivo de la papaya (Carica papaya), Agronomía Costarricense 2000;24(1):29-36 [ Links ]
9.Hernández Lauzardo A.N., et.al., Prospectiva de Extractos Vegetales para controlar Enfermedades Postcosecha Hortofrutícolas, Rev. Fitotec. Mex. 2007; 30(2):119–123 [ Links ]
10.Mendoza, C.B., et.al., Evaluación del efecto de Extractos Vegetales sobre el Crecimiento in Vitro de Phytophthora palmivora Butl. y Colletotrichum gloeosporioides (Penz.) Penz. & Sacc., Tierra Tropical,2007; 3(1):81–89 [ Links ]
11.Zapata R., et.al., Reducción del desarrollo de hongos fitopatógenos con extracto de cardón lefaria (Cereus deficiens Otto & Diert), Interciencia, 2003,28(5):302-306 [ Links ]
12.Mesa Arango A.C., et.al., Productos naturales con actividad antimicótica, Rev. Esp. Quimioterapia, 2004;17(4):325-331 [ Links ]
13.Davicino R., et.al., Actividad antifúngica de extractos de plantas usadas en medicina popular en Argentina, Rev. Peru. Biol., 2007; 14(2):247-251 [ Links ]
14.Marín Ocampo A. M.., et.al., Actividad antifúngica de los extractos acuosos de Baccharis trinervis, Baccharis latifolia y Solanum dolichosepalum, Biosalud, 2006; 5:51–59. [ Links ]
15.Coelho M.G.P., Anti-arthritic effect and subacute toxicological evaluation of Baccharis genistelloides aqueous extract, Toxicol. Lett. 2004;154:69–80 [ Links ]
16.Gonzaga Verdi L., et.al., Gênero Baccharis (Asteraceae): Aspectos químicos, econômicos e biológicos, Quim. Nova, 2005; 28(1):85-94, [ Links ]
17.Madeira Moreira F. P., et. Al., Flavonoides e Triterpenos de Baccharis pseudo tenuifolia – Bioatividade sobre Artemia salina, Quim. Nova, 2003;26(3):309-311 [ Links ]
18.Budel J.M., et. al., O progresso da pesquisa sobre o genero Baccharis, Asteraceae: I- Estudos botânicos, Rev. Brasileira de Farmacognosia, 2005;15(3): 268-271 [ Links ]
19.Márquez V. R. L., et.al., Actividad antifúngica del extracto total en etanol de las hojas frescas de Pedilanthus tithymaloides L.Poit (Ultimorrial), Scientia et técnica Año XIII, 2007; 33; 155 [ Links ]
20.Villagrán C.,et.al., Etnobotánica del Sur de los Andes de la Primera Región de Chile: Un enlace entre las Culturas Altiplánicas y las de Quebradas Altas del Loa Superior, Chungara, Revista de Antropología Chilena, 2003; 35(1):73-124 [ Links ]












 uBio
uBio 

