INTRODUCCIÓN
La conservación in vitro de especies vegetales es una estrategia fundamental para preservar la biodiversidad y mantener la viabilidad y la calidad genética de las especies vegetales a largo plazo. Según Almeida y Díaz (1), esta técnica se utiliza ampliamente para conservar especies agrícolas y forestales, asegurando que se puedan recuperar en el futuro. La capacidad de conservar germoplasma in vitro no solo protege las variedades locales, sino que también facilita el mejoramiento genético y la investigación agronómica (2).
Esta técnica se basa en la manipulación de tejidos vegetales en condiciones controladas, permitiendo su mantenimiento a largo plazo y evitando riesgos asociados al deterioro genético y fitosanitario. Las técnicas de conservación a corto plazo se emplean principalmente en bancos de germoplasma, donde se utilizan medios de cultivo con agentes osmóticos para inducir un crecimiento lento de los explantes, disminuyendo su metabolismo y prolongada viabilidad (3). El medio Murashige and Skoog (MS), ampliamente reconocido como estándar, puede modificarse con reguladores de crecimiento y carbohidratos específicos para optimizar su uso en la conservación in vitro (4, 5).
La conservación a largo plazo incluye la crioconservación, una técnica que consiste en el almacenamiento de tejidos vegetales en nitrógeno líquido a una temperatura de -196°C. Este método permite preservar el material genético por tiempo indefinido, asegurando la viabilidad de los tejidos tras el proceso de descongelación, siempre que se sigan protocolos adecuados para evitar daños por formación de cristales de hielo o estrés osmótico. La crioconservación es especialmente útil para la preservación de recursos genéticos valiosos y especies en peligro, proporcionando una solución eficaz para la conservación ex situ a largo plazo (6).
Por ello, el cultivo de tejidos in vitro se ha convertido en una herramienta esencial en la biotecnología agrícola, permitiendo la propagación y conservación de especies de interés, como la papa Solanum tuberosum L., que constituye uno de los cultivos más importantes a nivel mundial, tanto por su valor nutricional como por su versatilidad en la producción de alimentos. Este tubérculo, originario de los Andes, representa un recurso clave para la seguridad alimentaria global, al ocupar el cuarto lugar en producción detrás del trigo, el arroz y el maíz (7).
Este cultivo ofrece ventajas significativas, como la reducción del espacio necesario para el crecimiento de las plantas y la posibilidad de mantener condiciones controladas que favorecen el desarrollo de los explantes (8). Sin embargo, su cultivo enfrenta desafíos significativos como el estrés osmótico causado por condiciones ambientales adversas, el cual puede afectar negativamente su desarrollo y rendimiento y el manejo del crecimiento de los explantes (9).
En este contexto, la adición de agentes osmóticos como el manitol y el sorbitol en los medios de cultivo ha emergido como una estrategia prometedora para simular condiciones de estrés y promover respuestas fisiológicas que mejoren la tolerancia de las plantas (10). Estos compuestos contribuyen al control del potencial osmótico y la estabilización del metabolismo celular, reduciendo el estrés hídrico y oxidativo, además de facilitar la conservación de recursos genéticos bajo condiciones controladas (11).
En estudios recientes, como los desarrollados por Wada (12) y Sajid y Aftab (13), se ha demostrado que estos compuestos son efectivos para ralentizar el crecimiento de los explantes y mantener la estabilidad genética, minimizando el riesgo de mutaciones somanucleares. Además, son reguladores de crecimiento y se han utilizado ampliamente para controlar el desarrollo de brotes y la inducción de microtubérculos in vitro. Estos reguladores actúan promoviendo la división y elongación celular, así como el desarrollo de estructuras especificas según las condiciones de cultivo.
En consecuencia, la aplicación práctica del uso de manitol y sorbitol en la conservación in vitro tiene implicaciones significativas para la agricultura moderna. Con el aumento del interés por la sostenibilidad y la conservación de recursos genéticos, estas técnicas ofrecen soluciones viables para mantener variedades locales y mejorar la seguridad alimentaria. La capacidad para conservar germoplasma durante períodos prolongados permite a los investigadores realizar estudios genéticos y agronómicos sin comprometer las variedades originales (14).
Además, estas técnicas son especialmente relevantes en contextos donde las condiciones ambientales se están modificando rápidamente debido al cambio climático. La posibilidad de conservar variedades adaptadas a condiciones específicas puede ser clave para garantizar que los cultivos sigan siendo productivos frente a nuevos desafíos ambientales (15).
Independientemente de las ventajas expuestas, la conservación in vitro de Solanum tuberosum L. enfrenta diversas limitaciones que abarcan aspectos técnicos, económicos y ambientales, a nivel global y en América Latina, que afectan su implementación y eficacia y deben ser considerados para mejorar las prácticas de conservación (16). Por otra parte, la conservación in vitro requiere condiciones específicas que pueden ser difíciles de mantener. La técnica implica la modificación del medio de cultivo y el control riguroso de factores como la temperatura y la concentración de nutrientes, lo que puede resultar en un crecimiento subóptimo si no se manejan adecuadamente. Además, existe el riesgo de que los explantes sufran daños por condiciones inadecuadas, como la alta concentración osmótica o el oscurecimiento de los tejidos, lo que puede comprometer la viabilidad del material conservado (17).
De igual manera, la implementación de estas técnicas puede ser costosa debido a la necesidad de equipamiento especializado y condiciones controladas. Esto es especialmente relevante en países en desarrollo donde los recursos pueden ser limitados. La dependencia de insumos importados para la producción de cultivos también incrementa los costos, lo que puede limitar la disposición de los agricultores para adoptar estas tecnologías. En adición, existe una brecha en el conocimiento técnico sobre las mejores prácticas para la conservación in vitro entre los agricultores y técnicos en muchas regiones. La falta de capacitación adecuada limita la capacidad para implementar efectivamente estos métodos, afectando la calidad y la cantidad del material conservado (18).
En América Latina, las condiciones climáticas pueden ser un factor limitante significativo. El cultivo de Solanum tuberosum L. requiere temperaturas específicas para su crecimiento óptimo; variaciones extremas pueden afectar negativamente tanto su desarrollo como su conservación in vitro. Además, el cambio climático presenta nuevos desafíos al alterar estos patrones climáticos, complicando aún más las prácticas agrícolas (19).
Así mismo, muchos países latinoamericanos dependen en gran medida de fertilizantes químicos para maximizar la producción agrícola. Sin embargo, el uso excesivo de estos insumos puede llevar a problemas ambientales y de salud pública, además de afectar negativamente la calidad del suelo, lo que a su vez impacta la efectividad de las técnicas in vitro. Esto crea un ciclo vicioso donde se requiere más insumo para mantener rendimientos, lo cual no es sostenible a largo plazo. A esta situación se añade la falta de incentivos gubernamentales o apoyo financiero, que limita las iniciativas para establecer bancos de germoplasma y programas de conservación in vitro que podrían beneficiar a los agricultores locales (20).
Abordar estos desafíos requiere un enfoque integral que incluya mejoras técnicas, capacitación adecuada y políticas favorables que promuevan prácticas sostenibles. Es por ello pertinente considerar ¿cuál es el efecto de diferentes concentraciones de manitol en el crecimiento y desarrollo de explantes de Solanum tuberosum L. durante la conservación in vitro?, ¿existen interacciones significativas entre las concentraciones combinadas de manitol y sorbitol que afecten el rendimiento de los explantes durante el cultivo in vitro?
Teniendo en cuenta este contexto, el propósito de la presente investigación fue evaluar el efecto de diferentes concentraciones de manitol y sorbitol en el desarrollo de los microtubérculos producidos a partir de explantes in vitro de Solanum tuberosum L., con el fin de optimizar las condiciones para su conservación.
MATERIALES Y MÉTODOS
Se llevó a cabo un diseño experimental completamente aleatorizado con un arreglo factorial de dos factores, cada uno con tres niveles, 2x3, permitiendo evaluar de manera integral el efecto de ambos en el fenómeno estudiado. El factor 1 consistió en las concentraciones de manitol, que incluyeron los niveles del 0%, 2% y 4%. El factor 2 correspondió a las concentraciones de sorbitol, también con niveles del 0%, 2% y 4%.
Los explantes utilizados en esta investigación fueron obtenidos de brotes axilares de plantas madre de la especie vegetal Solanum tuberosum L., variedad Mariva; libres de patógenos y previamente cultivadas in vitro.
Preparación del Medio de Cultivo:
Se utilizó el medio suplementado con vitaminas y agar al 0.8%, más la incorporación de manitol y sorbitol en las concentraciones indicadas. Todos los medios fueron esterilizados por autoclave a 121 °C durante 20 minutos.
Procedimiento para el cultivo in vitro de Solanum tuberosum L., mejorada, variedad Mariva:
Los explantes se sembraron en bolsas de polipropileno con 20 mL de medio de cultivo, bajo condiciones de flujo laminar. Se emplearon brotes apicales, siguiendo protocolos similares a los desarrollados para la micropropagación de otras especies como el Chile chiltepín y la Pitahaya, destacando la importancia de condiciones estériles y combinaciones óptimas de reguladores de crecimiento.
Condiciones de crecimiento o desarrollo de la plántula:
Temperatura: 22 ± 2 °C.
Fotoperiodo: 16 horas de luz y 8 horas de oscuridad.
Humedad relativa: 70 %
Variables de Evaluación:
Crecimiento Vegetativo: Longitud de brotes (cm). Medida de altura a los 29, 62 y 93 días, respectivamente.
Análisis Estadístico:
Se llevó a cabo un análisis de varianza, ANOVA, para evaluar el efecto de los tratamientos y su interacción en las variables de respuesta. La combinación de diferentes concentraciones de sorbitol y manitol, junto con las réplicas, permitió evaluar la influencia de estos factores en la variable de respuesta elegida Tabla 1.
Para ello, se utilizó un modelo de diseño completamente aleatorizado, con un arreglo factorial. Las comparaciones post hoc se realizaron mediante la prueba de Dunnett con un nivel de significancia de p≤0.05. El análisis fue realizado utilizando el software estadístico Minitab.
RESULTADOS
A continuación, se presentan los hallazgos obtenidos, que incluyen análisis estadísticos que corroboran la significancia de los efectos observados y sus implicaciones en el contexto del estudio.
Los datos presentados en la Tabla 2, muestran las comparaciones múltiples, utilizando el método de Dunnett, con un nivel de confianza del 95% y revelan información significativa sobre el efecto de diferentes concentraciones de sorbitol en la altura de las plantas a los 29, 62 y 93 días. En el grupo control, sorbitol 0%, se observa que la altura promedio a los 29 días es de 2.33 cm, a los 62 días de 4.24 cm y a los 93 días de 5.17 cm, todas estas medias no presentan diferencias significativas entre sí.
Tabla 2. Efecto de diferentes concentraciones de sorbitol en la altura de las plantas.
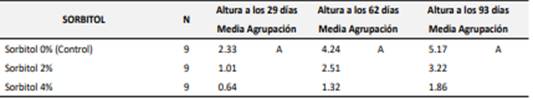
Las medias no etiquetadas con la letra A son significativamente diferentes de la media del nivel de control.
Por otro lado, las plantas tratadas con sorbitol al 2% y al 4% presentan alturas promedio notablemente inferiores en comparación con el control, alcanzando solo 1.01 cm y 0.64 cm a los 29 días, respectivamente, y mostrando un crecimiento limitado en las mediciones posteriores, 2.51 cm y 1.32 cm a los 62 días; 3.22 cm y 1.86 cm a los 93 días. Las medias correspondientes a estos tratamientos son significativamente diferentes del grupo control e indican un efecto inhibitorio del tratamiento sobre el crecimiento de la planta, lo que podría implicar un impacto adverso en su desarrollo y salud general. Este comportamiento podría ser relevante para futuras investigaciones sobre el uso de azúcares como reguladores del crecimiento vegetal o su efecto en condiciones de estrés ambiental.
El análisis de los datos presentados en la Tabla 3, que evalúa el efecto de diferentes concentraciones de manitol en la altura de las plantas, revela resultados significativos. En el grupo control, manitol al 0%, la altura promedio a los 29 días es de 2.21 cm, a los 62 días alcanza 4.24 cm, y a los 93 días llega a 5.18 cm, lo que indica que no son significativamente diferentes entre sí. En contraste, las plantas tratadas con manitol al 2% y al 4% muestran alturas promedio considerablemente menores, con 1.16 cm y 0.62 cm a los 29 días, respectivamente.
Tabla 3. Efecto de diferentes concentraciones de manitol en la altura de las plantas.
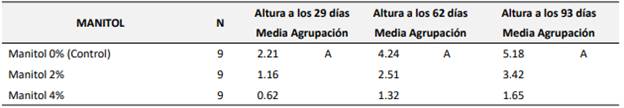
Las medias no etiquetadas con la letra A son significativamente diferentes de la media del nivel de control.
Las mediciones en los días posteriores también reflejan un crecimiento limitado, alcanzando solo 2.51 cm y 1.32 cm a los 62 días, y 3.42 cm y 1.65 cm a los 93 días. Las medias correspondientes a estos tratamientos confirman que son significativamente diferentes del grupo control. Estos resultados sugieren que la adición de manitol, incluso en concentraciones relativamente bajas, tiene un efecto negativo en el crecimiento de las plantas, lo que podría implicar un impacto adverso en su desarrollo general. Este resultado ofrece información relevante sobre el uso de manitol en cultivos y su potencial efecto como agente osmótico o regulador del crecimiento vegetal en condiciones específicas. En la Figura 1 se observa la representación gráfica del efecto de ambos tratamientos sobre el crecimiento de la planta.
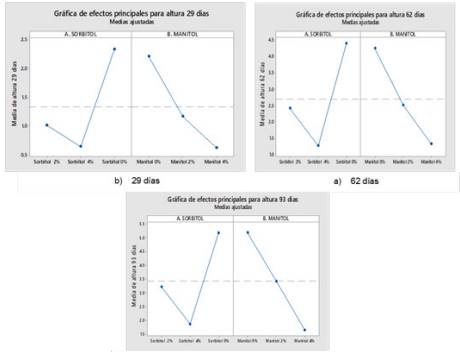
Figura 1. Efecto del sorbitol y el manitol sobre el crecimiento de la planta a los (a) 29, (b) 62 y (c) 93 días.
El análisis de los datos mostrados en la Tabla 4 y representados en la Figura 2, muestran el impacto de diferentes combinaciones de concentraciones de sorbitol y manitol en la altura de las plantas a los 29, 62 y 93 días. En el tratamiento control T9, que consiste en sorbitol 0% y manitol 0%, se observa la mayor altura promedio, alcanzando 4.38 cm a los 29 días, 6.47 cm a los 62 días y manteniendo la misma medida a los 93 días, lo que indica que no son significativamente diferentes entre sí.
Tabla 4. Efecto combinado de diferentes concentraciones de sorbitol y manitol en la altura de las plantas.
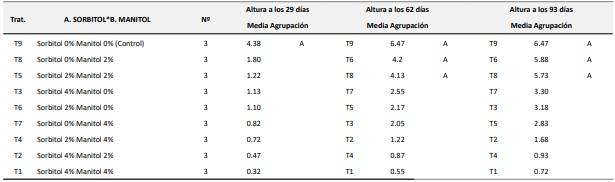
Las medias no etiquetadas con la letra A son significativamente diferentes de la media del nivel de control.
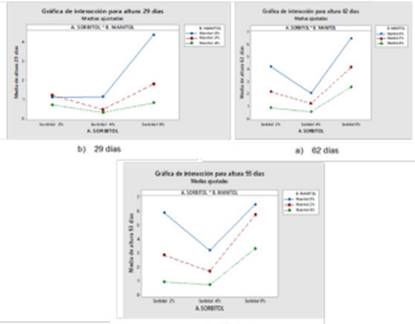
Figura 2. Efecto de la interacción del Sorbitol y el Manitol combinados sobre el crecimiento de la planta a los 29 (a), (62) y (93) días.
En contraste, los tratamientos con sorbitol y manitol presentan alturas notablemente inferiores. El tratamiento T8, sorbitol 0% y manitol 2%, muestra alturas de 1.80 cm a los 29 días, 4.20 cm a los 62 días y 5.88 cm a los 93 días. Los tratamientos que incluyen concentraciones más altas, como T1, sorbitol 4% y manitol 4%, muestran las alturas más bajas, con solo 0.32 cm a los 29 días, 0.55 cm a los 62 días y 0.72 cm a los 93 días. Estos resultados indican que ambos ejercen un efecto negativo sobre el crecimiento de las plantas, siendo más pronunciado en las combinaciones que incluyen mayores concentraciones de ambos compuestos. Estos hallazgos sugieren que su uso en cultivos debe ser cuidadosamente considerado, ya que sus efectos osmóticos pueden limitar el crecimiento vegetal en condiciones específicas.
Discusión
Los resultados obtenidos en este estudio evidencian el impacto dual de las concentraciones de sorbitol y manitol en el crecimiento de los explantes, destacando tanto los efectos positivos a bajas concentraciones como la inhibición provocada por altas concentraciones. Ambos tratamientos demostraron un efecto osmoprotector en bajas concentraciones, favoreciendo un crecimiento moderado de los explantes. Este resultado concuerda con estudios previos como el realizado por Freire (21), que sugiere que estos compuestos, en dosis moderadas, ayudan a regular el potencial osmótico sin causar estrés excesivo, y considera que la propagación de plantas, a través de la embriogénesis somática, representa un método eficiente de multiplicación clonal de plantas.
Estos hallazgos son corroborados por estudios previos en cultivos como la pitahaya, realizados por Salazar et al. (22), donde la suplementación con bencilaminopurina mejoró significativamente la tasa de brotación. La presente investigación evidencia que tanto el sorbitol como el manitol pueden actuar como reguladores osmóticos efectivos a bajas concentraciones, mejorando la adaptación de los explantes al medio de cultivo in vitro, lo que concuerda con Peña et al. (23), quienes demuestran que estos agentes osmóticos favorecen el equilibrio hídrico y reducen el estrés oxidativo en cultivos vegetales. Su uso potencial en la conservación de germoplasma ha sido reportado por Bhatia y Bera (24), como clave para mantener la viabilidad de tejidos a largo plazo en bancos de germoplasma bajo condiciones controladas.
En la presente investigación las concentraciones de 4% generaron efectos adversos significativos en el crecimiento, destacando la importancia de optimizar las dosis para evitar estrés osmótico excesivo; lo que coincide con los resultados obtenidos por Roca y Mroginski (25), quienes encontraron que a concentraciones elevadas, estos agentes osmóticos causaron estrés significativo, como lo observado en otros sistemas vegetales bajo condiciones similares. Este fenómeno es consistente con los resultados de Romero et al. (26), quienes demostraron que estas dosis se asocian a niveles elevados de agentes osmóticos con deshidratación celular y daño oxidativo.
Estos resultados son consistentes con Pineda et al. (10), que asocia altas concentraciones de agentes osmóticos con deshidratación celular y alteración de procesos metabólicos en tejidos vegetales. Estos autores obtuvieron la reducción del crecimiento de papa chaucha en condiciones in vitro con la adición de manitol en diferentes concentraciones, la cual presentó el efecto de reducir el crecimiento en la altura y número de nudos, obtenido explantes con medias de 3,91 de altura de planta y 3,80 número de brotes por explante con el tratamiento de manitol al 8%.
Estos autores recomiendan realizar más evaluaciones a los seis y ocho meses para determinar hasta qué punto el manitol permite reducir el crecimiento de los explantes y a la vez mantener la viabilidad del germoplasma de papa en condiciones in vitro, y también determinar el efecto de otros agentes osmóticos en la reducción del crecimiento de papa. Esto subraya la necesidad de realizar estudios más detallados sobre las respuestas fisiológicas específicas de Solanum tuberosum L. a diferentes agentes osmóticos.
Por otro lado, Carmona (27), también reportó que el sorbitol actúa como un agente osmótico que limita la disponibilidad de agua y nutrientes, lo que puede ser beneficioso para la conservación a largo plazo, pero perjudicial si se aplica en exceso. En su investigación sobre ñame, se encontró que una concentración moderada de sorbitol favoreció la supervivencia y recuperación de explantes, mientras que niveles más altos llevaron a un crecimiento deficiente.
En el contexto del uso combinado de manitol y otros inhibidores del crecimiento, se coincide con Chourasia et al. (28), quienes documentaron que la adición de manitol al 2% en medios MS resultó en un crecimiento controlado y una alta tasa de supervivencia para clones de boniato conservados durante largos periodos. Este hallazgo refuerza la idea de que las concentraciones adecuadas de osmorreguladores son cruciales para optimizar las condiciones in vitro y asegurar la viabilidad del material vegetal.
De manera similar, dos Santos et al. (29), compararon el efecto de diferentes osmorreguladores e inhibidores de crecimiento en la conservación in vitro de la caña de azúcar. Sus hallazgos indicaron que tanto el manitol como el sorbitol tienen un efecto positivo a bajas concentraciones, pero a niveles más altos, estos compuestos pueden inhibir el crecimiento y afectar negativamente la viabilidad de los explantes. Este trabajo subraya la necesidad de un enfoque equilibrado en la aplicación de osmorreguladores para maximizar los beneficios en cultivos in vitro.
En correspondencia, un estudio realizado por Bello et al. (30), también corroboró estos hallazgos al observar que el uso de manitol y sorbitol como osmorreguladores influye significativamente en la supervivencia y desarrollo de plantas in vitro, destacando que las concentraciones adecuadas son cruciales para evitar efectos adversos en el crecimiento. La investigación sugiere que un manejo cuidadoso de estos compuestos puede prolongar los períodos de subcultivo y mejorar la conservación efectiva.
En esta misma línea de hallazgos, De Guglielmo et al. (31), plantean que la interacción negativa observada en combinaciones altas sugiere que el uso simultáneo de manitol y sorbitol debe ser cuidadosamente calibrado y que las mezclas desbalanceadas de reguladores y agentes osmóticos pueden generar estrés acumulativo, afectando negativamente el desarrollo de los explantes. Sin embargo, en concentraciones moderadas, podrían tener un efecto sinérgico positivo al regular el potencial osmótico sin inducir toxicidad celular.
Estos estudios en conjunto refuerzan la idea de que los efectos del sorbitol y manitol son altamente dependientes de su concentración, mostrando tanto beneficios como inhibiciones en el crecimiento vegetal, lo cual es fundamental para optimizar las técnicas de cultivo in vitro.
CONCLUSIONES
Los resultados obtenidos en este estudio sobre el efecto de diferentes concentraciones de
sorbitol y manitol en el crecimiento in vitro de Solanum tuberosum L. a los 29, 62 y 93 días revelan patrones claros y significativos. Tanto el sorbitol como el manitol, en concentraciones bajas del 2%, demostraron un efecto osmoprotector, al mejorar moderadamente el crecimiento de los explantes. Esto sugiere que pueden ser utilizados como agentes efectivos en la propagación in vitro, ayudando a mitigar el estrés osmótico de manera controlada.
En contraste, las concentraciones elevadas de sorbitol y manitol al 4% ejercieron un efecto inhibitorio significativo sobre el desarrollo de los explantes. Este resultado confirma que un exceso de agentes osmóticos puede inducir estrés celular, afectando negativamente tanto el metabolismo como el crecimiento.
Asimismo, la combinación de altas concentraciones de sorbitol y manitol generó un efecto sinérgico negativo en el crecimiento, lo que resalta la necesidad de calibrar cuidadosamente las dosis para evitar efectos adversos. Aunque ambos agentes mostraron patrones similares, el manitol tuvo un impacto ligeramente positivo a bajas concentraciones, lo que podría estar relacionado con su capacidad para regular el balance osmótico celular.
Los hallazgos obtenidos pueden contribuir a proporcionar insumos para optimizar protocolos biotecnológicos enfocados en la propagación y conservación de este cultivo de importancia económica, favoreciendo soluciones sostenibles frente a los desafíos climáticos y productivos actuales. Además, estos avances podrían evaluarse en estrategias de mejora genética y conservación ex situ de recursos fitogenéticos valiosos.
CONFLICTO DE INTERESES.
Los autores declaran que no existe conflicto de intereses para la publicación del presente artículo científico.
















