Revista CON-CIENCIA
versión impresa ISSN 2310-0265
Rev.Cs.Farm. y Bioq vol.5 no.1 La Paz jun. 2017
ARTÍCULOS ORIGINALES
Parámetros de calidad de harinas de Amaranthus caudatus Linnaeus (amaranto),
Chenopodium quinoa Willd (quinua), Chenopodium pallidicaule Aellen (kañahua),
Lupinus mutabilis Sweet (tarwi)
Quality parameters of flour of Amaranthus caudatus Linnaeus (amaranth), Chenopodium quinoa Willd (quinoa),
Chenopodium pallidicaule Aellen (kañahua),
Lupinus mutabilis Sweet (tarwi)
MAMANI MAYTA, DEYSI DANITZA1 GUTIERREZ DURÁN, MARÍA DEL PILAR1 SERRUDO JUÁREZ, JORGE ARMANDO1 GONZALES DÁVALOS, EDUARDO1*
* Autor Correspondencia CORRESPONDENCIA: EDUARDO.GONZALEZ@GMAIL.COM
1 Área de Farmacología, Instituto de Investigaciones Fármaco Bioquímicas "Luis Enrique Terrazas Siles". Universidad Mayor de San Andrés, Av. Saavedra 2224. La Paz, Bolivia.
FECHA DE RECEPCIÓN: 19 DE ENERO DE 2017 FECHA DE ACEPTACIÓN: 12 DE ABRIL DE 2017
Resumen
Las especies vegetales Amaranthus caudatus Linnaeus (amaranto), Chenopodium quinoa Willd (quinua), Lupinus mutabilis Sweet (tarwi), Chenopodium pallidicaule Aellen (kañahua), llamados también granos andinos, son desde hace mucho tiempo la base de alimentación de muchas familias en nuestro país, estos granos son reconocidos por su alto valor nutricional. En la actualidad varias empresas de nuestra región comercializan estos granos en su forma procesada. Este trabajo tuvo como finalidad establecer los parámetros de calidad e identificación de las harinas de amaranto, quinua, kañahua y tarwi provenientes de los municipios de Ancoraimes, Tomina, Huancané y Peñas, para ello se realizó el análisis micrográfico encontrándose almidón, aleurona y grasa como principales elementos. El análisis fisicoquímico realizado reportó un contenido de humedad en quinua de 6,03%, cenizas totales 2,52% y 3,8 ml como índice de hinchamiento. En amaranto un contenido de humedad de 5,76%, cenizas totales 2,86% y 6,8 ml como índice de hinchamiento. Tarwi reportó un contenido de humedad de 6,69%, cenizas totales 3,53%, y 3,6 ml como de índice de hinchamiento. Kañahua reportó un contenido de humedad de 5,82%, cenizas totales 3,53% y 4,75ml como índice de hinchamiento. El análisis químico cualitativo en los granos muestra la presencia mayoritaria de flavonoides, aminoácidos, antocianidinas, taninos.
PALABRAS CLAVE
Parámetros de calidad, Amaranthus caudatus, Chenopodium quinoa, Chenopodium pallidicaule, Lupinus mutabilis
Abstract
The plant species Amaranthus caudatus Linnaeus (amaranth), Chenopodium quinoa Willd (quinoa), Lupinus mutabilis Sweet (tarwi), Chenopodium pallidicaule Aellen (kañahua), also called Andean grains, have long been the food base of many families in our Country, these grains are recognized for their high nutritional value. At present several companies of our region commercialize these grains in its processed form. The aim of this work was to establish the parameters of quality and identification of the amaranth, quinoa, kañahua and tarwi flours from the municipalities of Ancoraimes, Tomina, Huancané and Peñas. For this purpose, the micrographic analysis was performed with starch, aleurone and fat as main elements. The physicochemical analysis carried out reported a moisture content in quinoa of 6.03%, total ash 2.52% and 3.8 ml as swelling index. In amaranth a moisture content of 5.76%, total ash 2.86% and 6.8 ml as swelling index. Tarwi reported a moisture content of 6.69%, total ash 3.53%, and 3.6 ml as the index of swelling. Kañahua reported a moisture content of 5.82%, total ash 3.53% and 4.75ml as swelling index. The qualitative chemical analysis in the grains shows the majority presence of flavonoids, amino acids, anthocyanidins, tannins.
KEY WORDS
Quality parameters, Amaranthus caudatus, Chenopodium quinoa, Chenopodium pallidicaule, Lupinus mutabilis.
INTRODUCCIÓN
La quinua es una especie de amplia distribución y diversificación, en Bolivia la región de mayor diversidad y variación genética se encuentra a las orillas del Lago Titicaca (Mújica, 1992), su distribución geográfica se extiende desde los 5° de Latitud norte al sur de Colombia hasta los 43°de latitud sur en la décima región de Chile. Su distribución altitudinal varía desde el nivel del mar en Chile hasta los 4000 m.s.n.m. en el altiplano que comparten Bolivia y Perú existiendo así quinuas de costa, valles, valles interandinos, puna y altiplano (Lescano, 1994). El amaranto también crece en zonas que van desde el nivel del mar hasta los 3000 m.s.n.m., su distribución geográfica en Bolivia es más reducida que la quinua y la kañahua. El tarwi se cultiva aproximadamente desde los 2000 a 3800 m. s n. m. La kañahua crece mayormente en regiones altiplánicas de Bolivia y Perú entre los 3800 y 4300 m.s. n.m. (Jacobsen, 2004).
Los granos andinos por sus características de adaptabilidad ecológica, su alto valor nutritivo, su gran potencial de comercialización en los mercados nacionales e internacionales, tienen gran importancia económica. Un factor principal para su consumo es que se pueden preparar de diferentes maneras y son relativamente económicas comparadas con productos de origen animal, se consideran además alimentos funcionales y con gran potencial agroindustrial. Por ello en la actualidad se están abriendo muchos mercados de consumo nacional, y es notable la cantidad de productos procesados de estos granos que se pueden encontrar para el consumo.
La identificación, recolección, desecación y almacenamiento de estos granos se convierte en un grave problema que afecta a la materia prima. Los problemas principales que afectan la calidad de los productos a partir de la harina de estos granos es la recolección no cualificada, la poca capacidad de estandarización y la gran variabilidad de la materia prima al momento del acopio, ya sea porque no ha sido recogida en la mejor época o porque no ha sido secada convenientemente para permitir un almacenaje correcto. Por ello es que en este trabajo se estableció los parámetros de calidad e identificación de las harinas de amaranto, quinua, kañahua y tarwi provenientes de la producción local de los municipios de Ancoraimes, Tomina, Huancanéy Peñas, para ello se realizó el análisis micro-gráfico, el análisis farmacognóstico y el análisis químico cualitativo.
MATERIAL Y MÉTODOS
Material vegetal
Las especies vegetales se recolectaron de productores locales en Bolivia. A. caudatus, del municipio de Tomina, provincia de Tomina, Chuquisaca (latitud 19 ° 25'53.96S y longitud 64 ° 15'5.44W). C. quinoa de Huancane (latitud 16 ° 18'14.14S y longitud 68 ° 32'35.88W) y C. pallidicaule de la localidad de Peñas (latitud 16 ° 13'55.02S y longitud 68 ° 29'41.70W) municipio de Batallas, Provincia de Los Andes, La Paz. L. mutabilis del municipio de Ancoraimes, provincia de Omasuyos, La Paz (latitud 15 ° 55'19.3S y longitud 68 ° 53'50.1W). Un ejemplar de cada planta, A. caudatus (N° EG-1, Amarantha-ceae), C. quinoa (N° EG-2, Amaranthaceae), C. pallidicaule (N° EG-3, Ama-ranthaceae), L. mutabilis (N° EG-1, Fabaceae) fue identificado y certificado por el Herbario Nacional de Bolivia de la Universidad Mayor de San Andrés y ha sido depositado en el Departamento de Farmacología del Instituto de Investigaciones Farmaco-Bioquímicas, UMSA, La Paz, Bolivia.
Obtención de los extractos
Los granos fueron secados y molidos, empleando 100 g por cada especie vegetal. Este material fue sometido a una extracción por maceración, a temperatura ambiente, con EtOH de 70° durante 48 horas y hasta agotamiento, obteniendo un extracto hidroetanolico que fue concentrado por rota evaporación hasta eliminación completa del solvente.
Análisis micrográfico
El método utilizado fue adecuado al material estudiado (Gutierrez, 2011), se utilizó el método micrográfico estándar que consiste en el tratamiento de la muestra reducida a polvo y examinada al microscopio, utilizando agua e hidrato cloral como aclarantes y fluoroglucina clorhidrica para la coloración de tejido lignificado (coloración rosa). Se prepararon las muestras y se observó al microscopio óptico entre porta y cubreobjetos con gotas de agua, hidrato cloral y fluoroglucina clorhídrica, para diferentes preparaciones, en el microscopio se reconocieron los elementos celulares de interés micrográfico.
Análisis fisicoquímico
Análisis de las características organolépticas
Se analizaron las características organolépticas como olor, color, sabor, condición y textura de la droga pulverizada.
Determinación del contenido de humedad
La determinación del contenido de humedad se realizó por el método directo, se pesó 1g de harina de los granos y se lo transfirió al plato de la balanza de humedad (AND-MX50), donde se registró el porcentaje de humedad.
Determinación de cenizas totales
Para esta determinación se utilizó un horno mufla (WiseTherm FP-03, FHP-03), se emplearon 2g de harina de los granos exactamente pesados en un crisol de porcelana previamente calibrado, la muestra se carbonizó en una cocina y luego se incineró en un horno mufla a 550 °C por dos horas, luego el crisol se enfrió en un desecador y se procedió a pesarlo. El proceso se repitió a partir de la carbonización de la muestra hasta obtener un peso constante, el ensayo se realizó por triplicado.
Índice de hinchamiento en ambas plantas recolectadas
Se llevó 1g de muestra a una probeta con tapón esmerilado, se humedeció la muestra con alcohol, y se añadió 25 ml de agua destilada, se tapó la probeta y se agito cada 10 minutos durante una hora, se dejó en reposo por cuatro horas, se procedió a eliminar la mayor parte del líquido retenido a nivel de la muestra así como las partículas que flotan, finalmente se midió el volumen ocupado por la muestra incluyendo el mucílago.
Análisis químico cualitativo
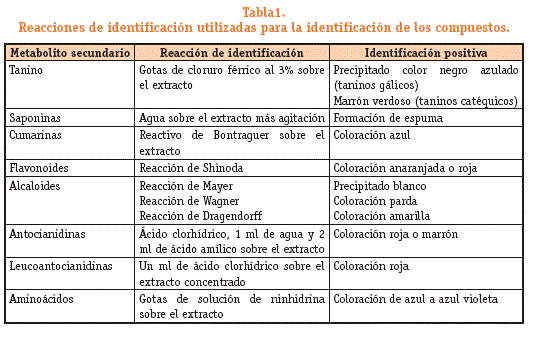
Para la determinación de grupos de compuestos más importantes en el extracto hidro-etanólico se realizó un screeningfitoquímico cualitativo, mediante reacciones colorimétricas y de precipitación en tubos de ensayo (Tabla 1).
RESULTADOS Y DISCUCIÓN
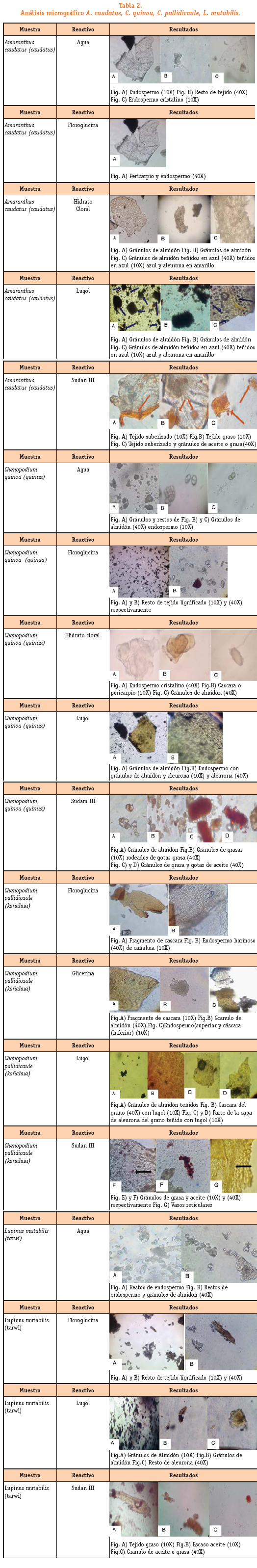
En Amaranthus caudatus se observó la presencia de restos de tejido en-dospermático cristalino y harinoso; gránulos de almidón abundantes, además de aleurona; se evidencio la presencia de tejido graso o aceitoso y tejido su-berizado, los ácidos grasos presentes en amaranto son el ácido palmítico en un 19 %, el oleico en un 26 %, el linoleico en un 47 % y el ácido linolénico en un 1,4 % (Bergery col., 2003). No se encuentra lignina ni tejido lignificado porque se trata de granos (semillas). En Chenopodium pallidicaule se observó tejido del pericarpio y endospermo, con presencia de gránulos de almidón y aleurona, se evidenció la presencia de tejido graso o aceitoso. No se observó tejido lignificado. En Chenopodium quinoa se observaron gránulos de almidón abundantes en restos de tejido endospermático, restos de aleurona, lignina en poca cantidad, tejido graso y gotículas de aceites. En la quinua el hidrato de carbono más importante es el almidón y está presente en un 32 % a 69.2 %, (Ahamed y col., 1998; Ando y col., 2002; Chauhan y col., 1992 a, b; Lin-deboom 2005; Oshodi y col., 1999; Ranhotra y col., 1993). La amilosa (Repo-Carrasco y col., 2003; Wright 2002;), con un alto contenido de D- xilosa y maltosa y bajo contenido de glucosa y fructosa (Ogunbengle, 2003). El contenido de aceite en la quinua varía de 1.8 % a 9.5 %, el ácido linoléico es uno de los más abundantes ácidos grasos poliinsaturados identificados. En Lupinus mutabilis se observaron gránulos de almidón y de aleurona, restos de tejido endospermático, escasa cantidad de tejido lignificado, gotículas de grasa y aceite (Tabla 2). En el tarwi las proteínas y aceites representan más de la mitad del peso de la semilla (Jacobsen y Mujica, 2006).
Una manera de conservar las especies vegetales es eliminar su exceso de humedad, evitando la transformación de sus constituyentes químicos causada por la hidrólisis y el crecimiento de bacterias y hongos en la misma.
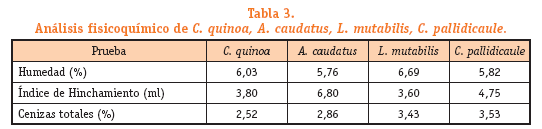
El porcentaje de humedad determinado por el método directo para la especie vegetal C. quinoa es 6,03%, este valor es menor a 10%, y se encuentra dentro del rango establecido para garantizar su estabilidad vegetal (British Pharma-copoea, 2004; Sharapin, 2000) y según la Norma Boliviana (NB 312026-2006) el valor máximo para C. quinoa es de 13,5%. Para la especie vegetal A. caudatus el porcentaje de humedad obtenido fue 5,76%, según la Norma Boliviana (NB 662-1996) el valor referencial debe ser menor o igual al 12%. El porcentaje de humedad para la especie vegetal L. mutabilis es 6,69%, según la Norma Boliviana (NB 074-2000) los valores referenciales son como mínimo 11% y máximo 12%. Para la especie vegetal C. pallidicaule el porcentaje de humedad obtenido fue 5,82%, no se cuentan con valores de referencia.
Las cenizas totales se componen generalmente de fosfatos, carbonatos, sulfatos, sílice y silicatos. La cantidad de ceniza que se obtiene por incineración de muestras vegetales es un indicativo de la calidad de la muestra estudiada y constituye la base para evaluar su pureza, también brinda información acerca de una posible adulteración de la droga con material inorgánico o cuerpos extraños y de su contenido en sales inorgánicas.
El porcentaje de cenizas totales para la especie vegetal C. quinoa fue de 2,52 %, según la Norma Boliviana (NB 312030-2006) el valor máximo para C. quinoa es 3,5%. Para la especie vegetal A. caudatus fue 2,86 %, según la Norma Boliviana (NB 664-1996) el valor referencial debe ser menor o igual al 3,5 %. El porcentaje de cenizas totales para la especie vegetal L. mutabilis fue 3,43 %, el resultado Según la Norma Boliviana (NB 075-2000) el valor máximo es 6 %. Para la especie vegetal C. pallidicaule fue 3,53 %, no se cuenta con valores de referencia.
El índice de hinchamiento indica mayor o menor presencia de cadenas cortas de hidratos de carbono, o una mayor o menor presencia de sólidos solubles en agua, como minerales y vitaminas hidrosolubles. A. caudatus presentaría un mayor índice de absorción de agua y menor solubilidad (Tabla 3).
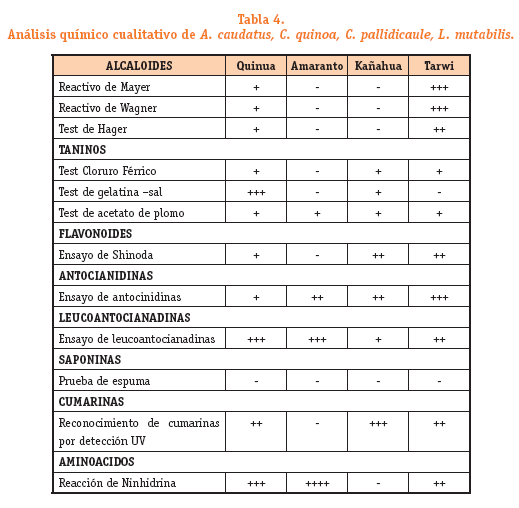
Chenopodium quinoa reporta la presencia de flavonoides, saponinas, terpenos, esteroles, alcaloides, vitaminas y minerales (Kokanova, 2009; Ritva 2008). Mediante los ensayos cualitativos se observó la presencia mayoritaria de taninos, aminoácidos y leucoantocianidinas. Amaranthus caudatus presenta un elevada cantidad de aminoácidos, leucoantocianidinas en mayor concentración. Chenopodium pallidicaule presenta taninos, flavonoides, antocianidinas y cumarinas en mayor concentración. Lupinus mutabilis presenta en mayor concentración alcaloides esto debido a que los granos fueron molidos con su cáscara, también reportó la presencia de taninos, flavonoides, antocianidinas y aminoácidos (Tabla 4). Se resalta la presencia de aminoácidos en los granos estudiados lo que les confiere un elevado valor nutritivo.
CONCLUSIONES
Este trabajo tuvo como finalidad establecer los parámetros de calidad e identificación de las harinas de amaranto, quinua, kañahua y tarwi provenientes de los municipios de Ancoraimes, Tomina, Huancané y Peñas, mediante el análisis micrográfico, análisis fisicoquímico y el análisis químico cualitativo, observándose que los valores determinados se encuentran dentro del rango de aceptabilidad y son aptos para su consumo.
Al proyecto UMSA-IDH "Evaluación de la actividad hipoglicemiante de las especies Amaranthus caudatus (amaranto), Lupinus mutabilis (tarwi) y Linum ussitatisimum (linaza) empleadas en la medicina tradicional boliviana". Al proyecto UMSA/ASDI "Diabetes Tipo II: Nuevas terapias".
BIBLIOGRAFÍA
Ahamed, T., Singhal, R., Kulkarni, P., and Pal, M. 1998. A lesser-known grain, Chenopodium quinoa: Review of the chemical composition of its edible parts. Food Nutr. Bull.19, pp. 61-70. [ Links ]
Ando, H., Chen, Y., Tang, H., Shimizu, M., Watanabe, K., and Miysunaga, T. 2002. Food Components in Fractions of Quinoa Seed.Food Sci. Technol. Res.8(1), 80-84. [ Links ]
Berger, A., Jones, P., and Abumweis, S. 2004. Plant sterols: Factors affecting their effi-cacy and safety as functional food ingredients. Lipids Health Dis. 3, 5. [ Links ]
Bhargava A, Rana TS, Shukla S and Ohri D. 2005. Seed protein electrophoresis of some cultivated and wild species of Chenopodium. Biol Plant; 49:505-511. [ Links ]
Chauhan, G., Eskin, N., Tkachuk, R. 1992a. Nutrients and antinutrients in quinoa seed. Cereal Chem;.69(1), 85-88. [ Links ]
Chauhan, G., Zillman, R., and Eskin, N. 1992b. Dough mixing and breadma-king properties of quinoa-wheat flour blends.Int. J. Food Sci. Technol; 27(6), 701-705. [ Links ]
Gutierrez, M., Limachi, G., Gonzales, E., Bermejo, P., (2011). Control de Calidad del Xanthium spinosum, planta medicinal expendida en la ciudad de La Paz, Boli-via. Biofarbo. (19)1. [ Links ]
Jacobsen, E. and Mujica, A. 2006. El tarwi (Lupinus mutabilis Sweet) y sus parientes silvestres. Universidad Mayor de San Andrés; 458-482. [ Links ]
Jacobsen, S.E. & A. Mujica. 2004. Geogra-fical distribution of the Andean lu-pin (Lupinus mutabilis Sweet). pp. 931-932 En: Jacobsen, S.-E., C.R. Jensen & J.R. Porter (eds.). Book of Proceedings. VIII ESA Congress: European Agricultu-re in a Global Context. KVL, 11-15 July 2004,Copenhagen. [ Links ]
Kokanova Z.; Nedialkov P.; Nikolov S. 2009. "The genus chenopodium: Phyto-chemistry, ethnopharmacology and pharmacology", Pharmacognosy Department, Faculty of Pharmacy, Medical University of Sofia, Dunavstr. 2,1000 Sofia, Bulgaria, Volume 3, Issue: 6, Page: 280-306. [ Links ]
Lescano JL. 1994. Genética y mejoramiento de cultivos altoandinos. Quinua, kañi-hua, tarwi, kiwicha, papa amarga, ollu-co, mashua y oca. Programa Interinstitu-cional de Waru Waru. Puno, Perú. [ Links ]
Lindeboom, N. 2005. Studies on the charac-terization, biosynthesis and isolation of starch and protein from quinoa (Chenopodium quinoaWilld.), University of Saskatchewan Degree of Doctor. [ Links ]
Menchú, MT; Méndez H. 2007. Tabla composición de alimentos de Centroaméri-ca. Guatemala INCAP/OPS. 2a Edición. [ Links ]
Mujica A. 1992. Granos y leguminosas andinas. En: Hernández J, Bermejo J, León J. (editores). Cultivos marginados: otra perspectiva de 1492. Organización de la Naciones Unidas para la Agricultura y la Alimentación FAO, Roma. pp. 129-146. [ Links ]
Ogunbengle HN. 2003. Nutritional evalua-tion and functional properties of quinoa (Chenopodium quinoa) flour. IntJ Food Sci Nutr; 54:153-158. [ Links ]
Oshodi, A., Ogungbenle, H., and Oladimeji, M. 1999. Chemical composition, nutri-tionally valuable minerals and functional properties of benniseed, pearl millet and quinoa flours. Int. J. Food Sci. Nutr; 50,325-331. [ Links ]
Ramírez, E. 2002. Proyecto de Inversión para la Industrialización y Comercialización del Grano de Amaranto en Diversos Productos en Huajuapan de León Oaxa- [ Links ]
Ranhotra,G., Gelroth, J., Glaser, B., Lorenz, K., and Johnson, D.1993. Composition and protein nutritional quality of qui-noa.Cereal Chem; 70(3), 303-305. [ Links ]
Repo-Carrasco R, Espinoza C and Jacob-sen SE. 2003, Nutritional value and use of the Andean crops quinoa (Chenopo-dium quinoa) andka" niwa (Chenopo-dium pallidicaule). Food Rev Int 19:179-189. [ Links ]
Ritva. R.; Encina C. 2008. "Determinación de la capacidad antioxidante y compuestos fenólicos de cereales andinos: quinua (Chenopodiumquinoa), de kañiwa (Chenopodiumpallidicaule) y kiwicha (Amaranthuscaudatus)", Revista de la sociedad quimica del Peru, Lima Peru, V 74 N°2, p. 85-99. [ Links ]
Wright KH, Pike OA, Fairbanks DJ and Huber SC, 2002. Composition of Atriplex hortensis, sweet and bitter Chenopo-dium quinoa seeds. Food Chem Toxicol; 67:1383-1385. [ Links ]












 uBio
uBio