Introducción
La producción de cacao (Theobroma cacao L.) como parte de los sistemas agroforestales, es una actividad cada vez más creciente en la región amazónica de La Paz, Bolivia. El cacao es un importante cultivo económico de la Amazonía boliviana, los productores bolivianos cultivan cacao y extraen frutos de rodales silvestres en la región del río Beni y valles de las estribaciones de los Andes, y el grupo de germoplasma tradicionalmente utilizado ahora se denomina Cacao Nacional Boliviano (CNB), Alto Beni en el departamento de La Paz, desde los años 60 desarrolló el cultivo hasta convertirse en la región con mayor capacidad de producción de cacao en Bolivia, albergando al mayor número de productores y hectáreas cultivadas, así como la cooperativa más importante, El Ceibo1,2.
El cacao (T. cacao) es originario de las regiones selváticas de América tropical, desde Perú hasta México, siendo su principal uso la producción de chocolate, seguido de otros usos como los cosméticos y materia prima3. Destaca su cultivo en regiones tropicales y su rendimiento se ve afectado por varias enfermedades como la pudrición de la vaina negra (o mazorca negra), su control podría lograrse si se establecen estrategias de manejo integrado, con la combinación de métodos biológicos y químicos, control genético y métodos de cultivo en un programa integrado4.
Los criterios de selección para el CNB fueron descritos en Alto Beni-Bolivia, y enfatizan que Bolivia es uno de los pocos países con cacao en estado silvestre y se posiciona entre los principales poseedores de cacao fino y aromático del mundo, sin embargo, a pesar de que su existencia es conocida y cultivada desde hace más de 200 años, no hay suficiente información disponible para iniciar un programa de selección de individuos destacados5. Se realizaron estudios sobre la variabilidad genética de CNB, indicando que el cacao silvestre es conocido por varios nombres: "cacao criollo", "cacao nacional boliviano", "cacao amazónico", "cacao silvestre" y "cacao". El cacao silvestre tiene varias ventajas: es un producto no perecedero que se puede cosechar, fermentar y secar en áreas distantes de los mercados, tiene una gran adaptabilidad a las ecorregiones y se puede producir incluso en largos períodos de inundación2,6. Sin embargo, el período de desarrollo de las plántulas en el vivero es más largo que el de los otros tipos de cacao, lo que dificulta el aumento de la producción.
Para obtener rendimientos óptimos, se requiere un manejo de este cultivo, como la obtención de portainjertos de calidad, que también pueden proporcionar cierta tolerancia al ataque de hongos u otros patógenos7. El uso de portainjertos, obtenidos a partir de semillas botánicas, permite reducir los costos de producción, las características descritas para el cacao foráneo, CNB e IMC-67 sugieren un amplio potencial para su producción como portainjertos en la región. Sin embargo, es necesario optimizar las condiciones de producción durante la fase de vivero, para maximizar su desarrollo y productividad. Dada la relevancia de este cultivo para el país y la creciente demanda de prácticas agrícolas sostenibles2, el uso de microorganismos beneficiosos como Trichoderma se presenta como una alternativa prometedora para mejorar la productividad y la salud de los cultivos, reduciendo la dependencia de agroquímicos8.
En cuanto a Trichoderma, se destacan sus características como mecanismo de acción como agente de biocontrol, para mitigar el ataque de fitopatógenos, como alternativa a los plaguicidas sintéticos, junto con otros beneficios conferidos por el desarrollo de los cultivos a través de su interacción simbiótica con las plantas y efectos biorremediales en campos contaminados8. También se añade que los agentes de biocontrol ideales como Trichoderma tienen cualidades como la producción de antibióticos, enzimas líticas que degradan las paredes celulares de los patógenos vegetales o la inducción de una respuesta de defensa en las plantas9.
Diferentes estudios verificaron las cualidades de Trichoderma en condiciones de vivero para la producción de plántulas, como la evaluación de 15 cepas endófitas para caracterizar su influencia en la inoculación de plántulas en el establecimiento del crecimiento endófito en plántulas de cacao10. También se verificaron los efectos de la colonización endófita de T. hamatum (DIS 219b) con o sin exposición a condiciones de sequía, obteniendo como efectos un aumento en el peso de las raíces frescas, el peso seco de las raíces y el contenido de agua de las raíces en las plántulas de cacao11. Otros autores evaluaron el efecto de diferentes manejos agroecológicos sobre el crecimiento de plántulas en la fase de vivero, como T. harzianum combinado con lixiviados de raquis de banano, vermicompost, Beauveria, entre otros12. También se evaluó el efecto de Trichoderma sp. sobre las características agronómicas de los ecotipos de T. cacao en condiciones de vivero, comparando tratamientos basados en T. harzianum + CCN51 y T. afroharzianum + TSHS565 con colonización del 100 % de pelos radiculares y tricomas en tallos13. Trichoderma se presenta como una alternativa para la producción orgánica de cacao, mejorando las características agronómicas del cultivo en condiciones de vivero.
En la actualidad, existe poca información sobre alternativas para mejorar la producción de portainjertos CNB, cuyas características organolépticas y de resistencia son deseables para la producción de cacao6. Además, existe la necesidad de promover la producción de plántulas de T. cacao con el uso de insumos orgánicos, ya que la certificación orgánica es un requisito para muchos mercados, para mejorar la valoración y el precio de un producto como el cacao de la zona de los Yungas2. Así, esta investigación tuvo como objetivo evaluar el efecto de la aplicación de T. harzianum con diferentes dosis (0, 80, 100 y 120 %), comparando 2 tipos de portainjertos de plántulas de cacao, CNB e IMC-67.
Materiales y métodos
Ubicación geográfica. El estudio se realizó en el vivero de la Estación Experimental Sapecho (EES), dependiente de la Facultad de Agronomía de la Universidad Mayor de San Andrés (UMSA), ubicado en la cuarta sección municipal de Palos Blancos, Provincia Sud Yungas del departamento de La Paz, Bolivia. La EES se encuentra ubicada entre las coordenadas 15º 32’ 54.4” de latitud sur, 67º 19’ 47.8” de longitud oeste, a una altitud promedio de 450 msnm, temperatura de media de 26º C y una precipitación media de 1800 mm año-1 y a una distancia de 260 km de la ciudad de La Paz. Se señala que la única colección de CNB que se tiene hasta el momento en el país, se encuentra resguardada en la EES5. El período de evaluación fue de mayo a agosto del 2021, en un vivero cubierto con malla de polietileno de semisombra sarán del 50 %.
Métodos. Como material biológico se tuvo semillas de CNB y cacao foráneo IMC-67 y T. harzianum obtenidas del laboratorio de Fitopatología de la Facultad de Agronomía de la UMSA. Las semillas fueron obtenidas de mazorcas colectadas en parcelas de la EES y posteriormente se empleó el método de preparación empleado por el personal de la EES, para el retirado el mucílago, mediante acción mecánica empleando aserrín. Luego fueron colocadas en una cama pre germinadora, con un sustrato compuesto por arena fina y aserrín, distanciadas entre sí por 2 cm. Se realizó un riego regular para garantizar una emergencia uniforme.
Preparación del sustrato. Se realizó el llenado de las macetas en bolsas negras de polietileno (11*27 cm) con una mezcla de sustrato: 50 % tierra del lugar, 30 % arena corriente, 20 % abono bocashi y 10 % de aserrín descompuesto obtenido mediante el humedecimiento por una semana. Asimismo, se colectó 1 kg de muestra del sustrato para su posterior envío y análisis en el Laboratorio de Suelos y Aguas de la Facultad de Agronomía (LAFASA) para conocer las características fisicoquímicas del suelo. Los resultados obtenidos correspondieron a una textura franco limoso, contenido de nitrógeno 0.35 %, materia orgánica 5.77 %, carbono orgánico 3.35 %, fósforo disponible 41.60 ppm, potasio intercambiable 1.90 mEq 100 g-1, magnesio intercambiable 3.14 mEq 100 g-1, acidez intercambiable (Al + H) 0.44 mEq 100 g-1, conductividad eléctrica en H2O 1:5 0.67 mmho cm-1, pH en H2O relación 1:5 6.1 ligeramente ácido.
Inoculación y aplicación de T. harzianum. La preparación de las concentraciones se realizó con base al procedimiento utilizado y recomendado por Cadena et al.14, que, para una mochila de 20 L, utiliza 200 g (peso fresco) o 68 g (peso seco) del hongo, lo que representa el 100 % de concentración. Para el presente estudio se preparó una solución de 3.6 L para 120 plantines o macetas (30 mL por maceta) para cada aplicación. La solución tuvo como componentes agua y té de estiércol al 20 %. En la primera aplicación fue el doble de las cantidades calculadas de T. harzianum (10.88, 13.6, 16.32 g), 15 días antes de la siembra de la semilla, con el objetivo de coadyuvar en el desarrollo del hongo14. Posteriormente se aplicó cada 15 días después de la siembra a cada tratamiento establecido, hasta la etapa de injerto de plantines de cacao, que en vivero se realiza cuando se alcanza un diámetro recomendado de 4 a 5 mm de diámetro15, y 5 mm es el diámetro empleado de forma tradicional en la región para esta etapa.
Labores culturales. Se efectuó el riego en función a la demanda del cultivo y la precipitación, junto al “destetado” de los plantines, práctica que consiste en el retiro de la testa de la semilla. Asimismo, se realizó el control fitosanitario mediante el control manual, retirando hojas dañadas, control de malezas y limpieza, junto al uso de insumos caseros como el piretro (dosis de 1 mL por cada 2 L de agua), para repeler insectos.
Tratamientos. Se establecieron 8 tratamientos en un diseño completamente al azar (DCA) con arreglo bifactorial y 3 réplicas cada uno, siendo el Factor 1: dosis de aplicación T. harzianum (0, 80, 100 y 120 %) y el Factor 2 tipo de patrones: CNB y cacao foráneo (IMC-67). Obteniendo un total de 24 unidades experimentales (UE) con 10 plantas cada una, haciendo un total de 240 plántulas de portainjertos de cacao, como se detalla en la Tabla 1.
Tabla 1 Tratamientos y descripción
| Tratamientos | Descripción |
|---|---|
| T1 | CNB y sustrato sin aplicación de T. harzianum (0 %) |
| T2 | CNB y dosis 80 % |
| T3 | CNB y dosis 100 % |
| T4 | CNB y dosis 120 % |
| T5 | IMC-67 y sustrato sin aplicación de T. harzianum (0 %) |
| T6 | IMC-67 y dosis 80 % |
| T7 | IMC-67 y dosis 100 % |
| T8 | IMC-67 y dosis 120 % |
Variables de estudio. Se evaluaron cada 15 días, altura cm (AP), medida desde la base de la planta hasta la yema apical en el vástago principal de la planta, diámetro de tallo mm (DT), medido con un vernier digital en la base de la corona radicular y número de hojas (NH), cuantificado por cada planta. Se registró un total de 7 evaluaciones en un total de 105 días. El área foliar se determinó mediante modelos estadísticos (ecuaciones de regresión lineales) para estimar el área foliar16.
Análisis estadístico. Se realizó mediante un análisis de varianza y la prueba de comparación de medias por Duncan al 5 % de significancia, utilizando el programa InfoStat para verificar las diferencias entre los tratamientos.
Resultados
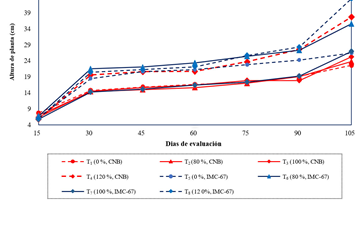
Altura de planta (cm). Figura 1, el incremento, en los diferentes tratamientos para un período de 105 días. Se observa T4 (120 %, CNB), T8 (120 %, IMC 67) y T6 (80 %, IMC 67) alcanzaron mayores alturas promedio en comparación a los demás tratamientos. Las menores alturas correspondieron, al CNB con dosis menores a 120 %.
Tabla 2 Análisis de varianza para la Altura de planta (cm) evaluada cada 15 días para los ocho tratamientos y prueba de comparación de medias mediante Duncan
| Evaluaciones de altura de planta (cm) cada 15 días | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Tratamiento | Dosis (%) | Patrón | 15 | 30 | 45 | 60 | 75 | 90 | 105 |
| T1 | 0 | CNB | 7.58a | 14.14d | 15.16c | 15.92d | 16.53c | 18.31c | 21.54e |
| T2 | 80 | CNB | 6.88ab | 13.83d | 14.43c | 15.03d | 16.32c | 18.23c | 22.67de |
| T3 | 100 | CNB | 6.30ab | 13.97d | 15.00c | 15.75d | 17.07c | 17.07c | 24.04cde |
| T4 | 120 | CNB | 5.72b | 18.65bc | 19.62b | 19.72c | 22.53ab | 26.15a | 35.68b |
| T5 | 0 | IMC-67 | 6.22ab | 17.68c | 19.72b | 20.30bc | 21.74b | 23.11b | 25.17cd |
| T6 | 80 | IMC-67 | 6.64ab | 20.48a | 21.01a | 22.25a | 24.17a | 25.94a | 33.70b |
| T7 | 100 | IMC-67 | 5.70b | 13.68d | 14.51c | 15.72d | 16.62c | 18.40c | 25.64c |
| T8 | 120 | IMC-67 | 6.03ab | 19.49ab | 20.27ab | 21.10b | 24.43a | 26.90a | 41.14a |
| P-valor. Dosis | .1219-ns | .0001** | .0001** | .0001** | .0001** | .0001** | .0001** | ||
| P-valor. Portainjerto | .1936-ns | .0001** | .0001** | .0001** | .0001** | .0001** | .0001** | ||
| P-valor. Portainjerto*Dosis | .1219-ns | .0001** | .0001** | .0001** | .0001** | .0002** | .0005** | ||
| Valor: R2 | .42 | .92 | .97 | .98 | .93 | .95 | .97 | ||
| C.V. (%) | 13.32 | 5.95 | 3.63 | 2.63 | 5.53 | 5.08 | 5.34 | ||
CV Coeficiente de variación, * significativo, ** altamente significativo, NS no significativo, CNB cacao nacional boliviano, IMC-67 cacao foráneo, Letras iguales indican que igualdad a un 5 % de significancia.
Tabla 2, a partir de los 30 días de evaluación, se obtuvieron diferencias altamente significativas (p˂0.01) para la variable AP para ambos factores de estudio y su interacción, con un coeficiente de determinación (R2) igual a 0.97. Destaca que, a los 105 días, la mayor AP fue para T8 (120 %, IMC 67) con 41.14 cm, que se distingue de los demás tratamientos. La segunda AP fue para T4 (120 %, CNB) con 35.68 cm y T6 (80 %, IMC67) con 33.70 cm, que no se diferencian estadísticamente entre sí. Para el CNB, todos los tratamientos obtuvieron alturas menores, con excepción del T4, al que se le aplicó una dosis de Trichoderma del 120 %.
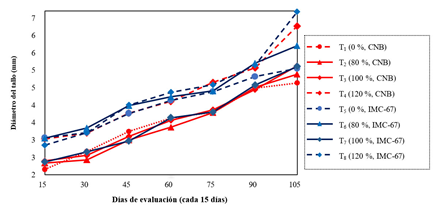
Diámetro del tallo (mm). Los patrones del tipo IMC 67 tuvieron una tendencia de incremento mayor en comparación a los portainjertos del tipo CNB, con excepción T4 (120 %, CNB) que presentó un aumento del DT similar al T8 (120 %, IMC 67) (Figura 2).
Tabla 3 Análisis de varianza para diámetro de planta (mm) evaluado cada 15 días para los ocho tratamientos y prueba de comparación de medias mediante Duncan
| Evaluaciones de diámetro de tallo (mm) cada 15 días | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Tratamiento | Dosis (%) | Patrón | 15 | 30 | 45 | 60 | 75 | 90 | 105 |
| T1 | 0 | CNB | 2.45b | 2.97b | 3.54b | 3.93b | 4.09b | 4.79 | 4.93e |
| T2 | 80 | CNB | 2.63b | 2.72b | 3.29b | 3.66b | 4.08b | 4.81 | 5.18de |
| T3 | 100 | CNB | 2.69b | 2.85b | 3.39b | 3.86b | 4.16b | 4.74 | 5.42d |
| T4 | 120 | CNB | 3.33a | 3.50a | 4.07a | 4.41a | 4.95a | 5.37 | 6.57b |
| T5 | 0 | IMC-67 | 3.36a | 3.51a | 4.06a | 4.43a | 4.68a | 5.11 | 5.35d |
| T6 | 80 | IMC-67 | 3.34a | 3.63a | 4.28a | 4.53a | 4.70a | 5.50 | 6.00c |
| T7 | 100 | IMC-67 | 2.67b | 2.95b | 3.27b | 3.93b | 4.10b | 4.88 | 5.41d |
| T8 | 120 | IMC-67 | 3.14a | 3.50a | 4.30a | 4.66a | 4.88a | 5.45 | 6.98a |
| P-valor Dosis | .0006** | .0031** | .0007** | .0001** | .0001** | .0069** | .0001** | ||
| P-valor Porta injerto | .0002** | .0006** | .0024** | .0001** | .0010** | .0119* | .0001** | ||
| P-valor Porta injerto*Dosis | .0001** | .0118* | .0182* | .0094** | .0014** | .2196-ns | .0163* | ||
| Valor: R2 | .85 | .77 | .78 | .85 | .88 | .66 | .95 | ||
| C.V. (%) | 6.06 | 7.06 | 7.24 | 4.32 | 3.66 | 5.18 | 3.4 | ||
CV: Coeficiente de variación, * significativo, ** altamente significativo, NS no significativo, CNB cacao nacional boliviano, IMC-67 cacao foráneo, Letras iguales indican que existe una igualdad a un 5% de significancia.
Tabla 3, se obtuvieron diferencias altamente significativas (p˂0.01) para ambos factores (Tipo de patrón y dosis), atribuyendo el efecto de Trichoderma en cada etapa evaluada, junto a la interacción de ambos factores, con un promedio de 6.98 mm, en cacao foráneo y CNB con 6.57 mm, correspondientes a la dosis 120 % a los 105 días. T4 (120 %, CNB), T5 (0 %, IMC 67), T6 (80 %, IMC 67) y T8 (120 %, IMC 67) alcanzaron diámetros superiores a los 5 mm a los 90 días de evaluación (Tabla 3), además, no se observa diferencias entre el T4 y el T8 a los 90 días, mientras que, a los 105 días, el T8 difiere de los demás tratamientos seguido del T4.
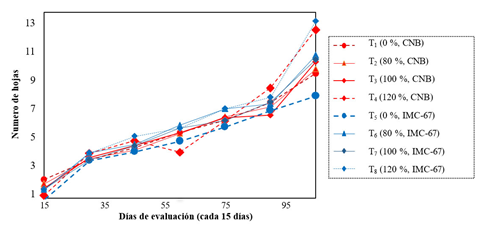
Como se verifica, Figura 3, existe una proximidad entre el NH del CNB y el IMC-67 para la dosis más alta de Trichoderma (120 %). Mientras que las dosis menores presentaron menores promedios para el NH en ambos tipos de portainjertos, verificándose que el factor dosis incurre en diferencias significativas a los 105 días (Tabla 4).
Tabla 4 Análisis de varianza para Número de hojas, evaluado cada 15 días para los ocho tratamientos y prueba de comparación de medias mediante Duncan
| Evaluaciones de número de hojas cada 15 días | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Tratamiento | Dosis (%) | Porta injerto | 15 | 30 | 45 | 60 | 75 | 90 | 105 |
| T1 | 0 | CNB | 2.30a | 3.67 | 4.52 | 5.58 | 6.46 | 7.69 | 9.72 |
| T2 | 80 | CNB | 2.00ab | 3.77 | 4.37 | 5.53 | 6.70 | 7.40 | 10.03 |
| T3 | 100 | CNB | 1.67abc | 3.83 | 4.67 | 5.57 | 6.63 | 6.80 | 10.54 |
| T4 | 120 | CNB | 1.17cd | 4.13 | 5.00 | 4.20 | 6.40 | 8.70 | 12.77 |
| T5 | 0 | IMC-67 | 0.89d | 3.63 | 4.25 | 5.00 | 5.99 | 7.13 | 8.15 |
| T6 | 80 | IMC-67 | 1.60bc | 4.17 | 4.76 | 6.10 | 7.24 | 7.59 | 10.99 |
| T7 | 100 | IMC-67 | 1.63abc | 3.67 | 4.67 | 5.90 | 6.43 | 7.73 | 10.70 |
| T8 | 120 | IMC-67 | 1.57bc | 4.17 | 5.33 | 5.90 | 7.27 | 8.07 | 13.40 |
| P-valor Dosis | .2596-ns | .0401-* | .1585-ns | .2009-ns | .3391-ns | .0586-ns | .0001-** | ||
| P-valor Portainjerto | .0268-* | .6324-ns | .6417-ns | .0877-ns | .5463-ns | .9534-ns | .9135-ns | ||
| P-valor Portainjerto*Dosis | .0036-** | .4067-ns | .7427-ns | .0700-ns | .3954-ns | .2250-ns | .1608-ns | ||
| Valor: R2 | .66 | .46 | .32 | .52 | .31 | .47 | .79 | ||
| C.V. (%) | 22.64 | 7.55 | 12.43 | 12.44 | 11.18 | 9.26 | 9.14 | ||
CV Coeficiente de variación, * significativo, ** altamente significativo, NS no significativo, CNB cacao nacional boliviano, IMC-67 cacao foráneo, Letras iguales indican que igualdad a un 5 % de significancia.
Para el NH, el análisis de varianza (Tabla 4) muestra diferencias estadísticas (p˂0.01) para el factor dosis de T. harzianum, y no así para el factor portainjerto y la interacción (p˃0.05). A los 105 días, la dosis de 120 % influyó en un mayor NH por planta para ambos tipos de cacao, siendo el promedio igual a 13.4 para IMC-67 y 12.77 para el CNB, no difieren estadísticamente entre sí, pero sí difieren de los otros tratamientos.
De acuerdo con el análisis de varianza para la variable área foliar (Tabla 5), se contó con diferencias altamente significativas para el factor dosis y la interacción (p˂0.01). Los mayores valores correspondieron para la dosis de 120 % en ambos tipos de cacao (85.05 cm2 IMC-67 y 78.82 cm2 CNB).
Tabla 5 Análisis de varianza para la variable área foliar (cm2) a los 105 días de evaluación
| Tratamiento | Dosis (%) | Porta injerto | Área foliar de la hoja (cm2) |
|---|---|---|---|
| T1 | 0 | CNB | 59.01de |
| T2 | 80 | CNB | 64.93cd |
| T3 | 100 | CNB | 69.80bcd |
| T4 | 120 | CNB | 78.82ab |
| T5 | 0 | IMC-67 | 63.23d |
| T6 | 80 | IMC-67 | 76.85abc |
| T7 | 100 | IMC-67 | 47.84e |
| T8 | 120 | IMC-67 | 85.05a |
| P-valor Dosis | .0001-** | ||
| P-valor Porta injerto | .9712-ns | ||
| P-valor Portainjerto*Dosis | .0027-** | ||
| Valor: R2 | .8 | ||
| C.V. (%) | 10.02 | ||
CV Coeficiente de variación, * significativo, ** altamente significativo, NS no significativo, CNB cacao nacional boliviano, IMC-67 cacao foráneo, Letras iguales indican que igualdad a un 5 % de significancia.
Discusión
Las diferencias en la AP entre el CNB y el IMC 67 pueden explicarse por las diferencias que distinguen el CNB de otros genotipos, dado que se encuentra en condiciones silvestres y en cultivo con diferentes grados de cruzamiento con materiales introducidos6. Sin embargo, con la aplicación de Trichoderma, el CNB tuvo un incremento en altura similar al IMC 67 para la dosis de 120 %. El T8 tuvo un índice de desarrollo promedio de 0.34 cm día-1 que superó al obtenido por Gamboa Tabares et al.17 que fue 0.2 cm día-1 para el crecimiento del mismo clon (IMC 67), verificando que este hongo también se encuentra asociado con un aumento en la eficiencia de las actividades fotosintéticas y respiratorias que indirectamente ayudan a la planta a crecer y desarrollarse18. La frecuencia de aplicación puede tener un efecto significativo, dado que la aplicación de T. harzianum en semillero y 15 días después de su siembra estimula el crecimiento en plantines, como el caso del cultivo de tomate19.
Al comparar diferentes abonos orgánicos en la producción de plantines de cacao, se obtuvo AP en un rango de 30.7 a 39.1 cm, sin embargo, estos fueron obtenidos hasta los 138 días20, se observó alturas entre 28.93 y 33.43 cm para el portainjerto ICS 6 a los 90 días, que difieren de las obtenidas en este estudio, y pueden explicarse por la diferencia entre genotipos21. Asimismo, una evaluación de varias cepas de Trichoderma, tuvo promedios de 29.83, 27.73 y 23.60 cm para T. harzianum con los clones CCN 51, TSH 565 y nativo fino de aroma, a los 90 días después de la siembra en Perú13, confirmando que el cacao nativo puede presentar un desarrollo más lento a comparación de otros genotipos. Sin embargo, el efecto de Trichoderma podría estar relacionado con el genotipo o la especie, T. harzianum incrementó AP, NH y biomasa seca del área foliar en plántulas de Cedrela odorata, mientras que en Leucaena leucocephala y Albizia saman solo provocó incrementos del diámetro basal22. Debido a que el hongo no tuvo un efecto considerable en el cacao nativo, contrario a los resultados de este estudio, T. harzianum ocasionó un incremento en la AP para el CBN13. T. longibrachiatum puede promover un crecimiento de (planta o altura ≥13 %)23.
A los 138 días de evaluación obtuvo diámetros entre 6.62 (gallinaza) y 6.86 (tierra + bocashi 2-1) mm, mediante la aplicación de diferentes abonos orgánicos en la producción de plantines del clon IMC 67, sin obtener diferencias estadísticas significativas20. Por lo que se observa que, con la aplicación de Trichoderma, es posible obtener el DT para la injertación en menores períodos de tiempo para ambos genotipos. Por otro lado, el portainjerto ICS 6 durante un período de evaluación de 3 meses, obtuvo DT entre 5.79 y 6.21 mm, valores mayores a los obtenidos en la presente investigación21. Estas diferencias pueden estar relacionadas a las características propias del portainjerto ICS 6 y al tipo de sustrato empleado. A 90 días los DT de 4.4, 3.77 y 4.25 mm, con aplicación de T. harzianum, destacando que, para un tipo de cacao nativo de Perú, el DT obtenido (4.4 mm) superó a los otros portainjertos13. Mayores DT a los 135 días, entre 7.22 y 8.16 mm mediante la aplicación de abonos líquidos a base de T. harzianum, superaron al tratamiento con aplicación de un fertilizante convencional (4.59 mm)12. Por otro lado, el factor determinante es el genotipo del portainjerto utilizado, obteniendo un DT de 4.58 mm para el IMC-67 a los 90 días de cultivo, mientras que el obtenido en este estudio fue 5.45 mm17. Sobre esta diferencia, puede atribuirse al empleo del hongo Trichoderma en el crecimiento, por sus beneficios como estimulante de defensas y promotor del crecimiento de las plántulas24,25. Su efecto como biocontrol puede actuar promoviendo el desarrollo de la planta, colonizando el suelo y/o parte de la planta y evitando la multiplicación de patógenos26, considerando que no se contó con presencia de enfermedades durante el período de evaluación. Muchas especies de este género pueden producir la auxina ácido indol-3-acético, que se ha sugerido que promueve el crecimiento de raíces, no obstante, los mecanismos y moléculas implicadas en la promoción del crecimiento son multivariables y se ven afectados por las condiciones ambientales27.
Para la variable NH, se obtuvo promedios mayores, que en un período mayor de evaluación obtuvo como mayor promedio 11.5 hojas por planta que no obtuvo diferencias significativas y evaluó un promedio de 11.4 hojas para un sustrato con tierra del lugar + bocashi20,21. A los 90 días, se registraron promedios mayores (9.67; 10.0 y 8.33 hojas por planta) al comparar los valores de este estudio, con excepción del T4 (120 %, CNB) que alcanzó 8.7 hojas13. Los mismos autores concluyen que la aplicación de Trichoderma en ecotipos de cacao presentaron efectos con características agronómicas ideales, y que el ecotipo nativo de aroma fino con mejores resultados en cuanto al NH, añadiendo que el T. harzianum + CCN 51 obtuvo 100 % de colonización en los pelos radiculares. A los 135 días, también registraron mayores promedios (19 a 20 hojas por planta) al aplicar productos a base de Trichoderma12. Por lo que la aplicación de Trichoderma con la mayor dosis si influye en un mayor número de hojas y, por tanto, en una mayor actividad fotosintética28. En cuanto al uso de bioestimulantes o plantas inoculadas con Trichoderma, también generan efectos positivos en el número de hojas en el cultivo de maracuyá y tomate en ambiente protegido29-31.
También, estudios respaldan que Trichoderma sp. mejora notablemente el crecimiento y desarrollo, influyendo en el área foliar32,33. Para las variables biomasa total y aérea, la combinación de T. harzianum y compost en plántulas de pino permite mayores y homogeneidad de valores si se comparan con un testigo34, considerando que el abono ofrece mejores condiciones para el desarrollo del hongo.
El efecto de Trichoderma spp. como promotor de crecimiento, se debe a que aumenta la superficie total del sistema radicular-posibilitando un mayor acceso a los elementos minerales presentes o a que son capaces de solubilizar e incrementar la disponibilidad de fosfatos, hierro, cobre, manganeso y zinc, u otros elementos, así como aumentar la eficiencia de la planta para utilizar algunos nutrientes como el nitrógeno35. Asimismo, las especies de Trichoderma son ampliamente conocidas como promotoras de crecimiento, y que este rasgo es más específico del aislado que de la especie, con aislados individuales que muestran diversos grados de especificidad vegetal25. También indican que los mecanismos de promoción del crecimiento incluyen el control de patógenos, mejoras en la absorción de nutrientes, aumento del metabolismo de carbohidratos y fotosíntesis, además de la síntesis de fitohormonas.
Los resultados obtenidos señalan un incremento de la AP, DT, NH y área foliar con relación a los testigos en los genotipos CNB e IMC 67 con la aplicación de T. harzianum a una dosis de 120 %, apoyan como alternativa que puede coadyuvar a un mayor aprovechamiento del potencial genético del CNB, mejorando las condiciones de su propagación en condiciones de vivero. También se destaca que el CNB, caracterizado por presentar un crecimiento lento para la obtención de plantines a comparación de plantines híbridos, obtuvo características de crecimiento similares al híbrido IMC 67, con la aplicación de Trichoderma.











 texto en
texto en 
 uBio
uBio