Introducción
Oryza sativa, un alimento esencial para más de la mitad de la población global, en Ecuador, se cultivan alrededor de 308211 ha, con una producción 1,546 523 t, un rendimiento promedio de 5.05 t ha-1. En la provincia de Los Ríos, se siembran cerca de 79379 ha, produciendo 358501 t con un rendimiento promedio de (4.52 t ha-1)1.
A nivel mundial, el cultivo de arroz enfrenta importantes desafíos fitosanitarios debido a la incidencia de agentes bióticos como bacterias, hongos, virus, espiroplasmas, micoplasmas, nemátodos y protozoarios. Estos patógenos, afectan de manera significativa el desarrollo del cultivo, provocando pérdidas considerables en su rendimiento, reduciendo la rentabilidad de los productores que dependen económicamente de esta gramínea como fuente principal de sustento2. Estudios realizados en Asia tropical, evidenciaron que la disminución del rendimiento varía según el tipo de enfermedad, en casos individuales, las pérdidas oscilan entre 1 y 10 %, mientras que la interacción simultánea de múltiples enfermedades, insectos y malezas pueden generar pérdidas promedio del 37.2 %, alcanzando hasta un 41 % en condiciones severas, dependiendo de la composición del sistema patológico y el entorno productivo3.
Esta gramínea de gran importancia agrícola es afectada por más de 40 enfermedades y trastornos de origen microbiano, que representan una amenaza considerable para su productividad a nivel global4. La magnitud de pérdidas económicas depende tanto, de la vulnerabilidad de las variedades cultivadas como del tipo de manejo agronómico aplicado5. En este contexto, es imprescindible validar la resistencia de variedades introducidas desde otras regiones, teniendo en cuenta que su desempeño fitosanitario puede diferir, según las condiciones agroclimáticas.
Uno de los patógenos más agresivos del arroz es el hongo necrotrófico Rhizoctonia solani Kühn (teleomorfo Thanatephorus cucumeris), pertenece a la familia Corticiaceae, orden Homenomycetales, de clase Basidiomycetes, este fitoparásito secreta una gran variedad de metabolitos secundarios que incluyen toxinas selectivas del hospedero y moléculas biológicamente activas6R. solani habita en el suelo e impacta negativamente diversos cultivos de gran relevancia económica a nivel mundial, por esta razón, sigue siendo objeto de investigación en distintas regiones del mundo7, Los principales cultivos que son afectados pertenecen a las familias: Poaceae (maíz, arroz, trigo, cebada, avena), Fabaceae (soya, maní, fréjol, alfalfa, lenteja, guisante), Solanaceae (tabaco, papa), Amaranthaceae (remolacha azucarera), Brassicaceae (canola), Rubiaceae (café), Malvaceae (algodón), Asteraceae (lechuga), Araceae (potos), Moraceae (ficus) y Linaceae (lino)8.
R. solani es responsable de la enfermedad conocida como tizón de la vaina (TV), que a nivel mundial está considerada la segunda enfermedad más importante en el cultivo del arroz, después del añublo del arroz9 y puede reducir considerablemente su rendimiento10. En países como Filipinas, las pérdidas ocasionadas por TV varían desde un 10 % en condiciones normales, hasta el 25-80 % en zonas altamente infectadas11. Este problema se agrava con la utilización de variedades de arroz semi-enanas de mayor rendimiento, alta densidad de siembra y uso excesivo de fertilizantes nitrogenados, además, el amplio rango de hospedantes de este patógeno y su capacidad para sobrevivir y persistir en estado latente bajo condiciones desfavorables dificulta su control12.
El TV afecta principalmente la vaina foliar y láminas de hojas, pudiendo afectar toda la planta, incluyendo panojas emergentes13. Los síntomas se manifiestan en la fase de macollamiento tardío y comienzos de la floración14. Un síntoma característico de la enfermedad es la formación de lesiones con apariencia húmeda, de color verde grisáceo sobre la vaina foliar, cerca del nivel del agua. Estas lesiones, inicialmente de forma circular, oblonga o elipsoidal, alcanzan cerca de 1 cm de largo, posteriormente se agrandan y adoptan formas irregulares, con un centro de color blanco grisáceo y bordes marrones. Las lesiones pueden aparecer en cualquier parte de la vaina y unirse hasta rodear el tallo. Bajo condiciones favorables, la infección se propaga hacia hojas superiores, lo que provoca la pudrición de la vaina y el secado completo de la hoja15. En fases avanzadas, esta enfermedad provoca un deficiente llenado de los granos16.
El manejo de enfermedades implica la combinación de métodos como, la resistencia genética, prácticas culturales, control químico y biológico, estrategias integradas que promueven la sostenibilidad, disminuyen el impacto ambiental y contribuyen a fortalecer la seguridad alimentaria17 y, que tienen como propósito disminuir la cantidad de inóculo patogénico a niveles tolerables18. Una de las prácticas más utilizadas en la agricultura moderna, es el uso de los fungicidas químicos, ya que estos productos han sido integrados de manera esencial en la producción eficiente de alimentos, por lo que su aplicación en muchas ocasiones resulta ser una solución rápida, práctica y rentable desde el punto de vista económico19. Aunque el control químico es uno de los métodos más empleados, presenta desafíos relacionados con la sostenibilidad, debido al aumento de costos, desarrollo de tolerancia a fungicidas, y preocupaciones por la toxicidad residual20,21, no obstante, el uso de fungicidas triazoles (Propiconazol, Tebuconazol y otros) fueron una de las estrategias más comunes durante años para controlar hongos del suelo22,23. Adicionalmente, los productos de origen sintético provocan efectos tóxicos en el ser humano y contaminan el ambiente24,25. Es por ello, que se promovió la utilización de alternativas sostenibles como los fungicidas biológicos26-28, extractos vegetales29 y el control con antagonistas microbianos30-32.
Estudios realizados por Bauzón et al.26 en el que se evaluó in vitro la eficacia de 5 biofungicidas, un agente biológico, un tratamiento químico y un control (sin tratamiento) frente a R. solani, señalaron que Melaleuca alternifolia + terpenos (3 mL L-1), Aloe vera + aceite de Melaleuca (3 mL L-1), Aloe vera (2 mL L-1) y Melaleuca alternifolia (2 mL L-1) resultaron altamente eficaces contra la enfermedad, comparables al tratamiento químico (Propiconazol+Difenoconazol), por lo que sugirieron validar estos hallazgos bajos condiciones in vivo con el fin de disminuir el uso de fungicidas y fomentar la sostenibilidad ambiental.
Serenade es un biofungicida a base de Bacillus subtilis cepa QST 713, actúa por antibiosis y resistencia inducida y ha sido evaluado junto con sus filtrados del producto y suspensión bacteriana en el control de la enfermedad clubroot (hernia de la raíz) en canola, cuyo agente causal es el hongo Plasmodiophora brassicae, obteniendo alta eficacia contra P. brassicae cuando se realizan 2 aplicaciones, logrando eliminar los síntomas de esta patología33. Timorex Gold es un biofungicida basado en el aceite esencial de árbol del té, derivado la planta Melaleuca alternifolia, que funciona eficazmente contra hongos fitopatógenos en diversos cultivos y ha señalado ser efectivo en el control de Sigatoka Negra, por lo que se destaca su potencial como una herramienta en programas de manejo integrado de plagas34.
Dentro del enfoque integrado, el empleo de variedades resistentes es muy efectivo para controlar enfermedades causadas por hongos, ya que, patologías graves como las royas, los marchitamientos vasculares y pudriciones radiculares se manejan de manera eficiente con dichas variedades. Estudios realizados en 10 cultivares de arroz bajo condiciones de invernadero refieren diferencias significativas entre los cultivares respecto a la susceptibilidad y resistencia al patógeno, señalando distintos niveles de incidencia y severidad de acuerdo a la variedad evaluada35.
Debido a que algunas variedades se cultivan en países vecinos, es crucial verificar si éstas son resistentes a diversas enfermedades cuando se cultivan en nuestro país, considerando que las nuevas variedades pueden presentar menor incidencia y severidad a enfermedades lo que permitirá la reducción de aplicación de plaguicidas.
En este contexto, es crucial adoptar tecnologías como el uso de productos biológicos y nuevas variedades que se encuentren adaptadas a nuestra zona de estudio, con el fin de disminuir el uso de pesticidas y aumentar rendimientos agrícolas. Por lo tanto, este estudio se centró en evaluar el impacto de diversos fungicidas en el control de R. solani en 3 variedades de arroz de origen peruano que son cultivadas en el cantón Babahoyo.
Materiales y métodos
La investigación se llevó a efecto en el km 9.0 de la vía Babahoyo - Montalvo, Ecuador, entre las coordenadas geográficas (UTM) 672845.34 de longitud Este y 9796946.78 de latitud Sur. El área experimental se encuentra a una altitud de 8 m. La zona presenta un clima tropical húmedo con una temperatura media anual de 25.6° C, precipitación anual 2329.8 mm, humedad relativa del 82 % y un promedio anual de 998.2 h de heliofanía. El suelo es de topografía plana, con textura arcillo-limosa y drenaje regular.
El experimento se efectuó durante el ciclo agrícola comprendido entre los meses de marzo-julio del 2021, en condiciones de campo. Como material vegetal se utilizaron 3 variedades de arroz de origen peruano conocidas como HP 102 FL- El Valor, Feron e INIA 515- Capoteña.
Los fungicidas que se utilizaron en la investigación fueron adquiridos en distribuidores certificados en el país. A continuación, se detallan los productos utilizados con su codificación respectiva, de acuerdo con su ficha técnica: i) Renaste (Epoxiconazol 50 g L-1+ Pyraclostrobin 133 g L-1), código: RNST-EPY 133, fabricado por la BASF, Alemania. ii) Serenade Max (Bacillus subtilis cepa QST 713), código: SRND-BSQ 713, registrado y distribuido por Bayer CropScience, EE.UU. iii) Timorex Gold (Extracto de Melaleuca alternifolia 26.8 %), código: TMRX-MEL 268, distribuido por STK Bioag Tecnologies, Israel. iv) Propiconazol 250 EC, código: PRPC-250 EC, de uso común y procedencia nacional, distribuido por diversas empresas locales. v) Tebuconazol 250 EW, código TBCN-250, formulado por Adama Agricultural Solutions Israel, con distribución local bajo licencia.
Las variables dependientes de la investigación fueron la incidencia y severidad de la enfermedad, eficacia de fungicidas y rendimiento del cultivo de arroz, mientras que las variables independientes incluyeron las variedades y los fungicidas Tabla 1.
Tabla 1 Descripción de tratamientos empleados en el estudio
| Tratamiento | Factor A (Variedades de arroz) | Factor B (Fungicidas + Dosis) |
|---|---|---|
| T1 | A1 | (B1) (Epoxiconazol + Pyraclostrobin) F1+(Bacillus subtilis QST 713) F2 + (Extracto de Melaleuca alternifolia) F3 (150 mL ha-1) + (500 mL ha-1) + (1000 mL ha-1). |
| T2 | A1 | (B2) (Epoxiconazol + Pyraclostrobin) + (Bacillus subtilis QST 713) + (Extracto de Melaleuca alternifolia) (300 mL ha-1) + (1000 mL ha-1) + (1500 mL ha-1). |
| T3 | A1 | (B3) Como lo maneja el agricultor (Propiconazol) F4+ (Tebuconazol) F5 (500 mL ha-1) + (500 mL ha-1). |
| T4 | A1 | (B4) Sin aplicación de fungicidas (0) |
| T5 | A2 | (B1) (Epoxiconazol + Pyraclostrobin) F1+(Bacillus subtilis QST 713) F2 + (Extracto de Melaleuca alternifolia) F3 (150 mL ha-1) + (500 mL ha-1) + (1000 mL ha-1). |
| T6 | A2 | (B2) (Epoxiconazol + Pyraclostrobin) + (Bacillus subtilis QST 713) + (Extracto de Melaleuca alternifolia) (300 mL ha-1) + (1000 mL ha-1) + (1500 mL ha-1). |
| T7 | A2 | (B3) Como lo maneja el agricultor (Propiconazol) F4+(Tebuconazol) F5 (500 mL ha-1) + (500 mL ha-1). |
| T8 | A2 | (B4) Sin aplicación de fungicidas (0) |
| T9 | A3 | (B1) (Epoxiconazol + Pyraclostrobin) F1+(Bacillus subtilis QST 713) F2 + (Extracto de Melaleuca alternifolia) F3 (150 mL ha-1) + (500 mL ha-1) + (1000 mL ha-1). |
| T10 | A3 | (B2) (Epoxiconazol + Pyraclostrobin) + (Bacillus subtilis QST 713) + (Extracto de Melaleuca alternifolia) (300 mL ha-1) + (1000 mL ha-1) + (1500 mL ha-1). |
| T11 | A3 | (B3) Como lo maneja el agricultor (Propiconazol) F4+(Tebuconazol) F5 (500 mL ha-1) + (500 mL ha-1). |
| T12 | A3 | (B4) Sin aplicación de fungicidas (0) |
A1= HP 102 FL- El Valor, A2= Feron, A3= INIA 515- Capoteña, F1 = El fungicida Renaste (Epoxiconazol + Pyraclostrobin) se aplicó a la semilla antes de la siembra.
F2 = El fungicida Serenade Max (Bacillus subtilis) cepa QST 713 se aplicó a los 35 días después de la siembra, F3 = El fungicida Timorex Gold (Extracto de la planta Melaleuca alternifolia) se aplicó a los 90 días del cultivo (máximo embuchamiento), F4 = El fungicida Propiconazol se aplicó a los 40 días del cultivo (como lo hace tradicionalmente el agricultor), F5 = El fungicida Tebuconazol se aplicó a los 90 días del cultivo (máximo embuchamiento), (como lo hace tradicionalmente el agricultor).
El experimento consistió en 12 tratamientos organizados en un diseño de bloques completos al azar (DBCA) con arreglo factorial A (variedades) x B (fungicidas), y 3 repeticiones. El Factor A correspondió a las variedades de arroz, mientras que el Factor B incluyó los tratamientos fungicidas con sus respectivas dosis. Cada unidad experimental (UE) estuvo constituida por un área de 4 m2 (2 m x 2 m), con una separación de 1.0 m entre bloques y de 0.5 m entre parcelas. Para evaluar los efectos de los tratamientos, se midieron los siguientes parámetros: Incidencia y severidad de la enfermedad, eficacia de los fungicidas, número de macollos, porcentaje de granos por panícula, peso de 1000 granos y rendimiento de grano.
La incidencia y severidad de las enfermedades se determinó a los 60 días después de la siembra (dds). La incidencia se refiere a la proporción de individuos enfermos, para ello, se registró el número de plantas enfermas por área útil y se dividió este número entre el total de plantas en la misma área, multiplicando el (resultado por 100)36.
La severidad se determinó a través de observaciones visuales del área afectada por la enfermedad, y los datos obtenidos se aplicaron en la ecuación propuesta por Ivancovich et al.37.
La eficacia de los fungicidas se calculó utilizando la fórmula de Abbott38:
Donde E representa la eficacia de los fungicidas, IT es la infección en el testigo y It es la infección en el tratamiento.
En Bolivia, una serie de estudios sobre la relación entre las economías campesinas andinas y la economía de mercado dominante habían ya señalado, desde los años 80, un proceso de debilitamiento de la economía campesina tradicional impulsado por la tecnologización del campo y la revolución verde, la funcionalización de la mano de obra campesina sobrante a la economía urbana capitalista y la 'descomposición' de la economía campesina (Tassi y Canedo, 2019).
Para calcular el número de macollos en el área útil de cada parcela experimental, una vez que el arroz alcanzó su madurez fisiológica, se utilizó un marco de 1 m2. En este marco se contaron los macollos presentes, y se empleó el mismo procedimiento que se utilizó para contar el número de panículas en cada UE.
Para determinar el porcentaje de granos vanos por panícula, se seleccionaron al azar 5 panículas de cada UE y se registró el porcentaje de granos llenos y vanos.
El peso de 1000 granos se obtuvo al seleccionarlos de cada parcela experimental, asegurándose de que estuvieran libres de daños por insectos y enfermedades. Los resultados se expresaron en gramos.
El rendimiento de grano se calculó a partir del peso de los granos recolectados del área útil de cada parcela experimental. Este peso se ajustó al 14 % de humedad y se transformó a kg ha-1. Los pesos se uniformizaron utilizando la fórmula de Azcón-Bieto & Talon39:
Donde: Pu es el peso uniformizado, Pa es el peso actual, ha es la humedad actual y hd es la humedad deseada.
Donde: Pu es el peso uniformizado, Pa es el peso actual, ha es la humedad actual y hd es la humedad deseada.
Para el análisis estadístico, los datos recolectados fueron organizados en planillas electrónicas. La prueba de normalidad de Shapiro-Wilk se aplicó por cada variable evaluada. Posteriormente, para analizar el efecto de los tratamientos, se empleó la prueba de Tukey con un 95 % de probabilidad. Para los análisis se usó el software estadístico SigmaPlot40, los datos se sometieron a la prueba de correlación de Pearson (r) a fin de determinar la relación existente entre las variables evaluadas.
Resultado
Incidencia de R. solani. Las variedades A1, A2 y A3, cuando se combinaron con fungicidas y dosis específicas, redujeron la incidencia de R. solani, en comparación con el testigo absoluto. La incidencia de R. solani osciló entre 39.42 y 41.38 %, siendo la variedad A3 que expresó el menor número de plantas afectadas, mientras que la variedad A1 presentó el mayor valor, respectivamente. La mayor incidencia de R. solani fue del 50.56 %. En las parcelas tratadas, la incidencia varió entre 36.61 y 37.17 %. En la interacción variedades con fungicidas y dosis, no se observaron diferencias significativas en la incidencia.
En las parcelas tratadas con fungicidas y distintas dosis, la incidencia fluctuó entre 35.00 y 38.67 %, sin diferencias significativas entre tratamientos. En contraste, las 3 variedades estudiadas sin tratamientos presentaron incidencias entre 49.33 y 51.33 %, valores que fueron superiores a los observados con los tratamientos y dosis, así como la interacción de estos factores. En la Tabla 2 se observa la incidencia de R. solani en función a los tratamientos aplicados.
Severidad de R. solani. No se observaron diferencias en la severidad entre los tratamientos con fungicidas y dosis, aunque se notó una leve disminución de daños en comparación con el testigo absoluto. La severidad fluctuó entre 38.25 y 39.75 %, siendo el valor más alto registrado en la variedad A1. Los tratamientos reportaron severidades que variaron entre 34.11 y 39.56 %. La menor afectación se observó con B3, comúnmente utilizado por los productores locales. La severidad entre los tratamientos no fue diferente.
En contraste, las plantas sin tratamientos B4 presentaron un mayor porcentaje de severidad, 43.67 %. No se observaron diferencias en la severidad entre las interacciones de variedad con fungicidas y dosis. Las variedades A2 y A3 que recibieron el tratamiento B3 reportaron la menor severidad con un porcentaje de 33.00 %, que fue inferior al de otros fungicidas, incluyendo las parcelas sin tratar (Tabla 2).
Tabla 2 Incidencia y severidad de R. solani en función a variedades y fungicidas
| Variedades | Fungicidas y dosis | Incidencia de R. solani (%) | Severidad de R. solani (%) |
|---|---|---|---|
| (A1) | - | 41.38 | 39.75 |
| (A2) | - | 40.25 | 38.25 |
| (A3) | - | 39.42 | 39.42 |
| - | (B1) | 37.17 b | 39.22 |
| - | (B2) | 37.06 b | 39.56 |
| - | (B3) | 36.61 b | 34.11 |
| - | (B4) | 50.56 a | 43.67 |
| (A1) | (B1) | 38.67 | 36.00 |
| (A1) | (B2) | 38.00 | 43.33 |
| (A1) | (B3) | 37.83 | 36.33 |
| (A1) | (B4) | 51.00 | 43.33 |
| (A2) | (B1) | 36.17 | 44.00 |
| (A2) | (B2) | 36.50 | 41.00 |
| (A2) | (B3) | 37.00 | 33.00 |
| (A2) | (B4) | 51.33 | 35.00 |
| (A3) | (B1) | 36.67 | 37.67 |
| (A3) | (B2) | 36.67 | 34.33 |
| (A3) | (B3) | 35.00 | 33.00 |
| (A3) | (B4) | 49.33 | 52.67 |
| Significancia Estadística | Variedades | ns | ns |
| Fungicidas y dosis | ** | ns | |
| Variedades* fungicidas y dosis | ns | ns | |
| Coeficiente de variación | 10.10 | 15.39 |
Medias con una letra en común no son significativamente diferentes (p> .05) según la prueba de Tukey al 5 % de probabilidad.
** Altamente significativo (p< .01), ns: No significativo (p> .05).
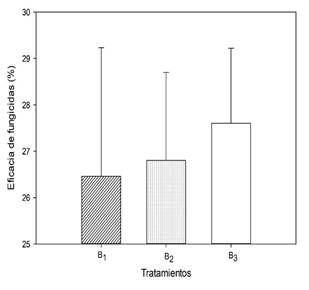
Eficacia de los fungicidas. El porcentaje de control de R. solani según los tratamientos analizados, Figura 1, reveló que B3 alcanzó una eficacia 27.60 %. B2 y B1 presentaron 26.80 y 26.46 %, respectivamente. Comparados entre sí, estos valores no difieren. El coeficiente de variación fue 22.08 %. En las variedades evaluadas, ninguna eficacia superó el 30 % con fungicidas y dosis aplicadas para el control de R. solani.
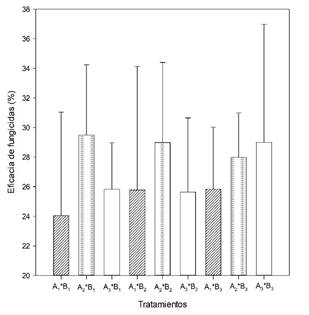
La interacción entre variedades y fungicidas no fue diferente, no obstante, en la Figura 2 se puede ver que para A2, B1 logró un control del 29.49 %. Este resultado fue similar a los obtenidos con 28.99 % y B3 27.98 % en la misma variedad. Por otro lado, en las variedades A1 y A3, los tratamientos con fungicidas reportaron eficacias que variaron entre 24.05 y 29 %. Estos valores no fueron diferentes. Además, el periodo de persistencia de los fungicidas superó los 20 días.
Número de macollos. Tabla 3 según los tratamientos evaluados, la variedad A1 presentó mayor número, con un promedio de 293.92, seguida por A3 con 286.08. B4 tuvieron un promedio de 306.67 por m-2. B2 y B1 resultaron en 289.67 y 280.56, respectivamente, mientras B3 produjo 277.67 macollos por m-2. Este último no difirió del número observado en las parcelas sin aplicación de fungicidas.
Al considerar la interacción entre variedades y fungicidas, el mayor número de macollos por m-2 se obtuvo en A1 sin fungicidas, con 316.33, seguido por A2 con B3, que reportó 309.67, y A3 sin fungicidas, con 306.00. La menor cantidad de macollos por m-2 se registró en la variedad A2 con B2 (261.33 macollos). Este valor fue similar al observado en A3 con B3 (261.67), A1 con B3 (261.67), A3 con B1 (267.67) y A2 con B1 (275.00).
Producción. Tabla 3 kg ha-1 de los diferentes tratamientos analizados. Los rendimientos de las variedades oscilaron entre 5192.32 y 6395.67 kg, destacando A3 como la mayor producción por unidad de superficie. La producción de A3 fue diferente de la obtenida con A2 y A1, cuyas producciones fueron similares entre sí.
En cuanto al factor de fungicidas y dosis, B3 y B1 lograron la mayor producción, con 5968.98 y 5786.79 kg, respectivamente, sin diferencias significativas entre ellos. Sin embargo, el rendimiento en B3 con 5968.98 kg fue diferente al B2 con 5231.15 kg y al del testigo absoluto con 5500.44 kg.
En la interacción entre variedades y tratamientos con fungicidas y dosis, la variedad A3 combinada B3 B1 y B2, mostraron las mayores producciones por hectárea, con 6891.73, 6749.49 y 6257.44 kg, respectivamente. No obstante, la producción de LAP-003-2020 con B1 no varió en comparación con el testigo absoluto 5684.00 kg.
Por otro lado, las menores producciones por hectárea se obtuvieron con A1 y B2, A2 y B2 y A1 y B1, alcanzaron 4692.05, 4743.95 y 4804.05 kg, en su orden. Estos valores no fueron diferentes de la producción de los testigos absolutos correspondientes.
Granos vanos. Figura 3A, la variedad A3 presentó el menor número de granos vanos por panícula, con 16.14 %. La Figura 3B muestra el porcentaje de granos vanos en respuesta a los distintos tratamientos con fungicidas y sus dosis. En esta variable, el porcentaje de granos vacíos por panícula osciló entre 18.79 y 23.85 %. El valor más bajo se registró en B3, fue diferente de B1, que reportó 23.85 % de granos vanos. El testigo absoluto reportó un 22.17 % de vaneamiento, pero esta cifra no difirió de los demás valores.
En la interacción entre variedades y tratamientos con fungicidas y dosis (Figura 3C), A3 sin fungicidas presentó 14.68 % de granos vanos, seguido por A3 con B2 que reportó 15.66 %, A3 con B1 reportó 16.26 % y A1 con B3 obtuvo 16.28 %. Los porcentajes alcanzados en estos tratamientos no manifestaron diferencias entre sí.
Discusión
Los resultados obtenidos evidencian que la integración de fungicidas biológicos y químicos, combinados con la selección adecuada de variedades de arroz, puede desempeñar un papel clave en la reducción de la incidencia y severidad de R. solani en condiciones de campo. Aunque ningún tratamiento superó el 30 % de eficacia, B1 y B3 destacaron frente al testigo absoluto, lo que respalda su incorporación como estrategia complementaria dentro de programas de manejo integrado. Esta moderada eficacia puede atribuirse a factores como la presión del inóculo en ambientes tropicales, el uso intensivo de fertilizantes nitrogenados y la susceptibilidad varietal, que enfatiza la necesidad de abordajes multifactoriales41-44. Es por ello, es imprescindible la aplicación de medidas integrales para el control de enfermedades, estas estrategias incluyen el uso de materiales resistentes o tolerantes, elección de épocas de siembra, nutrición balanceada, rotación de cultivos, incorporación de microorganismos antagonistas y la aplicación racional de fungicidas45-48, dado que estas medidas en conjunto han referido la menor incidencia de síntomas de R. solani, aproximadamente 8 % debajo del control químico, especialmente en la etapa inicial y durante el desarrollo vegetativo del cultivo49.
Tabla 3 Número de macollos y producción en función a los tratamientos estudiados
| Variedades | Fungicidas y dosis | Número de macollos m-2 | Producción (kg/ha-1) |
|---|---|---|---|
| (A1) | - | 293.92 | 5192.32 b |
| (A2) | - | 285.92 | 5277.53 b |
| (A3) | - | 286.08 | 6395.67 a |
| - | (B1) | 280.56 ab | 5786.79 ab |
| - | (B2) | 289.67 ab | 5231.15 c |
| - | (B3) | 277.67 b | 5968.98 a |
| - | (B4) | 306.67 a | 5500.44 bc |
| (A1) | (B1) | 299.67 a | 4804.05 d |
| (A1) | (B2) | 298.00 a | 4692.05 d |
| (A1) | (B3) | 261.67 b | 5818.40 bc |
| (A1) | (B4) | 316.33 a | 5454.77 bcd |
| (A2) | (B1) | 275.00 b | 5806.83 bc |
| (A2) | (B2) | 261.33 b | 4743.95 d |
| (A2) | (B3) | 309.67 a | 5196.80 cd |
| (A2) | (B4) | 297.67 a | 5362.56 cd |
| (A3) | (B1) | 267.67 b | 6749.49 a |
| (A3) | (B2) | 309.67 a | 6257.44 ab |
| (A3) | (B3) | 261.67 b | 6891.73 a |
| (A3) | (B4) | 306.00 a | 5684.00 bc |
| Significancia Estadística | Variedades | ns | ** |
| Fungicidas y dosis | ** | ** | |
| Variedades* fungicidas y dosis | ** | ** | |
| Coeficiente de variación | 3.13 | 4.87 |
La menor incidencia y severidad de la enfermedad se obtuvo con B1 y B3, en concordancia con estudios anteriores, su eficacia observada de B. subtilis y del extracto de M. alternifolia que destacan su capacidad de control mediante antibiosis, inducción de resistencia sistémica y competencia por nicho ecológico 26,33,34.
Diversos estudios confirmaron que el uso de B. subtilis como biofungicida puede mejorar significativamente la resistencia del arroz a patógenos del suelo. Por ejemplo, Lahlali et al.33 señalaron que Serenade Max, a base de B. subtilis cepa QST 713, induce resistencia sistémica y reduce la severidad de enfermedades en canola. De igual forma, Boukaew et al.28 señalaron que la combinación de agentes bio-controladores con fungicidas químicos puede incrementar la eficacia del control sobre R. solani sin generar efectos adversos sobre el ambiente ni inducir resistencia. En otro estudio, Rashid et al.27 reportaron que el uso de biopesticidas a base de extractos vegetales y bacterias beneficiosas fue eficaz en reducir la incidencia de la enfermedad del TV en arroz en Bangladesh, con resultados comparables a los tratamientos convencionales.
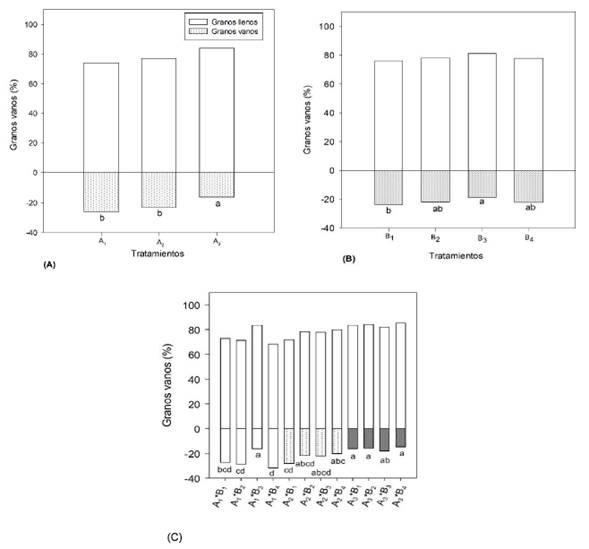
Figura 3 Granos vanos (%) y granos llenos (%) en las variedades (A), tratamientos con fungicidas y dosis (B) e interacción variedades con fungicidas y dosis (C). Barras con una letra en común no son significativamente diferentes (p>0.05) según la prueba de Tukey al 5 % de probabilidad
Además, Yang et al.29 señalaron que cepas bacteria-nas aisladas de estiércol bovino tenían potencial como agentes de control biológico contra R. solani, destacando la viabilidad de aprovechar microorga-nismos autóctonos como una solución sostenible y local. Este conjunto de evidencias fortalece la noción de que el enfoque de manejo integrado, basado en productos biológicos y su interacción con el material vegetal, constituye una estrategia sólida para dismi-nuir el impacto de patógenos y mejorar la estabilidad productiva en sistemas arroceros tropicales.
La variedad A3 manifesto menor afectación, la mis-ma que combinada con B1 presentó mayor rendimiento 6749.49 kg ha-1 y el menor porcentaje de granos vacíos (16.14 %) lo que evidencia una interacción favorable entre el material vegetal y la estrategia fito-sanitaria empleada. Hallazgos similares fueron re-portados previamente en los que se resalta la importancia de integrar prácticas de manejo, incluyendo la selección adecuada de variedades con niveles de tolerancia y complementar su manejo con fungicidas que tengan diferentes modos de acción para reducir sustancialmente la incidencia de enfer-medades en campo50.
Esto sugiere que la selección de la variedad, junto con el fungicida biológico correspondiente, es crucial para maximizar el control de R. solani. La interacción entre el hospedador, el patógeno y el agente bioló-gico debe ser objeto de más investigaciones para comprender mejor estos mecanismos, esto concuerda con lo señalado por Quiroz Ojeda et al.7, quienes mencionaron que R. solani interactua con sus hospederos desde perspectivas biológicas, genéticas y patogénicas, fundamental para entender la relación entre el hospedador y el patógeno en distintos pato-sistemas.
El porcentaje de granos vacíos afecta el rendimiento del cultivo al comprometer la fotosíntesis, la traslocación de nutrientes y el llenado de grano51. La variedad A3 reportó menor porcentaje de granos vacíos, sin importar el tratamiento aplicado, y un comportamiento similar se observó en la variedad A1 con la aplicación de Propiconazol y Tebuconazol, que reportó el 16.28 % de granos vacíos en la panícula. Esto sugiere que el porcentaje de granos vacíos podría están influenciados por factores bióticos (patógenos, insectos plagas y factores genéticos) y abióticos (baja temperatura, humedad relativa y nubosidad)45,52.
Por otra parte, los fungicidas sintéticos como el Propiconazol y el Tebuconazol continuan presen-tando cierto nivel de efectividad, así como lo eviden-cian investigaciones efectuadas por Pérez Vicente et al.53, aunque su uso continuo representa riesgos de generación de resistencia por parte del patógeno y pueden producirse impactos ambientales indeseables. Por lo mencionado, los resultados obtenidos en el presente estudio respaldan la transición progresiva de las moléculas sintéticas por bioproductos, en concordancia con enfoques agroecológicos.
Esta investigación se distingue por integrar en campo productos biológicos con variedades que estan siendo actualmente utilizadas por los agricultores, lo que no solo genera información valiosa, sino que fortalece las decisiones de los productores interesados en prácticas agrícolas más sostenibles en zonas arroceras del litoral ecuatoriano.











 texto en
texto en 
 uBio
uBio