Sus descubrimientos explican cómo el cuerpo evita atacarse a sí mismo mediante un sofisticado sistema de tolerancia inmunológica periférica. Identificaron un grupo de linfocitos denominados células T reguladoras, o TREG, que controlan respuestas autoinmunes destructivas.
Marcadas por el gen FOXP3, actúan como freno del sistema inmunitario, manteniendo su equilibrio y estabilidad interna. Si el gen FOXP3 se altera, surgen enfermedades autoinmunes graves como el síndrome IPEX en humanos y ratones.
El hallazgo demostró que el sistema inmune posee un mecanismo natural que distingue entre lo propio y lo ajeno. Contribuyendo al descubrimiento de las células T reguladoras y los mecanismos de la tolerancia inmune periférica, claves para entender cómo el sistema inmunitario evita atacarse a sí mismo. Gracias a estas investigaciones, se abrieron nuevas vías terapéuticas para tratar enfermedades autoinmunes, alergias, cáncer y rechazo de trasplantes.
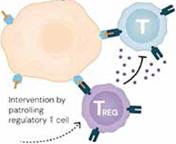
Fuente: Nobel Prize, 2025.
Figura 2 Las células T reguladoras descubren que el ataque es un error y lo calman, esta intervención es mediante el llamado “patrullaje”
¿QUÉ ES LA TOLERANCIA PERIFÉRICA?
El sistema inmune necesita atacar invasores y, a la vez, respetar los propios tejidos. Se pensaba que ese “filtro” ocurría solo en el timo (tolerancia central).
Los hallazgos premiados mostraron el descubrimiento de la tolerancia periférica, que se encuentra activa en la circulación y los órganos. Allí operan linfocitos especializados - las células T reguladoras- (TREG) que apagan respuestas peligrosas contra lo propio. Cuando fallan, emergen cuadros autoinmunes.
MARY ELIZABETH BRUNKOW
Conocida por identificar el gen, posteriormente denominado FOXP3 (2001), fenotipo de una cepa de ratones susceptibles a sufrir enfermedades autoinmunes , un hallazgo que se convirtió en fundamental para la biología moderna de las células T reguladoras.
Primeros años
• Nació en 1961 en EEUU, recibió su licenciatura en Biología Molecular y Celular por la Universidad de Washington y su maestría y doctorado en Biología Molecular por la Universidad de Princeton en 1991, donde su directora fue Shirley M. Tilghman (que participó en la primera clonación de un gen de mamífero).
Descubrimiento del gen FOXP3
La cepa de ratón, denominada “scurfy “, captó la atención de los investigadores. La genética molecular estaba en sus inicios, pero se dieron cuenta de que la mutación causante de esta enfermedad debía estar localizada en el cromosoma X de los ratones. La mitad de los ratones machos padecen la enfermedad, pero las hembras pueden convivir con esta mutación gracias a que poseen dos cromosomas X, de los cuales uno contiene ADN sano. De este modo, las hembras transmiten la mutación “scurfy” a las nuevas generaciones.
En la década de 1990, cuando las herramientas moleculares se habían perfeccionado considerablemente, los investigadores comenzaron a investigar por qué los ratones machos con caspa enfermaban tanto. Resultó que sus órganos estaban siendo atacados por células T que destruían los tejidos. Por alguna razón, la mutación con caspa pareció provocar una rebelión en el sistema inmunitario.
Brunkow y Ramsdell encuentran la aguja en el pajar del ADN
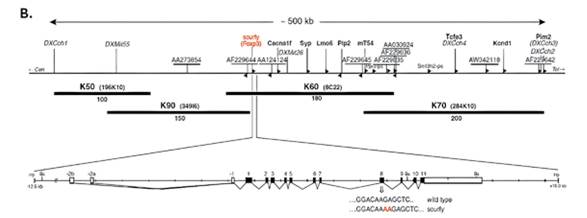
El mapeo había demostrado que la mutación scurfy debía estar en algún punto intermedio del cromosoma X. Brunkow y Ramsdell lograron reducir el área potencial a unos 500.000 nucleótidos. Posteriormente, emprendieron la enorme tarea de mapear esa área del cromosoma X en detalle.
Esto llevó mucho tiempo. Cuando Brunkow y Ramsdell terminaron, habían establecido que el área contenía 20 genes potenciales. Su siguiente reto fue comparar estos genes en ratones sanos y en ratones con caspa. Examinaron gen tras gen. Solo con el vigésimo y último gen pudieron decir la verdad. Tras años de trabajo dedicado, finalmente encontraron la mutación con caspa.
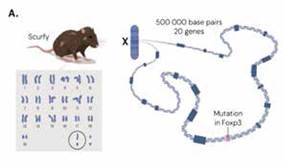
Figura 4 (A) Proyecto de mapeo de Brunkow y Ramsdell para identificar el gen defectuoso en ratones con caspa. Los resultados del paso final de secuenciación, que compara el gen candidato con sus homólogos en humanos y otras siete cepas de ratones.
SHIMON SAKAGUCHI
Nagahama, Japón 1951 es un inmunólogo, Trabaja en la Universidad de Kioto y la Universidad de Osaka. Es conocido por el descubrimiento del linfocito T regulador y la descripción de su participación en el sistema inmunitario, así como por la aplicación de este conocimiento en el tratamiento de la autoinmunidad y el cáncer.
Recibió un Doctorado en Medicina y otro en la Universidad de Kioto. Realizó investigación postdoctoral en los Estados Unidos en la Universidad Johns Hopkins y la Universidad de Stanford de 1983 a 1987 como becario de Lucille P. Markey. Trabajó como profesor asistente en el Departamento de Inmunología en el Instituto de Investigación Scripps. Después de regresar a Japón en 1991, se convirtió en el jefe del Departamento de Inmunopatología en el Instituto Metropolitano de Gerontología de Tokio.
Shimon Sakaguchi, y pronto otros investigadores, pudieron demostrar de forma convincente que el gen FOXP3 controla el desarrollo de las células T reguladoras. Estas células impiden que otras células T ataquen por error el propio tejido corporal, lo cual es importante para un proceso denominado tolerancia inmunitaria periférica. Las células T reguladoras también garantizan que el sistema inmunitario se tranquilice tras eliminar a un invasor, evitando que siga funcionando a toda velocidad.
El conocimiento fundamental adquirido por los investigadores gracias al descubrimiento de las células T reguladoras y su importancia para la tolerancia inmunitaria periférica ha impulsado el desarrollo de posibles nuevos tratamientos médicos. El mapeo de tumores muestra que estos pueden atraer grandes cantidades de células T reguladoras que los protegen del sistema inmunitario. Por lo tanto, los investigadores buscan maneras de desmantelar esta barrera de células T reguladoras para que el sistema inmunitario pueda acceder a los tumores.
FREDERICK JAY RAMSDELL
Frederick Jay Ramsdell (4 de diciembre de 1960) inmunólogo EEUU y director de investigación del Instituto Parker de Inmunoterapia del Cáncer en San Francisco. Graduado con licenciatura de bioquímica y biología Celular Universidad de California, San Diego en 1983.
En 1987 en la Universidad de California, Los Ángeles cursa el doctorado de microbiología e inmunología. Desde principios del 2016, director de investigación del Instituto Parker de Inmunoterapia de cáncer.
Como investigador postdoctoral trabajó en los Institutos Nacionales de Salud y posteriormente en empresas de biotecnología del área de Seattle. Tambien en ZymoGenetics y ocupó el cargo de director científico en Sonoma Biotherapeutics. Desde principios de 2016, ha sido director de investigación en el Instituto Parker de Inmunoterapia del Cáncer en San Francisco.
Ramsdell y su equipo identificaron la proteína Forkhead Box P3 (FOXP3) en ratones con caspa y en niños con síndrome IPEX enfermedad genética autoinmune rara que causa una respuesta inmune descontrolada. Se caracteriza por la disfunción de las células inmunitarias T reguladoras debido a mutaciones en el gen FOXP3, lo que provoca que el sistema inmunitario ataque a los propios tejidos del cuerpo. Los síntomas incluyen: diabetes, eccema severo, diarrea persistente y problemas de la sangre; que suelen aparecer en la infancia. (desregulación inmunitaria, poliendocrinopatía, enteropatía ligada al cromosoma X). Además, determinaron que la FOXP3 desempeña un papel crucial en el desarrollo de linfocitos T reguladores.