INTRODUCCIÓN
El diagnóstico prenatal temprano de anomalías cromosómicas es una necesidad en el control prenatal ya que logra identificar fetos con riesgo elevado para el desarrollo de las mismas.1 No todos los embarazos tienen la misma predisposición, ya que depende de diversos factores epidemiológicos; como la edad materna, antecedente de anomalías cromosómicas en un embarazo anterior, etc. El diagnóstico se establece mediante la identificación de signos ecográficos sugestivos y la presencia de marcadores bioquímicos en el primer trimestre.2 Si estos datos sugestivos están presentes se recomiendan métodos invasivos como la biopsia de vellosidades coriales o la obtención de muestra de líquido amniótico mediante amniocentesis, con el fin de conseguir células fetales, cultivarlas y obtener el cariotipo en los fetos con riesgo alto para estas anomalías.3
Los marcadores ecográficos indican malformaciones estructurales como el pliegue o traslucencia nucal aumentada,el higroma quístico, la ausencia de hueso nasal, la onda de velocidad de flujo anormal del ductus venoso o la onda invertida en la arteria umbilical, el flujo retrógrado en la válvula trícuspídea y otras alteraciones morfológicas del feto o de los anexos, lo que pasa en los fetos con trisomías 21, 18 y 13.4 En relación a los marcadores bioquímicos en suero materno se puede medir la concentración sérica materna de B-hCG libre, al igual que la proteína plasmática A asociada al embarazo (PAPP-A).5
El uso combinado de marcadores como la translucencia nucal, ausencia del hueso nasal, la B-hCG libre y PAPP-A en suero materno, puede identificar más del 50% de los fetos con trisomías.3,6 Es importante el uso de estas herramientas en etapas tempranas del embarazo para tener un buen manejo del mismo asegurando la salud materno fetal.
CASO CLÍNICO
Se presenta el caso de una paciente de 30 años de edad, casada, de ocupación profesora que acude al servicio de emergencias de ginecología. Como antecedentes de importancia la paciente, segundigesta nulípara, refiere síndrome de ovario poliquístico tratado con anticonceptivos orales durante un año y una cesárea previa hace 4 años debido a feto en presentación podálica.
La paciente refiere cuadro de un mes de evolución caracterizado por dolor abdominal de leve intensidad en región de hipogastrio, sin irradiación y de remisión espontánea; motivo por el cual acude a médico particular en donde realizan ecografía obstétrica temprana, misma que reporta alteraciones en la morfología fetal. Por ese motivo, después de la anamnesis y examen físico, se decide su internación.
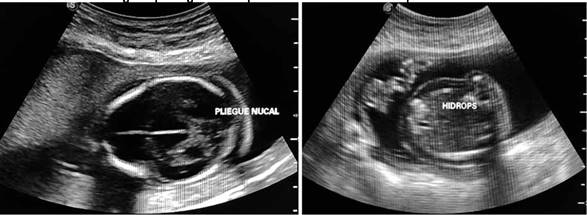
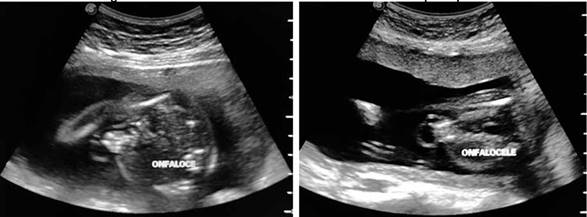
Durante su estadía se solicita una ecografía obstétrica estructural temprana, realizada por el servicio de Medicina Materno Fetal, la cual reporta un feto único vivo en presentación pélvica, situación longitudinal, dorso derecho, fetometría promedio 19.6 semanas de gestación, peso fetal estimado de 363 +/- 480 gramos, líquido amniótico cualitativamente normal con pool máximo de 4. A la evaluación estructural se observa a nivel cefálico, incremento del pliegue nucal (Figura 1), edema pericraneal y prenasal, fosa posterior aumentada y desplazada, con agenesia parcial de vermis cerebeloso. A nivel de columna cervical se encuentra edema, con tabicación que sugieren un higroma quístico. A nivel de tórax se evidencia edema de tejido subcutáneo, en el corte de cuatro cámaras se observa área anecoica en forma de luna bilateral importante que rodea al corazón, sugestivo de hidrotórax bilateral. No se aprecia tejido pulmonar en ningún hemitórax. A nivel de abdomen se evidencia defecto de pared de aproximadamente 12 mm en su base, por donde protruyen asas intestinales con membrana que los recubre, siendo los diámetros del saco del defecto de 25 x 20 mm (Figura 2). Todos los datos fueron compatibles con un embarazo de 19.4 semanas (según ecografía obstétrica temprana) y feto con Hidrops fetal no inmune con higroma quístico.
Con estos hallazgos, en coordinación con servicio de genética, se considera un diagnóstico probable de aneuploidía, por lo cual se realiza amniocentesis bajo guía ecográfica para obtener la muestra necesaria para los exámenes de laboratorio y biología molecular.
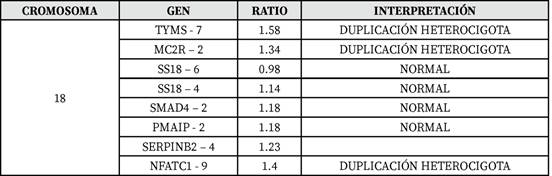
La amniocentesis es realizada con técnica de dos operadores bajo guía ultrasonográfica y punción con aguja 22G, extrayendo 20 ml de líquido amniótico. Una vez obtenida la muestra se solicitan exámenes para el complejo TORCH y biología molecular para el diagnóstico de cromosomopatías. Se obtiene reporte con PCR no detectada para CMV, VEB, VHS-1, VHS-2 y resultados llamativos de biología molecular (Tabla 1).
Después del análisis de los resultados se solicita valoración por psicología para orientar ampliamente a la paciente y su pareja sobre los hallazgos ultrasonográficos, así como alcances, limitaciones, y evolución del embarazo, además de pronóstico fetal reservado.
Se realiza una junta médica con la participación de múltiples especialidades para determinar el curso de la gestación. Considerando el diagnostico de aneuploidía incompatible con la vida (trisomía 18), se informa a los padres. Una vez recibida toda la información la paciente y esposo solicitan interrupción del embarazo.
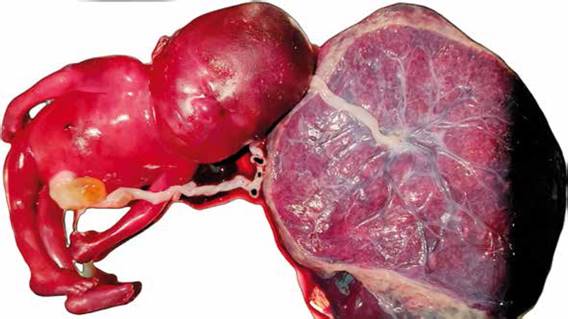
Se realiza interrupción del embarazo vía vaginal, mediante inducción usando análogos de prostaglandina E1. Al momento del nacimiento se evidencio feto de sexo masculino con un peso de 470 g. Se corroboró la presencia de higroma quístico, sumado a un edema generalizado (hidrops) y la presencia de onfalocele (Figura 3).
DISCUSIÓN
El abordaje multidisciplinario, que incluye la participación de Ginecología, Obstetricia, Medicina Materno Fetal y Genética, es fundamental para un cribado adecuado de aneuploidías, idealmente durante el primer trimestre de la gestación. El uso combinado de estudios ecográficos y bioquímicos permite la identificación temprana de marcadores sugestivos de cromosomopatías.7 Además, en el contexto del hidrops fetal no inmune, se deben considerar otras etiologías, como enfermedades infecciosas de origen viral, bacteriano o parasitario. Por ello, se recomienda incluir la evaluación diagnóstica de patógenos como Parvovirus B19, Citomegalovirus, Toxoplasma gondii y Treponema pallidum, entre otros.8
El diagnóstico tardío de estas condiciones puede derivar en un manejo obstétrico más complejo; como se evidenció en el caso de una paciente de 19 años con captación prenatal tardía y sin realización de cribado de cromosomopatías en el primer trimestre ni ecografía morfológica estructural, misma que resulta una herramienta fundamental para un adecuado y oportuno abordaje, como vimos en la descripción de este artículo. En dicho caso, el diagnóstico de sífilis se estableció a las 23 semanas, con un VDRL de 64 UI. A las 26 semanas, la ecografía reveló incremento del índice cardiotorácico, derrame pericárdico y edema subcutáneo.8 Al igual que en el presente caso, se adoptó un enfoque interdisciplinario que involucró a los servicios de Obstetricia, Neonatología, Cuidados Paliativos Neonatales y Salud Mental.
Asimismo, se reporta otro caso en la ciudad de Oruro (Bolivia), en el Hospital General San Juan de Dios, donde una gestante adolescente de 16 años acudió por primera vez a control prenatal a las 22 semanas de gestación. La ecografía reportó polihidramnios, placenta edematizada y ascitis fetal severa. Tras consentimiento informado, se practicó parto quirúrgico, obteniéndose un neonato con múltiples signos de hidrops fetal que falleció a los cinco minutos de vida.9 Este caso subraya nuevamente la relevancia del diagnóstico temprano para planificar una intervención oportuna y eficaz como se realizó en el caso de este artículo.
En los casos de hidrops fetal asociado a anomalías cromosómicas, adquieren particular importancia los procedimientos invasivos con fines diagnósticos y terapéuticos. Por ejemplo, se documentó un caso de Hidrops fetal secundario a trisomía del par 21 diagnosticado a las 31 semanas de gestación. La ecografía reveló polihidramnios, edema subcutáneo, hidrotórax y ascitis. El diagnóstico se confirmó mediante cordocentesis y análisis cromosómico de linfocitos, utilizando bandeo GTG, y posteriormente se realizó una amniocentesis evacuadora con la extracción de 850 mL de líquido amniótico.10 Si bien se ha debatido la sensibilidad y especificidad de las pruebas invasivas en el contexto del diagnóstico prenatal, su combinación puede incrementar la precisión diagnóstica, permitiendo una mejor detección de aneuploidías, malformaciones estructurales o enfermedades genéticas hereditarias.11,12
CONCLUSIONES
Si bien la ecografía obstétrica temprana como método de screening es crucial en todas las gestantes, se deben evaluar los factores de riesgo de la población estudiada y los medios disponibles para realizar un abordaje completo, que incluya pruebas de tamizaje. Es importante la responsabilidad que el médico tiene durante todo el proceso; desde el diagnóstico hasta el momento de informar y discutir las alternativas, riesgos y beneficios del posible tratamiento de alguna alteración cromosómica, asesorando a cada paciente según sus preferencias. Algunas pacientes solicitarán preparación psicológica para el nacimiento de un niño con cromosomopatía, en otros casos, optarán por la interrupción voluntaria del embarazo o no aceptarán la realización de técnicas invasivas por el riesgo de pérdida fetal.
El presente caso evidencia el embarazo de un feto con aneuploidía diagnosticado la primera mitad del embarazo, de pronóstico malo para la vida fetal que se manejó de manera multidisciplinaria, en donde fue fundamental la participación de las distintas especialidades. Se reconoce la utilidad y validez clínica del tamizaje de primer trimestre acompañado de marcadores ecográficos, bioquímicos y estudios invasivos geneticos para el diagnóstico, manejo y abordaje adecuado de posibles alteraciones cromosómicas.