INTRODUCCIÓN
Se calcula que 1 de cada 3 adultos tiene uno o más tipos de enfermedades cardiovasculares1 (ECV), la incidencia oscila en 0,7% en el grupo de 18 a 44 años y hasta 13,3% en >75 años o más; y las más frecuentes son la cardiopatía isquémica y enfermedad ateroesclerótica (30%), cardiopatía valvular (2,5%), insuficiencia cardiaca y miocardiopatías (7%)1,3 . La prevalencia de ECV aumentará debido al cambio poblacional de nuestras sociedades, ya que cada vez más personas llegan a edades avanzadas, sumado a la creciente incidencia de obesidad e hipertensión1, que son factores, que afectan predominantemente la morbimortalidad perioperatoria asociada a cirugía no cardiaca4. La insuficiencia cardiaca (IC) aumenta la mortalidad perioperatoria de tres a cinco veces y se asocia con un riesgo mayor que la enfermedad arterial coronaria y riesgo de infarto de miocardio perioperatorio5. Las valvulopatías aumentan el riesgo de complicaciones perioperatorias y éstas difieren en su comportamiento fisiopatológico y en los objetivos hemodinámicos que se deben cumplir durante el periodo anestésico1,6.
La hipertensión pulmonar (HP) es una entidad cuyo manejo debe realizarse por personal altamente capacitado, tomando en cuenta las complicaciones agudas que conlleva como falla cardiaca derecha, o hipertensión arterial pulmonar aguda7,8. En consecuencia, el propósito del presente artículo es exponer las generalidades de la optimización de la evaluación preanestésica y el manejo intraoperatorio que se deben considerar en pacientes con alteraciones cardiovasculares que presenta la paciente del caso clínico para lo cual se realizó una revisión de la literatura respectiva.
PRESENTACION DE CASO
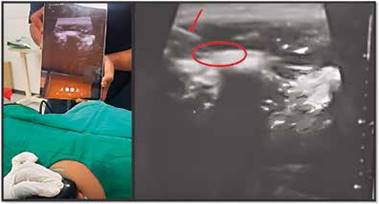
Paciente femenina de 52 años de edad, ingresa a urgencias por cuadro abdominal; valorada por el servicio de cirugía general y programado para colecistectomía laparoscópica vs abierta con el diagnóstico de colecistitis aguda litiásica. Durante la valoración preanestésica, paciente refiere antecedentes de: insuficiencia cardiaca (IC), hipertensión arterial pulmonar (HAP), estenosis mitral (EM) e insuficiencia tricuspídea (IT); en tratamiento con digoxina y carvedilol. Al examen físico peso registrado 84 Kg y talla 1.54 metros (IMC 36.7 KG/m2); signos vitales: presión arterial (PA) de 94/54mmHg, frecuencia cardiaca (FC) 67lpm, frecuencia respiratoria (FR) 22rpm, SpO2 86% con aporte de oxígeno a 3 L/min por cánula nasal; hallazgos positivos fueron: disnea a medianos esfuerzos, soplo sistólico mitral III/IV, estertores crepitantes en ambas bases pulmonares, hepatomegalia (2cm del reborde costal) y edema en ambas piernas fóvea (+++); parámetros de vía aérea: apertura oral 4cm, edéntula, Mallampati Samsoon III, distancia tiromentoniana > 6.5cm distancia esternomentoniana 11cm y Bellhouse Dore I. Los exámenes de laboratorios reportaron Hemoglobina 13.7g/dL, Hematocrito 40.6%, química sanguínea y coagulograma sin alteraciones. La ecocardiografía reportó área valvular mitral 0.8 cm2, dilatación de aurícula izquierda, dilatación de cavidades derechas, y derrame pericárdico leve. Al ingreso a quirófano la monitorización inicial (monitor SPACELABS Healthcare Ultraview SL™) registró una PA 106/71mmHg, FC 70lpm, FR 22rpm, SpO2: 88%. Se inició perfusión de noradrenalina a 0.05ug/kg/min por vía periférica y, en posición en rampa se realizó inducción anestésica con fentanil 150ug intravenoso (IV), propofol 100mg, ketamina 50mg IV y rocuronio 35mg IV (0.6mg/kg). Se realizó intubación endotraqueal sin complicaciones al primer intento. Se conectó a ventilador mecánico (General Electric Carestation 750), se programó ventilación controlada con volumen corriente (VC) 350ml, frecuencia ventilatoria (FV) 20- 24vpm, relación inspiración:espiración 1:3, PEEP 8cmHO2, FiO2 70%, obteniendo presión meseta o plateu (Pmest o Pplat) 22cmH2O y presión de distensibilidad (driving pressure (DV)) 14cmH2O. Posterior a esta, se evidenció ausencia de expansión torácica, del murmullo vesicular y de la onda de capnografía; por lo que se procedió a la administración de hidrocortisona 100mg IV y salbutamol 6 puff por tubo endotraqueal (TET) con respuesta satisfactoria y reversión de signos de broncoespasmo. Se realizó bloqueo del erector de la espina ecodirigido (Ecógrafo Butterfly iQ+™) a nivel del proceso transverso de T7 con 20 ml de bupivacaina al 0.25% (FIGURA 1).
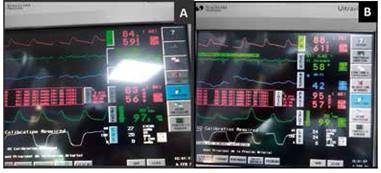
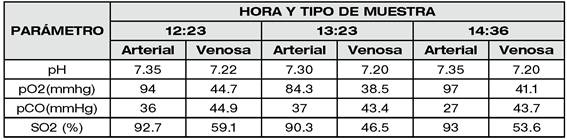
Se instaló línea arterial radial izquierda y catéter venoso central (CVC) subclavio. El mantenimiento de la anestesia se realizó con sevofluorano 1%-1.5%, fentanil y rocuronio a demanda. Durante el transoperatorio mantuvo una FC entre 60 - 70lpm y la PAM entre 57 - 67mmHg (FIGURA 2) con soporte vasopresor (noradrenalina 0.05-0.2ug/kg/min) por CVC. Se realizaron gasometrías arteriales y venosas para el control de la pCO2 y la SvO2 (TABLA 1). Concluido el procedimiento quirúrgico, la extubación se efectuó sin complicaciones previa administración de 6 puff de salbutamol por TET y lidocaína 2% 80mg IV. Como coadyuvantes se administraron ácido tranexámixo 1g IV, metoclopramida 10mg IV, dexametasona 8mg IV, paracetamol 1g IV y albúmina 20% 100ml IV. El balance hídrico fue negativo (92mL) con flujo urinario de 0.8mL//kh/h. Paciente pasó despierta y estable a la Unidad de Recuperación Postanestésica (URPA) y posteriormente a sala de internación del servicio de cirugía.
DISCUSIÓN
En pacientes cardiópatas que serán sometidos a cirugía no cardiaca, el manejo anestésico perioperatorio óptimo, debe basarse en el intercambio de información clínica entre anestesiólogos, cardiólogos, cirujanos y otros especialistas relevantes. Los pacientes con IC, valvulospatías e HAP plantean importantes desafíos perioperatorios, es por eso que para su manejo anestésico es necesario considerar los siguientes puntos:
Evaluación cardiaca preoperatoria y exámenes complementarios.
Hay 3 aspectos fundamentales para una correcta evaluación cardiaca preoperatoria: definir factores de riesgo mediante índices y/o puntuaciones, tipo de cirugía y la capacidad funcional.
De los índices clínicos de riesgo, 2 son los aceptados: Índice de Riesgo Cardíaco Revisado (Revised Cardiac Risk Index - RCRI) y el modelo de predicción del Colegio Americano de Cirujanos (ACS-NSQIP). El RCRI no requiere una conexión a internet, mientras que el ACS-NSQIP está disponible en internet y es específico para cada procedimiento6. El RCRI estima el riesgo de muerte, infarto de miocardio o parada cardiaca a los 30 días y se basa en seis variables (CUADRO 1)
CUADRO 1: Indice de Riesgo Cardiaco Revisado (RCRI en ingles)
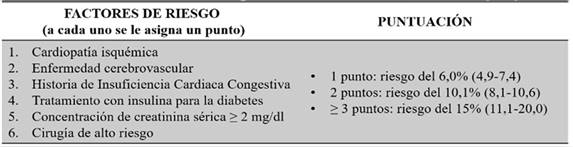
Fuente: 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery
El riesgo relacionado con la cirugía está determinado por el tipo y duración del procedimiento quirúrgico, además de la urgencia de la operación. La estimación del riesgo quirúrgico es un cálculo aproximado del riesgo de muerte cardiovascular, infarto de miocardio e ictus a los 30 días asociado a un procedimiento quirúrgico específico y no tiene en cuenta las comorbilidades de los pacientes9(CUADRO 2). La cirugía laparoscópica, comparada con la cirugía abierta, no reduce el riesgo cardiovascular de pacientes con enfermedad cardiovascular y se debe evaluar ambas opciones de la misma forma6.
CUADRO 2: Riesgo cardiovascular de acuerdo al procedimiento quirúrgico

Fuente: Urrea et al. Rev Colomb Cardiol. 2015;22(5):235-43.
La evaluación de la capacidad funcional (CUADRO 3) aporta información sobre la posibilidad de complicaciones cardíacas y necesidad de profundizar en estudios diagnósticos10,11. Pacientes con buena clase funcional (es decir >4 MET), pueden proceder con la cirugía programada sin necesidad de estudios adicionales o nueva terapia farmacológica. En pacientes con capacidad funcional baja (es decir <4 MET), si la cirugía es de riesgo intermedio (1 a 5%) además de la optimización médica preoperatoria, se recomienda llevar al procedimiento quirúrgico sin estudios adicionales4.
CUADRO 3: Capacidad funcional según los equivalentes metabolicos
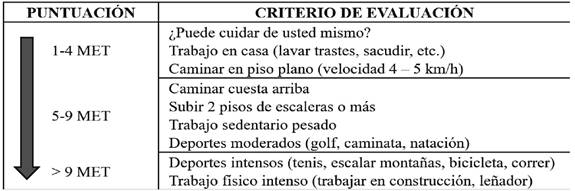
Fuente: Cruz -Ahumada S. Rev Mex Anestesiol. 2022;45(4):253-6.
Los exámenes preoperatorios que forman parte de la evaluación cardiaca y conducta para cirugía no cardiaca en pacientes de riesgo intermedio y alto son: a) Electrocardiograma (ECG): recomendado un EKG preoperatorio de 12 derivaciones en pacientes ≥65 años o con enfermedad cardiovascular conocida, factores de riesgo cardiovascular o síntomas indicativos de trastornos cardiacos o una puntuación de RCRI ≥ 11,6,10, b) Rx de tórax: Es para valorar situaciones específicas: enfermedad cardíaca y/o respiratoria descompensada e infección respiratoria baja6,10, c) Biomarcadores (troponinas cardíacas, péptido natriurético tipo B (BNP) y fracción N-terminal del propéptido natriurético cerebral (NTproBNP)): se recomienda su determinación, antes de la cirugía y 48-72h después, en pacientes de alto riesgo (<4 METs o RCRI >1 para cirugía vascular y >2 para cirugía no vascular), ECV conocida y factores de riesgo cardiovascular o ECV significativa6,10, d) Ecocardiograma transtorácico: en pacientes con sospecha/diagnóstico de falla cardíaca, capacidad funcional baja o con concentraciones altas de NT- proBNP/ BNP. Una fracción de eyección del ventrículo izquierdo (FEVI) <30% es predictor de resultados adversos perioperatorios y muerte1,6,10.
Consideraciones anestésicas y manejo intraoperatorio.
Insuficiencia cardiaca (IC): es un síndrome clínico complejo causado por cualquier trastorno cardíaco estructural/ funcional que afecta la capacidad del corazón para satisfacer las demandas metabólicas del organismo y suele ser secuela de una amplia gama de patologías subyacentes, entre ellas la cardiopatía valvular1. Para su manejo perioperatorio se recomienda administrar tratamiento médico óptimo. Debe prestarse especial atención al estado volémico del paciente, monitorización invasiva de la presión arterial para obtener parámetros oximétricos y metabólicos. Además, las variables dinámicas derivadas de la onda de la presión arterial (gasto cardiaco, variación volumen latido, variación de la presión del pulso) son útiles para guiar la terapia con objetivos protocolizados. El uso de otras técnicas invasivas, como cateterismo derecho o ecocardiografía transesofágica, debe valorarse en función de cada paciente. Debe mantenerse la medicación durante el periodo perioperatorio. Para los pacientes con descompensación aguda de IC en el posoperatorio, se recomienda realizar un EKG, la determinación de biomarcadores de daño miocárdico y un estudio ecocardiográfico con el fin de optimizar la estrategia terapéutica6,10.
Miocardiopatía dilatada (MCD): son enfermedades del miocardio asociadas con disfunción cardíaca. Su clasificación aún está evolucionando y hasta ahora se ha clasificado en dilatada, hipertrófica y restrictiva2. Los objetivos anestésicos incluyen reducción de la poscarga, optimización de la precarga y minimizar la depresión miocárdica. El fentanilo produce excelente anestesia y hemodinámica en pacientes con fracción de eyección inferior al 30%; la ketamina es una excelente opción con una dosis de alrededor de 0,5mg/kg junto con el fentanilo en pacientes con depresión miocárdica grave secundaria a miocardiopatía; y el uso de propofol sigue siendo motivo de preocupación debido a la depresión miocárdica1,4,10. La inestabilidad hemodinámica se puede tratar con inotrópicos y vasodilatadores en dosis bajas. Inhibidores de la fosfodiesterasa junto con agonistas beta como la milrinona y la adrenalina proporcionan estabilidad hemodinámica transitoria. La reducción de la poscarga mejora el rendimiento ventricular bajo anestesia junto con el control de la regurgitación valvular y el volumen auricular. Deben evitarse la hipopotasemia, la hipomagnesemia y la estimulación simpática excesiva. Los medicamentos antiarrítmicos son peligrosos en pacientes con función ventricular deficiente debido a sus efectos inotrópicos negativos. La amiodarona es el agente preferido porque se asocia con menores efectos inotrópicos negativos en comparación con otros fármacos1,2.
Estenosis mitral: frecuente en mujeres de edad fértil y la causa más común es la enfermedad reumática3. La EM representa un estado de gasto cardíaco fijo. La anestesia general ofrece la ventaja del control hemodinámico, la anestesia neuroaxial puede ser peligrosa1,3. Los problemas principales en pacientes con EM incluyen el manejo de la precarga ventricular, la frecuencia cardíaca y la hipertensión pulmonar coexistente, así como la función contráctil del VD y VI posiblemente disminuida1,7. Para la precarga se debe apuntar a la normovolemia con un manejo juicioso de líquidos, teniendo en cuenta que los bolos de líquido pueden empeorar el edema pulmonar y una reposición adecuada de la pérdida de sangre3. Se debe mantener la poscarga ya que cualquier reducción de la resistencia vascular sistémica (RVS) puede provocar una disminución de las presiones de perfusión coronaria; puede ser adecuado reducir la RVS con un VI que tiene una disfunción sistólica marcada, pero se debe tener cuidado, porque una reducción en la poscarga está inevitablemente acompañada por una reducción en la precarga, que puede que no sea deseable en pacientes con EM significativa. Evitar la hipoxia, la hipercapnia y la acidosis para prevenir la descompensación aguda del ventrículo derecho1,3. Debe evitarse el uso de vasodilatadores arteriales y la detección de fibrilación auricular posoperatoria es de suma importancia. En pacientes asintomáticos con estenosis mitral moderada o grave y en pacientes sintomáticos, se debe considerar la comisurotomía mitral percutánea (CMP) antes de la cirugía no cardiaca de alto riesgo, o la cirugía no cardiaca solo debe realizarse si es imprescindible6. Se recomienda una monitorización hemodinámica invasiva que permite mantener una precarga adecuada. Los pacientes sintomáticos con hipertensión pulmonar pueden beneficiarse del catéter en la arteria pulmonar (CAP) y/o del eco transesofágico (ETE) para evaluar la función biventricular, la presión de la arteria pulmonar y la presión de la AI. Se deben mantener medicamentos como betabloqueantes, amiodarona, para el ritmo sinusal y la FC lenta; inotrópicos (adrenalina, milrinona) para apoyar la insuficiencia del corazón derecho; fenilefrina para mantener la RVS y óxido nítrico inhalado o prostaciclina para la hipertensión pulmonar3,12.
Insuficiencia tricuspídes: es una anormalidad valvular causada por dilatación del ventrículo derecho y el anillo tricuspídeo. Los pacientes con IT leve o moderada son generalmente asintomáticos. El tratamiento preoperatorio debe guiarse por la presencia de cualquier afección subyacente, la insuficiencia cardíaca derecha y la hipertensión pulmonar conocida o presunta. Ya no se recomienda la profilaxis de la endocarditis infecciosa. El manejo anestésico estará determinado fundamentalmente por la lesión valvular del lado izquierdo, ya que la mayor parte sucede en el contexto de una patología aórtica o mitral significativa. La excepción es la presencia de hipertensión pulmonar significativa e insuficiencia del VD. En estas condiciones, el principal impedimento para la estabilidad hemodinámica será la insuficiencia ventricular derecha. La colocación de un CAP será de gran ayuda y será más útil cuando se use la ETE intraoperatoria. El GC en la insuficiencia del VD podría aumentarse a menudo con vasodilatadores, y la optimización del GC se realizará mediante determinaciones seriadas del GC. La posibilidad de un desplazamiento septal y de un deterioro secundario de la distensibilidad diastólica del VI debería considerarse cuidadosamente cuando haya una distensión significativa del VD. La combinación de un inhibidor de la fosfodiesterasa con un vasodilatador y una infusión de catecolaminas será sumamente útil. Las determinaciones seriadas del GC para equilibrar la presión sistémica y el gasto y el llenado del VD serán cruciales12.
Hipertensión arterial pulmonar (HP): se define como una presión de arteria pulmonar (PAP) media >20mmHg o >30mmHg con el ejercicio, esto se asocia con intolerancia al ejercicio y disminución de la capacidad funcional, que parecen tener importantes repercusiones pronósticas6,13. Aunque el tratamiento está dirigido a la circulación arterial pulmonar, el objetivo final es para optimizar el rendimiento del lado derecho del corazón con el uso de diuréticos, oxígeno suplementario, reposición de hierro y el mantenimiento del ritmo sinusal para función óptima del VD. Los pacientes con HAP significativa son muy sensibles a la precarga; por lo tanto, la hipovolemia debe tratarse de forma inmediata e intensiva. Es fundamental proporcionar una anestesia suave desde la inducción hasta la recuperación. El uso tanto de agentes anestésicos volátiles como de anestesia intravenosa total (TIVA) sigue siendo seguro. Los anestésicos volátiles atenúan la respuesta de vasoconstricción pulmonar hipóxica, suprimen la RVS y aumentan las concentraciones de dióxido de carbono al final de la espiración. El isoflurano y el desflurano tienen reducciones dosis dependientes en la contractilidad del VD y aumentan marginalmente la RVP; el sevoflurano reduce la contractilidad del VD y tiene poca influencia sobre la RVP. Sin embargo, se debe evitar el óxido nitroso ya que aumenta la RVP. Los fármacos de inducción intravenosos, incluidos los opioides, se pueden emplear de forma segura en pacientes con HAP8. El etomidato (0,15-0,3mg/kg) tiene un efecto mínimo sobre los efectos sistémicos y RVP, frecuencia cardíaca y contractilidad, sin embargo; por su efecto inhibidor de la enzima adrenocortical debe evitarse. La ketamina está asociada con un aumento de RVP en adultos13, sin embargo, muchos estudios sugieren que el efecto de la ketamina sobre la RVP es mínimo y puede contrarrestarse con su efecto simpático positivo que aumenta el rendimiento del VD y mantiene la RVS. El propofol puede directa o indirectamente afectar negativamente la contractilidad del VD y debe utilizarse con precaución porque puede requerir la administración de un vasopresor o inotrópico. Los opioides, cuando se administra solos, tiene efectos mínimos sobre circulación pulmonar y reducen la respuesta al sistema simpático, pero pueden inducir bradicardia desfavorable en dosis mayores, el fentanilo (1-2μpg/kg) y lidocaína, 50 a 100mg IV, son útiles para mitigar aumentos del tono simpático durante la laringoscopia. Los objetivos de ventilación giran en torno a evitar la hipoxia, favoreciendo la hipocapnia leve (30-35mmHg) y evitar presiones inspiratorias altas y PEEP que puede comprometer el retorno venoso, reducen gasto cardíaco, aumenta la RVP y empeora la función del VD. Los objetivos hemodinámicos intraoperatorios en pacientes con HAP deben centrarse en prevenir la disfunción aguda del VD y mantener índice cardíaco para asegurar una perfusión adecuada del órgano terminal. Para esto de recomienda: evitar la hipotensión arterial sistémica (Noradrenalina hasta 0,5ug/kg/min es el tratamiento de primera línea), mantener un ritmo sinusal normal, evitar o mitigar los factores que se sabe que aumentan la RVP (hipoxia, hipercapnia, acidosis, hipotermia, y dolor), evitar presiones altas en las vías respiratorias (Pmest <28cmH2O, DV <15cmH2O) y presiones espiratorias positivas (PEEP baja de 5 a 10mmHg), mantener las condiciones de carga euvolémicas, optimizar la presión venosa central y la precarga del VD, aumentar la contractilidad del VD y la función cardíaca con apoyo inotrópico y mejorar la vasodilatación pulmonar para reducir la RVP y, siempre que sea posible, se deben considerar opciones de anestesia regional para evitar la anestesia general o para la disminución del dolor postoperatorio. La monitorización debe ser minuciosa y debe utilizarse presión arterial invasiva. El catéter venoso central se puede utilizar para monitorizar la saturación de oxígeno venoso central como sustituto de la oxigenación tisular.
Analgesia posoperatoria en pacientes cardiópatas.
El manejo del dolor posoperatorio es fundamental para disminuir morbilidad, estancia y costos hospitalarios, y se asocia a complicaciones cardiovasculares, pulmonares, mala respuesta al estrés quirúrgico, delirio, dolor crónico y consumo persistente de opioides. La analgesia regional es fundamental en el manejo del dolor perioperatorio y es recomendada por los programas ERAS (Enhanced Recovery After Surgery) para disminuir el uso de opioides y sus efectos colaterales. Se han estudiado diferentes técnicas de anestesia regional para cirugías que abarcan la región torácica y abdominal entre ellas los bloqueos interfasciales, como el bloqueo erector de la espina (ESP) el cual surge como una alternativa, debido a su efecto analgésico, perfil de seguridad y facilidad de realización mediante ultrasonido14,15.
CONCLUSIONES
La presencia de comorbilidades cardiovasculares aumenta el riesgo de complicaciones posoperatorias y/o muerte. El presente caso es un claro ejemplo del manejo anestésico durante todo el perioperatorio de pacientes cardiópatas sometidos a cirugía no cardiaca, en el cual se realizó una adecuada valoración preanestésica para estimar el riesgo perioperatorio. El manejo intra y posoperatorio se orientó a equilibrar la fisiopatología de la enfermedad cardiaca con los efectos de los fármacos anestésicos.
El aporte científico respecto a estos casos, constituye una herramienta fundamental en el desarrollo de habilidades teóricas y prácticas para una anestesia segura y de calidad.