INTRODUCCIÓN
La pandemia de gripe de 1918 fue el evento de mayor mortalidad en la historia humana (50 millones o más muertes, equivalente en proporción a 200 millones en la actual población mundial). Durante más de un siglo, se ha mantenido como un punto de referencia para analizar la dimensión de todas las demás pandemias y enfermedades emergentes. Debemos recordar la pandemia de 1918, cuando nos enfrentamos a otra enfermedad infecciosa emergente, como la creciente epidemia por la enfermedad por coronavirus en el 2019 (COVID-19) que dio origen al síndrome respiratorio agudo severo por coronavirus 2 (SARS-CoV-2) porque ya existía el SARS-CoV-1. Este virus se extendió en dos meses por toda China(1) con una diseminación mundial rápida que incluye: al continente Asiático, Europeo, América del Norte, Sud América, África, Oceanía y ha estado sembrando más de dos casos secundarios por cada caso primario.(1-2) La tasa de letalidad global estimada es de 5,3%.(3) Se trasmite por vía respiratoria de persona a persona por contacto directo, indirecto y posiblemente por vía fecal-oral.(1) El 11 de marzo de 2020 la Organización Mundial de la Salud ha declarado la epidemia como una emergencia de salud pública de preocupación internacional.(2)
Microbiología de los coronavirus
Los coronavirus (CoV) (derivan de la palabra latina corona) se denominan así, porque con microscopía electrónica se observa que tienen una superficie cubierta de proyecciones en forma de una corona que sobresalen hacia la periferia y corresponden a las proteínas de superficie largas que tienen forma de espigas. (4-5) Pertenecen a la familia coronaviridae y orden Nidovirales, forman parte de una gran familia de virus zoonóticos, poseen un genoma de ARN monocatenario de polaridad positiva.(6) Cada partícula viral tiene un diámetro de 60-140 nm y posee una membrana glucoproteíca que envuelve al material genético (figura 1)(7)
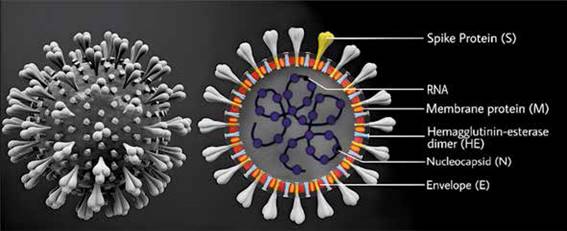
La figura representa la estructura viral del SARS-CoV-2. La glucoproteína espiga (proteína S) confiere una apariencia de corona al virus, de ahí el nombre “coronavirus”. La proteína S media la unión del virus a los receptores celulares. El papel de la hemaglutinina- esterasa (HE) en los coronavirus no se comprende bien, pero se informa que influye en la unión del virión en otros virus. Chakraborty R, Parvez S. COVID-19: An overview of the current pharmacological interventions, vaccines, and clinical trials.Biochem Pharmacol 2020;180:1-16
Figura 1. Microbiología y Patogenia de la COVID-19. Representación esquemática de la estructura SARS-CoV-2).
Estructura del genoma y factores virales relevantes en la transmisión de la enfermedad. El genoma completo de una cepa de SARSCoV-2 fue obtenido de una muestra de hisopado oro-faríngeo.(8) El SARS-CoV-1, el síndrome respiratorio de Medio Oriente (MERS-CoV), y el SARS-COV-2 tienen genomas de ARN de polaridad positiva de 27,9 kb, 30,1 kb y 29,9 kb respectivamente.(8-9) El SARSCOV-2 contiene un número variable (611) de marcos de lectura abierta (ORF).(10) Dos tercios del ARN viral se localizan en el primer ORF (ORF1a/b) que traduce dos poli-proteínas, la pp1a y pp1ab, y codifica 16 proteínas no estructurales (nsp1 a nsp16), mientras que los ORF restantes codifican cuatro proteínas estructurales esenciales que incluyen: la S, la de envoltura pequeña (E), de la matriz (M), otra de la núcleo-cápside (N) y varias proteínas accesorias, que interfieren con la respuesta inmune innata del hospedero. (10-12) La envoltura incluye tres proteínas: la proteína M que se une a la nucleo- cápside y mejora el ensamblaje viral y la gemación; la proteína E involucrada en la morfogénesis viral, la liberación y la patogénesis; y la proteína S es la encargada de reconocer al receptor celular que ayuda al virus invadir las células blanco.(13)
Wu y col.,(14) realizó una secuenciación meta-transcriptómica profunda en el Wuhan-Hu-1 coronavirus (WHCV), que contenía 16 NSP y exhibía similitud genómica y filogenética con el SARS- CoV, -en particular- en el gen de la glucoproteína S y del dominio de unión al receptor (RBD), que indica la capacidad de transmisión humana directa. Si comparamos la secuencia de todo el genoma del SARS-CoV, del MERS-CoV y SARS-CoV-2, este último es el que tiene mayor similitud al coronavirus de los murciélagos. La mayoría de las proteínas genómicas codificadas de los SARS- CoV-2 son similares a los SARS-CoV con ciertas diferencias proteicas, si bien, no hay sustituciones de aminoácidos en NSP7, NSP13, sobre, matriz o proteínas accesorias p6 y 8b, estas son evidentes en NSP2, nSp3, proteína S y RBD.(15) La mutación en NSP2 y NSP3 es relevante en la capacidad infecciosa y mecanismo de diferenciación de SARS-CoV-2.(16) Zhang y col.,(17) analizó el genotipo de la COVID-19 en diferentes pacientes de varias provincias y descubrieron que el SARS-CoV-2 había mutado en distintos pacientes en China. Aunque el grado de diversificación de SARS-CoV-2 es menor respecto a la mutación de la gripe aviar H7N9.(18) Tang y col.,(19) realizaron análisis genéticos poblacionales de 103 genomas de SARS-CoV-2 y clasificó dos tipos mayores de evolución prevalentes, el tipo L (~ 70%) y tipo S (~ 30%). Las cepas en el tipo L, derivadas del tipo S, son evolutivamente más agresivas y contagiosas. Por lo tanto, los virólogos y epidemiólogos necesitan monitorear de cerca el nuevo coronavirus, para identificar de manera adecuada la virulencia y la epidemia.
Replicación y patogenia del coronavirus. Se ha confirmado que la enzima convertidora de angiotensina 2 (ACE2), que se encuentra en la parte externa de las células del tracto respiratorio inferior, es reconocida como el receptor de entrada celular del SARS-CoV y SARS-CoV-2(20-21) y es el responsable de regular tanto la transmisión entre especies como la diseminación de persona a persona, pese a la variación importante de aminoácidos en el SARS-CoV-2.(21-22) La glucoproteína-S que se halla en la superficie del coronavirus, es la encargada de unirse al receptor ACE2 de las células humanas. (23) Posee dos subunidades, la S1 que identifica a las células union luego, ingresa y finalmente se replica; (4,25) asimismo, es la responsable del tropismo celular junto al dominio de unión del receptor - RBD, mientras S2 media la fusión de la membrana celular del virus con dos dominios el “heptad repite 1” (HR1) y HR2. (26-27) Luego de producirse la fusión de la membrana, el genoma ARN viral se libera en el citoplasma y traduce dos poliproteínas, la pp1a y pp1ab, que codifican proteínas no estructurales, y forman el complejo de replicación- transcripción (RTC) en una vesícula de doble membrana.(28-29) Luego el RTC se replica y sintetiza un conjunto anidado de ARNs sub-genómicos, que codifican proteínas estructurales y accesorias. (30) El retículo endoplásmico (ER) y el aparato de Golgi, (31) nuevamente forman el ARN genómico, las proteínas del cápside nuclear y de envoltura. Las glucoproteínas se ensamblan y forman brotes de partículas virales. Finalmente, las vesículas que contienen viriones se fusionan con la membrana celular plasmática para liberar el virus a la circulación sanguínea. (7,32) En resumen, podemos señalar que la unión y la afinidad de la glucoproteína S al receptor ACE2 es un paso crítico para la entrada del virus. La detección sistemática de los receptores Kl-CoV muestran que las células humanas que expresan ACE2, pero no dipeptidil peptidasa-4 humana (DPP4) o amino- peptidasa N (APN), aumentan la afinidad del SARS-CoV-2 para ingresar a la célula.(32) La unión de la proteína S al receptor ACE2 es de 10 a 20 veces más alta que el SARS-CoV.(33) A diferencia del SARS-CoV, la COVID-19 se transmite con mayor facilidad, mientras causa una infección humana de menor gravedad, pero es menos virulento que el SARS- CoV y MERS-CoV porque tiene una tasa de mortalidad menor.(9)
La familia Coronaviridae puede infectar a una variedad de animales (incluido el ganado, mascotas y aves) y producir serios problemas respiratorios, entéricos y neurológicos.(34-35) Se dividen en cuatro géneros: alfa, beta, delta y gamma, de los cuales los coronavirus (CoV) alfa y beta se hallan principalmente en mamíferos, como murciélagos, roedores, civetas y humanos.(36-38) En humanos, los CoV causan, en especial, enfermedades respiratorias con síntomas gastrointestinales, que van desde el resfrío común hasta enfermedades más severas que incluyen a la bronquitis, neumonía, síndrome de dificultad respiratoria aguda severa, coagulopatía, falla orgánica múltiple y muerte. (36,39-42) Los coronavirus humanos (HCoV) también se asocian con exacerbaciones de enfermedad pulmonar obstructiva crónica, fibrosis quística y asma. (43-45) Los CoV delta y gamma tienden a infectar a las aves.(46)
Los CoV tienen la capacidad de mutar, recombinarse rápidamente y promover nuevos coronavirus que pueden diseminarse de animales a humanos(47) En un inicio se identificaron 4 HCoV que pueden infectar a los humanos susceptibles (HCoV-229E, NL63, OC43 y HKU1). Se caracterizan por ser endémicos y de baja patogenicidad en todo el mundo.(46,48) Los otros tres, SARS-CoV-1, síndrome MERS- Co y SARS-CoV-2 producen el SDRA, potencialmente fatal.(46)
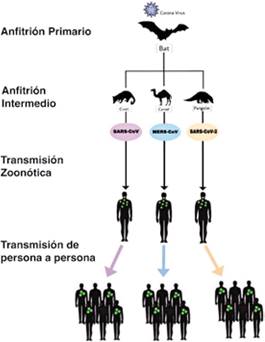
El virus responsable de la COVID-19, mide de 60 nm a 140 nm y es más grande que los virus de influenza, SARS-CoV-1 y MERS,(7,24) pertenece al género beta-coronavirus zoonótico, subgénero sarbecovirus, subfamilia Orthocoronavirinae.(22,49) Es un descendiente de los varios coronavirus del murciélago. El más parecido genéticamente al SARS-CoV-2 es el virus que se originó del murciélago Rhinolophus que tiene una homología del 96,2%, mientras que la similitud con el SARS-Cov-1 es tan solo del 79,5% y con el MERS-CoV 51.8%.(50) Si bien, desde un punto de vista filogenético la COVID-19 se relaciona con los coronavirus que producen SARS; sin embargo, las proteínas ORF8 y ORF3b le confieren diferencias en patogenicidad y transmisión de la enfermedad. (51) Las secuencias genéticas casi idénticas de 90 casos analizados fuera de China, sugieren que el SARS-CoV-2 surgió del murciélago y fue transmitido al humano por otros animales de momento desconocidos que sirvieron de hospederos intermediarios (probablemente mamíferos), que facilitaron la recombinación, mutación y expansión de su diversidad genética. (49,50,52) Los siguientes hechos, sugieren la presencia de otro animal que estaría actuando como anfitrión intermediario entre el murciélago y el humano: primero, cuando se informó del brote a finales de diciembre de 2019, la mayoría de las especies de murciélagos de Wuhan estaban hibernando; segundo, no había murciélagos para la venta ni se encontró ninguno en el mercado de mariscos de Wuhan, mientras que varios animales no acuáticos (incluidos mamíferos) estuvieron disponibles para la compra; tercero, la identificación secuencial entre el nuevo coronavirus 2019 (nCOV- 19) y sus parientes más cercanos (bat- SL-CoVZC45 y bat-SL-CoVZXC21) fue inferior al 90%.(22) Por lo tanto, ambos no son antepasados directos del nCOV- 19 y; cuarto, en el SARS-CoV y MERS- CoV, los murciélagos actuaron como reservorio natural, con otro animal, los gatos civeta (mamíferos nocturnos, cuya carne se vende en China) para SARS-CoV(53) y camellos dromedarios para el MERS-CoV)(54) que actúo como hospedero intermediario e infectó a los humanos que se constituyen en el hospedero final (figura 2). Por ello, sobre la base de los datos actuales, parece probable que el nCoV-19 que causo el brote de Wuhan, se alojó inicialmente en murciélagos y luego fue transmitido a humanos a través de uno o más animales salvajes que se vendían en el mercado de Wuhan. Los científicos en Guangzhou han demostrado un coronavirus del pangolín que posee una homología del 99%, con un receptor de unión idéntico al del SARS-CoV-2. Sin embargo, el pangolín, es un mamífero que se alimenta de hormigas y se halla en peligro de extinción porque es muy traficado en el mundo por la propiedades medicinales de su carne y sus escamas; considerando su rareza, puede no ser el único mamífero involucrado; sin embargo, esta teoría no ha sido confirmada.(7,24)
Esta representación esquemática ilustra el origen ecológico, los diferentes animales hospedadores y la posterior transmisión de SARS-CoV, MERS-CoV y SARS-CoV-2 a la población humana, lo que finalmente resultó en las tres principales epidemias / pandemias del siglo XXI.
EPIDEMIOLOGIA
Los coronavirus en un inicio fueron reconocidos en 1930 como patógenos de animales. Treinta años más tarde, fueron identificados como patógenos humanos el HCoV 229E y el OC43 (OC es el acrónimo en inglés de cultivo de órgano).(4-5) Los coronavirus HCoV NL63 y HKU1 se describieron en 2004 y 2005, respectivamente, y junto con HCoV 229E y OC43 se transmiten por secreciones respiratorias. (4) En general, son los responsables de hasta un 35% de las infecciones leves del tracto respiratorio superior (similares al resfrío común) durante las fases de máxima actividad viral. (4,55) En conjunto, la proporción de resfriados en adultos por HCoVs puede estimarse de forma razonable en un 15%.(4) Pueden ser aislados en el 4% al 6% de niños hospitalizados por infecciones agudas del tracto respiratorio. (44,56-57) y en el 8% de los niños en un entorno ambulatorio. (56,58-59) Son afectados con mayor frecuencia los niños menores de 3 años y aquellos con una cardiopatía de base. (56,60-61) Se han descrito casos fatales por HCoV NL63 en inmunodeprimidos. (62-63) Los datos de seroprevalencia sugieren que la exposición a estos coronavirus es común en la infancia temprana y cerca del 90% de los adultos son seropositivos para el 229E, OC43 y NL63 y 60% para el HKU1.5 Sin embargo, son frecuentes las reinfecciones,(5,64-65) pese a que la mayoría de las personas presentan seroconversión a HCoVs durante la infancia. (66-68) A diferencia de otros virus del tracto respiratorio (v.g. virus sincicial respiratorio (VSR)) no disminuye su prevalencia al incrementarse la edad. (39-40) En el 11% a 46% de los casos son detectados en coinfecciones con otros patógenos virales como: adenovirus, bocavirus, sincicial respiratorio, influenza y parinfluenza, siendo difícil comprender su verdadero papel. (47) De los 4 HCoV circulantes comunes, el NL63 y OC43 son las especies aisladas con mayor asiduidad.(39,44,56,60-61) Se ha observado patrones cíclicos con brotes cada 2-4 años de 229E y OC43,(39,56,60,65,69,70-72) de ambos el OC43 es el más prevalente y es identificado sobre todo en niños menores de 5 años. (71) Los HCoVs 229E, OC43, NL63 y el GHKU1 se hallan distribuidos en todo el mundo y causan mayor enfermedad en los meses de invierno y primavera.(5) En el hemisferio norte, los HCoV circulantes causan infecciones humanas entre diciembre y mayo, en el Hemisferio Sur entre marzo y noviembre con picos de infección por 229E y OC43 a finales de invierno y principios de la primavera y de NL63 en otoño. El HKU1 se presenta en primavera y verano en Hong Kong, pero en invierno y primavera en el Reino Unido y Brasil.(47)
Si bien, los coronavirus son agentes causales de infecciones respiratorias e intestinales en animales y humanos,(11) no fueron considerados altamente patógenos para el hombre hasta el brote del síndrome respiratorio agudo severo (SARS) en la provincia de Guangdong, China en el 2002 y 2003,(73-76) donde causó un brote que duro 9 meses con 8.096 casos y 774 fallecimientos, (5) similar a los coronavirus comunes que circulaban antes de ese tiempo, causó infecciones leves en humanos, en especial, en la población inmunocompetente. Diez años después del SARS, desde septiembre de 2012, surge otro coronavirus altamente patógeno en los países del Medio Oriente, siendo denominado síndrome respiratorio por coronavirus del Medio Oriente (MERS-CoV).(77) Al inicio, fue identificado en un hombre de 60 años de Arabia Saudita que presentó neumonía aguda severa y falleció por insuficiencia respiratoria y falla renal. (4-5) Este virus fue el responsable de 2.494 casos confirmados de infección con 858 muertes, incluyendo 38 fallecimientos en Corea del Sur.(78-79) Hasta la fecha, se continúa informando casos de MERS-CoV en personas que residen o han viajado a Medio Oriente o tuvieron contacto con un caso de dicha región. Se ha observado transmisión de persona a persona que incluye grupos de casos. Sin embargo, en base a la información disponible de todos los países recientemente afectados, no hay evidencia de transmisión humana sostenida en la comunidad. (5) SARS- CoV (SARS- CoV-1) y MERS- CoV se transmitieron directamente a humanos de civetas de mercado y camellos dromedarios, respectivamente,(53,54-80) y se cree que ambos virus se originaron en murciélagos. (81-87) El coronavirus del SARS-CoV-1 utiliza como receptor a la enzima convertidora de angiotensina-2 (ACE2) e infecta, en particular, a las células epiteliales ciliadas de los bronquios y a los neumocitos tipo II,(88-89) mientras que el MERS-CoV usa como receptor a la dipeptidilpeptidasa 4 (DPP4), también conocida como CD26 e infecta a las células epiteliales bronquiales no ciliadas y neumocitos tipo II.(90-92)
En diciembre de 2019, en Wuhan, provincia de Hubei en China se presentaron una serie de casos de neumonía, causados por un recientemente identificado K-coronavirus de linaje B(49,93) La mayoría de los enfermos tenían una historia de exposición en el mercado de Wuhan, donde se vendían mariscos, pescados y muchas especies de animales vivos, lo que induce a pensar que tuvieron contacto con la fuente de infección en dicho mercado. El 31,3% de los pacientes enfermos recientemente habían viajado a Wuhan y el 72.3% de los no residentes de Wuhan tuvieron contactó con personas de esta ciudad. (94) Sin embargo, llama la atención que un paciente nunca visitó este sitio, pero tenía el antecedente de haberse alojado en un hotel cercano al mercado, antes del inicio de su enfermedad; este hallazgo sugiere una posible transmisión por gotas o que el paciente fue infectado por una fuente en la actualidad desconocida.(22,95) El 12 de enero de 2020 la Organización Mundial de la Salud (OMS) lo denomino como el nuevo coronavirus 2019 (nCoV-19) y el 11 de febrero de 2020 designa de manera oficial a este padecimiento como “enfermedad por coronavirus 2019 (COVID-19)”.(96) En la misma fecha el Comité Internacional de Taxonomía de Virus, lo renombro como síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2).(12) El 7 de enero de 2020 los científicos chinos, aislaron en un paciente al SARS-CoV-2 y realizaron la secuenciación de su genoma.(22).
Hasta el 2 de octubre de 2020 se registraron en el mundo (188 países) 34.471.204 casos y 1.025.815 muertes, en Bolivia se registraron se 136.219 casos con 8.045 decesos con un porcentaje de letalidad del 5,9%. El comportamiento de la curva epidemiológica en nuestro país se señala en la figura 3.
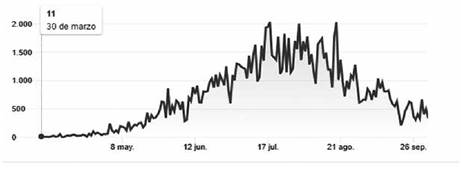
https://datosmacro.expansion.com/otros/coronavirus/bolivia año=2020
Figura 3 Numero de casos de la COVID-19 en Bolivia desde marzo a octubre de 2020
La definición operacional de caso sospechoso de COVID-19 en Bolivia ha cambiado desde el 19 de abril de 2020. El Ministerio de Salud señala que la nueva definición basada en protocolos internacionales vigentes, incluye a toda persona de cualquier edad que presente fiebre de 37.5°C o más, y uno o más de los siguientes síntomas: tos, dolor de garganta, falta de olfato o gusto (anosmia/disgeusia) sin otra enfermedad que explique completamente el cuadro clínico.
A estas características clínicas, se suma el hecho de que esa persona haya estado en los últimos 14 días en contacto con casos confirmados de COVID-19 o tenga un antecedente de viaje internacional o también un historial de viaje o residencia en zonas de transmisión local de coronavirus ya sea comunitaria o por conglomerados. La decisión de ampliar el criterio de caso sospechoso está relacionada con la llegada del frío y todo lo que el otoño y el invierno traen aparejados en cuanto a enfermedades estacionales.
En otros países como México, (97) la definición de caso sospechoso incluye: a todo paciente persona de cualquier edad que en los últimos 7 días haya presentado al menos dos de los siguientes signos y síntomas: tos, fiebre o cefalea. Acompañados de al menos uno de los siguientes signos o síntomas:
Dificultad respiratoria (dato de alarma), dolor en las articulaciones, muscular, de garganta, escurrimiento nasal, conjuntivitis (enrojecimiento, prurito y ojos llorosos, dolor en el pecho)
En menores de 5 años de edad, la irritabilidad puede sustituir a la cefalea.
De acuerdo a la evidencia disponible, los niños tienen una forma más leve de enfermedad causada por los coronavirus, incluyendo SARS-CoV-2. que los adultos. (98) y que las tasas de ataque clínicas del grupo de edad de 0 a 19 años son bajas.(99) De otra parte, la enfermedad leve en los niños puede estar relacionada con una inmunidad preparada, que se refiere a un nuevo modelo inmune por el empleo de ciertas vacunas como el bacilo de Calmette- Guerin (BCG) que activa la inmunidad innata y genera memoria inmune. Se ha demostrado que la BCG proporciona protección inespecífica contra la infección por virus de la gripe en ratones, probablemente por la inducción de inmunidad.(91) Otros datos preliminares de estudios en China relacionados con la transmisión en el hogar, sugieren que los niños se infectan de los adultos y no al revés. La mayor revisión de serie casos publicada por el grupo “Chinese Novel Coronavirus Pneumonia Emergency Response Epidemiology Team”: en 73.214 sujetos con 44.672 casos confirmados informa que solo el 2% fueron niños de 0 a 19 años, con un fallecido en el grupo de 10-19 años y sin defunciones en el de 0-10 años. (100) En el estudio de Dong y col. en 2.135 pacientes pediátricos (menores de 18 años),(95) con una media de edad de 7 años, de los cuales 1.208 casos (56,6%) fueron varones. Más del 90% fueron asintomáticos o presentaron una enfermedad leve o moderada, 5,2% tuvieron un cuadro grave y 0,6% una enfermedad crítica. La media del tiempo de inicio y diagnóstico de la enfermedad fue de 2 días (rango: 0-42 días). Concluye señalando que si bien todos los niños son susceptibles al COVID-19, incluyendo al recién nacido, presentan manifestaciones clínicas menores. Respecto al sexo, no existe una diferencia significativa. Si bien, en general, las manifestaciones clínicas en niños son menos severas comparadas con los adultos, los lactantes y niños menores de 5 años son los más vulnerables.
Si bien, el porcentaje de letalidad es incierta, se estima que se encuentra en un rango de 2 y el 5%, más baja que el SARS-CoV y MERS-CoV (6%-17% y 20% a 40% respectivamente). (7,47,101) La transmisión de COVID-19 entre los trabajadores de salud ocurrió en el 3.8%. Al contrario, la transmisión del SARS-CoV y del MERS-CoV es en especial es nosocomial, las infecciones en el personal de asistencia en salud se presentaron en el 33-42% en el SARS y en el 62-79% de MERS-CoV (la ruta más común de infección). (102-103)
Durante las últimas dos décadas, los brotes de coronavirus y las emergencias intermitentes de salud pública en todo el mundo nos recuerdan que estos virus siguen siendo una grave amenaza para la salud mundial y no deben ser ignorados. Según las últimas investigaciones, se necesita con urgencia información útil para el control de la enfermedad. (2)
El SARS-CoV-2 es sensible a los rayos ultravioleta y cuando se calienta a 60°C durante 30 minutos.(7) Los disolventes lipídicos como el éter, etanol, desinfectantes que contienen cloro, el ácido peracético y el cloroformo pueden inactivar eficazmente el virus (se describen con mayor detalle mas adelante).(2) El jabon es igualmente eficaz porque disuelve fácilmente la bicapa lipídica del virus.(7)
¿Como se transmite el COVID 19?
Se transmite de persona a persona por contacto directo con secreciones respiratorias de personas infectadas. Estas secreciones pueden diseminarse por gotas respiratorias (> 5 micras) que pueden alcanzar hasta dos metros de distancia cuando los pacientes hablan tosen o estornudan, otra forma de transmisión indirecta se produce al tocar manos, objetos (juguetes y perillas de las puertas) o superficies contaminadas con el virus y posterior contacto con la mucosa oral, ocular o nasal, requiriéndose una dosis infectante baja para lograr este propósito. (96,98,104) Las personas asintomáticas y presintomáticas también pueden transmitir la infección. (7) A diferencia de los coronavirus comunes que se trasmiten en los primeros días de la enfermedad y del SARS-CoV y MERS- CoV que se propagan durante la segunda semana de enfermedad, el SARS- CoV-2 es contagioso desde el inicio del período de incubación.(5,105) Se han creado situaciones experimentales, donde se demuestra que es viable en aerosoles (< 5 μm) durante 3 horas, hasta 72 horas en superficies de plástico y acero inoxidable, menos de 24 horas en superficies de cartón y menos de 4 horas en superficies de cobre; esta información sugiere que es posible la transmisión por aerosoles y fómites (dependiendo del inóculo) y al igual que el SARS-CoV-1, estas formas de transmisión pueden asociarse a diseminación y superdifusión nosomial. (48,106) También ha sido aislado en hisopos de heces en un paciente con neumonía grave.(107) Los hallazgos de SARS-Cov-2 en sangre y en heces, nos orientan a pensar en otras formas de transmisión múltiple. Como la proteína receptora del virus la ACE-2 se halla presente en abundancia sobre las células epiteliales alveolares del pulmón y en los enterocitos del intestino delgado, (108) puede ayudarnos a comprender las rutas de infección y manifestaciones clínicas. (105) Las principales razones de la velocidad de propagación del COVID-19 son: su alta tasa de reproducción (Ro) que varía de (2) a (6,47), a su largo período de incubación y un intervalo serial (SI) de 5 a 7.5 días. (7,109)
El período de incubación del COVID-19 es de 2 a 14 días,con una media de 3-7 días,(55,110) similar al SARS-CoV y MERS-CoV.(47,95,119,111-112) El inicio de los síntomas en el 97.5% de los casos se presentó en los primeros 11.5 días (IC, 8,2-15,6 días).(112) Mientras que la evidencia actual indica que en niños es de 2 días y se puede prolongar hasta 10 días. (113) La recuperación se ha producido en todos los casos entre 1 a 2 semanas. (55)
Transmisión vertical y COVID-19. La transmisión vertical hasta el momento no está documentada.(114) El estudio más reciente que incluyó a 33 mujeres embarazadas que presentaron infección por COVID 19, evidenció la presencia del virus en tres neonatos, a pesar de haber tenido las precauciones recomendadas, sugiriendo una posible transmisión vertical; sin embargo, esta afirmación continúa siendo controversial.(115) Chen y col., estudiaron nueve mujeres embarazadas con la COVID-19, en quienes luego del nacimiento por cesárea, se realizó RT-PCR para SARS- CoV-2 en líquido amniótico, sangre de cordón, exudado faríngeo del neonato y leche materna, resultando todas las pruebas negativas. (114) El estudio observacional de cohorte reciente de Salvatore y col.,(116) realizado en 120 neonatos, concluye señalando que es poco probable que se produzca la transmisión perinatal de la COVID-19 si se toman las precauciones de higiene correctas y concluyen señalando que permitir que los recién nacidos compartan el espacio con sus madres y realizen una lactancia materna directa son procedimientos seguros cuando se combinan con la educación efectiva de los padres sobre estrategias de protección infantil.
Lactancia materna. Se realizaron pruebas para reconocer al SARS CoV-2 en la leche de mujeres con COVID-19, pero hasta el momento no se ha identificado el virus. (114) La OMS recomienda mantener la lactancia materna tanto para casos de madres confirmadas como probables, enfatizando las medidas de prevención como el lavado de manos antes y después de tocar al bebe, limpiar y desinfectar de manera rutinaria las superficies con las que tuvo contacto, etiqueta respiratoria (toser o estornudar en el ángulo interno del codo o con pañuelo que deberá ser desechado y luego lavarse las manos). Si la madre es positiva, una alternativa para evitar el contagio durante la lactancia sería la extracción de la leche. (116)
¿Cuales son las características clínicas de la infección por SAR- CoV-2?
Los niños infectados con SAR-CoV-2 tienen manifestaciones clínicas leves de buen pronóstico (tabla 1). Usualmente se recuperan dentro 1 a 2 semanas después del inicio de la enfermedad. (98) En un estudio de 1,391 niños que fueron contactos de casos positivos o sospechosos; en 171 se estableció el diagnóstico de COVID-19 y las manifestaciones clínicas más frecuentes incluyeron: tos (48,5%), dolor faríngeo (46,2%), fiebre (41,5%) y la duración promedio de la enfermedad fue de tres días (rango 1-16 días). Otros síntomas menos frecuentes fueron: diarrea, fatiga, rinorrea, vómito y congestión nasal. De los pacientes hospitalizados, el 28,7% presentaron taquipnea y 48,2% taquicardia. (117) Se dice que un niño presenta un cuadro severo (tabla 1) cuando manifiesta disnea, cianosis central y una saturación menor de 93% (en la altura 90%) y un cuadro crítico cuando presenta insuficiencia respiratoria, síndrome de dificultad respiratoria aguda, choque o falla multiorgánica (v.g. encefalopatía, falla cardiaca, alteraciones de la coagulación y falla renal).(100) De otras 3 series de casos de niños infectados con SARS-CoV-2,(118-120) el estudio con el mayor número de casos (34 niños) proporciona más detalles clínicos: ninguno de los niños tuvo una enfermedad subyacente, el 65% tenía síntomas respiratorios comunes, el 26% presentaron una enfermedad leve y el 9% eran asintomáticos. Los síntomas más frecuentes fueron fiebre (50%) y tos (38%). (118) En la serie de casos de 20 niños, observaron fiebre leve o moderada o ausente, rinitis, tos, fatiga, cefalea, diarrea y en los casos más severos, disnea, cianosis y falta de apetito pero no especificaron el número. (119) Finalmente, en la serie de casos de 9 infantes, solo 4 presentaron fiebre y un infante fue asintomático.(120) En conclusión, podemos afirmar que tanto fiebre como la tos son los síntomas que se presentan con mayor frecuencia en los niños. Sin embargo, la población pediátrica -en general- es asintomática o presentan infecciones menos graves (levemente sintomáticos). Por ello, las pruebas de diagnóstico se realizarían con menor frecuencia en comparación con los adultos. Sin embargo, este grupo etario es importante en la transmisión de la enfermedad.(121)
Como el receptor humano predominante (ACE2) para la glucoproteína S del SARS se encuentra principalmente en el tracto respiratorio inferior, en lugar de la vía aérea superior, su distribución explica la escasez de síntomas respiratorios superiores en el inicio de la enfermedad y la mayor diseminación viral sea tardía (≈10 días), cuando las personas ya se encuentran hospitalizadas. (9) Hasta ahora, la mayoría de los niños infectados con COVID-19, han sido parte de un brote en un grupo familiar (100% en la serie de lactantes),(120) donde otro miembro de la familia presentó previamente la enfermedad; 82% en la serie de casos de Wang XF y col., (118) y en la mayoría de la serie de 20 casos (número exacto no especificado). (119) Estos datos son similares a los encontrados en las infecciones por SARS-CoV, donde el 50% -80%de los niños tenían un contacto familiar enfermo y en el MERS-CoV 32%. (122-125) Un estudio publicado a principios de marzo de 2020, aclara que los niños tienen la misma probabilidad de infectarse con COVID-19 que los adultos, pero son menos propensos a ser sintomáticos o desarrollar síntomas severos.(126)
Estudios de laboratorio y gabinete útiles en COVID-19
En los niños infectados con COVID-19 podemos encontrar, en general, un recuento normal de leucocitos y neutrófilos, en ocasiones suele observarse linfopenia y trombocitopenia, similar a las infecciones por los nuevos CoVs.(118,122,124,127-129) En general, los niveles de proteína C reactiva (CRP) y procalcitonina (PCT) se encuentran normales.(119) En casos severos, es posible que se eleven las enzimas hepáticas y (119,122,124,129) el lactato deshidrogenasa,(122) las pruebas de coagulación pueden encontrarse anormales e incrementarse el dímero D.(119,122,124,129) Asimismo, los niveles altos de IL-6 se asocian con una mayor mortalidad en niños < 5 años con neumonía severa que requiere ventilación mecánica (Cuadro 1).(130-131)
En la serie de casos de 34 niños, el recuento de glóbulos blancos fue normal en 83%, neutropenia y linfopenia se encontraron en 1 caso (3%). Los niveles de lactato deshidrogenasa fueron elevados en el 30% de los casos y los de proteína C reactiva y procalcitonina en 1 caso solamente (3%).(118) En otro estudio realizado por Henry y col., que resume los resultados de 12 investigaciones, donde se analizan en total 66 niños, señala que el 69,6% de ellos tuvieron leucocitos normales, en el 15,2% un recuento incrementado y en el resto (15,2%) un recuento disminuido de acuerdo a los límites de referencia. La mayoría presento un recuento normal de neutrófilos, neutrofilia 4,6%, neutropenia 6% y linfopenia el 3%, la proteína C reactiva y la procalcitonina se encontraron elevadas en el 13,6% y 10.6% de los casos respectivamente. (127) En parte, la falta de linfopenia significativa puede explicar el número limitado de COVID-19 severo en niños. Yang y col.,(132) informó que el 80% de los pacientes adultos críticos enfermos con COVID-19 tenían linfopenia, mientras que Chen y col.,(133) señalan que solo el 25% de los pacientes con COVID-19 leve tenían linfopenia, sugiriendo que la misma puede correlacionarse con la gravedad de la infección. Sin embargo, puede no manifestarse en niños muy pequeños debido a la relativa inmadurez de su sistema inmune y diferencias en su respuesta inmune en comparación con adultos.(134-135) Finalmente, se recomienda considerar el recuento de linfocitos y la proteína C reactiva como signos de infección severa, mientras se monitoriza la PCT para identificar una potencial coinfección bacteriana. La IL-6 debe investigarse como un potencial indicador pronóstico en COVID-19 severo. (127)
Tabla 1. Evolución clínica y de las pruebas de laboratorio y gabinete en niños. (118-119, 122,124, 128-130,137,140)
| Leve | Severo | |
|---|---|---|
| Cuadro clínico | Tos, dolor faríngeo, fiebre (no siempre presente). Con menor frecuencia congestión nasal, rinorrea, diarrea, cefalea, fatiga y vòmitos | Una semana después malestar, irritabilidad, rechazo de alimentación, hipoactividad, taquipnea, taquicardia, disnea, cianosis central, insuficiciencia respiratoria, síndrome de dificultad respiratoria aguda y falla multiorgánica. En algunos casos progresión rápida (1-3 días), fallo respiratorio no reversible con oxígeno, choque séptico, acidosis metabólica, coagulopatía y sangrados |
| Hemograma | Leucocitos normales o leucopenia y linfopenia leves | Linfopenia progresiva y trombocitopenia |
| Proteína C reactiva | Normal | Normal o elevada (sospechar sobreinfección bacteriana) |
| Procalcitonina (PCT) | Normal | PCT > 0,5 ng/mL (sospechar sobreinfección bacteriana) |
| Bioquímica | Normal | Elevación de transaminasas, LDH, enzimas musculares, mioglobina, dímero D, IL-6 |
| Rx tórax | Normal o infiltrados periféricos intersticiales | Opacidades bilaterales en vidrio esmerilado, engrosamiento peribronquial e imágenes de consolidación en parche bilaterales y multiples a menudo en la periferia de los pulmones. Derrame pleural infrecuente |
| TAC tórax | Las imágenes nodulares en vidrio esmerilado y los infiltrados en la zona media y externa del pulmón o por debajo la pleura, más evidentes en laTAC que en la Rx | Pueden aparecer imágenes de consolidación en parche bilateral múltiples |
Hallazgos imagenologicos relevantes
Curiosamente, los cambios radiográficos que son característicos de la infección por SARS-CoV-2, también pueden observarse en pacientes pediátricos, inclusive en aquellos que no evolucionan a una enfermedad severa.(136) En la radiografía de tórax, los niños muestran principalmente imágenes de consolidación en parche bilateral a menudo en la periferia de los pulmones, engrosamiento peribronquial y opacidades en vidrio esmerilado.(122-124,128-129,137) En series de casos de pacientes pediátricos en varias regiones de China, informaron que el 50% al 80% de la los niños infectados tenían hallazgos anormales en la tomografía computarizada (TC),(138-139) que incluyen: múltiples opacidades en parche bilaterales, opacidades nodulares en vidrio esmerilado, y/o infiltrado en la zona media y externa del pulmón o debajo de la pleura (119,140) Estos hallazgos son inespecíficos y más leves en comparación con los adultos. (140)
Diagnóstico microbiológico. Se realiza mediante reacción en cadena de polimerasa a tiempo real (rRT- PCR) que identifica a los ácidos nucleicos del SARS-CoV2 o mediante la secuenciación del gen viral. Se puede emplear muestras del tracto respiratorio superior: frotis orofaríngeo y nasofaríngeo (más adecuados en niños), del tracto respiratorio inferior: esputo espectorado, aspirado endotraqueal o lavado bronquioalveolar, de heces o sangre. En laboratorios especializados, el virus puede ser aislado en cultivo de células epiteliales respiratorias. (142) Se recomienda realizar un panel para otros virus respiratorios para descartar una coinfección, especialmente con influenza.(55)
Cuando se realiza un estudio microbiológico, es importante conocer que los métodos de PCR existentes tienen muy buena especificidad pero una sensibilidad variable, [cuando la PCR tiene un ciclo umbral < 40 (Ct< 40) la sensibilidad es de 68%, y la especificidad del 100%, el valor predictivo positivo del 100% y el valor predictivo negativo de 32%; mientras que cuando el Ct< 30 la sensibilidad es del 98% y especificidad del 100%(143-144) lo que significa que en ocasiones, los resultados negativos de las pruebas no siempre excluyen la presencia de SARS-CoV-2. De otra parte, si se contamina la muestra por la falta de control puede conducir a resultados falsos positivos. Además, las pruebas de rRT-PCR pueden ser falsamente negativas debido a material viral insuficiente o error operativo. Algunos pacientes con resultados negativos de rRT-PCR pueden presentar hallazgos positivos de COVID-19 en la tomografía computarizada de tórax. Concluimos señalando que si bien los resultados de la rRT-PCR pueden ayudar al diagnóstico clínico y evaluación, en ocasiones no confirman ni descartan la enfermedad. Para los pacientes con alta sospecha clínica con un rRT-PCR inicial negativo, puede ser útil realizar tomografía computarizada y repetir la prueba. (143)
Se han desarrollado diferentes pruebas rápidas para el diagnóstico de COVID-19; sin embargo, la única aprobada por la “Food Drug Administration” (FDA), es la plataforma “GeneXpert” que puede identificar a los ácidos nucleicos del virus mediante RT-PCR en 45 minutos. (145)
Las pruebas serológicas pueden ser útiles para el diagnóstico, sobre todo en estudios epidemiológicos.(146) Solo deben recomendarse, cuando no se dispone de RT-PCR porque la seroconversión para IgM e IgG ocurre entre 5-7 días y 12-14 días respectivamente, de haberse iniciado los síntomas y su realización temprana puede dar a lugar a falsos negativos. (146-147)