INTRODUCCIÓN
Una de las intervenciones de salud con mayor impacto para reducir la carga y mortalidad por enfermedades infecciosa son las vacunas, las políticas de salud a nivel mundial priorizan especialmente grupos de riesgo como son los niños, ancianos, personas con enfermedades de base y embarazadas. Este último grupo tiene un riesgo incrementado para infecciones que pueden repercutir sobre la salud de la mujer y el feto, condicionando infecciones más graves en la mujer, parto prematuro o incluso muerte fetal1,2.
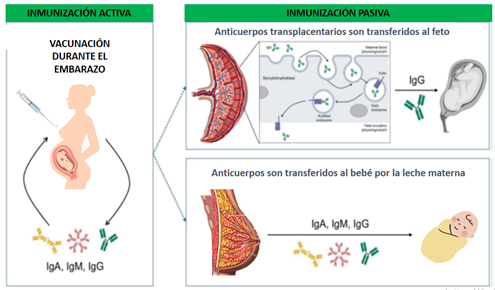
La vacunación de la gestante protege a la mujer, al feto y al niño en los primeros dos meses de vida donde aún no tiene oportunidad de recibir vacunas. Las vacunas en primer lugar protegen a la mujer gestante estimulando su sistema inmune y generando anticuerpos específicos (inmunidad activa artificial), en segundo lugar, transfieren anticuerpos de tipo IgG al feto a través de la placenta (inmunidad pasiva natural) especialmente en el último trimestre del embarazo y en tercer lugar al inicio de la vida pueden transferir anticuerpos secretores tipo IgA a través de la leche materna (figura 1)1,3,4.
Fuente: Modificado de Cho HK, Frivold C, Chu HY. Maternal Immunization. J Infect Dis. 2025;23:830-6. doi:10.1093/infdis/jiae5095.
El beneficio de la vacunación de la gestante para proteger a los niños al inicio de la vida se documentó por primera vez en 1879 cuando se observó que en mujeres que habían recibido la vacuna contra viruela, sus hijos no se contagiaban de la enfermedad, posteriormente en los sesenta se documentó este mismo mecanismo administrando toxoide tetánico a embarazadas a través de un ensayo clínico en Nueva Guinea para proteger del tétanos neonatal. Durante la pandemia de influenza del 2009 el riesgo aumentado de ingresos a unidades de cuidado intensivo en mujeres gestantes y el incremento de partos prematuros fue reducido sustancialmente por la vacunación de embarazadas, hecho demostrado en muchos estudios. Toda esta evidencia a favor del beneficio de la vacunación de las gestantes hizo que la recomendación se ampliara contra otras enfermedades como la tosferina, COVID 19 y recientemente virus sincitial respiratorio (VSR) con recomendaciones de la Academia Americana de Ginecología y Obstetricia, OMS y la FIGO4,5,6.
El objetivo del presente artículo de revisión es informar al personal de salud de las ventajas y vacunas indicadas durante la gestación, al mismo tiempo hacer una revisión de los avances recientes en el desarrollo de nuevas vacunas con este mismo propósito.
RACIONALIDAD PARA VACUNAR EN EL EMBARAZO
La vacunación durante la gestación genera inmunidad activa que protege a la embarazada, este cúmulo de anticuerpos más los generados por infecciones previas son transferidos activamente al feto a través de la placenta mediado por el receptor Fc presente en el sincitiotrofoblasto (FcRn)que se une al receptor Fc de los anticuerpos, principalmente IgG1. El proceso es dependiente del pH, es decir de un pH fisiológico de la circulación materna los anticuerpos son captados por endocitosis al endosoma de pH ácido y de ahí son liberados a la circulación fetal de pH fisiológico. El proceso comienza como a las 17 semanas de gestación y va in crescendo hasta el tercer trimestre del embarazo donde es más efectivo y los niveles de anticuerpos del feto pueden ser similares y equivalentes a los de la madre incluso hasta el momento del parto, luego protegen de forma eficaz los primeros dos meses de vida cuando los lactantes aún no han recibido vacunas. Posteriormente los anticuerpos van decayendo aproximadamente en los primeros 6 meses de vida como se ha visto con las vacunas de influenza y VSR, tiempo en el cual los lactantes reciben sus propias vacunas4,5.
Los factores que definen la transferencia transplacentaria más efectiva de anticuerpos son: el nivel de anticuerpos maternos, un adecuado estado nutricional materno, la vacunación reciente y la mayor edad gestacional. Por otro lado, condiciones de inmunosupresión pueden deteriorar el paso de inmunidad pasiva7.
El otro beneficio de la vacunación de la mujer embarazada o en el post parto es que las células plasmáticas de la glándula mamaria producen IgA y las células epiteliales de los acinos mamarios transportan los anticuerpos desde el tejido conectivo hasta la leche materna a través de transcitosis que involucra a un receptor polimérico de Ig. Se producen dos tipos de IgA, la IgA1 secretoria que es un anticuerpo que protege principalmente las superficies mucosas de vías respiratorias y la IgA2 que protege epitelio intestinal de patógenos sin absorberse7,8.
Además de la inmunidad pasiva transferida por la placenta y la leche materna se ha visto que pueden transferirse las células inmunitarias maternas, como los linfocitos B de memoria productores de IgG y los linfocitos T CD4+, que brindan protección adicional de tipo celular4,7,8.
La vacunación en la gestación especialmente la vacuna contra el sarampión puede generar un proceso denominado “interferencia”, que se caracteriza por reducción de la respuesta de anticuerpos del lactante a su vacunación primaria debido a que cuenta con anticuerpos maternos dirigidos contra ese antígeno, aunque la respuesta de células T no parece afectarse, este fenómeno parece compensarse con las posteriores dosis de refuerzo, por lo cual no tiene trascendencia clínica7.
SEGURIDAD DE LAS VACUNAS AUTORIZADAS DURANTE LA GESTACION
En general todas las vacunas inactivadas son seguras para la madre y el feto, sean estas provenientes de bacterias o virus completos inactivados, proteínas, polisacáridos y recientemente las vacunas de vector viral y ARNm. Las vacunas vivas atenuadas están contraindicadas en mujeres embarazadas por el riesgo teórico de paso a través de la placenta que cause infección fetal, aunque este hecho nunca ha sido demostrado pues existen reportes de administración inadvertida (mujeres que recibieron vacunas vivas atenuadas sin conocer que estaban gestando) de este tipo de vacunas en campañas masivas como el de la eliminación de la rubeola en las Américas donde ningún caso se asoció a defectos ni malformaciones4,5. Por esta razón cuando una mujer embarazada recibió inadvertidamente una vacuna viva atenuada no es razón para interrumpir el embarazo. Algunas vacunas vivas atenuadas pueden ser autorizadas bajo circunstancias especiales como es el de un brote epidémico o un viaje hacia un área endémica, siempre bajo un análisis de riesgo-beneficio5.
Algunas vacunas autorizadas en las gestantes están destinadas principalmente a proteger a los lactantes al inicio de la vida con un potencial beneficio marginal para la madre como son las vacunas contra el tétanos y la recientemente vacuna contra VRS aprobada por la Food and Drug Administration (FDA) en EE. UU. el 20238.
A pesar de que las vacunas inactivadas son seguras en general para su administración a mujeres gestantes, casi la totalidad de los ensayos clínicos para aprobar nuevas vacunas excluyen a las embarazadas, lo cual retrasa la posibilidad de una protección adecuada para las gestantes, el feto y los niños en sus primeros meses, por esto es una prioridad continuar investigando sobre la carga de enfermedad para madres y bebés, así como sobre la seguridad y eficacia de las vacunas durante el embarazo.
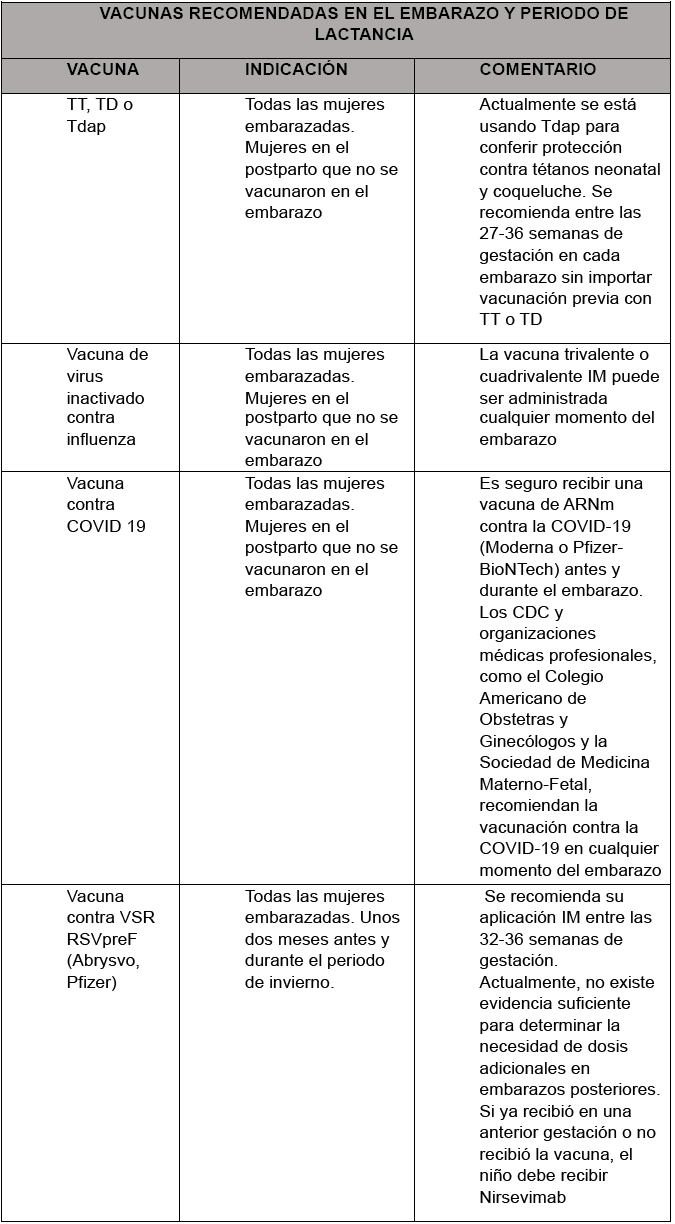
VACUNAS RECOMENDADAS DE RUTINA
Tétanos, difteria y coqueluche
Desde los ochenta la inmunización de gestantes y mujeres en edad fértil con el toxoide tetánico (TT) solo o combinado con toxina diftérica (DT) ha reducido sustancialmente las muertes por tétanos neonatal a nivel mundial, considerándose actualmente eliminado de varias regiones geográficas del planeta. Bolivia aún reporta casos esporádicos de tétanos neonatal de algunas áreas con baja cobertura de vacunación, por lo cual la vacunación con cualquier componente de TT a mujeres en edad fértil o gestantes es mandatorio. Los niños reciben una serie de 5 dosis hasta los 4 años y una dosis de refuerzo durante la adolescencia proporciona inmunidad que perdura durante gran parte de la edad fértil. Varios estudios han sugerido que la inmunidad protectora persiste entre 20 y 30 años después de la sexta dosis de la vacuna con un componente de toxoide tetánico1,4.
Debido al resurgimiento de la coqueluche en muchos países se recomienda actualmente vacunar gestantes con la Tdap (Toxoide tetánico, difteria reducida y pertusis acelular), con el objetivo principal de transferir IgG al feto que protegerá al niño en sus dos primeros meses de vida donde es más vulnerable a formas graves de coqueluche que producen internaciones y muertes. Existe también una protección adicional de transmisión postnatal de la madre inmunizada al niño, denominada protección capullo ya que la fuente de más del 80% de las infecciones por Bordetella pertussis en lactantes pequeños es el entorno familiar, más frecuentemente madres jóvenes que perdieron inmunidad contra coqueluche en el tiempo1,4,5,9.
No existe un consenso respecto al momento más eficaz de la aplicación de la Tdap, el Advisory Committee on Immunization Practices ( ACIP) y la OMS recomiendan que se aplique entre las 27 y 36 semanas de gestación en cada embarazo, sin embargo, en países como Gran Bretaña existen recomendaciones desde las 22 semanas. La inmunidad pasiva conferida de esta manera puede evitar más del 90% de las infecciones por B. pertussis en los primeros dos meses de vida9.
Respecto a la seguridad muchos estudios avalan que la Tdap no se asoció a eventos negativos como parto prematuro o muerte fetal. Algunos estudios informaron de una posible interferencia de anticuerpos maternos con la respuesta inmunitaria a las primeras dosis de vacunación al lactante, sin embargo, sin significancia clínica en el nivel de infecciones, porque esta reducción de la respuesta inmunitaria es luego compensada en las siguientes dosis de refuerzo10.
Influenza
Está demostrado que la infección por el virus de la influenza en mujeres gestantes y de post parto produce infecciones más graves con mayor riesgo de muerte e internaciones, además muerte fetal o riesgo de parto prematuro1,2,3,4. Por otro lado, los niños en los primeros 6 meses de vida donde no existe oportunidad de vacunarlos contra la influenza corren mayor riesgo de infecciones respiratorias bajas. Por lo anterior y en vista de los riesgos demostrados la OMS y otras instituciones relacionadas con la salud materna recomiendan que las gestantes deben ser vacunadas en cada embarazo y en cualquier etapa del embarazo o en el postparto si no se hubiera logrado la vacuna en el embarazo. Existen estudios comparando administraciones en diferentes trimestres del embarazo y al parecer hay una ligera ventaja del nivel de anticuerpos cuando se administra en el tercer trimestre. Pero el mejor momento para la administración de vacunas contra la influenza es antes del periodo de invierno sin importar el trimestre de gestación1,2,3,4,11.
La vacunación reduce el riesgo de hospitalización relacionada con la gripe en embarazadas entre un 50 y un 70 % y la transferencia transplacentaria de anticuerpos proporciona hasta 6 meses de protección pasiva a los lactantes, lo que reduce significativamente la incidencia de enfermedades respiratorias graves1,5,11.
La vacuna autorizada con suficientes estudios de eficacia y seguridad es de virus inactivado en su forma trivalente o cuadrivalente, las vacunas de virus vivo atenuado están contraindicadas por el riesgo teórico de paso al feto.
COVID-19
Los datos de la pandemia y otros brotes han demostrado que las mujeres embarazadas tienen mayor riesgo de infecciones graves, muerte y resultados adversos del embarazo como parto prematuro y muerte fetal. El CDC (center for disease control) el abril de 2021 recomendó las vacunas de RNAm (Pfizer y Moderna) basado en el análisis de 90.000 mujeres embarazadas que recibieron la vacuna sin ningún dato de eventos adversos1,4,5. La OMS recomienda el uso de la vacuna contra la COVID-19 en mujeres embarazadas cuando los beneficios de la vacunación para ellas superen los posibles riesgos. Ninguna de las vacunas actuales puede administrarse antes de los 6 meses por lo cual la protección ofrecida con inmunidad pasiva evita las infecciones graves en lactantes. Estudios recientes realizados en Estados Unidos e Israel han demostrado la transferencia placentaria de anticuerpos IgG anti-SARS-CoV-2 específicos de la vacuna, y también se han detectado anticuerpos IgA e IgG anti-SARS-CoV-2 en la leche materna de mujeres lactantes que fueron vacunadas durante el embarazo hasta 6 semanas después de la primera dosis de la vacuna5, 12.
El 27 de mayo de 2025 el Departamento de Salud y Servicios Humanos (HHS) de los EE. UU. hizo una declaración donde ya no recomienda las vacunas contra COVID-19 en niños sanos y en mujeres embarazadas, este hecho fue refutado por Steven J. Fleischman, presidente del Colegio Americano de Obstetricia y Ginecología, mencionando que el nuevo comité Asesor de Vacunas (ACIP) no siguió la larga tradición de revisión sólida e imparcial de evidencia científica confiable por parte de expertos médicos y de salud pública, por lo cual estarían desconociendo toda la evidencia sólida a favor de la vacunación contra COVID-19 en la gestación y poniendo en riesgo a muchas mujeres embarazadas y su descendencia12.
Virus Sincitial Respiratorio (VSR)
El VSR es la principal causa de infección respiratoria baja en menores de 1 año y por lo tanto una de las causas más importantes de muerte, especialmente en menores de 3 meses donde la infección es más grave. Cada año durante la época invernal se producen brotes epidémicos en zonas templadas y en época lluviosa en zonas tropicales1,4,13.
Emulando lo conseguido con la vacunación para otras infecciones después de muchos años de investigación se logra finalizar la fase 3 de un ensayo clínico doble ciego en 18 países de una vacuna administrada a mujeres gestantes de 24 a 36 semanas de gestación que recibieron una dosis única intramuscular de 120 μg de una vacuna bivalente basada en la proteína F de prefusión del VRS (RSVpreF) o placebo, cuyos resultados mostraron una eficacia de 81.8% de protección para enfermedad grave por VSR hasta los 90 días de vida y de 69.4% hasta 180 días posteriores al nacimiento. No se detectaron eventos adversos más que en el grupo placebo14. Por lo anterior fue autorizada por la FDA en los EE. UU. (Abrysvo, Pfizer ) para su aplicación entre las 32 y 36 semanas de gestación en dosis única, actualmente existen otras vacunas de diferentes plataformas próximas a su autorización después de finalizar la fase 3. La lucha contra el VSR es complementada con la aprobación también el 2023 de un anticuerpo monoclonal de dosis única denominado Nirsevimab, un anticuerpo monoclonal de vida media prolongada y alta potencia que se une al VSR evitando la fusión de este con las células del epitelio respiratorio, administrado en dosis única antes o durante la temporada de VSR1,4,5,8.
NUEVAS VACUNAS EN DESARROLLO
Streptococcus del grupo B
El estreptococo del grupo B (SGB) oStreptococcus agalactiaees un coco betahemolítico grampositivo que puede colonizar el tracto genitourinario y gastrointestinal de las embarazadas. El SGB puede pasar de una colonización asintomática a una bacteria patógena, lo que puede provocar consecuencias adversas para el embarazo, la madre y el neonato, en este último puede provocar sepsis, meningitis y neumonía. El tamizaje de mujeres gestante a través de cultivos y la profilaxis intraparto redujeron hasta en un 30%, los eventos indeseables en el neonato, pero en los países de bajos y medianos ingresos donde no se realiza esta estrategia la posibilidad de una vacuna a la gestante que transfiera anticuerpos al feto y proteja al recién nacido sería importante1,4,5,8.
El estreptococo del grupo B expresa polisacáridos capsulares (CPS), que son importantes factores de virulencia. Se han definido diez serotipos de CPS del estreptococo del grupo B (Ia, Ib y II a IX), seis de los cuales (Ia, Ib y II a V) se asocian con cepas que causan aproximadamente el 98 % de los casos de enfermedad invasiva en lactantes a nivel mundial. En este sentido se ha publicado la fase 2 de un ensayo clínico en Sudáfrica una vacuna hexavalente glucoconjugada que generó anticuerpos contra polisacáridos capsulares del estreptococo del grupo B en mujeres embarazadas que fueron transferidas a sus bebés, en niveles asociados con un menor riesgo de enfermedad invasiva por estreptococo del grupo B (ClinicalTrials.gov, NCT03765073 ). Actualmente también corren ensayos clínicos de vacunas basadas en proteínas recombinantes, todos estos esfuerzos a mediano plazo brindaran la oportunidad de protección efectiva contra una bacteria que, en un cálculo estimado de la carga global por este germen, una vacuna materna con una eficacia del 80 % y una cobertura del 90 % podría prevenir 107 000 muertes fetales e infantiles1,15,16.
Citomegalovirus (CMV)
El CMV es un herpes virus de ADN ubicuo en todo el planeta, las dos principales fuentes conocidas de infección primaria por CMV durante el embarazo son la actividad sexual y el contacto con niños pequeños. La infección primaria se presenta en aproximadamente el 1 al 4% de los embarazos y es mayormente asintomática, pero en países de bajos ingresos se calcula que el 100% de la población se infectó en la infancia y en la juventud, por lo cual las madres de países de bajos ingresos harán infecciones no primarias por reactivación o infección de otra cepa17. El CMV puede transmitirse de madre a hijo en el útero, durante el parto o durante la lactancia. La transmisión intrauterina puede provocar una infección congénita por CMV, una de las principales causas de pérdida permanente de la audición, pero también en algunos casos microcefalia, retraso mental, hepatoesplenomegalia y púrpura trombocitopénica. La gravedad de la infección en el feto depende de si la madre es seropositiva o seronegativa para el CMV. Las infecciones en mujeres embarazadas seronegativas transmitidas al feto tienen el peor pronóstico, pero los fetos infectados por madres seropositivas también pueden sufrir graves consecuencias1,4,5,8,17. Las tasas de transmisión congénita por CMV alcanzan el 50% en mujeres que adquieren la infección primaria por CMV durante el embarazo y son inferiores al 2% en mujeres con infección no primaria. Estos tipos diferentes de infección han dificultado el desarrollo de vacunas contra CMV, se ha visto que los anticuerpos son necesarios para proteger a mujeres seronegativas, pero también se requiere de respuesta de células T que evite la reinfección de mujeres seropositivas que justamente son infectadas por el CMV modificando la respuesta celular17.
Desde hace 5 décadas se ha estado buscando una vacuna efectiva, inicialmente con virus vivos atenuados como la cepa Towne, luego se desarrolló otra contra una glucoproteína (gB)de superficie de CMV con 50% de eficacia. Actualmente las más avanzadas y prometedoras son la vacuna contra el complejo pentamérico de proteínas de la superficie de CMV que ha producido más anticuerpos que la vacuna de gB. Finalmente, Moderna desarrolla una vacuna de que inicio el 2022 y espera finalizar el 2027 donde el objetivo principal del estudio es evaluar la seguridad e inmunogenicidad de diferentes dosis de ARNm-1647 frente a un grupo control en participantes sanos de ambos sexos, seronegativos y seropositivos al citomegalovirus (CMV), de 9 a 15 años. Además, se evaluará el ARNm-1647 en participantes de 16 a 25 años como cohorte de comparación. Siendo la vacuna contra CMV una prioridad declarada por la OMS, la Academia Americana de Medicina, se aguarda una vacuna efectiva en los próximos años4,17.
BARRERAS PARA LA VACUNACIÓN EN LA GESTACIÓN
A pesar de haberse comprobado que la inmunización de las gestantes son un método eficaz y seguro para la protección de la madre, el feto y el recién nacido aún existen barreras para su recomendación universal y aceptación de parte de las usuarias1,2,3. En general las coberturas de vacunación en mujeres embarazadas a nivel global no son óptimas, especialmente en países de medianos y bajos ingresos donde además no están disponibles todas las vacunas sancionadas para su uso en la gestación. Algunos de los factores que pueden convertirse en una barrera para elevar las coberturas de vacunación son:
Poca capacitación del personal de salud respecto a las ventajas de la vacunación durante la etapa de gestación, esto probablemente no posibilita una buena consejería, debería visualizarse este aspecto desde el pregrado en todas las carreras de salud, los estudios muestran que las mujeres se adhieren más a las vacunas si son recomendadas por sus ginecólogos.
La falta de percepción de riesgo en las mujeres gestantes acerca de las enfermedades y conocimiento de la eficacia de las vacunas son dos factores que afectan la adherencia a las vacunas, en un estudio muchas mujeres desconocían que podían transmitir la coqueluche a sus recién nacidos o que una gestante corre más riesgo de influenza grave y de tener un parto prematuro. Muchas mujeres pueden considerar que las vacunas son solo para los niños.
Algunas mujeres pueden tener experiencias negativas personales o de familiares con anteriores vacunas y efectos adversos, por esto es importante una comunicación clara y eficaz basada en evidencia.
Los servicios de salud y el control prenatal deberían estar ligados a la vacunación obligatoria de la gestante, por esto será importante contar con un carnet de vacunas de la embarazada.
La falta de programas integrales respecto a la vacunación en la gestación, con la colaboración entre profesionales de la salud, funcionarios de salud pública y grupos de defensa de los pacientes puede ayudar a superar las barreras y promover la aceptación de la vacuna.
Finalmente es importante mencionar que lamentablemente no hay una equidad en los ensayos clínicos de las vacunas donde generalmente no son incluidas mujeres gestantes, por lo cual se generan dudas acerca de su seguridad y eficacia, durante la pandemia Pfizer fue una de las pocas que refrendó la seguridad con un ensayo clínico5,8,18.












 uBio
uBio