INTRODUCCIÓN
El síndrome de Lemmel es un patología infrecuente que fue descrita por primera vez en 1934 por Gerhard Lemmel, basado en la observación de que la presencia de un divertículo duodenal peripapilar podría generar un síndrome biliar obstructivo. 1
Los divertículos gastrointestinales son protuberancias en forma de saco de toda o parte de la pared intestinal que pueden aparecer en cualquier parte del tracto digestivo. 2 Su localización más frecuente es el colon, seguido del duodeno. 3
Los divertículos duodenales generalmente son asintomáticos, se encuentran de forma incidental en hasta el 22% de la población en procedimientos diagnósticos realizados para otros trastornos gastrointestinales, de los cuales menos del 10% son sintomáticos, aunque se presentan a cualquier edad, son más frecuentes entre los 50 y 65 años, sin embargo, la mayoría de los casos de síndrome de Lemmel ocurre entre los 70-80 años. 2,3
Existen pocos casos reportados en la literatura, lo cual revela la importancia para presentar este caso clínico y realizar la revisión de la literatura.
CASO CLÍNICO
Mujer de 74 años de edad, diabética, hipertensa, con antecedente de colecistectomía abierta el año 2014. Acude al servicio de emergencias por cuadro clínico de 3 días de evolución caracterizado por dolor de inicio progresivo, localizado en mesogastrio, de moderada intensidad 7/10 según escala visual analógica del dolor, de tipo cólico, que se irradia a región dorsolumbar, se atenúa en posición decúbito dorsal. Asociado a náuseas que llegan al vómito en 4 ocasiones de tipo gastrobilioso, deposiciones líquidas en tres oportunidades por día y orinas turbias coluricas no fétidas. Además de alzas térmicas no cuantificadas de predominio nocturno. A su ingreso presenta FC: 86 lpm, FR: 19 rpm, PA: 120/80, T: 36.5º C, con facies álgida, ictericia de escleras y tegumentos, examen físico cardiopulmonar sin alteraciones, abdomen globoso a expensas de tejido celular subcutáneo, ruidos hidroaéreos positivos hipoactivos, doloroso a la palpación difusa en todo marco abdominal.
Los estudios de laboratorio a su ingreso al servicio de emergencias que orientaron a un síndrome ictérico obstructivo fueron, hiperbilirrubinemia (4,5 mg/dl) a predominio de bilirrubina directa (3,2 mg/dl) y bilirrubina indirecta (1,3 mg/dl), AST 28 UI/L, ALT 53 UI/L, FA 1070 UI/L, serología para hepatitis B y C negativa. Se realiza ecografía abdominal que muestra hepatomegalia a expensas del lóbulo izquierdo, dilatación de vía biliar principal proximal de 12 mm y vías intrahepáticas de hasta 4 mm, no se observa imágenes litiásicas en su interior ni masas en su segmentos valorables.
En una primera instancia se realiza el manejo conservador con reposición hidroelectrolítica y analgesia. Con posterior internación en el servicio de cirugía con el diagnóstico de síndrome ictérico obstructivo secundario a neoplasia probable. Se realiza laboratorios de control en donde se evidencia leucocitosis (16100/mm3) con desvío a la izquierda (segmentados 94%) y aumento de VES a 34 mm. Además de aumento en la concentración de bilirrubina total (9,2 mg/dl) con predominio de la bilirrubina directa (7,9 mg/dl) y bilirrubina indirecta de (1,8 mg/dl), AST 94 UI/L, ALT 75 UI/L, GGT 341,5 UI/L y disminución de la FA 135 UI/L.
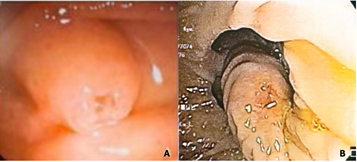
Se realiza una colangiopancreatografía endoscópica retrograda (CPRE), donde se identifica Papila de Vater intradiverticular que dificulta el acceso a la vía biliar principal, se realiza precorte, sin embargo, la canulación de la vía biliar fue fallida. (Figura 1)
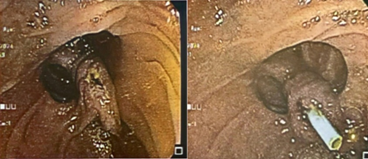
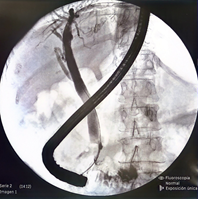
En consecuencia, se realiza una segunda donde se observa dilatación de la vía biliar extrahepática secundaria a papila intradiverticular, se realiza esfinterotomia por lo que se coloca prótesis biliar plástica de 10 Fr x 10 cm, corroborando su ubicación por fluoroscopia. (Figura 2 y 3)
La paciente tuvo una evolución favorable con resolución del cuadro clínico, es dada de alta a las 24 horas del procedimiento sin complicaciones.
DISCUSIÓN
El síndrome de Lemmel es una enfermedad rara que se presenta con ictericia obstructiva intermitente secundaria a un divertículo duodenal periampular, en ausencia de colelitiasis u otros factores obstructivos detectables (neoplasias), que comprimen la parte intrapancreática del conducto biliar común. 2, 5 Este proceso produce dilatación retrógrada de los conductos biliares extrahepáticos e intrahepáticos 2, 6
Un divertículo duodenal periampular es un pseudodivertículo, que se desarrolla dentro de un radio de 2 a 3 cm de la ampolla de Vater. 2, 7 El 6% aparecen en la primera porción, el 53-75% en la segunda porción, el 12% en la tercera porción y el 24% en la cuarta porción del duodeno. Es una afección poco frecuente, debido a que estos divertículos raramente presentan sintomatología y suelen ser un hallazgo incidental. 6
La fisiopatología que explica la sintomatología del síndrome de Lemmel no está completamente establecida, aunque se han propuesto diversas teorías. 8 La irritación mecánica directa de los divertículos periampulares puede causar inflamación crónica de la ampolla, lo que conduce a la fibrosis de la papila. También, pueden causar disfunción del esfínter de Oddi, lo que causa estasis y reflujo biliar desde el duodeno hacia el colédoco. 2, 4 Finalmente, el conducto biliar común distal o ampolla puede ser comprimido mecánicamente por divertículos periampulares ocupados por un enterolito o un bezoar. 2, 8 Estos mecanismos pueden actuar de forma simultánea o consecutiva favoreciendo el reflujo de contenido duodenal, con estasis biliar, sobrecrecimiento bacteriano y producción de cálculos biliares. 6
Existen dos clasificaciones endoscópicas para divertículos duodenales, la clasificación de Noda (Tabla 1) y la de Boix. Ayudan a planificar el procedimiento de CPRE y predecir la dificultad de la canulación de la papila. 6 Según Boix los divertículos periampulares se clasifican en tres tipos. (Tabla 2) También, clasificó la dificultad de canulación en: grado 1, canulación profunda fácil; grado 2, necesidad de guía de alambre esfinterotomo; grado 3, dificultad de canulación requiriendo esfinterotomía con aguja-cuchilla; grado 4, imposibilidad para canulación. 4
Tabla 1 Clasificación de Noda

Fuente: Dávila-Ruiz EO, García-Manzano RA, Barker-Antonio A, Martínez-Santiago NY, Isidoro-Hernández D, Sánchez-Guerrero RI. Ictericia obstructiva intermitente o síndrome de Lemmel: reporte de caso y revisión de la literatura. Cir Cir. 2020;88(S2):60-65. doi:10.24875/CIRU.20000332.
Tabla 2 Clasificación de Boix
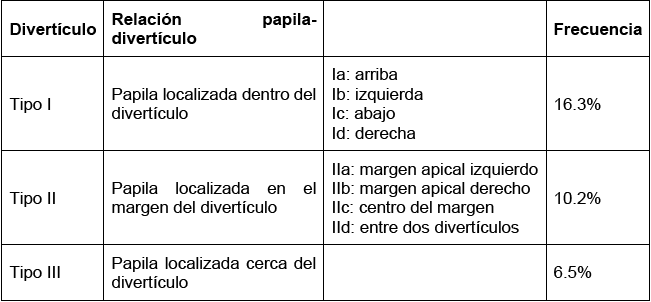
Fuente: Dávila-Ruiz EO, García-Manzano RA, Barker-Antonio A, Martínez-Santiago NY, Isidoro-Hernández D, Sánchez-Guerrero RI. Ictericia obstructiva intermitente o síndrome de Lemmel: reporte de caso y revisión de la literatura. Cir Cir. 2020;88(S2):60-65. doi:10.24875/CIRU.20000332.
El cuadro clínico es caracterizado por ictericia obstructiva y dolor abdominal postprandial. Además, puede imitar la sintomatología de los tumores periampulares. 2, 3, 6, 7, 8 El 1 % de los pacientes pueden sufrir complicaciones como colangitis aguda, siendo una de las más frecuentes. Otras complicaciones menos frecuentes son la pancreatitis aguda derivada de coledocolitiasis, diverticulitis, perforación y hemorragia digestiva alta. 3, 6, 9
El diagnóstico se realiza mediante métodos de imagen, que incluyen endoscopia digestiva alta, CPRE, colangioresonancia magnética (CRM) o tomografía computarizada (TC). 2 Se confirma con la visualización directa del divertículo duodenal a 2-5 cm de la papila en la CPRE. 8 Sin embargo, para descartar otras causas, la TC y la RM juegan un papel esencial, debido a que pueden indicar de forma no invasiva el diagnóstico y al mismo tiempo permitir la exclusión de otras enfermedades periampulares. 5 En la TC y la CRM, los divertículos pueden visualizarse como cavitaciones en la pared duodenal llenos de gas. 8 También el método de elección para diferencialos de un absceso pancreático, pseudoquistes pancreaticos, tumores quísticos de la cabeza pancreática o metástasis a nódulos linfáticos. 5 Se ha demostrado que la endoscopia digestiva alta con vista lateral es esencial para confirmar el diagnóstico. 2Nuevos métodos diagnósticos, como la ecoendoscopia, también son usados con la ventaja de permitir intervenciones terapéuticas durante el mismo procedimiento y descartar neoplasias con mayor precisión. 3, 6
En pacientes asintomáticos no se recomienda ningún tipo de manejo. 3 Los casos sintomáticos pueden abordarse mediante tratamiento conservador, endoscópico o quirúrgico. El principal objetivo terapéutico es resolver la obstrucción del sistema biliopancreático. 8, 10, 11
La CPRE utilizada inicialmente como un método diagnóstico, es ahora casi exclusivamente terapéutica y actualmente se considera la primera opción en el manejo. 3 Además, se realiza una esfinterotomía endoscópica para liberar la obstrucción del conducto biliar común. 5, 6
El manejo quirúrgico se realiza mediante el empleo de diversas técnicas como la inversión del divertículo, la diverticulectomía simple o asociada a derivación biliodigestiva (anastomosis del colédoco al duodeno, el yeyuno o incluso la pancreatoduodenectomía). 3, 5 El manejo quirúrgico está reservado para los casos en los que hay perforación o hemorragia posterior a la CPRE, cuando la canulación endoscópica es imposible por dificultades como litos > 20mm, falta de equipo, lito impactado en el colédoco distal, panlitiasis o en casos en los que los síntomas son recurrentes a pesar del tratamiento endoscópico. 3, 5, 6 La diverticulectomía simple se asocia a una alta morbimortalidad debido al riesgo de lesión del conducto biliopancreático, por ello es mandatorio localizar la ampolla de Vater mediante duodenectomía o de forma anterógrada a través del conducto cístico por coledocotomía. 7 Además de estas opciones, se han utilizado procedimientos de bypass para eliminar el divertículo del flujo alimentario, resolviendo los problemas de colangitis recurrente sin tener que extirparlo. 2 Actualmente no hay consenso sobre la técnica quirúrgica que se debe emplear. 3
En el caso presentado se descarta que el síndrome ictérico obstructivo haya sido de origen litíasico debido al antecedente de colecistectomia y la ecografía abdominal no reportaba la presencia de litos primarios. Debido a que es otra causa frecuente, se sospechó de un origen neoplásico, quedando descartado debido a la visualización del divertículo duodenal periampular mediante una CPRE.
Según las clasificaciones mencionadas, el presente caso corresponde a un divertículo periampular tipo I de Boix y tipo D de Noda. Además, de tener un grado 3 de dificultad de canulación. Debido a la indisponibilidad de otros métodos de diagnóstico en el momento de la presentación del caso no se lograron realizar otros estudios de imagen.
CONCLUSIÓN
En pacientes de edad avanzada con un cuadro clínico de síndrome ictérico obstructivo en ausencia de litiasis en el conducto biliar común o de una masa tumoral debe considerarse la posibilidad de que el paciente presente un divertículo periampular causante de la sintomatología. Se resalta la importancia de los exámenes de imagen como la CRM y la TC con contraste para descartar otras patologías, documentar el divertículo y la compresión de la vía biliar. Finalmente, la CPRE continúa siendo el tratamiento de elección.












 uBio
uBio