Introducción
Las termitas cumplen un papel ecológico fundamental en la descomposición de la materia vegetal (Laffont et al. 2004,Bignell et al. 2011). Su aporte al reciclaje de nutrientes es crucial para incrementar la fertilidad del suelo (Wood & Sands 1978,Bignell & Eggleton 2000,Tapia-Coral et al. 2016), ya que su actividad repercute directamente en el mantenimiento de la porosidad y en la aireación del sustrato (Lavelle et al. 1997). Además, actúan como organismos clave, debido a que en sus procesos constructivos incorporan numerosos componentes de materia en descomposición, al entorno lo que influye en las propiedades del medio donde habitan (Jones & Eggleton 2000,Mora et al. 2003,Yamada et al. 2005,Jouquet et al. 2011). En este sentido, este grupo se incluye dentro de una categoría de grupo funcional reciente denominada “ingenieros de los ecosistemas”, que, a diferencia de la clasificación clásica basada en hábitos alimenticios, se refiere al papel fundamental que desempeñan -junto con hormigas y lombrices- en la transformación de los ecosistemas naturales y antropizados mediante el movimiento de grandes cantidades de materia orgánica (Jones et al. 1997,Usman et al. 2016,Mekoten 2019).
En este contexto, diversos factores ambientales y estructurales influyen directamente en la distribución, comportamiento y ecología de las termitas en distintos ecosistemas. En bosques, por ejemplo, la presencia de árboles de mayor tamaño influye significativamente en la formación de termiteros, así como en la actividad y frecuencia de visitas de termitas (Jones & Gathorne-Hardy 1995,Gonçalves et al. 2005a,Araújo et al. 2010). Asimismo, tanto el tamaño del árbol como su grado de decaimiento actúan como indicadores de la abundancia y calidad de recursos disponibles para este grupo (Araújo et al. 2010). Además, el grosor de la corteza y su textura se muestra como un factor determinante en la presencia de termitas, ya que puede influir en el movimiento de las termitas sobre el árbol (Lee 2017,2018,de Souza 2020).
Pese a la relevancia ecológica de las termitas arbóreas, existen pocos estudios que aborden las variables que determinan su presencia (de Souza 2020,Gonçalves et al. 2005a,Chaves 2006). Asimismo, se conoce poco sobre las interacciones entre estas y las especies vegetales que les ofrecen hábitat o recursos (Ramírez & Lanfranco 2021). Por ello, comprender las condiciones en las que construyen sus termiteros no solo ampliará el conocimiento actual, sino que también facilitará, en el futuro, una planificación más efectiva del manejo de las áreas agroforestales, dado su importante papel en el proceso de la degradación de la materia orgánica y el ciclo de nutrientes. Aunque las termitas pueden generar conflictos en estar áreas, debido al “daño mecánico” a los árboles (Abadia et al. 2013,Cabrera & López 2013), está probado que son incapaces de atacar madera viva (Mathews 1977), debido a que la madera de los árboles vivos resulta tóxica o, al menos, poco palatable para las termitas (Chaves 2006).
En este contexto, el presente estudio tiene como objetivo evaluar si las características morfológicas de los árboles - como el diámetro a la altura del pecho (DAP), altura del árbol, cobertura y textura de la corteza-influyen en la presencia de termiteros. Planteamos la hipótesis de que la probabilidad de encontrar termiteros aumenta en árboles con determinadas características morfológicas, con predicciones específicas: árboles con mayor DAP y altura presentan más termiteros, al ofrecer una mayor superficie de apoyo y estabilidad; aquellos con mayor cobertura de dosel aumentan la probabilidad de albergar termiteros, ya que la sombra y la regulación microclimática podrían favorecer el establecimiento de los nidos; y los árboles con cortezas más rugosas permitiría un mejor anclaje de los termiteros al árbol.
Área de estudio
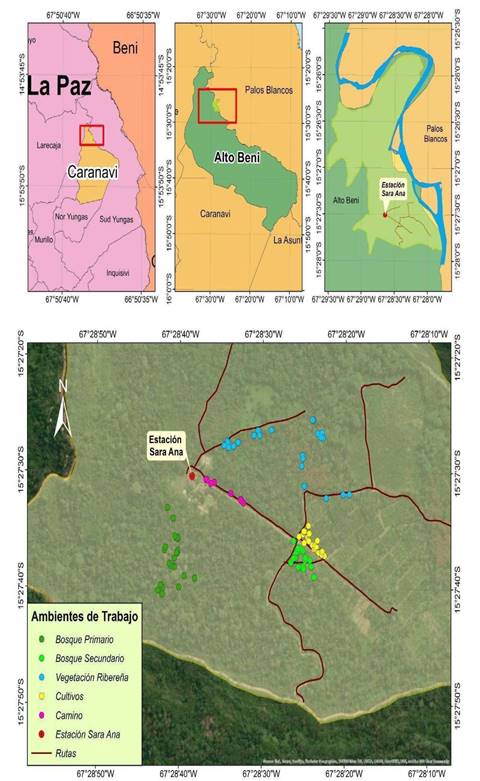
El estudio se llevó a cabo en el Centro de Investigación y Capacitación Sara Ana, ubicado en el Municipio de Alto Beni, Provincia de Caranavi, Departamento de La Paz, Bolivia (15°27'30"S, 67°28'38"O; 390 m), con una extensión aproximada de 500 ha (Limachi et al. 2024). Este centro se sitúa en una zona de transición entre los Andes y las tierras bajas bolivianas (Montes de Oca 1989). Los bosques de Alto Beni son un conjunto de bosques siempreverdes estacionales del suroeste de la amazonia con influencia de la flora yungueña (Navarro 2011). Dentro del área hay una mezcla de bosques primarios y secundarios con especies de árboles como Swartzia jorori (Fabaceae), Cecropia concolor (Cecropiaceae) y bambúes gigantes del género Guadua (Poaceae), así como fragmentos de bosque maduro, de transición y cultivos de cacao, plátano y otros, reflejando distintos grados de conservación y regeneración natural (Schneider et al. 2017,Marconi et al. 2021,Plata et al. 2021). La región presenta un clima tropical con verano húmedo, una temperatura media anual de 26.9°C; julio es el mes más frío, con una media de 24.5°C, mientras que noviembre es el más cálido, alcanzando una temperatura promedio de 28.1°C y con una precipitación media anual de 1.645±249 mm al año (Ripa & Naoki 2021).
Métodos
El muestreo se realizó durante la segunda semana de julio de 2024, bajo la realización de un curso de campo, el diseño y las variables fueron elaborados, siguiendo criterios del equipo de trabajo. Se efectuaron recorridos exploratorios por distintos tipos de ambientes que forman un mosaico de vegetación propia de la zona, tales como bosque primario, bosque secundario, vegetación ribereña y áreas antrópicas (cultivos y caminos). En cada recorrido se registraron todos los árboles con termiteros encontrados (n=110) y, de forma sistemática, se registraron 330 árboles control (sin termiteros), midiendo uno de cada cinco árboles observados durante el recorrido (Fig. 1).
Para ambos tratamientos (árboles con termiteros y sin termiteros) se midieron las siguientes cuatro variables: 1) altura total de árbol (m), medida con un clinómetro; 2) diámetro a la altura del pecho (DAP), medido con una cinta métrica; 3) textura de la corteza, asignando una categoría del uno al cuatro (donde 1 corresponde a una corteza lisa y 4 muy rugosa) considerando la presencia de espinas u otras ornamentaciones (Fig. 2); 4) porcentaje de cobertura de dosel, medido con un densiómetro; y 5) adicionalmente para los árboles con termiteros se midió orientación del termitero, registrada con una brújula, según la dirección en que se extendía principalmente el crecimiento del termitero sobre el árbol.

Figura 2. Niveles de textura de la corteza de los árboles. a) 1: liso b) 2: rugosidad baja c) 3: rugosidad media y d) 4: rugosidad alta.
Cada variable fue medida por la misma persona, para reducir la variabilidad entre observadores (Sutherland 2006). Se recolectaron de 1-5 termitas por termitero, las cuales se conservaron en un tubo Eppendorf con alcohol al 70%. Posteriormente, las termitas se identificaron en laboratorio hasta el nivel de género utilizando claves dicotómicas (Thompson 2011), mediante con un estereoscopio (AmScope SE306).
Análisis estadístico
Se evaluó el efecto de las características morfológicas de los árboles (altura total, DAP, textura de la corteza y cobertura del dosel) sobre la presencia de termiteros mediante modelos lineales generalizados (GLM) con distribución binomial y función de enlace logit. La variable de respuesta fue la presencia o ausencia de termiteros; las variables independientes incluyeron tres continuas (altura, DAP y cobertura de dosel, escaladas para estandarizar unidades) y una variable ordinal (textura de corteza). Se construyeron modelos univariados y multivariados, comparados mediante AICc (paquete MuMIn), incluyendo el modelo completo con todas las variables, que resultó el mejor soportado por el análisis (Tabla 1). La colinealidad entre variables se evaluó con VIF, obteniéndose valores bajos (<2; Tabla 2). Los resultados se visualizaron con ggplot2 y la adecuación de los modelos se verificó mediante inspección de residuos con el paquete arm. De manera separada, se analizó la orientación de los termiteros mediante un GLM binomial, evaluando las posiciones más frecuentes de los termiteros sobre los troncos. Todos los análisis se realizaron en R v4.4.1 (R Core Team 2024).
Resultados
Todas las termitas recolectadas en este estudio pertenecen al género Nasutitermes. Las cuatro características morfológicas evaluadas en los árboles mostraron un efecto significativo sobre la presencia de termiteros (p < 0.05 para todas las variables; Tabla 3). Los coeficientes corresponden al modelo completo, el mejor soportado según AICc. En particular, la probabilidad de encontrar termiteros aumentó en árboles con un DAP superior a 20 cm (Figura 3a), en aquellos con mayor cobertura de dosel, especialmente cuando ésta supera el 50% (z = 2.094; p = 0.036, Fig. 3c), en árboles que superan los 10 m de altura (Fig. 3b), y en aquellos con cortezas de rugosidad media-alta (z = 3.544; p = 0.0004, Fig. 3d).
Orientación
En cuanto a la orientación de los termiteros, se logró determinar que la única orientación que presenta un valor estadísticamente significativo fue la orientación noreste (z=2.202; P=0.028), encontrándose un mayor número de termiteros respecto a las demás orientaciones (Tabla 4).
Tabla 1. Valores de AICc, ΔAICc y pesos relativos para los modelos que explican la presencia de termiteros según variables morfológicas de los árboles.
| Modelo | df | AICc | ΔAICc | Peso relativo |
|---|---|---|---|---|
| Altura+ DAP+T extura+ Dosel | 5 | 385.645 | 0.000 | 9.992e-01 |
| Altura+DAP | 3 | 400.055 | 14.410 | 7.424e-04 |
| Textura+Dosel | 3 | 435.080 | 49.435 | 1.841e-11 |
| DAP | 2 | 405.018 | 19.373 | 6.207e-05 |
| Textura | 2 | 443.259 | 57.614 | 3.083e-13 |
| Dosel | 2 | 466.602 | 80.956 | 2.632e-18 |
| Altura | 2 | 471.524 | 85.879 | 2.246e-19 |
| Null | 1 | 478.711 | 93.065 | 6.177e-21 |
Tabla 2. Factores de inflación de la varianza (VIF) para las variables morfológicas de los árboles.
| Variable | VIF |
|---|---|
| Altura | 1.76 |
| DAP | 1.75 |
| Textura de corteza | 1.09 |
| Cobertura de dosel | 1.01 |
Tabla 3. Coeficientes estimados del modelo completo de regresión logística binomial sobre la presencia de termiteros en función de las variables morfológicas de los árboles.
| Estimado | Error estándar | Valor de Z | P(>|z|) | R2 ajustado | |
|---|---|---|---|---|---|
| (Intercepto) | -2.547 | 0.413 | -6.160 | 7.28e-10 | |
| DAP | 1.109 | 0.177 | 6.252 | 4.05e-10 | 0.245 |
| Altura | -0.448 | 0.170 | -2.632 | 0.0085 | 0.032 |
| Textura de corteza | 0.576 | 0.162 | 3.544 | 0.0004 | 0.127 |
| Cobertura de dosel | 0.288 | 0.137 | 2.094 | 0.0363 | 0.049 |
Tabla 4. Parámetros estimados del modelo de regresión logística binomial sobre la variación en la orientación de los termiteros.
| Estimado | Error estándar | Valor de Z | P(>|z|) | |
|---|---|---|---|---|
| (Intercepto) | -1.386 | 0.354 | -3.921 | 8.82e-05 |
| Noreste | 0.997 | 0.453 | 2.202 | 0.028 |
| Este | 0.448 | 0.450 | 0.996 | 0.319 |
| Sureste | 0.167 | 0.474 | 0.352 | 0.725 |
| Sur | -0.267 | 0.507 | -0.526 | 0.599 |
| Suroeste | 0.511 | 0.468 | 1.090 | 0.276 |
| Oeste | 0.417 | 0.500 | 0.833 | 0.405 |
Discusión
Los termiteros se hallaron con mayor frecuencia en árboles de mayor tamaño, tanto en diámetro a la altura del pecho (DAP) como en altura. Este hallazgo coincide con estudios previos que demuestran una clara tendencia de las termitas a seleccionar árboles grandes (Gonçalves et al. 2005a,Cháves 2006,Araújo et al. 2010,de Souza 2020). También se observó una mayor actividad en árboles con un número elevado de ramas, debido al soporte estructural y a la abundancia y calidad de los recursos que estos proporcionan. Dichos factores facilitan a las colonias la construcción de termiteros de mayor envergadura (Gonçalves et al. 2005b,Widelmurth et al. 2021). Una explicación para esta selección es que las características de los árboles como el tamaño y el grado de inclinación del tronco determinan aspectos como la accesibilidad al termitero y la protección contra depredadores (DeSouza et al. 2009,de Souza 2020). Además, investigaciones llevadas a cabo en Brasil, Panamá, Indonesia y Australia, abarcando diversas especies de termitas arbóreas en distintos hábitats, han concluido que el tamaño del árbol hospedero es un factor fundamental para la presencia de termiteros (Roisin et al. 2006,Werner et al. 2007,Fernandes et al. 2018,Fajar et al. 2021). Esta asociación se ha documentado en el género Nasutitermes, el cual destaca por construir termiteros a mayor altura en comparación con otras termitas arbóreas (Boulogne 2017).
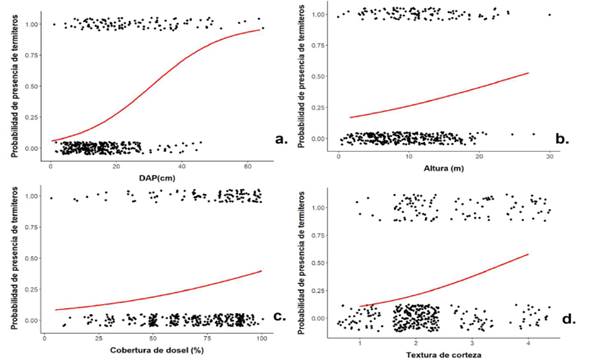
Figura 3. Probabilidad de presencia de termiteros en función de características morfológicas de los árboles. a. diámetro a la altura del pecho (cm), b. altura del árbol (m), c. cobertura de dosel (%), d. textura de corteza (1-4). Los puntos negros representan observaciones individuales y la línea roja el ajuste del modelo.
Los termiteros se encontraron predominantemente en árboles con mayor cobertura de dosel. Aunque aún no existen estudios que expliquen de forma directa la influencia de la cobertura de dosel en los nidos de termitas arbóreas, investigaciones en termitas subterráneas han demostrado una mayor abundancia y actividad en áreas con alta cobertura (Dibog et al. 1999,Zhou et al. 2020). Esto sugiere que la cobertura de dosel actúa como un protector contra la lluvia y ayuda a regular la temperatura interna de los nidos, dado que las termitas sólo pueden sobrevivir en un rango térmico estrecho (Eggleton 2010). Por ello, la mayoría de las termitas aprovechan las propiedades térmicas del sustrato y hábitat como tal en el que anidan, para mantener condiciones óptimas de todo el termitero (Jones & Oldroyd 2006). Asimismo, existe evidencia en otros insectos sociales, como abejas y hormigas arbóreas, que muestra que un dosel denso favorece la selección de hábitat (Dantas 2014) y se asocia con una mayor abundancia y diversidad (Urban-Mead 2021,Davis 2022). Por el contrario, en ambientes donde la cobertura del dosel se reduce, la riqueza y la ocupación de nidos disminuyen (Philpott 2005), lo que refuerza la idea de que la cobertura del dosel constituye un factor importante que influye directamente en los sitios de nidificación de los insectos sociales.
También encontramos que el grado de textura tiene una relación directa con la presencia de termiteros en los árboles, siendo aquellos con mayor rugosidad los que tienen mayor probabilidad de ser colonizados por las termitas para construir su nido. Posiblemente, el grado de rugosidad y presencia de espinas podrían ser un factor persuasivo que garantice a las termitas protección contra sus depredadores (Chaves 2006). Esto también podría deberse a que las superficies rugosas ofrecen una mejor sujeción, lo que reduce la probabilidad de que los nidos se desprendan, al estar más firmemente adheridos al árbol. Además, en superficies con rugosidad media, la velocidad de las termitas tiende a ser mayor que en superficies lisas o muy rugosas (Lee 2018). Esto puede afectar a la eficiencia y posiblemente la elección del lugar de búsqueda de alimento en los árboles (de Souza 2020,Lee 2017,2018).
En relación con la orientación de los termiteros, se observó que la mayoría se construyó hacia el noreste, lo que evidencia un patrón en la disposición en la que son construidos. Leponce et al. (1995) también reportaron que el noreste era la dirección predominante en la posición de termiteros de Nasutitermes princeps en Papúa Nueva Guinea. Estos autores exploraron si la posición relativa al sol influía en esta tendencia, dado que en termitas terrestres se ha evidenciado una orientación que favorece la termorregulación del nido (Grigg 1973,Grigg & Underwood 1977,Bordy et al. 2004); sin embargo, no pudieron determinar si evitar la exposición excesiva al sol incidía en la orientación de los termiteros.
La selección del lugar, la orientación y la arquitectura son los mecanismos principales que utilizan los insectos sociales para regular el microclima de su nido (Jones & Oldroyd 2006). Si bien las termitas y abejas pertenecen a órdenes diferentes, comparten similitudes en sus comportamientos sociales y en la organización de sus colonias, que incluyen castas especializadas (Carrijo et al. 2012). En tal sentido, en la abeja Melipona subnitida, un estudio en la costa oriental de Brasil encontró que el patrón de anidamiento predominante es hacia el noreste, y aunque aún no se ha establecido la razón exacta, una teoría sugiere que esta orientación ayuda a mantener la temperatura ideal para el desarrollo larvario (Vaz et al. 2021). Asimismo, en Frieseomelitta, Partomona, Plebeia y Scaptotrigona, se ha observado una tendencia similar (da Costa-Macedo et al. 2020). Cabe destacar que todos estos estudios incluido el nuestro, se realizaron en regiones dentro de la franja tropical, donde la trayectoria solar y la incidencia de radiación presentan patrones comparables. Pero aún se desconoce el mecanismo que determina la orientación del nido y se requieren de estudios adicionales para determinar las razones detrás de este patrón.
Además de los factores morfológicos evaluados, un aspecto relevante pero que no se abordó en este estudio es la distribución espacial de los termiteros. En áreas pequeñas y heterogéneas, donde el clima es relativamente contaste, la vegetación y el tipo de suelo son determinantes para la distribución y abundancia de termitas (Tunes-Buchini 1999). Los análisis espaciales podrían revelar procesos adicionales que influyen en la construcción de los nidos y su relación con la disponibilidad de árboles. Este aspecto representa una línea de investigación importante para futuros estudios, que permitiría complementar los resultados obtenidos sobre las características morfológicas y de cobertura del dosel.
Conclusiones
Los resultados de este estudio resaltan la relación entre las características de los árboles y la presencia de termiteros, evidenciando que tanto las propiedades morfológicas como las condiciones estructurales de hábitat son determinantes para su establecimiento. La presencia de termiteros en árboles de mayor tamaño, con una mayor cobertura de dosel y una corteza de textura rugosa, sugiere que estas características no solo proporcionan refugio y un sustrato seguro, sino que también influyen en las condiciones ambientales internas de los termiteros, que son esenciales para su desarrollo y supervivencia.












 uBio
uBio