Introducción
Las especies poseen preferencias específicas de hábitat donde la sobrevivencia y la reproducción sean las más adecuadas (Khelifa et al. 2013). Los factores que determinan la distribución de una especie en un hábitat son principalmente las condiciones abióticas, disponibilidad de recursos, depredación, competencia y parasitismo (Khelifa et al. 2013). El ambiente donde habitan las libélulas puede tener efectos significativos sobre su comportamiento (Cochran 2003), como el caso de la luz, temperatura, humedad relativa, precipitación y viento son algunos de los componentes ecológicos que ejercen mayor acción sobre los insectos (Ross 1964) influyendo además del comportamiento, en el ciclo de vida, reproducción, entre otros (Yela & Holyoak 1997,Hykel et al. 2019,Lim-Franco & Trapero-Quintana 2020,Mariani-Ríos et al. 2022).
Las libélulas adultas habitan cerca de algún cuerpo de agua la mayor parte su vida (Gaynor 2008). No obstante, los periodos diarios de actividad pueden variar entre las especies, incluso también fluctúan entre machos y hembras (Gaynor 2008), las hembras realizan visitas a los sitios acuáticos para el apareamiento y la oviposición, mientras que los machos se encuentran más tiempo cerca de la fuente de agua esperando la llegada de las hembras (Gaynor 2008) defendiendo los sitios de oviposición, realizando vuelos de patrullaje o posándose en lugares prominentes (Switzer 2002,Gaynor 2008). El tipo de comportamientos de las libélulas adultas en los cuerpos de agua son los vuelos de patrullaje, cortejo y reproducción, protección de la pareja y peleas aéreas entre machos (Kirkton & Schultz 2001).
Los periodos de actividad de las libélulas también dependen de factores ambientales, como la temperatura que influye sobre los patrones de actividad diaria (Lutz & Pittman 1970,Switzer 2002,Hykel et al. 2019,Trapero-Quintana et al. 2021,Castillo-Pérez et al. 2022) e historia de vida (Zavorskas 1999,Stahl & Johansson 2024). La luz solar es importante debido a que influye como estímulo para la medida del tiempo en los ritmos diarios de actividad y estacionales como la reproducción (Krebs 1986) y el comportamiento de vuelo (Lutz & Pittman 1970,Hirota & Obara 2000,Gaynor 2008,Lambret & Stoquert 2011).
El viento afecta la abundancia (Suryanarayana et al. 2010), dispersión (Manoukis et al. 2011), disponibilidad de alimento (Dunn 1975,Khelifa et al. 2013) y en el éxito reproductivo de algunas especies (Weimerskirch et al. 2012).
Los ambientes urbanos pueden ser habitados por especies tolerantes a las condiciones que los influencian. Se sugiere que los ambientes lénticos urbanos son lugares importantes para la conservación de especies de odonatos (Román 2020). En el área urbana de la ciudad de La Paz se han registrado dos especies de libélulas (Limachi et al. 2015), Rhionaeschna peralta (Aeshnidae: Odonata) es una especie de tipo “volador”, es decir, durante el período de actividad está predominantemente en vuelo (Westfall 1978,Zavorskas 1999), habita aguas de poca corriente con mucha vegetación como pozos de agua y lagunas con macrófitas, vegetación densa o áreas abiertas (Roldan 1988,Dejoux 1991), es la especie de mayor distribución en el valle de La Paz, encontrándose en lagunas naturales y artificiales (Hurtado 2015). Sympetrum gilvum (Libellulidae: Odonata) es una especie de tipo “perchero”, es decir que frecuentemente perchan en el período activo y solo vuelan para capturar presas o interactuar con otras libélulas (Zavorskas 1999), habita en pozos y remansos con mucha vegetación (Roldán 1988), en el valle de La Paz aparentemente se encuentra en lagunas con abundantes macrófitas (Hurtado 2015).
En el presente estudio, se evalúa el patrón de actividad diaria a través del número de individuos activos de Rhionaeschna peralta (Fig. 1) y Sympetrum gilvum (Fig. 2) según algunos factores ambientales como temperatura, intensidad de luz y de viento en un estanque del Jardín Botánico La Paz del campus universitario de Cota Cota.
Área de estudio
El estudio se realizó en la ciudad de La Paz, Provincia Murillo del departamento de La Paz, en un estanque artificial del Jardín Botánico "La Paz", ubicado en el Campus universitario de Cota Cota de la zona sur de La Paz, un espacio con vegetación que se encuentra en medio del área urbana (16°32’20.01’’S, 68°04’08.96”W) a 3.400 m de altitud. El estanque está recubierto de piedras y cemento, en el interior se encuentran algas Bacillariophytas, macrófitas sumergidas (Elodea sp.) y macrófitas helófitas como Phragmites australis. El clima de La Paz presenta amplias variaciones de temperatura en el día y pocas variaciones a lo largo del año (Vargas 1992). Los meses más cálidos se presentan desde enero hasta abril y de octubre a diciembre, con temperatura media anual de 13.8 °C (Miranda et al. 2015) y las temperaturas más bajas ocurren durante junio a septiembre. Las precipitaciones ocurren durante los meses de diciembre a marzo (Vargas 1992) con promedio anual de 596.4 mm (Miranda et al. 2015), los meses de menor precipitación y radiación son de abril a agosto (Vargas 1992).
Métodos
El estudio se realizó entre abril y junio del 2004, que es la época de transición húmeda-seca hasta inicios de la seca en junio, caracterizada por heladas en las noches.
Se aplicó un esfuerzo total al trabajo de nueve días (94 horas), con datos registrados cada 15 minutos desde las 07:00 hasta 19:00 h, con el número de individuos por especie (Rhionaeschna peralta y Sympetrum gilvum) mediante conteo por caminatas alrededor del estanque. Paralelamente, se registró la temperatura con termómetro de ambiente, intensidad de luz mediante un luxómetro, que proporciona información de la iluminancia definida como la relación entre el flujo luminoso que incide sobre una superficie y el tamaño de esta superficie, su unidad es el lux (lx); finalmente, la intensidad de viento con un anemómetro. Estos instrumentos se instalaron en la orilla de la laguna a un metro de altura.
Para el análisis de los datos, debido a que no presentaron una distribución normal, determinado por la prueba de D’Agostino (p < 0.01), se utilizó una prueba no paramétrica para correlacionar los factores ambientales y el número de individuos de ambas especies mediante coeficiente de correlación Spearman con el programa Biostat (Ayres et al. 2004). Las diferencias entre especies fueron analizadas con la prueba U de Man-Withney Z(u para muestras independientes (significancia del 5%).
Resultados
La actividad de Rhionaeschna peralta se inicia a partir de las 08:15 h, aumenta hasta las 10:00 h con un máximo de 6 individuos y posteriormente disminuye paulatina e irregularmente hasta las 18:00 h, hasta que la actividad concluye a las 18:30 h (Fig. 3). Sympetrum gilvum presenta un rango de actividad más estrecho que R. peralta a lo largo del día, el tiempo activo de los individuos ocurre a partir de las 11:00 h, con puntos máximos de 12:00 - 13:15 h con un máximo de 15 individuos en la laguna y finaliza a las 15:00 h (Fig. 3). El promedio del número de individuos de ambas especies presentó diferencias, así el valor de Rhionaeschna peralta es ligeramente mayor que Sympetrum gilvum (Prueba U de Man-Whitney Z(u = 2.98, p < 0.05). No obstante, la variación de individuos de S. gilvum es mayor a la de R. peralta en el periodo de tiempo donde presenta mayor actividad en la laguna.
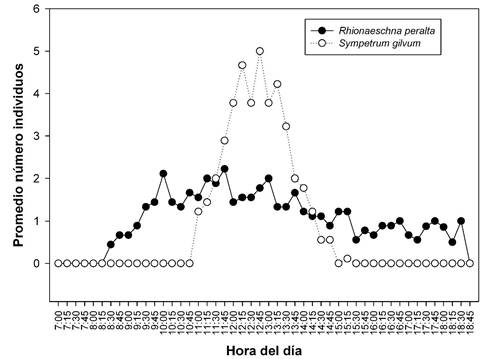
Figura 3. Variación del número promedio de individuos de Rhionaeschna peralta y Sympetrum gilvum de acuerdo a la hora del día.
Temperatura
La temperatura presentó un promedio de 15.3°C, el mínimo registrado fue de 1.5°C y el máximo de 22.5°C. La actividad de R. peralta está relacionada positivamente con la temperatura ambiental (rs = 0.57, p <0.05, Fig. 4) la cual se presenta a intervalo entre 7°C y 22°C; la máxima actividad se concentra entre 15°C y 16°C (Fig. 5).
La actividad de S. gilvum tiene correlación positiva con la temperatura (rs = 0.51, p <0.05) sin embargo, el intervalo de actividad se encuentra reducido, entre 13°C y 22°C, la máxima actividad se presenta entre los 18 y 19°C. Se observa disminución del número de individuos de ambas especies con las temperaturas más elevadas (Fig. 6).
Intensidad de luz
La actividad de R. peralta presenta relación positiva con intensidad de luz (rs = 0.62, p <0.05). Durante el día, el máximo de intensidad corresponde entre las 11:00 h y 13:00 h (Fig. 5). La actividad de S. gilvum está mejor relacionada a este factor (rs = 0.72, p <0.05, Fig. 4). En ambas especies, se observa que, al aumentar y disminuir la intensidad de luz, el número de individuos presenta la misma tendencia.
Intensidad de viento
La intensidad de viento es reducida, no hallándose velocidades promedio superiores a 2 km/h. El número de individuos de R. peralta está escasamente correlacionado con la velocidad del viento (rs = 0.27, p= 0.013), la actividad de los individuos se presenta entre 0.4 y 1.2 km/h.
Sympetrum gilvum también muestra tendencia positiva (rs = 0.49, p<0.05, Fig. 4), el intervalo de actividad varía entre 0.7 y 1.2 km/h. La actividad de ambas especies se reduce cuando la intensidad de viento aumenta en horas de la tarde (Fig. 6).
Discusión
La variabilidad en el número de individuos activos de ambas especies en la laguna, podría estar relacionada con una marcada estacionalidad de los odonatos adultos, es decir, están activos durante ciertos meses del año, el periodo de vuelo dura solo unas pocas semanas (McMillan 2000,Westfall 1978). El número de individuos en la laguna en ambas especies presentan diferencias posiblemente influenciadas por las características inherentes a la naturaleza del grupo taxonómico (Familia) al que pertenece, así R. peralta pertenece a la familia Aeshnidae grupo de los “voladores” (Corbet & May 2008) donde generalmente de uno a dos machos controlan, patrullan y defienden el territorio de la laguna para aparearse y las hembras visitan para ovipositar (De Marco et al. 2005). Mientras que Sympetrum gilvum pertenece al grupo de los “percheros” (Corbet & May 2008) donde varios individuos machos controlan y vigilan un pequeño espacio de la orilla de la laguna, suelen pasar tiempo posados sobre ramas o piedras y realizan vuelos rápidos para repeler otros machos que ingresan a su espacio territorial y seguir a las hembras durante la oviposición (De Marco et al. 2005).
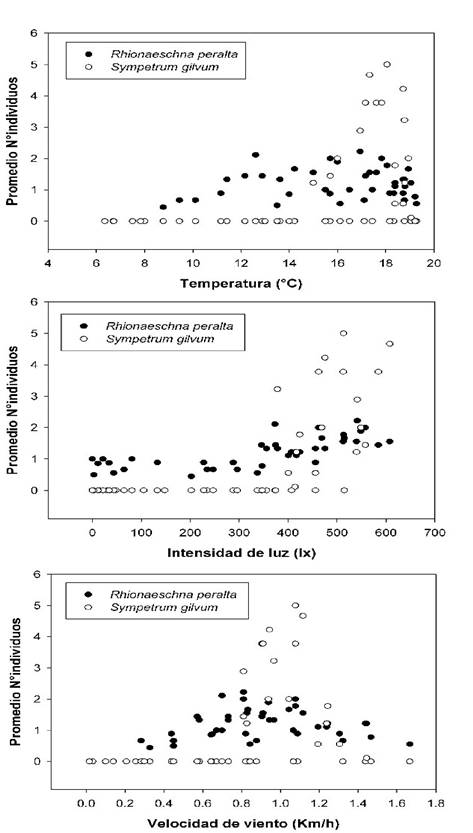
Figura 4. Distribución del promedio del número de individuos de Rhionaeschna peralta y Sympetrum gilvum respecto a la temperatura, intensidad de luz y velocidad del viento.
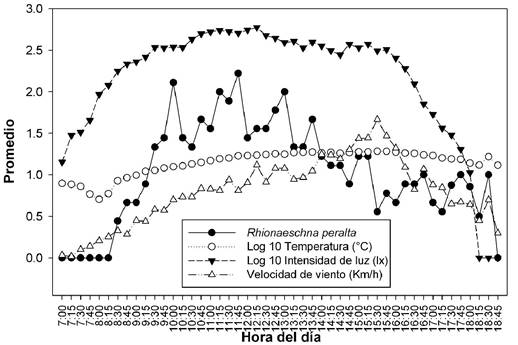
Figura 5. Variación del número de individuos de Rhionaeschnaperalta, temperatura, intensidad de luz y velocidad del viento de acuerdo a la hora del día.
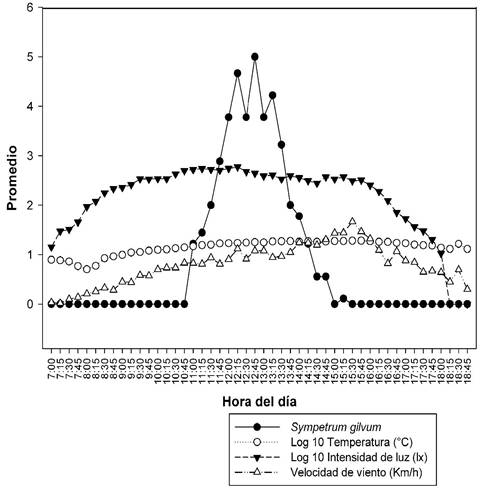
Figura 6. Variación del número de individuos de Sympetrum gilvum, temperatura, intensidad de luz y velocidad del viento de acuerdo a la hora del día.
La mayor parte de los individuos adultos presentes en los cuerpos de agua son machos territoriales, los cuales dedican la mayor parte del tiempo en defender el territorio donde la hembra deposita sus huevos (Cochran 2003,Luna-León et al. 2014). La actividad de Rhionaeschna peralta inicia a partir de las 08:00 h, mientras que Synpetrun gilvum inicia a las 11:00 h. En ecosistemas templados de América del Norte en altitudes cercanas al nivel del mar, especies de aeshnidos (Anax) inician su actividad entre las 07:00 h y 08:00 h (Lutz & Pittman 1970,May 1995), otras a las 09:00 h (Mc Elwey 1997). Algunos libellulidos, inician su actividad entre las 08:00 h y 10:00 h (Lutz & Pittman 1970,Fincke 1992,Koenig 1990). En este estudio, la actividad de las libélulas se inicia más tarde debido posiblemente a las condiciones meteorológicas poco favorables de la ciudad de La Paz como la baja temperatura del ambiente y elevada altitud.
La actividad de las dos especies se relaciona significativamente con la temperatura, como en la mayoría de los insectos, la temperatura regula la actividad de las libélulas (McElwey 1997). La fluctuación diaria de temperatura es probablemente el factor más importante que determina los patrones de actividad de adultos como los ritmos diarios de vuelo, alimentación y reproducción (Lutz & Pittman 1970,Zavorskas 1999).
La temperatura mínima de inicio de actividad es de 8 °C para R. peralta, mientras que S. gilvum inicia a los 15 °C. En altitudes menores, los odonatos inician actividad a 19 °C (May 1995), 25 °C (Lutz & Pittman 1970); otros insectos inician entre 15 °C y 18 °C (Marden 1995,Hirota & Obara 2000) y, en el Valle de La Paz, los himenópteros inician su actividad a entre 10 °C y 14°C (Altamirano 1991,Loayza 1998). Estudios con himenópteros en La Paz, muestran que la actividad también se correlaciona con la temperatura (Loayza 1998).
La libélula R. peralta presenta el mayor número de individuos activos entre 14°C y 16 °C, y la temperatura máxima de actividad a 21 °C. En S. gilvum la mayor actividad ocurre entre 17 °C y 19 °C, la mayor temperatura de actividad a 21 °C. Estos valores son similares a la máxima actividad de otros insectos en la región del valle (Altamirano 1991,Loayza 1998).
Las libélulas, como organismos poiquilotermos, aprovechan las respuestas de comportamiento para evitar temperaturas extremas o para elevar su temperatura lo suficiente para realizar sus actividades (termorregulación) (Hoar 1978,Robertson et al. 1996). R. peralta inicia su actividad a tempranas horas con bajas temperaturas (menor a 10 °C), para esto, necesita termorregularse adecuadamente mediante el uso de la energía metabólica y la energía solar (Hoar 1978) "temblando", agitando las alas o mediante posturas que aumentan la superficie de exposición a la luz del sol para calentarse (Cochran 2003,Robertson et al. 1996,Zavorskas 1999). Si la temperatura ambiental es elevada, la temperatura corporal se reduce mediante el percheo en sombra (Cochran 2003).
La regulación de la temperatura corporal en S. gilvum como un típico libelúlido, cambia su temperatura alterando la orientación del cuerpo respecto a la luz solar y modifican el tiempo de actividad diurna (Corbet & May 2008). Ellos son incapaces de calentarse a sí mismos "temblando" y no pueden transferir el exceso de calor desde el tórax a su abdomen, como lo realizan los aeshnidos (Marden 1995,May 1995). Es posible que estas razones explican que R. peralta presenta actividad en un amplio rango de temperatura y S. gilvum es activo en un rango más estrecho de temperatura.
La luz juega un papel importante en la vida de las libélulas, ya que éstas pueden detectar visualmente la superficie del agua al percibir una superficie reflectante (Torralba & Ocharan 2005). Para ambas especies, la actividad está fuertemente relacionada con la intensidad de luz, donde la máxima actividad coincide con la máxima intensidad lumínica (Fig. 5, 6). La radiación solar en los días soleados permite una intensa actividad de patrulleo, forrajeo y reproductiva (Cordero 2002,Cochran 2003). En Pieridae (Lepidoptera), la intensidad de luz también se correlaciona significativamente con la actividad (Hirota & Obara 2000).
En contraste a lo observado en el presente estudio, Lutz & Pittman (1970) mencionan que la actividad no coincide precisamente con los cambios en la intensidad de luz ya que cuando la intensidad es muy alta, la actividad disminuye para poder refrescarse en la sombra. Rhionaeshna peralta y Synpetrun gilvum no disminuyen su actividad a la máxima intensidad lumínica debido a que las máximas temperaturas son menores que en zonas de menor altitud, entonces necesitan de altas temperaturas para estar activas.
La actividad de ambas especies se correlaciona positivamente con la velocidad del viento, posiblemente se debe a que las velocidades son bajas y no afecta en gran medida a la actividad de ambas especies. Al parecer, no tiene un efecto significativo en la actividad de las libélulas (May 1995), el efecto podría ser indirecto sobre la temperatura reduciendo la difusión de calor. Sin embargo, a inicios de la época seca, se puede observar incremento de la velocidad de viento durante la tarde (Urcullo 1997) y coincide con una drástica disminución de la actividad de las dos especies. La actividad de ambas especies se presenta hasta un máximo de 1.2 km/h, la velocidad con mayor actividad se ha registrado entre 0.8 y 1 km/h. Popova & Haritonov (2014) registraron que la velocidad del viento óptima para actividad de algunos odonatos es de 0.3 a 0.5 km/h.
Mediante observaciones in situ, se evidenció que existen "ráfagas" de viento espontáneas especialmente en horas de la tarde, el cual llega a interrumpir el vuelo incluso influye en la muerte de individuos, provocando desequilibrio de los que vuelan muy cercanos a la superficie del agua en la laguna. Un factor no evaluado en el estudio es la nubosidad, se observó que cuando se nubla esporádicamente, la cantidad de individuos de Synpetrun gilvum disminuye al alejarse del estanque para refugiarse entre los árboles cercanos y regresan a la laguna cuando retorna la luz solar directa. En general, de todos los factores analizados, ninguno influye a tal punto que podría explicar por sí solo las actividades de las libélulas, el que se aproxima más es la intensidad de luz. Lutz & Pittman (1970) mencionan que los efectos de la hora del día, temperatura ambiental y la intensidad de luz sobre la actividad de las especies no puede ser claramente separada ya que son factores interdependientes.
Conclusiones
El número de individuos adultos de libélulas en un estanque artificial en un área verde de la ciudad de La Paz varía según la especie, Rhionaeschna peralta ha sido registrado hasta un máximo de seis individuos, cuya actividad se inicia a partir de las 08:00 h hasta las 18:30 h en el periodo de estudio. Synpetrun gilvum registró hasta 15 individuos y presenta un intervalo de actividad más estrecho, desde las 11:00 h hasta las 15:15 h. Existe una correlación positiva entre la temperatura ambiental y el número de individuos de R. peralta cuya actividad se encuentra entre 7 y 22°C y en menor grado S. gilvum, con actividad entre 13 y 22°C. La intensidad de luz es uno de los factores que más se correlaciona positivamente con la actividad de ambas especies de libélulas, principalmente sobre S. gilvum. La intensidad del viento también se correlaciona con el número de individuos de ambas especies. Finalmente, un solo factor no puede explicar la actividad de las dos especies, sino que son factores muy relacionados que en conjunto influyen en el comportamiento de las libélulas. La presencia de cuerpos de agua y vegetación en ambientes urbanos es importante para la existencia de organismos poco conocidos como las libélulas, a la vez, la documentación de las condiciones meteorológicas puede ser útiles para monitorear el impacto de las variaciones de temperatura a nivel regional sobre las comunidades de organismos.












 uBio
uBio 



