Ecología en Bolivia
versión impresa ISSN 1605-2528versión On-line ISSN 2075-5023
Ecología en Bolivia v.48 n.1 La Paz abr. 2013
Fenología reproductiva de la kewiña (Polylepis tomentella, Rosaceae) en la puna semihúmeda de Chuquisaca (Bolivia)
Reproductive phenology of kewiña (Polylepis tomentella, Rosaceae) in the semi-humid puna of Chuquisaca (Bolivia)
Alejandra I. Domic1,2, Evelina Mamani3 & Gerardo Camilo1
1Departamento de Biología, Saint Louis University, 3507 Laclede Ave, San Louis, MO 63103, USA
2Herbario Nacional de Bolivia, Campus Universitario, Cota Cota, Casilla 10077 - La Paz, Bolivia,
Email: alejandradomic@gmail.com Autora de correspondencia
3Carrera de Ingeniería de Recursos Naturales, Universidad Mayor, Real y Pontificia de San Francisco Xavier de Chuquisaca, Calle Calvo 132, Sucre, Bolivia
Resumen
En el presente estudio evaluamos la fenología reproductiva de la kewiña (Polylepis tomentella, Rosaceae) en la puna semihúmeda de Bolivia. Esta especie crece en el límite superior del bosque de Bolivia y se encuentra amenazada por bajas tasas de regeneración, intensificación del uso del suelo y cambio climático. Durante dos años consecutivos, realizamos visitas mensuales para determinar la época de floración y fructificación en una población ubicada en Jumbate, Chuquisaca. Los resultados mostraron que un elevado porcentaje de los individuos de P. tomentella (90% en 2009 y 80% en 2010) florecieron durante la época seca (mayo-octubre) y fructificaron a principios de la época húmeda (agosto-diciembre). Los árboles produjeron tres veces más flores (44.7 ± 6.4 flores/rama) y frutos (24 ± 2.7 frutos/rama) que los arbustos (15.86 ± 2.18 flores/rama; 9.3 ±1.3 frutos/rama). Los árboles con una copa mayor a 200 m2 produjeron 2.5 veces más flores frutos que árboles más pequeños. Los patrones reproductivos de P. tomentella son similares a los de especies arbóreas que habitan los bosques secos tropicales. Los resultados del estudio pueden apoyar a programas de reforestación porque se identificaron épocas de floración y fructificación, así como las características morfológicas de los individuos potencialmente semilleros.
Palabras clave: Andes, Bosques altoandinos, Chuquisaca, Límite superior del bosque, Producción de flores y frutos.
Abstract
This study evaluated the reproductive phenology of the kewiña (Polylepis tomentella, Rosaceae) in the semi-humid puna of Bolivia. The species grows in the treeline of Bolivia and is threatened by low rates of regeneration, land-use intensification, and climate change. For two consecutive years, we carried out monthly visits to determine the flowering and fruiting time in in Jumbate, Chuquisaca. Results showed that a large percentage of individuals of P. tomentella (90% in 2009 and 80% in 2010) produced flowers during the dry season (May-October) and fruits at the beginning of the wet season (August-December). Trees produced three times more flowers (44.7 ± 6.4 flowers/branch) and fruits (24 ± 2.7 fruits/branch) than shrubs (15.86 ± 2.18 flowers/ branch; 9.3 ±1.3 fruits/branch). Furthermore, large individuals with a canopy area of 200 m2 exhibited 2.5 times higher flower and fruit production than smaller trees. Reproductive patterns of P. tomentella are similar to those of tree species inhabiting tropical dry forests. The results of the study can support reforestation programs as we identified periods of flowering and fruiting as well as the morphological characteristics of potentially seeder individuals.
Keywords: Andes, Chuquisaca, Flower and fruit production, High Andean forests, Treeline.
Introducción
El estudio de la biología reproductiva de especies amenazadas constituye un aspecto importante para el desarrollo exitoso de programas de conservación (Andersson 1995, Tye 2002). El entendimiento del efecto de las actividades humanas en la reproducción de especies de plantas requiere conocer aspectos básicos de la biología reproductiva de las especies como la fenología, sistema de incompatibilidad y grado de especialización del sistema de polinización (Roldán & Larrea 2003, Menz et al. 2011). Asimismo, este conocimiento puede ser utilizado para implementar estrategias de conservación, permitiendo promover el flujo genético entre individuos y así aminorando los efectos deletéreos de la endogamia y deriva genética (Oostermeijer et al. 2003).
En los Andes, los bosques de Polylepis constituyen un componente arbóreo importante del límite superior del bosque. Forma parches de bosques monoespecíficos distribuidos en laderas de montañas y roquedales (Kessler 1995a, b). Los bosques proveen valiosos servicios ambientales y socioeconómicos, como la protección de fuentes de agua, control de erosión, regulación del microclima y hábitat para numerosas especies de animales y plantas (Fjeldså & Kessler 1996). Sin embargo, los bosques de Polylepis han sido impactados negativamente por actividades antrópicas, como la extracción de leña, incendios, sobrepastoreo y agricultura. Estas actividades han producido la pérdida de extensas áreas boscosas, cambios en los patrones de regeneración y composición de especies (Renison et al. 2002, 2006, Capriles & Flores-Bedregal 2002, Cierjacks et al. 2008 a, b).
La conservación de los bosques de Polylepis ha estado orientada mayormente a la reforestación de bosques degradados, con la meta de incrementar la densidad de la cobertura vegetal y/o aumentar el área boscosa (Fjeldså & Kessler 1996, Renison et al. 2005). Adicionalmente, se han desarrollado programas de forestación en áreas consideradas potencialmente adecuadas para Polylepis con la intención de disminuir la erosión del suelo y escorrentía (Ibisch 2002). La reforestación ha sido adoptada ampliamente por ser económicamente atractiva, asociada con el bajo costo de inversión y el alto potencial de recuperación de los bosques (Fjeldså & Kessler 1996). Sin embargo, el grado de éxito de estos programas ha estado limitado por el pobre conocimiento sobre la ecología de las especies, particularmente información sobre la biología reproductiva, germinación de semillas y requerimiento de hábitat de las plántulas.
Dado el conocimiento fragmentado sobre la biología reproductiva de Polylepis, en el presente estudio evaluamos la fenología de Polylepis tomentella por dos años consecutivos. Esta especie fue escogida porque todavía posee grandes extensiones de bosques, distribuidos en forma de fragmentos boscosos (Navarro et al. 2010). Los objetivos de la investigación fueron: 1) determinar la época de floración y fructificación y 2) determinar la relación entre producción de flores y frutos y el tamaño de la planta. Consideramos que el entendimiento de los patrones fenológicos proveerá una mejor perspectiva sobre los ciclos reproductivos de la especie. Asimismo, apoyará a los programas de reforestación al determinar épocas para la recolección de semillas, así como las características morfológicas de los individuos semilleros.
Área de estudio
El estudio se realizó en la región sur-central de los Andes de Bolivia, específicamente en la comunidad de Jumbate (Municipio de Tarabuco, Departamento de Chuquisaca) con coordenadas 19º10'50" S, 64º54'48" O. La región se caracteriza por un clima semiárido con una pronunciada época seca entre mayo y octubre. La temperatura promedio es de 15.8°C y la precipitación total anual es de 445 mm (SENAMHI 2010). La vegetación del área es característica de la puna semi-húmeda (Ibisch et al. 2003) e incluye mayormente pastizales, arbustales, bosques de Polylepis y vegetación herbácea aislada a mayores elevaciones. Los bosques de P. tomentella son unidades aisladas, distribuidas entre 3.300-3.800 m; se encuentran ubicados en laderas rocosas con suelos mayormente superficiales y con una textura franco-arenosa. Las plantas que componen el subdosel incluyen arbustos de Baccharis y Colletia spinosissima, pastos (Stipa spp. y Festuca spp.) y pequeñas hierbas (Plantago tomentosa y Gamochaeta spicata).
Descripción de la especie de estudio
Polylepis tomentella Weddell (Rosaceae, Tribu Sanguisorbeae) incluye árboles y arbustos siempreverdes que crecen en los Andes de Perú, Bolivia y Argentina (Kessler 1995a). En la región sur-central Andina de Bolivia, por encima de los 3.000 m, constituye el elemento arbóreo dominante. Crece en suelos rocosos y arenosos, formando fragmentos de bosques donde constituye la única especie arbórea (Navarro et al. 2010). Las plantas producen inflorescencias erectas o colgantes, con 1-5 flores (hasta 8). Las flores son hermafroditas y pequeñas (2 mm de diámetro) y poseen características asociadas con la polinización por el viento, incluyendo corolas inconspicuas y reducidas, estambres grandes, un estigma amplio y seco y protoginia (Simpson 1979, Kessler 1995a). Durante la maduración de las flores, el gineceo madura primero, caracterizado por un estigma amarillo receptivo al centro de la flor (estadio femenino; Fig. 1b). Después de 48 horas, las flores se abren totalmente, las anteras se rompen longitudinalmente y el estigma se marchita (estadio masculino; Fig. 1c) (Domic 2012). Los frutos son aquenios con una sola semilla, dispersados por el viento. La especie se encuentra categorizada como Casi Amenazada (UICN 2012).

Métodos
Realizamos un estudio fenológico de P. tomentella durante dos años consecutivos, entre julio de 2009 y junio de 2011. El área de estudio fue seleccionada por su fácil accesibilidad y factibilidad para realizar visitas mensuales. En 2009, 40 individuos fueron marcados permanentemente y en 2010, se incluyó un segundo grupo de 40 plantas. Los individuos monitoreados en 2009 también fueron evaluados en 2010. En total, 80 individuos fueron monitoreados, de los cuales 40 fueron árboles y 40 arbustos. Los árboles fueron clasificados como individuos con una altura mayor a 50 cm y un tallo monopodial de por lo menos 30 cm de altura; mientras que a los arbustos como individuos con una altura mayor 50 cm y con múltiples tallos basales. A partir de julio de 2010, cuantificamos mensualmente el número de flores en estado femenino (estigma receptivo) y en el masculino (estambres maduros y estigma marchito).
Seleccionamos cuatro etapas fenológicas antes de comenzar la evaluación: a) brotes florales, b) flores maduras, c) frutos maduros y d) frutos secos retenidos en la planta (Fig. 1). La aparición de hojas verdes no fue incluida como parte de este estudio porque otros estudios mostraron que la producción de hojas en Polylepis no difiere significativamente a lo largo del año (Hensen 1995, Nina et al. 2004). En cada planta seleccionamos cuatro ramas de 40 cm de largo y cuantificamos el número de brotes florales, flores y frutos. Las ramas fueron seleccionadas considerando la representatividad de producción de estructuras reproductivas en comparación a toda la copa. Las ramas tenían diferentes exposiciones en la copa pero siempre al alcance del evaluador.
Las plantas de P. tomentella fueron medidas, registrando los siguientes caracteres alométricos: Altura total, altura del tronco, diámetro del tallo y área del dosel. Debido a que los árboles raramente alcanzan alturas mayores a 2 m y el tronco es usualmente menor a 1 m, medimos el diámetro del tallo a una altura de 0.5 m de la base. En el caso de los arbustos, medimos el diámetro de los tallos a 0.1 my sólo se incluyeron los tallos principales (Dallmeier 1992).
Análisis de datos
Para determinar la relación entre éxito reproductivo, hábito y tamaño de la planta, utilizamos la producción máxima de flores y frutos de los individuos por cada ciclo reproductivo.
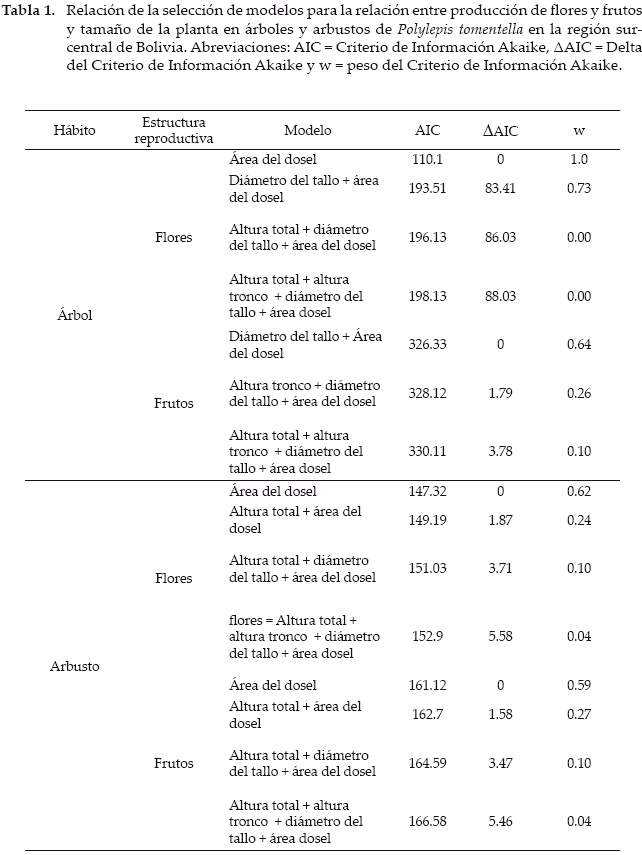
Utilizamos una ANOVA de una vía para determinar diferencias en la producción de flores y frutos entre árboles y arbustos. Realizamos una serie de modelos lineares generalizados (MLG) para determinar la relación entre producción de flores, frutos y caracteres alométricos. Los modelos morfométricos fueron analizados para árboles y arbustos por separado. El modelo inicial incluyó todos los caracteres cuantificados (altura total, altura tronco, diámetro del tallo y área de la copa). Subsecuentemente se obtuvieron una serie de modelos mediante regresiones escalonadas (en inglés: stepwise regressions). Para determinar el modelo que mejor explica la relación entre producción rendimiento reproductivo y tamaño de la planta, utilizamos el Criterio de Información Aikaike (AIC por sus siglas en inglés). Considerando que AIC es sólo un estimado, también empleamos ΔAIC y el peso de AIC para apoyar la selección del modelo (Richards 2005). Los modelos con el valor más pequeño de AIC y con un valor de ΔAIC < 2 fueron considerados como los más parsimoniosos. Cuando dos modelos fueron seleccionados en base a ΔAIC, el peso de AIC fue utilizado para seleccionar sólo uno de ellos. Todos los análisis estadísticos fueron realizados utilizando el entorno R versión 2.9.0 (R Development Core Team 2011).
Resultados
Fenología reproductiva
La producción de brotes florales se produjo durante la época seca (mayo hasta septiembre) (Figura 2a). La floración de P. tomentella comenzó a principios de la época seca (junio) y duró hasta inicios de la época húmeda (octubre) (Fig. 2b). El pico de floración fue registrado al final de la estación seca, entre julio y septiembre, cuando un gran porcentaje de los individuos florecieron (90% en 2009 y 80% en 2010). Una pequeña proporción de individuos reproductivos (10%) produjo flores durante todo el año. Los árboles y arbustos exhibieron una sincronización en la floración y producción de brotes florales. Las plantas de P. tomentella produjeron en promedio 18.9 ± 4 flores/rama durante la época de floración (abril-septiembre). La mayoría de las plantas experimentó una menor producción de flores en 2010 (18.8 ± 3.5 flores/rama) en comparación al 2009 (25.0 ± 4.6 flores/rama), pero esta diferencia no fue estadísticamente significativa (F = 1.84, P = 0.17).
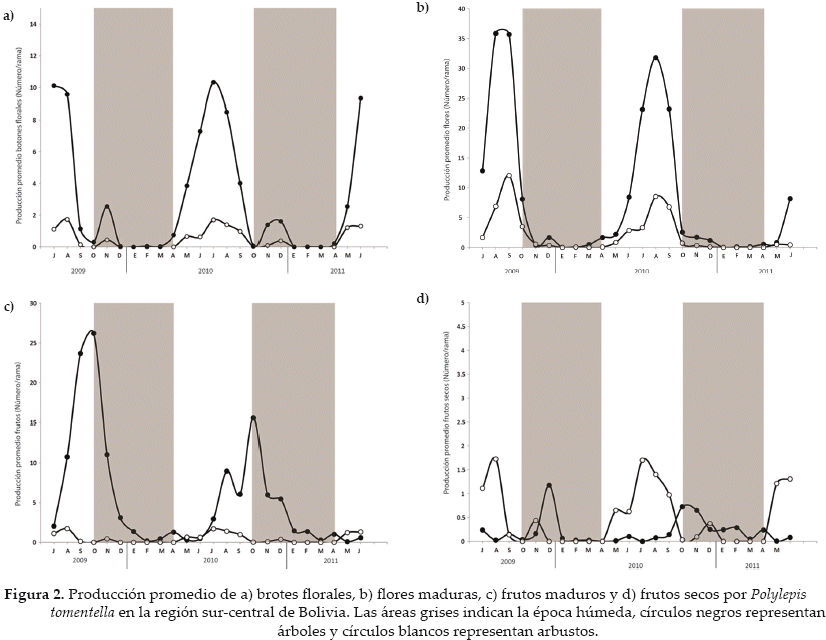
Una mayor proporción de flores en estado masculino fue observada durante la temporada de floración. La mayor producción de flores masculinas se observó en agosto, cuando los árboles contenían en promedio 15.3 ± 2.6 flores masculinas/rama, la mayor producción de flores femeninas también se observó en agosto, cuando los árboles contenían 8.5 ± 1 flores femeninas/rama. En 2010, se observó una relación entre flores femeninas/masculinas de 0.4 durante la época de floración (julio-octubre). Las plantas fructificaron a partir de mediados de la estación seca e inicio de la húmeda (agosto-diciembre) con un pico de fructificación entre septiembre y octubre (Fig. 2c). Una pequeña proporción de las plantas (< 20%) produjo frutos durante todo el año. No se observó una clara sincronía en el tiempo de fructificación en árboles y arbustos debido a que los arbustos produjeron un número despreciable de frutos (< 5 frutos/rama). Las plantas produjeron en promedio 3.0 ± 0.6 frutos/rama durante la época de fructificación (septiembre-octubre; Fig. 2c). En 2009, los individuos reproductivos produjeron 11.1 ± 1.9 frutos/rama y en 2010 6.2 ± 1.0 frutos/rama (F = 4.58, P < 0.05). Se observaron frutos secos en las plantas durante todo el año, particularmente entre julio y septiembre en 2010 y entre mayo y junio de 2011 (Fig. 2d). El monitoreo de individuos de P. tomentella durante dos años mostró que no todas las plantas permanentemente marcadas eran fértiles. Específicamente cuatro arbustos, monitoreados entre 2009 y 2011, no produjeron flores ni frutos durante el período en que el estudio fue llevado a cabo.
Producción de flores y frutos
Se observaron diferencias significativas en el éxito reproductivo entre árboles y arbustos (producción máxima de flores: F = 11.65, P < 0.0001; producción máxima de frutos: F= 19.75, P < 0.0001). Los árboles produjeron tres veces más flores (44.7 ± 6.4 flores/rama) y frutos (24.0 ± 2.7 frutos/rama), que los arbustos (15.9 ± 2.2 flores/rama; 9.3 ±1.3 frutos/rama).
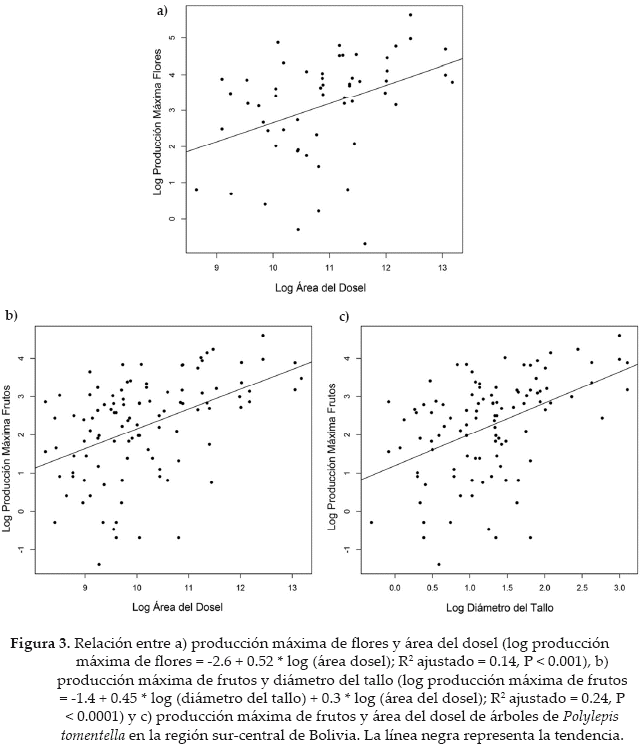
En el caso de los árboles, el modelo más parsimonioso que explicó la relación entre producción máxima de flores y el tamaño de la planta fue aquel que incluyó sólo área del dosel (Fig. 3a; log producción máxima de flores = -2.6 + 0.52 * log área dosel; R2 ajustado = 0.14, P < 0.001). El modelo exhibió el menor valor de ΔAIC y peso AIC (Tabla 1). En el caso de la producción máxima de frutos, el modelo más parsimonioso fue aquel que incluye el diámetro del tallo y el área del dosel (Figs. 3b-c; log producción máxima de frutos = -1.4 + 0.45 * log diámetro del tallo + 0.3 * log área del dosel; R2 ajustado = 0.24, P < 0.0001). En ambos casos, la producción estuvo relacionada positivamente con el tamaño de la planta. Para los arbustos, la producción máxima de flores y frutos fue explicada por los modelos que incluyeron solo el área del dosel como variable explicativa (log producción máxima de flores = 0.38 + 0.2 * log área dosel; R2 ajustado = 0.01, P = 0.51; log producción máxima de frutos = -1.39 + 0.33 * log área dosel; R2 ajustado = 0.003, P = 0.28). Sin embargo, la varianza explicada por ambos modelos fue despreciable.
Discusión
Fenología reproductiva
Polylepis tomentella florece mayormente durante la estación seca (mayo-octubre) y fructifica a comienzos de la temporada de lluvias (septiembre-noviembre). El patrón de floración y fructificación de la especie es similar al de otras especies de Polylepis (Hensen 1995, Kessler 1995b), así como de especies de árboles de los bosques secos tropicales (McLaren & McDonald 2003, Salinas-Peba & Parra-Tabla 2007). Por ejemplo, Justiniano & Fredericksen (2000) registraron que cerca del 50% de las especies arbóreas produjo flores durante la época seca, seguida por un pico de fructificación durante la época húmeda en un bosque seco boliviano.
Actualmente, existen muy pocos estudios sobre la fenología reproductiva de Polylepis. Los estudios publicados han mostrado que las especies de Polylepis que habitan ecosistemas semiáridos, poseen patrones fenológicos similares a P. tomentella. Por ejemplo, la maduración de los frutos de P. besseri ocurre al final de la estación seca hasta mediados de la época húmeda (Hensen 1995). En base colectas de herbario de especies de Polylepis bolivianas, Kessler (1995b) reportó un pico de floración durante la época seca y uno de fructificación a principios de la húmeda. En contraste, los patrones de floración y fructificación de P. tomentella difieren de los de P. quadrijuga, una especie que habita los páramos húmedos de Colombia, puesto que ésta florece durante la última temporada de lluvias y los frutos maduran durante la estación seca (Vélez et al. 1998).
Las condiciones ambientales durante la época seca favorecen el transporte de polen de las especies anemofílicas, como es P. tomentella. Por ejemplo, la baja humedad atmosférica, escasa precipitación y vientos frecuentes promueven la dispersión de polen y la fertilización de óvulos de individuos conespecíf icos (Russell et al. 1998, Culley 2002). Por otro lado, en el caso de las especies que florecen durante la época húmeda, los mecanismos involucrados en el transporte de polen son menos claros puesto que las lluvias pueden dañar las flores, reducir la viabilidad del polen e inhibir el transporte de polen (Fan et al. 2012). El movimiento de granos de polen bajo condiciones de alta humedad es un aspecto que merece ser estudiado en detalle para poder entender las estrategias reproductivas de especies anemófilas que habitan zonas húmedas. En todo caso, las estrategias demográficas comúnmente compartidas por varias especies de Polylepis crean condiciones favorables para el transporte de polen y por consiguiente el intercambio genético entre individuos. Particularmente resalta la tendencia a formar parches de bosques monoespecíficos con una alta densidad de individuos adultos (Cázares-Martínez et al. 2010).
Los patrones reproductivos de P. tomentella también apoyan la hipótesis de momento óptimo de germinación desarrollada por Van Schaik et al. (1993). La hipótesis postula que el tiempo de fructificación se ajusta de tal forma que precede al momento óptimo de germinación de semillas. En este sentido, la fructificación a finales de la estación seca podría haber evolucionado como una estrategia para incrementar la germinación de semillas y promover la supervivencia de plántulas. La fructificación a principios de la temporada de lluvias aumenta la posibilidad de establecimiento de las plántulas, puesto que las semillas tienen mayores probabilidades de llegar a suelos húmedos, donde pueden germinar y las plántulas pueden crecer antes de la próxima época seca (Garwood 1983). Altas tasas de emergencia de plántulas han sido observadas en otras especies de árboles que habitan los bosques secos estacionales de Botswana y Bolivia: En Acacia erioloba (Barnes 2001) y Anadenanthera columbrina (Federicksen et al. 2000), la emergencia de plántulas ocurre poco tiempo después de las primeras lluvias.
Polylepis tomentella muestra diferencias espaciales en el tiempo de floración y fructificación. Nina et al. (2004) llevaron a cabo estudios fenológicos en Puina (Departamento de Potosí, Bolivia) y mostraron que la especie florece principalmente durante la época húmeda (septiembre-febrero) y produce frutos a la mitad de la húmeda (diciembre-enero). Las plantas de nuestro estudio florecieron y frutificaron cuatro meses antes que las plantas del estudio de Nina et al. (2004). Las diferencias en el tiempo de floración y fructificación de las poblaciones de P. tomentella podrían estar relacionadas con la variación ambiental y genética (Elzinga et al. 2007). Aunque ambos sitios están situados cercanamente (83.26 kilómetros distancia euclidiana) y reciben similares cantidades de precipitación (455 mm/ año en ambos sitios), nuestra área de estudio es relativamente más cálido (temperatura promedio anual Jumbate: 15.8°C; Puina: 11.8°C) y se encuentra ubicado a un menor rango elevacional (Jumbate: 3.300-3.800 m, Puina: 3.600-4.200 m).
La asincronía de la fenología a lo largo de gradientes elevacionales ha sido comúnmente interpretada como producto de señales ambientales, particularmente la temperatura ambiental, que induce la formación de tejidos embrionarios (Stinson 2004). Sin embargo, experimentos que mantuvieron individuos de diferentes poblaciones bajo las mismas condiciones experimentales muestran que la fenología está determinada mayormente por la variabilidad genética (por ejemplo, Premoli et al. 2007, Vitasse et al. 2009). Esto sugirie que los individuos ubicados a elevaciones mayores y que tienden a florecer más tardíamente poseen una mayor ventaja para evitar daños a los tejidos por heladas.
Producción de flores y frutos
Los resultados mostraron una relación positiva entre el tamaño de los árboles de P. tomentella y la producción de flores y frutos. Al igual que en esta especie, la relación positiva entre producción de frutos y diámetro del tallo ha sido documentada en otras especies de árboles tropicales (Plumptre 1995, Snook et al. 2005, Arteaga 2007). Por ejemplo, Wright et al. (2005) encontraron una asociación positiva entre la reproducción y DBH para 16 especies de árboles en Barro Colorado (Panamá). Asimismo, Snook et al. (2005) mostraron que los árboles de Swietenia microphylla con un DBH mayor a 75 cm produjeron cuatro veces más frutos en comparación a los árboles más pequeños.
Una mayor producción de flores y frutos por los árboles más grandes de P. tomentella podría estar asociado con una mayor capacidad para invertir reservas en la reproducción sexual en vez de invertirlas en otras funciones, como crecimiento y mantenimiento de tejidos (Berry & Gorchov 2007). El incremento gradual en la producción de flores y frutos con el tamaño de los árboles de P. tomentella también sugiere que los individuos adquieren una capacidad progresiva para invertir recursos en la reproducción a medida que crecen (Snook et al. 2005, Domic & Capriles 2009). Nuestros resultados también mostraron que los árboles produjeron tres veces más flores y frutos que los arbustos. La mayor capacidad de producción de estructuras reproductivas por los árboles puede estar relacionada con una mayor capacidad para capturar la luz solar. Adicionalmente, los árboles probablemente poseen raíces comparativamente más grandes y profundas que los arbustos, lo cual les podría permitir capturar mayores cantidades de agua, reduciendo el estrés hídrico durante la época seca (Snook et al. 2005).
A pesar que los modelos morfométricos permitieron identificar los caracteres asociados con la producción de flores y frutos en P. tomentella, la varianza explicada por los mismos fue muy baja, particularmente para el caso de los arbustos (producción flores R2= 0.01; frutos R2 ajustado = 0.003). La baja varianza explicada por los modelos constituye una limitante para poder predecir efectivamente la reproducción según el tamaño de los individuos. Para poder mejorar los modelos morfométricos, se requiere incrementar el tamaño muestral así como el tiempo de monitoreo de la fenología reproductiva.
Debido a que no se encontró un punto de inflexión entre la reproducción y el tamaño de los árboles, sugerimos que los árboles podrían eventualmente producir mayores cantidades de flores y frutos a medida que crecen. Este fenómeno podría estar relacionado con la baja estatura de las plantas en comparación a otras poblaciones de la región. Domic (2012) encontró que la población de P. tomentella ubicada en Jumbate está compuesta mayormente por árboles (altura promedio: 100 cm; diámetro promedio del tallo: 4.3 cm) y arbustos pequeños (altura promedio: 67.4 cm; diámetro promedio tallo: 1.8 cm), lo cual podría estar relacionado con la extracción intensiva de leña en el pasado. Entre los siglos XVI y XIX, los bosques de Tarabuco fueron explotados para proveer leña y carbón vegetal para la ciudad de Sucre y para la activad minera en Potosí (Lizarraga 1987, Gade 1999). La intensa extracción de leña posiblemente produjo la pérdida de los individuos más grandes y promovió la transición hacia remantes de bosques dominados por pequeños árboles y arbustos (Renison et al. 2011). Con la gradual disminución de la demanda de leña desde el siglo XX, es posible que esta población se haya regenerando gradualmente y actualmente se encuentre en estadio temprano de sucesión.
Conclusiones
El presente estudio es uno de los pocos en reportar la fenología reproductiva de Polylepis tomentella, una especie de árbol que habita la puna semihúmeda de Bolivia. Los resultados muestran que la especie posee patrones de floración y fructificación similares a las especies típicas de bosques secos tropicales, es decir florece durante la época seca y fructifica durante la época húmeda. El análisis morfométrico mostró una asociación positiva entre la producción de flores y frutos y el tamaño de los árboles, pero no así para el caso de los arbustos. Asimismo, los árboles más grandes tendieron a producir una mayor cantidad de flores y frutos en comparación a los arbustos.
Debido a que la mayoría de las especies de Polylepis se encuentra amenazada (UICN 2012), la mejora de los programas de conservación constituye una prioridad. La restauración de los bosques degradados debe incluir prácticas que permitan reemplazar los individuos talados a través de regeneración natural y/o reforestación. Los resultados de este estudio sugieren que la tala de los individuos de mayor tamaño podría potencialmente disminuir la producción de frutos y semillas en el siguiente ciclo reproductivo, afectando negativamente en la regeneración de los bosques. Las actividades de conservación deben promover el mantenimiento de los árboles de mayor tamaño, los cuales pueden ser utilizados para colectar semillas y la producción de plantines en invernadero. Sin embargo, es importante tomar en cuenta varios aspectos al momento de la recolección de semillas; la recolección de semillas de los individuos más grandes puede incrementar la producción de plantines, sin embargo la diversidad genética de las poblaciones podría estar afectada (Breed et al. 2013). Si es que sólo se colectan semillas de algunos individuos, es posible que no todos los genotipos de la población sean incluidos, afectando la diversidad genética de los bosques a largo plazo (Ledig & Kitzmiller 1992). Por lo tanto, la reforestación de Polylepis debe considerar la promoción de altos niveles de variabilidad genética, particularmente en ambientes heterogéneos e imprevisibles los cuales son más vulnerables al cambio climático.
Agradecimientos
Agradecemos a Arely Palabral y Juan Alberto Peñaranda por sus sugerencias y apoyo en el campo. También agradecemos a Stephan Beck, Rosa Isela Meneses, José Capriles, Martha Serrano, Herbario Nacional de Bolivia y Herbario del Sur por el apoyo logístico. Este proyecto fue financiado por la Fundación Internacional para la Ciencia (IFS GRANT D/4839 Domic), Idea Wild y Brennnan Summer Fellowship otorgados a A. Domic y Beaumont Faculty Award de Saint Louis University otorgado a G. Camilo. Este estudio fue parte del doctorado de A. Domic.
Referencias
Andersson, G. J. 1995. Systematic and reproductive biology. Monographs in Systematic Botany of the Missouri Botanical Garden 53: 263-272. [ Links ]
Arteaga, L. 2007. Fenología y producción de semillas de especies arbóreas maderables en un bosque húmedo montano de Bolivia (PN ANMI Cotapata). Revista Boliviana de Ecología y Conservación Ambiental 21: 57-68. [ Links ]
Barnes, M. E. 2001. Seed predation, germination and seedling establishment of Acacia erioloba in northern Botswana. Journal of Arid Environments 49: 541-554. [ Links ]
Berry, E. J. & D. L. Gorchov. 2007. Female fecundity is dependent on substrate, rather than male abundance, in the wind-pollinated, dioecious understory palm Chamaedorea radicalis. Biotropica 39:186-194.
Breed, M. F., M. G. Stead, K. M. Ottewell, M. G. Gardner & A. J. Lowe. 2013. Which provenance and where? Seed sourcing strategies for revegetation in a changing environment. Conservation Genetics 14:1-10.
Capriles, J. M. & E. Flores Bedregal. 2002. The economic, symbolic, and social importance of the "keñua" (Polylepis spp.) during prehispanic times in the Andeanhighlands of Bolivia. Ecotropica 8: 225-231.
Cázares-Martínez, J., C. Montaña & M. Franco. 2010. The role of pollen limitation on the coexistence of two dioecious, wind-pollinated, closely related shrubs in a fluduating environment. Oecolia 164: 679-687.
Cierjacks, A., N. R. Katrin, K. Wesche & I. Hensen. 2008a. Effects of altitude and livestock on the regeneration of two tree line forming Polylepis species in Ecuador. Plant Ecology 194: 207-221.
Cierjacks, A., S. Salgado, K. Wesche & I. Hensen. 2008b. Post-fire population dynamics of two tree species in high-altitude Polylepis forests of Central Ecuador. Biotropica 40:176-182.
Culley, T. 2002. The evolution of wind pollination in angiosperms. Trends in Ecology & Evolution 17: 361-369. [ Links ]
Dallmeier, F. (ed.). 1992. Long-termmonitoring of biological diversity in tropical forest areas: methods for establishment and inventory of permanent plots. MAB DIGEST 11. UNESCO, Paris. 72 p. [ Links ]
Domic, A. I. & J. M. Capriles. 2009. Allometry and effects of extreme elevation on growth velocity of the Andean tree Polylepis tarapacana Philippi (Rosaceae). Plant Ecology 205: 223-234.
Domic, A. I. 2012. Effect of athropogenic disturbances on the regeneration of an Andean tree species. Tesis de doctorado en biología, Saint Louis University, Saint Louis. 169 p. [ Links ]
Elzinga, J. A., A. Atlan, A. Biere, L. Gigord, A. E. Weis & G. Bernasconi. 2007. Time after time: flowering phenology and biotic interactions. Trends in Ecology and Evolution 22: 432-439.
Fan X-L., S. C. H. Barrett, H. Lin, L-L. Chen, X. Zhou & J.-Y. Gao. 2012. Rain pollination provides reproductive assurance in a deceptive orchid. Annals of Botany 110: 953-958.
Fjeldså, J. & M. Kessler. 1996. Conserving the biological diversity of Polylepis woodlands of the highland of Peru and Bolivia. A contribution to sustainable natural resource management in the Andes. NORDECO, Copenhagen. 250 p.
Fredericksen, T. S., M. J. Justiniano, B. Mostacedo, D. Kennard & L. M. C. Donald. 2000. Comparative regeneration ecology of three leguminous timber species in a Bolivian tropical dry forest. New Forests 20: 45-64.
Gade, D. 1999. Nature and culture in the Andes. University of Wisconsin, Madison. 287 p. [ Links ]
Garwood, N. C. 1983. Seed germination in a seasonal tropical forest in Panama: a community study. Ecological Monographs 53:159-181. [ Links ]
Hensen, I. 1995. Estudios ecológicos y fenológicos sobre Polylepis besseri Hieron en la cordillera oriental boliviana. Ecología en Bolivia 23: 21-32. [ Links ]
Ibisch, P. 2002. Evaluation of a rural development project in southwest Cochabamba, Bolivia, and its agroforestry activities involving Polylepis besseri and other native species - A decade of lessons learned. Ecotropica 8: 205-218. [ Links ]
Ibisch, P. L., S. G. Beck, B. Gerkmann & A. Carretero. 2003. Ecorregiones y ecosistemas. pp. 47-88. En: Ibisch, P. L. & G. Mérida (eds.). Biodiversidad: La Riqueza Natural de Bolivia. Editorial FAN, Santa Cruz. [ Links ]
Justiniano, M. J. & T. S. Fredericksen. 2000. Phenology of tree species in Bolivian dry forests. Biotropica 32: 276-281.
Kessler, M. 1995a. The genus Polylepis (Rosaceae) in Bolivia. Candollea 50:131-171. [ Links ]
Kessler, M. 1995b. Polylepis-Wälder Boliviens: Taxa, Ökologie, Verbreitung und Geschichte. Dissertationes Botanicae 246, J. Cramer, Berlin. 303 p. [ Links ]
Kessler, M. 2002. The Polylepis problem: Where do we stand? Ecotropica8:97-110. [ Links ]
Ledig, F. T. & J. H. Kitzmiller. 1992. Genetic strategies for reforestation in the face of global climate change. Forest Ecology and Management 50:153-169.
Lizarraga, R. de. 1987[1605]. Descripción del Perú, Tucumán, Río de la Plata y Chile. Edición facsimíl. Historia 16, Madrid. 475 p. [ Links ]
McLaren, K. P. & M. A. McDonald. 2003. Seedling dynamics after different intensities of human disturbance in a tropical dry limestone forest in Jamaica. Journal of Tropical Ecology 19:567-578.
Menz, M. H. M., R. D. Phillips, R. Winfree, C. Kremen, M. A. Aizen, S. D. Johnson & K. W. Dixon. 2011. Reconnecting plants and pollinators: challenges in the restoration of pollination mutualisms. Trends in Plant Science 16: 4-12.
Navarro, G., S. Arrázola, J. A., Balderrama, W. Ferreira, De la Barra, N., C. Antezana, I. Gómez & M. Mercado. 2010. Diagnóstico del estado de conservación y caracterización de los bosques de Polylepis en Bolivia y su avifauna. Revista Boliviana de Ecología y Conservación del Medio Ambiente 28:1-35.
Nina, R., F. Marino & R. Veliz. 2004. Establecimiento de fuentes semilleras de Polylepis tomentella, Acacia feddeana y Prosopis ferox. Universidad Autónoma Tomas Frías, Potosí. 76 p. [ Links ]
Oostermeijer, J., S. H. Luijten & J. C. M. den Nijs. 2003. Integrating demographic and genetic approaches in plant conservation. Biological Conservation 113: 389-398.
Plumptre, A. J. 1995. The importance of seed trees for the natural regeneration of selectively logged tropical forest. Commonwealth Forest Review 74: 253-258. [ Links ]
Premoli, A. C., E. Raffaele & P. Mathiasen. 2007. Morphological and phenological differences in Nothofagus pumilio from constrasting elevations: evidence from a common garden. Austral Ecology 32: 515-523.
R Development Core Team. 2011. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna. http://www.R-project.org [ Links ]
Renison, D., A. M. Cingolani & R. Suarez. 2002. Efectos del fuego sobre un bosquecillo de Polylepis australis (Rosaceae) en las montañas de Córdoba, Argentina. Revista Chilena de Historia Natural 75: 719-727.
Renison, D., A. M. Cingolani, R. Suarez, E. Menoyo, C. Coutsiers, A. Sobral & I. Hensen. 2005. The restoration of degraded mountain woodlands: effects of seed provenance and microsite characteristics on Polylepis australis seedling survival and growth in Central Argentina. Restoration Ecology 13:129-137.
Renison, D., I. Hensen, R. Suarez & A. M. Cingolani. 2006. Cover and growth habit of Polylepis woodlands and shrublands in the mountains of central Argentina: human or environmental influence? Journal of Biogeography 33:876-887.
Renison, D., I. Hensen & R. Suarez. 2011. Landscape structural complexity of high-mountain Polylepis australis forests: a new aspect of restoration goals. Restoration Ecology 19: 390-398.
Richards, S. A. 2005. Testing ecological theory using the information-theoretic approach: examples and cautionary results. Ecology 86: 2805-2814. [ Links ]
Roldán, A. I. & D. M. Larrea. 2003. Fenología de 14 especies arbóreas y zoócoras de un bosque yungueño en Bolivia. Ecología en Bolivia 38:125-140.
Russell, S. K., E. W. Schupp & V. J. Tepedino. 1998. Reproductive biology of curlleaf mountain mahogany, Cercocarpus ledifolius (Rosaceae): self-compatibility, pollen limitation, and wind pollination. Plant Species Biology 13: 7-12.
Salinas-Peba L. & V. Parra-Tabla. 2007. Phenology and pollination of Manilkara zapota in forest and homegardens. Forest Ecology and Management 248: 136-142.
Snook, L. K., L. Cámara-Cabrales & M. J. Kelty. 2005. Six years of fruit production by mahogany trees (Swietenia macrophylla King): patterns of variation and implications for sustainability. Forest Ecology and Management 206:221-235.
Stinson, K. A. 2004. Natural selection favors rapid reproductive phenology in Potentilla pulcherrima (Rosaceae) at opposite ends of subalpine snowmelt gradient. American Journal of Botany 91: 531-539. [ Links ]
Tye A. 2002. Threatened species management in an oceanic archipelago: the Galapagos Islands. pp: 323-347. En: Maunder, M., Clubbe C., Hankamer C. & M. Groves (eds.) Plant Conservation in the Tropics: Perspectives and Practice. Royal Botanic Gardens, Kew. [ Links ]
UICN. 2012. La lista roja de especies amenazadas de la UICN. Versión 2012.2. http://www.iucnredlist.org Descargada 17 de octubre de 2012. [ Links ]
Van Schaik, C. P., J. W. Terborgh & S. J. Wright. 1993. The phenology of tropical forests: Significance and consequences for primary consumers. Annual Review of Ecology and Systematics 24: 353-377.
Velez, V., J. Cavelier & B. Devia. 1998. Ecological traits of the tropical treeline species Polylepis quadrijuga (Rosaceae) in the Andes of Colombia. Journal of Tropical Ecology 15: 771-787.
Vitasse, Y., S. Delzon, C. C. Bresson, R. Michalet & A. Kremer. 2009. Altitudinal differentiation in growth and phenology among populations of temperature-zone tree species growing in a common garden. Canadian Journal of Forest Research 39:1259-1269.
Wright, S. J., M. A. Jaramillo, J. Pavon, R. Condit, S. P. Hubbell & R. B. Foster. 2005. Reproductive size thresholds in tropical trees: variation among individuals, species and forests. Journal of Tropical Ecology 21: 307-315.
Artículo recibido en: Enero de 2013.
Manejado por: Mónica Moraes.
Aceptado en: Marzo de 2013.












 uBio
uBio 

