Ecología en Bolivia
versión impresa ISSN 1605-2528versión On-line ISSN 2075-5023
Ecología en Bolivia v.39 n.1 La Paz jul. 2004
Artículo
Composición, estructura y dinámica de un bosque seco semideciduo en Santa Cruz, Bolivia
Composition, structure, and dynamic of a semideciduous dry forest in Santa Cruz, Bolivia
Ynes V. Uslar 1, 2, 4, Bonifacio Mostacedo3 & Mario Saldias1
1Museo de Historia Natural Noel Kempff Mercado, Casilla # 2489, Santa Cruz, Bolivia
2Proyecto BOLFOR, Casilla # 6204, Santa Cruz, Bolivia
3Instituto Boliviano de Investigación Forestal (IBIF), Casilla #6204, bmostacedo@scbbs.net
4Dirección actual: Calle Padre Arce # 262, Casilla de correo # 903, Santa Cruz, Bolivia; e-mail:ynesuslar@scbbs.com.bo
Resumen
Analizamos la estructura, composición y dinámica de un bosque seco semideciduo en el Jardín Botánico de Santa Cruz, mediante dos evaluaciones (años 1995 y 2002). Medimos la riqueza y abundancia, el diámetro a la altura del pecho (DAP), posición de copa y presencia de bejucos en los árboles. Con estos datos, determinamos también la regeneración natural, tasas de mortalidad y reclutamiento, además de las tasas de incremento diamétrico y de área basal. Encontramos un promedio de 29.5 especies y 526 individuos, siendo mayores en la primera evaluación. Las especies más abundantes y frecuentes fueron Aspidosperma cylindrocarpon y Phyllostylon rhamnoides, mientras que las especies con mayor área basal fueron Anadenanthera colubrina y Gallesia integrifolia. Según la posición de la copa, la mayor parte de los árboles en esta área son co-dominantes o suprimidos. También encontramos que el 76% de los árboles tenían bejucos sea en el fuste o en la copa, pero solo el 7.5% de los árboles estuvieron severamente infestados. La distribución diamétrica para el bosque tuvo un patrón de “J invertida”, lo cual indica que tiene una buena regeneración; sin embargo, pocas son las especies que tienen este patrón. La tasa anual de mortalidad fue de 1.98%, mientras que la tasa anual de reclutamiento fue de 0.73%. La tasa anual de incremento de área basal fue de 1.78%, siendo A. colubrina la que tuvo mayor tasa de incremento. Finalmente, el incremento diamétrico anual varió entre 0.11 y 0.71 cm, siendo mayor en categorías de 50 a 60 cm de DAP. Los resultados apoyan a que el bosque estudiado es un bosque de transición entre el bosque semideciduo y el bosque chaqueño. Por su baja diversidad y problemas de regeneración, este bosque debe considerarse frágil para propósitos de manejo.
Palabras clave: Bosque seco semideciduo, estructura de bosques, riqueza florística, dinámica de bosques, Santa Cruz, Bolivia.
Abstract
This study analyses the structure, composition and dynamic of a semideciduous dry forest in the Botanical Garden of Santa Cruz. In 1995 and 2002, we measured the richness and abundance, diameter at breast height, crown position, and liana infestation of all trees. With this data we have evaluated the rate of natural regeneration, mortality recruitment rate, basal area, and diameter increment. On average, we have found 19.5 species and 526 individuals, with higher numbers in the first evaluation. Aspidosperma cylindrocarpon and Phyllostylon rhamnoides were the most abundant and frequent species, while Anadenanthera colubrina and Gallesia integrifolia had the larger basal area. In regards to crown position, most of the trees were found as co-dominants and suprime. In addition, 76% of trees were covered with lianas on the trunk or crown, but only 7.5% of trees were severely infested. Diametric distribution of all trees in the forest had a “J inverted” pattern, indicating that the forest has a good regeneration; however, few species showed this pattern. Annual mortality rate was 1.98%, while the annual recruitment rate was 0.73%. The annual basal area increment rate was 1.78%; A. colubrina presented the highest increment rate. Finally, annual diameter increment varied between 0.11 and 0.71 and was greater in individuals of 50 to 60 cm dbh. These results suggest that this forest is in transition to Chaco forest with low diversity and regeneration problems that should be considered as fragile for management purposes.
Key words: Dry forest, forest structure, floristic richness, forest dynamics, Santa Cruz, Bolivia.
Introducción
Los bosques secos tropicales son considerados como los más frágiles debido a la lenta capacidad de regeneración y a la persistente amenaza de deforestación por causas naturales o antropogénicas (Janzen 1988). Debido a las condiciones de sequía que padecen los bosques secos, el reclutamiento de plántulas y las tasas de crecimiento son afectadas y son menores a la de los bosques tropicales húmedos (Gerhardt 1994, McLaren & McDonald 2003). Asimismo, los bosques secos están sujetos a incendios forestales de gran magnitud, debido a la acumulación de materia orgánica seca sin descomponer, aunque existen evidencias que estos bosques son menos susceptibles a estos eventos por las adaptaciones que tienen sus especies (Pinard & Huffman 1997, Tito et al. 2003). Sin embargo, los incendios también son prácticas realizadas por agricultores para eliminar la cobertura forestal.
A pesar de estos factores negativos, los bosques secos de las tierras bajas en Bolivia son considerados entre los más diversos (Parker et al. 1993) y con grandes potenciales de uso por la gama de productos maderables (Mostacedo et al. 2001) y no maderables (Centurión & Kraljevic 1996, Vásquez & Coimbra 1996, Rumiz et al. 2001).
Para un manejo sustentable, es necesario tener información básica de la composición, estructura y la dinámica de estos bosques para ajustar las normas técnicas (MDSP 1998) que regulan esta ley. A partir de la emisión de las normas técnicas, muchas preguntas han surgido que se deben responder con bases científicas. Por ejemplo, determinar los ciclos de corta y los diámetros mínimos de corta son aspectos que deben ser respondidos al conocer la ecología y dinámica de un ecosistema o de las especies que la habitan.
En Bolivia, a pesar que hay varios estudios en composición y dinámica de especies (Nebel et al. 2001, Poorter et al. 2001) de los bosques tropicales húmedos, existen pocos estudios en bosques tropicales secos. Los estudios en bosques secos bolivianos están concentrados en composición y diversidad (Saldias 1991, Parker et al. 1993, Uslar 1997, Killeen et al. 1998) pero no en su dinámica.
Hace siete años, se instaló una parcela permanente de una hectárea en el bosque seco del Jardín Botánico de Santa Cruz, donde se realizó un estudio de composición y estructura del bosque. Esta parcela, con una diversidad menor a la de otros lugares en la región (Killeen et al. 1998), está ubicada en un lugar protegido y con muchas ventajas logísticas para hacer estudios de la dinámica de este tipo de bosque. Después de siete años de la primera evaluación, esta parcela fue utilizada para realizar un estudio sobre los cambios en el bosque y la dinámica de los árboles. Los objetivos de este estudio fueron: a) determinar los cambios en la composición y estructura del bosque, b) evaluar la regeneración natural y c) analizar el incremento en área basal, el crecimiento en diámetro, la tasa de mortalidad y reclutamiento.
Métodos
Area de estudio
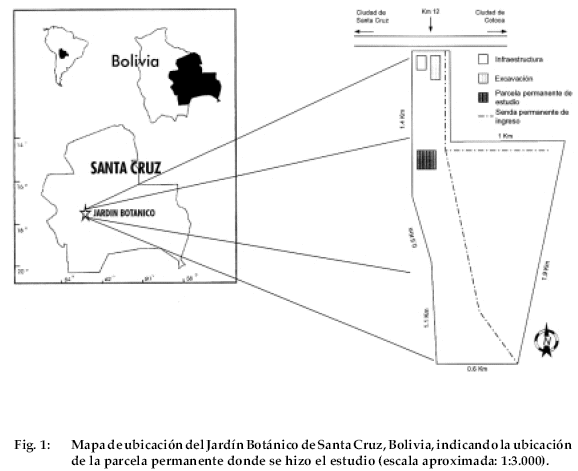
Este estudio fue realizado en el Jardín Botánico de Santa Cruz (Fig. 1), ubicado a 12 km de la ciudad de Santa Cruz (17o47’S, 63o04’W). Aun no existe una estación meteorológica en la misma zona, sin embargo las estaciones más cercanas reportan una temperatura media anual de 24.3 oC y una precipitación media anual de 1122 mm (CORDECRUZ 1995). La época seca es de mayo a octubre (Saldias 1991).
El área de estudio se encuentra en un bosque seco semideciduo (Navarro 1997). La altura promedio de este bosque es de 20 m, pero existen árboles emergentes que llegan a los 25 m. Las especies abundantes son Aspidosperma cylindrocarpon, Phyllostylon rhamnoides, Anadenanthera colubrina, Caesalpinia pluviosa, Achatocarpus nigricans, Gallesia integrifolia, Myrciaria cauliflora, Acacia paniculada, Bougainvillea modesta, Chrysophyllum gonocarpum y Triplaris americana (Saldias 1991, Uslar 1997).
Diseño experimental y colección de datos
En el año 1995 instalamos una parcela permanente de 1 ha, la cual fue dividida en 25 sub-parcelas de 20 x 20 m. En la parcela permanente, los árboles se identificaron a nivel de especie y se marcaron con placas de aluminio; se midió el DAP (diámetro a la altura del pecho) en individuos iguales o mayores a 10 cm.
En el año 2002, remedimos la parcela tomando en cuenta los mismos parámetros anotados en la instalación de esta parcela. En la segunda evaluación adicionalmente medimos otros parámetros como la infestación de bejucos y la posición de copa de cada planta. Para la infestación de bejucos se consideraron las siguientes categorías: 0, sin bejucos; 1, con bejucos solamente en el fuste; 2, con bejucos en la copa pero que cubren menos del 60% de la copa; y 3, con bejucos en la copa que cubren la copa más del 60% (Lowe & Walker 1977). Para la posición de la copa, se utilizó una clasificación modificada de Dawkins, con lo cual se caracterizó en 1 dominante; 2 codominante y 3, suprimido (Dawkins 1958). En esta segunda evaluación, también se adicionaron los nuevos individuos que ingresaron a la categoría igual o mayor a 10 cm. Al mismo tiempo, se tomaron en cuenta los individuos muertos.
Además, para evaluar la regeneración natural en las 25 sub-parcelas de 20 x 20m, se instalaron sub-parcelas de 20 x 10m, donde se contabilizaron a plantas de 3 a 10 cm de DAP. En estas sub-parcelas se identificaron todas las especies, además que también se midió su diámetro.
Análisis de datos
Composición, estructura y regeneración natural
Se hicieron cálculos de abundancia, frecuencia y área basal para las especies registradas en la parcela permanente y se compararon con los resultados del primer estudio. Para calcular la abundancia relativa por especie, se utilizó la siguiente fórmula Ar = (Ai / ∑ ) 100, donde Ar es la abundancia relativa, Ai es la abundancia absoluta de la especie i y ∑A es la abundancia total de las especies. Para obtener la frecuencia relativa, se utilizó la siguiente fórmula:Fr = (Fi / ∑ Fx)x100 , donde Fr es la frecuencia relativa para cada especie, Fi es la frecuencia absoluta de la especie i de cada especie en las sub-parcelas y ∑F es el número total de frecuencia absoluta para todas las especies. El área basal fue calculada mediante el DAP, donde AB = 0.7854*DAP2. Para determinar la dominancia de las especies, se utilizó la siguiente fórmula: Dr = (ABi/∑AB)x100, donde Dr es la dominancia relativa para cada especie, ABi es la sumatoria del área basal de la especie i y ∑AB es la sumatoria total del área basal de todas las especies. Al mismo tiempo, se hicieron tablas de frecuencia en cada categoría con los datos de infestación de bejucos y con la posición de copas de las diferentes especies. También se evaluó la composición y la abundancia de la regeneración por clases diamétricas.
Dinámica del bosque
Para el análisis de la dinámica del bosque, se calcularon las tasas de mortalidad y reclutamiento, y el aumento en área basal basándose en un modelo exponencial de incremento en tiempos continuos (Nebel et al. 2001). La tasa anual de mortalidad fue calculada de la siguiente manera: tm= (ln(No) – ln(Nm))/∆t. La tasa anual de reclutamiento: rr= (ln(No – N m + N r) – ln(No–– Nm))/∆t. La tasa anual de incremento del área basal: rg= (ln(No – N m + ∆N) – ln(No–– Nm))/∆t, donde No es el número de individuos o área basal al comienzo del período ∆t; Nm es el número de individuos muertos en una determinada área y Nr son los individuos que fueron reclutados en las diferentes categorías de área basal durante el período ∆t, respectivamente; ∆N es el incremento del área basal de individuos sobrevivientes del período ∆t (Nebel et al. 2001).
Resultados
Composición y estructura
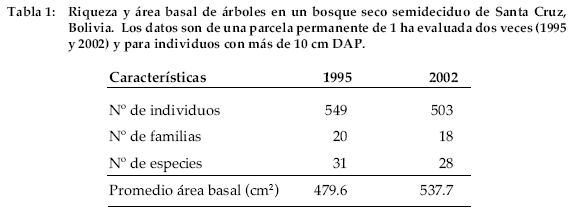
Durante los siete años, la parcela permanente tuvo una disminución en el número de especies y en el de individuos, y un aumento en el área basal de 479.6 - 537.7 cm2 (Tabla 1).
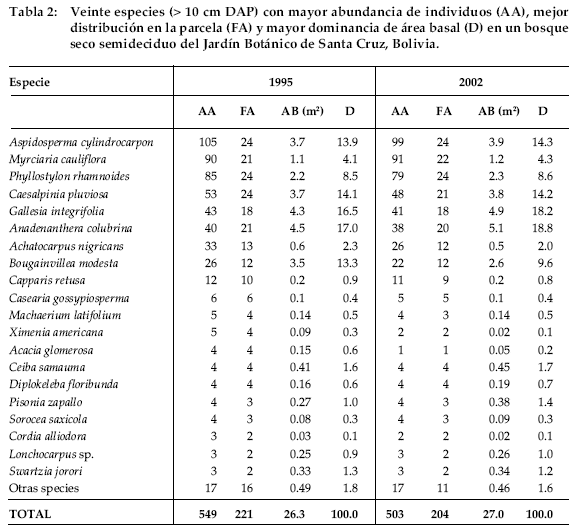
La familia más diversa y abundante fue Leguminosae, seguido por Apocynaceae y Myrtaceae. Las especies más abundantes y frecuentes, tanto en el año 1995 como en el año 2002 fueron: Aspidosperma cylindrocarpon, Myrciaria cauliflora, Phyllostylon rhamnoides y Caesalpinia pluviosa. Las especies dominantes, de acuerdo a su área basal, fueron Anandenanthera colubrina y Gallesia integrifolia (Tabla 2).
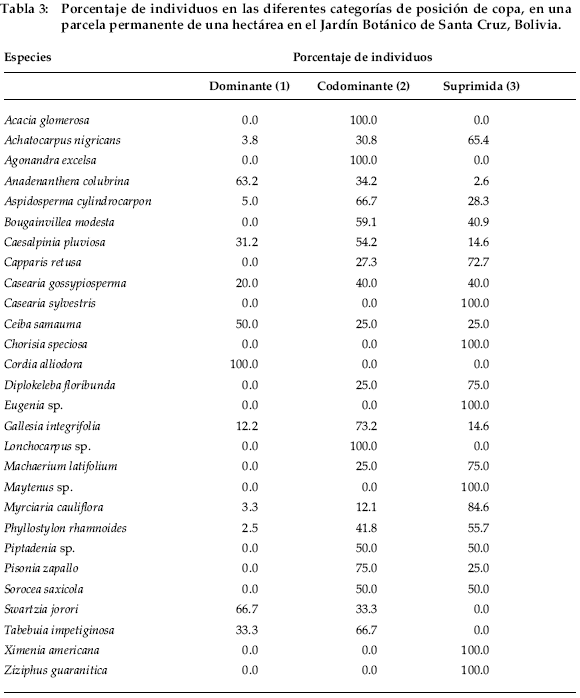
Respecto a la posición de la copa de los árboles, de los 503 individuos registrados en el año 2002 con diámetro igual o mayor a 10 cm DAP, el 12.5% de los árboles es dominante, 44.1% es codominante y el 43.3% es suprimido. Entre las especies con copa dominante tenemos a: Cordia alliodora,Swartzia jorori y Anadenanthera colubrina. Las especies co-dominantes son Acacia glomerosa, Agonandra excelsa,Lonchocarpussp.,Pisonia zapallo, Gallesia integrifolia, Aspidosperma cylindrocarpon y Tabebuia impetiginosa. Finalmente, entre las especies con copa suprimida tenemos a Casearia sylvestris, Chorisia speciosa, Eugenia sp., Maytenus sp., Ximena americana, Ziziphus guaranitica, Myrciaria cauliflora, Diplokeleba floribunda, Machaerium latifolium y Capparis retura (Tabla 3).
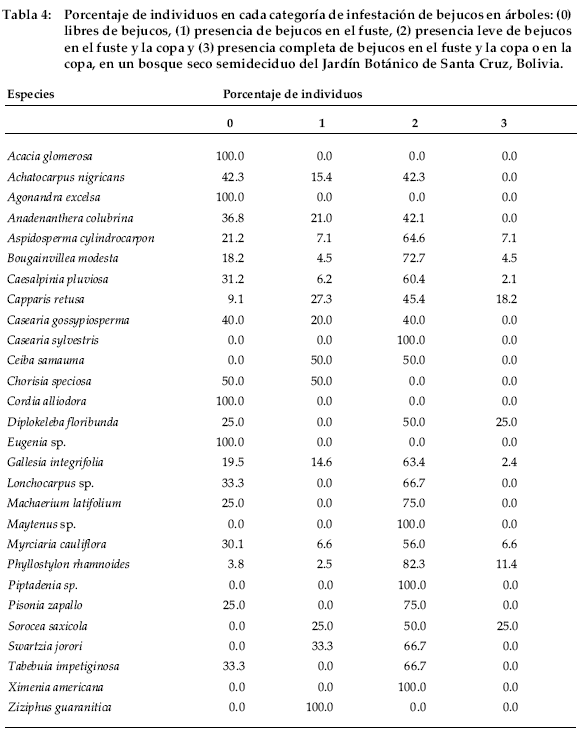
La mayoría de los árboles (76.5 %) registrados en el 2002 presenta lianas en el fuste y/o copa. De este porcentaje, el 12% estuvo infestado solamente en el fuste de los árboles, mientras que el 80% tenía bejucos tanto en el fuste y parcialmente en la copa. Solamente el 7.5% de los árboles tenía la copa totalmente cubierta por bejucos. Apenas cuatro especies no estuvieron infestadas de bejucos (Acacia glomerosa, Agonandra excelsa, Cordia alliodora y Eugenia sp.). Al contrario, Diplokeleba floribunda y Sorocea saxicola presentaron el mayor porcentaje de infestación de bejucos, siendo que el 25 % de los individuos de estas especies tenía la copa totalmente cubierta de bejucos (Tabla 4).
Regeneración Natural y Dinámica del Bosque
Distribución diamétrica
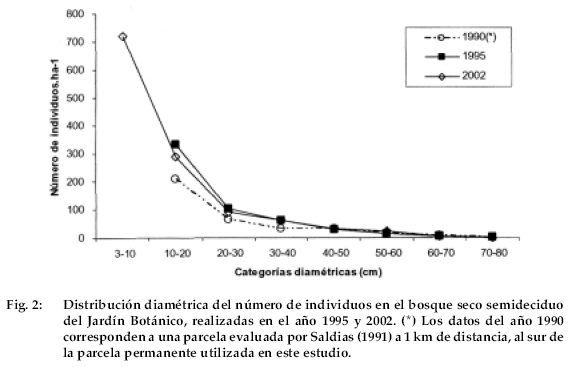
La distribución diamétrica del total de individuos tuvo un patrón de “J invertida”, lo que indica que se encontró mayor número de individuos en las categorías menores y menor en las categorías mayores (Fig. 2). Este patrón fue similar en diferentes años de evaluación.
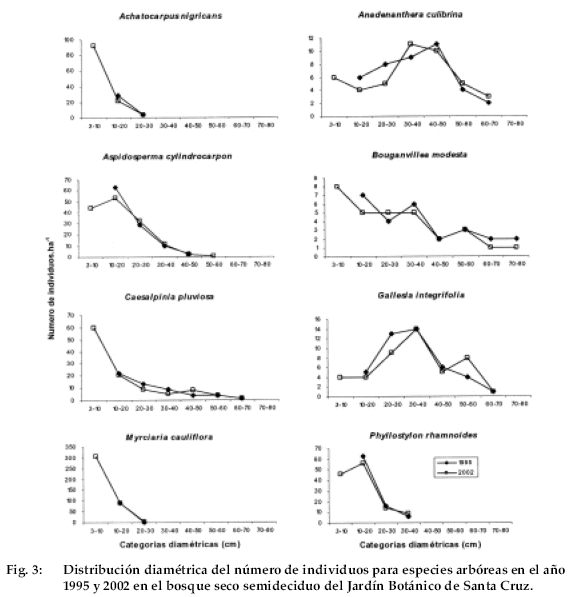
Para las especies con suficientes individuos, para analizar la distribución diamétrica, se pudo observar dos patrones (Fig. 3).
El primer patrón lo componen especies que tienen una distribución de “J invertida” donde hay mayor número de individuos en las categorías menores. Ejemplos de este patrón tenemos a Achatocarpus nigricans, Bouganvillea modesta, Caesalpinia pluviosa y Myrciaria cauliflora. Aunque Aspidosperma cylindrocarpon y Phyllostylon rhamnoides, presentan pocos individuos en la categoría de 3 a 10 cm de DAP, estas especies tienden a tener un gran número de individuos a partir de los 10 cm de DAP. El segundo patrón lo conforma las especies que tienen más individuos en categorías diamétricas intermedias. Ejemplos de este patrón se tiene a Anadenanthera colubrina y Gallesia integrifolia. Cabe resaltar que estos patrones fueron similares en ambas evaluaciones.
Mortalidad y reclutamiento
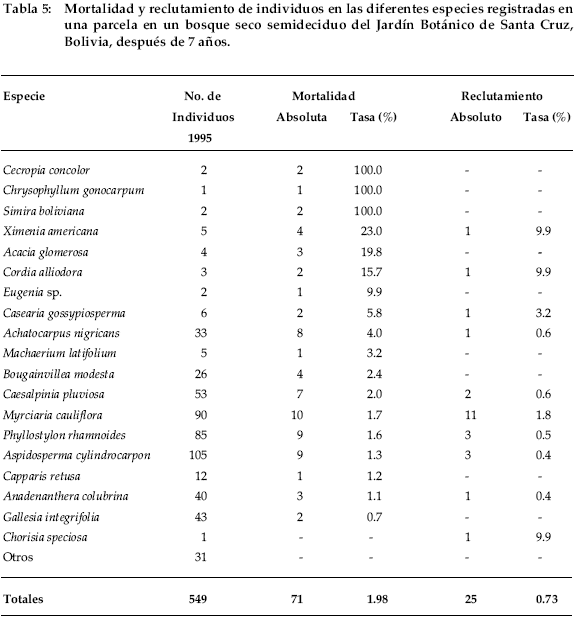
La tasa de mortalidad anual de árboles fue de 1.98%. El 58% del total de especies arbóreas tuvo diferentes porcentajes de mortalidad. Cecropia concolor, Chrysophyllum gonocarpum y Simira boliviana fueron las especies que tuvieron la mayor tasa anual de mortalidad (100%), seguidas de Ximenia americana (22.9%), Acacia glomerosa (19.8%) y Cordia alliodora (15.7%) (Tabla 5).
La tasa anual de reclutamiento fue de 0.73%. Solo 10 especies reclutaron entre 1-11 individuos. Chorisia speciosa, Cordia alliodora, Ximenia americana, Casearia gossypiosperma y Myrciaria cauliflora fueron las especies con mayor tasa de reclutamiento (Tabla 5).
Incremento de área basal
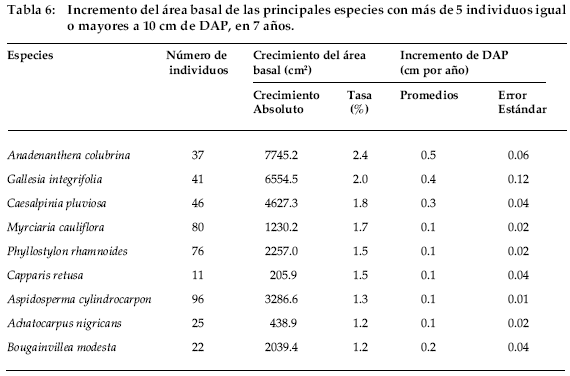
La tasa anual del incremento de área basal para 478 árboles fue de 1.78%, con un incremento de DAP promedio de 0.20 cm y un error estándar de 0.02 cm. Anadenanthera colubrina, Gallesia integrifolia, Caesalpinia pluviosa y Myrciaria cauliflora fueron las especies con tasas de incremento alto (Tabla 6).
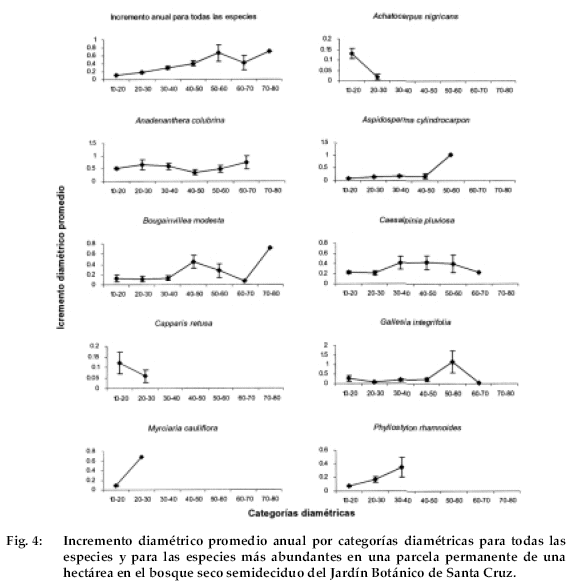
El incremento diamétrico promedio anual por clases diamétricas varió entre 0.11 y 0.71 cm, siendo mayor en la categoría de 50-60 cm de DAP, disminuyendo en la categoría de 6070 (Error estándar = 0.18), para luego volver a incrementar en la posterior categoría. Sin embargo, cada especie tuvo un el incremento diamétrico diferente. Por ejemplo, Anadenanthera colubrina tuvo un incremento diamétrico similar en la mayoría de las clases diamétricas, mientras que en Aspidosperma cylindrocarpon, Bougainvillea mosdesta, Cesalpinia pluviosa y Gallesia integrifolia presentaron incremento más notable a partir de los 40 cm de DAP (Fig. 4).
Discusión
Composición y estructura
Los resultados encontrados acerca de la composición con este estudio concuerdan en muchos aspectos a los encontrados por otros autores en otros bosques secos. Por ejemplo, varios autores (Lott et al. 1987, Gentry 1995, Gillespie et al. 2000, Kessler et al. 2000) hacen notar que las familias de árboles más dominantes de los bosques secos neotropicales son Leguminosae, Apocynaceae, Ulmaceae (arbustos y árboles), resultado similar encontrado con este estudio. Sin embargo, a medida que los bosques secos se van alejando de la línea del Ecuador, las familias predominantes son otras (Quigley & Platt 2003).
Respecto a la abundancia de especies en bosques secos, en este estudio se encontró que Fabaceae fue una de las familias más abundante en individuos arbóreos. Cinco familias tuvieron solo un individuo y una especie representante, de las cuales la familia Boraginaceae y Rhamnaceae presenta árboles mayores a 15 m de altura y las demás tres familias tienen árboles menores a 8 m de altura.
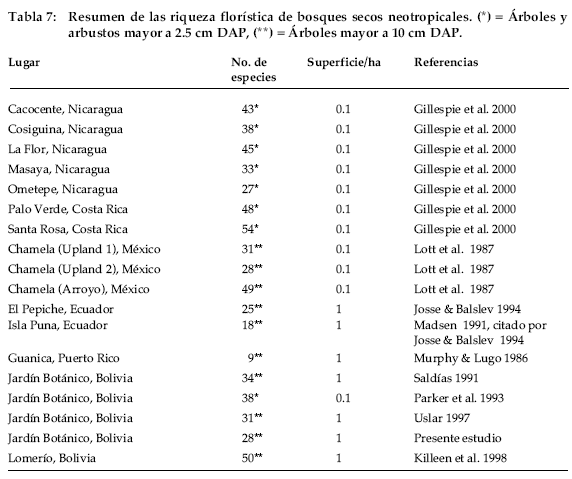
Los bosques tropicales secos de Centro y Sud América (Tabla 7) tienen riqueza de especies mayores a las del Jardín Botánico, excepto los que se encuentran en el Ecuador (Josse & Balslev 1994). Por ejemplo, el bosque seco de Chamela, México es uno de los que tiene alta riqueza florística de árboles (Quigley & Platt 2003). Inclusive, otros muestreos realizados en otros sitios del Jardín Botánico (Saldias 1991, Parker et al. 1993) muestran que la riqueza de especies es mayor a la de la parcela de estudio. Es posible que la baja diversidad se debe a que este bosque esta ubicado en una transición entre el bosque seco alto y el bosque chaqueño, mientras que las otras áreas muestreadas son áreas con bosque seco alto.
La disponibilidad de luz es uno de los factores importantes para el crecimiento y el establecimiento de muchas especies arbóreas.
Una forma de determinar esta disponibilidad es midiendo la posición de la copa respecto al sol (Dawkins 1958), lo cual da una idea de la estructura de cada especie en el bosque. La mayoría de las especies son codominantes y muy pocas especies llegan a ser dominantes en este bosque. Este mismo resultado fue encontrado en un bosque seco de la Chiquitanía (Killeen et al. 1998). Anadenanthera colubrina y Swartzia jorori son especies con la mayor parte de sus individuos dominantes del bosque. Al contrario, aunque todos los individuos de Cordia alliodora están como dominantes, en el campo se ha observado que esta especie se la encuentra en lugares abiertos. Finalmente, Phyllostylon rhamnoides tiene árboles grandes, pero la mayoría de sus individuos se encontraron como suprimidos, junto con otras especies de porte pequeño tales como Casearia sylvestris, Eugenia sp. y Ximenia americana.
Respecto a la infestación de bejucos, alrededor del 75% de árboles mayores a 10 cm de DAP estuvieron infestados por bejucos. Similar resultado (77%) fue encontrado en otro bosque seco en Las Trancas, Bolivia (Carse et al. 2000). Otros bosques sub-húmedos tuvieron también altos porcentajes de árboles infestados (Pérez-Salicrup 1998, Alvira 2002). El porcentaje de árboles infestados en el Jardín Botánico, además de otros bosques secos y sub-húmedos en Bolivia, es alto en comparación con lo encontrado en bosques tropicales húmedos. Por ejemplo, en Costa Rica y Sabah (Clark & Clark 1990, Campbell & Newbery 1993), se encontró entre 57 a 58% de árboles infestados por bejucos.
Los bejucos constituyen un problema serio, debido al efecto negativo que tienen en la tasa de crecimiento de los árboles y en la producción de semillas (Putz 1991). Aunque existe poca información del efecto negativo de los bejucos, es de suponer que especies o individuos con alto porcentaje de bejucos tienen mayores desventajas (Stevens 1987). En este sentido, algunas especies como Aspidosperma cylindrocarpon, Capparis retusa, Diplokeleba floribunda y Phyllostylon rhamnoides tienen mayores problemas. En otro bosque seco de Bolivia, tanto Aspidosperma como Phyllostylon, dos especies maderables, tuvieron alto grado de infestación de bejucos (Carse et al. 2000). Si se quiere utilizar y manejar este bosque, por ejemplo con fines de aprovechamiento de madera, las especies mencionadas anteriormente deberían ser las primeras en recibir una práctica silvicultural. Esta práctica puede ser el corte de bejucos con dos finalidades: para evitar la caída de otros árboles vecinos y para eliminar los bejucos de tal forma que favorezca el crecimiento de árboles jóvenes (Vidal et al. 1997, Pérez-Salicrup 1998).
Regeneración natural
La información proporcionada sobre regeneración natural en este artículo se basa en el número de individuos con diferentes categorías diamétricas, lo que muestra el estado de individuos jóvenes con relación a los adultos. En general, el bosque seco semideciduo del Jardín Botánico tiene buena regeneración, ya que hay más individuos jóvenes que adultos (Fig. 2). Este patrón parece mantenerse a través de los años y es posible que es un bosque más dinámico en comparación a otro similar en la misma área (Saldías 1991), ya que el número de individuos jóvenes es mucho mayor en la parcela permanente utilizada para este estudio, comparado con la parcela utilizada por Saldias (1991).
Por otro lado, aunque solo se analizaron pocas especies en detalle, esta información nos muestra que existen dos patrones de regeneración natural. El primer patrón es que varias especies en este bosque tienen una estructura poblacional que indica que estas tienen una buena regeneración (ejemplos: Achatocarpus nigricans y Caesalpinia pluviosa) (Figura 3). El segundo se refiere a que otras especies tienen una distribución atípica del número de individuos con relación a las categorías diamétricas. En este caso, el mayor número de individuos está en las categorías intermedias y existen pocos individuos en las categorías inferiores y superiores (ejemplos: Anadenanthera colubrina y Gallesia integrifolia) (Figura 3).
Los patrones de regeneración pueden o no mantenerse de igual manera en otros lugares y dependerá más del tipo de uso que estén teniendo estos bosques o especies. Por ejemplo, Caesalpinia pluviosa, Aspidosperma cylindrocarpon y Phyllostylon rhamnoides tienen similar estructura poblacional, tanto en el bosque estudiado como en el bosque seco de Las Trancas (Killeen et al. 1998). En cambio, Anadenanthera colubrina y Gallesia integrifolia tienen mayor número de individuos en categorías diamétricas menores en Las Trancas (Killeen et al. 1998), cosa que no ocurre en el Jardín Botánico.
Finalmente, es importante notar que la estructura poblacional de algunas especies fue similar a través de los años (Fig. 2). Probablemente esto se debe a que este lugar no ha sufrido grandes perturbaciones en los últimos siete años, los que puede cambiar rotundamente las curvas de la estructura poblacional (Fredericksen & Mostacedo 2000).
Mortalidad, reclutamiento e incremento diamétrico
La tasa anual de mortalidad arbórea en los bosques tropicales normalmente oscila entre 1 y 3% (Nebel et al. 2001, Asquith 2002). Los bosques tropicales húmedos, que son más dinámicos, generalmente presentan tasas de mortalidad más altas que los bosques secos (Phillips et al. 1998). Por ejemplo, Nebel et al. (2001) y Poorter et al. (2001) obtuvieron tasas de 2.1 a 3.2 % para bosques amazónicos. En cambio, la tasa anual de mortalidad en bosques secos puede oscilar entre 1.7 a 2.3% (Swaine et al. 1987, 1990). Considerando el rango obtenido en otros bosques, la tasa de mortalidad obtenida en el bosque seco del Jardín Botánico parece ser intermedia (1.98%). Las altas tasas de mortalidad fueron principalmente para especies pioneras y también para especies del dosel inferior. La muerte de especies pioneras fue debida seguramente por la competencia con otras especies tolerantes a la sombra, mientras que las especies del dosel inferior probablemente fueron afectadas por perturbaciones humanas.
La tasa de reclutamiento de 0.73% es baja, comparada con los datos que obtuvieron Swaine et al. (1990) en un bosque tropical seco (1.51%/año) y Nebel et al. (2001) en un bosque húmedo (2.99-4.57% por año). Es predecible que los bosques secos tengan bajas tasas de reclutamiento debido a que las de crecimiento también son bajas. Sin embargo, hay especies de árboles que han tenido tasas de reclutamiento muy altos (cercano a 10%) y están asociadas a especies demandantes de luz. Por ejemplo, Chorisia speciosa y Cordia alliodora se reclutan más rápido que otras especies.
Respecto al incremento diamétrico, comparado con otros estudios en bosques húmedos (3-4.5 mm/año) (Valerio 1997, Nebel et al. 2001, Peralta & Tejerina 2002), los bosques secos tienen incrementos bajos (1-2 mm/año) (Murphy & Lugo 1986). Al igual que otros bosques secos, en el bosque seco del Jardín Botánico el incremento diamétrico también es bajo. Por otro lado, el incremento diamétrico aumenta de acuerdo al tamaño de los árboles. Es decir, árboles pequeños tienen incrementos bajos y árboles grandes tienen incrementos altos. Sin embargo, la variación de tasas de incremento es mayor en árboles grandes en comparación a los pequeños (Fig. 4).
Conclusiones
- El bosque seco del Jardín Botánico tiene un promedio de 526 individuos/ha mayor a los 10 cm de DAP; 29 especies y 508.6 cm2 de área basal por árbol.
- De acuerdo a la posición de copas, la mayoría de los árboles mayor a los 10 cm de DAP está en la categoría de codominantes.
- Más del 75% de los árboles está infestado por bejucos, aunque un pequeño de estos porcentajes tiene copas totalmente infestadas. La infestación de bejucos es uno de los más altos en los bosques tropicales.
- La tasa anual de mortalidad de árboles fue de 1.98%, siendo Cecropia concolor, Chrysophyllum gonocarpum y Simira boliviana las que especies que obtuvieron un 100% de mortalidad. Por su parte, la tasa anual de reclutamiento fue de 0.78%.
- El incremento diamétrico de área basal promedio fue de 1.78% y el incremento de DAP fue de 0.20 cm. La variación fue alta analizando las especies por separado.
- Los resultados sugieren que el bosque seco semideciduo del Jardín Botánico se encuentra en transición con el bosque chaqueño con baja diversidad y tiene problemas de regeneración, por lo que debe considerarse frágil para propósitos de manejo.
Agradecimientos
Este estudio fue realizado gracias a la colaboración de la Dirección del Jardín Botánico de Santa Cruz que facilitó la instalación de la parcela permanente. La segunda evaluación de este sitio fue financiada por el Proyecto BOLFOR. Agradecemos al Dr. Gonzalo Navarro y a la Dra. Marielos Peña por sus comentarios y sugerencias tanto en la primera como en la segunda fase de este estudio.
Referencias
Alvira, D. 2002. Liana loads and post-logging liana densities after liana cutting in a lowland forest in Bolivia. Tesis M.Sc. Universidad de Florida, Gainesville, Florida, 41 p.
[ Links ]Asquith, N. M. 2002. La dinámica del bosque y la diversidad arbórea. pp. 377-406. En: Kattan, G. H. (ed.). Ecología y Conservación de Bosques Neotropicales. Libro Universitario Regional, Cartago.
[ Links ]Campbell, E. J. F. & D. M. Newbery. 1993. Ecological relationships between lianas and trees in lowland rain-forest in Sabah, East Malaysia. Journal of Tropical Ecology 9: 469-490.
Carse, L. E., T. S. Fredericksen & J. C. Licona. 2000. Liana-tree species associations in aBolivian dry forest. Tropical Ecology 41: 1-10.
Centurión, T. R. & I. J. Kraljevic (eds.) 1996. Las plantas útiles de Lomerío. Proyecto BOLFOR, Santa Cruz, Bolivia. 434 p.
[ Links ]Clark, D. B. & D. A. Clark. 1990. Distribution and effects on tree growth of lianas and woody hemiepiphytes in a Costa Rican tropical wet forest. Journal of Tropical Ecology 6: 321-331.
CORDECRUZ. 1995. Anuario meteorológico de Santa Cruz. Corporación Regional del Departamento de Santa Cruz, Santa Cruz, Bolivia.
[ Links ]Dawkins, H. C. 1958. The management of tropical high forest with special reference to Uganda. Imperial Forestry Institute Paper No 34. University of Oxford.
[ Links ]Fredericksen, T. S. & B. Mostacedo. 2000. Regeneration of timber species following selection logging in a Bolivian tropical dry forest. Forest Ecology and Management 131: 47-55.
Gentry, A. H. 1995. Diversity and floristic composition of neotropical dry forests. pp. 146-194. En: Bullock, S. H. (ed.). Seasonally Dry Tropical Forests. Cambridge University Press, Cambridge.
[ Links ]Gerhardt, K. 1994. Seedling development of four tree species in secondary tropical dry forest in Guanacaste, Costa Rica. Doctoral Dissertation. Uppsala University, Uppsala. 142 p.
[ Links ]Gillespie, T. W., A. Grijalva & C. N. Farris. 2000. Diversity, composition, and structure of tropical dry forests in Central America. Plant Ecology 147: 37-47.
Janzen, D. H. 1988. Management of habitat fragments in a tropical dry forest: growth. Annals of Missouri Botanical Garden 75: 105-116.
[ Links ]Josse, C. & H. Balslev. 1994. The composition and structure of a dry semideciduous forest in Western Ecuador. Nordic Journal of Botany 14: 425-434.
Kessler, M., K. Bach, N. Helme, S. G. Beck & J. Gonzales. 2000. Floristic diversity of Andean dry forests in Bolivia: an overview. pp. 219-233. En: Breckle, S. W., B. Schweizer & U. Arndt, (eds.). Results of Worldwide Ecological Studies. Proceedings of the 1st Symposium of the A. F. W. Schimper-Foundation. Verlag Gunter Heimbach, Stuttgart.
[ Links ]Killeen, T. J., A. Jardim, F. Mamani & N. Rojas. 1998. Diversity, composition and structure of a tropical semideciduous forest in the Chiquitania region of Santa Cruz, Bolivia. Journal of Tropical Ecology 14: 803-827.
Lott, E. J., S. H. Bullock & J. A. Solis-Magallanes. 1987. Floristic diversity and structure of a tropical deciduous forest of Coastal Jalisco. Biotropica 19: 228-235.
Lowe, C. & P. Walker. 1977. Classification of canopy, stem, crown status and climber infestation in natural tropical forest in Nigeria. Journal of Applied Ecology 14: 897-903.
McLaren, K. P. & M. A. McDonald. 2003. The effects of moisture and shade on seed germination and seedling survival in a tropical dry forest in Jamaica. Forest Ecology and Management 183: 61-75.
MDSP (Ministerio de Desarrollo Sostenible y Planificación). 1998. Normas técnicas para la elaboración de instrumentos de manejo forestal (inventarios, planes de manejo, planes operativos, mapas) en propiedades privadas o concesiones con superficies mayores a 200 hectáreas. Resolución Ministerial No 248/98, La Paz. 66 p.
[ Links ]Mostacedo, B., J. Justiniano, M. Toledo & T. S. Fredericksen. 2001. Guía dendrológica de especies forestales de Bolivia. Proyecto BOLFOR, Santa Cruz. 215 p.
[ Links ]Murphy, P. G. & A. E. Lugo. 1986. Ecology of tropical dry forest. Annual Review of Ecology and Systematics 17: 67-88.
Navarro, G. 1997. Contribución a la clasificación ecológica y florísitica de los bosques de Bolivia. Revista Boliviana de Ecología y Conservación 2: 3-37.
[ Links ]Nebel, G., L. P. Kvist, J. K. Vanclay & H. Vidaurre. 2001. Forest dynamics in flood plain forests in the Peruvian Amazon: effects of disturbance and implications for management. Forest Ecology and Management 150: 79-92.
Parker, T. A., A. H. Gentry, R. B. Foster, L. H. Emmons & J. V. Remsen. 1993. The lowland dry forests of Santa Cruz, Bolivia: A global conservation priority. Conservation International, Rapid Assessment Program Working Paper No 5, Washington, D. C.
[ Links ]Peralta, R. & E. Tejerina. 2002. Proyección preliminar del crecimiento y evaluación de la tasa de aprovechamiento de las especies maderables comerciales en la Concesión de IMAPA S. A. Documento Técnico # 5, Proyecto de Manejo Forestal Sostenible de Pando, Cobija, Pando. 26 p.
[ Links ]Pérez-Salicrup, D. R. 1998. Effects of liana cutting on trees and tree seedlings in a tropical forest in Bolivia. Ph. D. Thesis. University of Missouri, St. Louis. 130 p.
[ Links ]Phillips, L., V. P. Nuñez & M. E. Timana. 1998. Tree mortality and collecting botanical vouchers in tropical forests. Biotropica 30: 298-305.
Pinard, M. A. & J. Huffman. 1997. Fire resistance and bark properties of trees in a seasonally dry forest in eastern Bolivia. Journal of Tropical Ecology 13: 727-740.
Poorter, L., R. G. A. Boot, Y. Hayashida-Oliver, J. Leigue-Gomez, M. Peña-Claros & P. A. Zuidema. 2001. Estructura y dinámica de un bosque húmedo tropical en el norte de la Amazonía boliviana. Informe Técnico No.2, Programa Manejo de Bosques de la Amazonía Boliviana, Riberalta, Beni.
[ Links ]Putz, F. 1991. Silvicultural effects of lianas. pp. 493-501. En: Mooney, H. A. (ed.). Biology of Vines. Cambridge University Press, Cambridge.
[ Links ]Quigley, M. F. & W. J. Platt. 2003. Composition and structure of seasonally deciduous forests in the Americas. Ecological Monographs 73: 87-106.
Rumiz, D., D. Guinart, L. R. Solar & F. J. C. Herrera. 2001. Logging and hunting in community forests and corporate concessions. pp. 333-357. En: Fimbel, R., A. Grajal & J. G. Robinson (eds.). The Cutting Edge: Conserving Wildlife in Logged Tropical Forests. Columbia University Press, New York.
[ Links ]Saldias, M. 1991. Inventario en el bosque alto del Jardín Botánico de Santa Cruz, Bolivia. EcologÌa en Bolivia 17: 31-41.
[ Links ]Stevens, G. C. 1987. Lianas as structural parasites -theBursera-Simaruba example. Ecology 68: 77-81.
[ Links ]Swaine, M. D., J. B. Hall & I. J. Alexander. 1987. Tree population-dynamics at Kade, Ghana (1968-1982). Journal of Tropical Ecology 3: 331-345.
Swaine, M. D., D. Lieberman & J. B. Hall. 1990. Structure and dynamics of a tropical dry forest in Ghana. Vegetatio 88: 31-51.
Tito, N., V. Molina & F. Contreras. 2003. Sistema de alerta temprana de incendios forestales (SATIF): Evaluación de Incendios Forestales Año 2002. Superintendencia Forestal y Proyecto BOLFOR, Santa Cruz, Bolivia. 34p.
[ Links ]Uslar, Y. V. 1997. Estructura, composición y sucesión del bosque sub-húmedo semideciduo de llanura en el Jardín Botánico de Santa Cruz de la Sierra, Bolivia. Tesis de Licenciatura. Universidad Autónoma Gabriel René Moreno, Santa Cruz. 60 p.
[ Links ]Valerio, J. 1997. Crecimiento y Rendimiento. Documento Técnico # 51, Proyecto BOLFOR, Santa Cruz.
[ Links ]Vásquez, R. & G. Coimbra. 1996. Frutas Comestibles de Santa Cruz. Gobierno Municipal de Santa Cruz de la Sierra, Santa Cruz. 267 p.
[ Links ]Vidal, E., J. Johns, J. J. Gerwing, P. Barreto & C. Uhl. 1997. Vine management for reduced-impact logging in eastern Amazonia. Forest Ecology and Management 98: 105-114.
Artículo recibido en: Junio de 2003.
Manejado por: Stephan Halloy
Aceptado en: Abril de 2004.












 uBio
uBio