Considerar el comportamiento de forrajeo de visitantes florales es importante para muchos estudios de polinización ya que puede influenciar directamente sobre muchos aspectos de la interfase entre plantas y sus polinizadores como, por ejemplo, el flujo genético (Kearns & Inouye 1991). Al mismo tiempo, la dependencia que existe entre el comportamiento de forrajeo de los polinizadores y las condiciones ambientales (p.e. temperatura, radiación solar, humedad) ha sido notada por muchos autores (Baker 1961cit. enMartínez del Río & Búrquez 1986,Faegri & Van Der Pijl 1971,Cruden 1973,Martínez del Río & Búrquez 1986,Herrera 1995a). Se sabe que la temperatura afecta las tasas de visita de los polinizadores (reprimiendo o incrementando su actividad) (Lundberg 1980cit. enHerrera 1995b,Kearns & Inouye 1991) y que puede influenciar su comportamiento en las flores (Corbet 1978). Un grupo importante de polinizadores en las Américas (Owen 1980), en los que se ha observado una relación entre la temperatura y el comportamiento de forrajeo (Taylor & Kamp 1985) son los picaflores. Estas aves poseen un metabolismo muy alto, por lo que necesitan alimentarse cada 10 ó 15 minutos, 50 ó 60 veces al día y pueden consumir hasta 2/3 de su masa corporal en azúcar diariamente (Berger 1989,Stewart 1997).
El picaflor más grande del mundo, Patagona gigas, es un ave territorialista que habita en zonas áridas y en vegetación arbustiva estepada (Fjeldså y Krabbe 1990,Proctor et al. 1996). En el valle de La Paz P. gigas visita, entre otras, flores de Malva sp. (Malvaceae), Tecoma sp. (Bignoniaceae), Trichocereus sp. (Cactaceae), Opuntia sp. (Cactaceae) y Nicotiana glauca (Solanaceae) (obs. pers.). Sin embargo, exceptuando a N. glauca que florece todo el año, todas estas especies presentan sólo un pico de floración al año, por lo que N. glauca se constituye en un recurso de néctar importante para P. gigas, especialmente durante la época seca, cuando escasean otros recursos florales. En la presente nota, describimos la actividad alimenticia de P. gigas en arbustos de N. glauca y observamos si ésta se encuentra asociada con la temperatura del ambiente.
Realizamos el estudio en dos laderas del valle de La Paz, ubicadas al SE de la ciudad. La zona está sujeta a una marcada estacionalidad en lo referente a precipitación (Arellano 1990). La temperatura media es elevada, con amplitudes térmicas importantes. La temperatura diurna puede alcanzar los 30 °C al medio día y descender , en la noche, a valores menores o cercanos a 0 °C (Loayza, datos no publicados). Ambas laderas están caracterizadas por presentar vegetación xerofítica (Urcullo 1997) en las que predominan arbustos de N. glauca, sin embargo también se observó, aunque en menor número, individuos de Tecoma arequipensis(Bignoniaceae), Wissadula annina (Malvaceae), Prosopis laevigata (Leguminosae), Agalinis sp. (Scrophulariaceae), Pluchea fastigiata (Compositae), Solanum sp. (Solanaceae), Senecio clivicolor (Compositae), Schinus molle (Anarcardiaceae), Atriplex semibaccata (Chenopodiaceae) y Chenopodium sp. (Chenopodiaceae) (obs. pers.).
En septiembre de 1997 cuantificamos las visitas de Patagona gigas a las flores de N. glauca durante 15 días a partir de las 8:00 a.m. hasta las 6:00 p.m. Se trabajó en este rango de horas ya que observamos que la actividad de individuos comenzaba alrededor de las 7:30 a.m. y cesaba alrededor de las 6:30 p.m. Consideramos como visita únicamente cuando el picaflor libaba de las flores y no cuando estaba involucrado en otras actividades dentro del área (p.e percha, vigilancia y captura de insectos en el aire). Cuantificamos el número de visitas de los tres individuos presentes en el área de estudio, los cuales eran distinguibles uno del otro debido a que, por su comportamiento territorialista, cada uno siempre forrajeaba en distintos manchones de plantas de N. glauca. Para diferenciar visitas sucesivas de un mismo individuo trabajamos bajo la suposición de que una visita se diferenciaría de otra, si el picaflor perchaba durante al menos tres minutos entre cada visita. Durante cuatro días en septiembre de 1998, desde las 8:00 a.m. hasta las 6:00 p.m., contamos el número de flores libadas por visita cronometrando su duración. Así obtuvimos una tasa de forrajeo expresada como: número de flores libadas/visita/minuto. De igual manera, consideramos todos los individuos en el área (n = 2) y una visita, del mismo individuo, se diferenciaba de otra, cuando el picaflor perchaba durante al menos tres minutos entre visitas sucesivas. En ambas oportunidades, para evaluar si el número de visitas observadas y la tasa de forrajeo estaban asociadas con la temperatura, tomamos datos de la temperatura del ambiente cada hora a partir de las 8:00 a.m. hasta las 6:00 p.m. Posteriormente calculamos el grado de asociación entre el número de visitas y la tasa de forrajeo con la temperatura del ambiente mediante correlaciones de Spearman.
Patagona gigas mostró dos picos de actividad alimenticia diarios (Fig. 1). Uno mayor, temprano en la mañana y otro menor alrededor de las cinco de la tarde. Estos picos pueden deberse en parte a los cambios de temperatura que se dan durante el día, ya que observamos una asociación entre la temperatura del ambiente y el número de visitas a N. glauca (rs= -0,61, P<0,009, n = 50). Cómo podría explicarse esta asociación? A medida que aumenta la temperatura del ambiente, el gasto energético para mantener la temperatura corporal se incrementa, hasta que llega un punto en que la oferta energética del recurso (el néctar) no compensa el gasto energético del animal (Berger 1989). Durante este período de tiempo, que en el caso del estudio oscilaba entre las 12:00 y las 14:30, los individuos de P. gigas podrían estar mostrando homeotermia conductual, ya que observamos que su actividad disminuía y que perchaban en lugares frescos (Loayza 1998, obs. pers.). Sin embargo, es preciso aclarar que este argumento es válido sólo para el rango de temperatura considerado en el estudio (entre 14 y 32 °C). Como la relación entre el número de visitas de picaflores y la temperatura no es lineal, existe un rango de temperatura a partir del cual la correlación se torna positiva, es decir que a menor temperatura habrá menor número de individuos activos. Si la temperatura del ambiente es muy baja, el gasto energético para mantener la temperatura corporal es, al igual que si la temperatura del ambiente es muy alta, mayor, por lo que los picaflores entran en torpor para conservar su energía (Berger 1989,Fjeldså y Krabbe 1990,Proctor et al. 1996).
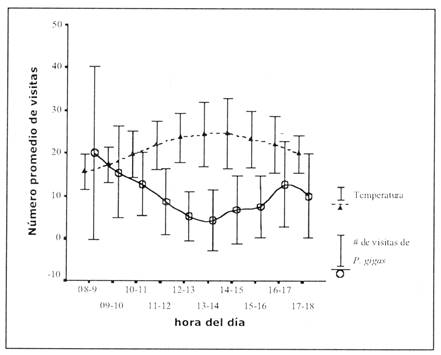
Fig. 1: Temperatura ambiente promedio y número promedio de visitas de P. gigas a flores de N. glauca a lo largo del día. Los datos representan promedios de 15 días de observaciones. Las barras verticales representan ± ds.
La tasa de forrajeo promedio por individuo de P. gigas es 44 flores libadas/visita/minuto (x= 43,96, ds= ± 14,87, n = 26), y no parece variar junto con los cambios diurnos en la temperatura del ambiente, ya que no observamos ninguna asociación (rs= -0,044, P=0,829, n = 26). Al igual que las visitas, observamos dos picos diarios (Fig. 2) y es posible que estos picos estén relacionados con la disponibilidad de néctar en las flores. Temprano en la mañana, cuando el número de picaflores forrajeando las flores de N. glauca en el área era elevado (Fig. 1), también lo era la cantidad de néctar disponible en las flores. A medida que transcurre el día, las flores son "vaciadas" por los visitantes hasta que, a media tarde éstas vuelven a producir una pequeña cantidad de néctar (Loayza 1998). Entonces, podríamos pensar que para obtener la misma cantidad de energía, un picaflor -por visita- necesitaría forrajear más flores cuando el recurso por flor es bajo (antes del mediodía, cuando se da el primer pico, Fig. 2) y menos cuando el recurso por flor es alto (temprano en la mañana). El segundo pico de forrajeo se da entre las cuatro y cinco de la tarde. Ocurre, posiblemente, como medida de seguridad, ya que los picaflores tienden a elevar sus reservas energéticas al final de la tarde antes de entrar en torpor (Stewart 1997), consintiéndose con un festín antes del anochecer. Observamos también que el pico de la tarde es menor al de la mañana, sugiriendo varias posibilidades. 1) Es posible que los individuos de P. gigas tengan, de tarde, menor demanda energética que en la mañana. Se sabe que, a pesar de que los picaflores consumen de día la mitad de su masa corporal en azúcar, de noche se acercan al punto de inanición mientras duermen (Stewart 1997), por lo que en la mañana necesitan compensar toda la energía perdida. Por lo tanto en la mañana los picaflores estarían consumiendo más néctar que en la tarde, vaciando rápidamente las flores e incrementando la tasa de forrajeo a su pico máximo (71 flores libadas/visita/minuto). 2) Debido a la pequeña producción de néctar que se da temprano en la tarde, P. gigas podría necesitar menos flores para cumplir con su demanda energética. Al haber una nueva producción de néctar en las flores (Loayza 1998), aunque ésta sea pequeña, el recurso por flor lógicamente será mayor y los individuos forrajeando podrán visitar un menor número de flores para obtener la misma cantidad de energía. 3) Durante la tarde pueden estar disponibles otros recursos como, insectos y otras flores. Sin embargo, en los alrededores del área de estudio, la única planta en flor disponible para picaflores, además de N. glauca, era Tecoma arequipensis. Ésta, además de presentarse en bajo número, presenta flores con corola larga, curvada, con poca producción de néctar concentrado (obs. pers.) por lo que no creemos que fuera una fuente importante de néctar para P. gigas. En lo referente a insectos, no observamos mayor actividad de "captura" en la mañana que en la tarde, pero, debido a que el número de visitas si era menor en la tarde, es posible que los individuos de P. gigas buscaran en otro lugar este recurso.
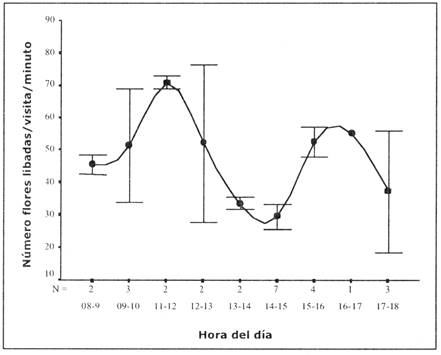
Fig. 2: Número de flores libadas por individuo de P. gigas por visita por minuto. Los datos representan promedios de observaciones de cuatro días. Las barras verticales representan ± ds. N representa el número de visitas observadas.
Finalmente, estas observaciones nos dan una percepción sobre la naturaleza del comportamiento alimenticio de P. gigas en arbustos de N. glauca, nosotros observamos la relación con la temperatura pero pueden existir otros factores que tengan un rol más importante sobre este aspecto. Estudios del comportamiento de forrajeo de picaflores son de fundamental importancia, ya que nos proveen información sobre la historia natural de las interacciones planta-polinizador. Esta información, casi inexistente en valles mesotérmicos, adquiere mayor relevancia en este tipo de hábitat el cual, debido al alto grado de intervención humana al que está sometido, está desapareciendo.












 uBio
uBio 

