Introducción
Los bosques tropicales estacionalmente deciduos se diferencian de bosques siempreverdes por contener 40-100 % de especies leñosas deciduas, las cuales usualmente pierden su follaje más o menos simultáneamente durante la época seca (Medina 1993,Bullock et al. 1995). Su ocurrencia está determinada por ciclos climáticos anuales con dos a ocho meses de sequedad marcada (Vareschi 1980,Bullock et al. 1995), usualmente con una precipitación media anual de menos de 1600 mm (Gentry 1995). Tales bosques secos tienen una amplia distribución en el Neotrópico, desde el occidente mexicano hasta Costa Rica, en varias islas del Caribe, el norte de Colombia y Venezuela, el sudoeste ecuatoriano y noroeste del Perú así como desde el noreste brasileño (Caatinga) hasta el sudoeste de Paraguay, el norte de Argentina y el sur Boliviano (Chaco y Chaco serrano, Bosque Chiquitano) (Hueck 1966,Bullock et al. 1995,Ribera et al. 1996). Además, existen una serie de "islas" de bosque deciduo esparcidas a lo largo de los Andes en valles secos debido al fenómeno de sombra de lluvia (Troll 1952,Prado & Gibbs 1993).
Aunque mundialmente los bosques deciduos cubren un área más grande que los bosques tropicales siempreverdes, hasta el presente existen relativamente pocos estudios sobre su distribución, fauna, flora y ecología, resaltando los trabajos de Janzen (1988) en Costa Rica y Bullock et al. (1995) quienes por primera vez dedicaron un volúmen completo a los bosques deciduos. En Bolivia, Ribera et al. (1996) reconocen seis tipos de bosques deciduos y semideciduos: 1) el Bosque Subhúmedo Submontano de la formación tucumano-boliviana, 2) el Bosque Deciduo del Chaco Serrano en la vertiene subandina del sur de Bolivia, 3) los Matorrales Microfoliados y Restos de Bosque Seco Caducifolio en los valles secos interandinos, 4) el Bosque Deciduo Seco del Chaco, 5) el Bosque Subhúmedo de las Serranías Chiquitanas, y 6) el Bosque Semideciduo del Escudo Brasileño.
Recientemente Navarro (1997) presentó una clasificación ecológica y florística de los bosques de Bolivia, la cual contiene 93 series de vegetación, incluyendo 34 tipos de bosque pluvioestacionales y ocho tipos de vegetación azonales asociados a bosques caducifolios. Esta proporción bastante alta de tipos de vegetación deciduos y semideciduos refleja la importancia de estos bosques en Bolivia.
Estudios florísticos puntuales de bosques caducifolios bolivianos existen en el valle de Capinota, Cochabamba (tipo 3 de Ribera et al. 1996;Pedrotti et al. 1988), en el Jardín Botánico de Santa Cruz (mezcla de tipos 2, 4 y 5 de Ribera et al. 1996;Nee & Coimbra 1991,Saldias 1991), el valle de Tucavaca, Santa Cruz (tipos 5 y 6 de Ribera et al. 1996;Parker et al. 1993), los valles del departamento de Cochabamba (tipo 3 de Ribera et al. 1996; sup>Navarro et al. 1996) y la cuenca del Río Camacho, Tarija (Beck et al. 1992). Además hay estudios sobre la vegetación del norte Argentino (p.ej.,Hauman et al. 1947,Czajka & Vervoorst 1956,Cabrera 1971) y de los valles peruanos (Weberbauer 1945).
Sin embargo, hasta el presente el conocimiento de la flora y vegetación de los bosques deciduos bolivianos, en particular en la zona andina, es insuficiente, sobre todo si se considera que estas zonas representan importantes centros de asentamientos humanos tanto precolombinos como actuales (Morales 1995). Por lo tanto, el estudio de ecosistemas de bosques deciduos representa una prioridad para estudios científicos (Moraes & Beck 1992,Navarro et al. 1996,Ribera et al. 1996).
El presente estudio pretende aportar al conocimiento fitogeográfico de los bosques secos de los valles y la vertiente andina en Bolivia (tipos 1-3 de Ribera et al. 1996), presentando una caracterización preliminar de los tipos de vegetación en base a un análisis fitosociológico de grupos indicadores botánicos. Esta tipificación es comparada con las clasificaciones de Ribera et al. (1996)yNavarro (1997). Cabe resaltar que la metodología del presente trabajo difiere considerablemente del estudio de Navarro (1997), el cual se basa en un análisis ecoclimatológico y de las especies de plantas dominantes. Ya que aún estamos lejos de obtener una clasificación coherente de los tipos de bosques caducifolios en los Andes bolivianos (véase discusión) hemos optado por no nombrar los tipos de bosques diferenciados en nuestro estudio. De este modo esperamos evitar una acumulación innecesaria de nombres preliminares, muchos de los cuáles tendrían que ser redefinidos o desechados a medida que se obtengan conocimientos más profundos.
Área de estudio
Se estudiaron 13 localidades de bosque deciduo andino y una adicional en tierras bajas (Santa Cruz) (Fig. 1), representando la mayoría de los areales de dicho tipo de bosque en los Andes norte y centrales de Bolivia.
1) Consata (C, ver Fig. 1), depto. La Paz, provs. Saavedra y Muñecas (15°23'S, 68°31'W; 1000-1400 m; 30/5-3/6/1995): un valle andino muy estrecho cuya topografía y la influencia de los vientos secos (Troll 1952) generan un cambio brusco en la vegetación de matorrales espinosos a bosques húmedos montanos en tan sólo unos 10 km dentro del valle, limitando los bosques deciduos al área intermedia de las laderas. Se levantaron 13 relevamientos en bosques zonales poco disturbados.
2) Las Mercedes (L), depto. La Paz, prov. Sud Yungas (16°13-17'S, 67°13-23/W; 800-1300 m; 2-7/10/1995): en valle del Río Boopi entre Villa Barrientos y La Asunta se encontraron bosques bien preservados en los cuales se levantaron 16 relevamientos.
3) Miguillas (M), depto. La Paz, prov. Inquisivi (16°33'S, 67°22'W; 1100-1600 m; 21-25/9/1995): ésta y la siguiente localidad se encuentran en el valle del Río La Paz. Ambas contienen bosques deciduos fuertemente degradados. Se establecieron 11 relevamientos en bosques zonales.
4) Huara (H), depto. La Paz, prov. Sud Yungas (16°34-37'S, 67°25-28'W; 1200-1800 m; 27/9-2/10/1995): 13 relevamientos de bosques zonales.
5) Inquisivi (I), depto. La Paz, prov. Inquisivi (16°54'S, 67°09'W, 2050-2500 m; 14-21/9/1995): ésta localidad incluye la parte más alta de los bosques secos del Río Cotacajes, que se extienden desde 1400 m hasta los 2500 m. Cerca a Inquisivi, estos bosques están fuertemente perturbados. Se levantaron 13 relevamientos en bosques zonales.
6) Río Caine (Z), depto. Potosí, prov. Charcas y depto. Cochabamba, prov. Arze (17°53'-18°06'S, 65°46-55'W; 2050-2400 m; 11-14/6/1995): se estudiaron 14 relevamientos a lo largo de la carretera Anzaldo - Torotoro y en quebradas protegidas a cierta distancia del camino. En general, los bosques en esta región están bastante degradados.
7) San Juan del Potrero (J), depto. Santa Cruz, prov. Florida (17°59'S, 64°15'W; 1500-1950 m; 3-8/9/1995): bosques deciduos bastante degradados aprox. 5 km al SE de San Juan del Potrero. Se hicieron 16 relevamientos de bosques zonales.
8) Novillero (N), depto. Cochabamba, prov. Campero (18°13-18'S, 65°15-18'W; 2400-2800 m; 16-20/6/1995): a lo largo del camino de Novillero a Santiago, se obtuvo acceso a una variedad de bosques deciduos hasta semi-deciduos, todos ellos fuertemente perturbados. Se establecieron 15 relevamientos.
9) Masicurí (U), depto. Santa Cruz, prov. Vallegrande (18°49'-19°04'S, 63°41-48'W; 500-800 m; 9-14/7/1995): bosque alto dominado por Anadenanthera colubrina (= A. macrocarpa) en el fondo del valle de Masicurí, desde la confluencia con el Río Grande hasta su transición hacia bosques húmedos de mayor elevación. Se levantaron 13 relevamientos.
10) Río Grande (G), depto. Chuquisaca, prov. B. Boeto (18°50-19°02'S, 64°12-18'W; 900-1700 m; 5-7/7/1995): a lo largo de la carretera Vallegrande - Padilla se estudió la transición altitudinal desde bosques espinosos en el fondo del valle del Río Grande hasta la transición hacia bosques siempreverdes arriba de 1800 m. Se hicieron ocho relevamientos.
11) Oron'kota (O), depto. Chuquisaca, prov. Yamaparaez y depto. Potosí, prov. Linares (19°23-34'S, 64°48-51'W; 2050-2450 m; 22-24/6/1995): a lo largo del camino Icla - Oron'kota se estudiaron algunos relictos de bosques deciduos en la cuenca del Río Pilcomayo. Cinco relevamientos en bosques zonales.
12) Río Acero (A), depto. Chuquisaca, prov. Siles (19°32-47'S, 64°02-10'W; 1000-1500 m; 27/6-4/7/1995): esta localidad corresponde a los amplios bosques semideciduos del “Chaco Serrano”, en este caso como parte de la Cordillera de los Milagros. Se levantaron 23 relevamientos en bosques zonales.
13) Tarvita (T), depto. Chuquisaca, provs. Azurduy y Tomina (19°39'S, 64°28'W; 2100-2500 m; 25-26/6/1995): en la vertiente oriental de la Cordillera de Mandinga, se estudiaron algunos relictos de bosque semideciduos en su transición hacia bosques siempre verdes boliviano-tucumanos. Seis relevamientos.
14) Santa Cruz (S), depto. Santa Cruz, prov. Ibañez (17°43'S, 63°03'W; 400 m; 26/8-1/9/1995): en el Jardín Botánico de Santa Cruz se levantaron 14 relevamientos en bosques zonales.
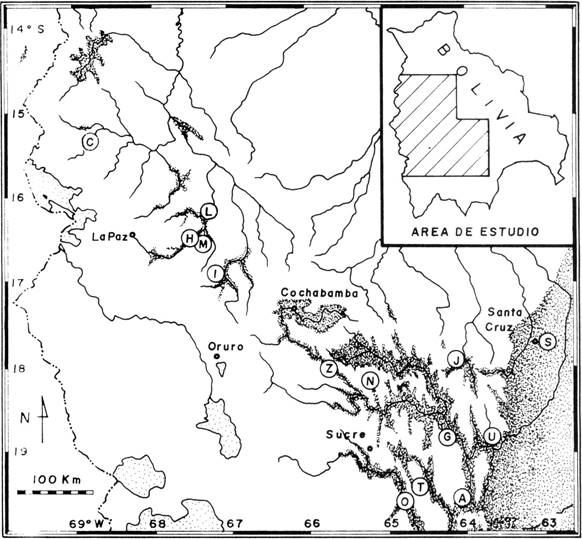
Fig. 1: Localización de bosques caducifolios en los Andes de Bolivia (áreas punteadas) y localización de las áreas de estudio (círculos): A: Río Azero, C: Consata, G: Río Grande, H: Huara, I: Inquisivi, J: San Juan del Potrero, L: Las Mercedes, M: Miguillas, N: Novillero, O: Oron'kota, S: Santa Cruz, T: Tarvita, U: Masicurí, Z: Río Caine.
Métodos
Uno de los grandes impedimentos para estudios de la vegetación en bosques tropicales es el alto número de especies, lo cual limita el área que pueda ser estudiada o impone inversiones extremadamente altas de tiempo y personal (Ellenberg 1975,Whitmore 1993,Ibisch 1996). Esto resulta en estudios puntuales con el uso de grupos indicadores, sean briófitas (Frahm & Gradstein 1991), plantas leñosas de más de 10 (Holdridge et al. 1971) o 2,5 cm de diámetro (Gentry 1982) o familias selectas de plantas vasculares (Tuomisto & Ruokolainen 1994). Otro problema frecuente en tales estudios es la dificultad de identificación de las especies encontradas (Gentry 1982,Tuomisto 1994). En el presente estudio encontramos ambos problemas: por un lado al tratar de cubrir un área geográfica amplia nos enfrentamos a un número muy alto de especies (tan solo para el bosque seco de valle del Tuichi se estiman más de 1200 especies de plantas vasculares; M. Kessler, datos no publicados), por otro lado el conocimiento florístico de los bosques secos bolivianos es aún incipiente, lo que dificulta la identificación de las muestras botánicas. En este sentido, los bosques deciduos presentan un problema especial: por razones de acceso fue necesario realizar el trabajo de campo en la época seca durante la cual gran parte de los árboles, hierbas y geófitas se encuentran en estado deciduo, imposibilitando su identificación.
Por estas razones, decidimos concentrar nuestro estudio en seis grupos de plantas: Acantáceas, Aráceas, Bromeliáceas, Cactáceas, Palmeras y Pteridofitas. Las Melastomatáceas, no son de relevancia para el presente trabajo, ya que es típico de bosques siempreverdes; en efecto, durante el trabajo de campo utilizamos a esta familia para delimitar los bosques secos de bosques siempreverdes. Estas familias reúnen una serie de características que las hacen muy útiles para estudios de vegetación: 1) son grupos fácilmente reconocibles como tales, lo que facilita encontrar las especies en el campo, 2) tienen un número relativamente alto de especies, muchas de las cuáles tienen distribuciones geográficas o ecológicas bien delimitadas, 3) como grupo, tienen una distribución amplia en una variedad de hábitats, y 4) su identificación puede ser efectuada por especialistas, garantizando un alto grado de identificaciones correctas a nivel de especies. Las Cactáceas forman una excepción a esta última regla, pero por ser de importancia crítica en paisajes áridos, han sido incluidas en el presente estudio. Por último, estos grupos mayormente consisten de plantas de porte pequeño a mediano, por lo cual es posible encontrar un número casi ilimitado de individuos y especies en áreas pequeñas (p. ej., 400 m2), sobre todo en el caso de epífitas (Ibisch 1996). A diferencia de esto, para el estudio de árboles se requiere de áreas mucho mayores para encontrar un número representativo de especies (Gentry 1982,Henderson et al. 1991). En lugares montañosos con un microrelieve muy diferenciado frequentemente es difícil encontrar áreas ecológica y florísticamente homogéneas de incluso pocos cientos de metros cuadrados. Análisis realizados por Bach (1997) demostraron que los grupos escogidos son representativos de las relaciones florísticas entre las comunidades completas.
Los relevamientos fitosociológicos (método estándar según Mueller-Dombois & Ellenberg 1974) fueron hechos en áreas de 20x20 m; ocasionalmente adaptamos este tamaño a formas naturales del terreno (p.ej., en quebradas), intentando mantener el área total constante. En bosques deciduos, áreas de 400 m2 satisfacen el criterio del tamaño mínimo de relevamientos fitosociológicos (Mueller-Dombois & Ellenberg 1974), sobre todo si no se consideran árboles de gran porte (M. Kessler, datos no publicados). La selección de los lugares de relevamientos se hizo subjetivamente tratando de escoger muestras representativas de todos los tipos de vegetación presentes en un área de estudio. Los relevamientos fueron caracterizados mediante elevación, exposición, inclinación, datos estructurales de la vegetación (porte y cobertura de los estratos de vegetación) así como la influencia humana (tala, pastoreo, quema). La abundancia de las especies indicadoras fue anotada según la escala de abundancia de Braun-Blanquet (1964).
Todas las especies encontradas en cada área de estudio fueron herborizadas por triplicado y depositadas en el Herbario Nacional de Bolivia (LPB), con los especialistas correspondientes y en el Herbario de la Universidad de Göttingen (GOET).La identificación de las muestras fue realizada por K. Bach (Pteridophyta en parte), W. Barthlott (Cactaceae, epífitas), T. Croat (Araceae), M. Kessler (Cactaceae, terrestres), H. Luther (Bromeliaceae), M. Moraes (Palmae), R. Moran (Pteridophyta en parte), B. 0llgaard (Pteridophyta en parte), D. Wasshausen (Acanthaceae) y J. Wurdack (Melastomataceae).
El ordenamiento de las tablas fitosociológicas se efectuó mediante el método tradicional de Braun-Blanquet (1964) (véase Mueller-Dombois & Ellenberg 1974) con ayuda del programa TAB (Peppler 1988).
Resultados
Los resultados presentados aquí cubren 189 relevamientos localizados en bosques zonales (vegetación climatófila según Rivas-Martinez 1994), es decir bosques típicos del lugar cuya fisionomía y composición están principalmente determinadas por factores climáticos (Walter 1973).
De las aproximadamente 355 especies de plantas vasculares de nuestros grupos indicadores encontradas en estos 189 relevamientos, 220 especies (62%) solamente aparecieron en una localidad de estudio y no fueron utilizadas para la siguiente clasificación a fin de reducir el efecto de características regionales. De las restantes 135 especies, 100 especies (28% del total de especies) estuvieron presentes en más del 6% de los relevamientos. Solamente estas especies fueron utilizadas para la clasificación de la vegetación.
Se reconocieron 11 tipos de vegetación zonal, descritos a continuación, caracterizados por la presencia o ausencia de 73 especies agrupadas en 20 grupos de especies con características similares (Tabla 1). Estas especies fueron agrupadas por mostrar patrones similares de presencia y/o ausencia en los relevamientos, indicando que su distribución está determinada por factores ecológicos y/o biogeográficos similares. Debido a esto, estos grupos de especies pueden ser utilizados para inferir factores generales que influyen la asociación de especies de plantas en tipos de vegetación. Las restantes 27 especies no pudieron ser agrupadas en grupos de especies, ya sea por estar presentes en prácticamente todos los relevamientos (p.ej., Tillandsia streptocarpa) o por mostrar patrones individuales que pudieron ser combinados con los de otras especies para obtener grupos de especies (p.ej., Opuntia brasiliensis) (véase discusión). Debido a que la delimitación de los tipos de vegetación en muchos casos fue gradual, la siguiente clasificación no incluye un orden jerárquico (ver discusión). Recomendamos consultar la tabla 1 al estudiar el texto siguiente.
Tipo I: Este tipo, caracterizado por las especies del grupo 1 y 15 como Doryopteris colina, Ruellia brevifolia, Anemia phyllitidis y Tillandsia tricholepis, Tillandsia didistichia, Polypodium squalidum, Doriopteris concolor, respectivamente. De todas las áreas estudiadas, esta tiene la mayor precipitación media anual (1792 mm en el poblado de Masicurí, algo menos a elevaciones menores hacia el Río Grande). Es interesante notar que la única especie presente del grupo 4, típico de elevaciones bajas con humedad relativamente alta, es Philodendron camposportoanum. No tenemos una explicación para la ausencia de especies como Tillandsia spiralipetala o Epiphyllum phyllanthus. Especies comunes adicionales, en su mayoría exclusivas de esta área de estudio, incluyen Bromelia serra, Cereus haenkeanus, Adiantum tetraphyllum y A. pectinatum (estas especies, así como las especies adicionales mencionadas en los otros tipos de vegetación, no fueron utilizadas para la clasificación de los tipos y son mencionadas por ser elementos comunes dentro de los relevamientos establecidos). El bosque corresponde a un bosque alto (15-20 m) mayormente deciduo dominado por Anadenanthera colubrina. A mayores elevaciones y correspondientemente en regiones más húmedas, aparecen elementos típicos de bosques siempreverdes como Cecropia sp., Myrtáceas y Lauráceas.
Tipo II: Caracterizado por la presencia exclusiva del grupo 2 como Anthurium plowmannii y Cereus stenogonus así como la presencia compartida con otros tipos de vegetación del grupo 15 como Tillandsia tricholepis, Polypodium scualidum y Doryopteris concolor este tipo fue encontrado exclusivamente en el Jardín Botánico de Santa Cruz. Es posible reconocer dos subtipos de vegetación. El primero, con la presencia sólo esporádica de especies del grupo 3 con Tillandsia vernicosa y Rhipsalis baccifera. Corresponde a un bosque alto (15-20 m) con Galles¡a integrifolia, Enterolobium contorquisiliquum, Anadenanthera colubrina, Aspidosperma cyllndrocarpum, Phyllostylon brasiliensis y Casearia gossypifolia (Saldias 1991,Parker et al. 1993). El segundo subtipo, con la presencia de Ruellia erythropus y Microgramma vaccinifolia así como de Epiphyllum phyllanthus y Selenicereus setaceus del grupo 4, algunas son especies epífitas de amplia distribución en tierra bajas. La fisonomía corresponde a un monte achaparrado de 4-6 m de porte de tipo chaqueño (Parker et al. 1993). Otras especies características de ambos tipos de bosque son Pseudananas sagenarius, Harrisia pomanensis y Cleistocactus baumannii. En la clasificación de Navarro (1997) este tipo corresponde aproximadamente a la “serie termotropical seco-subhúmeda de Diplokeleba floribunda y Phyllostylon rhamnoides (C.b.1.)” aunque hay diferencias florísticas marcadas.
Tipo III: Este tipo, que incluye todos los relevamientos del valle de Consata, está caracterizado por la presencia compartida de los grupos 4, 5 y 8 con las especies: Epiphyllum phyllantus, Tillandsia spiralipetala, Philodendron camposportoanum, Selenicereus setaceus; Pecluma plumula; Tillandsia krukoffiana, Tillandsia juncea y Microgramma vaccinifolia, Aechmea distichantha Doryopteris palmata, Anthurium paraguayense y la ausencia conspicua del grupo 15. No tenemos una explicación convincente para la falta de este último grupo de amplia distribución en bosques secos. Considerando la posición geográfica aislada y la pequeña extensión de los bosques deciduos en el valle de Consata sería posible que la falta de estas especies se deba a factores biogeográficos, es decir, que estas especies nunca hayan llegado a este valle o que se hayan extinguido. Al igual que en el tipo II, en los bosques del valle de Consata es posible distinguir dos subtipos de vegetación, caracterizados por la presencia (subtipo 1: Anthurium plowmannii, Cereus stenogonus y Acanthaceae 5390) o ausencia (subtipo 2: Tillandsia vernicosa y Rhipsalis baccifera) de las especies del grupo 3. Es también conspicua la falta de Philodendron camposportuanum (grupo 4) en el primer subtipo. Este subtipo corresponde a un bosque relativamente seco y bajo (8-15 m) con especies de árboles tales como Jacaranda mimosifolia y Tabebuia sp.. Este subtipo ocurre principalmente en la parte más alta del valle (hacia el oeste) y se extiende valle abajo sobre todo en el lado sur del valle. El segundo subtipo es un bosque más alto (1520 m) dominado por Anadenanthera colubrina que ocurre sobre todo en laderas de exposición sur. Sin embargo, a diferencia del bosque alto (subtipo 1) del Jardín Botánico de Santa Cruz (tipo II), el bosque alto del valle de Consata no tiene una ausencia conspicua de epífitas, estando los árboles cubiertos de densas masas de epífitas de los grupos 4 y 5 como Epiphillum phyllanthus, Tillandsia spiralipetala, Pecluma plumula, Tillandsia krukoffiana y Tillandsia juncea. Otras especies comunes en el valle de Consata son Cereus sp. “A”, Justicia viscosa y J. rusbyana así como Polypodium furfuraceum. Este tipo está incluido en la “serie termotropical pluviestacional húmeda de Myroxylon balsamum y Schinopsis brasiliensis (D.a.3.)” de Navarro (1997), así como los tipos IV, V y VIII.
Tipos IV y V: Estos dos tipos de vegetación se distribuyen en el valle del Río Boopi (La Paz) y sus afluentes en la parte central del departamento de la Paz. El tipo IV corresponde a los bosques de elevaciones menores (850-1000 m) estudiados en los alrededores de Las Mercedes y el tipo V incluye los relevamientos realizados en los alrededores de La Plazuela, el valle de Miguillas y en dirección hacia Lambate entre 900 y 1950 m. El tipo IV es algo más húmedo que el tipo V. Ambos están caracterizados por la presencia de los grupos 5, 6, 8 y 15 con: Tillandsia krukoffiana, Tillandsia juncea; Fosterella weddelliana, Pereskia weberiana, Samaipaticereus inquisivensis, Cereus huilunchu; Microgramma vaccinifolia, Aechmea distichantha, Doryopteris palmata, Anthurium paraguayense y Tillandsia tricholepis, Tillandsia didisticha, Polypodium squalidum, Doryopteris concolor diferenciándose entre ellos por la presencia (tipo IV) o ausencia (tipo V) del grupo 4 con las especies: Epiphyllum phyllanthus, Tillandsia spiralipetala, Philodendron camposportuanum, Selenicereus setaceus y Pecluma plumula, compartido con el tipo III. Tillandsia krukoffiana y Tillandsia juncea (grupo 5) caracteriza a los bosques relativamente húmedos de las partes bajas de los valles interandinos del departamento de La Paz. Las especies del grupo 6 (Fosterella weddelliana, Pereskia weberiana, Samaipaticereus inquisivensis y Cereus huilunchu) son Cactáceas y Bromeliáceas endémicas de los valles secos del departamento de La Paz que son parcialmente compartidas con el tipo de vegetación VIII, que corresponde a los bosques secos de mayores alturas en estos valles. Todos estos tipos de vegetación están en contacto directo entre ellos y estudios adicionales en áreas intermedias sin duda demostrarían cambios graduales entre ellos. Es notable que las especies del grupo 6 falten por completo o parcialmente en algunos de los relevamientos del tipo IV. Los relevamientos sin estas especies corresponden a bosques más húmedos y mejor conservados, mientras que la presencia de estas especies indica condiciones más secas o bosques abiertos por pendientes abruptas o influencia humana. En caso extremo, en tales relevamientos (p.ej., no. 287) pueden faltar las especies del grupo 4 como Epiphyllum phyllanthus, Tillandsia spiralipetala y Philodendron camposportuanum, por lo cual corresponden al tipo de vegetación V. Especies adicionales incluyen Anthurium clavigerum y A. ottonis, Tillandsia variabilis, Fosterella elata, Asplenium dimidiatum y la palmera endémica Syagrus yungasensis en el tipo IV, así como Opuntia quimilo, Tillandsia carnosa y T. denudata, Anemia ferruginea, Trachypteris pinnata y Justicia subintegrifolia en en tipo V. El árbol dominante en todo el valle es Anadenanthera cf. peregrina.
Tipo VI: Este tipo fue encontrado en la localidad de San Juan del Potrero y se caracteriza por la presencia casi exclusiva del grupo 7 con Tillandsia tenuifolia, Opuntia diascolor vel. sp. aff., Cleistocactus buchtienii, Lepismium lumbricoides y Ruellia erythropus así como la presencia compartida de los grupos 8, 15 y 19 con Microgramma vaccinifolia, Aechmea distichantha, Tillandsia tricholepis, Harrisia tetracantha, Opuntia sulphurea vel. sp. aff., Corryocactus melanotrichus. Al igual que en el tipo III, es notable la ausencia de tres de las cuatro especies del grupo 15 (Tillandsia didistichia, Polypodium squalidum y Doryopteris concolor), aunque en este caso seguramente esto no se debe a factores biogeográficos. Las especies del grupo 19 (Harrisia tetracantha, Opuntia sulphurea vel. sp. aff., Corryocactus melanotrichus) son típicas de matorrales espinosos a elevaciones mayores (tipo X). Su presencia, al igual que la gran abundancia de Aechmea distichantha (grupo 8), se debe a la alta presión por pastoreo típica en todos los valles centrales bolivianos, la cual favorece a estas especies no palatables. Dentro de este tipo nuevamente es posible distinguir dos subtipos diferenciados por su humedad. El subtipo más seco, incluyendo los relevamientos hacia la izquierda en la tabla, se caracteriza por la ausencia de Doryopteris palmata y Anthurium paraguayense del grupo 8. En el subtipo más húmedo se nota la falta de Opuntia discolor y Cleistocactus buchtienii y la aparición del grupo 9, compartido con los tipos VII y VIII. Otras especies incluyen Neoraimondia herzogiana y Lepismium monacanthum.
Tipo VII: Este tipo incluye 30 relevamientos en valles interandinos de Chuquisaca entre 1050 y 2100 m, mayormente del área de estudio de Río Acero así como algunos relevamientos de Río Grande y Tarvita. Se caracteriza por la presencia de los grupos 9, 10 (exclusivo a este tipo) con Adiantum raddianum, Fosterella penduliflora y Tillandsia lorentziana y el grupo 15. Se puede diferenciar fácilmente tres subtipos, los primeros dos de los cuales se caracterizan por la presencia de algunas especies de los grupos 3 y 4 (p.ej., Rhipsalis baccifera, Epiphyllum phyllanthus) así como de Anemia phyllitidis (grupo 12). Estos dos subtipos constituyen los representantes típicos de los bosques deciduos del tipo VII, dominados por la especie arbórea Anadenanthera colubrina y fueron encontrados exclusivamente en los alrededores del Río Acero. El subtipo 1 corresponde a los bosques relativamente más húmedos con el grupo 11 con las especies Asplenium bangii, A. Bradei, Aechmea bromeliifolia, Pteris denticulata, Justicia ramulosa, Blechnum occidentale, Aphelandra hieronymi, además de Polystichum platyphyllum, Syagrus cardenasii, Pteris quadriaurita, P. deflexa y P. splendens, Rueilla sanguínea y Ctenitis submarginalis, mientras que el subtipo 2 incluye los relevamientos más secos con las especies del grupo 13 con Doryopteris lorentziana, Hemionitis tomentosa, Cereus validus, así como Asplenium pumilum y A. formosum, Adiantopsis chlorophylla y Justicia kuntzei. El tercer subtipo es un grupo de relevamientos bastante heterogéneo caracterizado por el grupo de especies 14 (parcialmente compartidas con el subtipo 2) con Rhipsalis floccosa / Campyloneurum aglaolepis y Anemia villosa, incluyendo relevamientos de las tres localidades arriba mencionadas. La presencia de especies como Rhipsalis floccosa y Campyloneurum aglaolepis indica una afinidad hacia los bosques siempreverdes del tipo Boliviano-Tucumano ("Bosque Subhúmedo Submontano" correspondiente al piso inferior de la formación Tucumano-Boliviana según Ribera et al. 1996). Este tipo incluye la "serie termotropical inferior pluviestacional subhúmeda de Schinopsis haenkeana y Tabebuia impetiginosa (C.a.7.)" de Navarro (1997) aunque la delimitación geográfica no es idéntica, excluyendo a la serie de Navarro el área del Río Grande.
Tipo VIII: Este tipo, que corresponde a los bosques de elevaciones mayores (2200-2500 m) en los valles superiores de los ríos La Paz, Ayopaya y Santa Rosa (Cochabamba) se caracteriza por la presencia de algunas especies del grupo 6 como Samaipaticereus inquisivensis y Cereus huilinchu del grupo 7 con Tillandsia tenuifolia, los grupos 9, 15 y 16 con: Tillandsia usneoides, Microgramma squamulosa; Tillandsia tricholepis, T. Didisticha y Polypodium pycnocarpon s.l., Cheilanthes sinuata, Cheilanthes myriophyilla, Tillandsia sphaerocephala, Anemia myriophyilla y Pellaea ovata, faltando un grupo de especies exclusivas a este tipo. Esto se debe a las graduaciones ya mencionadas hacia el tipo V así como hacia el tipo IX. De este modo, este tipo incluye tanto especies de amplia distribución en tierras de mediana elevación (p.ej., Tillandsia tenuifolia, T. usneoides, T. didisticha, T. tricholepis, Microgramma squamulosa), algunas especies endémicas de los valles de La Paz (Samaipaticereus inquisivensis, Cereus huilunchu , Lepismium paranganiensis) así como especies típicas de elevaciones mayores relativamente secas como el grupo 16 (Polypodium pycnocarpon s.l., Cheilanthes sinuata, Cheilanthes myriophyilla, Tillandsia sphaerocephala, Anemia myriophylla y Pellaea ovata). Además, en algunos relevamientos se encontraron especies típicas de bosques montanos húmedos (p.ej., Chamaedorea pinnatifrons, Racinaea flexuosa), mostrando una transición hacia estos bosques. Especies adicionales incluyen Dicliptera aff. scutellata y Polypodium thyssanolepis.
Tipos IX y X: Estos dos tipos corresponden a los bosques bajos y matorrales espinosos secundarios de elevaciones mayores (20002800 m) en los valles secos de Cochabamba y Chuquisaca. Ambos tipos comparten las especies del grupo 17 con Tillandsia virescens, T. Caliginosa, Cereus comarapanus y Tillandsia bryoides, las cuales son muy raras en otros tipos de vegetación. Además, se caracterizan por la ausencia de muchas especies de amplia distribución a menores elevaciones y en regiones algo más húmedas (p.ej., grupos 8, 9 y sobre todo 15 como Microgramma vaccinifolia, Tillandsia usneoides y T. tricholepis respectivamente, aunque algunas especies de muy amplia distribución en bosques deciduos (p.ej., Tillandsia streptocarpa, T. capillaris, T. duratii) demuestran una conección florístca con los otros tipos de vegetación discutidos en el presente trabajo.
El tipo IX muestra una transición hacia el tipo VIII mediante el grupo de especies 16. Los bosques del tipo IX fueron encontrados exclusivamente en el área de Novillero. Se trata de bosques de aproximadamente 15 m de altura dominados por Tipuana tipu y Escallonia millegrana descritos en mayor detalle por Navarro et al. (1996). El tipo X incluye relevamientos en regiones aún más secas (Oron'kota y Río Caine) con mayor influencia humana. El primer factor se evidencia en la presencia de epífitas endémicas de los valles secos internandinos (p.ej., Tillandsia cardenasii), mientras que el sobrepastoreo conlleva una dominancia de especies de Cactáceas (p.ej., Opuntia pubescens, O. sulphurea, Harrisia tetracantha, Corryocactus melanotrichus) y Bromeliáceas terrestes espinosas (Deuterocohnia longipetala). Naturalmente, este tipo correspondería a bosques semicaducifolios dominados por Schinopsis haenkeana, Aspidosperma quebracho-blanco y Jacaranda mimosifolia aunque en la actualidad los árboles dominantes son especies espinosas de bajo porte, como Acacia macracantha, Prosopis kuntzei, P. laevigata y Zizphus mistol. Una localidad coneste tipo de vegetación en el valle de Capinota (Cochabamba) fué descrita por Pedrotti et al. (1988).
Tipo XI: Este último tipo, que fue encontrado exclusivamente en la parte baja (950-1300 m) de la transecta altitudinal del Río Grande, tiene una posición algo aislada en la tabla. Sin embargo, la presencia de Tillandsia streptocarpa, T. capillaris y T. duratii así como de unas pocas especies de los grupos 17 y 18 como Tillandsia bryoides y Deuterocohnia longipetala respectivamente, demuestra conexiones con los demás tipos de vegetación, en especial con el tipo X. Esto se debe a que no hemos estudiado otras localidades tan áridas a elevaciones relativamente bajas. Por otro lado, el grupo de especies 20 con Neocardenasia herzogiana, Pereskia sacharosa, Espostoa guentheri, Corryocactus pulquinensis y Gymnocalycium pflanzii caracteriza claramente a estos bosques espinosos bajos, descritos como "Serie de Neocardenasia ( = Neoraimondia) herzogiana y Schinopsis haenkeana" por Navarro et al. (1996).
Discusión
Los tipos de vegetación descritos en el presente trabajo en su mayoría corresponden a localidades individuales de estudio. Esto se debe a que, a pesar de haber excluido especies que solamente ocurren en una localidad, los relevamientos de cada área de estudio son en su mayoría más similares entre sí que a relevamientos de otras localidades. Esto no significa que no sea posible relacionar los tipos de vegetación. Diez de los 20 grupos de especies ocurren en más de un tipo de vegetación y determinan el orden de los tipos y la estructura de la tabla. En este sentido resaltan grupos como el 8 y el 15 que tienen distribuciones amplias pero bien definidas en la tabla, lo cual corresponde a distribuciones geográficas y ecológicas discretas en la naturaleza. Especies con distribuciones aún mayores en los bosques secos ocurren en la mayoría de las localidades y por lo tanto no pueden ser utilizadas para un agrupamiento. Estas especies (Tillandsia streptocarpa, T. loliacea, T. capillaris y T. duratii) se encuentran en la parte inferior de la tabla. Otras especies comunes, p. ej., Opuntia brasilienses y Argyrochosma nivea, tienen distribuciones amplias pero con límites claros. Sin embargo, por tratarse de especies aisladas, no son utilizadas para delimitar tipos de vegetación. Si se incluiría relevamientos considerando la vegetación total, es muy probable que se encontraría especies adicionales con patrones similares. Por ejemplo, Anadenanthera colubrina y A. cf. peregrina, los árboles dominante en los tipos I a VII, en nuestra área de estudio tienen un patrón de distribución casi idéntico a Opuntia brasiliensis (aunque esta también ocurre en regiones más húmedas del Beni, S. Beck, com. pers.).
A pesar de que los tipos de vegetación en la tabla 1 están claramente delimitados y son fácilmente diagnosticables, en muchos casos encontramos transiciones, tanto entre tipos de vegetación como entre grupos de especies. Por ejemplo, el grupo 14 tiene una ocurrencia bastante gradual. Otros grupos, p. ej., los números 3, 5, 12, 16 y 17, no sirven para delimitar tipos individuales de vegetación, sino más para establecer transiciones entre estos. En otros casos, encontramos "grupos" de especies constantes en un tipo de vegetación que se componen de algunas especies de otros grupos (p.ej., en los tipos VI, abajo, VII y VIII, arriba). Todo esto indica que el agrupamiento de especies y relevamientos en "tipos" y "grupos" es hasta cierto punto artificial y corresponde parcialmente a la localización aislada de los lugares de estudio (p.ej., claramente en el caso del tipo XI). Esto se evidencia al considerar las transiciones ya descritas (ver resultados) entre ciertos tipos de vegetación (p. ej., IV y V, IX y X) o localidades vecinas. Sin duda, un estudio de localidades adicionales intermedias resultaría en transiciones más graduales entre los "tipos".
Un ejemplo de ésto es el gradiente altitudinal estudiado en el valle del río Grande (Tabla 2). Aquí, la distribución continua de los relevamientos a lo largo de la transecta resulta en un intercambio gradual de especies, el cuál hace imposible delimitar tipos de vegetación o grupos de especies. Desde luego que las comunidades vegetales en los extremos del gradiente son totalmente diferentes, reflejan condiciones ecológicas distintas y merecen ser descritas como tipos diferentes: los relevamientos más bajos corresponden al tipo XI de la tabla general, mientras que los más altos pertenecen al subtipo 3 del tipo VII. Los relevamientos intermedios no correponden a ninguno de estos tipos y representan comunidades vegetales distintas. Analizando la distribución de las especies en la transecta, se observa que cada una de ellas muestra patrones individuales. Los problemas al definir los grupos de especies en la tabla general, descritos arriba, también sugieren que las especies no reaccionan como grupos, sino individualmente. Desde luego que hay muchas especies con patrones bastante similares, pero un análisis detallado en la mayoría de los casos elucidará diferencias ecológicas. La delimitación de tipos de vegetación y grupos de especies es útil para describir los cambios de la vegetación y los factores ecológicos correspondientes, pero éstos no deben ser interpretados como entidades naturales discretas.
En la tabla 1 se evidencia claramente un ordenamiento de los tipos y grupos de arriba a la izquierda hacia la derecha abajo. Para una interpretación ecológica de este patrón hemos ordenado los relevamientos y los tipos de vegetación en relación a la elevación y la precipitación media anual (Fig. 2). Estos son los factores principales que determinan la vegetación zonal (Walter 1973,Lauer 1986). Se observa que el ordenamiento obedece principalmente a un gradiente de elevación (de elevaciones menores a mayores) combinado con un gradiente de precipitación (de húmedo a seco). La interacción de ambos factores resulta en un patrón algo difuso y no podemos deducir claramente cuál de ellos sea el principal. Sin embargo, la subdivisión de ciertos tipos de vegetación en subtipos obedece en todos los casos a factores de humedad, lo que sugiere que este sea el factor subordinado. Esto no significa necesariamente que la elevación sea un factor más importante que la precipitación en la determinación natural de la vegetación zonal. Nosotros creemos que la dominancia aparente de la elevación se deba a la selección subjetiva de lugares de estudio y que la inclusión de otras localidades podría resultar en un patrón diferente. Probablemente la elevación (y los factores correlacionados: temperatura, insolación, etc.) y la humedad tengan una influencia similar en la determinación de la vegetación natural de los valles secos de Bolivia.
Comparando la clasificación presentada aquí con la de Ribera et al. (1996), el presente trabajo incluye una tipificación bastante más detallada, la cual refleja de un manera más directa la diferenciación climática y biogeográfica de los bosques secos andinos de Bolivia. En comparación con el trabajo de Navarro (1997) inicialmente resalta la dificultad de correlacionar los tipos de vegetación descritos. Esto se debe principalmente a la selección de especies características totalmente diferentes (mayormente especies leñosas por Navarro; grupos indicadores en el presente trabajo). Por lo tanto, una correlación es posible solamente mediante datos de elevación y localización geográfica. Aquí, se evidencian discrepancias claras. Por ejemplo, el presente trabajo diferencia cuatro tipos de vegetación en los valles secos del depto. La Paz (y existen varios tipos adicionales en los valles de Camata, Tuichi, Inicua, etc.), mientras que Navarro solo reconoce un tipo. Por otro lado, Navarro describe no menos que 17 series climatófilas en los valles secos de Cochabamba, Chuquisaca y Tarija, donde el presente trabajo solamente diferencia seis. Estas discrepancias sin duda reflejan diferentes intensidades de estudio de parte de los autores. Por otro lado, se evidencia que aunque el conocimiento de la vegetación de los valles andinos de Bolivia ha avanzado considerablemente en los últimos años, aún estamos lejos de obtener una clasificación coherente.
Actualmente el factor preponderante en los bosques deciduos es la influencia humana. Esta se evidencia de diferentes maneras en zonas ecológicas distintas. A elevaciones bajas en áreas húmedas los bosques dominados por Anadenathera colubrina (tipos I, III, IV, VII) están relativamente bien conservados en la mayoría de las localidades y solo localmente sufren presión por extracción de especies maderables, chaqueo para cultivos, pastoreo o quema indiscriminada. En bosques más secos y a elevaciones mayores, las condiciones ecológicas más extremas reducen la resistencia de las comunidades vegetales a disturbios y fuerzan a la población humana a utilizar los bosques más intensivamente. Esto, combinado con densidades humanas relativamente altas en muchas regiones, resulta en una degradación fuerte y general de estos bosques. Esto se evidencia de forma más clara en los tipos más secos y altos (IX- XI). Aquí el sobrepastoreo, en especial, reduce la cubierta vegetal y la hace propensa a la erosión y desertificación.
En épocas precolombinas los valles altos y relativamente secos fueron utilizados intensivamente para la agricultura, tanto en las planicies de los valles, como en laderas con andenes. La utilización de los bosques como lugares de pastoreo para el ganado recién comenzó con la introducción de estas especies por los españoles. Por lo tanto, la degradación masiva de estos bosques ha tenido lugar durante los últimos 500 años. En cambio, los bosques deciduos algo más húmedos de elevaciones menores (hasta unos 1800 m) también estuvieron habitados antiguamente, pero hoy en día han recobrado su cubierta vegetal. En los valles de Camata, Coroico, La Paz, Miguillas y Cotacajes hemos encontrado extensas áreas de ruinas precolombinas (andenes y viviendas) dentro de lo que hoy en día son los bosques mejor conservados. Es posible que estos vestigios correspondan a la cultura Mollo (Boero 1992) u otras culturas preincaicas. No sabemos cuando, ni por que razones estos asentamientos hayan sido abandonados, pero la cobertura vegetal actual demuestra el potencial de la vegetación para recuperarse. Por otro lado, hay que considerar que la composición actual de la vegetación puede no corresponder a aquella de los bosques naturales.
Tabla 2: Cambios en la composición florística a lo largo de una transecta altitudinal desde el Río Grande hacia el pueblo de Nuevo Mundo a lo largo de la carretera Vallegrande-Padílla. Para una explicación de los símbolos véase tabla 1.
| No. de relevamiento | 131 | 130 | 132 | 134 | 133 | 136 | 135 | 137 | 138 | 139 | 140 | 141 | 142 | 144 | 143 |
| Elevación (10m) | 210 | 210 | 185 | 170 | 175 | 170 | 170 | 150 | 150 | 130 | 125 | 110 | 110 | 95 | 90 |
| Exposición | NW | NW | E | SW | NE | W | S | N | NW | E | N | E | SE | E | N |
| Inclinación | 25 | 30 | 10 | 30 | 50 | 25 | 40 | 3 | 5 | 25 | 25 | 5 | |||
| No. de especies | 8 | 8 | 9 | 7 | 5 | 7 | 12 | 4 | 12 | 11 | 10 | 10 | 7 | 11 | 6 |
| Aphelandra hieronymi | 1 | 1 | 1 | ||||||||||||
| Dicliptera tweediana | + | 1 | 1 | ||||||||||||
| Polystichum platyphyllum | 1 | 1 | + | ||||||||||||
| Tillandsia usneoides | + | 1 | + | ||||||||||||
| Justicia sp. MK 5175 | 3 | 1 | + | ||||||||||||
| Tillandsia didisticha | 2 | 1 | + | ||||||||||||
| Lepismium ianthotele | 1 | 1 | 1 | ||||||||||||
| Rhipsalis floccosa | 1 | 1 | + | 1 | 1 | + | 1 | ||||||||
| Microgramma squamulosa | 2 | 2 | 1 | 1 | 1 | + | 1 | ||||||||
| Puya sp. MK 5173 | + | + | 1 | + | 2 | ||||||||||
| Cereus comarapanus | + | 1 | 1 | 1 | 1 | ||||||||||
| Tillandsia capillaris | + | + | 1 | ||||||||||||
| Anemia ferruginea | + | + | + | ||||||||||||
| Echinopsis cf. quadratiumbonatus | + | 1 | + | ||||||||||||
| Acanthaceae sp. MK 5190 | 1 | 2 | 2 | 1 | 2 | ||||||||||
| Tillandsia loliacea | + | 1 | + | + | + | ||||||||||
| Gymnocalycium pflanzii | + | 1 | + | + | 1 | ||||||||||
| Opuntia discolor | + | + | + | 1 | 1 | 1 | |||||||||
| Tillandsia streptocarpa | + | + | 1 | 2 | 2 | 2 | 1 | 1 | 3 | + | |||||
| Corryocactus cf. pulquinense | 1 | + | 1 | 2 | 1 | 1 | 2 | + | |||||||
| Pereskia sacharosa | 1 | 1 | 1 | 1 | 1 | + | |||||||||
| Deuterocohnia longipetala | 3 | + | 3 | 3 | 1 | ||||||||||
| Tillandsia bryoides | 3 | + | 3 | 3 | 1 | ||||||||||
| Neoraimondia herzogiana | 1 | + | 1 | 1 | |||||||||||
| Cheilanthes sp. MK 5199 | 1 | + | 1 | 1 | |||||||||||
| Espostoa guentheri | 1 | 2 | 2 | ||||||||||||
| Tillandsia lorentziana | 2 | + | 1 | + | + | + | 1 | 2 | 1 | 1 | 1 | + | 1 | ||
| Tillandsia bandensis | 1 | + | 1 | 1 | 1 | 2 | 1 | 1 | 1 | + | + | + | |||
| Tillandsia duratii | 1 | 1 | 1 | + | 2 | + | + | 1 | + | + | 1 | ||||
| Tillandsia tricholepis | + | + | + | 1 | + | + | 2 | + | |||||||
| Polypodium squalidum | + | 1 | 1 | 1 | |||||||||||
| Adiantum sp. MK 5162 | 2 | 2 | 1 | 1 | |||||||||||
| Pereskia diaz-romeroana | + | + | 1 | ||||||||||||
| Echinopsis sp. MK 5204 | 1 | + | |||||||||||||
| Opuntia cf. pubescens | + | 1 | |||||||||||||
| Quiabentia verticillata | 1 | 2 | |||||||||||||
| Adiantum sp. MK 5161 | + | + | |||||||||||||
| Asplenium sp. MK 5168 | + | + | |||||||||||||
| Cheilanthes pruinata | + | + | |||||||||||||
| Selaginella sp. MK 4896 | 1 | 1 | |||||||||||||
Además:
Adiantum raddianum (130), Campyloneurum lorentzii (130), Pleopeltis macrocarpa (130), Campyloneurum aglaolepis (131), Justicia kuntzei (131), Asplenium bradei (131), Justicia sect. Chaetothylax (132), Acanthaceae sp. MK 5170 (132), Tillandsia sphaerocephala (133), Fosterella cf. penduliflora (135), Asplenium depauperatum (135), Doryopteris lorentzii (135), Asplenium sp. MK 5179 (135), Thelypteris sp. (136), Opuntia sulphurea (141), Opuntia retrorsa (142), Tillandsia lotteae (144), cf. Stetsonia coryne (144).
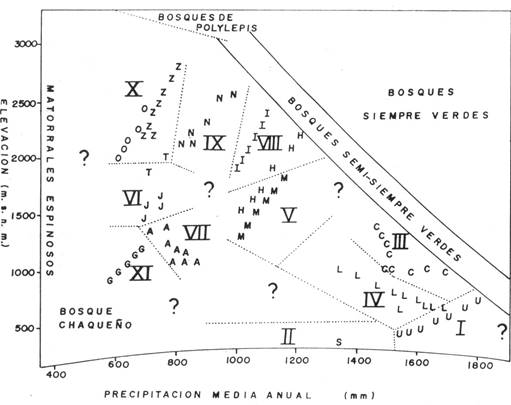
Fig. 2: Distribución ecológica de los tipos de vegetación zonal reconocidos en este estudio en relación a elevación y precipitación media anual, así como su relación con otros tipos de vegetación. Las letras corresponden a las localidades de estudio (A: Río Azero, C: Consata, G: Río Grande, H: Huara, I: Inquisivi, J: San Juan del Potrero, L: Las Mercedes, M: Miguillas, N: Novillero, O: Oron'kota, S: Santa Cruz, T: Tarvita, U: Masicurí, Z: Río Caine), los números romanos a los tipos de vegetación. Signos de interrogación muestran dificultades en la delimitación de los tipos o la falta de estudios en localidades con tales características ecológicas. Los valores de precipitación son aproximaciones en base a datos proporcionados por el SENAMHI (1993).
Conclusiones
El presente estudio demuestra la posibilidad de utilizar grupos indicadores para estudios de vegetación en bosques tropicales de alta diversidad. Desde luego que estudios completos de la vegetación serían preferibles, sin embargo, tales estudios son casi imposibles dado el número muy alto de especies y la dificultad de identificar muchos grupos. Por lo tanto consideramos que el método utilizado aquí representa un compromiso practicable entre clasificaciones puramente fisonómicas (como, p.ej., aquella de Ribera et al. 1993) y la situación ideal (pero no realizable por el momento) de estudios de vegetación que incluyen un análisis florístico de la vegetación completa.
Nuestro estudio además demuestra una variabilidad regional marcada en la composición florística de los bosques deciduos andinos de Bolivia. Considerando que muchas de las especies encontradas son endémicas a uno o pocos valles adjacentes (p.ej., Cactáceas: Navarro 1996, Palmeras: Moraes 1996) se evidencia que la conservación de muchas de estas especies depende de la preservación de más de un "tipo de vegetación de bosques andinos deciduos". Por ejemplo, aunque los bosques del Río Tuichi (incluidos en el Parque Nacional y Área Natural de Manejo Integrado Madidi) y del Río Boopi son fisonómicamente muy parecidos, hay un número considerable de especies no compartidas entre ambas localidades (p.ej., Syagrus yungasensis, Tillandsia krukoffiana, Parodia miguillensis). Por lo tanto, será necesario conservar ejemplos representativos de cuantos bosques secos andinos sea posible. Debido a la fuerte presencia humana en muchos valles andinos, esto frequentemente no será posible mediante el establecimiento de áreas protegidas, sino dependerá del desarrollo de un entendimiento de la función ecológica (protección contra erosión, estabilización del régimen hígrico, proporcionamiento de hábitat para plantas y animales utilizables, etc.) de los bosques por parte de la población rural y de la implementación de métodos agrícolas sostenibles. Esperamos que nuestro estudio ayude a resaltar la diversidad florística de los bosques deciduos andinos de Bolivia, los cuáles hasta el presente han sido mayormente ignorados por actividades de conservación, aunque representan algunas de las regiones más densamente pobladas del país y con una larga historia de colonización y utilización.












 uBio
uBio 

