Introducción
Las poblaciones humanas que habitan regiones rurales del Neotrópico dependen en gran medida del consumo de animales silvestres (Redford & Robinson 1987). En Bolivia y otros países de América tropical, los animales más apetecidos son aquellos de mayor tamaño, especialmente herbívoros y frugívoros de las familias Tayassuidae, Tapiridae, Cebidae y Cracidae (Redford & Robinson 1987,Redford & Stearman 1989,Peres 1990,Chicchón 1992,Encarnación et al. 1993). La cacería de subsistencia puede reducir el tamaño de las poblaciones animales, llegando a la extinción local o funcional de algunas especies (Peres 1990,García & Tarifa 1991,Roldán 1997). Estas extinciones pueden producir un “bosque vacío”; es decir, un bosque aparentemente intacto en su vegetación, pero alterado en sus interacciones planta- animal (Redford 1992).
La extinción de mamíferos herbívoros reduce la presión de herbivoría y con ello puede ocasionar aumento en la dominancia de plántulas de algunas especies arbóreas, con la consiguiente disminución en la diversidad específica (Dirzo & Miranda 1991,Leigh et al. 1993), aunque estos efectos no son siempre evidentes (Terborgh & Wright 1994,Roldán 1997). A nivel poblacional, los efectos de la defaunación se manifestarían en un aumento en el reclutamiento de algunas especies, por disminución de la presión de herbivoría; y en la disminución del reclutamiento para otras, por falta de sus agentes de dispersión, todo lo cual ocasiona cambios en la estructura de la vegetación. La intensidad de estos cambios, sin embargo, dependería del grado de defaunación que haya sufrido el bosque (Roldán 1997).
Con respecto a la dispersión de semillas, se ha estimado que más del 4% de las especies dispersadas por frugívoros en los bosques de Uganda podrían extinguirse ante la ausencia de éstos, por la baja probabilidad de reclutamiento debajo de los parentales (Chapman & Chapman 1995). Dos factores relacionados a la probabilidad de reclutamiento son la distancia a la cual son dispersadas las semillas y la agregación de las mismas, como producto de la dispersión por frugívoros.
Las semillas dispersadas lejos de los parentales tendrían mayor probabilidad de sobrevivir, dado que así escaparían a la acción de agentes de mortalidad distancia o denso-dependientes (Janzen 1970). Trabajos experimentales indican que dicho patrón se cumple para algunas especies (Clark & Clark 1984,Fragoso 1997), no obstante el reclutamiento de la mayoría de las especies estudiadas a la fecha no es significativamente afectado por la distancia a los conespecíficos adultos (Hubbell 1980,Condit et al. 1992).
La ausencia de dispersión por frugívoros determinaría mayor agregación de semillas debajo de los parentales y, si la depredación de semillas es denso-dependiente, la mortalidad de semillas por depredación sería mayor en ausencia de los dispersores. La susceptibilidad de las semillas a la depredación y competencia es dependiente del patrón de agregación de las semillas generado por los frugívoros. Las especies dispersadas en agregados deberían ser tolerantes a la competencia, ya que la interacción con otros individuos de la misma u otra especie se daría naturalmente, tanto para semillas dispersadas lejos de los parentales como para aquellas que caen debajo de los mismos. Las semillas dispersadas en forma aislada deberían ser sensibles a la competencia tanto intra como interespecífica, dado que el desarrollo de atributos que den ventajas competitivas sería innecesario para especies que generalmente no interactúan con otros individuos (Howe 1989). Si lo anterior se cumple, las especies dispersadas en agregados deberían ser menos vulnerables a la pérdida de sus dispersores de semillas, ya que con o sin esos vectores las semillas formarían agregados debajo de los parentales. Consecuentemente, la sobrevivencia de semillas y plántulas de especies dispersadas en agregados no debería ser afectada por la falta de dispersión de las semillas (Howe 1989). En el caso de las especies dispersadas en forma aislada, la ausencia de dispersión y consiguiente agregación debajo de los parentales implicaría aumentar las interacciones competitivas, por lo que debería producirse mayor mortalidad de semillas y plántulas; por tanto esas especies serían más vulnerables a la extinción de sus dispersores (Howe 1989).
Los frugívoros que dispersan semillas en forma aislada generalmente son aquellos de menor tamaño (< 3 kg), mientras que la dispersión en agregados la realizan principalmente animales de gran tamaño (Foster & Janson 1985,Wheelwright 1985a,b,1991,Howe 1989,1990,Jordano 1983,1992,Mack 1993). Dado que la cacería de subsistencia se centra en los frugívoros de gran tamaño, éstos son los más vulnerables a la extinción local o funcional. Entonces, serían las especies dispersadas en agregados las que perderían sus dispersores más frecuentemente, pero serían también las menos afectadas en su demografía por dicha pérdida. La consecuencia inmediata de la extinción de los dispersores sería un acortamiento en la cola de la sombra de semillas, lo cual produciría agregados de semillas y plántulas debajo de los parentales y ausencia de las mismas lejos de ellos. Sin embargo, si las semillas son dispersadas en agregados, su sobrevivencia y la de las plántulas no debería ser afectada por los cambios en abundancia y distribución de las mismas (Howe 1989).
El sistema en estudio
Los primates son frugívoros de gran tamaño y frecuentemente sufren extinción local por cacería de subsistencia (Peres 1990,García y Tarifa 1991). Los primates neotropicales son principalmente frugívoros y comúnmente actúan como dispersores de semillas (van Roosmalen 1985a,b,Chapman 1989,Terborgh 1986,Benítez-Rodríguez et al. 1993,Estrada y Coates- Estrada 1993,Julliot y Sabatier 1993,Peres 1994), dándose casos en que algunas especies dependen fuertemente de aquellos para la dispersión de sus semillas. Este es el caso de Ateles paniscus (Cebidae) y algunos árboles neotropicales, como Rheedia sp., Brosimum parinarioides y Trichilia spp. (van Roosmalen 1985a,b). Esto significa que la extinción de A. paniscus equivaldría a una reducción significativa del proceso de dispersión para algunas plantas.
En los bosques de la Reserva de la Biósfera Estación Biológica Beni (EBB), en Bolivia, coexisten el árbol Inga ingoides (Mimosoideae) y el primate A. paniscus. Los frutos de I. ingoides son consumidos por A. paniscus y sus semillas son dispersadas principalmente por este primate en la EBB (I. Guareco, com. pers.). Ateles paniscus ha sido eliminado en algunas regiones de la EBB hace unos 10 años por la cacería de subsistencia, practicada principalmente por pobladores Tsimane y colonos, pero permanece abundante en otras regiones de la misma donde la cacería es ocasional o inexistente (García & Tarifa 1991). La ruptura local de la interacción entre A. paniscus e I. ingoides, proporciona un escenario adecuado para poner a prueba las predicciones expuestas arriba sobre las consecuencias de la pérdida de un dispersor de semilla sobre la demografía de una especie arbórea.
Inga es un género de árboles de flor hermafrodita con 61 especies registradas en Bolivia (Saldias 1993). Inga ingoides alcanza unos 20 m de altura, florece entre octubre y noviembre y fructifica entre diciembre y marzo (obs. pers.). No se conoce su forma de polinización, aunque podría ser similar a otras especies del género Inga, las que son polinizadas principalmente por colibríes y polillas, además de mariposas, abejas y murciélagos (Koptur 1983,1984,Schierenbeck et al. 1997). El 100% (n = 6) de las especies de Inga estudiadas en bosques nublados de Costa Rica son autoincompatibles (Koptur, 1984). Los frutos de Inga son consumidos casi exclusivamente por primates (Charles-Dominique 1993), aunque dos especies de Inga fueron encontradas en heces de Tapirus terrestris en el Parque Noel Kempff Mercado, Santa Cruz, Bolivia (Herrera y Taber 1998). Los frutos de I. ingoides son vainas indehiscentes que alcanzan 25-60 cm de longitud y 1,5-2 cm de ancho y contienen generalmente más de 20 semillas de aproximadamente 1 cm de largo (obs. pers.). En la EBB, sus frutos son consumidos por varias especies de primates (Alouatta seniculus, Cebus apella, Aoutus azarae y Saimiri boliviensis), pero A. paniscus parece ser el único que traga la semilla (referencias locales y obs. pers.). Los frutos que caen al suelo son atacados por coleópteros y patógenos, y las semillas germinadas son depredadas por pecaríes (Tayassu pecari y Pecari tajacu). No se conocen dispersores terrestres en la EBB.
Ateles paniscus es uno de los primates neotropicales de mayor tamaño, alcanzando hasta 9 kg (Symington 1988). Su dieta consiste principalmente de frutos, aunque también ingiere hojas y flores (van Roosmalen 1985b,White 1986). Se mueve en pequeños grupos mixtos de hasta 15 individuos, los cuales son parte de un grupo mayor que ocupa un área de 153-231 ha, con movimientos diarios entre 200 y 4000 m (White 1986,Fedigan et al. 1988,Symington 1988). En la EBB los grupos varían entre 3-26 individuos, que consumen frutos de al menos 26 especies de árboles (F. Méndez, datos no publ.). Se mueven rápidamente por el dosel del bosque y se les ha visto trasladarse a distancias mayores a 1 km (en línea recta), en menos de 5 minutos (obs. pers.). Las tasas reproductivas de Ateles son bajas, con intervalos entre nacimientos de 25-42 meses, luego de una gestación de 7,5 meses, lo cual los hace muy sensibles a las perturbaciones humanas (Eisenberg 1983,Symington 1988). De esta manera, se tiene una especie de dispersor que es rápidamente exterminada por cacería de subsistencia y una especie de árbol que parece depender en gran medida de ese agente para la dispersión de sus semillas.
Las observaciones de campo indican que A. paniscus dispersa las semillas de I. ingoides en agregados. Ateles paniscus produce agregados de semillas a dos escalas: semillas en las deposiciones y agregados de deposiciones en el bosque, esto último por su comportamiento gregario (obs. pers.). Si A. paniscus es el principal dispersor de I. ingoides, su ausencia debería ocasionar que la sombra de semillas se restrinja al área debajo del dosel de los parentales. Dado que las semillas son dispersadas en agregados, esos cambios en distribución y abundancia no deberían afectar la sobrevivencia de las semillas y plántulas (Howe 1989).
En este contexto y bajo el supuesto que A. paniscus es un dispersor “legítimo” (sensuBustamante et al. 1992) de semillas de I. ingoides, es posible explicitar las siguientes hipótesis:
1) En ausencia de A. paniscus, la distribución de semillas y plántulas de I. ingoides debería estar restringida al área debajo de la copa de los árboles, mientras que en presencia de A. paniscus, debería extenderse lejos de los árboles (Fig. 1).
2) De acuerdo a lo propuesto por Howe (1989), la sobrevivencia de semillas y plántulas no debería diferir a distancias cerca y lejos de los árboles parentales, ni entre sitios con y sin presencia de A. paniscus.
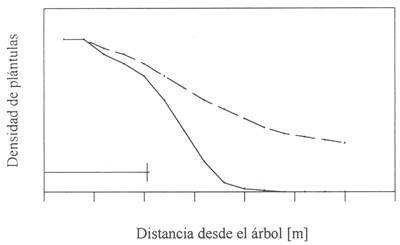
Fig. 1: Distribución hipotética de plántulas de Inga ingoides con respecto a la distancia a los árboles en sitios con presencia (CD = con dispersor) y ausencia (SD = sin dispersor) de su principal dispersor de semillas, Ateles paniscus. La línea por encima del eje correspondiente a distancia desde el árbol representa la media del borde de la copa de los árboles.
Material y métodos
El estudio se basó en experimentos de campo y natura, por comparación de un sitio en que A. paniscus está presente (CD = Con Dispersor) con otro en que fue eliminado por cacería (SD = Sin Dispersor). Todas las observaciones y experimentos se realizaron en ambos sitios.
1. Area de estudio
El estudio se realizó en la Reserva de la Biósfera Estación Biológica Beni (EBB), localizada dentro de las provincias Yacuma y Ballivián, Departamento Beni, Bolivia (14°30’-14°50’S y 66º00’-66º40’ O; Fig. 2). La EBB cubre una superficie de 135.000 ha y está ubicada sobre una llanura aluvial a 210 m snm, la cual sufre inundaciones estacionales que afectan hasta un 70% de su superficie. La vegetación de la EBB es un mosaico de varios tipos de formaciones boscosas que alternan con parches de zonas permanentemente inundadas y sabanas estacionalmente inundables. A la fecha, se han registrado aproximadamente 2.000 especies de plantas vasculares, siendo las familias más importantes Palmae, Moraceae, Leguminosae y Meliaceae (Miranda et al. 1991).
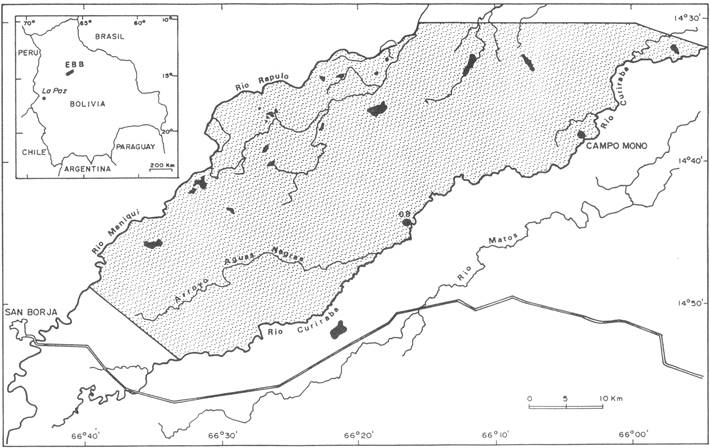
Mapa del área de estudio Estación Biológica Beni (área sombreada). Los sitios de estudio están indicados por círculos negros (08 = Comunidad Chimane, sitio Sin Dispersor; Campo Mono = sitio Con Dispersor).
Los sitios de estudio (Con Dispersor y Sin Dispersor) están separados unos 30 km. El sitio donde A. paniscus fue eliminado por cacería de subsistencia (SD) está situado a unos 2 km al norte del asentamiento Tsimane “08”, ubicado al sureste de la EBB, a orillas del río Curiraba. Este asentamiento fue establecido hace aproximadamente 30 años y A. paniscus está extinto localmente hace unos 10 años (I. Guareco, com. pers.). El otro sitio (CD) fue llamado “Campo Mono” por la frecuente presencia de A. paniscus. La vegetación de ambos sitios corresponde a un bosque tropical aluvial de inundación estacional, que se caracteriza por permanecer inundado tres o cuatro meses al año (Miranda et al. 1991). Sin embargo, en los sitios de estudio ocurre solamente inundación parcial, siendo más bien un bosque de terra firme, alternando con áreas de bajío inundadas durante el período más húmedo (Roldán 1997).
Los bosques presentan un estrato emergente (mayor de 40 m), dos estratos arbóreos (30 y 20 m) y uno arbustivo (5 m). Ambos bosques fueron descritos en detalle por Roldán (1997), cuyos sitios Con Cacería y Sin Cacería corresponden a los sitios SD y CD de este estudio, respectivamente. Ambos bosques son similares florísticamente en la composición de especies arbóreas, siendo las familias más importantes por el número de especies Moraceae, Leguminosae, Meliaceae, Palmae, Rubiaceae y Sapindaceae. Las especies de árboles más abundantes en ambos sitios son Astrocaryum gratum, Rheedia sp., Pseudolmedia laevis, Trichilia sp., Celtis schippii, Virola sebifera y Chamaedorea angustisecta. Inga ingoides tiene densidades medias de adultos de 0,32 ind/100 m2 (ds = 0,60) y 0,35 ind/100 m2 (ds = 0,60) en los sitios SD y CD, respectivamente (Roldán 1997).
Además de A. paniscus, las poblaciones de otras especies de mamíferos grandes presentes en el sitio CD están localmente extintas (T. pecari) o reducidas (P. tajacu, A. seniculus, C. apella, Mazama gouazoubira) en el sitio SD y estas diferencias son atribuidas también a la cacería de subsistencia (Roldán 1997).
2. Viabilidad de las semillas de Inga ingoides dispersadas por Ateles paniscus
Para determinar si A. paniscus defeca semillas viables de I. ingoides, supuesto básico del estudio, se hicieron pruebas de germinación para semillas recolectadas de heces. Para ello se recolectaron frutos en los sitios de estudio y se ofrecieron a un ejemplar cautivo de A. paniscus en la ciudad de La Paz. Cuarenta y cinco semillas recogidas de las heces se pusieron en una cámara de germinación a 30°C y humedad > 90% durante cuatro días, con revisiones diarias para contar las semillas germinadas. Las semillas se consideraron germinadas si los cotiledones estaban separados y la radícula emergiendo más de 1 mm del borde de la semilla.
3. Abundancia y distribución de frutos
Para evaluar la abundancia y distribución de frutos en el suelo se escogieron 20 árboles de I. ingoides (10 en cada sitio) y se hicieron conteos de los frutos (vainas) caídos a lo largo de un transecto de 30 x 1 m, partiendo de la base de cada árbol en una dirección escogida al azar. En cada transecto se evitó pasar cerca (<20 m) de un conespecífico reproductivo. Los conteos se hicieron en marzo de 1997, al final del período de fructificación. La distancia a la cual se encontraron las vainas se midió en intervalos de 1 m. Para el análisis estadístico, las observaciones se agruparon en dos clases de distancia: 0-10 m, correspondiendo al área bajo el dosel y >10 m desde el parental, fuera del dosel. La clase de distancia de 0-10 m fue definida en base al borde del dosel de los árboles (media = 7,7 m; d.e. = 2,2; n = 30). No se consideraron más clases de distancia, dado que sólo se encontró una vaina a más de 20 m del parental (27 m en CD). Para el análisis estadístico se utilizó un Análisis de Varianza (ANDEVA) de dos vías, con densidad de frutos/sección de transecto como variable dependiente (transformada a √x+0,5 para normalizar las variables) y con sitio (CS, SD) y distancia (0-10m, >10m) como factores. Para las comparaciones a posteriori se usó una prueba de Duncan (Ott 1988).
4. Depredación de semillas
Para evaluar si la depredación de semillas es dependiente de la distancia a los árboles, en marzo de 1997 se hicieron experimentos manipulativos para analizar la tasa de granivoría en función de la distancia al árbol parental. Para ello se extrajeron semillas sanas de frutos de I. ingoides y se colocaron en grupos de 30 semillas (simulando deposiciones agregadas) cerca (5 m) y lejos (30 m) de cuatro árboles adultos de I. ingoides por tratamiento en cada sitio. Los árboles focales para los tratamientos de 5 y 30 m fueron los mismos (modificado de Howe et al. 1985,Howe 1990). Las deposiciones simuladas se visitaron una vez al día durante cuatro días. Los datos de los conteos finales se analizaron con una prueba de Kruskal-Wallis (Ott 1988) con distancia (cerca y lejos) y sitio (SD y CD) como tratamientos y el número de semillas sobrevivientes como la variable dependiente. Para las comparaciones a posteriori se usó una prueba “tipo Tukey” no paramétrica (Zar 1984:199).
5. Abundancia y distribución de plántulas
La abundancia de plántulas se evaluó por conteos, que se realizaron en transectos de 30 x 1 m, partiendo en una dirección al azar desde la base de un adulto reproductivo, pero evitando pasar a menos de 20 m de otro adulto reproductivo. Los conteos se hicieron en marzo de 1996 y marzo de 1997. Sólo se consideraron las plántulas menores de 1 año, menores a 20 cm de altura o sin desarrollo de corteza. Las plántulas se contaron en intervalos de 1 m, pero para el análisis estadístico las observaciones se agruparon en tres clases de distancia: cerca (< 10 m), mediana distancia (10 - 20 m) y lejos (20 - 30 m). La clase “cerca” incluye las distancias debajo de la copa de los árboles, la clase “lejos” representa las distancias que las semillas alcanzarían sólo con la participación de un agente de dispersión distinto a la gravedad. No se consideraron distancias mayores por la dificultad de evitar el ingreso a la influencia de la sombra de semillas de otro árbol. El análisis estadístico se realizó con un ANDEVA de dos vías, con el número de plántulas/transecto (para cada clase de distancia) como variable dependiente (transformada con √x+0,5), con sitio (SD y CD) y distancia (cerca, mediana, lejos) como factores. Las comparaciones a posteriori se hicieron con una prueba de Duncan (Ott 1988).
Para evaluar las diferencias en la distribución de plántulas entre sitios Con y Sin Dispersor, se graficó la proporción de transectos (del total realizado para cada sitio) en que se encontraron plántulas de I. ingoides para las tres clases de distancia antes mencionadas. La frecuencia de transectos con plántulas lejos (20 - 30 m) de los árboles se comparó entre sitios con una Prueba Exacta de Fisher (Zar 1984).
6. Sobrevivencia de plántulas
Para evaluar si la sobrevivencia es independiente de la distancia de la plántula al adulto más próximo y comparar la sobrevivencia de plántulas entre sitios, se procedió de la siguiente forma: en marzo de 1996, se marcaron todas las plántulas encontradas en un transecto de 30 x 1 m partiendo de dos árboles en el sitio CD y cuatro árboles en el sitio SD (Tabla 1). El seguimiento de esas plántulas (cohorte I) se hizo mensualmente hasta junio de ese año, con un muestreo final en noviembre de 1996. Durante el censo de abril, se marcaron todas las plántulas de semillas germinadas en ese período (cohorte II) y éstas se siguieron como una cohorte independiente de la marcada en marzo.
Tabla 1: Número inicial de plántulas marcadas en cada transecto y cada cohorte.
| Cohorte | CD1 | CD2 | SD1 | SD2 | SD3 | SD4 |
|---|---|---|---|---|---|---|
| I | 45 | 98 | 16 | 26 | 18 | 21 |
| II | 24 | 17 | 22 | 23 | 2 | 9 |
CD indica los transectos del sitio Con Dispersor y SD los transectos del sitio Sin Dispersor. Cohorte I son aquellas plántulas marcadas al inicio del período de muestreo (marzo 1996) y que se supone son menores de 1 año, Cohorte II incluye las plántulas marcadas durante el primer censo de plántulas marcadas (abril 1996) y que tienen menos de 1 mes de edad. Las cohortes del transecto CD1 no se visitaron en el mes de noviembre de 1996, cuando se hizo el censo final para el resto de las plántulas marcadas en ambos sitios, sino en marzo de 1997.
Uno de los transectos en el sitio CD (CD1) no pudo ser visitado durante el censo final de noviembre y las plántulas marcadas del mismo pudieron ser recontadas sólo en marzo de 1997. Esto impidió considerar ambos transectos del sitio CD para la comparación entre sitios y ésta se hizo con las plántulas de los cuatro transectos del sitio SD versus las plántulas del transecto CD2. Sin embargo, el seguimiento del transecto CD1 hasta marzo permitió obtener datos de 11 y 12 meses para la sobrevivencia de las plántulas de las cohortes II y I respectivamente, marcadas en ese transecto. Con las observaciones de cada cohorte por separado y juntando las observaciones de todos los transectos de cada sitio se hizo el siguiente análisis. La distancia de cada plántula a la base del árbol del cual partía el transecto se correlacionó (correlación por rangos de Spearman) con el tiempo que sobrevivió dicha plántula. Una correlación positiva indicaría que a mayor distancia de la plántula al árbol adulto conespecífico más próximo, la probabilidad de sobrevivencia es mayor. Este análisis se hizo primero considerando la sobrevivencia hasta el mes de junio (todos los transectos para ambos sitios), luego considerando la sobrevivencia hasta el mes de noviembre (CD2 y todos los transectos para el sitio SD) y finalmente hasta el mes de marzo para el transecto CD1. De esta manera se obtuvo información sobre la sobrevivencia a corto plazo (marzo y abril hasta junio, cohortes I y II respectivamente) para plántulas en dos transectos en el sitio CD y cuatro transectos en el sitio SD, información de sobrevivencia para ocho y siete meses (cohortes I y II) con un transecto en el sitio CD y cuatro en el sitio SD y, finalmente, información de sobrevivencia de doce y once meses para las plántulas de las cohortes I y II del transecto CD1.
El tiempo de sobrevivencia (días) utilizado para los análisis debe entenderse como un intervalo y no como el tiempo exacto que sobrevivieron las plántulas. Aquellas plántulas que no sobrevivieron al primer censo se les asignó sobrevivencia de cero días, pero esto no significa que murieron inmediatamente después de marcadas.
La comparación entre sitios se realizó con las curvas de sobrevivencia para el total de las plántulas de cada sitio, independientemente de la distancia al árbol adulto. Esta comparación se hizo con las observaciones de sobrevivencia hasta el mes de noviembre en los transectos CD2 en el sitio CD versus las observaciones de todos los transectos en el sitio SD, y para ambas cohortes. Las curvas de sobrevivencia se compararon con la prueba de logrank de Peto y Peto (Pyke y Thompson 1986,Hutchings et al. 1991).
La metodología anterior entregó datos para un tiempo relativamente largo, pero con un bajo número de árboles por sitio, lo cual hizo necesario apoyar los datos con un número mayor de transectos para obtener información menos afectada por posibles eventos particulares a un transecto (Howe 1993a). En noviembre de 1996 se marcaron entre 21 y 30 plántulas en 10 transectos para cada sitio, con un total de 300 plántulas marcadas en el sitio CD y 275 en el sitio SD. Todas las plántulas marcadas correspondían al reclutamiento de marzo-mayo de ese año. En lo posible, se marcaron plántulas repartidas equitativamente a lo largo de los 30 m del transecto. La menor densidad de plántulas en el sitio SD, especialmente a distancias mayores a 10 m del adulto, obligó a marcar plántulas fuera del transecto de 30 x 1 m, ampliándose en ocasiones hasta 8 m de ancho. Las plántulas se censaron en tres oportunidades (enero, marzo y abril) a lo largo de un período de 136 días. Las observaciones se sometieron al mismo tipo de análisis que las marcadas anteriormente, pero en esta ocasión se consideraron todos los transectos de cada sitio para todos los análisis.
Resultados
1. Viabilidad de las semillas de Inga ingoides dispersadas por Ateles paniscus
Las primeras semillas aparecieron en las heces de A. paniscus aproximadamente a las 4 horas desde que el ejemplar consumió el alimento y continuaron apareciendo hasta 18 horas después. Las primeras semillas germinaron al segundo día de colocadas en la cámara de germinación. A los cuatro días, 49% (22/45) de las semillas habían germinado, lo cual demuestra que A. paniscus es un legítimo dispersor de semillas de I. ingoides.
Al momento de ofrecer frutos a A. paniscus, se hizo lo mismo con un individuo de A. seniculus y dos individuos de C. apella. Alouatta seniculus no consumió el fruto; los C. apella sí lo hicieron, pero escupían la semilla en lugar de tragarla, lo cual sugiere que ellos no son agentes de dispersión de I. ingoides por endozoocoria.
2. Abundancia y distribución de frutos en el suelo
Los frutos se restringen a las cercanías del borde del dosel de los árboles (Fig. 3). Agrupando las observaciones por clases de distancia al árbol, la densidad de frutos difirió con la distancia (< 10 y > 10 m) a los árboles (ANDEVA, F1,36 = 7,6; P < 0,01), pero no entre sitios (F1,36 = 0,61; P > 0,43). La interacción entre los factores no fue significativa (F1,36 = 0,01; P > 0,9). Las densidades de vainas por transecto fueron mayores cerca del árbol para ambos sitios (46,6 ± 16,99 vainas/transecto versus 14,2 ± 13,87 en el sitio CD y 38,5 ± 10,68 versus 3,1 ± 2,56 en el sitio SD; Duncan, (α = 0,05).
3. Depredación de semillas
La depredación de semillas en las deposiciones experimentales no difirió con la distancia de la deposición al adulto más próximo de I. ingoides en ninguno de los dos sitios; no obstante, fue mayor en el sitio CD que en el sitio SD para ambas distancias. El 0 ± 0 % y 25 ± 22 % de las semillas sobrevivieron a la depredación en el sitio CD a distancias cerca y lejos de los adultos respectivamente, mientras que el 100 ± 0 % y 98 ± 1 % de las semillas sobrevivieron en las deposiciones en el sitio SD (Kruskal-Wallis H = 11,14; P < 0,02 y prueba a posteriori “tipo Tukey” no paramétrica, (α = 0,05).
En las deposiciones experimentales de semillas se encontraron larvas y adultos de Coleoptera, presumiblemente de la misma especie. En estos casos, las semillas depredadas estaban total o parcialmente destruidas (reducidas a un polvillo). También se observaron hormigas (Atta sp.) llevándose las semillas a su guarida. Los pobladores Tsimane indican que los pecaríes (T. pecari y P. tajacu) comen las semillas y los cotiledones que encuentran al hozar las plántulas jóvenes. Todos estos animales actuarían como depredadores de las semillas de I. ingoides.
4. Abundancia y distribución de plántulas
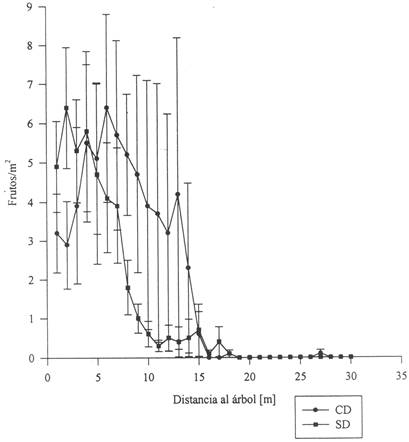
La densidad de plántulas difirió de un año al otro en ambos sitios, aunque la densidad fue mayor en el sitio CD que en SD para ambos años (Fig. 4). En 1996, la densidad de plántulas fue cinco veces mayor cerca (< 10 m) que lejos (> 20 m) de los árboles en CD y 17 veces mayor cerca que lejos en SD. En total, las plántulas fueron 3,6 veces más abundantes en el sitio CD que en SD en 1996. Un ANDEVA de dos vías mostró que tanto el efecto distancia (F2,51 = 22,8; P < 0,001) como el efecto sitio (F1,51 = 26,4; P < 0,001) resultaron significativos (la interacción entre factores no fue significativa, F2,51 = 0,7; P > 0,19).
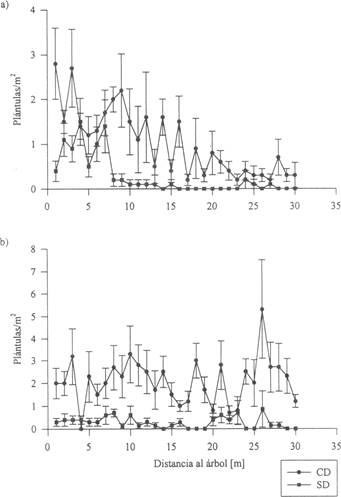
Fig. 4: Abundancia de plántulas de I. ingoides (Media ± EE) con respecto a distancia al árbol más próximo. CD = Con Dispersor, SD = Sin Dispersor. a) 1996 (10 transectos en CD y 9 en SD), b) 1997 (6 transectos en CD y 7 en SD).
La densidad de plántulas difirió entre todos los tratamientos para 1996. Es decir, la densidad de plántulas es mayor en CD a todas las distancias desde el parental, y la densidad fue mayor cerca a los adultos en ambos sitios en 1996 (prueba de Duncan, (α = 0,05). En 1997, la densidad de plántulas fue nueve veces mayor en el sitio CD que en SD, con un efecto significativo del factor sitio (F1,33 = 53,0; P < 0,001), de manera similar a lo encontrado para 1996. Sin embargo, las densidades de plántulas no difirieron dentro de cada sitio en función a la distancia al parental (F2,33 =0,8; P > 0,45; Fig. 4b). La interacción entre ambos factores no fue significativa (F2,33=0,2; P > 0,84).
La distribución de plántulas difirió entre los sitios para ambos años (Fig. 5). La frecuencia de transectos en que se encontraron plántulas lejos del adulto focal (20-30m) fue significativamente mayor en CD que en SD para ambos años (90% versus 20% para 1996 y 100% versus 40% para 1997, Prueba exacta de Fisher P< 0,01 y P<0,05 para 1996 y 1997 respectivamente). Entonces, las plántulas de I. ingoides no fueron sólo más abundantes en el sitio CD, sino que se las encontró más frecuentemente lejos de los árboles adultos en presencia de su dispersor A. paniscus.
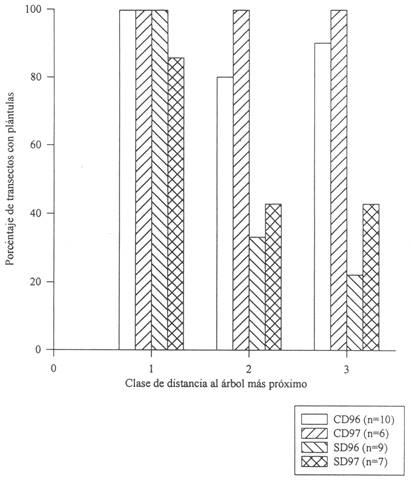
Fig. 5: Porcentaje de transectos con plántulas de I. ingoides en cada clase de distancia al árbol más próximo. 1=0-10m,2 = 10-20m,3 = 20-30m. Resto leyenda como enFig 4.
5. Sobrevivencia de plántulas
En general, existe una tendencia al aumento de la sobrevivencia con la distancia de la plántula al árbol mas próximo de I. ingoides para ambos muéstreos, aunque esta tendencia fue significativa sólo para el transecto CD1 del primer muestreo (Tabla 2, Fig. 6). También se observó un aumento consistente en esa tendencia (medida por un aumento en el valor de rs) con el tiempo; con excepción del muestreo realizado para la cohorte II del transecto CD2, el resto de los análisis con la sobrevivencia hasta junio y luego hasta noviembre (SD1 - SD4) y marzo (CD1) mostraron un incremento en el rS (mayor tendencia a que la sobrevivencia de plántulas sea mayor lejos de los árboles conespecíficos), para ambas cohortes (Tabla 2). Esto sugiere que la tendencia a un aumento en la sobrevivencia para las plántulas que crecen alejadas de los adultos se haría más importante a medida que pasa el tiempo. No se hizo un análisis como éste con las observaciones del segundo muestreo, por abarcar un período más corto.
Tabla 2: Correlación entre la distancia de las plántulas al árbol más próximo y el tiempo de sobrevivencia.
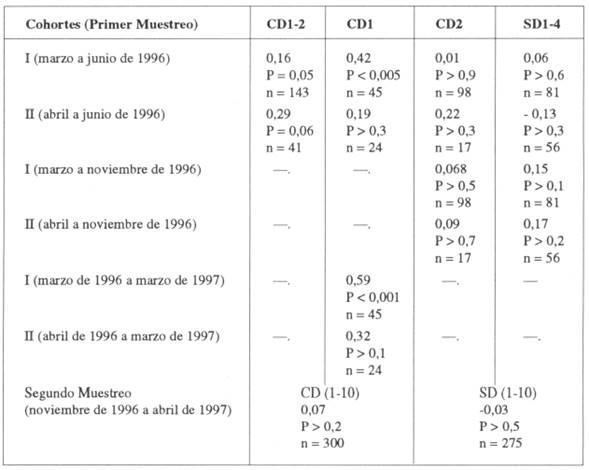
CD = sitio Con Dispersor, SD = sitio Sin Dispersor. Los números indican el transecto considerado, los guiones indican agrupación de las observaciones de los transectos señalados. Los datos son coeficientes de correlación de Spearman (rs), “P* es la probabilidad de que el rs sea distinto de cero y “n” es el número de plántulas consideradas para el análisis. Las cohortes son grupos de plántulas marcadas en distinto instante de tiempo y entre paréntesis se indica el período de muestreo.
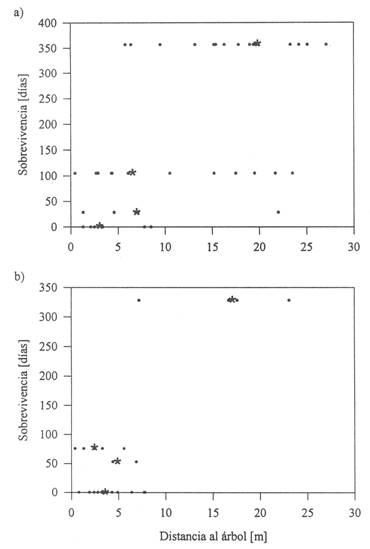
Fig. 6: Sobrevivencia de plántulas en función a su distancia al adulto más próximo (transecto CD1). a) Cohorte I, rs=0,59; n=45; P<0,001. b) Cohorte II, rs=0,32; n=24; P>0,1. Cada punto es una plántula. * son medianas por intervalo de tiempo.
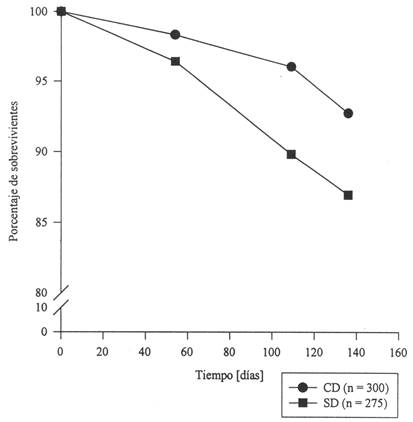
Finalmente, la sobrevivencia de plántulas, independientemente de su distancia al árbol más próximo, fue mayor en el sitio SD para ambas cohortes del primer muestreo, aunque significativamente sólo para la cohorte I (logrank X2 = 6,3; g.l. = 1; P < 0,025 y X2 = 1,9; g.l. = 1; P > 0,1 para las cohortes I y II respectivamente; Fig. 7). En el segundo muestreo la sobrevivencia fue mayor en el sitio CD (X2 = 5,2; g.l. = 1; P < 0,025; Fig. 8).
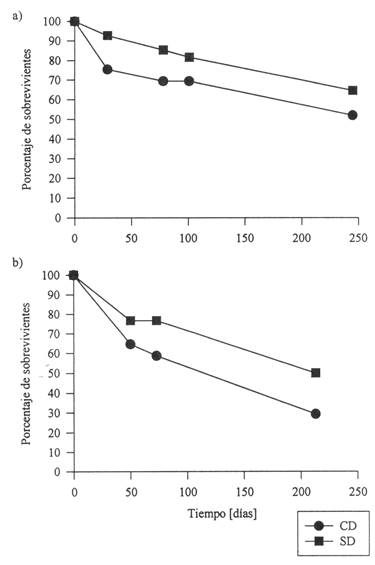
Fig. 7: Sobrevivencia de plántulas en dos sitios de la EBB, independientemente de su distancia al árbol más próximo. CD = Con Dispersor, SD = Sin Dispersor. a) Cohortes I, marzo a noviembre 1996; n = 98 (CD) y n = 81 (SD). Logrank X 2 = 6,3; P < 0,025; b) Cohortes II, abril a noviembre de 1996; n = 17 (CD) y n = 56 (SD). Logrank X 2 = 1,9; P > 0,1.
Discusión
Ateles paniscus defeca semillas viables de I. ingoides, con lo cual el supuesto básico que A. paniscus es un dispersor legítimo es sustentado por la evidencia empírica. Por otra parte, los otros primates presentes en la zona de estudio parecen no ser importantes como dispersores de I. ingoides. Entre ellos, Alouatta no es un frugívoro especialista (Estrada y Coates-Estrada 1993) y su efecto, si existe, sería mínimo; mientras que C. apella y los otros primates más pequeños parecen ser incapaces de tragar las semillas de I. ingoides (obs. pers.). El efecto de estas especies como dispersores de I. ingoides podría estar restringido al transporte de frutos y desecho de semillas a distancias cortas desde los parentales. Por tanto, el potencial de los primates de la EBB como dispersores de I. ingoides recaería principalmente en A. paniscus. Por ello, razonablemente se puede suponer que las diferencias en los procesos estudiados se deben principalmente a la ausencia de A. paniscus en el sitio SD, suponiendo todo lo demás constante (condición ceteris paribus).
La dispersión de semillas de I. ingoides lejos del parental parece no liberarlas de la acción de los depredadores, ya que la tasa de depredación no difiere con la distancia a los árboles. Avispas y coleópteros son conocidos como depredadores de semillas de Inga (Koptur 1984), ambos grupos de gran movilidad y autonomía, lo cual podría facilitarles el encuentro de las semillas. Observaciones de campo no cuantificadas indican que las semillas tardan semanas en germinar si no son liberadas del fruto. Koptur (1984) también encontró que las semillas de otras especies de Inga germinan casi inmediatamente después que son liberadas de la vaina. Esto implica que las semillas que quedan dentro del fruto permanecen más tiempo expuestas a la acción de los depredadores y patógenos, abundantes en los frutos debajo de los parentales. Entonces, al ingerir las semillas y defecarlas en pocas horas, A. paniscus actuaría disminuyendo el tiempo que las semillas están expuestas a los depredadores y de esa manera podría tener un efecto positivo en la cantidad de semillas germinadas. Sin embargo, este efecto sería producido también por cualquier otro de los primates que consumen I. ingoides, aún cuando no traguen ni dispersen la semilla.
El patrón de depredación de semillas corresponde al propuesto por Howe (1989), en sentido que las semillas dispersadas en agregados serían tolerantes a los factores de mortalidad dependientes de la distancia a los árboles parentales. La rapidez con que ocurre la depredación de semillas puede explicar el que los depredadores no actúen en función a la distancia. En el caso de las hormigas (Atta sp.) esto es claro por la gran movilidad de estos insectos y su amplio rango de acción (obs. pers.). En el caso de los coleópteros, hay que suponer que también son capaces de encontrar las semillas en el bosque rápidamente. Finalmente, los vertebrados que son conocidos depredadores de semillas de I. ingoides, están reducidos (P. tajacu) o ausentes (T. pecari) en el sitio SD (Roldán 1997), lo cual podría explicar la mayor depredación de semillas en el sitio CD con respecto al sitio SD. Los sitios libres de depredadores de semillas son generalmente raros e impredecibles en espacio y tiempo (Whelan et al. 1991); sin embargo, las altas tasas de depredación de semillas en condiciones experimentales en el sitio CD no conducen a una menor densidad de plántulas en ese sitio; al contrario, las plántulas son menos abundantes en el sitio SD.
De acuerdo a lo propuesto originalmente, las plántulas fueron menos abundantes y estuvieron mayormente restringidas a las cercanías de los árboles en el sitio donde A. paniscus fue eliminado por la cacería de subsistencia. La menor abundancia de plántulas en el sitio SD podría ser atribuida a la ausencia de A. paniscus, por cuanto además de dispersar, tendría un efecto positivo sobre la tasa de germinación al liberar las semillas de la vaina, y con ello reduciría la mortalidad por depredación. El efecto positivo de A. paniscus en la abundancia de plántulas de las especies que consume también ha sido propuesto para otras dos especies arbóreas en la EBB (I. nobilis y Ampelocera ruizii), cuyas plántulas son más abundantes en el sitio CD, a pesar que la densidad de árboles adultos no difiere entre los sitios, al igual que el caso de I. ingoides (Roldán 1997). En Santa Rosa, Costa Rica, Chapman (1989) estimó que más de 300 semillas grandes por hectárea de bosque por semana caen al suelo como producto de las heces de primates. La ausencia de un aporte de esta magnitud por A. paniscus podría estar determinando las diferencias en la abundancia de plántulas de I. ingoides en SD.
Las inundaciones estacionales que afectan gran parte de la superficie de la EBB no afectan los sitios de estudio, con excepción de depresiones del terreno o “bajíos”. El bosque entero se inunda ocasionalmente, pero la distribución de los frutos en el suelo, restringida a las zonas cercanas a los árboles, sugiere que la dispersión secundaria por agua debe ser insignificante.
Las semillas de I. ingoides llegan eventualmente lejos (30 m ó más) de los parentales en ausencia de A. paniscus, pero tanto la densidad de plántulas como la frecuencia con que se las encuentra lejos de los adultos conespecíficos es significativamente mayor cuando A. paniscus está presente. Es importante recalcar que la distancia de 30 m no representa el máximo que alcanzan las semillas dispersadas por A. paniscus; los movimientos de estos sobrepasan los 1.000 m/día (Symington 1988, obs. pers.), mientras que el paso por el tracto digestivo de este primate tarda varias horas (Milton 1980 en White 1986, obs. pers.), lo cual implica que las semillas de I. ingoides pueden ser dispersadas a gran distancia y constituir una importante vía de flujo génico (Pacheco 1997).
Contrariamente a lo esperado, en sentido que la sobrevivencia de plántulas sería similar con respecto a la distancia a los árboles, la sobrevivencia de plántulas aumentaría lejos de los adultos. Si bien la dispersión por A. paniscus no es la única forma para las semillas de llegar lejos de los árboles, la probabilidad de hacerlo se reduce significativamente en ausencia de ese dispersor. Por tanto, en ausencia del A. paniscus, una mayor proporción de semillas germinaría cerca a los parentales, donde la sobrevivencia como plántulas podría ser menor en comparación a las que germinaron lejos. Sin embargo, el probable aumento en la mortalidad de plántulas cerca a los parentales no significa que el reclutamiento cerca a los conespecíficos no sea posible en I. ingoides. De hecho, existen individuos adultos muy cerca uno del otro (2-3 m), lo cual corresponde más al patrón propuesto por Hubbell (1980) que al de Janzen (1970). La minoría de las especies de árboles (n = 80) estudiadas por Condit et al. (1992) muestran reducción en el reclutamiento cerca a los adultos, por lo que ellos postulan que la mayoría de las especies no estarían reguladas por efectos de la distancia al parental sobre el reclutamiento.
Dado que el efecto distancia en la sobrevivencia de plántulas fue significativo sólo en un transecto (aunque la tendencia fue general), es posible que la mayor sobrevivencia de plántulas lejos del parental en el transecto CD1 se deba a un efecto del vecindario de ese transecto en particular. Howe (1993b) indica que luego del establecimiento de plántulas de Virola surinamensis (> 12 semanas), es más fuerte el efecto del vecindario que el de la distancia al parental. Posiblemente la mayor mortalidad cerca al adulto más próximo en el transecto CD1 se deba a efectos del ambiente particular y no a un efecto distancia. La susceptibilidad al ataque de herbívoros, por ejemplo, es influenciada por el ambiente (luz, nutrientes y ataques previos de herbivoría; Marquis y Braker 1994). La existencia de palmeras pequeñas y otras especies de sotobosque disminuye la sobrevivencia y crecimiento de plántulas de dos especies de Inga en Costa Rica, en relación a sitios en que las plántulas están libres de ese efecto (Denslow et al. 1991). Por tanto, la evidencia presentada aquí sobre un efecto positivo directo de la dispersión de semillas en el reclutamiento de I. ingoides (aumento en la sobrevivencia de las plántulas que son alejadas de los parentales) no es concluyente.
Las diferencias en sobrevivencia de plántulas de I. ingoides entre sitios son aún más complejas de explicar. La mayor sobrevivencia en el sitio SD para el primer muestreo podría ser ocasionada por la reducción o ausencia de otros mamíferos grandes en ese sitio (Roldán 1997). Sin embargo, la reducción de estas especies no explicaría por sí sola el cambio en la sobrevivencia de plántulas entre sitios. No tenemos explicación para ese resultado.
En resumen, las semillas de I. ingoides son dispersadas viables por A. paniscus y, si bien el alejamiento de las semillas del parental no disminuye la depredación de las mismas directamente, las observaciones no cuantificadas sugieren que las semillas liberadas del fruto germinan más rápidamente, lo cual disminuiría el tiempo que las semillas están expuestas a depredación. La ausencia de A. paniscus disminuye la cantidad de semillas que germinan lejos de los paren tales y ocasiona también una disminución en la densidad total de plántulas de I. ingoides en el suelo del bosque. Además, el germinar lejos de los adultos podría representar una ventaja adicional para la sobrevivencia de las plántulas. Por tanto, la ausencia de A. paniscus podría afectar la demografía de I. ingoides, produciendo poblaciones menos densas y más agregadas en el largo plazo. Es decir, la mayoría de las semillas germinarían cerca los parentales y probablemente en menor número. El reclutamiento lejos de los parentales disminuiría produciendo áreas con menor densidad de árboles y el reemplazo de individuos se produciría principalmente cerca a los ya establecidos.
Es posible especular sobre los efectos de la pérdida del dispersor en la selección fenotípica a nivel de frutos de I. ingoides. Si el sistema A. paniscus-I. ingoides funciona de manera similar al estudiado por Wheelwright (1993), en que las aves dispersoras de Ocotea tenera escogen los frutos de mayor tamaño, Ateles tendería a escoger las vainas de mayor tamaño y con más pulpa. Si estas vainas obtienen ventaja selectiva de la presión del dispersor (son consumidas con preferencia) y existe heredabilidad en los caracteres (grande y mucha pulpa), la cual fue encontrada por Wheelwright en 0. tenera, la ausencia del dispersor produciría diferencias en las frecuencias de fenotipos de frutos. Suponiendo que las semillas dispersadas tienen ventaja sobre las no dispersadas, la ausencia del dispersor eliminaría esa ventaja a las semillas en frutos grandes y con mucha pulpa. Por último, es posible que el mayor tamaño y cantidad de pulpa del fruto sean una desventaja para la germinación de las semillas dentro del fruto. De esta manera, podría esperarse que la selección favorezca una reducción en el tamaño y cantidad de pulpa de los frutos en las poblaciones sin dispersor. Esto si las condiciones de ausencia del dispersor persisten por varias generaciones y no existe compensación por otros frugívoros.
Dado que las poblaciones de primates neotropicales de gran tamaño, como Ateles, tienen poco potencial para recuperarse rápidamente de las perturbaciones (Robinson y Ramírez 1982,Symington 1988,Eisenberg 1983,Peres 1990) y las poblaciones humanas en la EBB tienden a crecer (junto con sus demandas de caza), la probabilidad que el efecto de la extinción local de A. paniscus persista y se extienda en el área es muy grande. Este problema no se da sólo en la EBB, la cacería de subsistencia ha afectado también las poblaciones de primates de gran tamaño y otros mamíferos en otras regiones del Neotrópico (Peres 1990,Encarnación et al. 1993,Bodmer et al. 1997).
Los efectos de la ausencia (o reducción de la población) del dispersor de semillas podrían extenderse a otras especies de plantas. Ateles paniscus consume frutos de al menos 26 especies de árboles en la EBB (F. Méndez, datos no publicados) y este primate es considerado dispersor exclusivo de al menos 11 especies en Surinam (van Roosmalen 1985a,b). En general, si la defaunación tiende a incrementarse otras especies de animales pueden desaparecer local o totalmente. Si pensamos en que cerca a 90% de las especies de bosque maduro son dispersadas por animales (van Roosmalen 1985a,b), es fácil imaginar que la estructura del bosque Neotropical puede cambiar enormemente. Es decir, la cacería de subsistencia practicada por los pobladores rurales no sólo afecta directamente las poblaciones animales, sino que sus efectos indirectos pueden evidenciarse en los patrones de abundancia y distribución espacial de las especies vegetales, como se comprobó para I. ingoides por la extinción de su principal dispersor de semillas, A. paniscus.












 uBio
uBio