Antecedentes
La Reserva Nacional de Fauna Andina Eduardo Avaroa, ubicada en el extremo sur-oeste de Bolivia, es un área protegida que forma parte del Sistema Nacional de Areas Protegidas (SNAP). La Reserva se distingue por ser una de las áreas protegidas altoandinas con una base de información relativamente buena, especialmente sobre aves (Rocha y Quiroga, 1996a).
El grupo más estudiado son los flamencos y existen trabajos sobre la ecología de flamencos en Laguna Colorada y Laguna Verde (Johnson et al., 1958;Peña, 1961;Johnson, 1965). Otros trabajos sobre población y distribución de flamencos fueron realizados por Hurlbert (1978,1981,1982) y,Hurlbert y Keith (1979). Trabajos sobre ornitolimnología, con énfasis en la alimentación de flamencos fueron realizados por Patrick (1961),Hurlbert (1982),Hurlbert y Chang (1983). Estudios sobre aspectos de ecología y conservación de flamencos fueron realizados por Campos (1987,1990),Maier et al. (1993)yRocha (1994,1995).
El trabajo de diagnóstico realizado por el Instituto de Ecología, Museo Nacional de Historia Natural y Centro de Estudios Ecológicos y de Desarrollo Integral (1990), contiene información básica sobre el área y alguna información sobre reptiles, anfibios y peces. Existe un trabajo que describe una nueva especie de anfibio de la región para Bolivia (Lavilla y Ergueta, 1995).
Es notable la ausencia de estudios ecológicos y de monitoreo sobre las especies de la Reserva, aunque durante el año 1997 se ha llevado a cabo el Primer Censo Simultáneo Internacional de los Flamencos Phoenicoparrus jamesi y P. andinus en Argentina, Bolivia, Chile y Perú, realizado del 23 al 30 de enero de 1997. Desde el presente año, se realiza el monitoreo de las poblaciones de flamencos en el altiplano de Bolivia (Rocha, no publ.)
Actualmente se desarrolla el Plan de Manejo de la Reserva, instrumento que permitirá una redefinición de límites y objetivos, además de establecer normas, zonificación y programas de manejo para una de las áreas protegidas más importantes de Bolivia.
Area de estudio
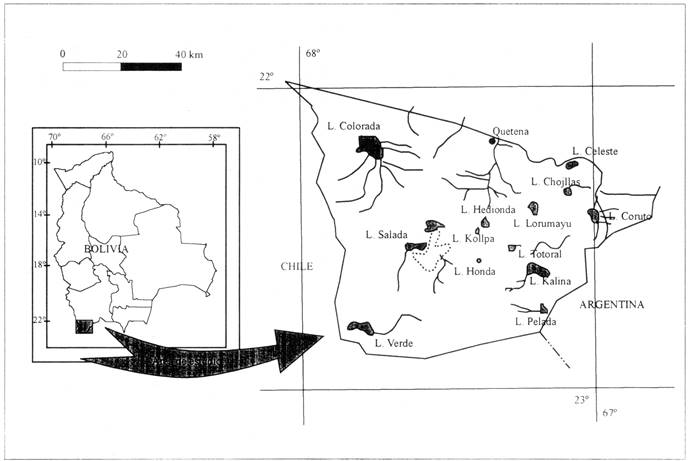
La Reserva Nacional de Fauna Andina Eduardo Avaroa se encuentra en la provincia Sud Lípez del Departamento de Potosí, y limita al oeste con la República de Chile y al sur-este con la República Argentina (Figura 1). Fue creada en 1981 con el objetivo de proteger las aves que habitan Laguna Colorada, otras especies de fauna andina y también para controlar y suprimir la actividad de caza furtiva (Ergueta y Gómez, 1997).
Con una superficie aproximada de 714.745 ha, pertenece a la Cordillera Occidental o volcánica, encontrándose en alturas que oscilan entre los 4200 y 6000 m snm. Las precipitaciones son escasas y no superan los 100 mm anuales, mientras que la temperatura puede llegar a -25° C en el invierno.
La vegetación del área pertenece al semidesierto altoandino (Ribera et al., 1996). La vegetación predominante es el pastizal abierto de Festuca ortophylla, Stipa figida, Senecio algens y Pycnophyllum tetrastichum, se encuentran hasta los 4800 m snm (García e Hinojosa, 1990). Existen pequeñas áreas con matorrales formados por Adesmia, Baccharis y Parastrephia y Polylepis tomentella (queñua) que se encuentra en zonas rocosas asociada a Azorella compacta (yareta). La zona de bofedales es pequeña y asociada a los ríos de mayor tamaño.
La población que vive en la Reserva es de origen quechua, con una densidad que no supera a los 0,1 habitantes por km2, siendo su principal actividad la cría de llamas. La agricultura es una actividad marginal, debido a las condiciones climáticas extremas (Ergueta y Gómez, 1997).
De acuerdo con Ergueta y Gómez (1997), la fauna de la Reserva está sometida a presiones, como la recolección de huevos de flamencos, suri y soca cornuda, que aún se practica en algunos sectores de la Reserva y la actividad minera no regulada, dirigida a la producción de ácido bórico, ulexita y azufre, que causaría contaminación a los cuerpos de agua y suelos; la posible implementación de un proyecto para la generación de energía geotérmica en Laguna Colorada y el fuerte impacto que ocasiona el turismo masivo no planificado, son amenazas de gran impacto para la Reserva.
Metodología
El presente artículo es producto del trabajo realizado por el equipo de fauna (los autores) que participan en el Plan de Manejo de la Reserva Nacional de Fauna Andina Eduardo Avaroa, licitado por la Dirección Nacional de Conservación de la Biodiversidad y ejecutado por el consorcio Centro de Datos para la Conservación (ahora TRÓPICO - Asociación Boliviana para la Conservación) y Swedforest International.
Para el trabajo los autores han realizado una recopilación bibliográfica intensa. El trabajo de campo se realizó en marzo de 1997 y comprendió la colecta de peces, anfibios y reptiles; censos y observaciones de flamencos adultos, juveniles y nidos; censo puntual y estimación de densidad de vizcachas por el método “trapping web” (Greenwood, J. 1996); además de la recopilación de datos de uso y amenazas sobre la fauna a través de conversaciones con las comunidades locales y cuerpo de guardaparques.
Se comparó la diversidad de vertebrados de la Reserva, con dos áreas protegidas bolivianas con ecosistemas andinos; la Reserva Nacional de Fauna Ulla Ulla (RFU, (69°25’ - 69°00’ O,14°40’ - 15° 15’ S) y el Parque Nacional Sajama (PNS, 68°40’- 69°10’ O, 17°55’- 18°15’ S). Los datos de ambas áreas protegidas fueron proporcionados por la Dirección Nacional de Conservación de la Biodiversidad en los documentos de Planes de Manejo, que actualmente se encuentran en elaboración.
También se compara la diversidad con un área de estudio en el altiplano central conocida como Huaraco (HU, 17°22’ S, 67°38’ O) (Morales, 1994). La comparación se realizó a través del índice de Sorenssen (Krebs, 1985).
Para el presente artículo se ha utilizado la información generada por el I Censo Internacional de Flamencos (Rocha y Quiroga, 1997), y los datos de varios años de trabajo sobre los flamencos de la Reserva de Omar Rocha.
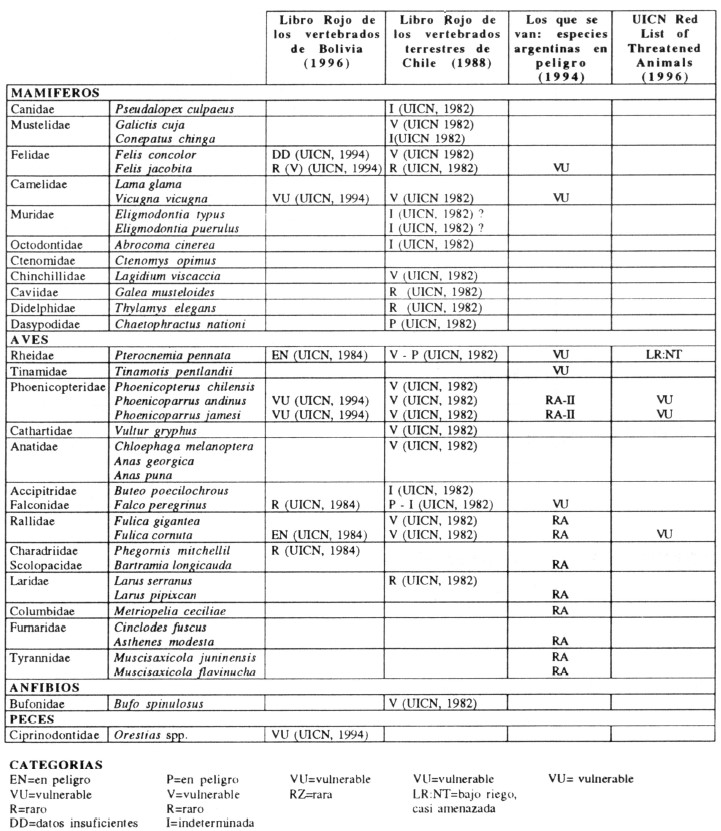
Las especies prioritarias para la conservación de la Reserva se analizan de acuerdo a dos métodos, el primero es una comparación entre el “Libro Rojo de los Vertebrados de Bolivia” (Ergueta y Morales, 1996), el “Libro Rojo de los Vertebrados Terrestres de Chile” (Glade, 1993) y “Los que se van, especies argentinas en peligro” (Chebez, 1994), que permitió elaborar una lista y asignar la categoría de conservación que corresponde a las especies de la Reserva en el ámbito nacional y regional.
El segundo método de análisis, se basa en la propuesta metodológica de Úbeda et al. (1994), quienes desarrollaron un índice para analizar el estado de conservación de la mastofauna del Parque y Reserva Nacional Nahuel Huapi (en Argentina), el mismo que es aplicado para algunas especies de la fauna de mamíferos y aves de la Reserva.
Según el método de Úbeda et al. (1994) las especies son calificadas con un índice (SUMIN) compuesto de 12 variables relevantes para su sobrevivencia o su conservación:
• Distribución continental (DICON)
• Distribución nacional (DINAC)
• Amplitud en el uso del hábitat (AUHA)
• Amplitud en el uso del espacio vertical (AUEVE)
• Tamaño corporal (TAM)
• Potencial reproductivo (POTRE)
• Amplitud trófica (AMTRO)
• Abundancia (ABUN)*
• Singularidad taxonómica (SEMTA)
• Singularidad (SING)
• Acciones extractivas (ACEXT)
• Grado de protección de las especies (PROT)*
• Protección local (PROLOG)
• Abundancia local (ABLOC)
* Se refiere a su estado en el ámbito nacional.
La ponderación de cada variable componente del SUMIN se encuentra en la tabla 1.
El índice de calificación (SUMIN) puede obtenerse sumando los valores correspondientes. Para cada especie debe considerarse cada una de las variables, asumiendo un valor numérico dentro de un rango determinado. Las especies pueden ordenarse de acuerdo a su valor de SUMIN, resultando un listado ordenado según su estado y urgencia de conservación.
Resultados
1. Los vertebrados de la Reserva
Entre los mamíferos se encuentran camélidos silvestres y domésticos como Vicugna vicugna (vicuña) y Lama glama (llama). Aunque las poblaciones de la vicuña son pequeñas respecto a las encontradas más al norte (Lípez y Pastos Grandes), las llamas, por otro lado, son muy abundantes, ya que como se mencionó antes, la principal actividad económica en la Reserva es la ganadería de camélidos.
Tabla 1: Descripción de las variables que componen el SUMIN (según Úbeda et al., 1994) y sus valores
| VARIABLE | VALOR 0 | VALOR 1 | VALOR 2 | VALOR 3 | VALOR 4 | VALOR 5 |
|---|---|---|---|---|---|---|
| DICON | Todo el continente o su mayor parte | Aproximadamente la mitad del continente | Menos de la mitad del continente | Restringida | ||
| DINAC | Todo el país o su mayor parte | Aproximadamente la mitad del país | Menos de la mitad del país | Restringida | Muy localizada o ende mismo | Microendemismo |
| AUHA | Puede utilizar 4 o más ambientes | Puede utilizar 2 ó 3 ambientes | Puede utilizar sólo 1 ambiente | |||
| AUEVE | Puede utilizar 4 o más estratos | Puede utilizar 2 ó 3 estratos | Puede utilizar sólo 1 estrato | |||
| TAM | Menor de 25 cm o menor de 1 kg | De 25 a 200 cm o de 1 a 12 kg | Mayor de 200 cm o mayor de 12 kg | |||
| POTRE | Elevado (+ de 6 crías) | Mediano (3 a 5 crías) | Bajo (1 ó 2 crías) | |||
| AMTRO | Omnívoras, herbívoras y generalistas | Herbívoras especialistas, carnívoras especilistas y carroñeras | Carnívoras especilistas | |||
| ABUND | Abundante o común | Escasa | ||||
| SINTA | Ausencia | Pertenece a un género monotípico | Rara o muy rara | |||
| SING | Ausencia | Presencia | Pertenece a una familia o taxón superior mono- típicos | Extracción por 3 o más motivos anteriores | Explotación intensiva de piel, cuero, lana, carne y otros | |
| ACENT | No hay | Por temor o repulsión, por ser considerada plaga o perjudicial, para aprovechamiento a pequeña escala o para uso de subproductos | No protegida | |||
| PROT | Protegida por 3 o más unidades de conservación | Protegida por 2 unidades de conservación | Caza deportiva y/o explotación comercial mediana escala o por ser declarada plaga oficialmente | |||
| PROLOC | Distribuida en la Reserva y área de influencia | Distribuida en sólo la Reserva | Protegida por 1 unidad de conservación | |||
| ABLOC | Abundante o común | Escasa | Rara o muy rara |
Entre los félidos se destaca la presencia de Felis jacobita (gato andino), que frecuenta los roquedales y los bosques de Polylepis.
Otro carnívoro presente en el área es Pseudalopex culpaeus (zorro andino), con importantes poblaciones. También puede encontrarse a Conepatus chinga (zorrino o anatuya) y Galictis cuja (hurón).
Entre los roedores se encuentran los géneros Akodon, Phyllotis, Eligmodontia y Choroecomis. Otro elemento importante de la fauna de roedores es Lagidium viscacia (vizcacha) muy abundante en los roquedales, así como Ctenomys opimus (tuco tuco).
Las aves son el grupo más estudiado y notorio en la Reserva, siendo las familias más abundantes Phoenicopteridae, Anatidae, Thinocoridae, Furnaridae, Tyrannidae y Fringilidae. Los ambientes acuáticos constituyen los centros de aglomeración más importantes para las aves, por ejemplo, en las lagunas con alta concentración de sales se encuentran flamencos, patos y playeros, entre los más abundantes y, en las lagunas menos saladas se encuentra a Fulica cornuta, F. gigantea, Podiceps occipitalis y algunos anátidos.
En las zonas de pajonales las especies más representativas son Pterocnemia pennata y Tinamotis pentlandii. En la vegetación arbustiva se encuentran en su mayoría aves paseriformes.
Entre las especies de aves más importantes para la Reserva se encuentran los tres flamencos andinos (Phoenicopterus chilensis, Phoenicoparrus andinus y Phoenicoparrus jamesi), la especie más abundante es P. jamesi con 900 a 2750 individuos en invierno y en verano entre 12.000 a 40.000 individuos (Rocha, 1994).
Los datos de varios años de observaciones y censos sobre aves de la Reserva, indican que existen 21 especies comunes, 23 poco comunes, 12 muy comunes y 24 especies en la categoría de excepcionales que han sido registradas una sola vez. Este último dato sugiere que el 30% de las especies de aves de la Reserva son visitantes esporádicos o de paso muy corto por el área.
Los reptiles de la Reserva están representados únicamente por lagartijas (Iguanidae) del género Liolaemus, adaptadas a las condiciones del medio. Por la información obtenida de los pobladores de Quetena Grande y Quetena Chico se descarta la presencia de culebras del género Tachymenis. Se han identificado 4 especies, con poblaciones relativamente reducidas y localizadas en ciertos sectores de la Reserva, principalmente en pastizales rodeados de roquedales.
Liolaemus dorbigny y Liolaemus orientalis chlorostictus se encontraron en el Campamento Khastor a 4.600 m snm y la última en el cerro Kalina (4.800 m snm). Liolaemus islugensis erguetae se halló en el Salar de Chalviri y Laguna Colorada, mientras que Liolaemus jamesi pachecoi se encontró únicamente en los alrededores de Laguna Colorada. Liolaemus islugensis erguetae y Liolaemus jamesi pachecoi, son subespecies endémicas y que hasta el momento han sido encontradas únicamente en la Reserva (Laurent, com. pers.).
Los anfibios de la Reserva pertenecen a las familias Leptodactylidae y Bufonidae. La primera está compuesta por 3 especies, Pleurodema cinereum, Telmatobius huayra y Telmatobius sp. Las especies acuáticas del género Telmatobius, han sido encontradas en bofedales o turberas.
Telmatobius huayra, especie endémica de Bolivia (Lavilla y Ergueta, 1995), es propia de las turberas que se encuentran en los alrededores del campamento Khastor, y Telmatobius sp. (probablemente una especie nueva, en proceso de descripción), tiene su hábitat en los bofedales del río Quetena, con una altura aproximada de 4.100 ms.n.m.
Pleurodema cinereum es una especie que ha sido encontrada únicamente en los bofedales del campamento Khastor y en muy baja densidad. El único representante de la familia Bufonidae, Bufo spinulosus, es una especie terrestre de gran resistencia a las condiciones de extrema aridez, pero también tiene poblaciones relativamente poco abundantes y localizadas dentro de la Reserva.
La Reserva se encuentra en el sector más septentrional de la Cuenca del Altiplano, que cuenta con ríos poco extensos y un elevado número de microcuencas endorreicas. Los peces de la Reserva son Orestias polonorum y Trichomycterus sp., que fueron encontrados en el río Quetena y sus bofedales, y también en el arroyo Cajchita.
2. Características ecológicas y de conservación
La fauna de la Reserva presenta ciertas características ecológicas y de conservación, que se analizan en los siguientes puntos. Entre estas características se tiene a) comunidades animales particularmente frágiles; b) una diversidad y composición de especies singulares; c) la presencia de poblaciones con abundancias elevadas; y d) presencia de un importante número de especies prioritarias para la conservación.
a) Comunidades animales particularmente frágiles
En la Reserva el paisaje está dominado por áreas abiertas, bajo la gran influencia de factores climáticos como el viento, bajas temperaturas y una alta radiación solar entre otros. En este paisaje abierto, donde predomina el semidesierto altoandino, casi totalmente desprovisto de vegetación, se encuentra una limitada cantidad de hábitats para la fauna, como lagunas salinas y dulces, bofedales, pastizales, matorrales y roquedales, mientras que el desierto altoandino no cuenta con comunidades propias y sólo pueden observarse allí visitantes temporales (principalmente aves).
Esta conformación del sistema altoandino desértico, determina que los hábitats y por ende las poblaciones y comunidades de la Reserva se encuentren “fragmentados naturalmente”, presentando una estructura espacial y temporal en forma de mosaico. Los efectos de un hábitat fragmentado son claros e influyen en la dinámica de la población de especies sensibles al aislamiento, que son afectadas por las barreras de dispersión existentes; especies sensibles al tamaño del área, debido a que tienen requerimientos de áreas extensas no fragmentadas para satisfacerlos; especies sensibles a cambios físicos y biológicos relacionados a los bordes; y especies invasoras que se dispersan y colonizan los nuevos hábitats creados (Centro de Biología de la Conservación, 1996).
b) Diversidad y composición de especies singulares
Se ha confirmado la presencia de 113 especies de vertebrados en la Reserva (Anexo 1), que constituyen el 4,4 % de las especies de vertebrados de Bolivia. Las 113 especies encontradas corresponden a 23 especies de mamíferos (además de 8 especies probables), 80 especies de aves (inventario completo), 4 especies de reptiles, 4 especies de anfibios y 2 especies de peces.
Las 80 especies de aves de la Reserva se encuentran distribuidas en 26 familias; de las cuales 52 especies pertenecen al orden no Passeriformes y 28 especies a las aves Passeriformes. Remsen y Traylor (1989) citan para la región altoandina de Bolivia 126 especies, cerca del 10% del total de especies reportadas para Bolivia. El registro de 80 especies de aves para la Reserva, representa el 63,5% de las especies reconocidas para toda la región altoandina del país, constituyendo una riqueza específica importante.
De acuerdo con el método aplicado para la comparación de la biodiversidad entre las tres áreas protegidas y Huaraco se obtuvieron los siguientes índices de similitud:
| REA: | Reserva Nacional de Fauna Andina Eduardo Avaroa |
| PNS: | Parque Nacional Sajama |
| RFU: | Reserva Nacional de Fauna Ulla Ulla |
| HU: | Huaraco |
Se observa que la similitud encontrada en los tres casos es cercana al 60 %, lo que significa que existe un 40 % aproximadamente de diferencias en la composición de especies. Varias de las especies analizadas son habitantes exclusivos de la Reserva, tal es el caso de las especies endémicas de anfibios y reptiles, las aves como Fulica cornuta, los flamencos P. andinus, P. jamesi y paseriformes como Upucerthia validirostris, Cinclodes atacamensis y Phrygilus dorsalis. Entre los mamíferos se encuentran algunas especies de roedores con distribución restringida y una especie del género Akodon aún no identificada.
Fjeldsȧ (1985) cita para la zona de la puna varios taxa endémicos de distinta apariencia. Algunos de estos son muy locales como Rollandia microptera y F. cornuta. Otros son bastante locales como P. andinus y P. jamesi, que habitan principalmente el desierto de la puna. Las especies que habitan mayores extensiones en la zona son Anas puna, Charadrius alticola, Recurvirostra andina y Gallinago andina. Hay pocas especies que extienden su área de distribución en las partes más altas del sur de los Andes: Chloephaga melanoptera, Phegornis mitchellii y Larus serranus, y otras que extienden su área hacia los páramos.
Los endemismos nacionales están representados por una especie endémica de anfibio (Telmatobius huayra) (Lavilla y Ergueta, 1995), y probablemente una nueva especie del mismo género, mientras que entre los reptiles se encuentran dos subespecies endémicas (Liolaemus islugensis erguetae y Liolaemus jamesi pachecoi) (Raymond Laurent, com. pers.).
Es probable que se encuentre un endemismo en el género Akodon (especie aún no identificada) y Trichomycterus.
c) Presencia de poblaciones con abundancias elevadas
Otra característica que se destaca es la presencia de algunas especies que tienen poblaciones con abundancias elevadas, ya sea en forma estacional, como es el caso de los flamencos, o bien en forma permanente, a saber el zorro y la vizcacha.
Tabla 2: Número de flamencos en las lagunas de la Reserva Nacional de Fauna Andina Eduardo Avaroa
| LAGUNA | Número de flamencos | TOTAL | |||
|---|---|---|---|---|---|
| P. chilensis | P. andinus | P. jamesi | No identif. | ||
| L. Colorada | 65 | 1018 | 13400 | 3537 | 18020 |
| L. Polkes | 15 | 180 | 195 | ||
| L. Herrera | 13 | 11 | 2 | 26 | |
| L. Puripica chico | 4 | 1010 | 923 | 1937 | |
| L. Verde | 455 | 394 | 19 | 868 | |
| L. Honda S | 31 | 210 | 26 | 267 | |
| L. Kalina | 204 | 1668 | 7657 | 9529 | |
| L. Catalcito | 248 | 1035 | 228 | 1511 | |
| L. Totoral | 10 | 1 | 11 | ||
| L. Kollpa | 4 | 75 | 643 | 722 | |
| L. Hedionda S | 86 | 1049 | 1135 | ||
| L. Coruto | 11 | 35 | 65 | 67 | 178 |
| L. Chojllas | 1123 | 122 | 9 | 1254 | |
| Vertiente de Chalviri | 16 | 6 | 22 | ||
| L. Chalviri | 3 | 39 | 20 | 62 | |
| L. Cristal | 3 | 1 | 58 | 62 | |
| L. Mama Khumu | 2 | 68 | 3 | 73 | |
| TOTAL | 2293 | 6922 | 23053 | 3604 | 35872 |
| BOLIVIA | 9764 | 10219 | 30898 | 50881 | |
| Porcentaje | 23.5% | 67.7% | 74.6% | 70.5% | |
Fuente: Rocha y Quiroga (1997)
La población global de P. andinus ha sido estimada entre 50.000 y 150.000 individuos, para P. jamesi de 50.000 individuos y para P. chilensis entre 200.000 y 500.000 ejemplares, sin conocer con exactitud cual es su población real (Kahl, 1975;Johnson, 1995).
El Primer Censo Internacional Simultáneo de Phoenicoparrus jamesi y P. andinus, en Argentina, Bolivia, Chile y Perú, realizado del 23 a 30 de enero de 1997, registró en los cuatro países 33.927 individuos de P. andinus, lo que representa una cifra mucho más baja que la población global anteriormente estimada. El Censo Internacional Simultáneo registró una cifra de 47.619 individuos de P. jamesi, que indicaría que la población de se habría mantenido estable.
En Bolivia, se realizaron censos de las tres especies de flamencos, con énfasis en P. jamesi y P. andinus en 31 sitios, para estimar sus poblaciones totales en el país. Se contaron 30.898 individuos de P. jamesi, 10.219 de P. andinus, 9.764 de Phoenicopterus chilensis y 6.177 individuos no identificados al nivel de especie, contabilizando un total de 57.058 flamencos (Tabla 2) (Rocha y Quiroga, este número). La cifra para P. chilensis es sólo parcial puesto que no se visitaron algunos sitios de gran importancia para su distribución en Bolivia, ya que no se consideraba como objetivo de este trabajo censar a esta especie en su totalidad.
Como se puede observar en la tabla 2, el 70,5% de la población total de flamencos registrada por el Primer Censo Internacional en Bolivia se encuentra en la Reserva, las poblaciones de P. jamesi en la Reserva representan el 74,6% de la población, el caso de P. andinus es similar, ya que el 67,7% de la población registrada en Bolivia se encuentra en la Reserva.
Laguna Colorada, primer y único sitio RAMSAR de Bolivia, es el principal centro de nidificación para P. jamesi, donde los grupos superan los 25.000 flamencos adultos. Las poblaciones fluctúan fuertemente de acuerdo a la estación del año; ya que las mismas en invierno (julio-agosto) a veces no exceden de mil individuos (Rocha, 1994).
Entre otras lagunas con grandes concentraciones de flamencos, que superan los mil individuos, están Laguna Kalina o Busch, Laguna Catalcito, Laguna Hedionda Sur, Laguna Chojllas y Puripica Chico (Figura 1) (Rocha y Quiroga, 1997).
Durante la realización del Plan de Manejo se evaluó de manera preliminar la densidad de vizcachas (Lagidium viscacia) en la Reserva, en un roquedal situado en la orilla norte de la Laguna Colorada, en el área conocida como Chanka Negra y donde, por informes de los guardaparques, se verifica una alta concentración de vizcachas. La estimación realizada durante el trabajo de campo muestra una densidad preliminar de 8 vizcachas/ha.
No existen otras evaluaciones sobre la densidad de esta especie, que permitan comparar las abundancias, pero es más elevada en comparación con la densidad de “vizcachas”, de la especie Lagostomus maximus, encontrada en el Parque Nacional Lihué Calel, de la Argentina, donde se encontró una densidad de 6 vizcachas/ha (Branch y Villarreal, 1988), valor inferior al estimado para la Reserva.
El zorro andino o culpeo (Pseudalopex culpaeus) es una especie de amplia distribución en la región altoandina del país, y de acuerdo a los datos preliminares no cuantificados es muy abundante en la Reserva, particularmente alrededor de los cuerpos de agua, donde aparentemente se alimentan de flamencos. Es también abundante en las áreas donde se encuentran poblaciones elevadas del tuco tuco (Ctenomys opimus).
Heces fecales colectadas y analizadas han mostrado la presencia de dientes y huesos del tuco tuco, así como también plumas de flamencos. Es importante mencionar que el zorro puede consumir restos de comida cerca de áreas antrópicas, de acuerdo a las referencias proporcionadas por O. Rocha, pues el zorro ha sido observado al imentándose en áreas donde se encuentran restos y desperdicios dejados por los pobladores y turistas.
d) Presencia de especies prioritarias para la conservación
Se consideran especies prioritarias para la conservación a las especies endémicas del país que se encuentran en la Reserva, las migratorias y aquellas que presentan algún grado de amenaza.
Los endemismos nacionales están representados por 6 especies de vertebrados, citados anteriormente.
Entre las aves migratorias, se registran nueve especies procedentes del Hemisferio Norte: Pluvialis dominica, Bartramia longicauda, Tringa melanoleuca, Tringa flavipes, Phalaropus tricolor, Calidris bairdii, Calidris himantopus, Larus pipixcan e Hirundo rustica. Así como también, ocho especies migrantes australes como Cinclodes fuscus, Leptasthenura aegitaloides, Muscisaxicola capistrata, M. flavinucha, M. frontalis, Knipolegus aterrimus, Notiochelidon cyanoleuca y Anthus correndera.
Se encuentran ocho especies listadas con algún grado de amenaza por el Libro Rojo de los Vertebrados de Bolivia (Ergueta y Morales, 1996), estas son: Pterocnemia pennata y Fulica cornuta en la categoría “En Peligro”; Vicugna vicugna, Felis jacobita, Phoenicoparrus andinus, P. jamesi y Orestias spp., se encuentran categorizados como “Vulnerables”; Felis concolor, se encuentra en la categoría “Insuficientemente Conocida”; y Phegornis mitchelli, como “Rara”.
El suri (Pterocnemia pennata) tiene carne comestible y la recolección de huevos es intensa. Es cazado para utilizar principalmente sus plumas, con las cuales se fabrican plumeros de uso doméstico en la limpieza. Las plumas se usan también en prácticas de magia tradicional y creencia popular y son ofrecidas en puestos de venta especializados en La Paz (Hanagarth y Weick, 1988). Así también las plumas son utilizadas para la confección de trajes de baile o danza de los “suri-sikuris” en el carnaval o fiestas populares de Bolivia. En algunas regiones del sur del Altiplano se pudo observar la cría y domesticación de suris inmaduros por campesinos lugareños (O. Rocha, obs. pers.). En la Reserva Eduardo Avaroa, el suri es considerado como una especie poco común o rara, puesto que su avistamiento es muy esporádico y casual, al parecer esta especie se ha alejado a la zona este de la Reserva donde no hay actividad turística o flujo de vehículos, y donde las condiciones para alimentación son óptimas (Rocha, obs. pers.). En toda la extensión de la Reserva, se estima que no existen más de 30 individuos adultos (Rocha, obs. pers.).
Sin embargo, en otras zonas fuera de la Reserva, como en los alrededores del Salar de Pastos Grandes son vistos regularmente en grupos familiares de 3 y 5 individuos. En regiones más al noroeste de la Reserva, en la República de Chile, se encuentran muy buenas poblaciones de suris, avistándose en un recorrido de una hora en vehículo más de 30 suris, atribuyéndose este éxito al control estricto y monitoreo de la especie por parte de guardaparques chilenos (Rocha, obs. pers.).
En el ámbito regional, según el Libro Rojo de la UICN (Baillie y Grommbridge, 1996) el suri se encuentra en la categoría “bajo riesgo, casi amenazado”, sin embargo, tanto en Argentina como en Chile se encuentra categorizado como “vulnerable” (Glade, 1988;Chebez, 1994) (Anexo 2).
La soca cornuda (Fulica cornuta) es otra de las especies identificadas como prioritaria para la conservación. En el ámbito regional, no se conoce actualmente cual es la situación de esta especie. Un reciente estudio realizado por Caziani y Derlindati (1996) reportan para la Argentina 8.988 individuos de F. cornuta y 180 nidos activos en octubre de 1995, en un área fronteriza con Bolivia y próxima al lado este de la Reserva, consignándose éste como el registro más alto para la especie.
En Bolivia, Rocha y Quiroga (no publicado) realizaron los primeros censos parciales de las poblaciones de F. cornuta que están fuera del limite este de la Reserva, contabilizando en doce lagunas, 176 individuos entre los meses de noviembre y diciembre de 1992 y 2.152 en el censo parcial de 1994. En este sector, sólo existen caminos de herradura y el acceso de la mayoría de las lagunas es dificultoso, debiendo realizarse los recorridos a pie. En el censo de 1992 se registraron 34 nidos activos y en 1994 un total de 55 nidos activos.
Las poblaciones con mayor abundancia en territorio boliviano se encuentran en lagunas como Khastor, Pelada, Chojllas y otras al sur de la provincia Sud Lípez, habiéndose identificado pocas poblaciones ubicadas dentro del área de la Reserva.
Los polluelos de este rallido son constantemente depredados por la gaviota andina (Larus serranus), el zorro andino (Pseudalopex culpeus) y pobladores locales utilizan los huevos para suplementar su dieta.
En el sector de Pampa Lagunillas, al noreste de Laguna Celeste, se encuentran alrededor de 100 lagunas pequeñas de agua dulce con abundante vegetación acuática sumergida, proporcionando el típico hábitat de F. cornuta, por lo que se presume que esta área pueda albergar a la mayor población de la especie en el ámbito regional (Rocha, no publ).
A escala regional se encuentra en la categoría “vulnerable” (según Baillie y Grommbridge, 1996); en Chile se encuentra categorizada como “vulnerable” (Glade, 1988); mientras que, en Argentina es una especie “rara” (Chebez, 1994) (Anexo 2).
Sin duda, el grupo prioritario para la conservación en la Reserva son los flamencos. De las seis especies de flamencos existentes, tres ocurren en Bolivia: Phoenicopterus chilensis (flamenco chileno), Phoenicoparrus andinus (parina grande o flamenco andino) y Phoenicoparrus jamesi (parina chica o flamenco de .Lunes). En Bolivia, P. andinus y P. jamesi habitan exclusivamente en el Altiplano, en los departamentos de Oruro, Potosí y Tarija, mientras que P. chilensis tiene una distribución más amplia hacia el norte y este del país, abarcando también los departamentos de La Paz, Cochabamba y ocasionalmente Santa Cruz (Rocha, 1994). Los flamencos en Bolivia están resguardados parcialmente en algunas áreas protegidas como la Reserva Nacional de Fauna Andina Eduardo Avaroa (Potosí), Parque Nacional Sajama (Oruro), Reserva de Fauna de Ulla Ulla (La Paz) y la Reserva Biológica de la Cordillera de Sama (Tarija).
Entre las amenazas para estas especies, están la recolección de huevos; matanzas de miles de pichones y juveniles para la utilización de sus plumas y carne y la contaminación de los lagos y lagunas producto de la actividad minera. En Laguna Colorada, principal centro de nidificación de P. jamesi, una amenaza importante es la gran actividad turística informal y descontrolada, principalmente en época de reproducción (Rocha y Quiroga, 1997). Hasta el año 1993, varios son los autores como Walcott (1925),Johnson, et al. (1958),Johnson (1965),Peña (1961),Hurlbert (1978;1981;1982), Campos, (1987)yMaier et al. (1993) para citar algunos, que han reportado la recolección de huevos de flamencos en Laguna Colorada. Sólo a partir del año 1994, con el establecimiento de la Administración de la Reserva Eduardo Avaroa, estas colonias son protegidas por guardaparques.
Además de la presencia de poblaciones con alta abundancia en el área de la Reserva, también la misma alberga 3 colonias de nidificación, de acuerdo a los datos del Censo Internacional (Laguna Colorada, Laguna Busch o Kalina y Laguna Chiar Khota).
En Laguna Colorada se realizó un conteo parcial de 3.000 nidos de P. jamesi, en Laguna Busch o Kalina aproximadamente 300 nidos de P. andinus y P. jamesi, y en Laguna Chiar Khota, alrededor de 100 nidos. Mayores detalles se pueden encontrar en el siguiente artículo de esta misma revista (Rocha y Quiroga, 1997).
Datos de la época de reproducción en Laguna Colorada del período 1992-1993 registraron alrededor de 9.400 polluelos (Maier et al. 1993) y en el período 1996-1997 un total de 10.423 (Rocha, no publ.). Entre los años 1992-1993 aún no se contaba con guardaparques, por lo cual las colonias de nidificación estaban sometidas al saqueo y recolección de huevos. Actualmente hay guardaparques que realizan patrullajes de control y vigilancia, por lo que posiblemente la reproducción de flamencos en Laguna Colorada sea más exitosa. Entre otros sitios de importancia para la nidificación de flamencos en la Reserva está Laguna Guayaques, donde se encontraron 409 polluelos de P. jamesi (Rocha y Quiroga, 1997).
Además de la recolección de huevos, otros de los factores que se pueden mencionar para que ocurra el abandono de las colonias de nidificación, es la intervención de predadores como el zorro andino (Pseudalopex culpaeus). El déficit hídrico y el congelamiento del espejo de agua, son otros factores que pueden impedir que una colonia de flamencos tenga éxito reproductivo (Rocha y Quiroga, 1997).
Laguna Colorada está bien resguardada. Sin embargo, otros sitios de nidificación en la Reserva y sus alrededores, como Laguna Busch o Kalina, Laguna Guayaques y Laguna Chiar Khota deben ser controlados y patrullados. P. andinus aparentemente es la especie con la menor población de las tres especies de flamencos altoandinos y, sin duda, la de mayor riesgo.
En el ámbito regional P. andinus y P. jamesi están categorizados como “vulnerables” (Baillie y Grommbridge, 1996), mientras que en Argentina son especies categorizadas como “raras” (Chebez, 1994). En Chile las tres especies de flamencos se encuentran en la categoría “vulnerable” (Glade, 1988) (Anexo 2).
La vicuña (Vicugna vicugna) en Bolivia se encuentra distribuida a lo largo del altiplano, entre los paralelos 14°40’ y 22°50’ LS, cubriendo un rango latitudinal que varía entre los 3600 y los 4800 msnm, aproximadamente (Villalba, 1992;Anderson, 1997). En la reserva la distribución de la vicuña se restringe al sector noreste, en la zona de Quetena.
A pesar de existir una amplia legislación especial, la regulación y prohibición de caza, posesión y comercio de la vicuña sigue siendo el principal factor de amenaza de la especie. Otros factores son la competencia por espacio y alimento con ganado doméstico (Tarifa, 1996).
En Bolivia la vicuña ha merecido legislación especial amplia; la prohibición de exportación de cueros y lana de vicuña más antigua fue la Ley s/n del 01-12-1918, ratificada posteriormente por varias leyes. En 1969 se firmó entre los gobiernos de Bolivia y Perú el Convenio para la Conservación de la Vicuña. La legislación incluye la creación de áreas protegidas. La gestión de conservación y manejo de la vicuña en el país no tuvo continuidad: en 1977 se crea el INFOL como institución encargada de la protección de la vicuña, posteriormente en 1989 se autoriza al INFOL el traspaso de vicuñas al IBTA, quedando posteriormente el INFOL disuelto. Actualmente la vicuña se encuentra protegida tanto por legislación especial relativa a este camélido silvestre, como a través del Decreto de Veda General Indefinida (Tarifa, 1996).
Finalmente, el año 1997, mediante decreto supremo 24529, referido a la Reglamentación para la Conservación y Manejo de la Vicuña, se otorga a las comunidades campesinas la custodia de la vicuña, bajo la normatividad y fiscalización de la DNCB y con responsabilidades compartidas con las autoridades y gobiernos municipales.
Este mismo decreto determina que la Sociedad Nacional de Manejadoras de Vicuña, formada por las comunidades campesinas, podrá realizar la esquila de animales vivos, previa presentación y aceptación de un Plan de Manejo específico.
El Censo Nacional de la Vicuña de 1996 (Dirección Nacional de Conservación de la Biodiversidad, 1997), registró una población total de 33.844 vicuñas distribuidas en 9 unidades de conservación. Respecto al anterior censo realizado (1986) la población de vicuña del país se ha visto incrementada en un 185%.
La unidad de conservación Lípez - Chichas, se constituye en el área con una población total de vicuñas mayor (9.057 individuos), aunque dada su gran superficie, la densidad relativa (vicuña/ha), la hace una de las pobremente pobladas. La Reserva se ubica dentro de esta unidad de conservación Lípez - Chichas. En la Reserva, el Censo Nacional de la Vicuña ha registrado un total de 378 individuos, que representa el 4% del total de vicuñas dentro de áreas protegidas (7 áreas protegidas poseen 9.091 vicuñas en su interior) y el 1,1% del total de vicuñas en el territorio nacional (Dirección Nacional de Conservación de la Biodiversidad, 1997).
Según los datos del Censo Nacional, el número de individuos registrados en la Reserva probablemente podría ser mayor, pues debido a la época de realización del censo en la zona (julio - agosto), los individuos podrían haber migrado a territorio argentino y chileno (Dirección Nacional de Conservación de la Biodiversidad, 1997). Sin embargo, dada la alta territorialidad que caracteriza el comportamiento de las vicuñas esta posibilidad es poco probable.
Pese a que en los tres países (Bolivia, Chile y Argentina) la vicuña se encuentra categorizada como “vulnerable”(Ergueta y Morales, 1996;Glade, 1988;Chebez, 1996), a escala regional la misma no se encuentra bajo ninguna categoría de amenaza (Baillie y Grommbridge, 1996) (Anexo 2).
Según Pacheco y Salazar (1996) el gato andino (Felis jacobita) habita el altiplano de Bolivia, aunque se tienen pocos registros de esta especie. Según los campesinos de la Reserva, el gato andino ha sido siempre raro, lo que sugiere que está en peligro, debido a lo restringido de su distribución y la pérdida de hábitat. Sin embargo, el gato andino es también raro en otros países, como Chile y Argentina (donde está categorizado como raro) (Glade, 1993). Un aspecto interesante de estudiar es que a pesar de su amplia distribución (Perú hasta Chile) no es común en su área de distribución (Anderson, 1997).
Se encuentra categorizada como “rara” en Chile (Glade, 1988) y “vulnerable” en Argentina (Chebez, 1994). En el ámbito regional no se encuentra bajo ninguna categoría de amenaza (Baillie y Grommbridge, 1996) (Anexo 2).
Los pobladores de la Reserva indican que el puma (Felis concolor) habitaba la región en el pasado y que desapareció cuando disminuyeron las poblaciones de vicuña (Pacheco y Salazar, 1996). El puma es una especie categorizada como "vulnerable’' en Chile (Glade, 1988).
El género Orestias está caracterizado por su alto grado de endemismo. La mayoría de las especies son endémicas del Lago Titicaca, pero se conocen endemismos locales en sistemas aislados. Hasta la fecha no existe un programa de conservación para las especies de este género (Sarmiento y Barrera, 1996).
Phegornis mitchelli es una especie de chorlito inconfundible por su coloración llamativa. Se encuentra solitario o en pequeños grupos. Es poco frecuente en la región. Se alimenta principalmente de insectos (Rocha y Quiroga, 1996a;1996b).
3. Indice de conservación de la RNFA Eduardo Avaroa
Los resultados relativos al estado de conservación a través del método de Úbeda et al. (1994) se encuentran en la tabla 3.
En el caso de los mamíferos el valor máximo es de 16 (Vicugna vicugna y Felis jacobita) y el mínimo de 9 (Pseudalopex culpaeus). En el caso de las aves, el valor máximo es de 22 (Upucerthia validirostris) y el mínimo es de 15 (Phrygilius dorsalis). La media del SUMIN es de 15,87 (d.s. = 4,12, n=15).
Comparando los valores del SUMIN obtenidos con el grado de amenaza de las especies, descritos en el Libro Rojo de los Vertebrados de Bolivia (Ergueta y Morales, 1996), podemos observar que el valor más alto del SUMIN en el caso de los mamíferos (16 para Vicugna vicugna y Felis jacobita), corresponden a la categoría VU (Vulnerable), por lo que podemos observar que el análisis llevado a cabo es válido, para este caso.
Sucede lo contrario para las aves, pues el valor más alto, correspondiente a Upucerthia validirostris no corresponde a ninguna categoría de amenaza en el Libro Rojo; pero como puede observarse en la tabla, los valores correspondientes a DINAC (distribución nacional) y ABLOC (abundancia local) son altos, pues se trata de una especie de distribución restringida y rara, por lo que podría categorizarse como tal.
Posteriormente tenemos a Fulica cornuta y Phoenicoparrus andinus (con un valor de SUMIN igual a 21), con las categorías “En Peligro” y “Vulnerable” del Libro Rojo, posición que nos indica su actual estado de conservación. Con un valor inferior de SUMIN (igual a 20), se encuentra P. jamesi, que posee un valor inferior por ser más abundante que la especie anterior, pero de igual modo se encuentra categorizado como “Vulnerable” en el Libro Rojo de los Vertebrados de Bolivia (Ergueta y Morales, 1996).
Un aspecto importante es que Pterocnemia pennata, categorizada como “En Peligro”, presenta un valor de SUMIN (igual a 19) inferior a las especies categorizadas como “Vulnerables”, debido a los bajos valores de POTRE (potencial reproductivo) y AMTRO (amplitud trófica), que alcanza esta especie.
Es notable que el valor del SUMIN de las aves es significativamente mayor que el de los mamíferos, principalmente debido a que tanto a escala continental como nacional (DICON y DINAC) las aves del análisis presentan distribuciones más restringidas, hecho que eleva el valor de SUMIN.
En el caso de la variable distribución nacional (DINAC), de las 15 especies analizadas, ninguna presenta microendemismos; el 20% de las especies presentan endemismos o una distribución muy localizada; el 27% una distribución restringida; el 13% se encuentran distribuidos en menos de la mitad del país; el 27% en aproximadamente la mitad del país; y el restante en más de la mitad del país (Figura 2a.).
En el caso de las acciones extractivas (ACEXT), de las 15 especies incluidas en el análisis, 27% de las mismas sufren de una explotación intensiva; 7% son perseguidas por caza y/o explotación a gran escala comercial; 13% por caza y/o explotación a mediana escala; el 27% es cazado por temor u otras causas, así como para un aprovechamiento a baja escala; y el resto no sufre de ninguna actividad extractiva. Es preocupante que más del 70% de las especies analizadas se encuentren amenazadas por algún tipo de extracción (Figura 2b).
Tabla 3: Valores de SUMIN para las especies seleccionadas en la Reserva Nacional de Fauna Andina Eduardo Avaroa
| ESPECIE | DICON Distribución continental | DINAC Distribución nacional | AUHA Amplitud en el uso del habitat | AUEVE Amplitud en uso del espacio vertical | TAM Tamaño corporal | POTRE Potencial reproductivo | AMTRO Amplitud trófica | ABUND Abundan cia | SINTA Singularidad taxonómica | SING Singulari dad | ACEXT Acciones extractivas | PROT Grado de protección de las especies | PROLOC Protección local | ABLOC Abundancia local | SUMIN | LRVB |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pseudalopex culpaeus | 2 | 1 | 0 | 1 | 1 | 2 | 1 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 9 | NL |
| Felis concolor | 0 | 0 | 0 | 1 | 2 | 2 | 1 | 1 | 0 | 0 | 2 | 0 | 1 | 2 | 12 | DD |
| Felis jacobita | 3 | 1 | 0 | 1 | 1 | 2 | 1 | 2 | 0 | 0 | 2 | 0 | 1 | 2 | 16 | VU |
| Vicugna vicugna | 3 | 1 | 0 | 1 | 2 | 2 | 1 | 1 | 0 | 0 | 3 | 0 | 1 | 1 | 16 | VU |
| Lama glama | 2 | 1 | 0 | 1 | 2 | 2 | 1 | 0 | 0 | 0 | 4 | 0 | 0 | 0 | 13 | NL |
| Ctenomys opimus | 3 | 2 | 2 | 2 | 0 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 12 | NL |
| Lagidium viscacia | 2 | 0 | 2 | 1 | 1 | 2 | 0 | 0 | 0 | 0 | 1 | 0 | 1 | 0 | 10 | NL |
| Phoenicoparrus andinus | 3 | 3 | 2 | 2 | 2 | 2 | 1 | 1 | 0 | 0 | 4 | 0 | 0 | 1 | 21 | VU |
| Upucerthia validirostris | 3 | 4 | 2 | 2 | 0 | 2 | 2 | 2 | 0 | 0 | 0 | 2 | 1 | 2 | 22 | NL |
| Phoenicoparrus jamesi | 3 | 3 | 2 | 2 | 2 | 2 | 1 | 1 | 0 | 0 | 4 | 0 | 0 | 0 | 20 | VU |
| Fulica cornuta | 3 | 4 | 2 | 2 | 2 | 1 | 1 | 2 | 0 | 0 | 1 | 2 | 0 | 1 | 21 | E |
| Pterocnemia pennata | 3 | 3 | 1 | 2 | 2 | 0 | 0 | 2 | 0 | 0 | 4 | 0 | 0 | 2 | 19 | E |
| Fulica gigantea | 3 | 2 | 2 | 2 | 2 | 1 | 1 | 1 | 0 | 0 | 1 | 0 | 0 | 1 | 16 | NL |
| Phegornis mitchelli | 3 | 3 | 2 | 2 | 0 | 1 | 1 | 2 | 0 | 0 | 0 | 0 | 0 | 2 | 16 | R |
| Phrygilius dorsalis | 3 | 4 | 2 | 2 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 2 | 1 | 0 | 15 | NL |
* NL: no listado en el Libro Rojo de los Vertebrados de Bolivia (Ergueta y Morales, 1996)
El grado de protección (PROT) presenta dos extremos: un 80% de las especies del análisis se encuentra protegida en 3 o más unidades de conservación (particularmente, en nuestro análisis la Reserva, el PN Sajama y la RNF Ulla Ulla), y el 20% restante se encuentra protegida en una sola unidad de conservación (en consecuencia la Reserva) (Figura 2c).
Finalmente, la abundancia local (ABLOC), muestra que el 33% de las especies seleccionadas son raras; el 27% escasas; y el 40% restante son abundantes (Figura 2d).
Conclusiones
El trabajo realizado acerca de la fauna de vertebrados de la Reserva de Fauna Andina Eduardo Avaroa, muestra varios aspectos importantes relacionados con la conservación y el futuro manejo de la Reserva. Como se menciona en el trabajo, el área es una de las mejor documentadas en el área andina de Bolivia, pero se requieren realizar estudios que complementen el conocimiento sobre ciertos grupos, como los reptiles, anfibios y peces; y principalmente impulsar el estudio sobre la biología y ecología de las especies consideradas prioritarias para la conservación.
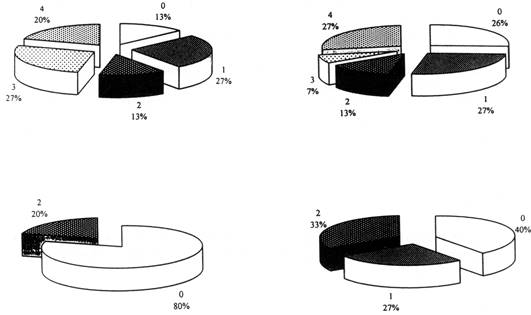
Fig. 2: Distribución porcentual de las variables importantes para la conservación. A. Distribución nacional. B. Acciones extractivas. C. Grado de protección. D. Abundancia local. Para una interpretación de cada variable ver la Tabla 1.
La Reserva tiene una singular importancia como integrante del Sistema Nacional de Areas Protegidas, debido a que es un ecosistema particularmente frágil, con una diversidad y composición de especies notable en el conjunto de áreas protegidas andinas de nuestro país. La concentración de poblaciones numerosas de algunas especies y la presencia de un número importante de especies consideradas prioritarias para la conservación, son otras dos características que refuerzan la importancia del área en el contexto del SNAP.
Los índices SUMIN obtenidos y las categorizaciones del Libro Rojo de los Vertebrados de Bolivia, nos sugieren algunos aspectos que deben ser considerados en las políticas y actividades de protección, investigación y monitoreo de la Reserva.
Al respecto, se destaca el caso de las aves Fulica cornuta y Phoenicoparrus andinus, que presentan un índice SUMIN elevado y categorías de jerarquía en el Libro Rojo (En Peligro y Vulnerable, respectivamente). En el caso de F. cornuta se sugiere, como parte de la estrategia global de protección de la especie, la ampliación de la Reserva en el sector nor-este (Pampa Lagunillas), donde se encuentran poblaciones importantes, que deben ser protegidas y monitoreadas.
Es importante, además, señalar que estas dos especies se encuentran amenazadas en los países limítrofes a la Reserva y a escala regional.
Laguna Colorada es sin duda uno de los humedales de mayor importancia en la región andina de Sud América, que requiere de una política de protección estricta, debido a las fuertes presiones que ejerce sobre ella el turismo no planificado, que es una de las más serias amenazas que enfrenta la Reserva. Laguna Colorada es sitio de nidificación de las tres especies de flamencos, y se sugiere su categorización a Santuario Nacional, como una estrategia para la conservación de los flamencos y la belleza imponente del paisaje.
Otro aspecto que merece ser considerado en el manejo de la Reserva, es que más del 70 % de las especies de fauna analizadas se encuentran sometidas a algún tipo de extracción, la misma que ha disminuido en los últimos años debido al trabajo de protección del personal del área, pero es aún un tema prioritario, que debe ser trabajado en forma conjunta, principalmente con las comunidades locales y el ejército, de manera de lograr una conservación en armonía con los habitantes del área.












 uBio
uBio