1. Introducción
Akodon boliviensis Meyen 1933 y Phyllotis darwini Waterhouse 1837 son las especies más frecuente y más abundante, respectivamente, en la valle de La Paz (Yoneda, 1984a;Mercado, 1990;Mercado y Miralles, 1991); sin embargo el conocimiento de su reproducción es casi nulo. Yoneda (1984a) realizó un estudio del ciclo reproductor basado en la presencia de esperma en el epidídimo de los machos y estableció la época de reproducción para P. darwini entre los meses de febrero a abril, con un segundo período entre agosto y septiembre.
El estudio de la reproducción de estas dos especies nos permitirá determinar si existe una respuesta adaptativa convergente hacia los factores climáticos y la latitud.
2. Metodología
La colecta de especímenes se efectuó una vez al mes, desde octubre de 1993 a octubre de 1994. Cada colecta tuvo una duración de 4 días y 3 noches, según aconsejan Day et al. (1980). Se utilizaron trampas Sherman de captura viva. Los animales se transportaron al Laboratorio de Embriología del Instituto Boliviano de Biología de la Altura, donde fueron sacrificados para su posterior estudio.
Los datos biométricos tomados incluyen longitud total, longitud de la cola, largo del tarso, largo de la oreja y peso total. Los datos biológicos son, en el caso de las hembras: estado de la abertura vaginal, presencia u ausencia de embriones por medio de palpación. En el caso de los machos se observó la posición de los testículos. Posteriormente, se extrajeron los ovarios, los oviductos y el útero en el caso de las hembras, o los testículos y el epidídimo en el caso de los machos. En hembras preñadas se obtuvo el útero con los fetos, los cuales fueron fijados en Bouin después de ser sacados de la bolsa amniótica y separados de la placenta. Se anotó el número de fetos y su posición en los cuernos uterinos.
Con los datos obtenidos se calculó la prevalencia de preñez mensual, dividiendo el número de hembras preñadas entre el número de hembras capturadas (Crespo, 1966) y el índice ovárico dividiendo el peso de los ovarios en promedio (en mg) por el peso total del individuo (en g) (Kirkpatrick y Satterfield, 1973). En el caso de los machos se calculó el índice testicular, que según Brown (1969), se obtiene dividiendo la longitud de los testículos en promedio (en mm) por la longitud total del individuo (en mm).
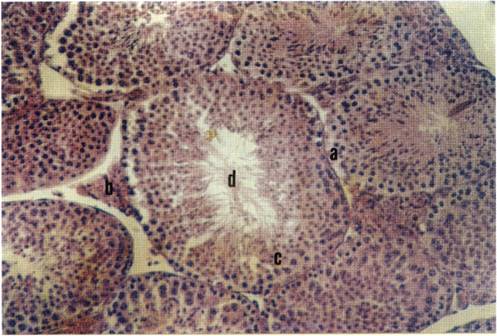
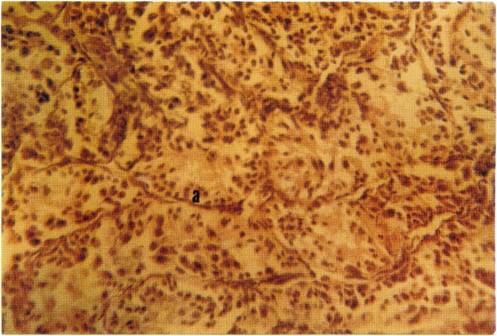
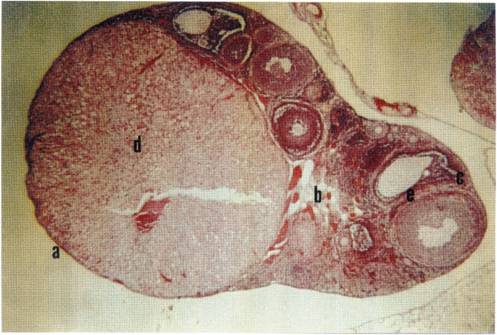
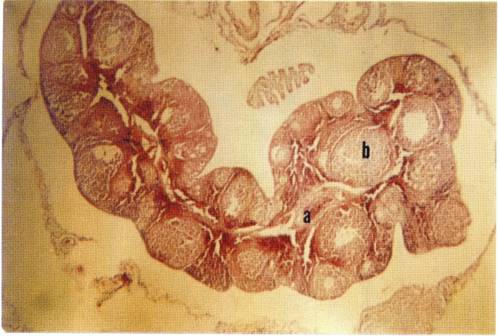
Se evidenció el estado de madurez sexual de los individuos a través de la histología de los testículos en el caso de machos, y ovarios en el caso de las hembras, por medio de las descripciones de Gómez (1995). Se utilizó la técnica progresiva de tinción universal descrita en Flores et al. (1994) (ver fotografías en anexo, pp. 68-70). Finalmente, se conservó el cráneo y la piel de los especímenes sacrificados, según técnicas convencionales.
3. Area de Estudio
El área de estudio se encuentra en el valle de La Paz, el cual está situado en el departamento del mismo nombre con una altura promedio de 3.700 m snm dentro de las cadenas montañosas que constituyen la Cordillera de los Andes; el valle tiene una orientación norte-sud, con un drenaje hacia la cuenca amazónica. Huajchilla se encuentra ubicada a 17 km al sur de la ciudad, en el margen izquierdo del río La Paz, con las coordenadas geográficas: 68°03’O y 16°37’S (Fig. 1) y a 3050 m snm.
La zona está sometida a una estacionalidad notable en la precipitación, con un período seco de cuatro meses (abril-agosto). Los meses con mayor precipitación corresponden a diciembre, enero y febrero. Las temperaturas son relativamente uniformes a lo largo del año, con una variación máxima de 3°C, aunque la variación entre la temperatura de día y de noche es más extrema.
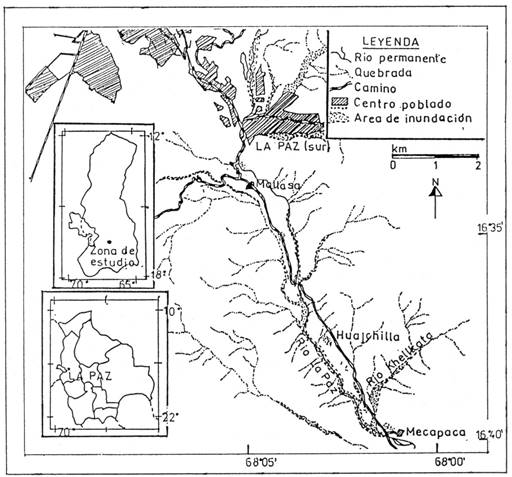
Fig. 1: Área de estudio. Mapa de ubicación del área de estudio en el valle de La Paz. Modificado de Forno y Baudoin (1993).
La duración del día durante el año no varía muy significativamente. En el mes de diciembre se registra la máxima duración del día con 13 horas 15'. Durante el mes de junio se registra la duración mínima del día con 11 horas 8'.
La vegetación actual de los valles está muy alterada. Por la intervención humana la vegetación predominante es arbustiva, con plantas espinosas y suculentas (cactáceas). Un matorral abierto se distribuye en las laderas, quebradas y terrazas altas, sobre los ríos o en las planicies pedregosas. En el fondo del valle existen varios cultivos irrigados. La vegetación se describe más detalladamente en Gómez (1995).
4. Resultados y discusión
4.1. Capturas y éxito de captura.
Producto de las capturas realizadas durante el año de estudio se obtuvo un total de 141 roedores, de los cuales 64 pertenecían a Phyllotis darwini y 77 a Akodon boliviensis (Tabla 1). Durante los meses de noviembre y enero no se obtuvieron hembras de A. boliviensis, el resto de los meses se capturó, por lo menos, un individuo de ambos sexos y ambas especies.
Tabla 1: Número total de capturas, por mes y por especie, además del esfuerzo de trampeo expresado en número de trampas por noche (TN) y, éxito de captura mensual expresado en número de roedores capturados por 100 TN
| MES | A. boliviensis | P. darwini |
TRAMPAS POR NOCHE |
EXITO DE CAPTURA | ||||
|---|---|---|---|---|---|---|---|---|
| Hembra | Macho | Hembra | Macho | General | Akodon | Phyllotis | ||
| OCT | 2 | 1 | 1 | 6 | 65,50 | 15,27 | 4,58 | 10,69 |
| NOV | 3 | 3 | 3 | 82,67 | 10,89 | 3,63 | 7,26 | |
| DIC | 2 | 1 | 4 | 3 | 77,50 | 12,90 | 3,87 | 9,03 |
| ENE | 1 | 1 | 4 | 37,50 | 16,00 | 2,67 | 13,33 | |
| FEB | 3 | 3 | 1 | 1 | 59,33 | 13,48 | 10,11 | 3,37 |
| MAR | 4 | 5 | 3 | 4 | 72,30 | 22,13 | 12,45 | 9,68 |
| ABR | 10 | 6 | 2 | 3 | 57,00 | 36,84 | 28,47 | 8,77 |
| MAY | 2 | 7 | 3 | 4 | 63,50 | 25,19 | 14,17 | 11,02 |
| JUN | 4 | 2 | 3 | 2 | 71,00 | 15,49 | 8,45 | 7,04 |
| JUL | 3 | 3 | 1 | 2 | 56,00 | 16,07 | 10,71 | 5,35 |
| AGO | 3 | 4 | 1 | 3 | 81,50 | 13,49 | 8,59 | 4,91 |
| SEP | 6 | 2 | 2 | 4 | 69,50 | 20,14 | 11,51 | 8,63 |
| TOT. | 39 | 38 | 25 | 39 | x= 66,07 | X= 18,16 | x= 9,90 | x= 8,26 |
| NUMERO TOTAL DE CAPTURAS: 141 | ||||||||
En cuanto al éxito de captura general (figura 2), se observa que existe una mayor efectividad entre los meses de marzo y mayo, los demás meses, excepto septiembre, se encuentran por debajo del promedio general de éxito, que fue de 18,16 roedores por 100 trampas-noche.
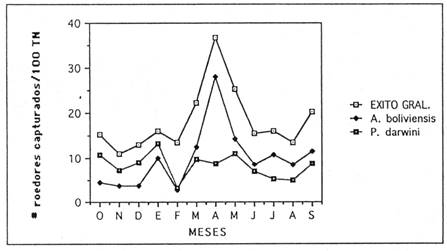
Fig. 2: Éxito de captura expresado en número de roedores capturados/100 trampas noche (TN), de manera general (EXITO GRAL.) y para cada especie estudiada.
En lo referente a P. darwini, no existe gran variación en cuanto al éxito de captura a lo largo del año, teniendo sus valores más altos en los meses de enero, abril y mayo. Por el contrario, en el caso de A. boliviensis, existe una gran diferencia en el éxito de captura que explica las diferencias observadas en el éxito general. El hecho de un mayor éxito de trampeo en los meses de abril hasta septiembre, se debe a la mayor proporción de individuos juveniles en la población.
Yoneda (1984a) basó sus conclusiones sobre la reproducción de P. darwini en la misma área sobre un total de 58 roedores capturados. Crespo (1966), realizó estudios en el Partido Rojas de la provincia de Buenos Aires con diferentes especies utilizando 182 roedores en el caso de Oryzomys flavecens, 90 en el caso de Akodon obscurus, 98 en el caso de Calomys laucha. Este estudio tuvo una duración de 18 meses. Crespo et al. (1970) realizaron estudios similares en el sur de la provincia de Córdoba utilizando un total de 378 roedores en el caso de Akodon azarae, 633 roedores en el caso de Calomys musculinus; 61 ejemplares de Mus musculus, 51 ejemplares de Oryzomys flavescens, 35 ejemplares de Akodon obscurus y 24 ejemplares de Calomys laucha; este estudio tuvo una duración de 36 meses. En nuestro caso el número capturado está por debajo de los trabajos citados y se encuentra relacionado con el esfuerzo de captura realizado durante un año.
4.2. Estructura de la población
Para A. boliviensis, la proporción de machos y hembras es casi idéntica (50,65 % de hembras). En P. darwini, la situación es diferente, pues los machos superan claramente a las hembras con un 60,94 % del total de las capturas.
La proporción precisa de individuos juveniles y adultos en la población, fue obtenida a través de los cortes histológicos que, según Arruda (1983), son utilizados por varios autores para una correcta determinación del estado de madurez sexual. Los resultados de estas observaciones se presentan en la tabla 2. La estructura de la población de ambas especies nos brinda el primer indicativo de un tipo de reproducción estacional, pues los individuos juveniles están presentes en la población durante una sola época del año.
Tabla 2: Número y distribución porcentual de individuos adultos y juveniles en las poblaciones de las especies estudiadas en base a la observación microscópica de cortes histológicos de testículos y ovarios.
| MES | Akodon boliviensis | Phyllotis darwini | ||||||
|---|---|---|---|---|---|---|---|---|
| TOTAL | PORCENTAJE | TOTAL | PORCENTAJE | |||||
| ADULTO | JUVENIL | ADULTO | JUVENIL | ADULTO | JUVENIL | ADULTO | JUVENIL | |
| OCT | 2 | 1 | 66,67 | 33,33 | 2 | 5 | 28,57 | 71,43 |
| NOV | 3 | 0 | 100,00 | 0,00 | 6 | 0 | 100,00 | 0,00 |
| DIC | 3 | 0 | 100,00 | 0,00 | 7 | 0 | 100,00 | 0,00 |
| ENE | 1 | 0 | 100,00 | 0,00 | 5 | 0 | 100,00 | 0,00 |
| FEB | 5 | 1 | 83,33 | 16,67 | 2 | 0 | 100,00 | 0,00 |
| MAR | 6 | 3 | 66,67 | 33,33 | 5 | 2 | 71,43 | 28,57 |
| ABR | 12 | 4 | 75,00 | 25,00 | 4 | 1 | 80,00 | 20,00 |
| MAY | 5 | 4 | 55,56 | 44,44 | 3 | 4 | 42,86 | 57,14 |
| JUN | 2 | 4 | 33,33 | 66,67 | 3 | 2 | 60,00 | 40,00 |
| JUL | 3 | 3 | 50,00 | 50,00 | 3 | 0 | 100,00 | 0,00 |
| AGO | 3 | 4 | 42,86 | 57,14 | 2 | 2 | 50,00 | 50,00 |
| SEP | 2 | 6 | 25,00 | 75,00 | 3 | 3 | 50,00 | 50,00 |
En el caso de A. boliviensis podemos observar que entre los meses de noviembre y enero el total de la población capturada está compuesta por individuos adultos. El resto de los meses, se observa la presencia de individuos juveniles en algún porcentaje, particularmente en los meses de otoño e invierno. La proporción más alta de juveniles se registró en el mes de septiembre (con 75 % del total de la población).
En lo que respecta a P. darwini, la presencia de sólo individuos adultos se prolonga hasta febrero; en el resto de los meses, se observa un porcentaje de individuos juveniles variable, el más alto se registró en el mes de octubre (con 71,43 % del total de la población).
4.3. Variación mensual del peso promedio
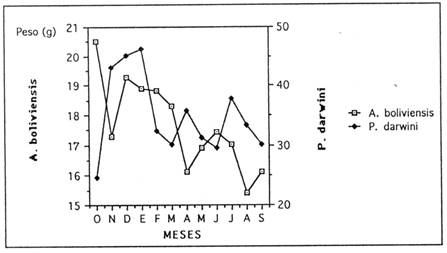
A fin de determinar la madurez sexual de los individuos de las poblaciones estudiadas, se obtuvo el promedio mensual del peso corporal por especie. Estos resultados están resumidos en la figura 3.
Un análisis de la gráfica nos indica que la variación del peso promedio de P. darwini es muy fluctuante entre los meses de julio a octubre, esta fluctuación puede deberse al amplio intervalo de pesos encontrados en los individuos capturados.
En el caso de A. boliviensis no hay variaciones mensuales claras en el promedio de peso. Esto puede deberse a que los individuos juveniles están presentes durante casi todo el año; se puede pensar que existe una ganancia rápida de peso por parte de los recién nacidos. Esto fue observada experimentalmente por Hudson (1974) en Baiomis taylori, donde el bajo peso de los recién nacidos causa problemas de termorregulación que deben ser equilibrados por una ganancia rápida de peso.
Tanto en A. boliviensis como en P. darwini, el peso corporal es un descriptor poco recomendable para estimar la condición reproductiva. En efecto, no muestra ninguna relación con otras características reproductivas, por ejemplo el índice testicular. Crespo (1966) admite que es arriesgado asumir la hipótesis de que el peso es directamente proporcional a la edad de los individuos.
4.4. Posición de los testículos.
4.4.1. Actividad sexual.
La presencia de los testículos en el escroto, nos indica que el individuo capturado es activo sexualmente. En el caso de los individuos con los testículos en el abdomen tenemos dos posibilidades, que se trate de individuos maduros pero en un período de inactividad sexual, o que sean individuos juveniles; la discriminación entre ambos fue hecha a través de la histología de los testículos.
El número y distribución porcentual de individuos adultos con testículos escrotales y testículos abdominales para cada mes se presenta en la figura 4. Podemos observar en el caso de A. boliviensis, tomando en cuenta sólo a los individuos adultos, que el 100 % de individuos con testículos escrotales se presenta entre los meses de octubre y marzo (sin embargo en noviembre se da solamente en el 66,67 % de los casos), para ir descendiendo paulatinamente hasta el 0 % entre los meses de julio a agosto y aumentar nuevamente en septiembre.
En el caso de P. darwini, el 100 % de testículos escrotales fue observado entre los meses de octubre a mayo, luego desciende a 0 % entre junio y agosto, para finalmente ascender a un tercio de los individuos durante el mes de septiembre.
Para analizar el desarrollo del tamaño de los testículos obtuvimos el índice testicular, que se presenta en la tabla 3. En el caso de A. boliviensis, el desarrollo del tamaño testicular muestra diferencias entre una época de actividad reproductora y una época de inactividad, donde el tamaño de los testículos se reduce. La época donde los testículos son más grandes corresponde a los meses comprendidos entre octubre a mayo, para luego observar una reducción de tamaño entre los meses de junio a septiembre. El máximo valor del índice testicular fue observado durante el mes de enero, el menor en junio. El desarrollo del tamaño de los testículos en P. darwini nos muestra una variación más clara. El máximo valor del índice testicular fue observado durante el mes de abril, el menor se registró también en junio.
Es interesante notar que en ambas especies, el inicio de la época con testículos más pequeños ocurre en los mismos meses.
Podemos afirmar que en el caso de A. boliviensis, los testículos con una longitud mayor o igual a 6 mm, corresponden a testículos de individuos adultos y activos sexualmente, dato que está de acuerdo con los resultados de Pearson (1951), quien afirma que los machos reproductores que él encontró, poseían testículos con una longitud superior a 6 mm.
En lo que respecta a P. darwini, el tamaño reproductivo de los testículos sería de 8 a 9 mm. Nuevamente, nuestros datos concuerdan con los obtenidos por Pearson (1951), quien afirma que la condición reproductora se alcanza entre los 9 a 10 mm de longitud.
Podemos relacionar la posición de los testículos y el índice testicular. En el caso de A. boliviensis, existe una correspondencia entre el tamaño de los testículos y su posición en los meses de octubre a marzo, correspondientes a la época de actividad sexual. Durante el mes de abril, los testículos todavía poseen un tamaño considerable, con un 25 % de ellos en el abdomen. Según Taylor y Homer (1970), la supresión de la actividad reproductiva se caracteriza por un aumento en la cantidad de tejido conectivo del testículo. Iriarte (1991) demostró que la criptorquidia provocada experimentalmente no causa una reducción inmediata del tamaño testicular.
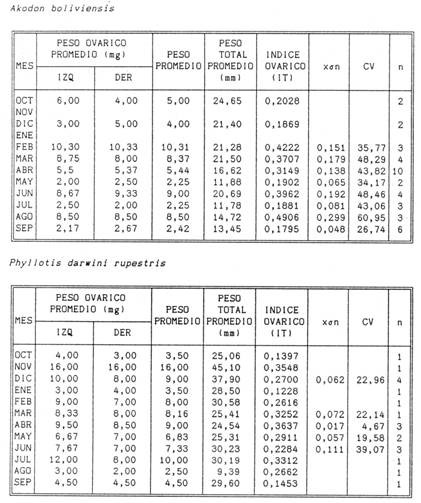
Tabla 3: Indice testicular (IT) (longitud más larga promedio de ambos testículos en mm/ longitud total en mm), para las dos especies estudiadas. Además de la desviación estandard (xon), el coeficiente de variación (CV) y el número de individuos medios (n).
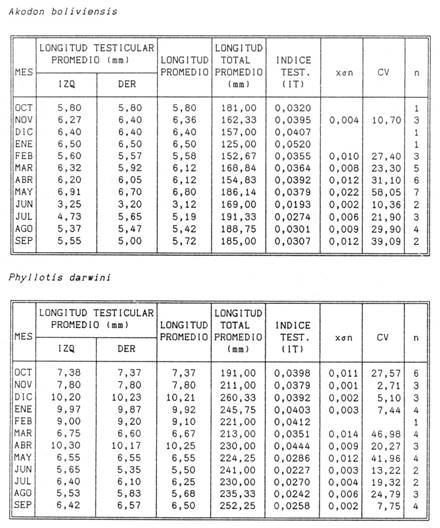
En lo que respecta a P. darwini, tal correspondencia es también observada, pues más del 50 % de la población de machos tienen testículos escrotales a partir de octubre a mayo, coincidiendo con los meses en que se registran el mayor tamaño de los testículos. Por todo ello podemos situar la época reproductiva de los machos entre octubre a mayo, tanto para A. boliviensis como para P. darwini.
4.4.2. Peso medio para la actividad sexual.
Según Crespo (1966)yCrespo et al. (1970) es costumbre determinar el peso medio para el cual el 50 % de la población alcanza la madurez sexual, lo cual se hace más factible cuando existe una época de reproducción marcada.
Para A. boliviensis, el 50 % de los machos alcanza la posición escrotal entre los meses de septiembre a marzo, con un peso promedio de 20,68 ± 5,6 g. Entre los meses de abril y mayo el porcentaje de testículos escrotales se mantiene por debajo del 50 %, aunque no es igual acero, con un peso promedio de 24,46 ± 0,9 g durante este período de inactividad sexual.
Siguiendo el mismo análisis para P. darwini, podemos observar que el 50 % de individuos con testículos escrotales están presentes entre los meses de octubre a mayo, con pesos que oscilan entre 25 y 60 g y un peso medio de 45,75 ± 12,18 g.
4.5. Estado de la abertura vaginal
4.5.1. Actividad sexual.
El estado de la abertura vaginal nos indica la predisposición de la hembra para reproducirse. Una vagina cerrada nos indica inactividad sexual, debido a que la hembra se encuentra en diestro vaginal y comportamental, o debido a que está preñada. Una vagina abierta nos indica actividad sexual, es decir, que la hembra se encuentra o está próxima al estro.
En el caso de A. boliviensis, observamos que durante los meses de abril y septiembre existen hembras con la vagina abierta, durante el resto de los meses se encuentran con la vagina cerrada (figura 5). Sin embargo, este hecho no es debido a la inactividad sino a la prevalencia de preñez, ya que la mayoría de las hembras capturadas entre octubre a abril estaban preñadas.
De manera similar, en el caso de P. darwini, los meses con hembras con vagina abierta están entre noviembre y abril, los demás meses tienen un porcentaje igual a cero. Nuevamente debemos tomar en cuenta los valores de prevalencia de preñez para los meses de noviembre a abril.
Para analizar el desarrollo del peso de los ovarios obtuvimos el índice ovárico, que de manera resumida se presentan en la tabla 4, para ambas especies.
No existe diferencia en cuanto a qué especie presenta los ovarios de mayor tamaño relativo, es más, aparentemente, en ninguna de las dos especies parece observarse patrón alguno en cuanto al cambio del peso de los ovarios a lo largo de los meses. La variación observada no permite llegar a ninguna conclusión.
Es posible que la precisión de la balanza no fue suficiente para obtener resultados satisfactorios como los obtenidos, por ejemplo, por Kirkpatrick y Satterfield (1973), con el mismo método. Sin embargo, lo más probable es que el tamaño de la muestra es el que nos impide obtener resultados claros.
4.5.2. Peso promedio para la actividad sexual.
La madurez sexual (que en este caso incluye a las hembras con vagina abierta y las hembras preñadas), para el 50 % de la población de las hembras de A. boliviensis, se alcanzó con un peso medio de 22,39 ± 6,37 g. Entre los meses de octubre a febrero, toda la población de hembras tiene un peso superior al promedio.
La madurez sexual para el 50 % de la población de hembras de P. darwini, se alcanzó con un peso promedio de 29,39 ± 3,77 g. Durante los meses de enero, marzo y abril, los pesos medios se mantuvieron por debajo del peso medio para la actividad sexual.
4.6. Preñez y conteo de fetos.
Los resultados sobre el número de hembras preñadas por mes, presencia de embriones, número y posición de los mismos se presentan en la tabla 5.
Tabla 5: Número total de hembras capturadas (TOTAL), número de hembras preñadas (PREÑ.), prelavencia de preñez (P.V.), número (#EMB.) y posición (C.IZQ: cuerno uterino izquierdo y C.DER: cuerno uterino derecho) de los embriones, para ambas especies estudiadas de manera mensual.
| MES | Akodon boliviensis | Phyllotis darwini | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| TOTAL | PREÑ. | P. V. | #EMB. | C. IZQ | C.DER | TOTAL | PREÑ. | P. V. | #EMB. | C. IZQ | C.DER | |
| OCT | 2 | 1 | 0,50 | 5,00 | 2,00 | 3,00 | 1 | 0 | 0,00 | |||
| NOV | 3 | 1 | 0,33 | 4,00 | 2,00 | 2,00 | ||||||
| DIC | 2 | 2 | 1,00 | 5,00 | 2,00 | 2,00 | 4 | 2 | 0,50 | 3,00 | 2,00 | 1,00 |
| ENE | 1 | 0 | 0,00 | |||||||||
| FEB | 3 | 3 | 1,00 | 6,30 | 4,70 | 1,60 | 1 | 1 | 1,00 | 3,00 | 2,00 | 1,00 |
| MAR | 4 | 3 | 0,75 | 4,00 | 2,00 | 2,00 | 3 | 3 | 1,00 | 3,50 | 2,00 | 1,50 |
| ABR | 10 | 1 | 0,10 | 1,00 | 1,00 | 0,00 | 2 | 1 | 0,50 | 4,00 | 2,00 | 2,00 |
| MAY | 2 | 0 | 0,00 | 3 | 0 | 0,00 | ||||||
| JUN | 4 | 0 | 0,00 | 3 | 0 | 0,00 | ||||||
| JUL | 3 | 0 | 0,00 | 1 | 0 | 0,00 | ||||||
| AGO | 3 | 0 | 0,00 | 1 | 0 | 0,00 | ||||||
| SEP | 6 | 0 | 0,00 | 2 | 0 | 0,00 | ||||||
El material reunido de A. boliviensis permite establecer la existencia de embriones visibles a ojo desnudo a partir de octubre hasta abril, sugiriendo una época de preñez de aproximadamente 210 días. En una ocasión, se constató la presencia de embriones a través de un corte histológico en el útero, durante el mes de marzo, este caso se incluyó en el conteo.
Si bien en noviembre y enero no se capturaron hembras de esta especie, los datos de diciembre y febrero, indican que este fenómeno difícilmente se haya interrumpido. En los meses de marzo y abril, se observa una reducción de la previdencia de preñez. A partir de mayo hasta octubre, el índice de prevalencia de preñez se mantuvo en cero.
El valor medio de embriones por hembra es de 4,5 ± 1,8; el caso con mayor número de embriones fue de siete (en diciembre) y el menor de 1 (en abril), notándose una tendencia a aumentar el promedio en febrero y disminuir en abril.
El peso de la hembra más joven con embriones fue de 10,42 g (en febrero), la cual probablemente nació entre mediados y fines del año anterior, o sea, se trata de hembras jóvenes adultas o primíparas.
Parece existir cierta preferencia hacia el cuerno uterino izquierdo pues el promedio de embriones en éste fue de 2,53 ±1,54, en cambio el cuerno uterino derecho tenía un promedio de 1,73 ± 0,95 embriones. Tales preferencias fueron también observadas por Corthum (1967) en Microtus ochrogaster y Microtus pennsylvanicus.
El material de P. darwini presenta datos más completos que en la especie anterior, la existencia de embriones se constató a partir de noviembre hasta abril. Durante el mes de marzo, se registró la presencia de embriones a través de un corte histológico en el útero. Se sugiere una época de preñez de 180 días. A partir del mes de mayo hasta octubre el valor de la prevalencia de preñez se mantuvo en cero.
En el mes de enero, no fue posible capturar hembras preñadas, por lo que el índice de prevalencia de preñez fue de cero. Sin embargo, y como en la especie anterior, los datos de diciembre y febrero indican que el proceso no pudo haber sido interrumpido.
El valor medio de embriones por hembra es de 3,43 ± 0,49; en todos los casos el número de embriones varía entre 3 y 4, sin notarse ninguna diferencia entre los meses de preñez.
El peso de la hembra más joven con embriones fue de 23,86 g (en marzo), cuyo nacimiento probablemente se registró a fines del año anterior.
La posición de los embriones en los cuernos uterinos no muestra una diferencia significativa pues el promedio en el cuerno uterino izquierdo fue de 2 y en el derecho de 1,5 ± 0,2.
El número de embriones merece especial atención debido a que según Spencer y Steinhoff (1968) y Blus (1966), existe una variación tanto latitudinal como altitudinal en el número de embriones por camada.
Pearson (1951) realizó colectas en el Perú, en las localidades de Pairumani y Santa Rosa (Andes Centrales del Perú) aproximadamente entre los paralelos 10 y 12 grados, menores a los de nuestra región de estudio, pero a alturas mayores (aproximadamente 3.500 m snm). Encontró un promedio de 5 embriones en A. boliviensis y 4 en P. darwini, sin embargo, no se halla detallada la desviación estadística.
Nuestros datos están de acuerdo con lo esperado pues existe una diferencia latitudinal, que implicaría encontrar un mayor promedio de embriones por camada, pero también existe una diferencia altitudinal que equilibra e iguala los promedios encontrados. La variación esperada es de 0,2 embriones por camada cada 100 m y de 0,1 embriones por camada cada grado latitudinal, por lo que la variación observada entre nuestros datos y los datos de Pearson (1951) es pequeña.
Según Luis y Granados (1990), además de la variación altitudinal y latitudinal debemos tomar en cuenta otros factores como el peso de la madre, su edad y el número previo de partos que ésta pudo tener. En el caso de A. boliviensis, los pesos promedio de las hembras preñadas fueron siempre superiores a 20 g. En un solo caso, se registró en marzo una hembra preñada con un peso de tan sólo 10,42 g y con 6 embriones contados. No parece existir correlación entre la edad o el peso y el número de embriones, pues durante ese mismo mes, todas las hembras tenían 6 embriones y sus pesos fueron muy variables, registrándose incluso, una hembra con 33,16 g, uno de los mayores pesos registrados.
4.7. Relación con los factores climáticos.
4.7.1. Efectos de la duración del día.
Para encontrar una relación entre las características reproductivas estudiadas y la longitud del día realizamos un análisis de regresión lineal. Los coeficientes de correlación encontrados para cada característica reproductiva están en la tabla 6.
Tabla 6: Coeficiente de regresión lineal, entre cada una de las características reproductivas estudiadas y, la longitud del día (L.D.), la temperatura (Temp.) y la precipitación (Prec.), para cada especie estudiada.
|
CARACTERISTICAS REPRODUCTIVAS |
Akodon boliviensis | Phyllotis darwini | ||||
|---|---|---|---|---|---|---|
| L.D. | Temp. | Prec. | L.D. | Temp. | Prec. | |
| Test. escrotales | 0,88 | 0,63 | 0,87 | 0,80 | 0,60 | 0,72 |
| Indice testicular | 0,83 | 0,72 | 0,69 | 0,79 | 0,83 | 0,63 |
| Vagina abierta | 0,49 | 0,52 | 0,39 | 0,49 | 0,52 | 0,39 |
| Prev. de preñez | 0,94 | 0,73 | 0,93 | 0,77 | 0,60 | 0,69 |
En el caso de A. boliviensis, la prevalencia de preñez está más influenciada por el fotoperíodo, seguida de la posición de los testículos. En cambio, en P. darwini, la mayor influencia se ejerce sobre la posición de los testículos.
Según Bligh (1976), el fotoperíodo juega un papel esencial sobre la espermatogénesis, ovulación y estro. Según Muul (1969), la respuesta de la reproducción al fotoperíodo se debe aun proceso acumulativo, que es disparado al sobrepasar una cierta cantidad de horas-luz. Esta acumulación puede hacerse entre los meses de agosto a noviembre, que es cuando existe un aumento efectivo en la duración del día. Además los meses de inactividad sexual (situados entre mayo y agosto) corresponden con la época en que la duración del día es menor. Si trazáramos una línea imaginaria entre estos meses, podría pensarse que luego de que la longitud del día supera las 11,35 horas/minutos, el mecanismo de respuesta al fotoperíodo es activado.
4.7.2. Efecto de la temperatura y precipitación.
Para analizar el efecto de la temperatura sobre la reproducción realizamos otra regresión lineal (tabla 6). En A. boliviensis, el mayor coeficiente de regresión (r = 0,73) está registrado para el índice testicular y para la prevalencia de preñez. En cambio, en P. darwini el coeficiente de regresión más alto (r = 0,83) se registra para el índice testicular.
Podemos observar entonces que la época fría corresponde con la época de inactividad sexual, mientras que el momento óptimo para la reproducción corresponde a los meses más cálidos, desde octubre hasta abril. La época donde los órganos se encuentran en estado reproductivo y los nacimientos son más activos, coinciden con la época más calurosa del año.
La temperatura no tiene un efecto tan evidente como la longitud del día. Según Bligh (1969), sólo el calor local puede causar un estrés térmico que cause esterilidad transitoria o total, aunque puede ejercer cierta presión sobre la espermatogénesis. Este hecho está reflejado en los coeficientes de regresión, pues todos los valores son menores a los encontrados en el caso de la regresión con la longitud del día. Según Rabinovich (1980), la temperatura y el fotoperíodo interactuan, para llevar al individuo a una actividad reproductora plena.
Finalmente, analizaremos el efecto de la precipitación sobre la reproducción. Los datos sobre la prevalencia de preñez tienden a apoyar la hipótesis de Louch et al. (1966) de que los cambios estacionales en la reproducción, pueden estar asociados a los cambios en la precipitación. La época de los nacimientos está ubicada después del final de la época seca y el máximo de previdencia de preñez, se registra durante el mes de febrero (uno de los meses más húmedos).
Estos resultados se contraponen con los obtenidos por Fleming (1973), quien encontró que el mayor porcentaje de actividad reproductiva, entre 47 especies de marsupiales y roedores de Panamá, se registra durante la época seca y no durante la época húmeda. Esto nos muestra la incertidumbre que aún existe acerca de cómo el factor de la precipitación puede, por sí solo, afectar a la reproducción.
Los coeficientes de regresión nos indican que las características reproductivas más ligadas a la precipitación son la previdencia de preñez en el caso de A. boliviensis y la posición de los testículos en P. darwini. Sin embargo, el coeficiente de regresión en el caso de la prevalencia de preñez, es aceptable (r= 0,69).
La alimentación es un factor que influye sobre el ciclo reproductivo (Sadleir, 1969;Piantanida, 1985;Chemineau, 1993); sin embargo, en el área de estudio y en el valle de La Paz, tanto A. boliviensis como P. darwini se acercan a un régimen alimenticio omnívoro (Mercado, 1990;1991) que les permitiría utilizar el alimento que encuentren disponible. Además, existe un fenómeno de “pseudo-domesticación”, pues ambas especies fueron capturadas ocasionalmente dentro de casas. Ambos factores hacen que el alimento se encuentre disponible todo el año, aunque no se hayan hecho estudios acerca de su calidad y abundancia.
Es también importante hacer notar que no se ha tomado en cuenta el factor social, que según Sadleir (1969), Meurling y Nyholm (1975)yRabinovich (1980), ejerce influencia para el inicio y terminación de la época reproductiva. Sin embargo es muy difícil realizar este tipo de estudio en condiciones silvestres, y poco probable que exista presión del factor social en ausencia de hacinamiento.
En resumen, de los tres factores climáticos tomados en cuenta: duración del día, temperatura y precipitación, podemos observar que la duración del día es el factor que ejerce mayor influencia sobre la reproducción, pitra ambas especies estudiadas. Con excepción de la relación temperatura - índice testicular en P. darwini, donde el coeficiente de correlación fue más alto que el obtenido con la duración del día (r = 0,84 y r = 0,82, para temperatura y duración del día respectivamente). Sin embargo no está de más hacer notar que estos tres factores ambientales no son independientes y se correlacionan entre sí.
4.7.3. Epoca óptima para la reproducción
En el ciclo anual de A. boliviensis, existen dos períodos claramente definidos: el primero corresponde al período de actividad sexual neta, donde la mayoría de los individuos adultos capturados estaban sexualmente activos (más del 50 %), y que se sitúa entre los meses de septiembre y abril. El período de inactividad sexual, con un porcentaje de 0 % de individuos activos se ubica entre los meses de junio a agosto. Sucede lo planteado por Chemineau (1993), quien afirma que los mamíferos limitan su reproducción a un período cuando el clima es menos rígido y la disponibilidad de alimentos abundante, es decir, al final del invierno e inicios del verano. Esta afirmación, sin embargo, era para zonas templadas.
P. Darwini presenta un comportamiento similar, pero con una época de actividad sexual más restringida, entre los meses de noviembre a abril. El resto de los meses presenta un porcentaje de individuos activos sexualmente menor al 50 %. Es interesante notar que los machos entran en actividad sexual antes que las hembras, y que éstas terminan su período de actividad sexual posteriormente a los machos. Este hecho está explicado porque, como indica Zuniño (1987), los machos deben estar preparados para la cópula cuando las hembras entren en estro, y posteriormente, las hembras siguen activas debido a la lactancia.
Según Asdell (1964)yVaughan (1969), los pequeños mamíferos que ocupan medios ambientes submontanos, se han adaptado de varias maneras al ciclo climático anual y a una corta época de crecimiento. Una de esas adaptaciones es la reproductiva, la cual hace que la época de nacimientos se limite o se reduzca a fin de elevar el éxito reproductivo.
Aparentemente, el factor altura, que es tomado por Sadleir (1969)yRabinovich (1980) como un “factor menor”, ejerce una influencia sobre la época reproductiva de tal manera que la limita a un período determinado del año. Ahora bien, la altura no debe tomarse como un factor por sí mismo, sino más bien debe pensarse en todos los factores climáticos sobre los cuales la altura causa variación.
La estacionalidad en la reproducción en latitudes mayores, está bien documentada por varios autores (Pearson, 1951;Crespo, 1966;Crespo et al., 1970) y en todos los casos que se refieren al hemisferio sur, la época reproductiva parece está suprimida totalmente durante los meses de invierno (junio, julio y agosto), aunque los límites son variables y tienden a extenderse mientras nos movemos más hacia el sur, llegando a incluir los meses de abril y mayo, como el caso de Akodon azarae en Buenos Aires (Crespo, 1966) y el sur de Córdoba (Crespo et al., 1970) en la República Argentina. Según afirma Asdell (1964), las camadas tienden a ser pocas entre julio y agosto, y en general, durante el invierno.












 uBio
uBio