Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Boliviana de Pediatría
versión On-line ISSN 1024-0675
Rev. bol. ped. v.49 n.3 La Paz 2010
COMUNICACIÓN ESPECIAL
Consenso de la Sociedad Latinoamericana de Infectología Pediátrica (SLIPE) sobre Neumonía Adquirida en la Comunidad (NAC), publicado en sitio web de SLIPE el 8 de Septiembre del 2010*
Comité de Infecciones Respiratorias de la Sociedad Latinoamericana de Infectología Pediátrica
Presidentes:
Dr. Enrique Gutiérrez Saravia (Colombia)
Dr. Raúl O. Ruvinsky (Argentina)
Coordinador:
Raúl O. Ruvinsky (Argentina)
Asesora permanente de este Consenso:
Dra. Carla Odio Pérez (Costa Rica): Presidenta de la SLIPE 2007-2009
Colaboradora en este Consenso:
Dra. Greta Miño León (Ecuador): Presidenta de la SLIPE 2009-2011
Participantes en la elaboración del documento y/o discusión en el plenario de Guayaquil (Ecuador), 12 Agosto de 2009:
Abdelnour Arturo (Costa Rica)
Arbo Antonio (Paraguay)
Arteaga Ricardo (Bolivia)
Bonilla Aníbal (Ecuador)
Castillo Olga (Venezuela)
Deseda Carmen (Puerto Rico)
Gentile Angela (Argentina)
Gentile Fernando (Argentina)
Galazka Jeannette (Uruguay)
Giachetto Gustavo (Uruguay)
Hernández Herminio (Perú)
Giglio Norberto (Argentina)
González Alemán Mabel (Cuba)
Grazioso Carlos (Guatemala)
Gutiérrez Saravia Enrique (Colombia)
Macías Parra Mercedes (México)
Montano Alicia (Uruguay)
Nascimento-Carvalho Cristiana (Brasil)
Odio Pérez Carla (Costa Rica)
Picón Teresa (Uruguay)
Pirez María Catalina (Uruguay)
Sarachaga María Julia (Uruguay)
Skarmeta Marcos (Chile)
Tirza de León (Panamá)
Profesionales Participantes y soporte de la industria farmacéutica para la realización del plenario en Guayaquil:
Dr. Cañé Alejandro (J. Wyeth)
Dr. Casellas Javier (GSK)
Dr. Debbag Roberto (Sanofi - Pasteur)
Dra. Grana María G. (Novartis)
Un especial agradecimiento a la Sra. Carmen Pereyra (Novartis)
y al Sr. Fernando Pilara de (GSK) por su dedicación para organizar el plenario
Articulo reproducido con permiso de la Sociedad Latinoamericana de Infectología Pediátrica (SLIPE) y que fue publicado en la revista de enfermedades infecciosas en Pediatría; noviembre 2010
Metodología:
Para la realización de este consenso sobre NAC, dirigido a todos los pediatras de Latinoamérica se desarrollaron las siguientes etapas:
1. Recopilación de evidencias a través de los estudios publicados en revistas médicas, presentados en congresos, colocados en distintos sitios de la web.
2. Calificación de cada informe siguiendo la tabla de grados de recomendación y calidad de evidencia (ver Cuadro N° 1).
3. Envío a los participantes de toda la bibliografía recopilada.
4. Organización del consenso en 10 temas designándose coordinadores y participantes según propuestas espontáneas de los infectólogos pediatras convocados.
5. Redacción de cada capítulo con la bibliografía correspondiente siguiendo el orden numérico del texto.
6. Corrección por el coordinador y la Dra. Carla Odio de todos los capítulos y reenvío para su evaluación y modificaciones a cada grupo de redacción.
7. Corrección final, adecuación por el coordinador y la Dra. Carla Odio y envío a todos los participantes para la corrección final.
8. Envío a Dra Greta Miño, Presidente SLIPE 2009 - 2011 para elevación a la página web de la SLIPE y envío a publicación en el órgano oficial de la SLIPE (Revista de Enfermedades Infecciosas en Pediatría).
9. Publicación de un resumen acotado en una revista indexada de habla inglesa.
10. Se realizará una actualización y revisión del documento en un año a partir de la fecha de publicación en el sitio web.

Temas y colaboradores:
1. Morbimortalidad:
Coordinadores:
Arturo Abdelnour, Raúl O. Ruvinsky
Integrantes:
Carla Odio, Ángela Gentile
2. Factores de riesgo
Coordinadores:
Raúl O. Ruvinsky, Arturo Abdelnour
Integrantes:
Ángela Gentile, Carla Odio, Herminio Hernández
3. Etiología de las NAC
Coordinadores:
Olga Castillo, Mabel González Alemán
Integrantes:
Antonio Arbo, Carla Odio, Cristiana Nascimento-Carvalho, Raúl O. Ruvinsky
4. Diagnóstico clínico
Coordinadores:
Herminio Hernández, Raúl O. Ruvinsky
5. Diagnóstico de Laboratorio
Coordinadores:
Carla M. Odio Pérez, Raúl O. Ruvinsky
6. Derrame Pleural
Coordinadores:
María C. Pírez, Mercedes Macías Parra
Integrantes:
Gustavo Giachetto, Jeannette Galazka, María J Sarachaga, Gabriela Algorta, Osvaldo Martínez, Antonio Arbo, Carlos Grazioso, Carla Odio Pérez, Fernando Gentile, Raúl O. Ruvinsky
7. Diagnóstico por imágenes
Coordinador:
Fernando Gentile
Integrantes:
Carla Odio, Carlos Grazioso, Ricardo Arteaga
8. Tratamiento antimicrobiano
Coordinadores:
Antonio Arbo, Carlos Grazioso
Integrantes:
Marcos Skarmeta, Tirza León, Cristiana Nascimento-Carvalho Ricardo Arteaga, María C. Pírez Gustavo Giachetto, Jeannette Galazka, María J Sarachaga, Gabriela Algorta, Osvaldo Martínez
9. Prevención
Coordinadores:
Ángela Gentile, Olga Castillo
Participantes:
Arturo Abdelnour, Carla Odio, Carlos Grazioso, Carmen Deseda, Raúl O. Ruvinsky,
10. Valoración Económica en la región
Coordinador:
Norberto Giglio
SIGLAS
Ac: Anticuerpos
ACIP: Comités Asesor en Prácticas de Inmunizaciones
Ag: Antígenos
AIEPI: Atención Integrada de Enfermedades Prevalentes de la Infancia
ARM: Asistencia respiratoria mecánica ATB: Antibiótico
AVAD: Años de vida ajustados en función de discapacidad
BAAR: Bacilos Ácido alcohol resistentes
β-L: β-lactámico
Bp: Bordetella pertussis
Carrier: Proteína transportadora
CHERG: Child Health Epidemiology Reference Group
C. pneumoniae: Chlamydophila pneumoniae
C. trachomatis: Chlamydophila trachomatis
CIE: Contrainmunoelectroforesis
CLSI: Comité Estadounidense de Estándares de Laboratorio
DALY's: Años perdidos por discapacidad
DHL: Deshidrogenasa láctica
DPN: Derrame Pleural Paraneumónico
EEUU: Estados Unidos de Norte América
EßHGA: Estreptococo ß-hemolítico del grupo A
EGB: Estreptococo ß-hemolítico del grupo B
ELISA: Enzimo-Inmuno-Ensayo
ENI: Enfermedad neumocócica invasora
ETI: Enfermedad tipo influenza
FR: Factor de riesgo
GB: Glóbulos Blancos
H: Hemaglutinina del virus influenza
HAART: Tratamiento antiretroviral de alta eficacia
Hib: Haemophilus influenzae tipo b
HAF: Hemaglutinina filamentosa de Bp
FC: Fijación de Complemento
IA: Influenza A
IFD: Inmuno Fluorescencia Directa
IFI: Inmuno Fluorescencia Indirecta
IRA: Infecciones Respiratorias Agudas
LPN: Leucocitos Polimorfo-Nucleares
MDG: Millenium Development Goal
M. pneumoniae: Mycoplasma pneumoniae
N: Neuraminidasa del virus influenza
NAC: Neumonía Adquirida en la Comunidad
NPB: Neumonía Probablemente Bacteriana
OMA: Otitis Media Aguda
OMS: Organización Mundial de la Salud
OPA: Opsonofagocitosis
OPS: Organización Panamericana de la Salud
PCR: Reacción en cadena de polimerasas
Pn: Pertactina de Bordetella pertussis
RIA: Radioinmunoensayo
RT-PCR: PCR en tiempo real
SAMR-AC: S. aureus meticilino-resistente adquirido en la comunidad
SAP: Sociedad Argentina de Pediatría
SARS: Síndrome agudo respiratorio severo
SRIS: Síndrome de respuesta inflamatoria sistémica
S. aureus: Staphylococcus aureus
ST: Serotipo
TAC: Tomografía axial computarizada
TP: Toxina de Bordetella pertussis
UCI: Unidad de Cuidados Intensivos
VES: Velocidad de Eritrosedimentación
Vacuna Conjugada Neumocóccica Heptavalente: VCN-7 V (Prevenar-7)
Vacuna Conjugada Neumocóccica Decavalente: VCN-lOV(Synflorix)
Vacuna Conjugada Neumocóccica Trecevalente: VCN-13 V (Prevenar-13)
Neumonía Adquirida en la Comunidad (NAC)
1. Morbimortalidad
A) Mundial
La Neumonía Adquirida en la Comunidad (NAC) es una de las causas infecciosas más frecuentes de morbi-mortalidad a nivel mundial; su magnitud y severidad se concentran en los niños < 1 año que residen en países en vías de desarrollo.
Anualmente se registran entre 140 y 160 millones de episodios nuevos de NAC con un 8% de hospitalización1; la tasa anual es de 270 por 100.000, principalmente entre los lactantes < de 2 años2. La letalidad promedio es del 4% en los pacientes hospitalizados y de < 1% en los ambulatorios.
Se ha estimado que de los 1,8 a 1,9 millones de defunciones reportadas en el año 2 000 en niños < de 5 años, el 30% correspondieron a NAC3. Esta cifra probablemente subestima la realidad ya que la información se extrajo exclusivamente de las muertes censadas en los hospitales. Las tasas de mortalidad por NAC varían regionalmente: 70% se registran en países en vías de desarrollo como África y Asia. Más de la mitad de los casos se han presentado en 5 países donde habita el 44% de los niños < de 5 años: India, China, Pakistán, Indonesia y Nigeria4-8. Según la Organización Mundial de la Salud (OMS), alrededor de 1.6 millones de las NAC invasoras se debieron a Streptococcus pneumoniae (S. pneumoniae). Este germen es responsable de 0,7 a 1 millón de las NAC en los niños < de 5 años que habitan en los países en vías de desarrollo, donde la tasa de ataque es 40 a 100 veces más elevada que la de los países desarrollados9-10.
De acuerdo a un análisis del hospital Johns Hopkins11, la mortalidad global por esta enfermedad descendió en más del 30% durante la última década; no obstante, en ciertos países y regiones continúa siendo inaceptablemente alta. Esto originó que entidades técnicas como el grupo Millenium Development Goal (MDG) propusiera reducirla en dos terceras partes durante el período comprendido entre 1990 y 2015. Para obtener datos confiables, trazaron como una de sus metas elementales determinar con certeza la mortalidad por NAC en niños < de 5 años12.
En el año 2 001 la OMS creó el grupo "Child Health Epidemiology Reference Group" (CHERG) integrado por expertos independientes; su objetivo consistió en la revisión sistemática de todos los casos de NAC y de las defunciones en < de 5 años de edad, a través de la optimización de los métodos de recolección de datos. Los resultados de este análisis sistemático mostraron que la incidencia anual de casos nuevos de NAC clínica era de 155 millones; de éstos, 151 millones se registraron en países en vías de desarrollo y el 10% correspondió a pacientes hospitalizados.
B) En América Latina
La información sobre la tasa de ataque poblacional de NAC bacteriana disponible en los países de América Latina es escasa. La OMS y la Organización Panamericana de la Salud (OPS) organizaron el programa "Infección Respiratoria Aguda" (IRA), actualmente extendido a la Atención Integrada de Enfermedades Prevalentes de la Infancia (AIEPI), que contribuyó al descenso de la mortalidad9. Según un informe de OPS, en 1999 fallecieron 550,000 niños < de 5 años en Latinoamérica y el Caribe; en 80,000 de ellos el diagnóstico de defunción fue IRA (NAC 85%). La etiología fue predominantemente bacteriana, con predominio de S. pneumoniae; la población más afectada fue la más deprivada social y culturalmente. En el 2002, se registraron en Latinoamérica 60.800 defunciones pediátricas por IRA, de éstas 18,000 fueron ocasionadas por S. pneumoniae13. Esto resultó en la pérdida acumulada de 617,000 "años de vida ajustados en función de discapacidad" (AVAD). Esta es la medida del número de años de vida perdidos o de discapacidad por esta enfermedad. El Proyecto "Carga de Enfermedad Global de la OMS" está procurando generar cálculos específicos de morbilidad atribuida a este germen en cada país. La cifra más alta de mortalidad se registró en Haití. Un meta-análisis presentado en un simposio en el 200714 mostró que la tasa promedio de NAC confirmada por Rx. de tórax en niños < de 2 años fue de 2,000/100,000. La NAC por S. pneumoniae fue de 51/100,000 y la letalidad del 8%. En este mismo meta-análisis, un análisis retrospectivo de vigilancia pasiva (niños hospitalizados) de carga de NAC por S. pneumoniae en niños < de 36 meses procedentes de dos áreas de Santiago de Chile fue de 90,6/100,000; en el análisis prospectivo de este mismo grupo etario la tasa fue de 60,2/100,000 y, en los de 12 a 23 meses, de 18,5/100,000. En Latinoamérica las tasas más bajas de mortalidad por NAC atribuida a S. pneumoniae se han registrado en Chile y Uruguay y las más altas en Bolivia, Perú y Guyana15.
Bordetella pertussis (Bp): Constituye un problema grave de salud pública debido a los brotes epidémicos que ocasiona. En Latinoamérica se han registrado más de 300,000 muertes anuales en lactantes < de 4 meses; la mayoría en países con bajas tasas de inmunización y altas tasas de mortalidad infantil16. Un porcentaje intermedio de estos casos presenta neumonía. Se ha demostrado que los adolescentes y los adultos son la fuente de transmisión del germen.
Haemophilus influenzae tipo b (Hib): Antes de la introducción de la vacuna conjugada, este germen fue una causa importante de morbimortalidad por NAC en niños < de 2 años17.
Staphylococcus aureus: Es causa infrecuente de NAC; predomina en neonatos y en lactantes ≤ 3meses. Durante los últimos 10 años la NAC por S. aureus meticilino-resistente adquirido en la comunidad (SAMR-AC) ha emergido y aumentado en forma gradual y consistente en todo el hemisferio occidental; se ha asociado a una morbimortalidad elevada18.
En Latinoamérica la OPS subvencionó varios estudios sobre carga de NAC probablemente bacteriana (NPB) aplicando un sistema evaluativo en el que la Rx. de tórax digitalizada fue analizada e interpretada por un observador único, estos fueron: en Brasil, Goiania; en Uruguay, Salto y Paysandú19. En Argentina, los Departamentos de Concordia y Paraná en la Provincia de Entre Ríos, y el Partido de Pilar en la Provincia de Bs. As.20-21; en la ciudad de Córdoba, una entidad privada efectuó un estudio de incidencia de NPB y de neumonía neumocócica; la tasa anual de NPB en los niños < de 5 años osciló entre 730/100,000 y 1,200/100,000 y, en los < de 2 años la tasa promedio fue de 2.000/100,00022. Se estima que en Argentina ocurren 30,000 casos anuales de NAC de etiología bacteriana en niños < de 5 años con una mortalidad de alrededor del 1 % (300 muertes anuales); la mayoría ocasionadas por S. pneumoniae. Algunos autores opinan que es necesaria una estimación más exacta de la carga de NAC23.
En Uruguay la tasa de ataque en niños < 5 años calculada por vigilancia pasiva de niños hospitalizados, fue de 1 152/100,000; en los < de 2 años fue más elevada19.
Las principales dificultades para estimar la verdadera incidencia de NAC y la mortalidad asociada se resumen a continuación:
1. Heterogeneidad en los criterios para la definición de caso
2. Falta de armonización de los criterios para considerar un infiltrado radiológico como consolidación; esto da lugar a reportes subjetivos que derivan en variaciones importantes de las tasas de incidencia.
3. La cuantificación de la mortalidad infantil por NAC depende de los registros de reporte y diagnóstico de causa de defunción. En Latinoamérica éstos oscilan entre 13% y 100%. Se ha observado que cuanto mayor es el porcentaje de notificación, el papel de la infección respiratoria disminuye como causa de muerte, y otras enfermedades y condiciones subyacentes adquieren mayor significancia.
El impacto que ha tenido la infección por el VIH en la mortalidad de los niños < de 5 años ha sido significativo, especialmente en África, donde la incidencia en embarazadas es alta. Es probable que gracias a la introducción gradual del tratamiento antiretroviral de alta eficacia (HAART), la tasa de mortalidad disminuya durante las próximas décadas24.
2. Factores de riesgo
La mortalidad por NAC en la infancia, en particular de etiología bacteriana, ha disminuido en las últimas décadas gracias a la identificación y difusión de los principales factores de riesgo (FR) de NAC severa25, (cuadro 2).
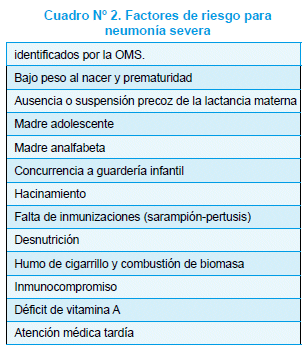
En los países en vías de desarrollo la tasa de morbi-mortalidad aún es inaceptablemente alta, especialmente en niños < 2 años. La disminución de la mortalidad en 2/3 partes para el año 2015 constituye la cuarta meta del milenio de la OMS/OPS, el grupo GAVI y la Sabin Foundation. Para lograrla, se han incrementando las tasas de inmunización contra Hib, el sarampión, la Bp, en todos los niños y el virus influenza en especial en aquellos con FR (ver recomendaciones del ACIP, Academia Americana de Pediatría). Dado que S. pneumoniae causa el mayor número de muertes por NAC en la población infantil, es primordial brindar una cobertura amplia con las vacunas antineumocócicas disponibles (ver capítulo prevención).
Un consenso de la Sociedad Argentina de Pediatría (SAP)26 identificó los siguientes FR para el desarrollo de NAC grave en niños < de 2 años de edad: < 3 meses, cardiopatía congénita, enfermedad pulmonar crónica, diabetes.
La NAC es más común en los meses fríos debido a que aumentan la diseminación de patógenos respiratorios de persona a persona, el hacinamiento, y disminuye la función mucociliar del huésped por la resequedad del aire ambiental. Pertenecer al género masculino, el tabaquismo activo y pasivo y el abuso del alcohol, aumentan el riesgo de NAC. La alimentación exclusiva al pecho materno durante los primeros meses de vida es un factor protector contra la NAC severa. Cuando sea necesaria la alimentación complementaria es importante que ésta aporte los nutrientes necesarios tal y como ha sido demostrado en varios estudios27-30. La leche materna es la única fuente de IgA US secretora, inmunoglobulina que evita la adherencia de virus y bacterias al epitelio respiratorio y funciona como anticuerpo específico.
Aproximadamente 44% de las muertes neonatales relacionadas a infección, incluyendo aquellas por IRA baja, y 20% de las que se presentan durante los primeros meses de vida con años perdidos por discapacidad (DALY's) fueron atribuidas a sub-óptima alimentación al pecho materno.
Fedson31 ha reportado una alta incidencia de cepas de S pneumoniae resistentes a la penicilina y de Hib productor de ß-lactamasa TEM-1. El hacinamiento, descrito como la convivencia y el dormir más de 3 personas en una misma habitación, situación frecuente en los grupos carenciados, favorece la colonización nasofaríngea de gérmenes patogénicos. La combustión de biomasa, presencia de fumadores en el hogar y la contaminación ambiental en general, bloquea la actividad ciliar, mecanismo fundamental para la defensa de la vía respiratoria. La desnutrición severa disminuye la inmunidad humoral y celular e incrementa la frecuencia de la NAC severa.
El uso amplio de vacunas para sarampión y Bp fue exitoso en la prevención de la NAC32. Las elevadas coberturas con vacunas contra Hib en casi todos los países y contra S. pneumoniae en algunos, redujeron la incidencia de NAC radiológica en 20%, según el estudio de Gambia desarrollado por Klugman y col.33.
Dos FR importantes en algunos grupos con deprivaciones socioeconómicoculturales señalados por la OPS, son la consulta tardía al servicio de salud, y la falla en la percepción del riesgo de NAC en el servicio de salud. En algunas regiones de Latinoamérica existe una relación directamente proporcional entre esta falla en la atención adecuada del niño con NAC y las elevadas tasas de derrame pleural y la mortalidad34.
Otros FR que inciden en la vulnerabilidad a la NAC, en particular neumocócica, son: bajos ingresos, nivel de educación deficiente, residencias de internos, la raza: en los Estados Unidos, los grupos de aborígenes americanos tienen la incidencia más alta de enfermedad neumocócica, seguidos por los afroamericanos.
Los niños con enfermedades subyacentes como la anemia de células falciformes, displasia broncopulmonar, reflujo gastroesofágico, asma, fibrosis quística, cardiopatía congénita y con el síndrome de inmunodeficiencia adquirida, corren un riesgo alto de complicaciones por NAC. Similarmente, los niños con enfermedades neuromusculares o convulsiones están en riesgo de neumonía aspirativa35.
Recientemente se puso énfasis en el suplemento alimentario con micronutrientes; la vitamina A y el zinc se asociaron a menor mortalidad, pero solo el zinc tendría efecto en la disminución de la NAC, según Hambidge y col.36. En síntesis, el uso adecuado de antibióticos para tratar NAC, el aporte de nutrientes incluyendo el suplemento de Zinc en algunas regiones, fueron considerados recursos necesarios para alcanzar las metas propuestas por la OMS, de descender la mortalidad infantil para el 201513.
No se conoce bien el mecanismo de la protección con zinc; existe evidencias que actúa a través de la fase aguda de la respuesta inmune a la infección; incluye a los macrófagos, los linfocitos, las células NK y la citotoxicidad anticuerpodependiente37,38; disminuiría el daño pulmonar relacionado a inflamación de la vía aérea y daño celular39. La información disponible es controversial: Un estudio informó que la suplementación con zinc resultó en una reducción escasa de las NAC, efecto limitado a niños con severa malnutrición proteica40. Por el contrario otro estudio realizado en Zanzíbar por Sazawal y col., zona endémica para malaria, informó reducción de 12% de mortalidad por NAC entre niños que recibían suplemento de zinc41.
En algunos países donde se informó déficit de vitamina A, su aporte en altas dosis constituyó un factor protector de NAC en niños42. En la India, el aporte de dosis elevadas de vitamina A disminuyó la mortalidad por NAC en el curso del sarampión, lo que fue también informado por otros autores43.
En síntesis, además del incremento en las inmunizaciones activas, la disminución de los FR mencionados fueron considerados recursos elementales para alcanzar la cuarta meta del milenio para el 201544.
3. Etiología de las NAC
Determinar la etiología de las NAC se dificulta debido a las siguientes causas:
1. En menos del 10% de los pacientes hospitalizados por NAC se aisla el germen en sangre. Este porcentaje aumenta cuando existe empiema y se cultiva una muestra del mismo.
2. En los niños, los gérmenes aislados del cultivo de muestras del tracto respiratorio superior corresponden a colonizantes usuales de la nasofaringe; los aislados del tracto respiratorio inferior son confiables, pero la obtención de la muestra usualmente requiere un procedimiento invasor como punción pulmonar, o métodos más sofisticados como la broncoscopía con cepillado y lavado bronco-alveolar. Los métodos para la obtención correcta de estas muestras y su debido procesamiento son poco accesibles en la mayoría de los hospitales. Usualmente se requiere la derivación del paciente a hospitales de atención terciaria y el envío de las muestras a laboratorios especializados o de referencia (ver el capítulo sobre diagnóstico etiológico).
Esto explica que la etiología de la NAC se logra documentar en el 27% y el 67% de los pacientes45.
Actualmente el S. pneumoniae es la bacteria predominante. El Hib era frecuente en < de 2 años antes de la introducción de vacunas conjugadas contra el mismo. La incidencia de Mycoplasma pneumoniae (M. pneumoniae) aumenta con la edad, especialmente a partir de los 5 años y, la de la Chlamydophila pneumoniae (C. pneumoniae) a partir de los 10 años, en particular en la adolescencia. La incidencia de esta última en < de 5 años fue subestimada durante años; actualmente se ha visto que es más frecuente que lo descrito anteriormente46,47. Chlamydophila trachomatis (C. trachomatis) es causa frecuente de NAC intersticial afebril en lactantes < de 4 meses de edad; se colonizan y/o se infectan en el canal de parto.
Los virus son la causa mas frecuente de NAC en los niños, especialmente en < de 2 años. En los < de 6 meses causan el 40% y entre los 6 meses y 2 años, el 30% de todos los casos. Por el contrario la etiología bacteriana aumenta con la edad: 25% en < de 6 meses y 40% en < de 5 años. La infección mixta o coinfección de virus y bacterias es aproximadamente del 23% en los < de 2; el daño ciliar que producen los virus predispone a la invasión y diseminación bacterianas45-48.
Los agentes causales varían con la edad, como se señala en el cuadro 335-48-51.
Etiología de las NAC con empiema: El derrame pleural paraneumónico se presenta entre el 0.6% y el 2% de los niños con NAC bacteriana; la tasa aproximada es de 3.3/100.00052. En dos reportes recientes provenientes de Estados Unidos de Norte América (EEUU)53,54, los casos de NAC con empiema aumentaron hasta 24% entre el 1993 y el 2001; luego declinaron a partir del año 2,000 con la introducción universal de la vacuna conjugada antineumocóccica. En un estudio sobre la incidencia de NPB (consolidante) en < de 5 años realizado en 2 áreas geográficas de Argentina: Pilar (Pcia. de Buenos Aires) y Concordia-Paraná (Pcia. de Entre Ríos), se identificó derrame pleural en el 8,8% y 13,3% de los casos, respectivamente20. En el estudio "Caribe"55 que incluyó a 240 niños con NAC por S. pneumoniae, procedentes de Argentina, Brasil y República Dominicana, se halló derrame pleural en el 54% de los casos. Se ha observado un aumento en la incidencia de los serotipos (ST) 1 y 19A en los > de 2 años y los < de 1 año, respectivamente. La NAC por S. aureus a menudo se asocia a derrame pleural; su incidencia ha aumentado en Latinoamérica a partir del 2,002, principalmente en los < de 1 año. El M. pneumoniae, la C. pneumoniae y los virus respiratorios raramente causan derrame pleural. En resumen, numerosas bacterias pueden ocasionar derrame pleural; la frecuencia varía según el tipo de germen, sus factores de virulencia, la susceptibilidad y la edad del paciente48 y para S. pneumoniae el ST.
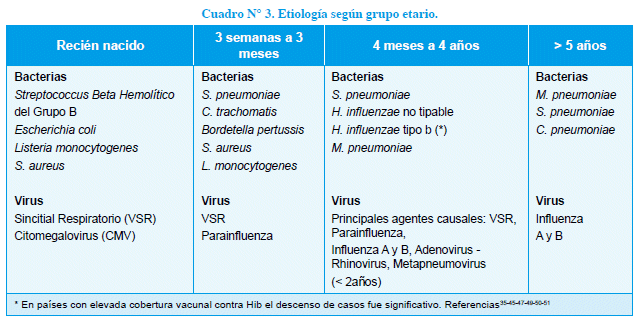
Agentes etiológicos:
S. pneumoniae: Coco Gram-positivo, posee una cápsula polisacárida que permite clasificarlo en 91 ST; constituye el principal factor de virulencia al evadir la fagocitosis por leucocitos polimorfonu-cleares y macrófagos. Puede ser resistente in vitro a la penicilina, las cefalosporinas de 3a generación y otros antimicrobianos. Es la bacteria que con mayor frecuencia produce NAC con consolidación en lactantes y preescolares. Existen diferencias geográficas y estacionales respecto a la predominancia de los STs. En Latinoamérica el proyecto SIREVA de la OPS aportó los datos de la vigilancia pasiva de ST y el patrón de resistencia antimicrobiana56. En el 2.005 los STs más frecuentemente aislados fueron: 14, 6B, 1, 5, 18C, 19F, 19A, 23F, 7F, 6A, 9V, 3 y 4; el ST 14 se encontró con mayor proporción en los < de 6 años. Con la reciente introducción de la vacuna conjugada de 7 ST a calendario en Costa Rica y Uruguay, es esperable cambios en el predominio de los ST aislados de sitios de colonización e infecciones invasivas.
S. aureus: Coco Gram-positivo que coloniza piel y mucosas en el 30-50% de los adultos y niños sanos; se transmite por contacto directo entre las personas. A partir del año 2 000 se publicaron reportes en EEUU57 de infecciones por S. aureus meticilino-resistentes adquiridas en la comunidad (SAMR-AC). Inicialmente se aislaron de infecciones de piel y faneras, posteriormente se incrementó la infección invasora. En el año 2.002 se describieron casos de enfermedad invasora en Uruguay58 y en el 2004 en Argentina59; la neumonía necrotizante fue una forma poco frecuente pero de mal pronóstico. La resistencia de este germen está codificada en el alelo IV del gen mecA que es de menor tamaño. Además, estas cepas contienen un gen que confiere el factor de virulencia que daña los leucocitos: la leucocidina de Panton-Valentine (LPV). Clínicamente debuta como una NAC rápidamente progresiva, asociada a elevada mortalidad60.
Hib: Cocobacilo Gram-negativo encapsulado, causa NAC en una proporción baja de la población infantil desde que se implemento la vacunación universal con la vacuna conjugada específica. Algunos países en desarrollo han reportado NAC por cepas de H. influenzae no tipificables; el diagnóstico fue hecho por medio de punción y aspirado pulmonar. Son difíciles de diagnosticar, usualmente no producen bacteriemia. En un estudio sobre NAC con derrame pleural realizado en la era prevacunal, el Hib fue responsable de 66.6% de las NAC en lactantes y niños de corta edad46. En países con altas coberturas de inmunización para Hib, este agente rara vez es causa de NAC46-49-61.
M. pneumoniae: Es el microorganismo más pequeño de vida libre; se han identificado 100 especies de las cuales 15 son patogénicas en humanos35; causa NAC en niños y adultos; su frecuencia aumenta a partir de los 5 años de edad y puede ser coinfectante junto con virus respiratorios y S. pneumoniae46-62.
C. trachomatis: Es un agente atípico que carece de pared celular; puede colonizar el canal de parto por lo que además de conjuntivitis neonatal también se asocia a NAC intersticial afebril en lactantes menores de 4 meses. Rara vez produce enfermedad severa que requiera hospitalización.
C. pneumoniae: Puede ocasionar NAC en niños de corta edad pero es más frecuente en los mayores de 10 años, adolescentes y adultos jóvenes.
Virus respiratorios: El VSR, parainfluenza 1, 2 y 3, influenza A (IA) y B y el adenovirus, son etiologías frecuentes de NAC en niños. El VSR es la causa más frecuente de bronquiolitis en los lactantes. El parainfluenza es más frecuente entre los 4 meses y los 5 años. El adenovirus puede causar una neumonía necrotizante con compromiso alveolar semejante a la observada con bacterias típicas y bronquiolitis obliterante con hiperlucencia o Síndrome de Sawer James. Otros virus respiratorios como los Rhinovirus50 también pueden causar NAC.
El virus Influenza pertenece a los Ortomyxovirus. Existen tres tipos: A, B y C y, en base a las proteínas de superficie, se clasifican en 9 subtipos de Neuraminidasa (N) y 15 de Hemaglutininas (H). Presenta cambios antigénicos de dos tipos: 1) menores (Drift) por mutaciones en los genes de H o N que originan nuevas cepas y 2) mayores (Shift) que sólo se produce en los virus A. Estos últimos consisten en la adquisición de un nuevo gen de H o N que conlleva a la producción de un nuevo subtipo capaz de ocasionar pandemia cuando la población es susceptible. En Venezuela el IA circula todo el año; aumenta entre mayo y agosto y de octubre a noviembre, principalmente en niños < de 9 años63 64.
Durante la última pandemia por IA emergió un nuevo virus originado por intercambios genéticos entre un tipo porcino, uno aviar y otro humano, el (H1N1) swl. Esta se originó en México entre marzo y abril del 2009 y se expandió rápidamente a casi todos los países del mundo. Se reportaron casos de NAC en lactantes, niños, y adultos jóvenes, en particular entre 20 y 40 años. La mortalidad fue del 8% en pacientes hospitalizados y 1% en la población general. Los más afectados fueron personas con enfermedades subyacentes como inmunodeficiencia, diabetes tipo 2, cardiopatías y neumopatías crónicas. También lo fueron las mujeres embarazadas y las personas con obesidad mórbida. En Argentina el brote se extendió a una gran parte de la población, especialmente durante las semanas epidemiológicas 21 y 25 en las que desplazó a otros virus como el VSR y el IA estacional. En Octubre del 2009 se presentó una segunda ola epidémica en EEUU. En el año 2010 se está aplicando la vacuna específica para la cepa pandémica, monovalente, con elevada cobertura en Argentina, donde hasta la semana epidemiológica 30 se denunciaron menos de 20 casos, lo que expresa la baja tasa de ataque. Esta situación epidemiológica favorable fue informada a nivel mundial por la OMS.
Virus respiratorios emergentes:
1. Metapneumovirus: Produce infección en lactantes, en individuos de la 3a edad y en los inmunocomprometidos. Después del VSR es la causa más frecuente de bronquiolitis.
2. Coronavirus: Un clon de este grupo causa un síndrome agudo respiratorio severo (SARS). Predomina en el Sureste asiático y en adultos; la mortalidad por esta infección es elevada.
3. Bocavirus: Fue aislado en el 2005 en Tailandia; se ha reportado en el 4.5% de niños< de 5 años con NAC que requieren hospitalización. La mayoría de los casos se asocian a coinfección con otros virus65.
4.Diagnóstico
Diagnóstico clínico:
Definición: Neumonía es la infección aguda del parénquima pulmonar con signos y síntomas de compromiso lobar o segmentario, puede ser uni o multifocal, configurando la bronconeumonía66. La respiración rápida y profunda o taquipnea, denota el compromiso pulmonar, la fiebre expresa la respuesta inflamatoria al proceso infeccioso y la tos, la irritación de la vía aérea.
Cuadro Clínico: A grandes rasgos se puede decir que las manifestaciones clínicas dependen de si la neumonía es con condensación o típica, o si es de compromiso intersticial, o atípica. Esta terminología ha perdido vigencia pero aún se utiliza en la práctica diaria.
Neumonía típica o consolidada: Es de instalación aguda, con fiebre elevada, tos y taquipnea con tiraje marcado.
La OMS diseñó un programa7 para el manejo estandarizado de las IRA. Está dirigido a todos los integrantes del equipo de salud y la comunidad con el objetivo de capacitar sobre el diagnóstico temprano y tratamiento oportuno de la NAC. Ha contribuido significativamente al descenso de la mortalidad. Define la presencia de taquipnea de acuerdo a la frecuencia respiratoria según el grupo etario: más de 40' en niños > de 1 año; más de 50' entre 2 meses y 1 año; más de 60' en < de 2 meses de edad9. Para los niños de 3 o más años la frecuencia respiratoria debe ser < 3067. Es importante señalar que estos puntos de corte tienen sensibilidad y especificidad mayor de 80% para el diagnóstico de NAC en ausencia de sibilancias (que expresan obstrucción de los pequeños bronquiolos). La frecuencia respiratoria se debe medir en el niño tranquilo, sin llanto y durante un minuto. El tiraje es signo de riesgo e indicación de atención hospitalaria.
La taquipnea es la respuesta fisiopatológica a la hipoxemia producida por la alteración del intercambio gaseoso a nivel del alvéolo; cuando ésta aumenta se traduce clínicamente como dificultad respiratoria con retracción del tórax o tiraje. Este inicialmente es subcostal, luego intercostal y supraesternal con compromiso de otros grupos musculares. Si no se compensa la hipoxia, el niño presentará cianosis y aleteo nasal que son signos de mal pronóstico68. La taquipnea y tiraje, signos cardinales señalados por OMS, demostraron tener alto valor predictivo para el diagnóstico de NAC, según los estudios clásicos de Shann, Spooner y Levental en < de 2 años69-70. El tiraje se manifiesta como una retracción de la base del tórax en inspiración; cuando el cuadro se agrava el paciente suele presentar aleteo nasal y quejido espiratorio, signos tardíos de hipoxia; la presencia de cianosis y reacciones de alarma como taquicardia o bradicardia, hipertensión o hipotensión arterial, obnubilación, convulsiones y coma, expresan un riesgo alto de muerte. Otros compromisos del estado general incluyen: somnolencia o irritabilidad, malestar, palidez, fascies ansiosa, vómitos, epigastralgia y distensión abdominal.
La tos, síntoma no siempre presente en < de 2 años, puede tornarse productiva con esputo denso y aún herrumbroso en niños > de 8 años; en estos casos es frecuente que el paciente refiera dolor torácico, en particular durante la inspiración (puntada de costado)71. Con menor frecuencia se han descrito otros signos: meningismo, esplenomegalia y exantemas entre otros; ello dependerá de la etiología o del número de órganos y sistemas comprometidos por el patógeno. Cuando la NAC se localiza en la base derecha del pulmón los paciente pueden presentar dolor en la fosa ilíaca derecha simulando un cuadro apendicular.
En el neonato la NAC puede debutar clínicamente con crisis de apnea, cianosis o con clínica de sepsis: rechazo del alimento, letargia, hipotonía, vómitos, distensión abdominal, palidez, cianosis, hipotermia, y grados variables de compromiso respiratorio como taquipnea, tiraje, aleteo nasal, estridor, quejido espiratorio y descenso de la barbilla. En ocasiones la auscultación pulmonar puede ser normal y la fiebre de bajo grado.
Se destaca la disminución de la mortalidad en sitios donde se aplicó el programa de signos y síntomas predictivos de NAC bacteriana desarrollado por la OPS72.
Cuando el paciente requiere hospitalización es importante su monitorización continua con saturómetría digital para detectar tempranamente la hipoxiasevera (< 90%), y la medición de gases arteriales. En pacientes con pO2 < de 55 mm de Hg y pCO2 > de 60 mm de Hg. se recomiendan la intubación y la ventilación mecánica electivas. En el cuadro N° 4 se describen los signos cardinales de la neumonía con consolidación de probable etiología bacteriana.

En el cuadro N° 5 se describen los signos de alto riesgo que requieren atención en la unidad de cuidados intensivos.

La semiología se caracteriza por los signos y síntomas del síndrome de condensación: Disminución del murmullo vesicular, generalmente unilateral y predominantemente derecho; estertores finos crepitantes o subcrepitantes y soplo tubario, ambos al final de la inspiración. La presencia de broncofonía y de pectoriloquia áfona son variables. La matidez a la percusión es poco frecuente en niños; expresa consolidación parenquimatosa y/o derrame pleural.
Todo lo anterior es altamente predictivo de que sea un proceso bacteriano.
Puede ser difícil determinar radiológicamente si una NAC presenta consolidación o se trata de un infiltrado intersticial68. La radiografía de tórax (Rx tórax) es útil para certificar la presencia de neumonía, pero no es imprescindible para decidir el inicio de tratamiento antibiótico ante un cuadro clínico con sospecha alta de NAC bacteriana, Ejemplo: cuando en el centro de salud que recibe al paciente no se cuenta con este recurso diagnóstico.
Varios estudios de carga de NAC en niños de Brasil, Uruguay y Argentina, han comparado el reporte radiológico de condensación hecho por pediatras del hospital con el de un radiólogo de referencia y han encontraron una discordancia del 15% al 25%21.
La mayoría de los casos de NAC con consolidación son causados por bacterias que colonizan habitualmente la vía aérea superior, en particular S. pneumoniae y menos frecuentemente Hib. El S. aureus predomina en neonatos; es infrecuente como causa de NAC en otras edades. La neumonía estafilocócica se caracteriza por evolucionar rápidamente hacia el deterioro clínico y radiológico. El paciente usualmente luce tóxico y presenta gran dificultad respiratoria. En la Rx. de tórax a menudo se observan: Derrame pleural, pneumatoceles, abscesos e infiltrados que tienden a confluir; rara vez se observa broncograma aéreo. El derrame pleural se observa en el 10% al 40% de los casos y usualmente traduce empiema; también se puede observar pioneumotórax o neumotorax hipertensivo. Debido a la rápida evolución radiológica, es recomendable repetir la Rx. De tórax, especialmente cuando el paciente evoluciona mal clínicamente. Cuando el derrame pleural es extenso, el drenaje de tórax es necesario. Los criterios de internación según fueran propuestos por el consenso de la Sociedad Argentina de Pediatría (SAP)73, se señalan en el cuadro N°6. Estos aplican para todos los grupos etarios pero en especial para los niños < de 2 años.

En conclusión, la detección de un síndrome de consolidación en una determinada área pulmonar es altamente sugestivo de proceso bacteriano.
Neumonías atípicas: La presencia de fiebre, tos, taquipnea, timpanismo a la percusión, espiración prolongada, sibilancias y estertores subcrepitantes difusos (en ambos tiempos respiratorios, cambiantes con la tos y con maniobras kinésicas), orientarán hacia un síndrome bronquiolítico de etiología viral, especialmente a VSR durante el invierno y en lactantes < de 1 año de edad. Otros virus causales pueden ser: Adenovirus, Influenza, Parainfluenza. Los infiltrados generalmente son de tipo intersticial, difusos y bilaterales. En algunos casos no es posible diferenciar clínica ni radiológicamente los procesos virales de los bacterianos. Este cuadro puede estar dado también por bacterias atípicas como M. pneumoniae, C. trachomatis, C. pneumoniae, y Bp, entre otros.
La neumonía intersticial afebril con tos persistente en infantes < de 4 meses orientará a C. trachomatis (colonizante del tracto genital materno) como agente etiológico, especialmente si existe historia de conjuntivitis neonatal.
Durante la edad escolar, la presencia de tos intensa, irritativa, a menudo dolorosa, acompañada a veces de mialgia, cefalea, fiebre, con presencia o no de sibilancias, orientará a M. pneumoniae y a C. pneumoniae. Es común la disociación clínicoradiológica74.
La tos de tipo coqueluchoide en lactantes y niños de corta edad, o las crisis de cianosis, apnea, o convulsiones en lactantes de los primeros meses de vida, orientarán a otros agentes etiológicos de la neumonía, como la Bp. Debe pensarse en este germen cuando existen antecedentes epidemiológicos familiares e intradomiciliarios. En adolescentes y adultos la causa más frecuente de tos persistente y prolongada es Bp. La Rx de tórax es inespecífica; se pueden observar infiltrados hiliofugales, intersticiales, bronconeumonía confluente segmentaria, imágenes pericárdicas poco densas con aspecto "espinoso" que corresponden a pequeñas atelectasias. Los niños > de 5 años con NAC y compromiso pleural (complicación frecuente de la neumonía bacteriana) pueden referir dolor torácico homolateral que se exacerba durante la inspiración profunda (pleurodinia). En estos casos es frecuente hallar matidez, disminución del murmullo vesicular, ausencia de las vibraciones vocales en la base pulmonar afectada, principalmente si hay derrame pleural. Este tema será desarrollado en el capítulo sobre derrame pleural.
5. Diagnóstico de Laboratorio
Pruebas para el diagnóstico microbiológico
La mayoría de las NAC en niños son de causa viral y se pueden manejar ambulatoriamente; en estos casos, en general, no se realizan estudios para documentar la etiología (salvo si son incluidos en protocolos de investigación). En niños que se internan, suelen realizarse estudios de pesquisa microbiológica orientados según el perfil clínico y radiológico, la edad, la situación epidemiológica, la cobertura vacunal y la evolución del cuadro clínico y radiológico.
Las pruebas de diagnóstico de Laboratorio se pueden clasificar en inespecíficas y específicas (cuadro N°7)
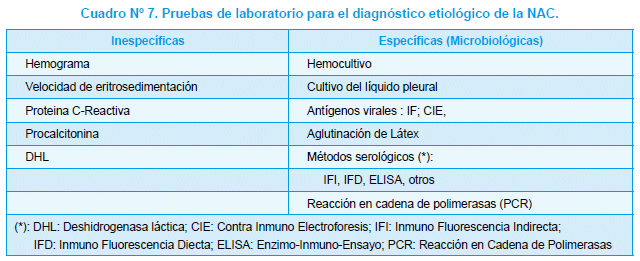
Pruebas Específicas
a) Cultivos: En los niños hospitalizados se deben obtener dos muestras de sangre de 1-2, 2-3 y 3-5 ml en promedio para neonatos, lactantes y niños menores de 40 Kg respectivamente, tomadas con 20 minutos de diferencia entre una y otra y de dos venas periféricas diferentes para hemocultivo; en < del 10% de los niños con NAC supuestamente bacteriana se aisla el agente etiológico de sangre. No hay datos que sugieran que el momento de la toma del hemocultivo en relación a la aparición de la fiebre o escalofríos maximizará el rescate bacteriológico. En el estudio de Concordia y Paraná patrocinado por la OPS, el aislamiento bacteriano fue del 7,1% y 6% respectivamente; se aisló S. pneumoniae en la mayoría de los casos20. Se debe cultivar cualquier lesión de piel con sospecha de infección bacteriana. Se debe obtener una muestra del líquido pleural en caso de que hubiere derrame importante, para tinción de Gram, celularidad, bioquímica (ver sección sobre derrame pleural) y cultivo. En los pacientes sépticos, con trastornos del sensorio o con signos meníngeos, se debe obtener por medio de una punción lumbar, una muestra del líquido cefalorraquídeo para tinción de Gram, celularidad, bioquímica y cultivo.
En niños, el cultivo de esputo no es útil ni específico porque la muestra refleja la flora oral. En los adolescentes puede ser útil cuando tiene < de 10 células epiteliales / campo y más de 25% de leucocitos polimorfo-nucleares/campo.
b) Métodos serológicos: Detectan antígenos (Ag) o anticuerpos (Ac), no siempre son asequibles, la estandarización es pobre, son de baja especificidad y sensibilidad.
c) Amplificación de ADN: La reacción en cadena de polimerasa es un método molecular que amplifica el ADN bacteriano, el viral y el fúngico; ha incrementado ostensiblemente la identificación etiológica de las NAC.
El principal reto para el pediatra ante un lactante o niño con NAC, es el de poder predecir si la etiología es bacteriana o viral y así poder tomar tempranamente la decisión del inicio o no de los antibióticos guiados por la edad del paciente, las condiciones subyacentes del mismo y la historia o el contexto epidemiológicos. Los métodos de laboratorio, aún con sus limitaciones, contribuyen con la toma de decisiones terapéuticas.
Pruebas inespecíficas
Hemograma: Debería realizarse sistemáticamente en niños con NAC que requieren hospitalización. Un recuento de Glóbulos Blancos > de 15.000/ mm3 con neutrofilia > del 70%, orienta a etiología bacteriana; no obstante, menos del 60% de los pacientes con NAC bacteriana van a tener estos recuentos inicialmente75-76. En un estudio prospectivo sobre la incidencia de NAC de etiología probablemente bacteriana realizado en Argentina, la leucocitosis tuvo un alto valor predictivo positivo pero no así la neutrofilia77-21. El recuento de GB y los reactantes de fase aguda como la proteina C reactiva, la VES y la procalcitonina (PCT) pueden servir de parámetro de respuesta terapéutica durante la evolución de la NAC.
Reactantes de fase aguda: La VES y la Proteína C Reactiva son de baja sensibilidad y especificidad para diferenciar etiología bacteriana de viral; la PCT es altamente sensible y específica para este fin76. Cuando la VES es > de 30 mm en la 1o hora, orienta hacia un proceso inflamatorio sistémico. El consenso de la SAP determinó que no es concluyente para diferenciar entre etiología bacteriana y viral26. La Proteina C Reactiva cuantitativa orienta hacia un proceso inflamatorio infeccioso cuando es > de 40 mg/L; no es concluyente pero sí orientadora para diferenciar etiología viral de la bacteriana78. En un meta-análisis que incluyó 1.230 niños con NAC, la proteína C reactiva > de 35-60 mg/L fue prevalente en las NAC de origen bacteriano: OR=2.58 (95% IC: 1.20-5.50)79.
La PCT es una molécula precursora de la calcitonina; Muller y col.80 hallaron niveles elevados en infecciones bacterianas y bajos en las virales. Según Briel y col.81 y otros82-83, es un marcador potencialmente útil para distinguir entre infección viral y bacteriana; además, fue un marcador útil para prescribir o no antibióticos. El punto de corte que utilizaron para determinar si se trataba de un proceso bacteriano o no, fue de > 0.25 μg/ml ; esto permitió disminuir el uso de antibióticos en el 72% de los casos. En el estudio de Korppi su valor fue limitado84.
Lácticodehidrogenasa (DHL): Según Rydell y col.85 los niveles elevados traducen necrosis celular y licuefacción pulmonar. Se han reportado niveles altos en el líquido pleural de niños con empiema y neumonía necrotizante extensa83. Es liberada por células que sufren necrosis primaria o secundaria. Se sintetiza y libera principalmente por los leucocitos polimorfonucleares apoptóticos que sufren necrosis secundaria84.
Aplicación práctica de los métodos de diagnóstico específicos e inespecíficos
1. NAC presuntivamente viral:
En pacientes que ameritan hospitalización por bronquiolitís, o por infiltrados intersticiales, es importante el identificar la presencia de virus respiratorios por medio de la inmuno fluorescencia indirecta (IFI). Esta detecta Ag virales (VRS, adenovirus, virus influenza, virus parainfluenza II y III, metapneu-movirus) en las células del aspirado nasofaríngeo y su resultado se puede obtener en < 2 horas. Es altamente específico y sensible cuando se realiza precozmente86. El cultivo viral positivo de secreciones respiratorias nasofaríngeas o bronquiolares certifica infección viral, pero no es útil ni práctico para la toma rápida de decisiones ya que el resultado dura varios días en obtenerse y la metodología es poco asequible87.
El método diagnóstico más sensible para el metapneumovirus es la PCR en tiempo real (RT-PCR) pero no está disponible en la mayoría de los nosocomios88.
El Multiplex es un método rápido de diagnóstico que se puede efectuar en pacientes de manejo ambulatorio. Esto implica un importante avance en la evaluación y manejo de las IRA bajas en niños; su limitante es la poca accesibilidad del método en la práctica clínica89.
El método diagnóstico inicial para el virus Influenza A (H1N1) consistió en su aislamiento por medio del cultivo de las secreciones nasofaríngeas y bronquiolares en líneas celulares. No obstante, en un período de 3 a 4 semanas se desarrolló una RT-PCR que logró el diagnóstico definitivo en pocas horas. Este método diagnóstico permitió certificar su circulación en la comunidad y tomar las medidas adecuadas para su contención. En la fase de mitigación de la pandemia, el diagnóstico por laboratorio se limitó a pacientes internados con NAC para decidir el tratamiento antiviral con oseltamivir o zanamivir (informes de OMS, CDC).
2. NAC probablemente bacteriana
Lo idóneo en el paciente hospitalizado es obtener 2 muestras para hemocultivo90. En el estudio multi-céntrico "Caribe" de OPS91, se aisló S. pneumoniae de sangre en el 10% (N=91) de 990 casos de niños argentinos con NAC probablemente bacteriana. En países en los que se aplicó ampliamente la vacuna conjugada anti-neumocócica, como EEUU, la prevalencia de S. pneumoniae en niños descendió significativamente (1,6%)92.
Otros métodos de identificación de bacterias típicas:
Para la búsqueda de S. pneumoniae, Hib y EGB, existen métodos rápidos que detectan los Ag polisacárídos por medio de CIE y aglutinación de partículas de látex; adolecen de ser poco específicos y poco sensibles: Alto porcentaje de falsos positivos y falsos negativos, respectivamente. Por su alto costo y poca eficiencia no se recomienda su uso rutinario en niños con NAC93-94.
Las técnicas de diagnóstico molecular como la RT-PRC incrementan dramáticamente el porcentaje de identificación etiológica de los patógenos comunes como el S. pneumoniae y el tiempo para obtener la información es corto. Su mayor inconveniente es la falta de estandarización y el poco acceso de los mismos en los sistemas de salud pública95. El test rápido (ELISA-Dot) es económico, tiene buena especificidad y sensibilidad para la detección de Ag de S. pneumoniae96.
En resumen:
1. Los exámenes diagnósticos habituales no son idóneos para el diagnóstico etiológico de la NAC bacteriana en la infancia.
2. Las reacciones de complejos Ag-Ac desarrolladas en las últimas dos décadas y la PCR han mostrado resultados contradictorios; no obstante, la sensibilidad y especificidad de los mismos están aumentando. También, cada vez se cuenta con técnicas de PCR que abarcan mayor número de bacterias y virus. La PCR será un método de diagnóstico etiológico útil y asequible en la mayoría de los hospitales de atención terciaria en un futuro cercano.
3. La proteína C reactiva y la procalcitonina son útiles para el diagnóstico de NAC bacteriana.
4. La RT-PCR cuantitativa de secreciones del tracto respiratorio inferior está siendo investigada; los resultados preliminares son prometedores97.
Conclusiones:
1. El hemograma es útil pero no imprescindible para decidir el inicio del tratamiento antibiótico.
2. No realizar el esputo para diagnóstico bacteriológico.
3. Limitar el hemocultivo a niños hospitalizados.
4. No solicitar Ag. en orina ya que su interpretación se presta a confusión.
5. Es útil determinar antígenos bacterianos en líquido pleural en casos de derrame pleural.
6. Cuando exista la sospecha de tuberculosis pulmonar se deben realizar una PPD y la búsqueda de bacilos ácido alcohol resistentes (BAAR) en esputo y en secreciones bronquiales (cuando se cuente con la infraestructura para una broncoscopía con cepillado y lavado bronco-alveolar).
3. Métodos diagnóstico para bacterias atípicas:
El desarrollo de métodos para diagnóstico de bacterias atípicas incrementó la proporción de casos con documentación etiológica, en especial en países desarrollados con mayor disponibilidad de recursos.
M. pneumoniae: Técnicas inmunológicas: IFI, fijación de complemento (FC) y la microaglutinación utilizan Ag lipídicos y proteicos que componen su membrana celular; tienen la limitante de múltiples reacciones cruzadas con glicopéptidos98. También se cuenta con métodos serológicos que detectan Ac. específicos como la hemaglutinación indirecta, el test de ELISA, la inhibición de crecimiento, la inmunoprecipitación, el radioinmunoensayo (RIA), la inhibición de la adherencia, la radioinmunoprecipitación. Una elevación en el título de Ac de 4 diluciones entre una muestra inicial y otra convalesciente (15-21 días entre ambas), determinadas por la FC, o una titulación única > 1:256 sugieren infección reciente99.
Las aglutininas frías o crioaglutininas son inespecíficas pero sensibles para determinar el diagnóstico etiológico de este germen. Su sensibilidad consiste en que son positivas en más del 70% de los casos y su inespecifidad, en que pueden positivizarse por otros microorganismos com VEB, CMV, Klebsiella pneumoniae, o por procesos malignos y autoinmunes100. Se han observado títulos elevados en el 18% de los casos de NAC por adenovirus101. La magnitud de los títulos guarda una relación directamente proporcional con la gravedad de la NAC.
Los métodos diagnósticos más utilizados son la IF y el ELISA. La identificación de IgM e IgA en una única muestra sérica y la elevación en cuatro diluciones de los títulos de IgG en muestras pareadas, tomadas en la fase aguda y convalescente, tienen una sensibilidad y especificidad similar a la FC; pueden persistir elevadas por varios meses. Por esta razón es conveniente que la muestra única sea confirmada por las con muestras pareadas.
La reacción en cadena de polimerasa de las secreciones nasofaríngeas es altamente sensible y específica pero poco asequible.
Chlamydophila trachomatis: El diagnóstico de la infección aguda por este germen se puede establecer por medio de la micro IF y de una IgM sérica > 1:32; la sensibilidad varía entre 33% y 90%102.
El Enzimo Inmuno Ensayo (EIA) de muestras del tracto respiratorio inferior ha sido aprobado por la FDA; es sensible y específico en infantes < de 4 meses. La PCR ha sido aprobada por la FDA pero la experiencia con esta prueba es limitada. Es más sensible para muestras obtenidas de la conjuntiva ocular que de las secreciones respiratorias.
Chlamydophila pneumoniae: Su aislamiento del cultivo de secreciones nasofaríngeas en líneas celulares H-Ep-2 es dificultoso y poco práctico ya que generalmente requiere > 7 días para su positivización.
El diagnóstico serológico se puede hacer por medio de la micro IFI que detecta IgM, IgA, IgG pero es poco accesible. Un título de IgM > 1:16 o de IgG > 1:512 indican infección aguda; no obstante, la elevación de IgG > de 4 diluciones en 2 muestras pareadas, obtenidas en la fase aguda y la convalescente es el método más sensible y específico y el único aceptado por la FDA 103. Lo anteriormente mencionado se debe a que la IgM puede no detectarse sino hasta la 3o semana del inicio de la infección y la IgG aún después.
La PCR es promisoria como método rápido de diagnóstico pero tanto el método utilizado como la lectura de los resultados aún no se han se han estandarizado.
6. Derrame Pleural
Se define como acumulación de líquido en el espacio pleural. En el cuadro N° 8 figuran las características que permiten diferenciar entre el exudado inflamatorio de una NAC y el de un trasudado secundario a hipoalbuminemia, insuficiencia cardíaca congestiva, cirrosis hepática con ascitis, mixedema, diálisis peritoneal, malignidad y, síndrome de distress respiratorio tipo adulto104.
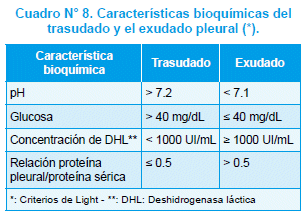
El derrame pleural para-neumónico (DPN) se define como la acumulación del exudado pleural inflamatorio adyacente a una neumonía generalmente bacteriana. Raramente se encuentra derrame pleural exudativo por causas no infecciosas. El germen más frecuentemente aislado es S. pneumoniae, seguido por S. aureus o por el Hib en niños no vacunados o con plan incompleto de la vacuna para Hib como causa de NAC y de derrame exudativo asociado105. La historia clínica y los antecedentes epidemiológicos pueden orientar hacia otros microorganismos menos frecuentes como los virus respiratorios, las bacterias atípicas y el Mycobacterium tuberculosis106.
Las manifestaciones clínicas del DPN son similares a las que se presentan en un niño con NAC (ver capítulo correspondiente). La fiebre sostenida y el dolor intenso a la inspiración profunda son característicos del compromiso pleural. Se pueden hallar una menor movilidad del hemitórax afectado, escoliosis ipsilateral, matidez a la percusión y disminución o ausencia de las vibraciones vocales y del murmullo vesicular. En general el niño presenta mal estado general, se encuentra tóxico y taquipneico.
Los pacientes con derrame pleural exudativo a menudo presentan complicaciones pulmonares como neumatoceles, pioneumatoceles, neumotorax, pioneumotórax simple o hipertensivo, fístula pleuro-pulmonar, absceso pulmonar. Los hallazgos radiológicos del DPN consisten en velamiento o borramiento del ángulo costo-diafragmático, presencia clara de línea de derrame en la Rx de tórax tomada en decúbito ipsilateral con rayo tangencial, opacidad en la proyección posteroanterior, y opacidad basal que borra el hemidiafragma del lado afectado. Estos hallazgos se hacen evidentes cuando el volumen de la colección pleural es ≥ 75 ml . La ecografía puede detectar derrames de 10 ml . Esta herramienta diagnóstica es útil para diferenciar entre derrame pleural y consolidación; también lo es para detectar bridas pleurales que dan lugar a loculaciones. La TAC no supera a la ecografía; se utiliza cuando se desea detectar masas ecográficas dudosas, absceso pulmonar, o para la localización exacta de lesiones pulmonares o pleurales en pacientes que requieren intervención quirúrgica mayor. El DPN se clasifica como no complicado cuando presenta un pH entre 7.2 y 7.3, glucosa > de 40 mg/dL, DHL entre 500 y 1000 UI/L, el líquido pleural es de aspecto claro, con escasa celularidad a predominio de LPN y el cultivo es generalmente estéril.
El DPN complicado o empiema macroscópicamente luce purulento o seropurulento; se observan bacterias en la tinción de Gram, se aislan bacterias al cultivarlo, o se detectan en el mismo Ag capsulares. Los criterios citológicos y bioquímicos más aceptados para su diagnóstico son: pH ≤ 7,1; DHL ≥ 1.000 UI/L, glucosa ≤ 40 mg/dl, leucocitos ≥ 103/mm3, LPN ≥ 90%.
La evolución del empiema cuenta con 3 etapas: la exudativa, la fibrinopurulenta y la organizada. Durante la etapa exudativa el líquido es escaso y sin tabiques o bridas pleurales. En la etapa fibrinopurulenta el derrame es espeso, se forman tabiques o septos de fibrina que lo definen como empiema loculado. En esta etapa el drenaje de tórax puede ser insuficiente ya que el tubo de drenaje se obstruye con frecuencia; la eliminación temprana u oportuna de las bridas pleurales a menudo evita la necesidad de la toracotomía y la decorticación que son procedimientos quirúrgicos más agresivos107-112.
La etapa organizada se caracteriza por la formación de una corteza fibrosa y restrictiva que limita la movilidad y expansión pulmonares.
Para diferenciar estas 3 etapas la ecografía o la TAC son importantes y útiles ya que podrán dictar tempranamente el tipo de intervención medicoquirúrgica a seguir.
La frecuencia del DPN oscila entre el 10% y 40% de los niños con NAC.
Se estima que su incidencia en la población pediátrica es de 3.3/100,000113.
Su diagnóstico temprano requiere de una alta sospecha clínica ante un niño con NAC bacteriana que presente los signos y síntomas mencionados anteriormente en el texto. Es aconsejable que los niños con DPN sean hospitalizados para la administración de antibióticos intravenosos y para valorar la realización de una tóracocentesis; esta última es imprescindible para determinar si se trata de un exudado pleural o de un empiema ya que el empiema es sinónimo de drenaje pleural. El diagnóstico y el tratamiento medico-quirúrgico precoces son fundamentales para reducir la morbimortalidad asociada a esta patología114. El diagnóstico de empiema se confirma mediante la toracocentesis y el análisis del líquido pleural, tal y como fue mencionado anteriormente115.
Manejo médico quirúrgico de la NAC con empiema: Como se señaló anteriormente, el tratamiento del niño con empiema amerita hospitalización y un enfoque integral multidisciplinario con la participación del pediatra, el cirujano, una enfermera y un fisioterapeuta. Utilizar ATB con adecuada concentración en líquido pleural es importante para lograr los mejores resultados116.
1. Manejo quirúrgico de la NAC con empiema:
El tipo de manejo quirúrgico dependerá en gran parte de la etapa del empiema en la que se encuentre el paciente. Durante la etapa exudativa el líquido es escaso, sin tabiques, puede ser evacuado fácilmente mediante toracocentesis y drenaje de tórax. Durante la etapa fibrinopurulenta el derrame es espeso y se forman tabiques o septos de fibrina, o empiema loculado. En estos casos, el drenaje de tórax puede ser insuficiente ya que el catéter intratorácico se puede obstruir. Si el empiema no se resuelve oportunamente, es probable que la tabicación requiera toracotomía y decorticación. Un procedimiento alternativo es la pleurotomía mínima para debridación mediante videotoracoscopia, para evitar la cirugía más agresiva y disminuir la morbimortalidad asociada con la toracotomía. Otro recurso útil es la instilación de fibrinolíticos intrapleurales como la estreptoquinasa117.
En la etapa organizada se forma una corteza fibrosa que restringe la movilidad y expansión pulmonares. En estos casos puede ser necesaria la toracotomía para hacer una decorticación y, en ocaciones, neumonectomía segmentaria o lobular.
En la fase fibrinopurulenta el debridamiento también se puede llevar a cabo por medio de videotoracoscopía; en general, se limita a aquellos pacientes que toleren la ventilación mecánica y selectiva de un pulmón. El mejor resultado se ha obtenido en las formas tempranas, es decir, durante el período inicial del empiema118-119. No es útil en la fase organizativa.
En el anexo número 3 se describe el protocolo de administración de estreptoquinasa que se utiliza en el Centro Hospitalario Pereira Rossell de Montevideo, Uruguay. En la Figura N° 1 se presenta un flujograma sobre el diagnóstico, el enfoque y el manejo del niño con empiema.
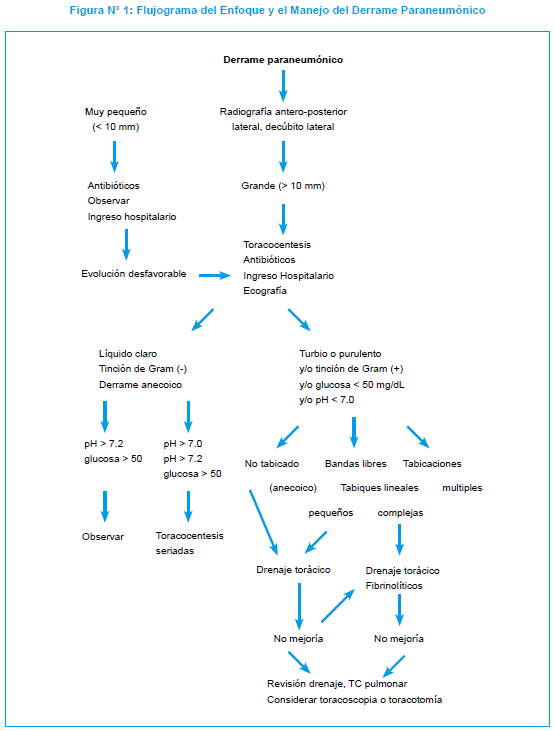
2. Tratamiento médico de la NAC con empiema:
Se recomienda adoptar las siguientes medidas terapéuticas:
Posición semisentada o elevación de la cama a 45° en los lactantes Alimentación: prestar especial atención al soporte nutricional.
Oxigenoterapia: vía cánula nasal (1-3 1/minuto) o con máscara simple, o máscara con reservorio con buena adaptación, con flujo de oxígeno entre 8 y 10 1/minuto para evitar que la saturación de O2 sea < 95%.
Antipiréticos y analgésicos según la condición del paciente y sus requerimientos.
No administrar sedantes, antitusígenos, ni expectorantes.
Tomado de: Asensio de la Cruz y col117. "Algoritmo diagnóstico-terapéutico en el derrame paraneumónico (modificado de Light) Asociación Española de Pediatría. Protocolos actualizados 2008.
La cobertura antibiótica dependerá de la edad del paciente, de los patrones epidemiológicos locales, del historial vacunal del paciente, y de los hallazgos clínicos y radiológicos. Debe iniciarse por vía intravenosa35.
Menores de 1 mes:
Ampicilina 200 mg/kg/día c/8 h, intravenoso (IV), más gentamicina 2.5 g/kg/dosis dosificada c/8 h IV, o más cefotaxima 100 mg/kg/día, c/8 h, IV
1 mes a 5 años:
Ampicilina 300-400 mg/kg/día c/4 h, IV (máximo 6 grs./día)
Mayores de 5 años:
Ampicilina, igual al esquema de 1 mes a 5 años, o penicilina cristalina sódica 200,000 U/kg/día c/4 h, IV.
En pacientes con presentación clínica y radiológica que no permitan establecer con claridad si se trata de una NAC bacteriana clásica o atípica, se recomienda asociar un macrólido.
En casos de sospecha de NAC por S. aureus y si el paciente no luce séptico, se puede iniciar el tratamiento con meticilina, oxacilina, o dicloxacilina a 200 mg/kg/día, c/6 h, IV. La cefalotina es una opción terapéutica en estos casos, a 150 mg/kg/día, c/ 6 h, IV.
Para pacientes con sospecha de NAC por SAMR-AC se podría iniciar el tratamiento con clindamicina a 40 mg/kg/día, en 4 dosis, IV; antes de utilizarla es importante descartar que el germen posea resistencia inducible a este antibiótico.
Otras alternativas terapéuticas en casos de sospecha de NAC por SAMR-AC son el linezolid a 30 mg/ kg/dosis c/12 h, IV, en niños menores de 12 años, y a 1,200 mg/día, IV para ≥ 12 años, o vancomicina 40 mg/kg/día, c/8 h, IV.
Una revisión de la Academia Americana de Pediatría publicada en el año 2008 propuso el uso de vancomicina o clindamicina como alternativas a las penicilinas antiestafilocócicas para infecciones pulmonares por SAMR-AC113
Cuando se documenta NAC por S. aureus en un paciente séptico con enfermedad rápidamente evolutiva, se recomienda la asociación de ceftriaxona 100 mg/kg/día, en dos dosis, IV, más vancomicina 40 mg/kg/día, c/6 h, IV.
Adecuación del tratamiento según los resultados del laboratorio de microbiología:
- Si se aisla S. pneumoniae con resistencia alta a penicilina (CIM > 8 μg/ml):
a) Si es sensible a cefalosporinas de 3a generación (CIM < a 1 μg/ml) o con sensibilidad intermedia (CIM 2 μg/ml) se recomienda ceftriaxona 100 mg/kg/día, en 2 dosis, IV. Como alternativa se puede utilizar cefotaxima a 200 mg/kg/día, en tres dosis, IV
b) Si es resistente a cefalosporinas de 3a generación (CIM ≥ 4 μg/ml), se recomienda tratamiento con una droga con actividad documentada in vitro Ejemplo: vancomicina, clindamicina, teicoplanina, quinupristina/dalfopristina116.
- En casos de NAC por S. aureus susceptible a meticilina: se puede iniciar el tratamiento con meticilina, oxacilina, o dicloxacilina a 200 mg/ kg/día, c/6 h IV.
La cefalotina es una opción terapéutica en estos casos, administrada a 150 mg/kg/día, c/6 h IV.
- En caso de NAC por SAMR-AC se podría iniciar el tratamiento con clindamicina a 40 mg/kg/ día dosificada en 4 dosis IV; antes de utilizarla es importante descartar que el germen posea resistencia inducible a la clindamicina.
Otras alternativas terapéuticas en casos de infección por SAMR-AC son el linezolid a 30 mg/kg/dosis, c/12 h IV en niños menores de 12 años, y a 1,200 mg/día, vía IV para ≥ 12 años, o vancomicina: 40 mg/kg/día, c/8 h, IV.
Duración del tratamiento antibiótico de NAC con empiema:
Se recomienda un mínimo de 21 días.
7. Diagnóstico por medio de imágenes:
La infección pulmonar compromete al espacio aéreo periférico, al intersticio o a la vía aérea. Inicialmente puede afectar al alvéolo que es responsable del intercambio de oxígeno (consolidación neumónica), la vía aérea y los espacios aéreos adyacentes, (bronconeumonía) o solamente la vía aérea de conducción (peribronquitis).
1) La alteración del espacio aéreo (enfermedad acinar) se caracteriza por la aparición de opacidades lobares, segmentarias o subsegmentarias coalescentes, con una trama discreta o irregular y broncogramas aéreos frecuentes
2) La afectación de la vía aérea da lugar a un engrasamiento de la pared bronquial (manguito peribronquial) más allá del tercio interno del pulmón. Se identifican una trama lineal parahiliar y sombras en anillo en la configuración anatómica y la localización de los bronquios. Con frecuencia, se observan opacidades lineales que parten de los huios (infiltrado parahiliar).
En una infección pulmonar pueden coexistir los patrones anteriormente citados, con características tanto de afectación del espacio aéreo como de la vía aérea. Este tipo de bronconeumonía es característico de infecciones virales, puede ser secundario a bacterias.
Existen diferencias en las imágenes radiológicas según la etiología de la NAC
1. Neumonía Viral: Estas infecciontes suelen producir bronquiolitis, bronquitis o bronconeumonía. Los hallazgos característicos incluyen hiperinsuflación, engrasamiento peribronquial y aumento de la trama lineal parahiliar.
2. Neumonía Bacteriana: La Rx de tórax muestra típicamente una opacidad parenquimatosa segmentaria o subsegmentaría con o sin atelectasia asociada. Puede también manifestarse como una densidad esférica o redondeada.
El primer paso para identificar radiológicamente la neumonía implica una familiarización completa con el tórax normal; las dos regiones hiliares deben tener una densidad relativamente igual, y a ambos lados de la columna vertebral la silueta cardiaca debe ser más o menos de la misma densidad. Se debe señalar que los márgenes del corazón y las cúpulas diafragmáticas usualmente están bien definidas. Esta observación es útil para interpretar el signo de la silueta de "Felson". Si alguno de los bordes cardiacos o diafragmáticos se vuelve impreciso o borroso, debe sospecharse una anormalidad adyacente (infiltración pulmonar, atelectasia). Normalmente el hemidiafragma derecho es un poco más alto que el izquierdo; por esto, en la proyección lateral suele aparecer mas elevado. En ocasiones se hallan superpuestos, pero la mayoría de las veces se observan como órganos separados. El hemidiafragma derecho se puede identificar también por el hecho de que habitualmente se observa en toda su extensión. El hemidiafragma izquierdo sólo suele verse hasta la pared cardiaca posterior ya que en este punto se confunde con la silueta cardiaca. En ocasiones también el hemidiafragma izquierdo puede verse íntegramente; en tales casos, la cámara de aire gástrica o la vena cava inferior, generalmente son visibles y pueden facilitar la diferenciación. La cámara de aire gástrica se halla bajo el hemidiafragma izquierdo y la vena cava inferior en el lado derecho; esto hace que a menudo se superponga con el hemidiafragama derecho y no se pueda delimitar con claridad.
El segundo paso para la adecuada lectura de una Rx. de tórax y poder identificar una NAC se basa en la premisa de que los infiltrados iniciales suelen ser leves y pasar desapercibidos, o ser mal interpretados como densidades costales y broncovasculares. En estos casos, el diagnóstico de NAC requerirá un alto índice de sospecha por parte de la persona que lee la Rx y una evaluación metódica de cualquier aumento de la densidad por dudoso que sea. En la práctica diaria, la lectura de la Rx se debe hacer colocándola en forma tangencial a la vista, y con cierta distancia entre los ojos y la placa.
El signo de la silueta de Felson es útil para detectar un infiltrado inicial o poco visible. Se produce cuando dos estructuras de igual densidad radiológica se hallan yuxtapuestas y la interfase entre ambas se borra, Ejemplo: si un órgano como el corazón que es altamente denso se superpone sobre un infiltrado pulmonar igualmente denso, la interfase entre ellos será leve o estará ausente. Normalmente, el corazón se encuentra yuxtapuesto al pulmón aereado que tiene poca densidad; dado que la densidad entre ambos es distinta, su interfase quedará claramente definida una línea nítida que corresponde al borde cardiaco.
El signo de la silueta se aplica a las neumonías del lóbulo medio derecho y de la língula. En el lóbulo medio derecho, las neumonías que producen el signo de la silueta se hallan en el segmento medial; las del segmento lateral no están yuxtapuestas al corazón, por lo que no se produce este signo. En la neumonía del segmento medial, el borde adyacente del corazón se difumina o desaparece. Cuando la neumonía se encuentra en la língula, se borra el borde izquierdo del corazón. El signo de la silueta ayuda a localizar los infiltrados pulmonares de lóbulo inferior 120-121.
El signo de la silueta puede producirse en situaciones normales, es decir en ausencia de neumonía; la ubicación más frecuente es al lado derecho del corazón. En los niños, a menudo las señales bronco-vasculares adyacentes al borde derecho del corazón son tan prominentes que se confunden con la silueta cardiaca y se observa un signo de la silueta. De no tener este fenómeno en cuenta, se puede confundir con un infiltrado de consolidación neumónico del lóbulo medio derecho122-124.
Existen ciertas áreas en la Rx de tórax, conocidas como zonas en las que se ocultan los infiltrados pulmonares iniciales o mínimos. Es importante estar familiarizados con estas imágenes; se debe analizar y estudiar la Rx por segunda vez; de no ser así, los infiltrados pulmonares pueden pasar inadvertidos.
Las neumonías del segmento apical de cualquiera de los lóbulos inferiores a menudo se ocultan detrás de una u otra de las regiones hiliares. Las de los lóbulos inferiores, localizados en el fondo de los ángulos costofrénicos posteriores, suelen pasar inadvertidas en la proyección frontal.
La neumonía con infiltrado intersticial es frecuente en niños y produce una imagen radiológica variable: desde infiltrados peribronquiales parahiliares, hasta los reticulados intersticiales difusos. Un ejemplo de esto es la neumonitis por varicela que causa neumonía pulmonar primaria en niños sanos. Es frecuente en niños con varicela que tienen depresión inmunológica de algún tipo. Recientemente se ha reportado este mismo tipo de infiltrado en adolescentes con mononucleosis infecciosa120.
Es importante la identificación de las atelectasias; expresan ausencia o pérdida de volumen pulmonar. En casos de pérdida del volumen es probable que la consolidación traduzca una atelectasia y no una NAC; esto se observa con frecuencia en las infecciones virales de la infancia120-121. En una NAC bacteriana no se detectará la perdida de volumen hasta que éste no inicie su resolución. Las atelectasias también se observan en pacientes con crisis asmática. En estos casos, la presencia de sintomatología obstructiva orientará hacia la atelectasia como probable causa de la consolidación.
Las opacidades pulmonares en parches representan exudado, edema o sangre en el espacio alveolar. Si los infiltrados se limitan a un lóbulo, la causa mas probable es una infección bacteriana o por M. pneumoniae. Los infiltrados alveolares bilaterales múltiples sugieren infección bacteriana. En algunos casos los signos radiológicos pueden orientar a un determinado agente etiológico, Ejemplo: la presencia de neumatoceles, pioneumotórax y absceso pulmonar orientan a S. aureus; no obstante, en la mayoría de los casos las imágenes de la Rx de tórax no permiten identificar el patógeno de la NAC.
Otros Métodos de Diagnóstico por Imágenes:
La Ecografía utiliza el ultrasonido. Está indicada cuando se produce un hemitórax opaco con sospecha fuerte de derrame pleural. Nos permite ver si éste está tabicado y, determinar el volumen y la extensión de la condensación y del derrame. Con el doppler color podemos valorar la neumonía y su vascularización pudiendo predecir la presencia de necrosis. Este método diagnóstico es útil para el seguimiento de la evolución de la NAC y del derrame.
La Tomografía Axial Computada (TAC) de alta resolución y con multidetectores, permite visualizar con niticez el parénquima pulmonar.
La Resonancia Magnética (MRI) permite ver áreas vasculares en el mediastino; no obstante, no define bien el parénquima pulmonar122.
8. Tratamiento
Criterios de Admisión al Hospital
La mayoría de los niños con NAC se manejan ambulatoriamente. Cuando presentan indicadores clínicos de gravedad o si el ambiente familiar no asegura el cumplimiento del tratamiento o la detección temprana de empeoramiento clínico, deben hospitalizarse. En el Cuadro N° 9 se enumeran los rasgos clínicos y/o de laboratorio mandatorios de hospitalización y en el Cuadro N° 10 los que determinan su derivación a la UCI.
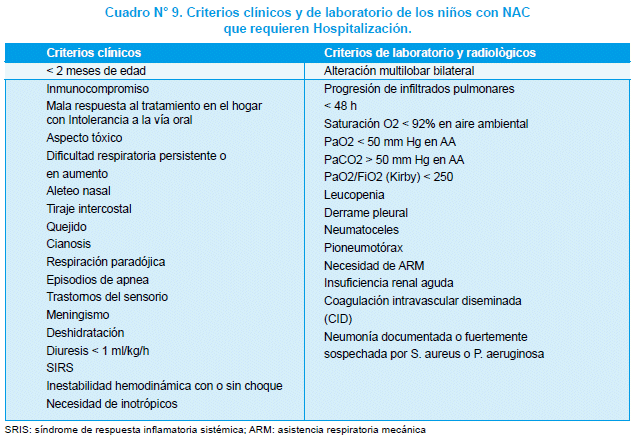

En el Cuadro N° 11 figuran las recomendaciones de OMS para orientar el nivel de atención de estos niños125. El cumplimiento de estas recomendaciones ha mostrado una disminución importante de la mortalidad por NAC en los niños126-127.

La selección del antibiótico empírico en los niños con NAC puede ser difícil ante la imposibilidad de diferenciar entre una NAC bacteriana y de causa viral128. Diferentes factores influyen en la selección inicial del ATB en el paciente pediátrico: la probable etiología, que dependerá de la edad del paciente, presentación clínica y Rx de tórax, comorbilidad subyacente; los antecedentes epidemiológicos, por ej. La prevalencia de SAMR-AC114. Lo ideal es dirigir el tratamiento al patógeno identificado; no obstante, esta información no está disponible en el momento del diagnóstico inicial; aún después de varios días de hospitalización, en la mayoría de los casos no se logra su identificación. Por ésto, la elección del ATB se hará de acuerdo a la información que se tenga de estudios sobre la etiología de las NAC en los niños. Lo idóneo sería contar con datos que se tenga del país, de la región y de la comunidad a la que pertenece el paciente129-130.
En la mayoría de los niños con NAC de leve a moderada los ATB administrados empíricamente, vía oral y, de acuerdo a la edad y a los datos regionales, son efectivos. Cuando se utiliza la vía parenteral las concentraciones del ATB en sangre y en el tejido pulmonar son altas y se alcanzan rápidamente. Esta es la ruta de administración de elección en casos de NAC moderada a severa90.
Una vez identificado el agente etiológico, se readecuarán los ATB al germen y a su patrón de susceptibilidad antibiótica; se recomienda iniciar con los de menor espectro antimicrobiano y de menor costo; claro está, adecuándolos a la gravedad del paciente. En el Cuadro N° 12 se encuentran las etiologías probables de acuerdo al grupo etario.

La elevada mortalidad de la NAC en niños < de 3 meses obliga a categorizarla como grave, independientemente de su presentación clínica125-131-132; estos niños deben hospitalizarse y recibir ATB por vía parenteral133. En las primeras 3 semanas de vida los patógenos bacterianos mas frecuentemente responsables son los señalados en el Cuadro N° 12131-134.
El esquema ATB empírico electivo inicialmente es un β-lactámico (β-L) como ampicilina más un aminoglucócido tipo gentamicina o amikacina; alternativamente podría ser tratado con ampicilina más cefotaxima130-134,135. En las formas graves el β-L de elección es la cefotaxima. Las dosis dependen de la edad cronológica y del peso del paciente136-137. Los aminoglucósidos pueden emplearse en dosis única, aunque algunos trabajos de farmacocinética no apoyan dicho esquema, los estudios de eficacia invivo apoyan esta dosificación. La ceftriaxona debe evitarse en la etapa neonatal porque se une a la albúmina transportadora de bilirrubina y podría desencadenar kernicterus en neonatos con hiberbilirrubinamia; también es conveniente evitar su uso en pacientes que estén recibiendo soluciones que contienen calcio. Existe alto riesgo incluso de muerte por precipitación de sales de calcio + ceftriaxona en el pulmón y riñon de los neonatos que reciben ambos medicamentos simultáneamente138. Otro efecto indeseable de la ceftriaxona en este grupo etario es la formación de pseudolitiasis y de barro biliar; es reversible y se resuelve al suspender el tratamiento. En el anexo se describen las dosis recomendadas para recién nacidos según peso y edad en días.
En el grupo etario entre 3 semanas y 3 meses, los agentes etiológicos predominantes de la NAC son los señalados en el Cuadro N° 12. El tratamiento empírico inicial debe incluir un β-L como cefotaxima o ceftriaxona y ampicilina; esta última porque aunque la L. monocytogenes es poco frecuente en este grupo etario, se han reportado casos de sepsis por la misma. En NAC severa con sospecha o confirmación de infección por S. aureus, debe agregarse una droga antiestafilocócica (ver sección de tratamiento de la NAC con piotórax). La tos persistente, paroxística, las apneas y las crisis de cianosis, orientan a etiología por Bp131. Cuando la evolución clínica es subaguda, con tos persistente y afebril, es altamente sugestiva de infección por C. trachomatis139; en estos casos es recomendable utilizar un macrólido por vía oral (VO): eritromicina 50 mg/kg/día c/6 h, por 14 días, o azitromicina a 20 mg/kg una vez al día por 3 días, o claritromicina 15 mg/kg/día en 2 dosis, por 14 días140. No se tiene suficiente información con respecto a la seguridad y la eficacia de los nuevos macrólidos para el tratamiento de la neumonía por C. trachomatis ni la producida por Bp.
Los niños > 3 meses a 5 años de edad con NAC leve a moderada se pueden manejar en forma ambulatoria; los casos de moderados a severos pueden requerir hospitalización ya que el riesgo de muerte es mayor. No existe evidencia de que la gravedad del cuadro clínico guarde relación con el agente etiológico, salvo en casos de NAC por S. aureus.
Después de la introducción de la vacuna anti-Hib conjugada, se ha observado que la gran mayoría de los casos de NAC bacteriana en los niños > 3 meses a 5 años de edad son causados por S. pneumoniae141.
En aquellos países en donde SAMR-AC ha emergido como problema de salud pública (Uruguay, Argentina, Costa Rica), debe plantearse esta etiología en pacientes con cuadros graves de NAC142. Su incidencia como agente etiológico de NAC es baja, pero aumenta en los casos graves. Es importante que cada país, región y comunidad conozcan su propia epidemiología.
Cuando se decide manejar la NAC ambulatoriamente, la droga de primera línea es la amoxicilina a 100 mg/kg/día, c/8 h, VO90-143. En niños sin vacunación previa contra Hib o con un esquema incompleto o desconocido, lo aconsejable es el tratamiento con amoxicilina+inhibidor de β-lactamasa.
Los pacientes manejados ambulatoriamente deben controlarse a las 24-48 h de iniciado el tratamiento; si existiera empeoramiento clínico o radiológico, o persistencia de la fiebre por más de 48 h postinicio del tratamiento, lo recomendable es hospitalizarlos e iniciar el tratamiento parentera190-114,126-136. Si después de hospitalizado e iniciado el tratamiento parenteral el paciente permaneciera estable, o con tendencia a la mejoría, podrá seguir siendo manejado en sala general; si su condición empeorara, es conveniente su traslado a UCI.
Dado que la mayoría de estos casos son causados por S. pneumoniae y han recibido un esquema vacunal completo contra Hib, podrán ser tratados con ampicilina o penicilina IV a dosis elevadas para cubrir cepas con sensibilidad disminuida a penicilina; Se recomienda ampicilina 200-300 mg/kg/día, c/6 h; para pacientes > de 4 años la alternativa es penicilina 200.000 UI/Kg/día, c/6 h, en ambos casos por vía IV135-144.
La resistencia del S. pneumoniae a penicilina aumentó mundialmente durante los últimos 20 años145. El Comité Estadounidense de Estándares de Laboratorio (CLSI) estableció en el año 2.008 146 nuevos puntos de corte para definir la sensibilidad a penicilina de este microorganismo, dependiendo del fluido corporal o foco de infección146. Para infecciones extrameníngeas, en particular NAC, se consideran sensibles: CIM < 2 μg/ml; resistencia intermedia: CIM de 4 μg/ml; y resistencia alta: CIM > 8 μg/ ml . El cambio en los puntos de corte obedece a que la concentración que alcanzan los β-L en alvéolo y líquido pleural es elevada y por lo tanto, las infecciones localizadas en pulmón y pleura pueden ser efectivamente tratadas con penicilina y otros β-L147.
Además, los β-L poseen efecto post-antibiótico, lasconcentraciones séricas de los mismos superan la CIM de S. pneumoniae durante más del 40% del intervalo entre dosis 148. Estudios realizados en Latinoamérica demostraron que en pacientes con infección por S. pneumoniae con resistencia alta a la penicilina, que fueron tratados con la misma o con ampicilina (y otros (3-L), la respuesta clínica y microbiológica fue satisfactoria49-148-150. En pacientes sin inmunización vs Hib y con NAC que no responde al tratamiento inicial con un β-L, es conveniente indicar amoxicilina o ampicilina + inhibidor de β-lactamasa (TEM-1)151-152. En varios países de Latinoamérica la resistencia del S. pneumoniae a los macrólidos es del 25% o más, por lo que se desaconseja su empleo como tratamiento inicial de las NAC en niños. Sus únicas indicaciones serían para pacientes con alta sospecha de NAC por gérmenes atípicos, o con antecedentes de reacción anafiláctica a los β-L135. Los nuevos macrólidos como azitromicina y claritromicina son rápida y ávidamente captados por los tejidos, alcanzando concentraciones séricas bajas y poco duraderas, por lo que serían inefectivos para controlar la infección en niños con NAC y bacteriemia.
En casos de NAC multilobar o complicada con empiema, neumatoceles y/o forma necrotizante, debería recomendarse un esquema empírico inicial con actividad para S. pneumoniae, Hib, y contemplar tratamiento vs S. aureus, sensible a las penicilinas antiestafilocócicas, o SAMR-AC, según la situación clínica (ver tratamiento en la sección de piotórax o derrame pleural purulento)134-153-158.
En niños de 5 a 15 años de edad S. pneumoniae es el patógeno bacteriano mas frecuente; sin embargo, las bacterias atípicas como M. pneumoniae y C. pneumoniae causan hasta el 30% de los casos de NAC; los pacientes con fuerte sospecha de NAC atípica y clínicamente estables, pueden ser efectivamente tratados con macrólidos en forma ambulatoria. La combinación de amoxicilina + macrólido es un esquema adecuado para aquellos pacientes en los que se sospeche coinfección de bacterias atípicas con lastípicas137-158. En ausencia de respuesta clínica adecuada luego de las primeras 72 h de tratamiento con un β-L, es aconsejable adicionar un macrólido tipo eritromicina, azitromicina o claritromicina137. El tratamiento de las NAC complicadas y el de los casos graves que requieren hospitalización en la UCI está descrito en la sección del tratamiento del derrame pleural purulento.
Una vez identificado el agente etiológico, los ATB deben readecuarse al germen y a su patrón de susceptibilidad antimicrobiana, como figura en el Anexo 2.
En los pacientes con NAC de probable etiología estafilocócica se seguirá el esquema descrito en la sección de tratamiento del derrame pleural purulento.
Los reportes de Uruguay, Argentina, Brasil y Costa Rica, han mostrado una creciente incidencia de SAMR-AC que frecuentemente ocasionan neumonía necrotizante159-163
Las cepas de SAMR-AC generalmente son susceptibles a otros ATB atibióticos como rifampicina, gentamicina, cotrimoxazol, doxiciclina, lincosamidas, estreptograminas, vancomicina, y las oxazolidinonas, específicamente al linezolid164-165.
Los macrólidos son ATB bacteriostáticos utilizados desde que la eritromicina fue lanzada al mercado en 1952166. Actualmente se dispone de macrólidos con menos efectos colaterales y vida media más prolongada como la azitromicina y la claritromicina. Se han recomendado tradicionalmente como ATB de 2a elección en NAC atípicas y en pacientes con NAC e historia de reacción anafiláctica a la penicilina167-168. Las dosis recomendadas son: eritromicina: 40-50 mg/kg/día VO, en 3 dosis, por 7 a 10 días; azitromicina 10 mg/kg/día en dosis única el ler día y luego 5 mg/kg/día en dosis única del día 2 al 5, VO; claritromicina: 15 mg/kg/día VO en 2 dosis, por 7 a 10 días. En pacientes con NAC atípica y que requieran hospitalización, debe de considerarse el uso de eritromicina, azitromicina o claritromicina IV
Con frecuencia se reportan brotes epidémicos de Bp, especialmente en lactantes < de 4 meses de edad, asociados a una mortalidad elevada. Los adolescentes y adultos son las fuentes de transmisión, al ser reservorios que infectan a los lactantes con un esquema incompleto de vacunación contra Bp. En casos de NAC fuertemente sospechada o documentada por Bp, las drogas de elección para el tratamiento y para la profilaxis son los macrolidos; todos han desmostrado la misma efectividad clínica y microbiológica. En los neonatos < de 15 días el uso de la eritromicina se ha asociado a hipertrofia pilórica por lo que se desaconseja su uso durante los primeros 15 días de vida167. En los mayores de 1 mes de vida se pude utilizar eritromicina por 14 días, claritromicina por 7 días, o azitromicina por 5 días todos por VO; son aconsejables dado por alcanzar altas concentraciones tisulares e intracelulares; permiten tratamientos acortados y se asocian a menos efectos colaterales que la eritromicina; estas fueron las recomendaciones de la Academia Americana de Pediatría en el 2006 y en el 2009136.
La elección del tratamiento empírico de las NAC se relaciona a la edad del paciente, las características clínicas del cuadro y las radiográficas, cuando se cuenta con la Rx de tórax; también se deben considerar las condiciones subyacentes y la epidemiología en el área169. En el Cuadro N° 13 se indican las diferentes opciones sugeridas según los aspectos antes mencionados153.
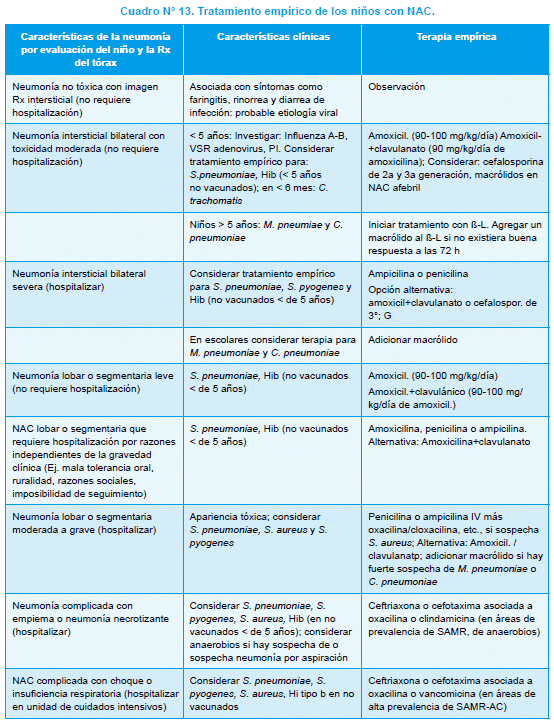
Duración del tratamiento y tratamiento secuencial parenteral-oral:
La duración del tratamiento del paciente con NAC es variable; la mayor parte de las recomendaciones no están basadas en evidencia sino, en esquemas tradicionales creados por autoridades en el tema. Existen estudios clínicos sobre tratamientos abreviados de < 3-5 días con amoxicilina170, la gran mayoría efectuados en el continente africano; adolecen de defectos importantes de diseño y desarrollo. En muchos de ellos no se documentó si la infección era bacteriana o viral, o no se realizaron estudios radiológicos para documentar la NAC. Un estudio reciente171 demostró que la prolongación del tratamiento no mejora el pronóstico ni la respuesta clínica o microbiológica, y predispone a la selección de resistencia bacteriana y suprainfecciones. La mayoría de los pacientes hospitalizados por NAC con tratamiento adecuado por vía IV, responden satisfactoriamente alrededor del 2°-3er día; es recomendable mantener esta vía por 1 o 2 días más172-173 y luego cambiar a la VO. Se recomienda tratar las NAC no complicadas causadas por S. pneumoniae, por 7 a 10 días; las causadas por M. pneumoniae por 10 a 14 días y aquéllas por Legionella pneumophila por 14 días. Todas las NAC complicadas, independientemente del agente etiológico, requieren 14 a 21 días de tratamiento137. El cambio de la vía IV a la VO permite el egreso hospitalario temprano, disminuye el riesgo de infecciones nosocomiales, los costos y la desorganización familiar. Debe considerarse en todo aquél paciente estable, en franca recuperación clínica y microbiológica, con aceptación y tolerancia de la VO y sin indicio de complicaciones; se recomienda utilizar un antibiótico con un espectro antimicrobiano similar al que estaba recibiendo por vía IV172. La dosis oral para el tratamiento secuencial parenteral oral debe equivaler a 2 o 3 veces la dosis oral usual de ese antibiótico174.
El 20% de los pacientes hospitalizados por NAC no responderán adecuadamente al tratmiento inicial174. En ellos la fiebre persiste más allá de los 5 días después de iniciado el tratamiento; a la auscultación se evidencia persistencia de estertores hasta 7 días, o hasta después de la suspensión del tratamiento; la resolución radiológica puede tomar varias semanas175.
Se debe plantear fracaso o respuesta sub-óptima ante un paciente con fiebre persistente y con deterioro clínico y radiológico después de 72 h. de iniciado el tratamiento176. Las razones de falla más frecuentes se asocian a condiciones o enfermedades subyacentes del paciente, a la virulencia y susceptibilidad antimicrobiana del patógeno, o a la farmacocinética y farmacodinamia del ATB empleado, entre otras. Se habla de falla primaria al tratamiento cuando se detecta un patógeno inesperado, no susceptible al anitmicrobiano empleado inicialmente, Ej. M. tuberculosis. Se considera infección persistente cuando se aisla nuevamente el patógeno inicialmente identificado. Como fue mencionado, el fracaso puede deberse a resistencia del microorganismo al ATB utilizado, Eje., SAMR-AC, S. pneumoniae con Resistencia alta a penicilina. Es importante estudiar al paciente por inmunodeficiencia congenita o adquirida, Ej., infección por VIH. En el cuadro N° 14 se resume todo lo todo lo anteriormente mencionado174.

Tratamiento de soporte en pacientes con NAC
La terapia ATB adecuada es la clave del manejo de los pacientes con NAC177. La mortalidad de las NAC bacteriémicas por S. pneumoniae antes de la introducción de los ATB era cercana al 80%, disminuyendo a < de 20% después de que se generalizó su uso176. No obstante, a pesar de la disponibilidad de mejores y nuevos ATB, la mortalidad ha permanecido inaceptablemente alta, debido a la creciente resistencia de los patógenos más prevalentes a los ATB más frecuentemente utilizados178. Otros elementos esenciales para disminuir la morbimortalidad de de los pacientes con NAC consisten en la medidas de soporte para el paciente. Estas se describen a continuación:
Medidas generales
Posición: Se recomienda la posición semisentada.
Oxigenoterapia y monitoreo de la concentración de Oxígeno: El aporte de O2 suplementario y la medición de la saturación del mismo en la sangre son elementales para disminuir la mortalidad de los niños con NAC. Si al recibir al paciente la SaO en aire ambiente es ≤ 92%, debe administrase suplemento de O2 por cánula nasal, por halo o con reservorio179. Es conveniente que la SaO2 se mantenga > 90%. (los detalles respecto a cómo lograr una oxigenación y saturación adecuada de O2 arterial se contemplaron en la sección del manejo del niño con derrrame pleural purulento). Mantener una hidratación adecuada del paciente es igualmente importante. Esto se logra por medio de la administración de líquidos VO cuando la condición clínica del paciente lo permita, o por vía IV cuando esté contraindicada la VO, o cuando el paciente no la acepte o tolere.
Uso de antipiréticos: Se puede indicar paracetamol cuando el paciente presente fiebre elevada que le ocasione malestar e irritabilidad.
Alimentación y nutrición: El aporte calórico adecuado es elemental para que el paciente con NAC experimente una recuperación temprana; la relación existente entre malnutrición y mortalidad por NAC es bien conocida180. En pacientes que están recibiendo lactancia materna, se debe estimular al máximo el mantenimiento de la misma. Si presentan taquipnea severa, la VO debe fraccionarse, o, suspenderla hasta que haya mejoría. Se puede recurrir al uso de sonda orogástrica. La suplementación alimenticia con micronutrientes debe considerarse en pacientes con desnutrición; se ha demostrado que el aporte de vitamina A y de Zinc disminuye la mortalidad en poblaciones desnutridas o con déficits alimenticios181.
Fisioterapia con percusión torácica, drenaje postural y ejercicios de respiración profunda: Es importante mantener las narinas permeables mediante la aspiración de las secreciones. El drenaje postural por medio de la percusión, ayuda al aclaramiento y eliminación de las secreciones; es importante que al realizar estos procedimientos se controlen la saturación de O2 y la frecuencia cardíaca, y que sean efectudos por personal calificado.
Antitusígenos. El uso de antitusígenos o expectorantes no está recomendado182.
9. Prevención
A. Medidas inespecíficas:
Reconocer y tratar de eliminar o disminuir al máximo los FR para IRA baja, en particular la NAC. Los pediatras que trabajan en los diferentes niveles de atención, juegan un papel protagónico en la concientización de la comunidad respecto a la importancia de las medidas preventivas inespecíficas, descritas en el Cuadro N° 15.

B. Medidas preventivas específicas:
Las vacunas específicas que inducen la respuesta inmune contra los agentes que causan las NAC han constituido el más poderoso logro de las últimas décadas. Para evitar situaciones de inequidad, los estados deberían realizar todos los esfuerzos necesarios para que estos inmunógenos, algunos de elevado costo, sean accesibles a toda la población, incluyendo los sectores más desprotegidos, en los que se registra la mayor morbimortalidad.
A continuación se discutirán exclusivamente las vacunas que están relacionadas con el control de la NAC en la infancia.
Vacuna contra la Bp: Componente de la vacuna triple bacteriana (DTP), es una suspensión de Bp muertos (inactivados por formalina o calor en fase 1), adsorbida con hidróxido o fosfato de aluminio. Es elaborada según criterios de OMS desde el 1979, a partir de células completas. Su potencia es de 4 UI, debe contener hasta 16 unidades opacimétricas de gérmenes muertos por dosis individual. Las vacunas antipertussis acelulares (Pa) contienen algunos de los componentes de Bp: Toxina pertussis (TP), Hemaglutinina filamentosa (HAF), Pertactina (Pn) y aglutinógenos de por lo menos dos tipos de fimbrias; son protectoras, con menor porcentaje de efectos adversos.
Las Pa fueron aprobadas en 1981. Desde el 2,005 la FDA de EEUU aprobó la administración a adolescentes y adultos de componentes acelulares (DTPa), no incluidos en el calendario nacional de la mayoría de los países. Estos son:
1.Boostrix®: contiene TP 8 μg; FHA 8 μg; Pn 2.5 μg. 2.
2.Adacel®: contiene TP 2.5 μg; FHA 5 μg; Pn 3 μg.
Existen diversas combinaciones de DTP y DTPa con otras vacunas: Hib, Hepatitis B y anti-poliomielítica inactivada (IPV).
Indicaciones: Todos los niños < 7 años deben ser vacunados con DTP a partir de los 2 meses de edad183-184, inclusive los que padecieron difteria o tétanos dado que estas enfermedades no dejan inmunidad permanente. Las vacunas acelulares para Bp tienen especial indicación en > de 7 años, adolescentes y adultos. El Comité Asesor de Vacunación del CDC de Atlanta (ACIP) recomendó la Boostrix® a partir de los 10 años, aunque puede aplicarse a partir de los 4 años; Adacel® desde los 11 a los 64 años en dosis única. No están indicadas para serie primaria.
Se pueden administrar como dosis de refuerzo a todos aquellos que han recibido el esquema básico con DTP. La eficacia clínica de la vacuna DTPa es > 84% y comparable con la DTP celular.
Nuevas estrategias de uso de vacunas acelulares183
1. Estrategia capullo: Vacunación de las madres o de padre y madre en el post parto inmediato. Los padres, hermanos mayores, incluso abuelos, pueden ser fuente de transmisión y reservorios de infección para el neonato; algunos países como Costa Rica las aplican a las mujeres en el post parto inmediato (solo la presentación aprobada para adolescentes y adultos). Esta estrategia exige diferir la vacunación con "doble" adultos durante el embarazo y en lo posible, tratar de que haya un intervalo interdosis de 2 años entre la última vacuna de la serie doble para adultos y las nuevas vacunas triples acelulares.
2. Vacunación de adolescentes de 11-12 años: Dado que en muchos países se observó un aumento de casos de infección por Bp en niños mayores y adolescentes, se recomienda una dosis adicional de DTPa a esta población.
3. Vacunación del equipo de salud: Los miembros del equipo de salud pueden ser fuente de contagio para niños hospitalizados, es conveniente considerar la vacunación de los mismos.
Esquema de vacunación, vía de administración y número de dosis: En el Io año de vida el esquema básico consiste en 3 dosis combinadas con la vacuna anti-Hib. Se inicia a los 2 meses de edad y se mantiene un intervalo de 4 a 8 semanas entre cada dosis. A los 12-15 meses se recomienda el primer refuerzo o 4a dosis y un 2° refuerzo al ingreso a la escuela. Estas 5 dosis constituyen el esquema completo.
En caso de interrumpirse el esquema, se continuará independientemente del tiempo transcurrido desde la última dosis. Si el segundo refuerzo se administrara entre los 4 y 6 años, no habrá necesidad de administrar la dosis al entrar a la escuela.
Si es factible, debe indicarse la misma marca de vacuna DTPa para todas las dosis ya que no hay datos disponibles sobre la seguridad, eficacia e inmunogenicidad de la alternancia de vacunas procedentes de diferentes laboratorios productores de biológicos184-185-186.
Inmunogenicidad y eficacia clínica: La vacuna protege contra la Bp por un período aproximado de 3 años. Se han reportado casos de Bp en niños con esquemas completos. La eficacia clínica es del 70% al 90% durante los primeros 3 años después de 4 dosis; para evitar las formas graves de Bp la eficacia ha sido > 90%.
La respuesta de anticuerpos es mayor para la HAF; el componente TP modificaría la calidad de respuesta a otros componentes en las diferentes combinaciones o asociaciones.
Vacuna conjugada contra Hib: El impacto de su administración universal ha sido dramático, con disminución total de casos de enfermedad invasora > 90%, incluyendo los casos de NAC. En el cuadro N° 16 se señala el esquema de vacunación según la edad del niño:

Los niños < de 24 meses que han padecido una enfermedad invasora por Hib deben recibir la vacuna dado que la enfermedad invasora en este grupo etario no confiere inmunidad permanente.
La concentración sérica protectora es de 0,15 μg/ ml ; 1 μg/ml confiere protección a largo plazo. La respuesta en anticuerpos anti-PRP es esencialmente de tipo IgG, corresponde a un antígeno timo-dependiente. Estimula la producción de IgA secretora en la orofaringe, lo que disminuye o elimina el estado de portador y por lo tanto la transmisión. Cuando se combina con otras vacunas la concentración de Acs PRP es menor, pero no menos protectora184-187.
Efectos adversos de la vacuna combinada DTP-Hib (cuádruple)
A) Locales: Aparición de dolor tumefacción, abscesos estériles y rara vez quistes en la zona de la inyección.
B) Generales: Los más comunes consisten en fiebre, malestar, anorexia, llanto persistente < de 3 h, vómitos, irritabilidad con llanto prolongado en el 1% de los casos. Todas estas reacciones son provocadas principalmente por el componente pertussis; se presentan habitualmente dentro de las primeras 48 h de aplicada la vacuna y sólo requieren analgésicos o antitérmicos. No constituyen una contraindicación para la aplicación de vacunas nuevas DTP.
Contraindicaciones: Las contraindicaciones son las mismas que para la DTP y DTPa: Reacción anafiláctica inmediata; encefalopatía no atribuible a otra causa dentro de los primeros 7 días después de la vacunación, que puede manifestarse en forma de crisis comiciales prolongadas, alteraciones graves de la conciencia, o signos neurológicos focales. Estos efectos se evidencian dentro de las primeras 72 h de la vacunación. Se contraindica la administración de nuevas dosis si estos efectos adversos ocurren dentro de los primeros 7 días después de la vacuna DTP o DTPa. En casos de enfermedad neurológica no clarificada es importantre identificar la etiología de la misma, e intervenir para tratar o paliar el daño neurológico.
Precauciones: Evaluar la continuación del esquema DTP o dar DTPa en niños que han presentado fiebre > 40°C, síndrome de hipotonía-hiporrespuesta, llanto persistente más de 3 h dentro de las primeras 48 h post-vacunación, sin otra causa identificable; convulsión febril o afebril dentro de los primeros 3 días después de la vacunación.
Falsas contraindicaciones:
a) Temperatura < 40.5°C; malestar o leve mareo posterior a 1 dosis previa de vacuna DTP/DTPa; historia familiar de convulsiones: en esta situación es recomendable administrar un antipirético en el momento de la vacunación y cada 6 h durante las primeras 24 h, para reducir la posibilidad de fiebre postvacunación.
b) Historia familiar de síndrome de muerte súbita del lactante, o de un evento adverso posterior a la administración de DTP o DTPa.
c) Condiciones neurológicas estables, Ej. parálisis cerebral, síndrome convulsivo controlado y retardo del crecimiento.
Quimioprofilaxis para contactos con Bp: Se recomiendan macrólidos para todos los contactos familiares e intradomiciliarios, o aquellos que estando en otras situaciones cumplan con la definición, independientemente del estado de inmunización. Su administración debe ser rápida y oportuna para evitar la transmisión. Los antibacterianos recomendados son los mismos para tratamiento como para quimioprofilaxis187-188.
Vacunación de los contactos:
1. A los contactos estrechos no vacunados o incompletamente vacunados se les debe iniciar o completar el esquema con DTP o vacuna combinada, según corresponda.
2. Los niños que recibieron la 3a dosis 6 meses o más antes de la exposición y son < de 7 años, deben recibir la 4a dosis de DTP o vacuna combinada, según corresponda.
3. Los que recibieron su 4a dosis 3 o más años antes de la exposición y son < de 7 años, deben recibir la 5a dosis de DTP o vacuna combinada, según corresponda.
Conclusiones: La estrategia principal consiste en mantener altas coberturas vacunales en lactantes y niños. Adicionalmente, desde la aparición de las vacunas acelulares, algunos países como EEUU, Australia, Austria, Canadá, Francia y Alemania han incorporado a sus calendarios un refuerzo con vacuna DTPa en la adolescencia. En Latinoamérica se están evaluando nuevas estrategias: la estrategia capullo en Costa Rica, vacunas acelulares en adolescentes en Argentina, entre otras.
Vacunas antineumocóccicas:
1. Vacunas basadas en polisacáridos capsulares:
La FDA de EEUU licenció en 1982 una vacuna elaborada con polisacáridos de la pared que incluyó 23 ST (23-Valente): 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, HA, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 22F, 23F Esta vacuna cubre más del 80% de los ST que causan enfermedad neumocócica invasora (ENI) en los países latinoamericanos. Se caracteriza por:
a) estimular solo respuesta humoral, no siendo eficaz en niños < de 2 años por su inmadurez fisiológica para elaborar estos Ac
b) generar Ac de breve duración, < a 5 años;
c) no erradicar S. pneumoniae de fauces;
d) no se puede indicar más de 2 dosis a lo largo de la vida.
El ACIP de la Academia Americana de Pediatría definió los grupos de riesgo que deben recibir esta vacuna: asplenia, diabetes mellitus, inmunodeficiencias, incluso VIH, enfermedad cardíaca y pulmonar crónica, asma tratado con altas dosis de corticoides, anemia drepanocítica, pérdida de LCR, procedimiento neurológico, insuficiencia renal crónica, síndrome nefrótico, neoplasias tratadas con inmunosupresores o radioterapia, transplantes, implante coclear189.
2. Vacunas conjugadas: Se desarrollaron 3 conjugados:
A. Vacuna Conjugada Neumocóccica heptavalente (VCN-7V) De 7 ST: 4, 6B, 9V, 14, 18C, 19F, 23F (7-V), conjugada a una proteína transportadora, la CRM 197 (Prevenar® de Pfizer).
B. Vacuna Conjugada Neumocóccica Decavalente (VCN-10V) De 10 ST: incorpora a la anterior los ST 1, 5 y 7F El ST 18C (10-V) es conjugado al toxoide tetánico, el 19F al toxoide diftérico y los 8 restantes a la proteína D del H. influenzae no tipificable (Synflorix® de GSK).
C. Vacuna Conjugada Neumocóccica Trecevalente (VCN-13V) Contiene 13 ST: incorpora a las anteriores los ST 3, 6A y 19a (13-V), también conjugada a la proteína CRM 197: Prevenar 13® de Pfizer.
La conjugación induce una respuesta inmunológica linfocito-T dependiente que elicita niveles elevados de Ac protectores específicos desde el ler mes de vida, erradica de la nasofaringe los ST contenidos en la vacuna; al disminuir su circulación, protege también a personas no vacunadas (inmunidad de rebaño). La duración de estos efectos aún no ha sido evaluada.
Se ha observado un fenómeno de reemplazo que consiste en la colonización nasofaríngea por ST no incluidos en la vacuna; el efecto de este fenómeno en la producción de infecciones invasoras o no, ha sido escasa190.
Inmunogenicidad y eficacia clínica de la vacuna conjugada heptavalente
Cubre más del 85% de los ST que producen infecciones invasoras en EEUU. Según el estudio de Black, Shinefield y col. (Norte California), su eficacia para disminuir ENI en particular NAC causadas por ST incluidos en la vacuna, fue del 97,4% en el grupo vacunado por protocolo, y del 85.7% en los vacunados parcialmente. La eficacia total fue de 89.1%191. En base a estos resultados fue licenciada por la FDA de ese país en febrero del año 2.000 para la inmunización universal de los niños < de 2 años y los de 2 a 5 años pertenecientes a grupos de riesgo189. En el 2.009 fue registrada en más de 70 países e incluida en el calendario nacional de más de 30 países para los niños < de 2 años.
Esquema de administración y número de dosis:
Deben administrarse 3 dosis en los primeros 6 meses de vida: 2°, 4° y 6o mes, y 1 dosis de refuerzo entre los 12-15 meses191.
Para el año 2,003, luego de 23 millones de dosis administradas en EEUU, el CDC de Atlanta reportó una reducción significativa de las ENI, en particular las causadas por los ST incluidos en la vacuna 7V. Según el programa ABC (Active Bacterial Core) de vigilancia sistémica del CDC de Atlanta, EEUU192, la incidencia de ENI por S. pneumoniae en 1.999 en niños < de 5 años, fue de 86/100.0000; en el 2.005 disminuyó a 1.5/100. 0005, con reducción del 98%. En el 2.005 se reportaron casos de colonización nasofaríngea e infecciones invasoras por ST no incluidos en la vacuna, en particular por el 19A; este ST presenta un clon altamente virulento y resistente a un gran número de antibióticos193. El cambio epidemiológico se detectó inicialmente en países con altas tasas de cobertura vacunal con la 7V y posteriormente, en aquellos en los que su uso fue limitado194. Varios estudios realizados en otros paises han reportado una eficacia similar y este mismo fenómeno de reemplazo195-196. Algunos autores han hipótetizado que el fenómeno de reemplazo se ha debido al desenmascaramiento de cepas previamente minoritarias197. Numerosos estudios realizados alrededor del mundo han avalado la eficacia protectora de esta vacuna contra ENI y contra NAC; en el caso de esta última, el mayor impacto se ha observado en la reducción de hospitalizaciones198-199. La efectividad para la prevención de NAC documentada radiológicamente y de probable etiología bacteriana, ha oscilado entre 21% y 37%200.
En Latinoamérica esta vacuna cubre menos del 70% de los ST invasores ya que no contiene los ST 1 y 5, causantes de > 20% de ENI. No obstante Costa Rica y Uruguay la incluyeron en el calendario nacional vacunal para niños < de 2 años, utilizando el esquema de 2 dosis: al 2o y 4o mes de edad, más refuerzo a los 12-15 meses, o al año de la 2° dosis. Las razones para la adopción de este esquema fueron el menor costo y los reportes de su efectividad en Québec (Canadá), en el Reino Unido, en Noruega, en Italia y en algunas regiones de Francia201. Se informaron concentraciones de Ac comparables con el esquema de 3 dosis para la serie primaria. Independientemente del esquema utilizado, la clave del éxito radica en la dosis de refuerzo entre los 12 y 15 meses de edad, que es necesario para alcanzar títulos de Ac elevados y sostenidos en el tiempo de todos los ST vacunales, eliminar el estado de portador en naso-faringe, y asegurar protección prolongada202. Datos presentados por el grupo de Uruguay (MC Pirez y col., poster, Simposio sobre enfermedades neumocócicas en Tel Aviv, Marzo de 2010), informaron disminución sinificativa de las ENI con el esquema mencionado.
En varios países de nuestra región se indica gratuitamente para los < de 2 años pertenecientes a los grupos de riesgo mencionados para la vacuna 23-V; sería recomendable extender esta indicación a < de 5 años.
De acuerdo a los indicadores Standard de la OMS y a varios estudios publicados en nuestra región203-204, se concluyó que su administración universal a < de 2 años sería costo/efectiva si el precio por dosis fuera < $30 dólares. Instituciones de prestigio como OMS, el grupo GAVI, el Sabin Institute, promovieron la realización de protocolos de estudio con la vacuna 7-V en Latinoamérica y el Caribe. También han subvencionado la vacuna en países con alta mortalidad infantil y bajos ingresos, entre ellos Bolivia, Cuba, Haití, Paraguay, ciertas regiones de Brasil y de México; el costo por dosis para cada país es de $5 dólares205.
Los eventos adversos son infrecuentes y leves. Locales: eritema y dolor en el sitio de la inyección. Generales: fiebre moderada, disminución del apetito y vómitos.
Las contraindicaciones para su administración serían: historia de alergia a alguno de sus componentes, antecedentes de reacción general intensa a una dosis previa. Los efectos de la vacuna sobre el desarrollo del feto son desconocidos por lo que no se aconseja su aplicación durante el embarazo.
Se considera de crucial importancia que el pediatra informe a los padres o encargados legales de los niños, sobre la existencia de vacunas conjugadas, los beneficios de su administración, y los costos en países que no la han incorporado al calendario. La familia decidirá si vacuna o no a su hijo, de acuerdo a sus posibilidades económicas.
Nuevas vacunas conjugadas:
Como ya se mencionó, existen dos vacunas conjugadas nuevas que fueron aprobadas y licenciadas: La VCN-10V (Synflorix® de GSK) licenciada en Europa para < de 2 años de edad y la VCN-13V (Prevenar-13® de Pfizer) licenciada por la ACIP en Febrero del 2.010 para todos los niños de 6 semanas a 59 meses, y para niños pertenecientes a los grupos de riesgo mencionados, hasta los 71 meses (ver informe publicado en MMWR, Marzo 2010;59 (09):258-61); en casos de especial riesgo: anemia de células falciformes, VIH, otros inmunocompromisos, pérdida de LCR, implante coclear se extiende la recomendación a los 18 años, incluso si estos niños hubieran recibido o no VCN-7V o vacuna polisacárida 23-V.
Ambos conjugados han incorporado entre otros los ST 1 y 5 con lo que su cobertura contra ENI en Latinoamérica ha aumentado a > del 80%.
Se acepta que ambas pueden intercambiarse con VCN-7V para la dosis de refuerzo; Según la FDA VCN-13V puede intercambiarse con VCN-7V en cualquier dosis del esquema primario, por utilizar el mismo carrier; este intercambio no está todavía definido para VCN-10V .
La vacuna de 10 ST posee el potencial beneficio de ampliar su cobertura contra la otitis media aguda por H. influenzae no tipificable (HiNT), al contener como proteina transportadora membrana externa de este germen. La VCN-13V ha sido elaborada con el mismo carrier utilizado en VCN-7V, lo que aseguraría una correlación inmunológica entre los ST compartidos. Además, extiende la cobertura contra el ST 19A, que presenta un clon multirresistentes a los ATB, e incrementó su frecuencia en el mundo; y el ST 3 que en Costa Rica se ha aislado con frecuencia creciente del fluido del oido medio en niños con OMA purulenta. Tiene el beneficio de ampliar su cobertura para ST que causan ENI.
Ambas vacunas cumplen con los criterios de no inferioridad respecto a VCN-7V, como fueron propuestos por OMS: nivel adecuado de IgG por ELISA, y/o funcionalidad de los Ac expresado por la opsonofagocitosis (OPA), logrando título > 1:8 para todo lo ST luego de cumplido el plan primario y el refuerzo a lo 12-15 meses.
La incorporación al calendario vacunal de alguno de estos nuevos conjugados dependerá de las decisiones que tomen en cada país los respectivos ministerios de salud, basadas en las posibilidades y las logísticas de cada uno de ellos. Es posible que en algunos sean prioritarias la disminución de las tasas altas de OMA, y en otros, la prioridad sea la disminución de la ENI.
Recomendaciones respecto a la inmunización con nuevas vacunas conjugadas:
- Esquema convencional: Vacunar en forma rutinaria a todos los niños a partir del 2° mes de vida, utilizando el mismo esquema de la 7-V con 3 dosis administradas a los 2, 4, 6 meses de edad y una 4a dosis o refuerzo entre los 12 y 15 meses.
- Esquema alternativo: Dos dosis aplicadas a los 2 y 4 meses con refuerzo a los 12-15 meses
- Esquema para niños mayores de 6 meses sin inmunización previa:
a) Entre 7 y 11 meses: 2 dosis con 2 meses de intervalo y refuerzo a los 12-15 meses
b) Entre 12 y 23 meses: 2 dosis con intervalo de 2 meses
c) 24 a 59 meses 1 sola dosis
Para pacientes de alto riesgo entre 24 y 59 meses con esquema incompleto: 2 dosis con intervalo de 2 meses; solamente 1 dosis si recibió 3 dosis de la 7-V.
Consideramos que debe ser un compromiso de salud pública de todos los países, el que alguna de estas nuevas vacunas sea incluida en el calendario vacunal nacional para minimizar al máximo la morbi-mortalidad por NAC y otras ENI, especialmente en niños pertenecientes a familias con deprivaciones socio-económicas y culturales.
Concentraciones protectoras de Acs contra la ENI: Se denomina "correlato de inmunidad" al nivel mínimo de Ac que correlacionan con protección clínica en los estudios previos con VCN-7V; es además medir su capacidad funcional, por opsonofagocitosis (OPA). Títulos > 1:8 o expresan adecuada funcionalidad. Los tests para demostrar esta funcionalidad no están aún estandarizados por laboratorios de referencia. Es por ello que el concepto de correlato de protección es crucial, ya que permite predecir efectividad en poblaciones donde no es posible hacer estudios clínicos de eficacia.
La concentración de Ac de 0.35 mg/ml, se establece como el nivel umbral que correlaciona con protección clínica contra ENI. Es importante enfatizar que el "correlato de protección" para ENI no predice la protección individual contra NAC, OMA, o reducción de la colonización nasofaríngea, donde los niveles necesarios podrían ser mayores206. Además es importante aclarar que la respuesta a la vacuna puede variar de una población a otra.
Otros autores han sugerido que los niveles de Ac protectores contra ENI podrían ser menores207; los expertos coinciden en la necesidad de lograr niveles más altos que 0.35 mg/ml para proteger contra enfermedad de mucosas y colonización nasofaríngea.
Vacuna anti-Influenza: El análisis de los datos recogidos durante los años 1994/98 a través de la red de vigilancia epidemiológica en Latinoamérica mostró diferencias entre las cepas circulantes y las vacunales. En base a estos datos, expertos mundiales de la OMS recomendaron desde 1999, la constitución anual de una vacuna específica para cada hemisferio.
La vacuna inactivada es producida en huevos embrionados y contiene 2 cepas del tipo A y una del B de las que circularon en la temporada anterior por lo que su composición varía anualmente. La denominación del virus se hace en base al lugar y a la fecha de aislamiento. Cada dosis de 0,5 ml contiene 15 μg de Hemaglutinina (H) de cada una de las cepas contenidas en la vacuna.
Preparaciones de uso corriente
Son de tres tipos:
1) Las de virus entero inactivado o inactivadas, elaborada de partículas virales purificadas.
2) Las de tipo subvirión, preparada tras la desintegración de la membrana lipídica del virus.
3) Las preparadas a partir del antígeno de superficie purificado.
Para minimizar las reacciones febriles se recomienda que los < de 13 años reciban las de tipo 2) o 3), arriba mencionadas208.
Con respecto a su almacenamiento, deben conservarse a temperatura entre 2°C y 8°C, en la parte central e inferior de la refrigeradora. No deben de congelarse.
Existe una vacuna anti-influenza de virus vivos atenuados, adaptados para crecer a una temperatura de 25° C por lo que sólo se replican en el tracto respiratorio superior, más específicamente, intranasalmente. Induce una respuesta inmunológica local inmediata y desarrolla inmunidad T-dependiente que es más duradera y sostenida. Está indicada para niños y adultos sanos entre los 5 y 49 años. Su eficacia en los niños parece ser superior a la de la vacuna inactivada. No está todavía disponible en nuestro medio.
Indicaciones209-210: Las vacunas inactivadas se pueden aplicar a partir de los 6 meses de edad; en muchos paises se administra universalmente unas 6 semanas antes del inicio de la estación epidémica. En otros paises solamente se aplica a individuos con FR para el desarrollo de enfermedad complicada como: mayores de 65 años; pacientes de cualquier edad con enfermedades metabólicas y endocrinológicas crónicas; individuos institucionalizados; niños y adultos con patología cardíaca o pulmonar crónica; asma grave; disfunción renal; hemoglobinopatías; inmunosupresión de cualquier índole; niños y adolescentes que reciben saliciloterapia crónica (por riesgo de desarrollar síndrome de Reye post-influenza); mujeres embarazadas en el 2° o 3o trimestre de gestación. También es conveniente vacunar a todas las personas en contacto con pacientes de riesgo a fin de reducir la posibilidad de transmisión de la enfermedad. Estas son: integrantes del equipo de salud de hospitales o sitios de tratamiento ambulatorio, personal de hogares de ancianos o instituciones de pacientes crónicos, convivientes con individuos de riesgo. Se ha hipotetizado que su administración a los niños de corta edad disminuiría los episodios de OMA recurrente.
En los pacientes con infección por VIH, con enfermedad avanzada y bajo recuento de CD4, la vacuna puede no inducir una respuesta protectora; en ellos, la administración de una 2a dosis no mejora la respuesta.
Actualmente se dispone de una vacuna monovalente para la nueva cepa pandémica A (H1N1), que confiere inmunidad específicamente contra este virus. En Argentina se indicó gratuitamente en los hospitales públicos a todas las personas incluidas en grupos de especial riesgo; además de los mencionados: todos los < de 5 años, embarazadas, puérperas dentro de los 6 meses del parto, obesidad mórbida. Se logró amplia cobertura, que condicionó para el año 2010 que a la semana epidemiológica 30, el virus pandémico prácticamente no circulara en el país (menos de 20 casos denunciados).
Se dispuso de una vacuna trivalente, que incluye la de Influenza estacional y la cepa H1N1 pandémica, indicada en particular por el subsector privado.
Las vacunas en uso confieren protección específica contra las cepas virales que contienen, no así contra otros virus de influenza como el aviar211. Reducen el riesgo de coinfección y recombinación del virus influenza A humano con el virus aviar; por ello se recomienda su aplicación a personas en riesgo de exposición al mismo212.
En EEUU, Canadá y en varios países de Europa y Latinoamérica, la vacuna anti-influenza ha sido incorporada al Calendario nacional a partir de los 6 meses de vida.
Número de dosis, esquema y vía de administración: Para los niños < de 3 años se indica media dosis (0,25 ml ) y para los > a 3 años 0,5 ml . Existe una presentación comercial "Júnior" de 0,25 ml . En niños < 9 años se deben aplicar 2 dosis para la primovacunación, con un intervalo de 1 mes entre ambas. Los mayores de esa edad sólo deben recibir 1 dosis. Puede administrarse concurrentemente con las demás vacunas del calendario. La aplicación debe ser intramuscular. En adultos y niños mayores se debe aplicar en el músculo deltoides y en lactantes y niños pequeños en la región antero lateral del muslo209.
Inmunogenicidad y eficacia clínica: La efectividad de la vacuna para prevenir o atenuar la enfermedad depende de varios factores como la edad del paciente, su estado inmunológico, la semejanza entre los Ag contenidos en la vacuna administrada y los de las cepas circulantes. La mayoría de los niños > de 2 años y los adultos jóvenes sanos alcanzan altos títulos de Ac inhibidores de la hemoaglutinación pocas semanas después de la vacunación213.
Cuando la relación entre los antígenos vacunales y los de los virus circulantes es estrecha, la protección preventiva es cercana al 70% en individuos sanos < de 65 años. La aplicación de la vacuna en cada país o región debe ser acorde con el inicio de la estación epidémica en cada uno de ellos. En los de clima templado con 4 estaciones, debe inciarse en otoño, en cuanto se disponga de ella. El tipo de virus circulante en cada estación epidémica no puede predecirse. En un mismo año puede haber más de un brote epidémico por país o región, por lo que deben extremarse los esfuerzos para vacunar tempranamente a las poblaciones de riesgo aún después del inicio de la estación epidémica214-215.
Revacunación: Se requiere una vacunación anualmente. La duración de la etapa vacunal en el tiempo será igual o levemente más prolongada a la de la estación epidémica210.
Efectos adversos: La reacción más frecuente es local y consiste en dolor en el área de la vacunación; se presenta en menos de un tercio de los vacunados y dura alrededor de 48 h. Las reacciones sistémicas como fiebre, malestar general, mialgias, son poco frecuentes; se observan especialmente en los individuos que han tenido contacto previo con el antígeno viral. Se presentan entre 6 y 12 h después de la vacunación y se prolongan por 1 o 2 días. En ensayos clínicos controlados con placebo y a doble ciego, llevados a cabo en adultos jóvenes sanos y personas mayores, la frecuencia de los síntomas generales fue similar en ambos grupos.
Las reacciones de hipersensibilidad a cualquiera de los componentes de la vacuna son raras pero han sido reportadas. No existen datos fehacientes que avalen la asociación entre la aplicación de la vacuna y el síndrome de Guillain-Barré. No obstante, se recomienda cautela al considerar la vacunación de personas que presentaron este síndrome ≤ 6 semanas antes de la vacunación209-210. Su coadministración con las otras vacunas habituales no ha sido contraindicada. Las presentaciones de multidosis contienen timerosal con trazas de mercurio; la cantidad de mercurio que contiene es muy escasa, no representan riesgo para los niños. Tampoco serían de riesgo en embarazadas, aunque sería proferible para este grupo usar en monodosis.
Contraindicaciones: No debe administrarse a personas con hipersensibilidad al huevo u otros componentes de la vacuna. No está indicada su aplicación a adultos febriles hasta tanto no se hayan resuelto la fiebre y/o el cuadro infeccioso que la ocasionó. En los niños con enfermedades febriles o no, no existe contraindicación para su aplicación.
10. Valoración Económica en la región
Introducción: La NAC es la causa más común de muerte en < de 5 años, lo que representa alrededor de un 2% de las 10 millones de muertes infantiles en todo el mundo4.
Las estadísticas de Salud Pública confirman que los < de 2 años que viven en países de bajos y medianos ingresos tienen mayores tasas de mortalidad por esta enfermedad comparado con los países de altos ingresos216.
Para estimar el impacto fármaco-económico de las NAC, los datos epidemiológicos de su incidencia y el costo de los recursos utilizados necesitan integrarse con las variables demográficas locales. De esta forma resulta posible estimar el costo asociado a la carga de enfermedad que genera esta patología en el país o región donde se realiza la valoración económica. Esta acción constituye un desafío particular, ya que por el momento no existe una única forma de valoración de la misma, en términos de patrones clínicos, radiológicos, de precios y utilización de recursos.
Datos de carga de enfermedad
Diferentes países en Latinoamérica han establecido la incidencia de NAC con base poblacional en relación a la confirmación diagnóstica por Rx de tórax. Con algunas variaciones en los criterios de inclusión, los resultados de los distintos estudios presentan resultados similares.
En un estudio realizado en la Ciudad de Córdoba, Argentina (M. Tregnaghi y col.), incluyendo < de 2 años (Diciembre 1999-Noviembre 2002), la incidencia anual de NAC probablemente bacteriana por criterios radiológicos, fue de 2769 episodios cada 105 de población22-217. En un estudio similar realizado en Uruguay, sobre un total de 2034 pacientes la tasa anual de incidencia de NAC consolidante fue de 1175/105 habitantes19. Existen estudios adicionales que refuerzan la solidez de los valores de incidencia de NAC confirmada por Rx descriptos anteriormente. En Argentina los estudios desarrollados durante 2002-2005 por Gentile A. y col. en el Partido de Pilar (Pcia. de Bs. As.)218, Ruvinsky R y col. en los Departamentos de Concordia y Paraná (Pcia. de Entre Ríos)20, y el de Lagos y col.219 en Santiago de Chile. Según estimaciones del Instituto Sabin220, el promedio anual de NAC probablemente bacteriana en < de 2 años para la región es de 2132/105 casos. Finalmente el estudio desarrollado en Goiana Brasil muestra tasas entre 1395 y 4277/105 para < de 2 años que se atienden en hospitales o servicios de atención primaria221-222.
Utilización de recursos y costos médicos
Los costos de atención de una neumonía varían considerablemente en función del estándar de tratamiento ambulatorio, la incidencia de complicaciones y el precio de los recursos utilizados. En la tabla 1 se describen los costos en dólares estimados para las distintas formas clínicas de NAC según diferentes estudios.

Para la mayoría de los Sistemas de Salud, el precio del "día cama" constituye el 95% del costo del día de internación,(a) ya que la mayoría de las prácticas y tratamientos se encuentran incluidos en este valor.
Distintos enfoques se han tomado para valorar el promedio de días de internación de una NAC. Los trabajos de Constela y col.203 se basan en un estudio multicéntrico realizado en 33 hospitales y 10 centros ambulatorios. El estudio realizado en Argentina223, utilizó la base de datos de IRA de un hospital pediátrico(b); el del Grupo liderado por Ciro de Quadros del Sabin Institute220 (c) utilizó entrevistas y reuniones de expertos con el mismo objetivo. En todos los casos los precios de los recursos utilizados se tomaron de departamentos hospitalarios o administraciones estatales.
(a): A excepción de las NAC complicadas con supuración pleuropulmonar donde los gastos de videotoracoscopia, anestesia constituyen el 32% del costo total de niños internados con complicaciones.
(b): La media de días de internación fue de 7 días (NAC con y sin complicaciones) sobre un N de 3491 NAC.
(c): La media de días de internación fue de 12,8 días (NAC por todas las causas) y de 14,8 días para las radiológicamente confirmadas.
Años ganados y calidad de vida: Los datos de mortalidad por NAC son fundamentales para el cálculo de años ganados por muertes evitadas en presencia de vacunación y constituyen una de las variables de mayor importancia para los modelos de evaluación económica; las diferentes valoraciones económicas utilizan el costo por DALY(d) evitado o QALY ganado(e).
De esta forma es posible establecer diferencias entre el valor subjetivo de 1 año de vida en perfecta salud (valor = 1) y 1 año de vida con discapacidad, dolor crónico o necesidad básica insatisfecha (valor < 1).
(d)- DALY (Disability-Adjusted Life Years): Unidad de medida del impacto de una enfermedad en términos de tiempo perdido debido a una muerte prematura (mortality) y el tiempo de vida vivido con discapacidad (morbidity) El Global Burden of Diseases Study (GBDS) patrocinado por el World Bank iniciado en 1992 tiene como objetivo cuantificar la carga de enfermedad mundial. Esa cuantificación requiere una armonización de la unidad de medida en salud y por esa razón la OMS utiliza el concepto de DALY para las valoraciones de enfermedad.
(e)- QALY (Quality Adjusted Life Year): QALY es una forma de validación universal aplicable a todas las enfermedades que permite en una única medida, valorar la cantidad y calidad de vida en años ganados. Canadá ha sido pionero en el desarrollo de este concepto.
Los datos de mortalidad por NAC varían según las distintas estimaciones: En la revisión realizada por el Sabin Institute220, de acuerdo a los trabajos seleccionados por ellos132-224-225-226, se estima una mortalidad por NAC clínica en niños < de 5 años del 3% y una mortalidad por NAC con hemocultivo + para S. pneumoniae de 5,4 %227-228-229.
Ajustar los años por DALY o QALY en niños constituye un desafío y existe un número importante de publicaciones que debaten esta cuestión230-231-232-233.
Dos trabajos han valorado el impacto específico de la NAC en la calidad de vida en niños bajo este enfoque. Con leves diferencias, vinculadas posiblemente a los distintos patrones culturales de la población incluida, han sido de utilidad para la estimación de QALYS en varias evaluaciones económicas234-235. Los valores de utilidad para la neumonía moderada fueron de 0.5 y 0.6 respectivamente.
Perspectiva de costos no médicos y ausentismo laboral: De acuerdo a quien asume los costos de la enfermedad, distintas perspectivas pueden considerarse para valorar la carga económica. Desde la perspectiva de la Sociedad, los gastos de transporte y ausentismo laboral de los padres que ocasionan las NAC, incrementan el costo de esta enfermedad y varía considerablemente en función de si los pacientes se manejan en forma ambulatoria o internados. Para las ambulatorias el gasto por ausentismo laboral y viajes varía entre 13,67 y 78,53 U$S según los diferentes países y para internados entre 61.2 y 248.4 U$S de acuerdo a los datos estimados por el Sabin Institute220.
Análisis de Impacto de la vacuna conjugada neumocóccica heptavalente (VCN-7V): El n° de episodios de NAC prevenidos varía fundamentalmente de acuerdo a la eficacia de la vacuna, la cobertura vacunal de la población, el descuento por año utilizado, la distribución de ST de S. pneumoniae, la duración estimada de la inmunidad y la valoración clínica de la misma. Para el grupo de Ciro de Quadros236, se evitaron 12,3 episodios de NAC por año c/1000 niños vacunados. Dada la prevalencia de S. pneumoniae en la etiología de la NAC, el número de casos evitados por la vacuna resulta de alto impacto en las valoraciones económicas. Además de correlacionarse fuertemente con el número de muertes evitadas(f), QALY ganados o DALY evitados, el impacto de este conjugado permite una reducción del 20% del costo total de todas las ENI estimado para el caso base.
(f) Del total de muertes evitadas por PCV7 para las distintas formas clínicas de ENI, 80% son por NAC.
A diferencia de los países del hemisferio norte donde el n° de años ganados c/1000 niños vacunados oscila en un promedio de 8.5237 (0.05 muertes evitadas c/1000 niños vacunados), los datos de valoración económica realizada por Ciro de Quadros y col.236, estiman un promedio de 27.5 DALY evitados (0.9 muertes evitadas c/1000 niños vacunados) y para el realizado en Argentina223-235 aproximadamente en 30 QALY ganados (1 muerte evitada c/1000 niños vacunados). Ello podría deberse a que las tasas de mortalidad de la región son superiores a las del hemisferio norte. En función de lo expresado anteriormente, se desataca que para la región el n° de NAC evitadas por la vacuna contribuye en 80% al total las muertes evitadas por ENI.
Conclusiones:
El costo de la NAC para un país depende de la incidencia poblacional, la proporción de pacientes que se internan, los precios de la prestación, gastos de viaje, ausentismo laboral y mortalidad.
La NAC compromete la calidad de vida de los niños y su familia.
Dada la incidencia y mortalidad elevada reportada, la NAC constituye un problema económico y de salud de gran importancia para la región.
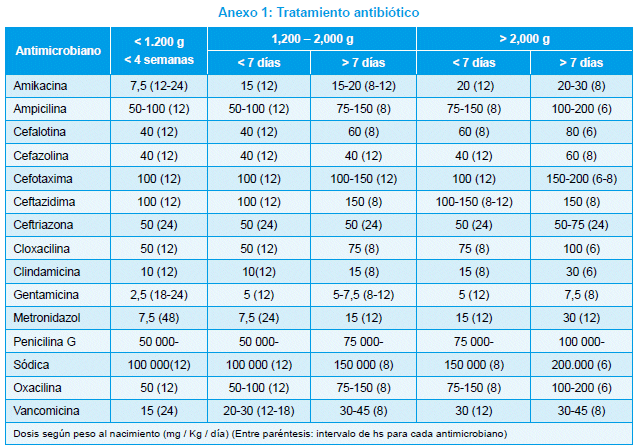
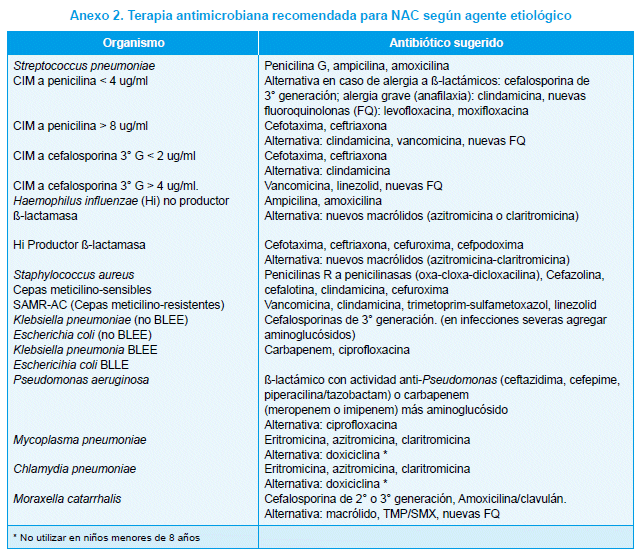
Anexo 3. Tratamiento del Empiema de la Neumonía Adquirida en la Comunidad
Uso de la estreptoquinasa en el manejo del derrame pleural
1. Instilación intrapleural de estreptoquinasa (STQ): A comienzos del año 2005, en la Unidad Médico-Quirúrgica del Hospital Pediátrico de referencia nacional Pereira Rossell del Uruguay, se decidió implementar un protocolo de instilación intrapleural de STK para el tratamiento de los niños con empiema complicado, como alternativa al tratamiento quirúrgico.
2. Se definió empiema complicado cuando una vez colocado el drenaje de tórax, el paciente presentaba fiebre durante más de 48 h, mal estado general o disfunción del tubo de drenaje, y en la ecografía de tórax se evidenciaba derrame complejo tabicado. Los niños que presentaron esta evolución en los primeros 8 días luego de colocado el drenaje de tórax, recibieron tratamiento con STK intrapleural durante 3 días, una dosis diaria de 100.000 UI (< 1 año) o 200.000 UI (> 1 año).
3. Al analizar los resultados de este protocolo se observó que en estos niños se evitó la toracotomía y se redujeron los días de drenaje de tórax post-procedimiento, de 9.5 días a 3.5 días. Una evaluación complementaria de los costos determinó la incorporación de la instilación intrapleural de STK como una alternativa terapéutica en niños con empiema complicado. A partir del 2007, basados en datos internacionales, en la unidad la decisión de iniciar tratamiento con STK intrapleural se toma en base a los siguientes criterios:
a. Cuando luego de colocado el drenaje de tórax el niño continúa febril (T°ax. > 38°C) durante más de 48 h, mal estado general, disfunción del tubo de drenaje, y la ecografía muestra presencia de derrame complejo, tabicado o con septos.
b. Cuando en la ecografía de tórax al ingreso, previo a la colocación deL drenaje, se observa derrame complejo, con septos, tabiques o partículas en suspensión; y/o se halló fibrina en el acto operatorio.
En los pacientes que tienen criterios de empiema complejo el tiempo mínimo ideal entre la colocación de drenaje y la administración de STK es 12 h.
Administración de estreptoquinasa en niños con empiema tabicado: Tiene la ventaja que es sencillo, se puede realizar en sala general por un equipo previamente entrenado, no requiere cuidados especiales, no interfiere con la actividad del niño ni con su alimentación. No se observaron reacciones adversas graves, fue bien tolerado por todos los pacientes, sin aumento de la morbilidad.
Recursos: Humanos:
1 Médico - 1 Enfermero.
Materiales:
- Sobretúnica, tapaboca, gorro y guantes estériles.
- Clorhexidina alcohólica.
- Campo estéril Gasas estériles.
- Jeringas de 50cc, 20cc, 10cc y 5cc.
- Pinzas de plástico para el clampeo.
- Suero fisiológico
- Hidrocortisona.
- Bupivacaína
- Estreptoquinasa.
- Hojas de bisturí.
Dosis:
Estreptoquinasa.
< de 1 año 100.000 unidades.
> de 1 año 200.000 unidades.
Bupivacaína al 0,25:
< de 1 año 10cc.
> de 1 año 20 cc.
Procedimiento.
Lavado de manos de los que participen en el procedimiento. El médico se viste con ropa estéril.
Preparación sobre campo estéril de bupivacaína y estreptoquinasa con dosis de acuerdo a la edad del niño.
La hidrocortisona es administrada IV por el personal de enfermería media hora antes del procedimiento.
Clampeo el tubo de drenaje y retiro el frasco midiendo el gasto y valorando las características del líquido drenado.
El médico conecta la jeringa con la dilución de bupivacaína en el catéter pleural, desclampea el catéter e inyecta la bupivacaína, espera unos minutos, vuelve a clampear e intercambia las jeringas colocando la que contiene estreptoquinasa, vuelve a desclampear e inyecta lentamente la misma luego de lo cual se deja clampeado por cuatro h.
Cumplido el plazo de las cuatro horas el enfermero conecta el drenaje nuevamente a un sistema cerrado.
Realiza medición del gasto, valora tolerancia al procedimiento y registra en historia clínica.
Bibliografía
1. Rudan I, Tomaskovic I, Boschi-Pinto C et al. Global estímate of the incidence of clinical pneumonía among children under 5 years of age. Bull. World Health Organ. 2004;82:895 [ Links ]
2. Kanno MB, Brown PD. Community acquired pneumonía: An Overview. Curr. Infect. Dis. Report 1991; 1:49-56 [ Links ]
3. Morris S, Tomaskovic L, Black R et al. Predicting the distribution of under-5 deaths by cause in countries without adequate vital registration systems. Int. J. Epidemiol. 2003 ;32:1041-51 [ Links ]
4. Williams BG, Gouws E, Boschi-Pinto C, et al. Estimates of world wide distribution of child deaths from acute respiratory infections. Lancet Infect Dis 2002;2:25-32 [ Links ]
5. Mulholland K. Global burden of acute respiratory infections in children: implications for interventions Pediatr. Pulmonol. 2003;36 (6):469-74 [ Links ]
6. Black R, Morris S, Bryce J. Where and why are 10 million children dying every year? Lancet 2003; 361:2226-34 [ Links ]
7. WHO (1990) Acute Respiratory Infections in Children: Case management in small hospital in developing Countries. A manual for doctors and others Sénior Health Workers.DocumentWHO/ARI/90.5. Geneve
8. Rudan I, Boschi-Pinto C. Biloglav Z, Mulholland K et al. Epidemiology and etiology of childhood pneumonia. Bull World Health Organ 2008 ;86:408-416 [ Links ]
9. Benguigui Y, López Antuñano FJ, Schmunis G y col. Infecciones respiratorias en niños. Serie HC17 AIEPI-1. OPS/OMS, 1999) [ Links ]
10. Weekly epidemiological record 2007;82 (12):93-104 :www.who.int/wer [ Links ]
11. Sazawal S, Black RE. Effect of pneumonia case management on mortality in neonates, infants and preschool children: a meta-analysis of community based trials Lancet 2003;3 (9):547-56. [ Links ]
12. United Nations Millennium Development Goals. Available from: http://www.un.org/millenniumgoals/ accessed on 1 April 2008. [ Links ]
13. Benguigui Y. Current health conditions and perspectives on the millenium developments goals related to childhood mortality in the Región of the Americas. IMCI Technical Advisory Group (TAG), 3th meeting, PAHO, Texas Children Hospital, 18-19 May, 2004: pp 15-23 [ Links ]
14. Simposio Sub-regional de Neumococo: Cono Sur. Santiago de Chile, 13-14 dic. 2007 [ Links ]
15. Levine MM, Lagos R, Levine OS.Epidemiology of invasive pneumococcal infections in infants and young children in Metropolitan Santiago, Chile Pediatr. Infect. Dis. J. 1998;17 (4):287-93 [ Links ]
16. Crowcroft NS, Stein C, Duelos P, Birmingham M. How best to estimate the global burden of Pertussis? Lancet Infect. Dis. 2003;3:413-8 [ Links ]
17. OMS. Hemophilus Influenzae tipo b. Nota descriptiva No. 294, 2005. www.who.int/mediacentre/factsheetss/fs294/es/index.html [ Links ]
18. Amorin MB, Castro M, Sandin D, Chamorro F, Romero C, Giachetto G, Pirez M.C. Infecciones invasivas por S. aureus meticilino resistente adquirido en la comunidad. Presentación clínica y evolutiva observada en dos centros universitarios. Uruguay 2003-2007. Rev Med Uruguaya. 2008;24:230-7 [ Links ]
19. Hortal M, Estevan M, Iraola I, De Mucio B. A population based assesment of the disease burden of Consolidated pneumonía in hospitalized children under five years of age. Int. J. Infect. Dis. 2007 May; 11 (3):273-7 [ Links ]
20. Ruvinsky R, Gentile A, Gentile F et al. Surveillance of Pneumonía Probably Bacteriana in Children in Argentina 15th Congress of Clinical Microbiology and Infectious Diseases, Copenhagen, Denmark, 2-5 April 2005, Abstract [ Links ]
21. Gentile A, Ruvinsky R, Bakir J et al. Surveillance of Probably Bacterial Pneumonia in children less than 5 years old in two geographical áreas in Argentina. 45th Intersc. Confer. On Antimicr.Agents and Chemother. (ICAAC), Wash.. DC, 17 December 2005-pp 236 G-82220 [ Links ]
22. Tregnaghi M, Cevallos A, Ruttiman R et al. Active epidemiologic surveillance of pneumonía and invasive pneumococcal disease in ambulatory and hospitalized infants in Córdoba, Argentina. Pediatr. Infect. Dis. J. 2006; Apr. 25 (4):370-221 [ Links ]
23. Mulholland K. Magnitude of the problem of childhood pneumonía. Lancet 1999; 354:590-92 [ Links ]
24. Walker N, Schwartlánder B, Bryce, J. Can HIV/ AIDS explain recent trends in child mortality in sub-Saharan África?. JAMA (in press) [ Links ]
25. Bulla A, Hitze KE. Acute Respiratory Infections: a review. Bull. World Health Organiz. 1978;56:481 [ Links ]
26. Consenso de la Sociedad Argentina de Pediatría. Comité Nacional de Neumonol. e Infectol. Recomendaciones para el diagnóstico y tratamiento
de las Infecciones Respiratorias Agudas Bajas en < de 2 años. Arch. Argent. de Pediatría 2006;104 (2): 157-76
27. Reilly JJ, Wells JCK. Duration of exclusive breastfeeding: introduction of complementary feeding may be necessary before 6 months of age. Br. J. Nutr. 2006;95:1229-30 [ Links ]
28. Black RE, Alien LH, Bhutta ZA et al. "A lack of exclusive breastfeeding in the first half of infancy is a risk factor for ALRI incidence, morbidity and death. Maternal and child under nutrition: global and regional exposures and health consequences" Lancet 2008 ;371:243-60 [ Links ]
29. Rice AL, Sacco L, Hyder A, et al. Malnutrition as an underlying cause of childhood deaths associated with infectious diseases in developing countries. Bull World Health Organiz. 2000;78:1207-21 [ Links ]
30. Víctora CG, Kirkwood BR, Ashworth A et al. Potential interventions for the prevention of childhood pneumonia in developing countries: improving nutrition. Am J. Clin. Nutr. 1999;70:309-20 [ Links ]
31. Fedson DS, Musher DM, and Eskola J. Pneumococcal vaccine. in "Vaccines" 3rd ed., Philadelphia PA, WB Saunders, 1999;553-67
32. Mulholland EK, Levine O, Nohynek H, Greenwood BM. The evaluation of vaccines for prevention of pneumonia in children in developing countries. Epidemiol. Rev. 1999;21:1-13 [ Links ]
33. Klugman KP, Madhi SA, Huebner RE et al. A trial of a 9-valent pneumococcal conjúgate vaccine in children with and those without HIV infection. N. Engl. J. Med. 2003 ;349:1341-48 [ Links ]
34. Boletín Epidemiológico de OPS: "Infecciones respiratorias agudas en las Américas" 1995;16 (4): 1-5
35. Durban WJ and Stille Ch. Pneumonia. Pediatr. Rev. 2008;29:147-60
36. Hambridge KM. Zinc and pneumonia. Am. J. Clin. Nutr. 2006; 83:991-92 [ Links ]
37. Gaetke LM, McClain CJ, Talwalkar RT and Shedlofsky SI. Effects of endotoxin on zinc metabolism in human volunteers. Am. J. Physiol. 1997; 272: e 952-e956 [ Links ]
38. Cousins, RJ 1985. Absorption, transport, and hepatic metabolism of copper and zinc: special reference to metallothionein and ceruloplasmin Physiol. Rev. 65:238-309
39. Truong-Tran AQ et al. Altered zinc homeostasis and caspase 3 activity in murine allergic airway inflammation. Am. J. Respir. Cell. Mol. Biol. 2002;27:286-296 [ Links ]
40. Makonnen B, Venter A, and Joubmrt G. A randomized controlled study of the impact of dietary zinc supplementation in the management of children with protein-energy malnutrition in Lesotho I: Mortality and morbidity. J. Trop. Pediatr. 2003;49:340-352
41. Sazawal S et al. Effect of zinc supplementation on mortality in children aged 1-48 months: a community based randomised placebo-controlled trial. Lancet 2007;369:927-934 [ Links ]
42. Jkolhede CL, Chew FJ, Gadomsky AM. et al. "Clinical trial of vitamin A as adjuvant treatment for lower respiratory tract infection". J. of Pediatr. 1995;126:807-12 [ Links ]
43. Huiming Y, Chaomin W and Meng, M. Vitamin A for treating measles in children. Cochrane Datábase Syst. Rev. 2005; CD 001479
44. Fuchs SC, Fischer GB, Black RE "The burden of pneumonia in children in Latin America" Pediatr. Respir. Rev. 2005 Jun;6 (2): 83-7 [ Links ]
45. Klig J.: Office Pediatrics: Current perspectives on the outpatient. Evaluation and Management of Lower Respiratory Infections in children. Current Opinion in Pediatrics. 2006;18:71-76 [ Links ]
46. Constantine A., Sinaniotis A. Community Acquired Pneumonia in Children. Current Opinión Pulmonary Medicine. 2006;11:218-25 [ Links ]
47. Korppi M, Heiskanen-Kosma T, Kleenola M. Incidence of community-acquired pneumonia in children caused by Mycoplasma pneumoniae: serological results of a prospective, population based study in primary health care. Respirol. 2004;9:109- 114 [ Links ]
48. Samsone D y col. Neumonía adquirida en la comunidad. Consenso de la Sociedad Venezolana de Neumonología y Cirugía de Tórax. 2005 [ Links ]
49. Audan I, Boschi-Pinto C, Biloglav Z et al. Epidemiology and Etiology of Childhood Pneumonia. Bull WHO 2008;86 (5):408 [ Links ]
50. Boyer K. Nonbacterial pneumonia in: Feigin, Cherry Textbook of Pediatric Infectious Diseases Saunders Ed. 5th Ed. 2004:286-87 [ Links ]
51. Klein J. Bacterial Pneumonia in Feigin, Cherry, Textbook of Pediatr. Infect. Dis. Saunders Ed. 5th Ed. 2004:301-10 [ Links ]
52. Hardie N, Bokube R, García FV Pneumococcal pleural empyema in children. Clin. Infect. Dis. 1996;22:1057-63 [ Links ]
53. Buckingham SC, King MD, Miller ML. Incidence and etiologies of complicated parapneumonic effusions in children, 1996 to 2001. Pediatr. Infect. Dis. /2003;22:499-504 [ Links ]
54. Schultz KD, Fan LL, Pinsky J, et al. The changing face of pleural empyema in children: epidemiology and management. Pediatrics 2004; 113:1735-1740 [ Links ]
55. Cardoso MR, Nascimento-Carvalho C, Ferrero F, Berezin EW, Ruvinsky R et al. Penicillin-resistant pneumococcus and risk of treatment failure in pneumonia. Arch. Dis. Child. 2008;93:221-25 [ Links ]
56. Gabastou JM, Agudelo CI, Brandileone MC , Castañeda E y col. Caracterización de aislamientos invasivos de S. pneumoniae, H. influenzae y N. meningitidis en América Latina y el Caribe: SIRE-VAII, 2000-05 Rev. Panamer. Salud Públ. 2008:24 (1):1-15
57. F. Chambers MD Community-Associated MRSA-Resistance and Virulence Converge. NEJM 2000;352:1485-1487
58. Pedreira W y Galiana A. Un nuevo clon de Staphylococcus aureus con resistencia a meticilina y alta virulencia emergente en la comunidad y en los grandes hospitales en Uruguay/ (cited 2005 May 26) http://www.higiene.edu.uy/clona.htm) [ Links ]
59.Notario R, Lejona S, Méndez E, y col. Aislamiento de S. aureus meticilino-resistentes adquiridos en la comunidad SAMR-AC. Rev. Méd. Rosario 2007;73:82- 85
60. Labandeira-Rey M, Couzon F, Boisset S, et al. S. aureus Panton-Valentine leukocidin causes necrotizing pneumonia. Science 2007;315:1130-33 [ Links ]
61. Castillo de Febres O, Casanova L, Graffe V, Sánchez de Naveda M y col. Evaluación y Diagnóstico de 140 Neumonías Bacterianas. Sabélica Médica 1986:11:217-52
62. Cherry J, Ching N. Mycoplasma and Ureaplasma Infections. In: Feigin, Cherry Textbook of Pediatric Infectious Diseases. Sanders 5th Ed. 2004:2516-47 noviembre 2010 21 [ Links ]
63. CDC Influenza MMWR Junio 28, 2006 [ Links ]
64. Cáceres C. Instituto Nacional de Higiene Rafael Rangel 2006 (INHRR) Boletín Epidemiológico. 28,
65. Kahr J. Newly Identified Respiratory Viruses. Pediatr. Infect. Dis. J. 2007;26:745-4 [ Links ]
66. Ruvinsky R, Dalamón R. Neumonía en la infancia: en: Voyer L, Ruvinsky R, Cambiano C, Pediatría, 2° Ed. 2005. Journal Ed., Bs. As. (en Prensa 3o ed.) [ Links ]
67. Gupta D, Mishra S, Chaturvedi P. Fast breathing in the diagnosis of pneumonia-A reassesment. J Trop Pediatr, 1996 ;42:196-199 [ Links ]
68. Lagos R, Di Fabio JL, Moenne K et al. Uso de la Rx de tórax para la vigilancia de neumonías bacterianas en niños en Latino América" Rev. Panamer. de Salud Pública, 2003;13 (5):294-302 [ Links ]
69. Spooner V, Barker J, Tulloch S et al. "Clinical signs and risk factors associated with pneumonia in children admitted to Goroka Hospital, Papua New Guinea" J. Trop Pediatr. 1989;35:295-300 [ Links ]
70. Leventhal J. Clinical predictors of pneumonia as guide to ordering chest roentgenograms Clin Pediatr. 1982;21:730-734 [ Links ]
71. Margolis P, Gadomski A. Does this infant have pneumonia? JAMA 1998;279:308-313 [ Links ]
72. Sazawal S, Black RE. Effect of pneumonia case management on mortality in neonates, infants and preschool children: a meta-analysis of community based trials" Lancet 2003;3 (9):547-56 [ Links ]
73. Comité de Neumonología de la Sociedad Argentina de Pediatría: "Consenso sobre infecciones respiratorias bajas" Arch. Argent. de Pediatría 1996;94:279-83 [ Links ]
74. Jadavji T, Law B, Lebel M, et al. A practical guide for the diagnosis and treatment of pediatric pneumonia. Can. Med. Assoc. J. 1997; 156 (supp1): S 703-11 [ Links ]
75. Kassisse E, Istúriz G, Sansone D, Villalón M, Contreras N, Urdaneta R y col. Consenso de la Sociedad Venezolana de Neumonología y Cirugía del tórax 2005
76. Korpi M. Non-specific host response markers in the differentiation between pneumococcal and viral pneumonia: whatis the most accurate combination? Pediatr. Int. 2004;46:545-550 [ Links ]
77. Ruvinsky RO, Quiriconi ME, Genre Bert Koll S y col. 4o Congr. Argent. de Infectol. Pediatr. Mendoza, Argentina, 27-30 de Abril, 2005, Poster [ Links ]
78. Prat C, Domínguez J, Rodrigo C, et al. Creactive protein, Procalcitonin, and leukocyte count in children with lower respiratory tract infection. Pediatr. Infect. Dis. J. 2003 ;22: 963-967 [ Links ]
79. Flood RG, Badik J, Aronoff SC. The Utility of Serum C-Reactive Protein in Differentiating bacterial from non-bacterial pneumonia in Children. A Meta Analysis of 1230 Children. Pediatr. Infect. Dis. J. 2008; 27 (2):95-99 [ Links ]
80. Muller B, Becker KL, Schochinger H. Calcitonine precursors are reliable markers of sepsis in a medical intensive care unit. Crit. Care Med. 2000 ;28 (4):977-83 [ Links ]
81. Briel M, Schltz P, Mueller B. Procalcitonin-Guided Antibiotic use vs. standard approach for Acute Respiratory Tract: Infections in Primary Care. Arch. Intern. Med. 2008;168 (18):2000-07 [ Links ]
82. López AF, Cubells L, Carda JG et al. Procalcitonin in pediatric emergency departments for the early diagnosis of invasive bacterial infections in febrile infants: results of a multicenter study and utility of a rapid qualitative test for this marker. Pediatr. Infect Dis J 2003 ;22:895-903 [ Links ]
83. Ulloa-Gutierrez R. Clin. Infect. Dis. 2008;47:729-30 [ Links ]
84. Korppi M, Remes S, Heiskanen-Kosma T. Serum procalcitonin concentrations in bacterial pneumonia in children: a negative result in primary healthcare settings. Pediatr. Pulmonol. 2003;35:56-61 [ Links ]
85. Rydell-Tormanen K, Uller L, Erjefalt JS. Direct evidence of secondary necrosis of neutrophils during intense lung inflammation. Eur. Respir. J. 2006;28:268-74 [ Links ]
86. Henrickson KJ. Costeffective use of rapid diagnostic techniques in the treatment and prevention of viral respiratory infections. Pediatr. Ann. 2005;34:24-31 [ Links ]
87. Shetty AK, Treynor E, Hill D, et al. Comparison of conventional viral cultures with direct fluorescent antibody stains for diagnosis of community-acquired respiratory virus infections in hospitalized children. Pediatr. Infect. Dis. J. 2003;22:789-794 [ Links ]
88. Lopez-Huertas MR, Casas I, Acosta-Herrera B, et al. Two RT-PCR based assays to detect human metapneumovirus in nasopharyngeal aspirates. J. Virol. Methods 2005; 129:1-7 [ Links ]
89. Klig JE: Office pediatrics: current perspectives on the outpatient evaluation and management of lower respiratory infections in children. Current Opinion in Pediatrics 2006,18:71-76 [ Links ]
90. BTS Guidelines for the management of community acquired pneumonia in childhood. Thorax 2002;57:S1-S24 [ Links ]
91. Ruvinsky RO, Ferrero F, Duran P et al. S. pneumoniae in vitro resistance to penicillin and clinical outcomes in children with severe pneumonia. 4th Congr. Amer. Soc. of Microbiol. (ICAAC), Wash. DC, Sept. 2004, oral slide session [ Links ]
92. Lin PL, Michaels MG, Janosky J, et al. Incidence of invasive pneumococcal disease in children 3 to36 months of age at tertiary care pediatric center 2
years after licensure of the pneumococcal conjugate vaccine. Pediatrics 2003;111:896-99.
93. Dowell, S.F, Garman, R.L., Liu, G., Levine, O.S., et al. Evaluation of Binax NOW, an assay for the detection of pneumococcal antigen in uriñe samples, performed among pediatric patients. Clin. Infect. Dis. 200132:824-825 [ Links ]
94. Hill, PC, et al. Nasopharyngeal carriage of S. pneumoniae in Gambian villagers. Clin. Infect. Dis. 2006;43: 673-679 [ Links ]
95. Carrol ED, Guiver M, Nkhoma S, et al. Ffigh pneumococcal DNA loads are associated with mortality in Malawian children with invasive pneumococcal disease. Pediatr. Infect. Dis. J. 2007;26:416-22
96. Requejo H. Community-Acquired Pneumonia in the Childhood: Analysis of the Diagnostic Methods. British J. Infect. Dis. 2007;11 (2):246-48 [ Links ]
97. Klugman KP, Madhi SA and Albrich WC. Novel Approaches to the Identification of S. pneumoniae as the cause of Community-Acquired Pneumonia Clin. Infect. Dis. 2008; 47: S202-6
98. Rev. Soc. Venezolana de Microbiología Vol 27, N° 2,2007 [ Links ]
99. Daxboeck F, Krause R, Wenisch C. Review: Laboratory diagnosis of M. pneumoniae Infect. Eur. J. Clin. Microbiol. Infect. Dis. 2003;9:263-73 [ Links ]
100. Cherry JD, Ching N. Mycoplasma and Ureaplasma infections in: Feigin RD, Cherry JD et al. Textbook of Pediatr Infect. Dis., 5th ed., Vol. 2, Saunders Ed. 2004; pp 2516-47 [ Links ]
101. Waris ME, Toikka P, Saarmen T et al. Diagnoses of M. pneumoniae pneumonia in children. J. Clin. Microbiol. 1998;36:3155-59 [ Links ]
102. Paisley JW, Laner BA, Melinkovich P et al. Rapid diagnosis of C. trachomatis in infants by direct IF. Microscopy of nasopharingeal secretions. J. of Pediatr. 1986; 109:653-55 [ Links ]
103. Grayston JT, Campbell LA, Kero CC. A new respiratory tract pathogen. C. pneumonia strain TWAR. J. Infect. Dis. 1990;161:618-25 [ Links ]
104. Pérez Frías J, Martínez León M, Cordón A M. Derrame Pleural: etiología y manejo. En: Cobos Barroso N y col. Tratado de Neumología Infantil. Ergon Madrid, 2003: 785-90 [ Links ]
105. Ferrari AM, Pírez MC, Martínez A, Algorta G, Chamorro F, Guana MJ, Zabala C, Giachetto G, Montano A. Etiología de la neumonía bacteriana adquirida en la comunidad en niños hospitalizados: Uruguay 1998-2004 Rev. Chil. Infectol. 2007;24 (1):40-47 [ Links ]
106. Navarro Merino M, Gómez Pastrana D. Neumonías Bacterianas e Infección Respiratoria por Mycoplasma en: Cobos Barroso N y col. Neumología Infantil. Ergon Madrid, 2003:405-26 [ Links ]
107. Le Mense G, Strange C, Sahn SA. Empyema thoracis: Therapeutic management and outcome. Chest. 1995; 107:1532-7 [ Links ]
108. Wait M, Sharma S, Hohn J, Dal Nogare A. A randomized trial of empyema therapy. Chest. 1997;111:1548-51 [ Links ]
109. Pothula V, Krellenstein DJ. Early aggressive surgical management of parapneumonic empyemas. Chest. 1994;105:832-6 [ Links ]
110. Jerges C, Ramírez A, Elizalde J. Intrapleural fibrinolysis with Streptokinase as and adjunctive treatment. In hemothorax and empyema. A multicenter trial. Chest. 1996; 109:1515-9 [ Links ]
111. Kooi Chin N, Lim T. Controlled trial on intrapleural Streptokinase in the treatment of pleural empyema and complicated parapneumonic effusion. Chest. 1997;111:275-9 [ Links ]
112. Grewal H, Jackson R, Wagner CW, Smith S. Early video-assisted thoracic surgery in the management of empyema. Pediatrics. 1999; May, 103(5):e63 [ Links ]
113. Mani C, Murray DL. Acute pneumonía and its complications. In: Long SS, Pickeriong LK, Prober CG et al. Principies and Practice of Pediatr. Infect. Dis. 3o Ed; Churchill, Livingstone. Philadelphia, 2008:245-57 [ Links ]
114. Pirez M.C. Montano A, Rubio I, Bello O, Scavone C. Neumonía bacteriana en: Atención Pediátrica. Pautas de diagnóstico, tratamiento y prevención. 6o ed, Ed.: Oficina del Libro, Montevideo 2007 [ Links ]
115. Light RW, Girard WN, Jenkinson SJ et al. Parapneumonic effusions. Am J Med. 1980;69:507-11 [ Links ]
116. Giachetto G, Pirez MC, Nanni L, Martínez A, Montano A, Kaplan SH. L., Ferrari AM. Ampicillin and penicillin conentration in serum and pleural fluid of hospitalized children with community acquired pneumonía. Pediatr. Infect. Dis. J. 2004;23:625-29 [ Links ]
117. Asencio de la Cruz O, Moreno Galdó A, Bosque García M. Derrame pleural paraneumónico. Guía diagnóstico terapéutica. Asociación Española de Pediatría. Protocolos actualizados al año 2008. www.aeped.es/protocolos/neumología/2.pdf Consultado 17/02/09
118. Fernández A, Giachetto G, Giannini G, Garat MC, Vero MA, Pastorini J et al. Instilación intrapleural de estreptoquinasa en el tratamiento del empiema paraneumónico complicado. An Pediatr (Barc). 2007;66 (6):586-590 [ Links ]
119. Doski JJ, Lou D, Hicks BA, Megison SM, et al, Management of parapneumonic collections infants and children. J Pediatr Surg. 2000;35:265-70 [ Links ]
120. Moenne,K., Ortega X. Diagnóstico por imágenes del tórax pediátrico Ed. Journal 2005 [ Links ]
121. Swischuk L. Emergency Pediatric Imaging: changes over the years. Review. Emerg. Radiol 2005; Jun 11(4):193-8 [ Links ]
122. Williams and Wilkins, 1997 cap. 1- pág. 1 y 3 [ Links ]
123. Kuhn J. Effmann E. Overview of imaging procedures in the pediatric neck and thorax. En: Caffey's pediatric diagnostic imaging. Pensilvania: Mosby 2004 [ Links ]
124.Swischuk L. Radiología de urgencia en pediatría Ed. Salvat 1983 [ Links ]
125. WHO: Integrated Management of Childhood 111-ness chart booklet. (WC 503.2) Geneva: WHO, 2008. Available at: http://whqlibdoc.who.int/publications/2008/9789241597289_eng.pdf. Accessed on January 15th 2009
126. Graham SM, English M, Hazir T, et al. Challenges to improving case management of childhood pneumonía at health facilities in resourcelimited settings. Bull WHO 2008;86:349-355 [ Links ]
127. Reyes H, Pérez-Cuevas R, Salmerón J, et al. Infant mortality due to acute respiratory infections: the influence of primary care processes. Health Policy Plan 1997;12:214-23 [ Links ]
128. Virkki R, Juven T, Rikalainen H, et al. Differentiation of bacterial and viral pneumonía in children. Thorax 2002;57:438-441 [ Links ]
129. Hale KA, Isaacs D. Antibiotics in childhood pneumonía. Paediatr. Resp. Rev. 2006;7:145-151 [ Links ]
130. Mclntosh K. Community-acquired pneumonía in children. N. Engl. J. Med. 2002;346:429-437. [ Links ]
131. Grant GB, Campbell H, Dowell SF, et al. Review and recommendations for treatment of childhood nonsevere pneumonía. Lancet Infect. Dis. 2009; Mar, 9 (3): 185-96 [ Links ]
132. Nascimento-Carvalho CM, Rocha H, Santos-Jesús R, Benguigui Y. Childhood pneumonía: clinical aspects associated with hospitalization and death. Braz. J. Infect. Dis. 2002;6:22-8 [ Links ]
133. Gessner BD, Castrodale L, Soriano-Gabarro M. Aetiologies and risk factors for neonatal sepsis and pneumonía mortality among Alas kan infants. Epidemiol. Infect. 2005; 133:877-81 [ Links ]
134. Guía clínica y formulario para el tratamiento de enfermedades infecciosas. Pan American Health Organization. Washington DC, EEUU. OPS/ HCP/210/2006
135. Nascimento-Carvalho CM, Souza-Marques HH. Recommendation of the Brazilian Society of Pediatrics for antibiotic therapy in children and adolescents with community-acquired pneumonia. Pan Am. J. Public Health 2004:380-387 [ Links ]
136. Amer. Acad. of Pediatr. Pickering LK, Baker CJ, Long SS, McMillan JA, eds. Red Book: 2006 Report of the Committee on Infect. Dis. 27th ed. Elk Grove Village, IL: Amer. Acad. of Pediatr; 2006 [ Links ]
137. Reese RE, Betts RF, Gumustop B. Handbook of antibiotics. 3rd ed. Philadelphia: Lippincott Williams and Wilkins; 2000 [ Links ]
138. Bradley JS, Wassel RT, Lee L, Nambiar S. Intravenous Ceftriaxone and Calcium in the neonate. Assesing the risk of cardiopulmonary events. Pediatrics 2009;123:e609-e613 http://www.rocheusa.com/products/rocephin [ Links ]
139. Portillo C, Lovera D., Arbo A. Neumonía por C. thracomatis en lactantes. Arch. Argent. de Pediatr. 1997;95 (Supl 1):42-46 [ Links ]
140. Shann F, Barker J, Poore P. Clinical signs that predict death in children with severe pneumonia. Pediatr. Infect. Dis. J. 1989;8:852-855 [ Links ]
141. Rudan I, Boschi-Pinto C, Biloglav Z et al. Epidemiology and etiology of childhood pneumonia. Bull WHO 2008;86:408-416 [ Links ]
142. Amorin B, Castro M, Sandin D, Chamorro F, Romero C, Giachetto G et al. Infecciones invasivas por S. aureus meticilino-resistente adquirido en la comunidad. Presentación clínica y evolutiva observada en dos centros universitarios. Uruguay 2003-2007. Rev. Med. Urug. 2008;24:230-237 [ Links ]
143. Maní C, Murray DL. Acute pneumonia and its complications. In: Long SS, Pickering LK, Prober CG. Principies and Practice of Pediatr. Infect. Dis. 3o Ed. Churchill, Livingst. Philad. 2008 pp. 245-257 [ Links ]
144. Pírez MC; Martínez O; Ferrari AM; Nairac A; Montano A; Rubio I; Sarachaga MJ; Brea S; Picón T; Pinchack MC; Torello P; Algorta G; Mogdasy MC. Standard case management of pneumonia in hospitalized children in Uruguay, 1997-1998. Pediatr. Infect. Dis. J. 2001 ;20:283-289 [ Links ]
145. Chetty K, Thomson AH. Management of community- acquired pneumonia in children. Pediatr. Drugs 2007;9:401-411 [ Links ]
146. CLSI. Performance Standards for Antimicrobial Susceptibility Testing; Sixteenth Informational Supplement. Wayne, USA: CLSI/NCCLS, 2008 [ Links ]
147. Giachetto G, Pirez MC, Nanni L, Martínez A, Montano A, Kaplan SH. L., Ferrari AM. Ampicillin and penicillin concentration in serum and pleural fluid of hospitalized children with community acquired pneumonia. Pediatr. Infect. Dis. J. 2004;23:625-29 [ Links ]
148. Nascimento-Carvalho CM, Ferrero F, Cardoso MR. New breakpoints to define resistance to penicillin among pneumococcal pneumonia strains. J. Clin. Invest. 2008; 118 (eletter): 1291-1300 [ Links ]
149. Cardoso MR, Nascimento-Carvalho CM, Ferrero F, Berezin E, Ruvinsky R et al. Penicillin resistant pneumococcus and risk of treatment failure in pneumonia. Arch Dis. Child. 2008;93:221-225 [ Links ]
150. Deeks SL, Palacio R, Ruvinsky R, et al. and the S. pneumoniae Working Group. Risk factors and course of illness among children with invasive penicillin-resistant S. pneumoniae. Pediatrics. 1999;103:409-13 [ Links ]
151. Esparza A, Arbo A. Tratamiento antibiótico de la neumonía adquirida en la comunidad. En: Antibioticoter. en Ped. Arbo A, Santos JI, ed. España: Ed. McGraw Hill-Interamer. 2008; pp. 206-35
152. Lovera D, Arbo A. Treatment of childhood complicated community-acquired pneumonia with amoxicillin/sulbactam. J. Chemotherapy 2005;17:283-8 [ Links ]
153. Hale KA, Isaacs D. Antibiotics in childhood pneumonia. Pediatr. Resp. Rev. 2006; 7:145-151 [ Links ]
154. Ferrari AM, Pírez MC, Martínez A y col. Etiología de la neumonía bacteriana adquirida en la comunidad en niños hospitalizados: Uruguay 1998-2004 Rev. Chil. Infect, 2007;24:40-47
155. Kaplan SL, Hulten KG, González BE, et al. Three-year surveillance of community-acquired S. aureus infections in children. Clin. Infect. Dis. 2005;40:1785-91 [ Links ]
156. Velazquez-Guadarrama N, Martínez-Aguilar G, Arellano-Galindo J, Zuñiga G, Arbo A. Methicillinresistant S. aureus colonization in Mexican children attending day care centres. Clin. Invest. Med. 2009; 32 (1): E57-E63 [ Links ]
157. Ribeiro A, Dias C, Silva-Carvalho MC, et al. First report of infection with community acquired methicillin resistant S. aureus in South America. J. Clin. Microbiol. 2005; 43 (4): 1985-8 [ Links ]
158. Ferrari AM, Pírez MC, Martínez A, Algorta G, Chamorro F, Guana MJ, Zabala C, Giachetto G, Montano A. Etiología de la neumonía bacteriana adquirida en la comunidad en niños hospitalizados: Uruguay 1998-2004 Rev. Chil. Infect.; 2007;24: 40-47 [ Links ]
159. Ma, Galiana A, Pedreira W, Mowszowicz M, Christophersen I, et al. Community Acquired methicillinresistant S. aureus, Uruguay. Emerg. Infect. Dis. 2005 Jun; 11 (6):973-6
160. Paganini H, Verdaguer V, Rodríguez AC et al. Infecciones causadas por S. aureus resistentes a la Meticilina en niños provenientes de la comunidad de la Argentina. Arch. Argent. Pediatr. 2006;104 (4):
161. Paganini H, Della Latta M P, Muller Opet B et al. Estudio multicéntrico sobre las infecciones pediátricas por S. aureus meticilino-resistente provenientes de la comunidad en la Argentina. Arch. Argent. Pediatr. 2008; 106:397-403 [ Links ]
162. Nascimento-Carvalho CM, Lyra TG, Alves NN et al. Resistance to methicillin and other antimicrobials among community-acquired and nosocomial S. aureus strains in a pediatric teaching hospital in Salvador, Northeast Brazil. Microb. Drug Resist. 2008; 14:129-31 [ Links ]
163. González BE, Kaplan SL Severe staphylococcal infections in children. Pediatr. Annals 2008;37:686-91 [ Links ]
164. Fergie J, Purcell K. The treatment of community acquired methicillin-resistant S. aureus infections. Pediatr. Infect. Dis. J. 2008;27:67-68 [ Links ]
165. Pelton SI, Hammerschlag MR. Overcoming current obstacles in the management of bacterial community acquired pneumonia in ambulatory children. Clin. Pediatr. 2005; 44:1-17 [ Links ]
166. Wahington JA, Wilson WR. Erythromycin. A microbial and clinical perspective after 30 years of clinical use. Mayo Clin. Proc. 1985;60:189-203 [ Links ]
167. Esposito S, Bosis S, Faelli N, et al. Role of atypical bacteria and azithromycin therapy for children with recurrent respiratory tract infections. Pediatr. Infect. Dis. J. 2005;24: 438-444 [ Links ]
168. Tiwari, T, Murphy, and J. Moran. Recommended antimicrobial agents for the treatment and postexposure prophylaxis of pertussis: CDC Guidelines. MMWR Recomm Rep 2005; 54 (RR-14): 1-16
169. Bradley JS. Management of community acquired pediatric pneumonia in an era of increasing antibiotic resistance Pediatr. Infect. Dis. J. 2002;21:592-8 [ Links ]
170. Pakistán multicentre amoxicillin short course therapy (MASCOT) pneumonia study group. Clinical efficacy of 3 days versus 5 days of oral amoxicillin for treatment of childhood pneumonia: a multicentre doubleblind trial. Lancet 2002;360:835-41
171. Fine MJ, Stone RA, Lave JR et al. Implementation of an evidencebased guideline to reduce duration of intravenous antibiotic therapy and length of stay for patients hospitalized with community-acquired pneumonia: A randomized controlled trial. Am J. Med. 2003;115:343-51 [ Links ]
172. Dagan R, Syrogiannopoulos G, Ashkenazi S, et al. Parenteraloral switch in the management of paediatric pneumonia. Drugs 1994;47 (suppl 3):43-51
173. Ayieko P, English M. Case management of childhood pneumonia in developing countries. Pediatr. Infect. Dis. J. 2008;26:432-440 [ Links ]
174. Tan JS. Non responses and treatment failures with conventional empiric regimens in patients with community-acquired pneumonia. Infect. Dis. Clin. N. Amer. 2004; 18: 883-897 [ Links ]
175. Niederman MS. Recent advances in communityacquired pneumonia: inpatient and outpatient. Chest 2007; 131:1205-15 [ Links ]
176. Austrian R, Gold J. Pneumococcal bacteremia with special reference to bacteremic pneumococcal pneumonia. Ann. Intern. Med. 1964;60:759-76 [ Links ]
177. Chiou CC, Yu LV. Severe pneumococcal pneumonia: new strategies for management. Curr. Opin. Crit.Care 2006; 12:470-6 [ Links ]
178. Plouffe JF, Martin DR. Reevaluation of the therapy of severe pneumonia caused by S. pneumoniae. Infect. Dis. Clin. N. Amer. 2004; 18:963-74 [ Links ]
179. Panicht H. Respiratory syncytial virus bronchiolitis: supportive care and therapies designed to overcome airway obstruction. Pediatr. Infect. Dis. J. 2003;22:S83-8 [ Links ]
180. Mulholland K. Childhood pneumonia mortality a permanent global emergeney. Lancet 2007 ;370:285-389 [ Links ]
181. Mahalanabis D, Lahiri M, Paul D, et al. Randomized, doubleblind, placebo-controlled clinical trial of the efficacy of treatment with zinc or vitamin A in infants and young children with severe acute lower respiratory infection. Am. J. Clin. Nutr. 2004;79:430-6 [ Links ]
182. Schaefer MK, Shehab N, Cohén AL et al. Adverse events from cough and cold medications in children. Pediatrics 2008;12:783-7 [ Links ]
183. American Academy of Pediatrics. Pertussis. En: Pickering LK ed. 2006 Red Book: Report of the Committee on Infect. Dis. 25th ed. Elk Grove Village, IL: Amer. Acad. of Pediatr. 2006:498-52
184. Soc. Argent. de Pediatr. Comité Nac. de Infectol. Bordetella Pertussis. Libro Azul de Infectol. Pediatr. Buenos Aires: 2007:556-562 [ Links ]
185. Center for Disease Control and Prevention, Prevention among Pertussis, Tetanus and Diphtheria among pregnant and postpartum women and their infants. MMWR, May 30th, 2008 [ Links ]
186. Center for Disease Control and Prevention. Preventing Tetanus, Diphtheria, and Pertussis Among Adults: Use of Tetanus Toxoid, Reduced Diphtheria Toxoid and Acellular Pertussis Vaccine. MMWR, December 15, 2006 / 55(RR17); 1-33 [ Links ]
187. Feigin R, Cherry JD. Tos ferina. En: Feigin R, Cherry JD Tratado de infecciones en pediatría.3° ed. Mc Graw-Hill Interamericana. 2005:1343-1353 [ Links ]
188. Hewlett E. Especies de Bordetella. En: Mandell, G.; Bennet, J.; Dolin, R. Principies and practice of infectious diseases. 5o ed. USA. Ed. Churchill Livingstone, 2005: 2932-2943 [ Links ]
189. Red Book, Report of the Committee on Infectious Diseases, 27th ed., 2006 [ Links ]
190. Plotkin SA, Orentein WA et al: Vaccines, 4th ed. 2004-Eskole, J et al. Pneumococcal Conjúgate Vaccines: 589-624
191. Black S, Shinefield H, Fireman B et al. "Efficacy, safety and immunogenicity of heptavalent pneumococcal conjugate vaccine in children. Pediatr. Infect. Dis. J. 2000; 19:187-95 [ Links ]
192. MMWR 2008; Feb 15, 57 (6): 144-8
193. MMWR "Emergence of antimicrobial resistant serotype 19A S. pneumoniae, Massachusetts (2001-2006). 2007; 56 (41): 1077-1080
194. Choi et al. Emmerg. Infect. Dis. 2008;14:275-281 [ Links ]
195. Huang SS, Platt R, Rifas SL et al. Post-PCV7 changes in colonizing pneumococcal serotypes in 16 Massachusetts communities, 2001 and 2004 Pediatr. 2005 Sep;116 (3):e408-13-Erratum in Pediatr. 2006 Feb; 117(2)593-4 [ Links ]
196. Kaplan SL, Masón EO Jr, Wald ER et al. Decrease of invasive pneumococcal infections in children among 8 children's hospitals in the US after the introduction of the 7-V pneumococcal conjugate vaccine Pediatr. 2004; 113:443-49 [ Links ]
197. Metas E, Brueggerman AD, Enright MC et al. Stability of serotypes during NP carriage of S. pneumoniae J. Clin. Microbiol. 2003;41:386-9225 [ Links ]
198. Zhou F, Kiaw MH, Shefer A et al. Health care utilización for pneumonia in young children after routine pneumococcal conjugate vaccine use in the United States. Arch. Pediatr. Adolesc. Med. 2007;161:1162-8 [ Links ]
199. Grijalva CG, Nwort JP, Arbogast PG et al. Decline in pneumonia admissions after routine childhood immunization with pneumococcal conjugate vaccine in the USA. A time-series analysis. Lancet 2007 ;369(9568): 1179-86 [ Links ]
200. Cameron C, pebody R. Introduction of pneumococcal conjúgate vaccine to the UK childhood immunization program, and changes to the meningitis C and Hib schedules. Europ. Surv. 2006;11(3):060302.4 [ Links ]
201. Káyhty H, Ashman H, Eriksson K, et al. Immunogenicity and tolerability of a heptavalent pneumococcal conjúgate vaccine administered at 3, 5 and 12 months of age. Pediatr. Infect. Dis. J. 2005 Feb ;24:108-14 (www.eurosurveillance.org/ew/2006/060302.asp#4) [ Links ]
202. Lockhart S, Hackell J, Fritzell B. Pneumococcal conjugate vaccines: emerging clinical information and its implications Expert. Rev. Vaccines. 2006 5 (4):553-64 [ Links ]
203. Constenla D. "Evaluating the cost of pneumococcal disease in selected Latin American countries. Rev. Panam. Salud Pública. 2007;22 (4):268-78 [ Links ]
204. Giglio N. Cost effectiveness of universal vaccination for infants in Argentina. ICAAC meeting 2008, Wash. DC Poster 2169 [ Links ]
205. World Health Organization. Pneumococcal conjugate vaccine for childhood immunization: WHO position paper. Weekly Epidemiol. Rep. 2007;12:93-104 [ Links ]
206. WHO (2005) Recommendations for the production and control of pneumococcal conjugate vaccines. WHO Technical Report Series No. 927
207. Henckaerts I, Goldblatt D, Ashton L, Poolman J. Critical differencies between pneumococcal polysaccharide enzymelinked assays with and without 22F inhibition at low antibody concentration in pediatric sera. Clin. Vaccine Immunol. 2006 Mar; 13 (3):356-60 [ Links ]
208. Iwane M, Edwards K, Szilagyi G, et al. Populationbased surveillance for hospitalizadons associated with Respiratory Syncytial Virus, Influenza Virus and Parainfluenza Viruses among young children. Pediatrics 2004; 113:1758-1764 [ Links ]
209. Prevention and Control of Influenza. Recommendations of the Advisory Committee on Immunization Practices (ACIP) MMWR, Vol. 56/ Early Release. June 29, 2007 [ Links ]
210. Red Book: Report of the Committe on Infectious Diseases, American Academy of Pediatrics, 27th ed. 2006 [ Links ]
211. Poland G. Vaccines against Avian Influenza A race against time. N. Engl. J. Med. 2006;354:1411-1413 [ Links ]
212. Izurieta H, Thompson W, Kramarz P, et al. Influenza and rates of hospitalization for respiratory disease among infants and young children. N. Engl. J. Med. 2000;342: 232-239 [ Links ]
213. Jefferson T, Smith S, Demicheli V et al. Assessment of the efficacy and effectiveness of influenza vaccines in healthy children: systematic review. Lancet 2005;365:773-80 [ Links ]
214. O'Brien M, Uyeki T, Shay D, et al. Incidence on outpatient visits and hospitalizations related to influenza in infants and young children. Pediatrics 2004;113:585-593 [ Links ]
215. Treanor J, Campbell J, Zangwill K, et al. Safety and inmunogenicity of an inactivated Subvirion Influenza A (H5N1) vaccine. N. Engl. J. Med. 2006 ;354:1343-1351 [ Links ]
216. Ruvinsky R S. pneumoniae: an old pathogen causing the emergence of new epidemiologic problems in Pediatrics. Arch Arg Pediatr. 2001 ;99(2): 101-4 [ Links ]
217. Tregnaghi M, Ceballos A, Ruttimann R, Ussher J, Tregnaghi P, Peters P, Hausdorff WP Active epidemiologic surveillance of pneumonia and invasive pneumococcal disease in ambulatory and hospitalized infants in Córdoba, Argentina. Pediatr. Infect. Dis. J. 2006;25(4):370-2 [ Links ]
218. Gentile A, Bakir J; Fernandez, MI; BialorusL, Terluk, M, Gil C, Regueira, M, Gentile,F, García S. Carga de neumonia consolidante en niños < de 5 años en el partido de pilar. 6° Congr. Argent. de Infectol. Pediatr. 16-19 de abril 2008. Soc. Argent. de Pediatría Bs As, Argentina [ Links ]
219. Lagos R, Muñoz A, Espinosa A, MoeneK, Hausdorff W, Ruttimann R et al. Population-Based surveillance for suspected and radiological confirmed CAP in children 1-35 month of age in 6 municipalities of metropolitan región Chile. 5th Internat. Sympos. on Pneumococci and Pneumococcal Diseases. Program and abstraes Book 2006: 218 [ Links ]
220. The burden of pneumococcal disease and costeffectiveness of a pneumococcal vaccine in Latin America and the Caribbean: A review of the evidence and a preliminary analysis (http://sabin.org/programs/pneumococcal/pneumostudy.html) [ Links ]
221. de Andrade AL, de Andrade JG, Martelli CM, et al. Effectiveness of Hib conjúgate vaccine on childhood pneumonia: a case-control study in Brazil. Int. J. Epidemiol. 2004Feb;33(1): 173-81 [ Links ]
222. De Andrade Al. Estudio LEAP-Simposio Sobre Nuevas Vacunas. Sabin Institute and the Pan American Health Organization Diciembre 1 y 2, 2009: Lima-Perú. [ Links ]
223. Giglio N, Micone P, Cañe A, Gentile A. Cost Effectiveness of CRM-based 7 valent Pneumococcal conjugated vaccine (PCV-7) in Argentina. Vaccine (2010), doi: 10.1016/j.vaccine.2009.12.070 [ Links ]
224. Constenla D Economic impact of Pneumococcal conjúgate vaccination in Brazil, Chile and Uruguay. Rev. Panam. Salud Pública. 2008 Aug; 24(2): 101-12 [ Links ]
225. Asturias EJ, Soto M, Menendez R, et al. Meningitis and pneumonia in Guatemalan children: the importance of H. influenzae type b and S. pneumoniae. Rev. Panamer. de Salud Pública 2003; 14 (6):377-84 [ Links ]
226. Vigilancia epidemiológica centinela de H. influenzae y S. pneumoniae en < de 5 años en el Perú. Rev. Per. Med. Exp. Salud Pública, Jul./Set. 2003; 20 (3): 150-55. [ Links ]
227. Lagos R; Muñoz A; Valenzuela M T; Heitmann I; Levine M. Population-based surveillance for hospitalized and ambulatory pediatric invasive pneumococcal disease in Santiago, Chile. The Pediatr. Infect. Dis. J. 2002;21(12): 1115-23 [ Links ]
228. Bakir J, Gentile A, López Holtmann, Procopio A y Vázquez M. Perfil epidemiológico de las infecciones invasivas por S. pneumoniae. Arch. Argent. Pediatr. 2001 ;99 (2): 111-18
229. Hortal M, Ruvinsky R and Grupo Sireva-Vigía et al. Impacto de S. pneumoniae en las neumonías del niño latinoamericano. Rev. Panam. Salud Pública [online]. 2000;8 (3) - cited 2009-07- 28, pp. 185-95 [ Links ]
230. Griebsch I, Coast J, Brown J. Quality-adjusted lifeyears lack quality in pediatric care: a critical review of published costutility studies in child health; a critical review. Pediatrics 2005 May; 115(5): e600-14 [ Links ]
231. Keren R, Pati S, Feudtner C. The generation gap: differences between children and adults pertinent to economic evaluations of health interventions. Pharmacoeconomics 2004;22:71-81 [ Links ]
232. Eiser C, Morse R. Quality-of-life measures in chronic diseases of childhood. Health Technol Assess. 2001;5:1-157 [ Links ]
233. Shaller D. Implementing and using quality measures for children's health care: perspectives on the state of the practice. Pediatrics 2004 Jan; 113(1 Pt2): 217-27 [ Links ]
234. Prosser LA, Ray GT, O'Brien M Preferences and willingness to pay for health states prevented by pneumococcal conjugate vaccine. Pediatr. 2004 Feb; 113(2):283-90 [ Links ]
235. Giglio N, Micone P, Venosa M, Carosella M, Gentile A, Cañé A. Preferences in Argentine population for Health States Prevented by Pneumococcal Conjugate Vaccine-6th Congr. on Vaccines, Immunization and immunotherapy Milán 2008 [ Links ]
236. Sinha A, Constenla D, Valencia JE, O'Loughlin R, Gómez E, de la Hoz F, Valenzuela MT, de Quadros CA, Cost effectiveness of pneumococcal conjúgate vaccination in Latin America and the Caribbean: a regional analysis. Rev. Panam. Salud Pública. 2008 Nov;24(5):304-313 [ Links ]
237. Ray Pharmacoeconomics of Pneumococcal Conjugate Vaccines-Pneumococcal Vaccines Ed. Siber, Klugman and Makela. ASM press WDC ISBN 978-1-5581-408-3 [ Links ]














