La obesidad y el sobrepeso son problemas significativos de salud pública, relacionados con una alimentación poco saludable y la falta de actividad física. En las Américas, la prevalencia del sobrepeso es casi el doble que el promedio mundial, con un 80,7% de los adolescentes que no realiza suficiente actividad física1.
La diabetes mellitus tipo 2 (DM2) es una enfermedad grave que puede causar complicaciones como retinopatía, insuficiencia renal y enfermedades cardiovasculares. Su control deficiente aumenta el riesgo de mortalidad prematura. Entre 2000 y 2016, la mortalidad prematura por diabetes aumentó un 5%, y en 2019 fue la sexta causa de muerte en las Américas, con aproximadamente 244.084 fallecimientos directamente atribuibles a la enfermedad1. La diabetes también representó la segunda causa de Años de Vida Ajustados por Discapacidad (AVAD), reflejando las complicaciones crónicas que enfrentan los pacientes a lo largo de su vida (1). El Ministerio de Salud del Estado Plurinacional de Bolivia, informo que, en los últimos cinco años, el registro de DM2 se incrementó en un 30 %, de 64.136 en 2010 a 89.916 en 2015. Se estima que para el 2020 la cifra de pacientes con esta enfermedad llegue a 180 mil2.
La DM2 es uno de los trastornos metabólicos más comunes en el mundo. Su desarrollo se debe principalmente a la combinación de dos factores clave: la secreción defectuosa de insulina por las células β del páncreas y la incapacidad de los tejidos sensibles a la insulina para responder adecuadamente a esta hormona3.
La liberación y la acción de la insulina deben ajustarse de manera precisa a la demanda metabólica del organismo. Por lo tanto, es esencial que los mecanismos moleculares implicados en la síntesis y liberación de insulina, así como la respuesta de los tejidos a la insulina, estén estrictamente regulados. Cualquier defecto en estos mecanismos puede ocasionar un desequilibrio metabólico que contribuye a la patogenia de la DM24.
La DM2 puede causar disnatremias a través de varios mecanismos 5,6. La glucosa actúa como una sustancia osmóticamente activa y, por lo tanto, la hiperglucemia incrementa la osmolalidad sérica. Esto provoca el movimiento de agua fuera de las células, resultando en una reducción de los niveles séricos de sodio ([Na+]) por dilución. Los electrolitos sodio y potasio son esenciales para diversas funciones celulares, y su equilibrio entre los espacios intracelular y extracelular es crucial para la homeostasis del organismo7.
La distribución del potasio entre los líquidos intracelulares y extracelulares está regulada en gran medida por la bomba ATPasa (Na+-K+), que introduce activamente potasio en la célula a cambio de sodio7. El potasio es un electrolito indispensable para el organismo, ya que participa en la contracción de los músculos esqueléticos, lisos y cardíacos, así como en la secreción de aldosterona, la función renal, el metabolismo de los hidratos de carbono y la síntesis proteica. La insulina, en condiciones de ayuno, ayuda a mantener los niveles plasmáticos de potasio dentro de rangos normales, actuando como regulador de la concentración de potasio en las células. Cuando los niveles de insulina disminuyen, la concentración plasmática de potasio ([K+]) se eleva, lo que puede conducir a una hipercalemia significativa. Además, el potasio se considera un estimulador conocido de la secreción de insulina en un organismo sano8.
Por otro lado, niveles elevados de ácido úrico (UA/AU) están asociados con una mayor incidencia de eventos cardiovasculares, siendo común la hiperuricemia en personas con obesidad e hipertensión. El mecanismo fisiopatológico que aumenta la concentración sérica de UA en la hipertensión esencial se relaciona con alteraciones en la excreción renal de ácido úrico9. En este contexto, una excreción renal comprometida de ácido úrico contribuye principalmente a la hiperuricemia, aunque la sobreproducción de ácido úrico también juega un papel en individuos obesos10.
En la actualidad, se han desarrollado productos naturales para la prevención y el tratamiento de patologías no transmisibles, entre los cuales destacan los alimentos nutracéuticos. Estos productos, que poseen un alto valor nutricional y medicinal, se utilizan para prevenir y tratar desórdenes metabólicos, y suelen minimizar los efectos secundarios de los tratamientos farmacológicos convencionales.
En la región altiplánica de Bolivia, se cultivan cereales como el amaranto (Amaranthus caudatus), la quinua (Chenopodium quinoa) y el tarwi (Lupinus mutabilis). Estos cereales no solo son ricos en macronutrientes como proteínas, carbohidratos, ácidos grasos y fibra, sino que también contienen minerales y vitaminas que aportan un alto valor nutricional a la dieta11,12. Su consumo contribuye a la prevención del sobrepeso y, por ende, de las enfermedades cardiovasculares, además de apoyar el tratamiento farmacológico de la diabetes tipo 2 e hipertensión.
El presente trabajo tiene como objetivo evaluar si un producto nutracéutico basado en amaranto, quinua y tarwi (AQT) coadyuva en el tratamiento de la DM2, el sobrepeso y la hipertensión, mejorando el estado de salud de los pacientes. Se busca determinar si el consumo de este producto regula y mantiene los niveles normales de [Na+], [K+] y ácido úrico en los participantes.
Materiales y métodos
El presente trabajo corresponde a un ensayo clínico preliminar, controlado, cuantitativo, prospectivo, correlacional deductivo, llevado a cabo en paralelo a un proyecto de investigación que evalúa las propiedades medicinales de productos nutracéuticos naturales como tratamiento para la DM2 y el sobrepeso. Este estudio se realizó en la ciudad de La Paz y El Alto durante la fase 2 de la gestión 2019, específicamente en el área de Farmacología del Instituto de Investigaciones Fármaco-Bioquímicas (IIFB) de la Facultad de Ciencias Farmacéuticas y Bioquímicas de la Universidad Mayor de San Andrés, en colaboración con la Agencia Sueca de Cooperación Internacional para el Desarrollo (ASDI).
Selección de grupos de estudio
El estudio contó con la participación de 120 voluntarios de ambos sexos, con edades entre 20 y 80 años, quienes acudieron de manera ambulatoria al área de Farmacología del IIFB. Se empleó un muestreo por conveniencia, no probabilístico y no aleatorio, seleccionando a aquellos individuos que cumplían con los criterios de inclusión y que, posteriormente, firmaron el consentimiento informado. El estudio excluyó a personas que tenían consumo excesivo de alcohol, desórdenes alimenticios, estaban tomando suplementos alimenticios, tenían complicaciones graves, no aceptaron participar o tenían menos de 20 años, para asegurar la seguridad y la precisión de los resultados.
Una vez seleccionada la muestra, los participantes fueron clasificados en diferentes grupos de estudio:
- Grupo 1: Individuos con diabetes mellitus tipo 2 (Glucemia > 120mg/dL; HbAlc > 6,5 %).
- Grupo 2: Individuos con Sobrepeso (IMC > 25 Kg/m2).
- Grupo 3: Individuos con hipertensión arterial (Sistólica >130 HHmg y diastólica >85 HHmg).
- Grupo 4: Control (sin consumo del producto AQT, sin diabetes mellitus tipo 2, sin hipertensión arterial y con un IMC < 25 Kg/m2) (Figura 1).
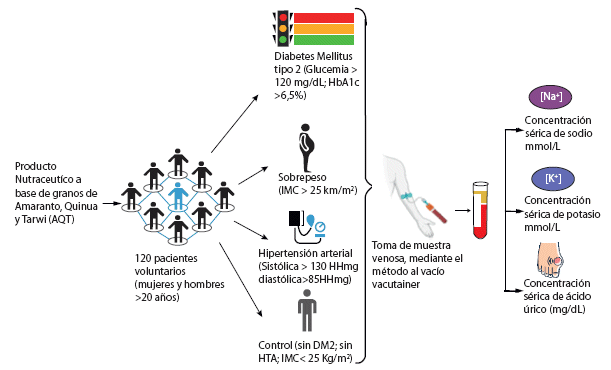
Figura 1. Representacion del procedimiento metodológico implementado en el ensayo clínico preliminar, realizado en paralelo al proyecto de investigación sobre las propiedades medicinales de productos nutracéuticos naturales como tratamiento para la diabetes y el sobrepeso en La Paz y El Alto durante la fase 2 de la gestión 2019. La figura muestra las etapas clave del estudio, que incluyen la selección de voluntarios, la extracción de muestras de sangre mediante venopunción, el manejo de las muestras (codificación y centrifugación) y a continuación procesos de análisis de biomarcadores.
Toma de muestra sanguínea
La extracción de muestras se llevó a cabo mediante la técnica de venopunción, utilizando tubos de vacío Vacutainer, con el objetivo de minimizar la contracción muscular y evitar el uso prolongado del torniquete, lo que podría alterar los biomarcadores analizados. Las muestras fueron recolectadas después de tres meses de consumo del producto AQT y se codificaron antes de ser centrifugadas de inmediato a 3500 rpm durante 10 minutos para obtener el suero (Figura 1).
La cuantificación de los biomarcadores analizados, que incluye los niveles de sodio, potasio y ácido úrico en sangre, se realizó de acuerdo con el procedimiento especificado en el kit comercial de Stanbio Laboratory. Se llevó a cabo un control de calidad interno (gráfica de Levey-Jennings +/- 2DS) y externo. Se conoce que los reactivos de la línea de Stanbio Laboratory son fabricados bajo las normas reguladas por la FDA (Administración de Alimentos y Medicamentos de EE.UU.) y cGMP (buenas prácticas de manufactura), son confiables, fáciles de usar y compatibles con analizadores. Ofrecen ensayos validados para diabetes y sepsis25.
Resultados
Los niveles de sodio sérico en pacientes con sobrepeso después del consumo del producto AQT, aumentaron de 138,0 (control) a 146,1 mmol/L (IMC>25+p), por otro lado, los niveles de ácido úrico se elevaron de 3,6 (control) a 5,0 mg/dL (IMC>25+p), siendo estas diferencias no significativas (Figura 2. A, C). En pacientes diabéticos (DM2), la concentración de ácido úrico mostró una diferencia significativa en comparación con el grupo control (*p<0,05). Después del consumo de AQT se observó un aumento de los niveles de ácido úrico de 3,6 (control) a 4,6 mg/dL (DM2+p), aunque esta diferencia no alcanzó significancia estadística (Figura 2. A, C).
Por otro lado, en pacientes con DM2, se registró una disminución en los niveles de potasio y ácido úrico en comparación con el grupo que no consumió AQT, aunque se observó un ligero aumento respecto al grupo control: los niveles de potasio pasaron de 4,6 (DM2+p), a 5,3 mmol/L (DM2), y los niveles de ácido úrico de 4,6 (DM2+p) a 5,5 mg/dL (DM2) (Figura 2. B, C). Sin embargo, los niveles de sodio (135,0 - 155,0 mmol/L), potasio (3,6 - 5,5 mmol/L) y ácido úrico (2,4 - 7,0 mg/dL) se mantuvieron dentro de los rangos normales en los tres grupos estudiados.
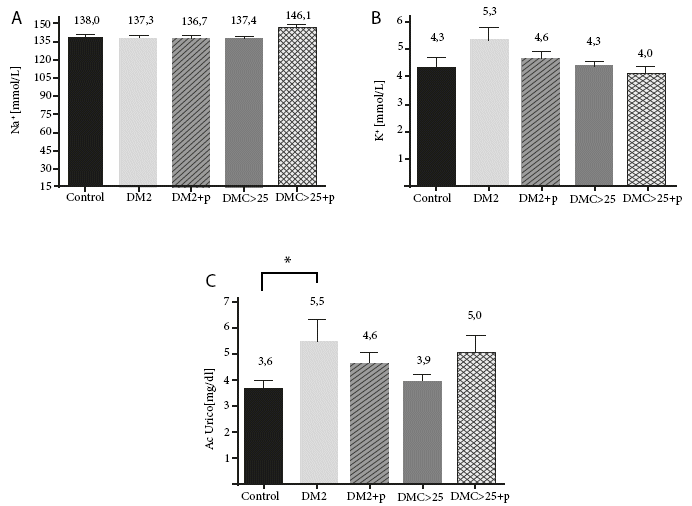
Figura 2. A). Concentración de sodio sérico en pacientes diabéticos y con sobrepeso; B) concentración de potasio en pacientes con diabetes mellitus tipo 2 y sobrepeso; C). Concentración de ácido úrico en pacientes diabéticos y con sobrepeso. Después de tres meses de consumo del producto AQT. +p (consumo del producto), diabetes mellitus tipo 2 (DM2) y sobrepeso (IMC> 25). Significancia estadística * p< 0,05.
Cuantificación de niveles séricos de sodio, potasio y ácido úrico en pacientes diabéticos y sobrepeso con hipertensión, tras el consumo del producto AQT
Después de tres meses de consumo de AQT, se observó un aumento en los niveles séricos de sodio en pacientes con DM2 e hipertensos, que pasaron de 138,0 (control) a 143,0 mmol/L(DM2+H+p) (Figura 2.A). Por otro lado, los pacientes con sobrepeso también experimentaron un ligero incremento, con niveles que variaron de 138,0 (control); 137,4(IMC>25) y 138,5 mmol/L(IMC>25+H+p). A pesar de estas variaciones, las diferencias no fueron estadísticamente significativas.
Con respecto a los niveles séricos de potasio, después del consumo del producto AQT, los niveles séricos en pacientes diabéticos se compararon a los del grupo control. Sin embargo, se observó una disminución en comparación con los grupos de pacientes DM2 y DM2 con hipertensión que no consumieron el producto, con niveles de potasio reduciéndose de 5,3 (DM2) y 4,7 (DM2+H) a 4,2 mmol/L (DM2+H+p), respectivamente (Figura 2.C). Asimismo, en pacientes con sobrepeso e hipertensión que consumieron AQT, los niveles de potasio sérico fueron notablemente más bajos que en los grupos sin consumo, disminuyendo de 4,3(IMC>25) y 4,0 (IMC>25+H) a 3,2 mmol/L (IMC>25+H+p) (Figura 3.D).
En cuanto a los niveles séricos de ácido úrico, se evidenció un incremento en pacientes con DM2 en comparación con los dos grupos, de control y aquellos que no consumieron AQT, pasando de 3,6 (DM2) y 4,6 (DM2+H) a 5,1 mg/dL (DM2+H+p) (Figura 2. E). En contraste, los pacientes con sobrepeso mostraron una disminución en sus niveles de ácido úrico en comparación a los grupos control y al grupo que no consumió el producto, disminuyendo de 3,6 (control); 3,9 (IMC>25) y 5,3 (IMC>25+H) a 3,2 mg/dL (IMC>25+H+p) (Figura 3.F).
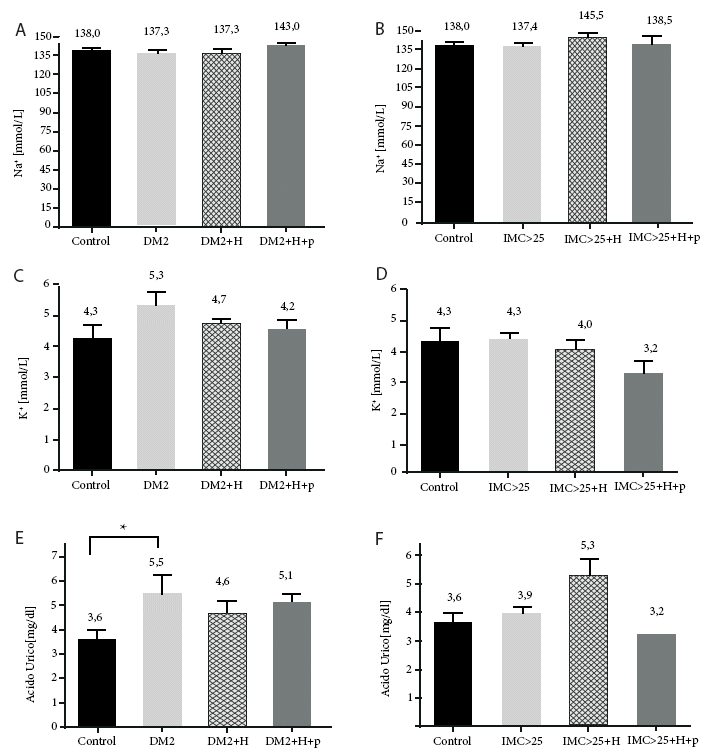
Figura 3. A) Concentración de sodio sérico de pacientes con diabetes tipo 2 y pacientes con diabetes e hipertensión; B) Concentración sérica de sodio en pacientes con sobrepeso e hipertensión; C) Niveles de potasio en sangre en pacientes con diabetes y diabetes con hipertensión; D) Concentración sérica de potasio en pacientes con sobrepeso e hipertensión; E) Niveles de ácido úrico en sangre en pacientes diabéticos y diabéticos con hipertensión; F) Concentración sérica de ácido úrico en pacientes con sobrepeso y sobrepeso e hipertensión. Los valores fueron medidos después de tres meses de consumo del producto AQT. +p (consumo del producto), diabetes mellitus tipo 2 (DM2), diabéticos e hipertensos (DM2+H), sobrepeso (IMC> 25) y sobrepeso e hipertensos (IMC> 25+H). Significancia estadística * p< 0,05.
Niveles sanguíneos de sodio, potasio y ácido úrico en pacientes diabéticos y con sobrepeso sin y con resistencia a la insulina, después del consumo del producto AQT.
En pacientes con DM2, los niveles de sodio sérico se incrementaron de 138,0 (control); 139,0 (DM2 Ins<10); 135,6 (DM2 Ins>10) a 141,1 mmol/l (DM2 Ins>10+p) (Figura 4. A) y en pacientes con sobrepeso se observó valores de 138,0 (control); 140,2 (IMC>25 Ins<10); 132,9 (IMC>25 Ins>10) a 141,5 mmol/l (IMC>25 Ins>10+p) (Figura 4. B).
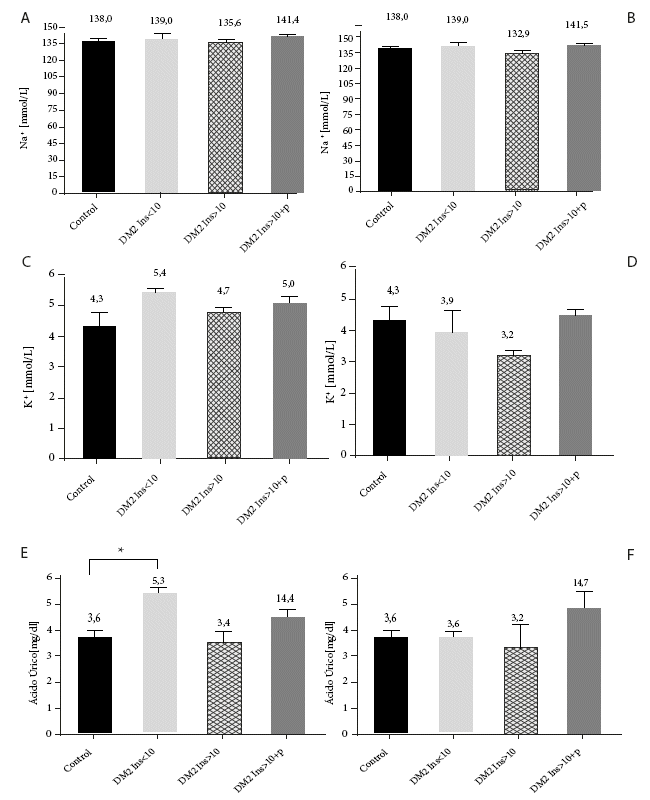
Figura 4. A) Concentración de sodio sérico de pacientes con DM2, sin resistencia a la insulina (RI) y con RI; B) Concentración sérica de sodio en pacientes con sobrepeso sin RI y con RI; C) Niveles de potasio en sangre en pacientes con diabetes, sin RI y con RI; D) Concentración sérica de potasio en pacientes con sobrepeso, sin RI y con RI; E) Niveles de ácido úrico en sangre en pacientes diabéticos, sin RI y con RI; F) Concentración sérica de ácido úrico en pacientes con sobrepeso, sin RI y con RI. Los valores fueron medidos después de tres meses de consumo del producto AQT; Diabetes tipo 2 sin resistencia a la insulina (DM2 Ins<10) y con resistencia a la insulina (DM2 Ins > 10) y diabéticos e hipertensos (DM2+H); Sobrepeso sin resistencia a la insulina (IMC>25 Ins< 10); Sobrepeso con resistencia a la insulina (IMC>25 Ins>10); +p (consumo del producto).
En cuanto a los niveles séricos de potasio, en pacientes diabéticos con resistencia a la insulina, se observó un aumento en comparación con los grupos de control y aquellos con DM2 sin consumo, pasando de 4,3 (control); 4,7 (DM2 Ins>10) a 5,0 mmol/l (DM2 Ins>10+p). En pacientes con sobrepeso, los niveles de potasio también mostraron un aumento en comparación con los grupos sin consumo, con cifras que pasaron de 4,3 (control); 3,9 (IMC>25<Ins10) y 3,2 (IMC>25>Ins10) a 4,4 mmol/l (IMC>25>Ins10+p) (Figura 4. D).
Por otro lado, los niveles de ácido úrico en pacientes con DM2 y resistencia a la insulina, después del consumo del producto
AQT, evidenció un aumento en comparación con los grupos control y en aquellos sin consumo, pasando de 3,6 (control); 3,2 (IMC>25>Ins10) a 4,7 mg/dl (IMC>25>Ins10+p) (Figura 4. E). Por el contrario, en pacientes con DM2 y resistencia a la insulina, se observó una disminución en comparación con el grupo de diabéticos sin resistencia, de 4,4 (DM2 Ins>10+p) a 5,3 mg/dl (DM2 Ins<10), junto con un aumento respecto a los grupos sin consumo (control y DM2 Ins> 10), que pasó de 3,6; 3,4 a 4,4 mg/dl, respectivamente (Figura 4. F).
Discusión
El ligero incremento en los niveles de sodio sérico en pacientes con sobrepeso y diabetes que consumieron AQT podría atribuirse a la retención de sodio inducida por la resistencia a la insulina asociada a la obesidad13. Esta tendencia al aumento de sodio sérico coincidiría con reportes que indican que la obesidad está relacionada con una mayor reabsorción tubular de sodio, mediada por hiperinsulinemia e hiperaldosteronismo8. Estudios previos han demostrado que la resistencia a la insulina se asocia con un incremento en la reabsorción tubular de sodio14. Además, el efecto más pronunciado en el grupo con sobrepeso e hipertensión respalda la interacción entre obesidad, presión arterial elevada y retención de sodio, tal como se ha descrito en investigaciones anteriores15.
La DM2 puede causar disnatremias por varios mecanismos, siendo la hiperglucemia uno de ellos, ya que esta aumenta la osmolalidad sérica y puede llevar a una disminución de los niveles de sodio en sangre debido a la dilución. Por otro lado, la cetoacidosis diabética conlleva una pérdida renal de sodio y otros electrolitos13. En pacientes diabéticos no controlados, la concentración sérica de sodio puede variar, reflejando el equilibrio entre la hiperglucemia y la diuresis osmótica.
El presente estudio evidenció que, después de tres meses de consumo del producto AQT, los niveles séricos de sodio mostraron una ligera disminución en pacientes con DM2 y sobrepeso, en comparación con un grupo control. Sin embargo, se observó que las semillas de amaranto, quinoa y tarwi, que son componentes de la dieta andina, podrían contribuir a mantener los niveles de sodio dentro de los rangos normales, incluso en situaciones de resistencia a la insulina.
Además, el consumo de AQT posiblemente mejoró la acción de la insulina y la excreción de potasio. El producto natural AQT a base de semillas de amaranto, quinoa y tarwi, pueden actuar como inhibidores de la enzima convertidora de angiotensina (ECA), previniendo así el aumento excesivo de sodio en pacientes con sobrepeso e hipertensión, así como la hiperpotasemia en diabéticos16,17.
La ligera disminución en los niveles de potasio sérico en pacientes diabéticos que consumieron AQT coincide con reportes que sugieren que la deficiencia de insulina altera la secreción renal de potasio, predisponiendo a la hipopotasemia18. Esta disminución también podría asociarse a una mejoría en la función de las células beta pancreáticas y una mayor secreción de insulina. Investigaciones previas indican que la deficiencia de insulina se relaciona con una menor excreción de potasio y con un aumento en el riesgo de hiperpotasemia19.
En el caso de pacientes con sobrepeso e hipertensión, la reducción en los niveles de potasio sérico bajo el consumo de AQT se alinea con hallazgos que indican que la hiperinsulinemia asociada a la obesidad favorece la entrada de potasio en las células, disminuyendo así sus niveles plasmáticos18. Sin embargo, el efecto antihipertensivo de los péptidos derivados de cereales andinos con actividad inhibidora de la ECA en AQT podría explicar la prevención de la hiperpotasemia en estos grupos de riesgo16,17.
Un estudio retrospectivo evidenció que el ácido úrico se correlaciona positivamente con la hiperinsulinemia y la resistencia a la insulina en pacientes con prediabetes. Este hallazgo ha sido identificado como un posible factor de riesgo para estas condiciones20. Además, se ha demostrado una correlación positiva entre los niveles elevados de ácido úrico sérico y el riesgo de hiperinsulinemia, así como entre el ácido úrico y el riesgo de resistencia a la insulina en la mayoría de los individuos, excepto en mujeres posmenopáusicas21.
La hiperuricemia está asociada con marcadores del síndrome metabólico, como dislipidemia, hipertensión arterial, obesidad central e intolerancia a la glucosa, todos factores de riesgo para enfermedades cardiovasculares22. Se han identificado nutracéuticos que podrían ser útiles en el tratamiento de patologías como la DM2 y la hipertensión arterial. Nuestro estudio indicó que después de tres meses de consumo del producto AQT, los niveles de ácido úrico en sangre no mostraron un incremento significativo en comparación con el grupo control, incluso cuando se sabe que la hiperuricemia se relaciona con un mayor riesgo de desarrollar hipertensión23.
Los mecanismos que vinculan la hiperuricemia con la hipertensión involucran el óxido nítrico y el sistema renina- angiotensina-aldosterona (RAAS). El ácido úrico puede causar disfunción endotelial y estimular la proliferación de células musculares lisas vasculares, además de activar directamente el RAAS24. En pacientes con DM2, se observó una disminución en los niveles de ácido úrico después del consumo del producto nutracéutico AQT en comparación con el grupo sin consumo, mientras que en pacientes obesos se registró un aumento de 4,1 a 5,0 mg/dL.
Conclusión
El producto AQT, compuesto por semillas andinas como amaranto, quinoa y tarwi, presenta un efecto beneficioso sobre los niveles séricos de sodio, potasio y ácido úrico en pacientes con alteraciones metabólicas como diabetes mellitus tipo 2, sobrepeso e hipertensión, Específicamente, el producto AQT ayudaría a prevenir desequilibrios como hiponatremia en pacientes diabéticos, hiperpotasemia en individuos con sobrepeso e hipertensión, e hiperuricemia en pacientes con sobrepeso. Estos efectos se atribuyen a los péptidos bioactivos derivados de las semillas andinas con propiedades inhibitorias de la enzima convertidora de angiotensina. Sin embargo, los cambios observados en los electrolitos séricos con el consumo de AQT fueron leves y no estadísticamente significativos en la mayoría de los grupos estudiados. Además, los niveles se mantuvieron dentro de rangos de referencia normales. Por tanto, el producto AQT muestra un potencial prometedor para el manejo de desequilibrios electrolíticos en diversas enfermedades metabólicas. Sin embargo, se requiere más evidencia científica, incrementando la muestra para respaldar su aplicación clínica. Cabe destacar que el presente estudio es una investigación preliminar para futuros estudios.















