Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta Médica Boliviana
versión impresa ISSN 1012-2966versión On-line ISSN 2227-3662
Gac Med Bol v.28 n.1 Cochabamba 2005
CASO CLINICO
NECROSIS EPIDERMICA TOXICA SINDROME DE LYELL-STEVENS JOHNSON
*Oscar Niño de Guzmán Peña, **lvone Gómez Valdez, ***Oscar Niño de Guzmán Luizaga.
* Jefe de Servicio del Dpto. Ginecología y Obstetricia Hospital Obrero No. 2.
** Residente Rll de Pediatría del Hospital Obrero No. 2.
*** Médico Interno del Hospital Obrero No. 2.
INTRODUCCION
Se presenta el caso médico de una paciente con un cuadro clínico único en nuestro servicio en mas de 15 años de uso del Diclofenaco Sódico como coadyuvante al Clorhidrato d-propoxifeno terapirol para potencializar la analgesia en las pacientes postoperadas.
El síndrome de Lyell o Necrosis epidérmica toxica (NET) es una enfermedad exfoliativa de la piel que puede afectar a toda la superficie cutánea corporal y a diferentes mucosas. El 80 % de los casos son producidos por un fármaco de origen antinflamatorio no esteroideo. La exfoliación se produce por despegamiento de la unión dermoepidérmica, que simula una quemadura dérmica superficial.
CASO CLINICO
Mujer de 28 años de edad, con el antecedente de cesárea por desproporción cefalo-pélvica, con un RN de 3200 gr. con APGAR de 8 al minuto y de 10 a los 5 minutos.
Sus antecedentes gineco obstétricos: realizó su control pre-natal en 6 oportunidades sin ningún antecedente patológico ni alérgico; Gl, P0, C0, A0; sin datos familiares y personales relacionados con su cuadro patológico, sus exámenes de laboratorio y gabinete dentro de parámetros normales en el embarazo.
Inicia trabajo de parto 2 días antes a su cuadro dérmico, con un embarazo de 40 semanas, sus datos de admisión fueron: presentación cefálica alta, posición dorso Izquierda, y situación longitudinal, dilatación de 4 cm. y un borramiento del 60 %, una variedad de posición de OIAI, bolsas de las aguas íntegras y pelvis androide. Con estos resultados se indica cesárea segmentaría. En el post operatorio se indicó líquidos endovenosos, gentamicina 160 mg./día y Ampicilina 2 gr./día, Analgésicos como d-propoxifeno terapirol y diclofenaco 75 gr. IM cada 8 hrs.
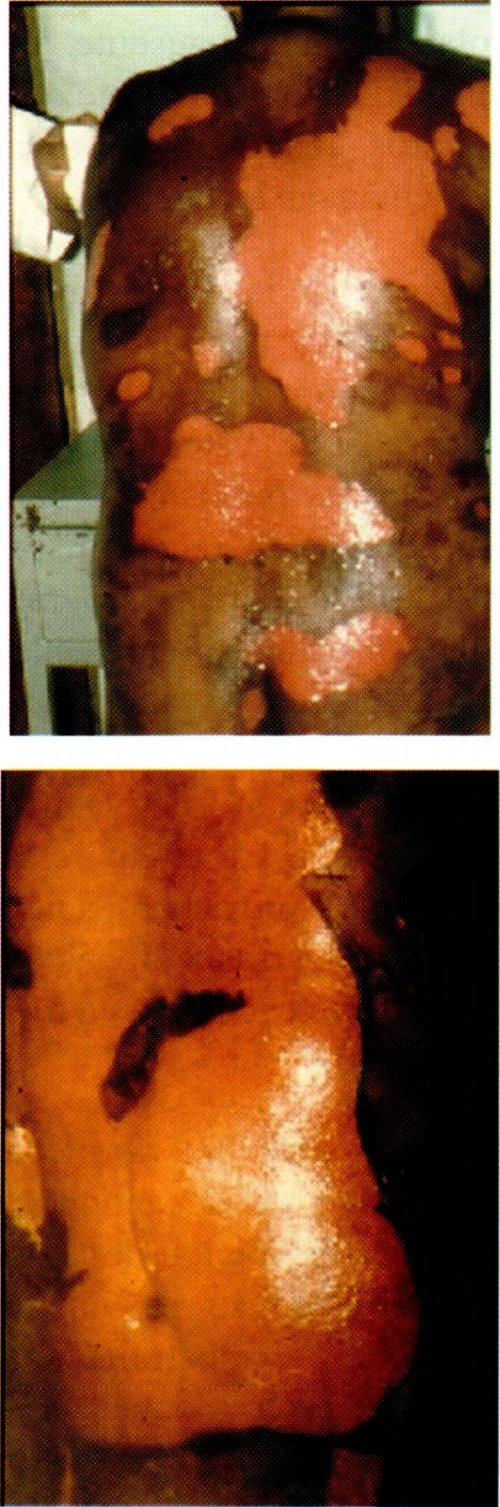
El segundo día presentó cuadro febril, rash acompañado de ardor a nivel cutáneo, de inicio en el cuello y la espalda acompañado de lesiones maculopapulares, a las 72 hrs., se presentaron ampollas que fueron tomando el tórax y abdomen anterior y posterior, miembros superiores, glúteos y parte superior de miembros inferiores simulando una quemadura superficial, no presentó lesiones de las mucosas.
Fue tratada por el departamento de cirugía plástica y dermatología con clorfeniramina vía oral cada 8 hrs., fluido-terapia de mas o menos de 5.000cc para 24 hrs. mas líquidos a tolerancia manteniendo una diuresis entre 1000 a 1500 cc./día, suspendiendo todos los antinflamatorios y alimento con saborizantes, colorantes, enlatados, etc. continuando con la antibiótico-terapia ya establecida; curaciones diarias, teniendo una evolución favorable; luego de 15 días, fue dada de alta médica
La histopatológica de la biopsia de piel mostró: edema de la dermis papilar, dilatación vascular, edema endotelial e infiltrado mononuclear perivascular. La dermis reticular normal y separación dermoepidérmica y necrosis de queratinocitos.
COMENTARIO
El síndrome de Lyell o necrólisis epidérmica tóxica (NET) es una enfermedad exfoliativa de la piel que puede afectar la totalidad de la superficie cutánea corporal y a diferentes mucosas. En el 80% de los casos se identifica un fármaco como posible causa, particularmente antiinflamatorios no esteroides, antibióticos y anticonvulsionantes. La exfoliación se produce por despegamiento de la unión dermoepidérmica, recordando a una quemadura de tipo dérmica superficial. Se trata de una enfermedad de carácter sistémico que se asocia con una morbimortalidad significativa. Estos enfermos presentan numerosas complicaciones, en relación con el desarrollo de sepsis, desnutrición, insuficiencia respiratoria y síndrome de disfunción multiorgánica. Estos problemas son similares a los encontrados en pacientes con quemaduras extensas1,3,6,12.
La NET afecta a más del 30% de la superficie corporal, se asocia con una mortalidad significativa (25-80%) y requiere tratamiento en un ambiente de cuidados intensivos15,21.
La NET presenta una prevalencia de 1-3 casos por millón de habitantes/año11,15. Aunque puede ocurrir en cualquier grupo de edad, presenta una mayor incidencia en adultos y en el sexo femenino9,16-19. La mortalidad, variable según las series, oscila entre el 25 y el 80%2,12,20. Se asocian con un peor pronóstico la edad extrema, la coexistencia de enfermedades sistémicas y el retraso del traslado a una unidad de grandes quemados 20,21. El pronóstico de la NET es peor que el de un quemado de la misma extensión cutánea22.
ETIOPATOGENIA
El antecedente farmacológico es el más importante (77-94%) para esta patología; se han descrito múltiples fármacos como implicados en el desarrollo de la NET. Los más frecuentemente descritos son los antibióticos (en el 29% de los casos de NET), anticonvulsionantes (en el 15%) y antiinflamatorios (en el 5%)11,12'16. También se ha descrito en relación con la administración de corticoides (lo que resulta curioso, ya que se trata de una medicación inmuno depresora, y la inmunidad celular está implicada en la fisiopatología de la NET), diuréticos, antigotosos,etc2,4,8,9,11.

Enfermedades autoinmunes y otras infecciones también pueden estar en relación con el desarrollo de este proceso patológico, como la enfermedad de Crohn, la colitis ulcerosa, el lupus eritematoso sistémico, las leucemias, la enfermedad del injerto contra el huésped, el virus de Epstein-Barr, el virus de la influenza y el VIH. El 22% de los casos de NET se produce en pacientes con infección por el VIH.
Esto puede estar producido por el estado de inmunodepresión (lo que resulta paradójico, ya que la fisiopatología de la NET parece implicar a la respuesta inmune celular) o por los fármacos que estos pacientes reciben, que frecuentemente son sulfamidas21. Los casos idiopáticos suponen un 4%. La patogenia de la NET aún no es conocida. Se han implicado los siguientes mecanismos:
a) reacción de hipersensibilidad retardada tipo IV; b) citotoxicidad contra los queratinocitos mediada por alguna sustancia linfocítica; c) reacción citotóxica tipo II, y d) necrólisis no mediada inmunológicamente. Estos factores, en conjunción con una predisposición a la infección o cierta susceptibilidad genética, son los considerados actualmente en la patogenia de la NET Se ha sugerido que los queratinocitos metabolizan anormalmente el agente responsable, produciendo un metabolito que se une con la molécula MHC-1 en la superficie celular, y es reconocido por linfocitos citotóxicos. Estos linfocitos migran dentro de la epidermis, reaccionan con los queratinocitos y causan necrólisis epidérmica.
El infiltrado epidérmico y dermoepidérmico corresponde a linfocitos T CD8, y el infiltrado dérmico a linfocitos T CD4. Se han observado células linfoides dendríticas opuestas a macrófagos dañados y a queratinocitos necróticos. En el punto de contacto con estos últimos, la membrana plasmática está ausente. También se ha observado una expresión aberrante de HLA-DR en los queratinocitos, fenómeno observado en otras enfermedades cutáneas inflamatorias
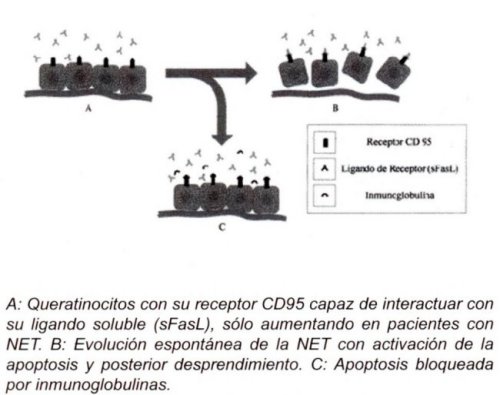
En la etiopatogenia de la NET, si bien no está del todo clara, se ha ido recolectando evidencia in vitro de que la apoptosis de los queratinocitos estaría involucrada en este proceso10-12. En un trabajo recientemente publicado12 se identificó al CD95 (FAS) como el receptor principal del proceso de la muerte celular programada de los queratinocitos, el cual está presente en similar cantidad en los pacientes sanos y aquellos con NET. Este proceso estaría gatillado por un aumento en la producción y activación del ligando soluble del CD95 (sFasL), el cual está aumentado en pacientes con NET, no así en pacientes con otro tipo de reacciones adversas a drogas o en pacientes sanos, en los cuales se encuentra en menor cantidad y sin actividad lítica13.
En relación con el trabajo anteriormente citado12 se demostró que el uso de un anticuerpo contra el sFasL producía una inhibición de la apoptosis, por lo que se planteó el uso de inmunoglobulinas policlonales16,18,19,21, demostrándose claramente que éstas producían un bloqueo in vitro de la apoptosis inducida por el sFasL En el mismo trabajo12 y otro en pacientes con SIDA15, si bien con un número pequeño de pacientes, se describió el uso de IGIV en pacientes con NET, todos los cuales presentaron una rápida y completa mejoría sin comunicarse efectos adversos y con efecto sostenido en el tiempo. La dosis de IG propuesta en ambos trabajos está en el rango de 0,2 a 0,8 g/kg/día con una duración estándar de 4 días.
EVOLUCION CLINICA
La NET es una enfermedad sistémica aguda caracterizada por fiebre y un cuadro similar a la gripe durante 1-3 días1. Estos síntomas habitualmente aparecen entre la primera y tercera semana de iniciar la administración del fármaco responsable. Posteriormente, aparece el rash, acompañado de un intenso dolor y quemazón. Inicialmente, la erupción es maculopapulosa, purpúrica y de distribución simétrica en la cara, el cuello y la parte alta del tórax. El rash se disemina rápidamente y es máximo en el curso de 3 o 4 días o incluso en horas. Presionando sobre el eritema o regiones adyacentes, se puede constatar el despegamiento epidérmico mediante fricción digital (signo de Nikolsky). Las lesiones cutáneas tenderán a coalescer y evolucionarán de máculas purpúricas a bullosas que, en los casos más graves y extensos, darán lugar a una pérdida de la epidermis, presentando una gran similitud con enfermos que han sufrido una quemadura de carácter dérmico superficial11.
DIAGNOSTICO
Los hallazgos de laboratorio son inespecíficos. Se pueden elevar las transaminasas, el nitrógeno ureico sanguíneo (BUN) y la creatinina. También es posible observar trombocitopenia, albuminuria y granulocitopenia. Estas últimas alteraciones pueden conllevar un peor pronóstico. El diagnóstico de certeza se obtiene realizando una biopsia de piel afectada. Se observa un despegamiento de la epidermis en su capa basal. Las células de la capa basal están vacuolizadas, dando lugar a un plano de clivaje subepidérmico y a una extensa necrosis de la epidermis. En la dermis papilar de lesiones recientes, se encuentra una moderada cantidad de histiocitos y de linfocitos CD4 en regiones perivasculares. En la epidermis lesionada se hallan linfocitos CD8, que también están en el líquido de las ampollas.
MEDIDAS GENERALES
La disminución de la mortalidad, desde el 70% comunicado en trabajos iniciales al 20% actual, se ha atribuido a diferentes factores: a) traslado temprano del paciente a una unidad de grandes quemados: b) tratamiento con antibióticos tópicos; c) uso de coberturas biológicas; d) tratamiento estándar de un paciente quemado, y e) retirada del tratamiento con corticoides.
Los pacientes son tratados de forma óptima en una unidad de grandes quemados. Es preciso que su traslado a esta unidad se realice con el menor retraso posible, una vez iniciado el cuadro. Numerosos estudios apoyan el concepto de que el traslado temprano de los pacientes con NET puede mejorar el pronóstico20. En un reciente estudio, los enfermos trasladados más de 7 días tras la aparición de los signos cutáneos tenían una estancia hospitalaria dos veces más prolongada que aquellos trasladados precozmente20. Un retraso superior a 48 h se asocia con un peor pronóstico y una estancia en cuidados intensivos más prolongada. La unidad de grandes quemados proporciona la experiencia necesaria en el manejo de enfermos con pérdida cutánea. Las complicaciones y la morbimortalidad de los enfermos con NET son similares a las presentadas por enfermos con quemaduras dérmicas superficiales. Por esto, su manejo exige un enfoque multidisciplinario, en el que el esfuerzo y la experiencia de cirujanos plásticos e intensivistas se aunan para conseguir el mejor resultado1,3.
Es precisa una valoración correcta de la superficie corporal afectada, de forma similar a la practicada en pacientes quemados, para instaurar el tratamiento de fluidoterapia. Aunque se puedan pautar de 5 a 7 L de sueroterapia en 24 h, es importante recordar que la aplicación de la fórmula de Parkland, la más utilizada para estimar de forma anticipada los requerimientos de fluidos de los enfermos quemados, puede sobreestimar las necesidades de los enfermos con NET. El objetivo de la fluidoterapia es mantener una diuresis entre 0,5 y 1 ml/kg/h, debiendo ajustarse el ritmo de infusión de líquidos de acuerdo con este objetivo. Es importante la selección adecuada y el cuidado de las vías intravenosas. Siempre que se pueda, se insertará un catéter venoso periférico para fluidoterapia. Si no hay superficie cutánea sana disponible, será necesaria la inserción de un catéter venoso central. No es necesario enfatizar la necesidad de una técnica aséptica para la canalización de vías venosas centrales.
El soporte nutricional es otro pilar básico en el tratamiento de estos pacientes. En muchos casos, debido a la afectación de la mucosa oro-digestiva, será necesaria la colocación de una sonda nasogástrica para conseguir un adecuado aporte de nutrientes.
El uso de antibioterapia sistémica profiláctica no está recomendado, pero debemos realizar cultivos periódicos de catéteres, sondas, piel y sangre, para realizar un tratamiento antibiótico orientado. Se debe realizar controles de flora (rectal, faríngea y nasal) dos veces por semana. Es necesario mantener un alto índice de sospecha clínica para el diagnóstico de sepsis ante signos como oliguria, hipotensión, fiebre o hipotermia, leucopenia, escalofríos o alteraciones del estado mental. Ante la sospecha de sepsis, es crucial comenzar tratamiento antibiótico intravenoso empírico de amplio espectro, mientras se obtiene la información microbiológica pertinente. La farmacocinética de estos pacientes está alterada por la pérdida de fluidos y por cambios en la función hepática y renal, por lo que es necesario un control de las concentraciones plasmáticas para garantizar la efectividad del tratamiento antibiótico y evitar su toxicidad.
La afectación ocular es frecuente y puede dar lugar a complicaciones importantes. Por esto, es necesaria una evaluación oftalmológica inicial y periódica. Se utilizarán lágrimas artificiales, colirios antibióticos, y retirada de costras y seudomembranas para evitar la formación de sinequias y lesiones conjuntivales. La revisión corneal se realizará con fluoresceína y lámpara de hendidura para vigilar la presencia de úlceras. En ocasiones, a pesar de los esfuerzos realizados, se producen complicaciones oculares, siendo necesario el tratamiento quirúrgico.
TRATAMIENTO MEDICO
Hasta hace relativamente poco tiempo, el tratamiento se realizaba con corticoides asociados o no a otros fármacos inmunodepresores. Los corticoides se han utilizado en la NET en el intento de inhibir la citotoxicidad dependiente de anticuerpos1,5. Esta práctica ha caído en desuso. No obstante, la carencia de estudios aleatorizados prospectivos hace difícil valorar su eficacia o sus indicaciones, si es que existen, en el tratamiento de la NET.
Se han publicado series en las que la administración de corticoides se asocia con una mayor mortalidad16,20, Los corticoides podrían tener un lugar en el tratamiento de enfermos con NET durante la fase eritrodérmica, antes de que aparezca una pérdida cutánea masiva. Se ha propuesto que, una vez que existe una descamación superior al 20%, el tratamiento con corticoides está contraindicado, debido al alto riesgo de aparición de complicaciones sépticas20. En un estudio20, el tratamiento con corticoides (previamente al desarrollo de la NET o tras su aparición, durante más de 48 hrs. se asociaba con mayor incidencia de infecciones, estancia
hospitalaria más prolongada, mayor incidencia de fracaso renal y hepático y mayor mortalidad20. En las unidades de referencia para el tratamiento de enfermos con NET, incluida la nuestra, no se utiliza el tratamiento con corticoides en la actualidad, y se lo retira si el enfermo viene referido con este tratamiento20.
TRATAMIENTO QUIRURGICO
Una vez que el enfermo está estabilizado, es necesaria la valoración de la superficie afectada, y la instauración de medidas locales encaminadas a evitar la desecación y la sobreinfección de la dermis expuesta. Asimismo, es importante proporcionar alivio del dolor y comodidad, ya que la pérdida epidérmica se asocia con gran dolor por exposición de las terminaciones nerviosas sensitivas.
Debe hacerse una limpieza de toda la superficie cutánea con soluciones antimicrobianas. La sulfadiacina argéntica no se debe utilizar para este fin, pues retarda la epitelización, se asocia con neutropenia y puede ser un agente etiológico de la NET. El nitrato de plata produce desecación de la dermis, puede asociarse con neutropenia, y las curas son muy dolorosas. La povidona yodada inhibe la epitelización, tiene una corta duración de acción (5-6 h.) y es muy dolorosa cuando se aplica. La solución antimicrobiana más recomendada es el gluconato de clorhexidina. Se utiliza el gluconato de clorhexidina al 0,1% en forma líquida, realizando las curas cada 12 h. La clorhexidina es bactericida frente a gram positivos y gram negativos, incluyendo Pseudomonas y estafilococos meticilín-resistentes.
Desde 1979 existe comercializada una cobertura semisintética temporal, cuyas indicaciones son la cobertura de zonas donantes de autoinjertos en pacientes quemados y la cobertura de quemaduras dérmicas superficiales. Este producto, denominado Biobrane® (Dow Hickam Pharmaceuticals Inc.; Sugar Land, Texas), está formado por una malla de nailon y colágeno porcino purificado, y una lámina externa de silicona que permite el paso de fluidos a su través9. La cobertura de la superficie cutánea perdida con Biobrane® se asocia con un mejor control de la flora, una mejor epitelización, una disminución del dolor, la prevención de la hipotermia y un control más eficaz de las pérdidas de fluidos y electrólitos a través de la piel lesionada. Además, el Biobrane® permite observar la evolución de la epitelización a su través. Para su correcta aplicación, es necesario que la superficie dérmica expuesta esté libre de restos de tejido necrótico y seco. Las láminas de Biobrane® se pueden aplicar en la misma habitación del enfermo, fijándose con grapas o con otros productos adhesivos. En las siguientes 48 h, no se permitirá la movilización al paciente para facilitar la adherencia definitiva. Pasado este tiempo, se pueden retirar las grapas y el paciente podrá deambular. Cuando se produce la epitelización, se irá despegando el Biobrane® espontáneamente. A medida que esto se produce, se debe recortar y aplicar vaselina estéril en la superficie cutánea. Aunque existen pocos trabajos que han comunicado la experiencia clínica con el uso de Biobrane® en pacientes con NET, nosotros hemos utilizado este producto en varios pacientes, cubriendo de forma masiva entre un 40 y un 60% de la superficie corporal total. Las ventajas observadas incluyen una mejoría del dolor y del disconfort, un mejor control de la colonización cutánea, la ausencia de necesidad de realizar curas con antiséptico tópico cada 12 h, la prevención de la hipotermia y una rápida epitelización.
Existen otros apositos biológicos (xenoinjertos porcinos y aloinjertos criopreservados), que se asocian con efectos similares a los de los biomateriales, No pensamos que el uso de estos injertos, que, además de ser más costosos, se asocian en sí mismos a ciertos riesgos, ofrezca ventajas significativas sobre el uso de Biobrane.
BIBLIOGRAFIA
1. Rzany B. Incidence of Stevens-Johnson Syndrome and Toxic Epidemial Necrolysis in patients with the acsquired inmunodeficiency syndrome in Germany. Arch Dermatol 1993; 129: 1059-61. [ Links ]
2. Revuz J. Toxic Epidermal Necrolysis: Clinical findings and prognosis factors in 87 patients. Arch Dermatol 1987; 123; 1160-5. [ Links ]
3. Ruiz-Maldonado. Acute disseminated epidermal necrolysis, Study of 60 cases. J Am Acad Dermatol 1985; 13: 623-35.
4. Correia O, Delgado L, Santos C. HIV virus in bullaes of HIV positive patients. Lancet 1994; 19; 1432-3. [ Links ]
5. Roujeau, JC, Stern RS. Severe Adverse Reaction to Drugs. N Engl J Med 1994; 331: 1272-83. [ Links ]
6. Bennet A. Ocular involvement in TEN. Ophtalmology 1995; 102: 1669-76. [ Links ]
7. Chasidow. Hyper almilasemia in Toxic Epidermal Necrolysis. Arch Dermatol 1993; 129: 792-3. [ Links ]
8. Chamuleau RA, Diekman MJ, Bos PJ, Smitt JH, Bosma A, Schellekens PT. Reappearance of bile ducts. Vanished bile ducts Syndrome. Hepatogastroenterology 1992; 39: 523-4. [ Links ]
9. Roujeau JC. Medication use and the risk of Stevens-Johnson syndrome or Toxic Epidermal Necrolysis. N Engl J Med 1995; 333: 1600-7. [ Links ]
8. Steller H. Mechanisms and genes of cellular suicide 1995; 267: 1445-9. [ Links ]
9. 11. Paul C, Wolkenstein P, Adie H, Wechsler J, Garchon HJ, Revuz J, Roujeau JC. Apoptosis as a mechanism of keratinocyte death in toxic epidermal necrolysis. Br J Dermatol 1996; 134: 710-4.
10. Viard I, Wehrli P, Bullani R, Schneider P, Holler N, Salomon D et al. Inhibition of Toxic Epidermal Necrolysis by blockade of CD95 with human intravenous immunoglobulin. Science 1998; 282: 490-3.
11. 13. Gutiérrez Steil C, Wrone Smith T, Sun X, Krueger JG, Coven T, Nickoloff BJ. Sunlight-induced basal cell carcinoma tumor cells and ultraviolet-B-irradiated psoriatic plaques express Fas ligand (CD95L). J Clin Invest 1998; 101: 33-9.
12. Revuz J, Roujeau JC. Treatment of Toxic Epidermal Necrolysis. Arch Dermatology 1987; 1156-8. [ Links ]
13. 15. Sanwo M, Nwadiuko R, Beall G. Use of intravenous immunoglobulin in the treatment of severe cutaneous drug reactions in patients with AIDS. J Allergy Clin Immunol 1996; 98: 1112-5.
14. Kaveri SV, Dietrich G, Kazatchkine MD. An intravenous immunoglobulin treatment regulates autoimmune responses?. Semin Hematol 1992; 29: 64-71. [ Links ]
15. Leung DY. Endothelial cell activation and high interleukin-1 secretion in the pathogenesis of acute Kawasaki disease. Lancet 1989; 1298-302. [ Links ]
16. 18. Ballow M. Modulation of in vitro synthesis of immunoglobulin and the induction of suppressor activity by therapy with intravenous immunoglobulin. J Allergy Clin Immunol 1989; 84: 595-602.
17. 19. Ballow M. Mechanisms of action of intravenous immune serum globulin in autoimmune and inflammatory diseases. J Allergy Clin Immunol 1997; 100: 151-7.
18. Debre M, Bonnet MC, Fridman WH, Carosella E, Philippe N, Reinert P et al. Infusión of F gamma fragments for treatment of children with acute ITP. Lancet 1993; 342: 945-9.
19. Basta M. Mechanism of therapeutic effect of high-dose intravenous immunoglobulin. Attenuation of acute complement dependent immune damage in a guinea pig model. J Clin Invest 1989; 84: 1974-81. [ Links ]
20. Chan HL, Stern Rs, Arndt KA. The incidence of erythema multiforme, Stevens-Johnson and toxic epidermal necrolysis: a population based study with particular reference to reactions caused by drugs among outpatients. Arch Dermatol. 1990;126:43-47. Organización Mundial de la Salud. Vigilancia farmacológica internacional. Función del Hospital. Serie de Informes Técnicos. Ginebra; 1969. [ Links ] [ Links ]
21. De Swarte RD. Drug allergy. En: Patterson R, Grammer LC, Greenberger PA, Zeiss CR, editores. Allergic Diseases: Diagnosis and Management. 4ta ed. Philadelphia: JB Lippincott; 1993. p. 395-551. [ Links ]
22. Faich GA. Adverse drug reaction monitoring. N Engl J Med. 1986;314:1589-92. Hoigne R, Schlumberger HU,Vervloet D, Zoppi M. Epidemiology of allergic drug reactions. En: Burr M, editor. Epidemiology of clinical allergy. Monographs in Allergy. 1993; 31:140-170. [ Links ]














